EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 31983L0514
Third Commission Directive 83/514/EEC of 27 September 1983 on the approximation of the laws of the Member States relating to methods of analysis necessary for checking the composition of cosmetic products
A treia Directivă a Comisiei din 27 septembrie 1983 privind apropierea legislației statelor membre cu privire la metodele de analiză necesare pentru controlul compoziției produselor cosmetice
A treia Directivă a Comisiei din 27 septembrie 1983 privind apropierea legislației statelor membre cu privire la metodele de analiză necesare pentru controlul compoziției produselor cosmetice
JO L 291, 24.10.1983, p. 9–46
(DA, DE, EL, EN, FR, IT, NL) Acest document a fost publicat într-o ediţie specială
(ES, PT, FI, SV, CS, ET, LV, LT, HU, MT, PL, SK, SL, BG, RO, HR)
 In force
In force
- Date of document:
- 27/09/1983
- Date of effect:
- 27/09/1983; intrare în vigoare data notificării
- Date of notification:
- 27/09/1983
- Date of transposition:
- 31/12/1984; cel târziu a se vedea articolul 2
- Date of end of validity:
- No end date
- Author:
- Comisia Europeană
- Responsible body:
- Directorate-General for Health and Consumers, DG24, SCOS
- Form:
- Directivă
- Addressee:
- Cele zece state membre: Belgia, Danemarca, Germania, Irlanda, Grecia, Franţa, Italia, Luxemburg, Ţările de Jos, Regatul Unit
- Additional information:
- extinderea aplicării pentru SEE prin 21994A0103(01)
- Authentic language:
- daneză, germană, greacă, engleză, franceză, italiană, neerlandeză, islandeză, norvegiană
- Co author:
- DG03/X/00, DG05/X/00, DG06/X/00, SJUR/X/00
- Treaty:
- Tratat de instituire a Comunităţii Economice Europene
- Legal basis:
-
- 31976L0768 - A08P1
- Link
- Link
- Link
- Select all documents mentioning this document
- Instruments cited:
- Link
- EUROVOC descriptor:
- Subject matter:
- Directory code:
|
13/Volumul 06 |
RO |
Jurnalul Ofícial al Uniunii Europene |
136 |
31983L0514
|
L 291/9 |
JURNALUL OFÍCIAL AL UNIUNII EUROPENE |
A TREIA DIRECTIVĂ A COMISIEI
din 27 septembrie 1983
privind apropierea legislației statelor membre cu privire la metodele de analiză necesare pentru controlul compoziției produselor cosmetice
(83/514/CEE)
COMISIA COMUNITĂȚILOR EUROPENE,
având în vedere Tratatul de instituire a Comunității Economice Europene,
având în vedere Directiva 76/768/CEE a Consiliului din 27 iulie 1976 privind apropierea legislației statelor membre cu privire la produsele cosmetice (1), modificată ultima dată de Directiva 83/341/CEE (2), în special articolul 8 alineatul (1),
întrucât Directiva 76/768/CEE prevede testarea oficială a produselor cosmetice cu scopul constatării îndeplinirii condițiilor stabilite de dispozițiile Comunității privind compoziția produselor cosmetice;
întrucât toate metodele de analiză necesare trebuie stabilite cât se poate de repede; întrucât au fost deja parcurse două etape pentru atingerea acestui obiectiv, prin definirea anumitor metode în Directivele 80/1335/CEE (3) și 82/434/CEE ale Comisiei (4), a treia etapă trebuie să constea în definirea metodelor pentru determinarea diclormetanului și 1,1,1-tricloretanului, identificarea și determinarea chinolin-8-ol-ului și sulfatului de bis(8-hidroxichinolină), determinarea amoniacului, identificarea și determinarea nitrometanului, identificarea și determinarea acidului mercaptoacetic în produse pentru ondularea părului, produse pentru întinderea părului și produse depilatoare, identificarea și determinarea hexaclorofenului (INN), tosycloramidei de sodiu (INN), determinarea fluorului total în paste de dinți, identificarea și determinarea compușilor organomercurici, determinarea sulfurilor elementelor alcaline și alcalino-pământoase;
întrucât măsurile prevăzute de prezenta directivă sunt în conformitate cu avizul Comitetului privind adaptarea Directivei 76/768/CEE la progresul tehnic,
ADOPTĂ PREZENTA DIRECTIVĂ:
Articolul 1
Statele membre adoptă toate măsurile necesare pentru a se asigura că în timpul testării oficiale a produselor cosmetice:
|
— |
determinarea diclormetanului și 1,1,1-tricloretanului; |
|
— |
identificarea și determinarea 8-chinolinolului și sulfatului de bis (8-hidroxichinolină); |
|
— |
determinarea amoniacului; |
|
— |
identificarea și determinarea nitrometanului; |
|
— |
identificarea și determinarea acidului mercaptoacetic în produse pentru ondularea părului, produse pentru întinderea părului și în produse depilatoare; |
|
— |
identificarea și determinarea hexaclorofenului (INN); |
|
— |
determinarea tosylcloramidei de sodiu (INN); |
|
— |
determinarea fluorului total în paste de dinți; |
|
— |
identificarea și determinarea compușilor organomercurici; |
|
— |
determinarea sulfurilor alcaline și alcalino-pământoase |
se efectuează în conformitate cu metodele descrise în anexă.
Articolul 2
Statele membre pun în aplicare actele cu putere de lege și actele administrative necesare pentru a se conforma prezentei directive până la 31 decembrie 1984.
Statele membre informează de îndată Comisia cu privire la aceasta.
Articolul 3
Prezenta directivă se adresează statelor membre.
Adoptată la Bruxelles, 27 septembrie 1983.
Pentru Comisie
Frans ANDRIESSEN
Membru al Comisiei
(1) JO L 262, 27.9.1976, p. 169.
(2) JO L 188, 13.7.1983, p. 15.
(3) JO L 383, 31.12.1980, p. 27.
(4) JO L 185, 30.6.1982, p. 1.
ANEXĂ
DETERMINAREA DICLORMETANULUI ȘI A 1,1,1-TRICLORETANULUI
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă descrie determinarea diclormetanului (clorură de metilen) și a 1,1,1-tricloretanului (metil cloroform) în toate produsele cosmetice în care este posibil să apară acești solvenți.
2. DEFINIȚIE
Conținutul de diclormetan și 1,1,1-tricloretan în probă determinate în conformitate cu aceastã metodă sunt exprimate în procente masice.
3. PRINCIPIU
Metoda folosește cromatografia de gaze, cu cloroform ca standard intern.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. Cloroform (CHCl3).
4.2. Tetraclorură de carbon (CCl4).
4.3. Diclormetan (CH2Cl2).
4.4. 1,1,1-Tricloretan (CH3 CCl3).
4.5. Acetonă.
4.6. Azot.
5. APARATURĂ
5.1. Aparatură de laborator obișnuită.
5.2. Cromatograf de gaze cu detector de conductivitate termică.
5.3. Flacoane de transfer de 50-100 ml (vezi metoda de prelevare a probelor de la 5.3) (1).
5.4. Seringă cu gaz comprimat de 25 sau 50 µl (vezi metoda de prelevare a probelor 5.4.2.2) (1).
6. PROCEDURĂ
6.1. Probă nepresurizată: se cântărește cu precizie într-un pahar conic cu dop. Se introduce o cantitate precis cântărită de cloroform (4.1) ca standard intern, echivalent cu presupusa cantitate de diclormetan și 1,1,1-tricloretan din probă. Se amestecă foarte bine.
Probă presurizată: se folosește metoda de prelevare a probelor descrisă la capitolul corespunzător, dar cu următoarele precizări suplimentare:
6.2.1. După transferarea unei probe într-un flacon de transfer (5.3), se introduce apoi în flaconul de transfer un volum de cloroform (4.1) ca standard intern echivalent cu presupusa cantitate de diclormetan și 1,1,1-tricloretan din probă. Se amestecă foarte bine. Se clătește volumul propriu al injectorului cu 0,5 ml tetraclorură carbon (4.2). După uscare se determină prin diferență, cu precizie, masa de standard intern adăugată.
6.2.2. După umplerea seringii cu probă, ștuțul seringii trebuie suflat cu azot (4.6) astfel încât să nu rămână nici un reziduu înainte de injectarea în cromatograf.
6.2.3. După prelevarea fiecărei probe, suprafețele injectorului și piesei de transfer trebuie clătite de mai multe ori cu acetonă (4.5) (folosind o seringă hipodermică) și apoi uscate complet cu azot (4.6).
6.2.4. Pentru fiecare analiză se fac măsurări folosind două flacoane de transfer diferite și cinci măsurări pentru fiecare pahar.
7. CONDIȚII DE CROMATOGRAFIERE
7.1. Precoloană
Tub: oțel inoxidabil
Lungime: 300 mm
Diametru: 3 sau 6 mm
Umplutură: același material care se folosește ca umplutură la coloana analitică.
7.2. Coloană
Faza staționară este din Hallcomid M 18 pe chromosorb. Coloana trebuie să realizeze o rezoluție, „R”, egală cu 1,5 sau mai bună, unde:
![]()
în care:
|
r1 și r2 |
= |
timpii de retenție (în minute), |
|
W1 și W2 |
= |
lățimea vârfurilor la jumătatea înălțimii (în milimetri), |
|
d′ |
= |
viteza graficului (milimetri pe minut). |
Exemple de coloane ce produc rezultatele dorite:
|
Coloana |
I |
II |
|
Material: |
Tubulatură din oțel inoxidabil |
Tubulatură din oțel inoxidabil |
|
Lungime: |
350 cm |
400 cm |
|
Diametru: |
3 mm |
6 mm |
|
Suport: | ||
|
chromosob: |
WAW |
WAW-DMCS-HP |
|
analiza sitei: |
ochiuri 100-200 |
ochiuri 60-80 |
|
Faza staționară: |
Hallcomid M 18, 10 % |
Hallcomid M 18, 20 % |
Condițiile de temperatură pot varia în funcție de aparatură. În exemple, ele au fost reglate în următorul mod:
|
Coloana |
I |
II |
|
Temperaturi: | ||
|
coloană: |
65 °C |
75 °C |
|
injector: |
150 °C |
125 °C |
|
detector: |
150 °C |
200 °C |
|
Gaz purtător: | ||
|
debit de heliu: |
45 ml/min |
60 ml/min |
|
presiune de intrare: |
2,5 bar |
2 bar |
|
Injecție: |
15 μl |
15 μl |
8. AMESTEC PENTRU STABILIREA FACTORILOR DE RĂSPUNS
Într-un pahar conic cu dop se realizează următorul amestec, cântărit cu precizie:
|
|
Diclormetan (4.3), 30 % (m/m). |
|
|
1,1,1-tricloretan (4.4), 35 % (m/m). |
|
|
Cloroform (4.1), 35 % (m/m). |
9. CALCULE
9.1. Calculul factorului de răspuns al unei substanței „p” relativ la o substanță „a” aleasă ca standard intern
Fie prima substanță „p”, unde:
|
kp |
= |
factorul său de răspuns, |
|
mp |
= |
masa sa în amestec, |
|
Ap |
= |
suprafața vârfului său. |
Fie a doua substanță „a”, unde:
|
ka |
= |
factorul său de răspuns (considerat egal cu unitatea), |
|
Ma |
= |
masa sa în amestec, |
|
Aa |
= |
suprafața vârfului său, |
atunci:
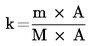
De exemplu, s-au obținut următorii factorii de răspuns (pentru cloroform: k = 1):
|
Diclormetan: |
k1 = 0,78 ± 0,03 |
|
1,1,1-tricloretan: |
k2 = 1,00 ± 0,03 |
9.2. Calculul procentelor % (m/m) de diclormetan și 1,1,1-tricloretan prezente în proba de analizat
Fie:
|
ma |
= |
masa de cloroform introdus (în grame), |
|
Ms |
= |
masa probei de analizat (în grame), |
|
Aa |
= |
suprafața vârfului cloroformului, |
|
A1 |
= |
suprafața vârfului diclormetanului, |
|
A2 |
= |
suprafața vârfului 1,1,1-tricloretanului, |
atunci:


10. REPETABILITATE (2)
Pentru un conținut de diclormetan și/sau 1,1,1-tricloretan de 25 % (m/m), diferența dintre rezultatele a două determinări executate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 2,5 % (m/m).
IDENTIFICAREA ȘI DETERMINAREA 8-CHINOLINOLULUI ȘI SULFATULUI DE BIS(8-HIDROXICHINOLINĂ)
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă descrie identificarea și determinarea cantitativă a 8-chinolinolului și a sulfatului său.
2. DEFINIȚIE
Conținutul de 8-chinolinol și de sulfat de bis(8-hidroxichinolin) din probă determinat prin această metodă este exprimat în procente masice de 8-chinolinol.
3. PRINCIPIU
3.1. Identificare
Identificarea se face prin cromatografie în strat subțire.
3.2. Determinare
Determinarea se realizează prin analiză spectrometrică la 410 nm a complexului obținut prin reacția cu soluția Fehling.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. 8-chinolinol.
4.2. Benzen. Din cauza toxicității sale, se lucrează cu mare atenție.
4.3. Cloroform.
4.4. Soluție apoasă de hidroxid de sodiu, 5 % (m/m).
4.5. Sulfat de cupru pentahidratat.
4.6. Tartrat de sodiu și potasiu.
4.7. Acid clorhidric M.
4.8. Acid sulfuric 0,5 M.
4.9. Soluție de hidroxid de sodiu M.
4.10. Etanol.
4.11. 1-butanol.
4.12. Acid acetic glacial.
4.13. Acid clorhidric 0,1.
4.14. „Celită 545” sau echivalent.
4.15. Soluții standard
4.15.1. Într-un balon cotat de 100 ml se cântăresc 100 mg 8-chinolinol (4.1). Se dizolvă în puțin acid sulfuric (4.8). Se aduce la semn cu acid sulfuric (4.8).
4.15.2. Într-un balon cotat de 100 ml se cântăresc 100 mg 8-chinolinol (4.1).Se dizolvă în etanol (4.10). Se aduce la semn cu etanol (4.10) și se amestecă.
4.16. Soluție Fehling
Soluția A
Într-un balon cotat de 100 ml se cântăresc 7 g sulfat de cupru pentahidratat (4.5). Se dizolvă în puțină apă. Se aduce la semn cu apă și se amestecă.
Soluția B
Într-un balon cotat de 100 ml se cântăresc 35 g tartrat de sodiu și potasiu (4.6). Se dizolvă în 50 ml de apă. Se adaugă 20 ml hidroxid de sodiu (4.4). Se aduce la semn cu apă și se amestecă. Imediat înainte de folosire, se pun cu pipeta 10 ml de soluție A și 10 ml de soluție B într-un balon cotat de 100 ml. Se aduce la semn și se amestecă.
4.17. Solvenți de eluție pentru cromatografia în strat subțire
|
I |
: |
1-butanol (4.11)/acid acetic (4.12)/apă (80:20:20; v/v/v) |
|
II |
: |
Cloroform (4.13)/acid acetic (4.12) (95:5; v/v). |
4.18. 2,6-dicloro-4-(cloroimino)ciclohexa-2,5-dienonă, 1 % (m/v) soluție în etanol (4.10).
4.19. Carbonat de sodiu, 1 % (m/v) soluție în apă.
4.20. Etanol (4.10), 30 % (v/v) soluție în apă.
4.21. Etilendiaminotetraacetat dibazic de disodiu, 5 % (m/v) soluție în apă.
4.22. Soluție tampon, pH 7
Într-un balon cotat de 1 l se cântăresc 27 g ortofosfat dibazic de potasiu anhidru și 70 g ortofosfat monobazic de dipotasiu trihidratat. Se aduce la semn cu apă.
4.23. Plăci pregătite pentru cromatografia în strat subțire
Plăci gata pregătite cu o grosime de 0,25 mm (de ex. Merck Kieselgel 60 sau echivalent). Înainte de folosire, se pulverizează 10 ml de reactiv (4.21) și se usucă la 80 °C.
5. APARATURĂ
5.1. Balon cu fund rotund și gât rodat de 100 ml.
5.2. Baloane cotate.
5.3. Pipete gradate de 10 și 5 ml.
5.4. Pipete de gaze de 20, 15, 10 și 5 ml.
5.5. Pâlnii de separare de 100, 50 și 25 ml.
5.6. Hârtie de filtru cutată, diametru 90 mm.
5.7. Evaporator rotativ.
5.8. Condensator de reflux cu gât rodat.
5.9. Spectrofotometru.
5.10. Cuve optice cu lungime de cale de 10 mm.
5.11. Fierbător cu agitator.
5.12. Dimensiunile coloanei cromatografice de sticlă: 160 mm lungime, diametru de 8 mm, o gâtuire la capătul de jos conținând un dop de vată de sticlă și un adaptor la capătul de sus pentru aplicarea presiunii.
6. PROCEDURĂ
6.1. Identificare
6.1.1. Probe lichide
6.1.1.1. PH-ul părții din proba analizată se reglează la 7,5 și 10 µl se picură pe linia de start a unei plăci de silicagel pentru cromatografie în strat subțire tratată în prealabil (4.23).
6.1.1.2. 10 și 30 µl soluție standard (4.15.2) se picură pe încă două puncte de pe linia de start, după care placa se developează într-unul dintre cei doi eluenți (4.17).
6.1.1.3. Când frontul de solvent a avansat 150 mm, placa se usucă la 110 °C (timp de 15 minute). La lumina unei lămpi UV (366 nm), petele de 8-chinolinol prezintă fluorescență galbenă.
6.1.1.4. Se pulverizează placa cu soluție de carbonat de sodiu (4.19). Se usucă și se pulverizează cu soluție de 2,6-dicloro-4-(clorimino)ciclohexa-2,5-dienonă (4.18). 8-chinolinolul devine vizibil ca pată albastră.
6.1.2. Probe solide sau creme
6.1.2.1. Se dispersează 1 g de probă în 5 ml soluție tampon (4.22), apoi se transferă cu 10 ml cloroform (4.3) într-o pâlnie de separare și se agită. După separarea stratului de cloroform, se extrage încă de două ori stratul apos cu 10 ml de cloroform (4.3). Extractele de cloroform filtrat și combinat se evaporă până aproape de uscare într-un balon de 100 ml cu fundul rotund (5.1) pe un evaporator rotativ (5.7). Se dizolvă reziduul în 2 ml de cloroform (4.3) și se picură 10 și respectiv 30 µl din soluția obținută pe placa de strat subțire de silicagel (4.23) conform metodei descrise în mai sus la 6.1.1.1.
6.1.2.2. Se aplică 10 și 30 µl de soluția standard (4.15.2) pe placă și se continuă așa cum s-a descris la 6.1.1.2 - 6.1.1.4.
6.2. Determinare
6.2.1. Probe lichide
6.2.1.1. Se cântăresc 5 g de probă într-un balon de 100 ml cu fund rotund. Se adaugă 1 ml soluție de acid sulfuric (4.8) și se evaporă amestecul până aproape de uscare, la presiune redusă și 50 °C.
6.2.1.2. Se dizolvă acest reziduu în 20 ml apă caldă. Se transferă într-un balon cotat de 100 ml. Se clătește de trei ori cu 20 ml de apă. Se completează cu apă până la 100 ml și se amestecă.
6.2.1.3. Se pun cu pipeta 5 ml din această soluție într-o pâlnie de separare de 50 ml (5.5). Se adaugă 10 ml soluție Fehling (4.16). Se extrage complexul 8-chinolinol cupru [cupru oxină (ISO)] obținut cu trei porțiuni de câte 8 ml de cloroform (4.3).
6.2.1.4. Se filtrează și se colectează stratul de cloroform într-un balon cotat de 25 ml (5.2). Se aduce la semn cu cloroform (4.3) și se agită vasul. Se măsoară densitatea optică a soluției galbene față de cloroform la 410 nm.
6.2.2. Probe solide sau creme
6.2.2.1. Într-un balon de 100 ml cu fund rotund se cântăresc 0,500 g de probă (4.1). Se adaugă 30 ml benzen (4.2) și 20 ml acid clorhidric (4.7). Se fierbe conținutul vasul la reflux, sub amestecare, timp de 30 minute.
6.2.2.2. Se transferă conținutul vasului într-o pâlnie de separare de 100 ml (5.5). Se clătește cu 5 ml de 1 N HCl (4.7). Se transferă faza apoasă într-un balon cu fund rotund (5.1) și se spală faza de benzen cu 5 ml acid clorhidric (4.7).
6.2.2.3. În cazul emulsiilor care stânjenesc tratarea în continuare, se amestecă 0,500 g de probă cu 2 g Celită 545 (4.14) pentru a forma o pudră liber curgătoare. Se transferă amestecul în porțiuni mici într-o coloană cromatografică de sticlă (5.12).
După fiecare adăugare, se îndeasă umplutura coloanei. De îndată ce tot amestecul a fost transferat în coloană se eluează cu acid clorhidric (4.13) astfel încât 10 ml de eluat să se obțină în aproximativ 10 minute (dacă este necesar, această eluție poate fi realizată sub o ușoară presiune de azot). În timpul eluției trebuie avut grijă ca tot timpul să existe acid clorhidric peste umplutura coloanei. Primii 10 ml de eluat se tratează mai departe conform 6.2.2.4.
6.2.2.4. Se evaporă fazele apoase colectate (6.2.2.2) sau eluatul (6.2.2.3) aproape până de uscare într-un evaporator rotativ la presiune redusă.
6.2.2.5. Se dizolvă reziduul în 6 ml soluție de hidroxid de sodiu (4.9). Se adaugă 20 ml soluție Fehling (4.16) și se transferă conținutul balonului într-o pâlnie de separare de 50 ml (5.5). Se clătește vasul cu 8 ml cloroform (4.3). Se agită și se filtrează faza de cloroform într-un balon cotat de 50 ml.
6.2.2.6. Se repetă extracția de trei ori cu 8 ml de cloroform (4.3). Se filtrează faza de cloroform și se colectează într-un balon cotat de 50 ml. Se completează până la semn cu cloroform (4.3) și se agită. Se măsoară densitatea optică a soluției galbene față de cloroform la 410 nm.
7. CURBA STANDARD
În patru baloane cu fund rotund de 100 ml (5.1), fiecare conținând 3 ml soluție apoasă de etanol 30 % (4.20), se pun cu pipeta 5, 10, 15 și 20 ml soluție standard (4.15.1) corespunzând la 5, 10, 15 și 20 mg 8-chinolinol. Se procedează conform 6.2.1.
8. CALCUL
8.1. Probe de lichid

unde:
|
a |
= |
miligrame de 8-chinolinol pe curba standard (7), |
|
m |
= |
masa (în miligrame) a porțiunii analizate (6.2.1.1) |
8.2. Probe solide sau creme

unde:
|
a |
= |
miligrame de 8-chinolinol pe curba standard (7), |
|
m |
= |
masa (în miligrame) a porțiunii de testare (6.2.2.1). |
9. REPETABILITATE (2)
Pentru un conținut de aproximativ 0,3 % 8-chinolinol, diferența dintre rezultatele a două determinări efectuate pe aceeași probă nu trebuie să depășească o valoare absolută de 0,02 %.
DETERMINAREA AMONIACULUI
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă descrie determinarea amoniacului liber în produsele cosmetice.
2. DEFINIȚIE
Conținutul de amoniac din probă determinat conform acestei metode este exprimat în procente masice de amoniac.
3. PRINCIPIU
Se adaugă soluție de clorură de bariu la o porțiune analizată de produs cosmetic diluată într-un mediu de soluție apoasă de metanol. Orice precipitat care s-ar putea forma se filtrează sau se centrifughează. Acest procedeu evită pierderile de amoniac, în timpul distilării cu abur, din anumite săruri de amoniu cum ar fi carbonatul și carbonații bazici precum și din sărurile acizilor grași, cu excepția acetatului de amoniu.
Amoniacul se distilează cu abur din filtrat sau din supernatant și se determină prin titrare potențiometrică sau alt tip de titrare.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. Metanol.
4.2. Clorură de bariu dihidrată, soluție 25 % (m/v).
4.3. Acid ortoboric, soluție 4 % (m/v).
4.4. Acid sulfuric, soluție standard 0,25 M.
4.5. Lichid anti-spumant.
4.6. Hidroxid de sodiu, soluție standard 0,5 M.
4.7. Indicator, dacă este necesar: se amestecă 5 ml soluție de roșu de metil 0,1 % (m/v) în etanol cu 2 ml soluție de albastru de metilen 0,1 % (m/v) în apă.
5. APARATURĂ
5.1. Aparatură de laborator obișnuită.
5.2. Centrifugă cu flacoane cu dop de 100 ml.
5.3. Distilator cu abur.
5.4. Potențiometru.
5.5. Electrod de sticlă indicator și electrod de referință diclorură de dimercur (calomel).
6. PROCEDURĂ
6.1. Într-un balon cotat de 100 ml se cântărește o cantitate (m) de probă corespunzătoare unui maximum de 150 mg amoniac.
6.2. Se adaugă 10 ml apă, 10 ml metanol (4.1) și 10 ml soluție de clorură de bariu (4.2). Se aduce la semn cu metanol (4.1).
6.3. Se amestecă și se lasă să stea peste noapte în frigider (5 °C).
6.4. Se filtrează sau se centrifughează soluția încă rece în eprubete închise, timp 10 minute, astfel încât să se obțină un strat de filtrat sau supernatant limpede.
6.5. Se pun cu pipeta 40 ml din această soluție limpede în distilatorul cu abur (5.3) și apoi se adaugă 0,5 ml de lichid anti-spumant (4.5), când unde este necesar.
6.6. Se distilează și se colectează 200 ml de distilat într-un pahar de 250 ml conținând 10 ml acid sulfuric standard (4.4) și 0,1 ml indicator (4.7).
6.7. Se titrează din nou excesul de acid cu soluție standard de hidroxid de sodiu (4.6).
6.8.
N.B.: Pentru determinarea potențiometrică se colectează 200 ml de distilat într-un pahar de 250 ml conținând 25 ml soluție de acid ortoboric (4.3) și se titrează cu acid sulfuric standard (4.4), înregistrând curba de neutralizare.
7. CALCUL
7.1. Calcul în cazul retitrării
Fie:
|
V1 |
= |
volumul (în mililitri) de soluție de hidroxid de sodiu (4.6) folosită, |
|
M1 |
= |
molaritatea sa reală (4.6), |
|
M2 |
= |
factorul de molaritate reală al soluției de acid sulfuric (4.4), |
|
m |
= |
masa (în miligrame) a porțiunii analizate (6.1) luate |
atunci:
![]()
7.2. Calcul în cazul titrării potențiometrice directe
Fie:
|
V2 |
= |
volumul (în mililitri) de soluție de acid sulfuric (4.4) folosit, |
|
M2 |
= |
molaritatea sa reală (4.4), |
|
m |
= |
masa (în miligrame) porțiunii analizate (6.1) prelevate, |
atunci:

8. REPETABILITATE (2)
Pentru un conținut de aproximativ 6 % amoniac, diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 0,6 %.
IDENTIFICAREA ȘI DETERMINAREA NITROMETANULUI
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă este adecvată pentru identificarea și determinarea nitrometanului până la un conținut de aproximativ 3 % din produsele cosmetice ambalate în pulverizatoare de aerosoli.
2. DEFINIȚIE
Conținutul de nitrometan din probă determinat conform acestei metode este exprimat în procente masice de nitrometan din totalul conținutului pulverizatorului de aerosoli.
3. PRINCIPIU
Nitrometanul este identificat prin reacție de culoare. Nitrometanul este determinat prin cromatografie de gaze după adăugarea unui standard intern.
4. IDENTIFICARE
4.1. Reactivi
Toți reactivii trebuie să fie de puritate analitică.
4.1.1. Hidroxid de sodiu, soluție 0,5 M.
4.1.2. Reactiv Folin
Se dizolvă 0,1 g 3,4-dihidro-3,4-dioxonaftalină-1-sulfonat de sodiu în apă și se diluează până la 100 ml.
4.2. Procedură
La 1 ml de probă se adaugă 10 ml de 4.1.1. și 1 ml de 4.1.2. Prezența nitrometanului este indicată printr-o colorare violetă.
5. DETERMINARE
5.1. Reactivi
Toți reactivii trebuie să fie de calitate analitică.
5.1.1. Cloroform (standard intern 1).
5.1.2. 2,4-dimetilheptan (standard intern 2).
5.1.3. Etanol 95 %.
5.1.4. Nitrometan.
5.1.5. Soluție de referință de cloroform
Într-un balon cotat de 25 ml tarat se introduc aproximativ 650 mg cloroform (5.1.1). Se recântărește cu precizie vasul și conținutul. Se aduce la semn cu etanol 95 % (5.1.3). Se cântărește și se calculează procentele masice de cloroform în această soluție.
5.1.6. Soluție de referință 2,4-dimetilheptan
Se realizează similar cu soluția de referință de cloroform, dar cântărind 270 mg 2,4-dimetilheptan (5.1.2) într-un balon cotat de 25 ml.
5.2. Aparatură
5.2.1. Cromatograf de gaze cu detector cu ionizare cu flacără.
5.2.2. Aparatură de prelevare a probelor de aerosoli (flacon de transfer, conectori de microseringi etc.), conform descrierii din capitolul II al anexei la Directiva 80/1335/CEE a Comisiei din 22 decembrie 1980 (1).
5.2.3. Aparatură de laborator obișnuită.
5.3. Procedură
5.3.1. Pregătirea probei
Într-un flacon de transfer de 100 ml tarat se purjează sau se evacuează conform procedeului descris la 5.4., capitolul II al directivei susmenționate, se introduc aproximativ 5 ml din una dintre soluțiile de standard intern (5.1.5. sau 5.1.6.). Se folosește o seringă de sticlă de 10 sau 20 ml, fără ac, adaptată la piesa de transfer, urmând tehnica descrisă la paragraful 5 din capitolul II al directivei susmenționate. Se recântărește pentru a determina cantitatea introdusă. Folosind aceeași tehnică, se transferă în acest pahar aproximativ 50 g din conținutul probei din pulverizatorul de aerosoli. Se cântărește din nou pentru a determina cantitatea de probă transferată. Se amestecă bine.
Se injectează aproximativ 10 µl folosind microseringa specificată (5.2.2.). Se efectuează cinci injectări.
5.3.2. Prepararea standardului
Într-un balon cotat de 50 ml se cântăresc cu precizie aproximativ 500 mg nitrometan (5.1.4) și fie 500 mg cloroform (5.1.1), fie 210 mg 2,4-dimetilheptan (5.1.2). Se aduce la semn cu etanol 95 % (5.1.3). Se amestecă bine. Se pun 5 ml din această soluție într-un balon cotat de 20 ml. Se aduce la semn cu etanol 95 % (5.1.3).
Se injectează aproximativ 10 µl cu microseringa specificată (5.2.2). Se efectuează cinci injectări.
5.3.3. Condiții pentru cromatografia de gaze
5.3.3.1. Coloană
Coloana este alcătuită din două părți, prima conținând didecil ftalat pe Gaz Chrom Q ca umplutură, a doua având Ucon 50 HB 280X pe Gaz Chrom Q ca umplutură. Coloana combinată astfel pregătită trebuie să producă o rezoluție „R” egală cu 1,5 sau superioară, unde:
![]()
fie:
|
r1 și r2 |
= |
timpii de retenție (în minute), |
|
W1 și W2 |
= |
lățimea vârfului la jumătatea înălțimii (în milimetri), |
|
d′ |
= |
viteza graficului (în milimetri pe minut). |
De exemplu, următoarele două părți realizează rezoluția cerută:
Coloana A:
|
|
Material: oțel inoxidabil |
|
|
Lungime: 1,5 m |
|
|
Diametru: 3 mm |
|
|
Umplutură: 20 % ftalat didecilic pe Gaz Chrom Q (100-120 ochiuri) |
Coloana B:
|
|
Material: oțel inoxidabil |
|
|
Lungime: 1,5 m |
|
|
Diametru: 3 mm |
|
|
Umplutură: 20 % Ucon 50 HB 280X pe Gaz Crom Q (100-120 ochiuri) |
5.3.3.2. Detector
O reglare adecvată a sensibilității pentru electrometrul detectorului cu ionizare cu flacără este 8 × 10-10A.
5.3.3.3. Condiții de temperatură
S-au găsit următoarele condiții adecvate:
|
|
Injector: 150 °C |
|
|
Detector: 150 °C |
|
|
Coloană: între 50 și 80 °C, în funcție de coloanele individuale și de aparatură. |
5.3.3.4. Alimentări cu gaz adecvat
Gaz purtător: azot
|
|
Presiune: 2,1 bar |
|
|
Debit: 40 ml/min |
|
|
Alimentări detector: conform specificațiilor fabricantului detectorului. |
6. CALCUL
6.1. Factorul de răspuns al nitrometanului, calculat cu în raport cu standardul intern folosit
Dacă „n” reprezintă nitrometanul:
fie:
|
kn |
= |
factorul său de răspuns, |
|
m′n |
= |
masa sa(în grame) în amestec, |
|
S′n |
= |
suprafața vârfului său. |
Dacă „c” reprezintă standardul intern, cloroform sau 2,4 dimetilheptan:
fie:
|
m′c |
= |
masa sa (în grame) în amestec, |
|
S′c |
= |
suprafața vârfului său, |
atunci:
![]()
(kn depinde de aparat).
6.2. Concentrația nitrometanului în probă
Dacă „n” reprezintă nitrometanul:
fie:
|
kn |
= |
factorul său de răspuns, |
|
Sn |
= |
suprafața vârfului său. |
Dacă „c” reprezintă standardul intern, cloroform sau 2,4-dimetilheptan:
fie:
|
mc |
= |
masa sa (în grame) în amestec, |
|
Sc |
= |
suprafața vârfului său, |
|
M |
= |
masa (în grame) de aerosol transferat, |
atunci procentul % (m/m) de nitrometan în probă este:

7. REPETABILITATE (2)
Pentru un conținut de nitrometan de aproximativ 0,3 % (m/m), diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 0,03 % (m/m)
IDENTIFICAREA ȘI DETERMINAREA ACIDULUI MERCAPTOACETIC ÎN PRODUSELE PENTRU ONDULAREA PĂRULUI, PENTRU ÎNTINDEREA PĂRULUI ȘI ÎN PRODUSE DEPILATOARE
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă descrie identificarea și determinarea acidului mercaptoacetic în produsele pentru ondularea părului, pentru întinderea părului și în produsele depilatoare în care pot fi prezenți și alți agenți de reducere.
2. DEFINIȚIE
Conținutul de acid mercaptoacetic în probă determinat conform acestei metode este exprimat în procente masice de acid mercaptoacetic.
3. PRINCIPIU
Acidul mercaptoacetic se identifică prin teste în picătură și prin cromatografie în strat subțire și se determină prin iodometrie sau cromatografie de gaze.
4. IDENTIFICARE
4.1. Identificare prin teste în picătură
4.1.1. Reactivi
Toți reactivii trebuie să fie de puritate analitică.
4.1.1.1. Hârtie cu diacetat de plumb.
4.1.1.2. Soluție de acid clorhidric (un volum acid clorhidric concentrat plus un volum apă).
4.1.2. Procedură
4.1.2.1. Identificarea acidului mercaptoacetic prin reacție de culoare cu diacetatul de plumb
Se pune o picătură de probă de analizat pe hârtia cu diacetat de plumb (4.1.1.1). Dacă apare o culoare galben intens, probabil este prezent acidul mercaptoacetic.
Sensibilitate: 0,5 %.
4.1.2.2. Caracterizarea sulfurilor anorganice prin formarea hidrogenului sulfurat la acidifiere
Într-o eprubetă se introduc câteva miligrame din proba analizată. Se adaugă 2 ml apă distilată și 1 ml acid clorhidric (4.1.1.2). Se eliberează hidrogen sulfurat, recunoscut după miros și pe hârtia cu diacetat de plumb se formează un precipitat negru de sulfură de plumb (4.1.1.1).
Sensibilitate: 50 ppm.
4.1.2.3. Caracterizarea sulfurilor prin formarea dioxidului de sulf la acidifiere
Se procedează conform descrierii de la 4.1.2.2. Se aduce la fierbere. Dioxidul de sulf se recunoaște după miros și prin proprietățile sale reducătoare în raport, de exemplu, cu ionii de permanganat.
4.2. Identificare prin cromatografie în strat subțire
4.2.1. Reactivi
Toți reactivii, exceptându-i pe cei pentru există precizări suplimentare, trebuie să fie de puritate analitică.
4.2.1.1. Acid mercaptoacetic (acid tioglicolic), puritate minimă determinată prin iodometrie 98 %.
4.2.1.2. Acid 2,2′-ditiodiacetic, puritate minimă determinată prin iodometrie 99 %.
4.2.1.3. Acid 2-mercaptopropionic (acid tiolactic), puritate minimă determinată prin iodometrie 95 %.
4.2.1.4. Acid 3-metcaptopropionic, puritate minimă determinată prin iodometrie 98 %.
4.2.1.5. 3-mercaptopropan-1,2-diol (1-tioglicerol), puritate minimă determinată prin iodometrie 98 %.
4.2.1.6. Plăci de strat subțire, silicagel, gata preparate, 0,25 mm grosime.
4.2.1.7. Plăci de strat subțire, oxid de aluminiu, Merck F 254 E sau echivalent.
4.2.1.8. Acid clorhidric concentrat, = 1,19 g/ml.
= 1,19 g/ml.
4.2.1.9. Acetat de etil.
4.2.1.10. Cloroform.
4.2.1.11. Eter diizopropilic.
4.2.1.12. Tetraclorură de carbon.
4.2.1.13. Acid acetic glacial.
4.2.1.14. Iodură de potasiu, soluție în apă 1 % (m/v).
4.2.1.15. Tetraclorură de platină, soluție în apă 0,1 % (m/v).
4.2.1.16. Solvenți de eluție
4.2.1.16.1. Acetat de etil (4.2.1.9), cloroform (4.2.1.10), eter diizopropilic (4.2.1.11), acid acetic (4.2.1.13) (20:20:10:10, în volume).
4.2.1.16.2. Cloroform (4.2.1.10.), acid acetic (4.2.1.13) (90:20, în volume).
4.2.1.17. Reactivi de detectare
4.2.1.17.1. Se amestecă, imediat înainte de folosire, volume egale de soluție (4.2.1.14) și soluție (4.2.1.15).
4.2.1.17.2. Soluție de brom 5 % (m/v).
Se dizolvă 5 g brom în 100 ml tetraclorură de carbon (4.2.1.12).
4.2.1.17.3. Soluție de fluoresceină 0,1 % (m/v):
Se dizolvă 100 mg fluoresceină în 100 ml etanol
4.2.1.17.4. Heptamolibdat de hexaamoniu, soluție în apă 10 % (m/v).
4.2.1.18. Soluții etalon
4.2.1.18.1. Acid mercaptoacetic (4.2.1.1), soluție în apă 0,4 % (m/v).
4.2.1.18.2. Acid 2,2′-ditiodiacetic (4.2.1.2), soluție în apă 0,4 % (m/v).
4.2.1.18.3. Acid 2-mercaptopropionic (4.2.1.3), soluție în apă 0,4 % (m/v).
4.2.1.18.4. Acid 3-mercaptopropionic (4.2.1.4), soluție în apă 0,4 % (m/v).
4.2.1.18.5. 3-mercaptopropan-1,2 diol (4.2.1.5), soluție în apă 0,4 % (m/v).
4.2.2. Aparatură
Aparatură uzuală pentru cromatografia în strat subțire.
4.2.3. Procedură
4.2.3.1. Tratamentul probelor
Se acidulează până la pH 1 cu câteva picături de acid clorhidric (4.2.1.8) și se filtrează dacă este necesar.
În anumite cazuri, poate fi indicată diluarea probei. În acest caz, se acidifiază cu acid clorhidric înainte de diluare.
4.2.3.2. Eluție
Se pune pe placă 1 μl soluție de probă (4.2.3.1.) și câte un litru din fiecare dintre cele cinci soluții etalon (4.2.1.18). Se usucă cu grijă în curent ușor de azot și se eluează placa cu solvenți (4.2.1.16.1 sau 4.2.1.16.2). Se usucă placa atât cât se poate de repede pentru a minimiza oxidarea tiolilor.
4.2.3.3 Detectare
Se pulverizează pe placă unul dintre cei trei reactivi (4.2.1.17.1, 4.2.1.17.3 sau 4.2.1.17.4). Dacă placa se pulverizează cu reactiv (4.2.1.17.3), se tratează mai departe cu vapori de brom (de exemplu într-un rezervor conținând un mic pahar de reactiv), până când petele devin vizibile. Detectarea cu pulverizare de reactiv (4.2.1.17.4) este satisfăcătoare numai dacă timpul de uscare pentru stratul subțire nu depășește 30 de minute.
4.2.3.4 Interpretare
Se compară valorile Rf și culoarea soluțiilor etalon cu cele ale standardelor. Valorile medii Rf date mai jos cu titlu informativ au valoare doar pentru comparație. Ele depind de:
|
— |
starea de activare a stratului subțire în momentul cromatografierii; |
|
— |
temperatura în rezervorul cromatografic. |
Exemple de valori Rf obținute pe un strat de silicagel
|
|
Solvenți de eluție | |
|
4.2.1.16.1 |
4.2.1.16.2 | |
|
Acid mercaptoacetic |
0,25 |
0,80 |
|
Acid 2-mercaptopropionic |
0,40 |
0,95 |
|
Acid 2,2′-ditiodiacetic |
0,00 |
0,35 |
|
Acid 3-mercaptopropionic |
0,45 |
0,95 |
|
3-mercaptopropan-1,2,-diol |
0,45 |
0,35 |
5. DETERMINARE (3) (vezi NB)
Determinarea trebuie să înceapă întotdeauna cu procedeul iodometric.
5.1. Iodometrie
5.1.1. Principiu
Determinarea se realizează prin oxidarea grupării „-SH” cu iod într-un mediu acid, conform ecuației:
2 HOOC - CH2SH + I2 → (HOOC - CH2 - S)2 + 2I– + 2H+
5.1.2. Reactivi
Iod, soluție standard 0,05 M.
5.1.3. Aparatură
Echipament de laborator obișnuit.
5.1.4. Procedură
Se cântărește cu precizie o cantitate între 0,5 și 1 g de probă, într-un pahar conic de150 ml cu capac conținând 50 ml apă distilată. Se adaugă 5 ml acid clorhidric (4.1.1.2) (pH-ul soluției aproximativ 0) și se titrează cu soluție de iod (5.1.2) până la apariția unei culorii galbene. Dacă se dorește, se poate folosi un indicator (de exemplu soluție de amidon sau tetraclorură de carbon).
5.1.5. Calcul
Conținutul de acid mercaptoacetic se calculează cu formaula:
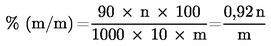
în care:
|
m |
= |
masa (în grame) a porțiunii analizate, |
|
n |
= |
volumul soluției de iod (5.1.2) folosite. |
5.1.6. Observații
Dacă rezultatul, calculat ca acid mercaptoacetic, este 0,1 % sau mult sub concentrația maximă autorizată, nu este mai necesară continuarea determinărilor. Dacă rezultatul este egal cu sau superior concentrației maxime admise și identificarea a arătat prezența unor agenți de reducere, este necesară realizarea unei determinări prin cromatografie de gaze.
5.2. Cromatografie de gaze
5.2.1. Principiu
Acidul mercaptoacetic este separat din excipient prin precipitare cu soluție de diacetat de cadmiu. După metilare cu diazometan, preparat in situ sau anterior într-o soluție de dietileter, derivatul metilic al acidului mercaptoacetic este măsurat prin cromatografie de gaz-lichid, octanoatul de metil fiind folosit ca standard intern.
5.2.2. Reactivi
Toți reactivii trebuie să fie de puritate analitică.
5.2.2.1. Acid mercaptoacetic, 98 %.
5.2.2.2. Acid clorhidric, = 1,19 g/ml.
= 1,19 g/ml.
5.2.2.3. Metanol.
5.2.2.4. Diacetat de cadmiu dihidratat, soluție în apă 10 % (m/v).
5.2.2.5. Octanoat de metil, soluție în metanol 2 % (m/v).
5.2.2.6. Soluție tampon de acetat (pH 5):
Acetat de sodiu trihidratat, 77 g.
Acid acetic (glacial), 27,5 g.
Apă demineralizată până la un volum final de 1 litru.
5.2.2.7. Acid clorhidric, soluție în metanol 3 M (5.2.2.3), proaspăt preparată.
5.2.2.8. 1-metil-3-nitro-1-nitrozoguanidină.
5.2.2.9. Hidroxid de sodiu, soluție 5 M.
5.2.2.10. Iod, soluție standard 0,05 M.
5.2.2.11. Dietileter.
5.2.2.12. Soluție de diazometan preparată din N-metil-N-nitrozotoluen-4-sulfonamidă (Fieser, Reagents for Organic Synthesis (Wiley), 1967).
Soluția obținută conține aproximativ 1,5 g diazometan în 100 ml dietileter. Diazometanul fiind un gaz toxic și foarte instabil, toate experimentele trebuie efectuate sub o hotă puternică și trebuie evitată folosirea aparaturii din sticlă cu dop rodat (în acest scop există truse speciale).
5.2.3. Aparatură
5.2.3.1. Aparatură obișnuită de laborator.
5.2.3.2. Aparatură pentru prepararea diazometanului in situ (vezi Fales, H.M., Jaouni, T.M. și Babashak, J.F. Analyt. Chem. 1973, 45, 2302).
5.2.3.3. Aparatură pentru pregătirea avansată a diazometanului (Fieser).
5.2.4. Pregătirea probei
Într-o eprubetă de centrifugare de 50 ml se cântărește precis o cantitate suficientă de probă pentru a obține cantitatea preconizată de 50 până la 70 mg acid mercaptoacetic. Se acidulează cu câteva picături de acid clorhidric (5.2.2.2.) pentru a obține un pH de aproximativ 3.
Se adaugă 5 ml apă demineralizată și 10 ml soluție tampon de acetat (5.2.2.6).
Se verifică cu hârtie de pH dacă valoarea pH-ului este aproximativ 5, apoi se adaugă 5 ml soluție de diacetat de cadmiu (5.2.2.4).
Se așteaptă 10 minute și apoi se centrifughează pentru cel puțin 15 minute la 4 000 g. Se îndepărtează lichidul supernatant, care poate conține o grăsime insolubilă (în cazul produselor cremă). Această grăsime nu poate fi confundată cu tiolii care se colectează într-o masă compactă la fundul eprubetei. Se verifică să nu se producă nici o precipitare la adăugarea câtorva picături de soluție de diacetat de cadmiu (5.2.2.4.) la supernatant.
Când identificarea anterioară nu a relevat alți agenți reductori în afară de tioli, se verifică iodometric dacă tiolul prezent în lichidul supernatant nu depășește 6 până la 8 % din cantitatea inițială.
Se introduc 10 ml metanol (5.2.2.3) într-o eprubetă de centrifugare conținând precipitatul și se dispersează fin precipitatul cu o tijă agitatoare. Se centrifughează din nou pentru cel puțin 15 minute la 4 000 g. Se scurge supernatantul și se verifică absența tiolilor.
Se spală precipitatul a doua oară urmând același procedeu.
Folosind în continuare aceeași eprubetă de centrifugă, se adaugă:
|
— |
2 ml soluție octaonat de metil (5.2.2.5); |
|
— |
5 ml de acid clorhidric în metanol (5.2.2.7). |
Se dizolvă complet tiolii (din excipient poate persista puțină materie insolubilă). Aceasta este soluția „S”.
Cu o porțiune din această soluție se verifică iodometric dacă conținutul de tioli este de cel puțin 90 % din cel obținut la 5.1.
5.2.5. Metilare
Metilarea se realizează fie prin preparare in situ (5.2.5.1), fie cu soluția de diazometan preparată anterior (5.2.5.2).
5.2.5.1. Metilare in situ
În aparatura de metilare (5.2.3.2) conținând 1 ml de eter (5.2.2.11) se introduc 50 μl soluție „S” și se metilează prin metoda (5.2.3.2) cu aproximativ 300 mg 1-metil-3-nitro-1-nitrozoguanidină (5.2.2.8). După 15 minute (soluția de eter trebuie să fie galbenă pentru a indica excesul de diazometan) se transferă soluția probă într-un flacon de 2 ml având un dop etanș. Se depozitează în frigider peste noapte. Se metilează două probe simultan.
5.2.5.2. Metilare cu soluție de diazometan preparată anterior
Într-un pahar cu dop de 5 ml se introduc 1 ml soluție de diazometan (5.2.2.12), apoi 50 μl soluție „S”. Se lasă în frigider peste noapte.
5.2.6. Preparare standard
Se prepară o soluție standard de acid mercaptoacetic (5.2.2.1) de concentrație cunoscută, conținând aproximativ 60 mg acid mercaptoacetic pur (5.2.2.1) la 2 ml.
Aceasta este soluția „E”.
Se precipită, determină și metilează conform 5.2.4 și 5.2.5.
5.2.7. Condiții pentru cromatografia de gaze
5.2.7.1. Coloană
Tip: oțel inoxidabil
Lungime: 2 m
Diametru: 3 mm
5.2.7.2. Umplutură
2 % didecil ftalat/chromosorb, WAW 80-100 ochiuri.
5.2.7.3. Detector
Ionizare cu flacără. O reglare adecvată a sensibilității electrometrului detectorului cu ionizare cu flacără este 8 × 10-10 A.
5.2.7.4. Alimentări cu gaz
Gaz purtător: azot.
|
|
presiune: 2,2 bar, |
|
|
debit: 35 ml/min. |
Gaz auxiliar: hidrogen.
|
|
presiune: 1,8 bar, |
|
|
debit: 15 ml/min. |
Alimentare-detector în conformitate cu indicațiile producătorilor aparatului.
5.2.7.5. Condiții de temperatură
Injector: 200 °C
Detector: 200 °C
Coloană: 90 °C
5.2.7.6. Viteza graficului de înregistrare
5 mm/min.
5.2.7.7. Cantitate injectată
3 μl. Se realizează cinci injectări.
5.2.7.8. Condițiile cromatografiei sunt date informativ. Ele permit realizarea unei rezoluții „R” egală cu 1,5 sau superioară, unde:
![]()
fie:
|
r1 și r2 |
= |
timpi de retenție (în minute), |
|
W1 și W2 |
= |
lățimile vârfurilor la jumătatea înălțimii (în milimetri), |
|
d′ |
= |
viteza graficului (în milimetri pe minut). |
Se recomandă ca procesul de cromatografiere să se termine prin reglarea temperaturii de la 90 la 150 °C cu o viteză de 10 °C pe minut, pentru a elimina substanțele care sunt susceptibile a interfera cu măsurătorile ulterioare.
5.2.8. Calcul
5.2.8.1. Coeficientul de proporționalitate pentru acidul mercaptoacetic
Acesta se calculează față de octanoatul de metil, pe baza unui amestec standard.
Dacă „t” reprezintă acidul mercaptoacetic:
fie:
|
kt |
= |
factorul său de răspuns, |
|
m′t |
= |
masa sa (în miligrame) în amestec, |
|
S′t |
= |
suprafața vârfului său. |
Dacă „c” reprezintă octanoatul de metil:
fie:
|
m′c |
= |
masa sa (în miligrame) în amestec, |
|
S′c |
= |
suprafața vârfului său, |
atunci:
![]()
Acest coeficient variază în funcție de aparatura folosită.
5.2.8.2. Concentrația de acid mercaptoacetic prezent în probă
Dacă „t” reprezintă acidul mercaptoacetic:
fie:
|
kt |
= |
factorul său de răspuns, |
|
St |
= |
suprafața vârfului său |
Dacă „c” reprezintă octanoatul de metil:
fie:
|
mc |
= |
masa sa (în miligrame) în amestec, |
|
Sc |
= |
suprafața vârfului său, |
|
M |
= |
masa (în miligrame) a porțiunii analizate inițiale, |
atunci procentul % (m/m) de acid mercaptoacetic prezent în probă este:

6. REPETABILITATE (2)
Pentru un conținut de acid mercaptoacetic de 8 % (m/m), diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 0,8 % (m/m).
IDENTIFICAREA ȘI DETERMINAREA HEXACLOROFENULUI
A. IDENTIFICARE
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă este adecvată pentru toate produsele cosmetice.
2. PRINCIPIU
Hexaclorofenul din probă este extras cu acetat de etil și identificat prin cromatografie în strat subțire.
3. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
3.1. Acid sulfuric, soluție 4 M.
3.2. Celită AW.
3.3. Acetat de etil.
3.4. Solvent de eluție: Benzen conținând 1 % (v/v) acid acetic glacial.
3.5. Agent de vizualizare I:
Soluție Rodamină B: se dizolvă 100 mg Rodamină B într-un amestec de 150 ml dietileter, 70 ml etanol absolut și 16 ml apă.
3.6. Agent de vizualizare II:
Soluție 2,6-dibromo-4-(cloroimino)ciclohexa-2,5-dienonă: se dizolvă 400 mg 2,6-dibromo-4-(cloroimino)ciclohexa-2,5-dienonă în 100 ml metanol (se prepară proaspăt zilnic).
Soluție carbonat de sodiu: se dizolvă 10 g carbonat de sodiu în 100 ml de apă demineralizată.
3.7. Soluție etalon:
Hexaclorafen, soluție 0,05 % (m/v) în acetat de etil.
4. APARATURĂ
4.1. Plăci pentru cromatografie în strat subțire Kiesel gel 254, 200 x 200 mm (sau echivalent).
4.2. Echipament uzual pentru cromatografia în strat subțire.
4.3. Baie termostatizată la 26 °C pentru tancul cromatografic.
5. PREGĂTIREA PROBEI ANALIZATE
5.1. Se amestecă foarte bine 1 g de probă omogenizată cu 1 g de Celită AW (3.2) și 1 ml acid sulfuric (3.1).
5.2. Se usucă la 100 °C timp de 2 ore.
5.3. Se răcește și se mărunțește fin reziduul.
5.4. Se extrage de două ori cu câte 10 ml acetat de etil (3.3), se centrifughează după fiecare extracție și se combină straturile de acetat de etil.
5.5. Se evaporă la 60 °C.
5.6. Se dizolvă reziduul în 2 ml acetat de etil (3.3).
6. PROCEDURĂ
6.1. Se pun 2 μl din soluția de probă analizată (5.6) și 2 μl din soluția etalon (3.7) pe placa de cromatografie în strat subțire (4.1).
6.2. Se saturează tancul (4.3) cu solvent de eluție (3.4).
6.3. Se pune placa în tanc și se eluează până la 150 mm.
6.4. Se scoate placa și se usucă într-un cuptor ventilat, la o temperatură de aproximativ 105 °C.
6.5. Vizualizare
Petele de hexaclorofen de pe placă se vizualizează conform indicațiilor de la 6.5.1 sau 6.5.2.
6.5.1. Se pulverizează uniform pe placă agent de vizualizare I (3.5). După 30 de minute se examinează placa la lumină UV 254 nm.
6.5.2. Se pulverizează uniform pe placă soluția de 2,6-dibromo-4-(cloroimino)ciclohexa-2,5-dienonă, agent de vizualizare II (3.6). După aceea se pulverizează pe placă o soluție de carbonat de sodiu (3.6). Se examinează placa la lumina zilei după 10 minute de uscare la temperatura camerei.
7. INTERPRETARE
7.1. Agent de vizualizare I (3.5):
Hexaclorofenul este indicat de o pată albăstruie pe un fond fluorescent galben-portocaliu și are o valoare a Rf de aproximativ 0,5.
7.2. Agent de vizualizare II (3.6):
Hexaclorofenul este indicat de o pată azurie spre turcoaz pe un fond alb și are o valoare a Rf de aproximativ 0,5.
B. DETERMINARE
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă se aplică tuturor produselor cosmetice.
2. DEFINIȚIE
Conținutul de hexaclorofen în probă determinat conform acestei metode este exprimat în procente masice de hexaclorofen.
3. PRINCIPIU
Hexaclorofenul este determinat, după conversia la derivat metilat, prin cromografie de gaze cu detector cu captură de electroni.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. Acetat de etil.
4.2. N-metil-N-nitrozo-p-toluensulfonamidă (diazald).
4.3. Dietileter.
4.4. Metanol.
4.5. 2-(2-etoxietoxi)etanol (carbitol).
4.6. Acid formic.
4.7. Hidroxid de potasiu, soluție apoasă 50 % (m/m) (proaspăt preparată zilnic).
4.8. Hexan pentru spectroscopie.
4.9. Bromclorofen (standard nr. 1).
4.10. 4,4′,6,6′-tetracloro-2,2′-tiodifenol (standard nr. 2).
4.11. 2,4,4′-tricloro-2-hidroxi-difenileter (standard nr. 3).
4.12. Acetonă.
4.13. Acid sulfuric 4 M.
4.14. Celită AW.
4.15. Acid formic/acetat de etil, soluție 10 % (v/v).
4.16. Hexaclorofen.
5. APARATURĂ
5.1. Sticlărie de laborator obișnuită.
5.2. Miniaparat pentru prepararea diazometanului (Analyt. Chem. 1973, 45,2302-2).
5.3. Cromatograf de gaze echipat cu un detector cu captură de electroni cu sursă 63 Ni.
6. PROCEDURĂ
6.1. Pregătirea soluției standard
Standardul este ales astfel încât să nu interfereze cu nici o substanță conținută în excipientul produsului analizat. De obicei, standardul nr. 1 este cel mai adecvat (4.9).
6.1.1. Într-un balon cotat de 100 ml se cântăresc cu precizie 50 mg standard nr. 1, 2 sau 3 (4.9, 4.10 sau 4.11) și 50 mg hexaclorofen (4.16). Se aduce la semn cu acetat de etil (4.1) (soluție A). Se diluează 10 ml soluție A cu acetat de etil (4.1) până la 100 ml (soluție B).
6.1.2. Într-un balon cotat de 100 ml se cântăresc cu precizie 50 mg de standard nr. 1, 2 sau 3 (4.9, 4.10 sau 4.11). Se aduce la semn cu acetat de etil (4.1) (soluție C).
6.2. Pregătirea probei (4)
Se cântărește cu precie 1 g probă omogenizată și se amestecă foarte bine cu 1 ml acid sulfuric (4.13), 15 ml acetonă (4.12) și 8 g Celită AW (4.14). Se usucă amestecul la aer pe o baie de abur timp de 30 minute, apoi se usucă o oră și jumătate într-un cuptor cu ventilație. Se răcește, se mărunțește fin reziduul și se transferă într-o coloană de sticlă.
Se eluează cu acetat de etil (4.1) și se colectează 100 ml. Se adaugă 2 ml soluție standard intern (soluție C) (6.1.2).
6.3. Metilarea probei
Se răcesc toți reactivii și aparatura între 0 și 4 °C timp de două ore. În compartimentul exterior al aparaturii de diazometan se pun 1,2 ml soluție obținută la 6.2. și 0,1 ml metanol (4.4). Se pun aproximativ 200 mg diazald (4.2) în rezervorul central, se adaugă 1 ml carbitol (4.5) și 1 ml dietileter (4.3) și se dizolvă. Se asamblează aparatul, se imersează pe jumătate într-o baie la 0 °C și se introduce cu seringa în rezervorul central aproximativ 1 ml soluție de hidroxid de potasiu răcită (4.7). Se asigură persistența culorii galbene obținute prin formarea diazometanului. Dacă culoarea galbenă nu persistă, se repetă metilarea cu alte 200 mg diazald (4.2) (5).
Aparatul se îndepărtează din baie după 15 minute, apoi se lasă închis la temperatură ambiantă timp de 12 ore. Se deschide aparatul, se tratează excesul de diazometan prin adăugarea câtorva picături de soluție de acid formic 10 % (v/v) în acetat de etil (4.15) și se transferă soluția organică într-un balon cotat de 25 ml. Se aduce la semn cu hexan (4.8).
Se injectează 1,5 μl din această soluție în cromatograf.
6.4. Metilarea soluției standard
Se răcesc toți reactivii și aparatura între 0 și 4 °C timp de două ore. Se introduc în compartimentul extern al aparatului pentru diazometan următoarele:
|
|
0,2 ml soluție B (6.1.1), |
|
|
1 ml acetat de etil (4.1), |
|
|
0,1 ml metanol (4.4). |
Se continuă metilarea conform descrierii de la 6.3. Se injectează în cromatograf 1,5 μl din soluția rezultată.
7. CROMATOGRAFIE DE GAZE
Coloana trebuie să realizeze o rezoluție „R” egală cu 1,5 sau superioară, unde:
![]()
fie:
|
r1 și r2 |
= |
timpii de retenție (în minute), |
|
W1 și W2 |
= |
lățimea vârfurilor la jumătatea înălțimii (în milimetri), |
|
d |
= |
viteza graficului (în milimetri per minut). |
Următoarele condiții au fost găsite adecvate pentru cromatografia de gaze:
Coloană: oțel inoxidabil.
Lungime: 1,7 m.
Diametru: 3 mm.
Suport:
|
|
chromosorb: WAW |
|
|
analiza sitei: 80-100 ochiuri |
Fază staționară: 10 % OV 17.
Temperaturi:
|
|
coloană: 280 °C, |
|
|
injector: 280 °C, |
|
|
detector: 280 °C. |
Gaz purtător: oxigen - liber de azot.
Presiune: 2,3 bar.
Debit: 30 l/min.
8. CALCUL
8.1. Coeficientul de proporționalitate al hexaclorofenului
Acesta este calculat în raport cu standardele alese față de amestecul standard.
Fie:
|
h |
= |
hexaclorofenul, |
|
kh |
= |
coeficientul său de proporționalitate, |
|
m′h |
= |
masa sa (în grame) în amestec, |
|
A′h |
= |
suprafața vârfului său, |
|
s |
= |
standardul ales, |
|
m′s |
= |
masa sa (în grame) în amestec, |
|
A′s |
= |
suprafața vârfului său, |
atunci:
![]()
8.2. Cantitatea de hexaclorofen în probă
Fie:
|
h |
= |
hexaclorofenul, |
|
kh |
= |
coeficientul său de proporționalitate, |
|
Ah |
= |
suprafața vârfului său, |
|
s |
= |
standardul ales, |
|
ms |
= |
masa sa (în grame) în amestec, |
|
As |
= |
suprafața vârfului său, |
|
M |
= |
masa (în grame) probei prelevate, |
atunci procentul % (m/m) de hexaclorofen din probă este:

9. REPETABILITATE (2)
Pentru un conținut de hexaclorofen de 0,1 % (m/m), diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 0,005 % (m/m).
DETERMINAREA CANTITATIVĂ A TOSILCLORAMIDEI DE SODIU (CLORAMINĂ-T)
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă se referă la determinarea cantitativă prin cromatografie în strat subțire a tosilcloramidei de sodiu (cloramină-T) în produsele cosmetice.
2. DEFINIȚIE
Conținutul de cloramină-T din probă, determinat conform acestei metode, este exprimat ca procentaj masic (m/m).
3. PRINCIPIU
Cloramina-T este hidrolizată complet la 4-toluensulfonamidă prin fierbere cu acid clorhidric.
Cantitatea de 4-toluensulfonamidă formată este determinată foto-densitometric prin cromatografie în strat subțire.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. Tosilcloramidă de sodiu (cloramină-T).
4.2. Soluție standard de 4-toluensulfonamidă: 50 mg 4-toluensulfonamidă în 100 ml etanol (4.5).
4.3. Acid clorhidric, 37 % (m/m), = 1,18 g/ml.
= 1,18 g/ml.
4.4. Dietileter.
4.5. Etanol, 96 % (v/v).
4.6. Solvent de developare
4.6.1. 1-butanol/etanol (4.5)/apă (40:4:9; v/v/v) sau
4.6.2. cloroform/acetonă (6:4; v/v).
4.7. Plăci pentru cromatografie în strat subțire gata pregătite, silicagel 60, fără indicator fluorescent.
4.8. Permanganat de potasiu.
4.9. Acid clorhidric, 15 % (m/m).
4.10. Reactiv pulverizat: 2-toluidină, soluție în etanol 1 % (m/v) (4.5).
5. APARATURĂ
5.1. Aparatură de laborator obișnuită.
5.2. Echipament uzual pentru cromatografie în strat subțire.
5.3. Fotodensitometru.
6. PROCEDURĂ
6.1. Hidroliză
Într-un balon de 50 ml cu fundul rotund se cântărește cu precizie aproximativ 1 g de probă („m”). Se adaugă 5 ml apă și 5 ml acid clorhidric (4.3) și se fierbe o oră folosind un condensator de reflux. Se transferă imediat suspensia fierbinte cu apă într-un balon gradat de 50 ml. Se lasă să se răcească și se completează până la semn cu apă. Se centrifughează la cel puțin 3 000 rpm timp de 5 minute și se trece lichidul supernatant printr-un filtru.
6.2. Extracție
6.2.1. Se iau 30 ml din filtrat și se extrage de trei ori cu 15 ml dietileter (4.4). Dacă este necesar, se usucă fazele eterice și se colectează într-un balon cotat de 50 ml. Se aduce la semn cu dietileter (4.4).
6.2.2. Se iau 25 ml extract eteric uscat și se evaporă până la uscare totală într-un curent de azot. Se dizolvă din nou reziduul cu 1 ml etanol (4.5).
6.3. Cromatografie în strat subțire
6.3.1. Se picură 20 μl reziduu etanolic (6.2) pe o placă de cromatografie în strat subțire (4.7).
În același timp și în același mod, se picură 8, 12, 16 și 20 μl de soluție standard de 4-toluensulfonamidă.
6.3.2. Se lasă să se developeze aproximativ 150 mm în solvent de developare (4.6.1 sau 4.6.2).
6.3.3. După evaporarea completă a solventului de developare, se pune placa pentru două sau trei minute într-o atmosferă de vapori de clor, produsă turnând 100 ml acid clorhidric (4.9) peste aproximativ 2 g permanganat de potasiu (4.8) într-un vas închis. Se îndepărtează excesul de clor prin încălzirea plăcii la 100 °C timp de cinci minute, apoi se pulverizează reactiv (4.10) pe placă.
6.4. Măsurare
După aproximativ o oră se măsoară petele violete prin intermediul unui fotodensitometru la 525 nm.
6.5. Trasarea curbelor de etalonare
Se trasează valorile înălțimii vârfului maxim descoperite pentru petele de 4-toluensulfonamidă față de cantitățile corespunzătoare de 4 -toluensulfonamidă (adică 4, 6, 8, 10 μg 4-toluensulfonamidă pe pată)
7. NOTĂ
Metoda poate fi controlată prin folosirea unei soluții de 0,1 sau 0,2 % (m/v) cloramină-T (4.1) tratată în același mod ca proba (6).
8. CALCUL
Conținutul de cloramină-T din probă, exprimat ca procent masic, se calculează astfel:
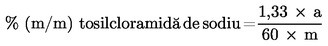
unde:
|
1,33 |
= |
factor de conversie 4-toluensulfonamidă – cloramină-T, |
|
a |
= |
cantitatea (în μg) de 4-toluensulfonamidă în probă citită de pe curbele de etalonare, |
|
m |
= |
masa (în grame) a probei analizate. |
9. REPETABILITATE (2)
Pentru un conținut de cloramină-T de aproximativ 0,2 % (m/m) diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 0,03 % (m/m).
DETERMINAREA FLUORULUI TOTAL ÎN PASTELE DE DINȚI
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă este destinată determinării fluorului total în pastele de dinți. Este adecvată pentru nivele care nu depășesc 0,25 %.
2. DEFINIȚIE
Conținutul de fluor din probă determinat conform acestei metode este exprimat ca procent masic.
3. PRINCIPIU
Determinarea este realizată prin cromatografie de gaze. Fluorul din compușii conținând fluor este convertit la trietilfluorsilan (TEFS) prin reacție directă cu clortrietilsilan (TECS) în soluție acidă și extras simultan cu xilen conținând ciclohexan ca standard intern.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. Fluorură de sodiu, uscată la 120 °C la masă constantă.
4.2. Apă, dublu distilată sau de calitate echivalentă.
4.3. Acid clorhidric,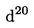 = 1,19 g/ml.
= 1,19 g/ml.
4.4. Ciclohexan (CH).
4.5. Xilen fără vârfuri în cromatogramă anterioare vârfului solventului când se cromatografiază în aceleași condiții ca și proba (6.1). Dacă este necesar, se purifică prin distilare (5.8).
4.6. Cloretrietilsilan (TECS Merck sau un echivalent).
4.7. Soluții standard de fluor
4.7.1. Soluție stoc, 0,250 mg F–/ml. Se cântăresc cu precizie 138,1 mg fluorură de sodiu (4.1) și se dizolvă în apă (4.2). Se transferă cantitativ soluția într-un balon cotat de 250 ml (5.5). Se diluează până la semn cu apă (4.2) și se amestecă.
4.7.2. Soluție stoc diluată, 0,050 mg F–/ml. Se transferă cu pipeta 20 ml din soluția stoc (4.7.1) într-un balon cotat de 100 ml (5.5). Se diluează până la semn cu apă (4.2) și se amestecă.
4.8. Soluție de standard intern
Se amestecă 1 ml ciclohexan (4.4) cu 5 ml xilen (4.5).
4.9. Clortrietilxilan/soluție de standard intern
Se transferă, cu pipeta (5.7), 0,06 ml TECS (4.6) și 0,12 ml soluție de standard intern (4.8) într-un balon cotat de 10 ml. Se diluează cu xilen (4.5) până la semn și se amestecă. Se prepară proaspăt zilnic.
4.10. Acid percloric, 70 % (m/v).
4.11. Acid percloric, 20 % (m/v) în apă (4.2).
5. APARATURĂ
5.1. Echipament de laborator obișnuit.
5.2. Cromatograf de gaze cu un detector cu ionizare cu flacără.
5.3. Amestecător turbionar Vortex sau echivalent.
5.4. Bühler, vibrator, tip SMB1 sau echivalent.
5.5. Baloane cotate de 100 și 250 ml, din polipropilenă.
5.6. Eprubete de centrifugă (sticlă); 20 ml cu capac filetat teflonat, Sovirel tip 611-56 sau echivalent. Se curăță eprubetele și dopurile prin plasare în acid perclorhidric (4.11) timp de câteva ore, urmată de cinci clătiri ulterioare cu apă (4.2) și în final de uscare la 100 °C.
5.7. Pipete reglabile pentru distribuirea de volume între 50 și 200 μl, cu vârfuri de plastic detașabile.
5.8. Aparat de distilare, echipat cu coloană Schneider cu trei bule sau cu o coloană Vigreux echivalentă.
6. PROCEDURĂ
6.1. Analiza probei
6.1.1. Se selectează un tub de pastă de dinți care nu a mai fost deschis, se deschide și se scoate tot conținutul. Se transferă într-un recipient de plastic, se amestecă în întregime și se păstrează în condiții care nu permit deteriorarea.
6.1.2. Se cântăresc cu precizie 150 mg („m”) din probă într-o eprubetă de centrifugare (5.6), se adaugă 5 ml apă (4.2) și se omogenizează (5.3).
6.1.3. Se adaugă 1 ml xilen (4.5).
6.1.4. Se adaugă cu picătura 5 ml acid clorhidric (4.3) și se omogenizează (5.3).
6.1.5. Se adaugă cu pipeta 0,5 ml clorotrietilsilan/soluție de standard intern (4.9) într-o eprubetă de centrifugă (5.6).
6.1.6. Se închide eprubeta cu un dop filetat (5.6) și se amestecă în întregime timp de 45 de minute pe un vibrator (5.4.) reglat la 150 de mișcări per minut.
6.1.7. Se centrifughează 10 minute la o viteză care să determine o separare netă a fazelor, se deschide eprubeta, se scoate stratul organic și se injectează 3 μl din faza organică în coloana cromatografului de gaze (5.2).
Observație: Este nevoie de aproximativ 20 de minute pentru ca toți componenții să fie eluați.
6.1.8. Se repetă injectarea, se calculează raportul suprafețelor medii ale vârfurilor (ATEFS/ACH) și se citește cantitatea corespunzătoare de fluor [în miligrame („m1”)] de pe curba de etalonare (6.3).
6.1.9. Se calculează conținutul total de fluor din probă (în procente masice de fluor), după cum este indicat la paragraful 7.
6.2. Condiții de cromatografiere
6.2.1. Coloana: oțel inoxidabil.
Lungime: 1,8 m.
Diametru: 3 mm.
Suport: Gaschrom Q80-100 ochiuri.
Fază staționară: ulei siliconic DC 200 sau echivalent, 20 %. Se condiționează coloana peste noapte la 100 °C (debit de gaz purtător la 25 ml azot pe minut) și se repetă în fiecare noapte. După fiecare 4 sau 5 injectări, se recondiționează coloana prin încălzire pentru 30 de minute la 100 °C.
Temperaturi:
|
|
coloană: 70 °C, |
|
|
injector: 150 °C, |
|
|
detector: 250 °C. |
Debit de gaz purtător: 35 ml azot per minut.
6.3. Curba de etalonare
6.3.1. Se pun cu pipeta în șase eprubete de centrifugă (5.6) 0, 1, 2, 3, 4 și 5 ml soluție standard de fluor diluată (4.7.2). Se aduce la un volum de 5 ml cu apă (4.2).
6.3.2. Se procedează conform descrierii de la 6.1.3 până la 6.1.6 inclusiv.
6.3.3. Se injectează 3 μl din faza organică în coloana cromatografului de gaze (5.2).
6.3.4. Se repetă injectarea și se calculează raportul mediu al vârfurilor (ATEFS/ACH).
6.3.5. Se trasează curba de etalonare corelând masa de fluor (în miligrame) în soluțiile standard (6.3.1) cu raportul suprafeței de vârf ATEFS/ACH măsurat în condițiile 6.3.4. Se unesc punctele graficului cu linia dreaptă interpolată cel mai bine calculată, prin analiză de regresie.
7. CALCUL
Concentrația conținutului de total fluor din probă (în procente masice de fluor) (% (m/m) F) este dată de:

unde:
|
m |
= |
porțiunea analizată (în miligrame) (6.1.2), |
|
m1 |
= |
cantitatea de F (în miligrame) citită de pe curba de etalonare (6.1.8). |
8. REPETABILITATE (2)
Pentru un conținut de fluor de aproximativ 0,15 % (m/m), diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească în valoare absolută de 0,012 % (m/m).
IDENTIFICAREA ȘI DETERMINAREA COMPUȘILOR ORGANOMERCURICI
OBIECTUL ȘI DOMENIUL DE APLICARE
Metoda descrisă mai jos poate fi utilizată pentru identificarea și determinarea derivaților organomercurici introduși cu rol de conservanți în produsele cosmetice pentru ochi. Este aplicabilă tiomersalului (INN) (2-(etilmercuritio)benzoat de sodiu) și fenilmercurului și sărurilor sale.
A. IDENTIFICARE
1. PRINCIPIU
Compușii organomercurici sunt complexați cu 1,5-difenil-3-tiocarbazonă. După extracția ditizonatului cu tetraclorură de carbon, se realizează cromatografia în strat subțire pe silicagel. Petele de ditizonați apar colorate portocaliu.
2. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
2.1. Acid sulfuric, 25 % (v/v).
2.2. 1,5-difenil-3- tiocarbazonă (ditizonă): 0,8 mg în 100 ml tetraclorură de carbon (2.4).
2.3. Azot.
2.4. Tetraclorură de carbon.
2.5. Solvent de developare: hexan/acetonă, 90:10 (v/v).
2.6. Soluție standard, 0,001 % în apă, de:
2-(etilmercuritio)benzoat de sodiu,
clorură de etilmercur sau clorură de metilmercur,
nitrat de fenilmercur sau acetat de fenilmercur,
diclorură de mercur sau diacetat de mercur.
2.7. Plăcuțe cu silicagel gata preparate (de ex. Merck 5721 sau echivalent).
2.8. Clorură de sodiu.
3. APARATURĂ
3.1. Echipament de laborator obișnuit.
3.2. Aparatură obișnuită pentru cromatografie în strat subțire.
3.3. Filtru pentru separarea fazelor.
4. PROCEDURĂ
4.1. Extracție
4.1.1. Se diluează 1 g de probă într-o eprubetă de centrifugă, prin titrare cu 20 ml apă distilată. Se obține dispersia maximă și se încălzește la 60 °C pe baie de apă. Se adaugă 4 g clorură de sodiu (2.8). Se agită. Se lasă să se răcească.
4.1.2. Se centrifughează timp de cel puțin 20 de minute la 4 500 rot/minut pentru a separa cea mai mare parte a solidului de lichid. Se filtrează printr-o pâlnie de separare și se adaugă 0,25 ml soluție de acid sulfuric (2.1).
4.1.3. Se extrage de mai multe ori cu 2 sau 3 ml soluție de ditizonă (2.2), până când ultima fază organică rămâne verde.
4.1.4. Se filtrează secvențial fiecare fază organică printr-un filtru separator de faze (3.3).
4.1.5. Se evaporă până la uscare totală într-un curent de azot.
4.1.6. Se dizolvă cu 0,5 ml de tetraclorură de carbon (2.4). Se folosește această soluție imediat, conform 4.2.1.
4.2. Separare și identificare
4.2.1. Se pun imediat 50 μl soluție de tetraclorură de carbon obținută la 4.1.6 pe o placă cu silicagel (2.7). Se tratează simultan 10 ml soluție standard (2.6) ca la 4.1 și se pun 50 μl din soluția obținută la 4.1.6. pe aceeași placă.
4.2.2. Se pune placa în solvent (2.5) și se lasă acesta să avanseze 150 mm. Compușii organomercurici apar ca pete colorate a căror culoare este stabilă, dacă placa este acoperită cu o placă de sticlă imediat după evaporarea solventului.
Ca exemplu, s-au obținut următoarele valori Rf:
|
|
Rf |
Culoare |
|
Tiomersal |
0,33 |
portocaliu |
|
Clorură de etilmercur |
0,29 |
portocaliu |
|
Clorură de metilmercur |
0,29 |
portocaliu |
|
Săruri fenilmercurice |
0,21 |
portocaliu |
|
Săruri mercurice (II) |
0,10 |
portocaliu |
|
Diacetat de mercur |
0,10 |
portocaliu |
|
1,5-difenil-3-tiocarbazonă |
0,09 |
roz |
B. DETERMINARE
1. DEFINIȚIE
Conținutul de compuși organomercurici determinat prin această metodă este exprimat în procente de masă (m/m) ca mercur în probă.
2. PRINCIPIU
Metoda constă în măsurarea cantității totale de mercur prezent. De aceea sunt necesare verificarea absenței mercurului în stare anorganică și identificarea derivatul organomercuric conținut în probă. După mineralizare, mercurul eliberat este măsurat prin absorbție atomică fără flacără.
3. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
3.1. Acid azotic concentrat, = 1,41 g/ml.
= 1,41 g/ml.
3.2. Acid sulfuric concentrat = 1,84 g/ml.
= 1,84 g/ml.
3.3. Apă redistilată.
3.4. Permanganat de potasiu, soluție 7 % (m/v).
3.5. Clorură de hidroxilamoniu, soluție 1,5 % (m/v).
3.6. Peroxodisulfat bipotasic, soluție 5 % (m/v).
3.7. Diclorură de staniu, soluție 10 % (m/v).
3.8. Acid clorhidric concentrat, = 1,18 g/ml.
= 1,18 g/ml.
3.9. Diclorură de paladiu impregnată pe vată de sticlă, 1 % (m/m).
4. APARATURĂ
4.1. Echipament de laborator obișnuit.
4.2. Aparatură pentru determinarea mercurului prin absorbție atomică fără flacără (tehnica vaporilor reci), inclusiv sticlăria necesară. Lungimea de cale a cuvei cel puțin 100 mm.
5. PROCEDURĂ
Se iau toate măsurile normale de protecție pentru analiza urmelor de mercur.
5.1. Separare
5.1.1. Se cântăresc cu precizie 150 mg probă („m”). Se adaugă 10 ml acid azotic (3.1) și se lasă timp de 3 ore într-un pahar etanș pus într-o baie de apă la 55 °C, agitându-l la intervale regulate. În același timp se realizează un test orb pe reactivi.
5.1.2. După răcire se adaugă 10 ml acid sulfuric (3.2) și se lasă din nou în baia de apă la 55 °C timp de 30 de minute.
5.1.3. Se pune paharul într-o baie de gheață și se adaugă cu grijă 20 ml apă (3.3).
5.1.4. Se adaugă o porțiune de 2 ml soluție de permanganat de potasiu 7 % (3.4), până când soluția rămâne colorată. Se pune din nou în baia de apă la 55 °C pentru alte 15 minute.
5.1.5. Se adaugă 4 ml soluție de peroxodisulfat de dipotasiu (3.6). Se continuă încălzirea în baie de apă la 55 °C pentru 30 de minute.
5.1.6. Se lasă la răcit și se transferă conținutul paharului într-un balon cotat de 100 ml. Se clătește vasul cu 5 ml clorură de hidroxilamoniu (3.5) și apoi se clătește de patru ori cu 10 ml apă (3.3). Soluția trebuie să fie complet decolorată. Se aduce la semn cu apă (3.3).
5.2. Determinare
5.2.1. Se pun 10 ml de soluție analizată (5.1.6) într-un vas de sticlă pentru determinarea mercurului în vapori reci (4.2). Se diluează cu 100 ml apă (3.3) și consecutiv cu 5 ml acid sulfuric (3.2) și 5 ml soluție diclorură de staniu (3.7). Se amestecă după fiecare adăugare. Se așteaptă 30 de secunde pentru reducerea tuturor ionilor de mercur la stare metalică și se face o citire („n”).
5.2.2. Se pune vată de sticlă impregnată cu diclorură de paladiu (3.9) între vasul de reducere a mercurului și cuva de curgere a instrumentului (4.2). Se repetă 5.2.1 și se înregistrează citirea. Dacă citirea nu este zero, mineralizarea nu a fost completă și analiza trebuie repetată.
6. CALCUL
Fie:
|
m |
= |
masa (în miligrame) a probei de testare, |
|
n |
= |
cantitatea de mercur (în μg) citită pe instrument. |
Cantitatea de mercur, exprimată ca mercur, în procente de masă, se calculează cu formula:

7. OBSERVAȚII
7.1. Pentru îmbunătățirea mineralizării, poate fi necesar să se înceapă prin diluarea probei.
7.2. Dacă se suspectează absorbția mercurului pe substrat, trebuie făcută o determinare cantitativă prin metoda adaosurilor standard.
8. REPETABILITATE (2)
În cazul unei concentrații de mercur de 0,007 %, diferența dintre rezultatele a două determinări efectuate în paralel pe acceeși probă nu trebuie să depășească o valoare absolută de 0,00035 %.
DETERMINAREA SULFURILOR ALCALINE ȘI ALCALINO- PĂMÂNTOASE
1. OBIECTUL ȘI DOMENIUL DE APLICARE
Prezenta metodă descrie determinarea sulfurilor prezente în produsele cosmetice. Prezența tiolilor sau a altor agenți reducători (inclusiv sulfiții) nu interferează.
2. DEFINIȚIE
Concentrația sulfurilor determinată prin această metodă se exprimă ca procente masice de sulf.
3. PRINCIPIU
După acidifierea mediului, hidrogenul sulfurat este antrenat într-un curent de azot și apoi fixat sub formă de sulfură de cadmiu. Aceasta se filtrează și se clătește și apoi se determină iodometric.
4. REACTIVI
Toți reactivii trebuie să fie de puritate analitică.
4.1. Acid clorhidric concentrat, = 1,19 g/ml.
= 1,19 g/ml.
4.2. Tiosulfat de sodiu, soluție standard 0,1M.
4.3. Iod, soluție standard 0,05 M.
4.4. Sulfură disodică.
4.5. Diacetat de cadmiu.
4.6. Amoniac concentrat, = 0,90 g/ml.
= 0,90 g/ml.
4.7. Soluția amoniacală de diacetat de cadmiu: se dizolvă 10 g diacetat de cadmiu (4.5) în aproximativ 50 ml apă. Se adaugă amoniac (4.6) până când precipitatul se dizolvă din nou (de exemplu, aproximativ 20 ml). Se aduce la 100 ml cu apă.
4.8. Azot.
4.9. Soluție de amoniac M.
5. APARATURĂ
5.1. Echipament de laborator obișnuit.
5.2. Balon de 100 ml cu fund rotund și trei gâturi rodate standard.
5.3. Două pahare conice de 150 ml cu gât rodat, echipate cu un dispozitiv alcătuit dintr-un tub plonjor și o țeavă de ieșire laterală pentru eliminarea gazelor antrenate.
5.4. Pâlnie cu tijă lungă.
6. PROCEDURĂ
6.1. Antrenarea sulfurilor
6.1.1. Se ia un ambalaj care nu a mai fost deschis. Se cântărește cu precizie, în balonul cu fund rotund (5.2), o cantitate („m”) (exprimată în grame) de produs, corespunzând la cel mult 30 mg ioni sulfură (5.2). Se adaugă 60 ml apă și 2 picături de lichid antispumant.
6.1.2. Se transferă 50 ml soluție (4.7) în fiecare dintre cele două flacoane conice (5.3).
6.1.3. Se fixează pâlnia picurătoare, tubul plonjor și țeava de ieșire pe balonul cu fund rotund (5.2). Se conectează țeava de ieșire la flacoanele conice (5.3) montate în serie prin intermediul unor țevi de PVC.
NB: Aparatul de antrenare trebuie să treacă de următorul test de etanșeitate: simulând condițiile de testare, se înlocuiește produsul care urmează să fie determinat în 10 ml soluție de sufură (preparată la 4.4) conținând „X mg” de sulfură (determinată iodometric). Fie „Y” numărul de miligrame de sulfură găsit la sfârșitul acestei operații. Diferența dintre cantitatea „X” și cantitatea „Y” nu trebuie să depășească 3 %.
6.1.4. Se trece curent de azot (4.8) prin interior timp de 15 minute, cu un debit de două bule pe secundă, în vederea eliminării aerului conținut în balonul cu fund rotund (5.2.)
6.1.5. Se încălzește balonul cu fund rotund la 85 ± 5 °C.
6.1.6. Se oprește curentul de azot (4.8) și se adaugă 40 ml de acid clorhidric (4.1) picătură cu picătură.
6.1.7. Se pornește din nou curentul de azot (4.8) atunci când aproape tot acidul a fost transferat, lăsând un pat de lichid minim pentru a preveni scăpările de hidrogen sulfurat.
6.1.8. Se oprește încălzirea după 30 de minute. Se lasă paharul (5.2) să se răcească și se continuă trecerea curentului de azot (4.8) prin interior timp de cel puțin o oră și jumătate.
6.2. Titrare
6.2.1. Se filtrează sulfura de cadmiu printr-o pâlnie cu tijă lungă (5.4).
6.2.2. Se clătesc paharele conice (5.3) mai întâi cu soluție de amoniac (4.9) și se toarnă în filtru. Apoi se clătește cu apă distilată și se folosește apa pentru a spăla precipitatul reținut de filtru.
6.2.3. Se completează apa de spălare a precipitatului cu 100 ml apă.
6.2.4. Se pune hârtie de filtru în primul pahar conic care conține precipitatul. Se adaugă 25 ml („n1”) soluție de iod (4.3), aproximativ 20 ml acid clorhidric (4.1) și 50 ml apă distilată.
6.2.5. Se determină excesul de iod folosind soluție de tiosulfat de sodiu („n2”) (4.2).
7. CALCUL
Conținutul de sulfură al probei, exprimat ca sulf în procente masice, se calculează cu următoarea formulă:

unde:
|
n1 |
= |
numărul (în mililitri) de soluție standard de iod (4.3) folosită, |
|
x1 |
= |
molaritatea acestei soluții, |
|
n2 |
= |
numărul (în mililitri) de soluție standard de tiosulfat de sodiu (4.2), |
|
x2 |
= |
molaritatea acestei soluții, |
|
m |
= |
masa (în grame) a probei analizate. |
8. REPETABILITATE (2)
Pentru un conținut de sulfură de aproximativ 2 % (m/m), diferența dintre rezultatele a două determinări efectuate în paralel pe aceeași probă nu trebuie să depășească o valoare absolută de 0,2 % (m/m).
(1) JO L 383, 31.12.1980, p. 27.
(2) Standardul ISO 5725.
NB: Determinarea acidului mercaptoacetic trebuie efectuată pe un produs nefolosit, dintr-un recipient proaspăt deschis, pentru a preveni oxidarea.
(4) Din cauza varietății produselor în care hexaclorofenul poate fi prezent, este important ca mai întâi să se verifice extragerea hexaclorofenului din probă prin acest procedeu, înainte de înregistrarea rezultatelor. Dacă extragerile sunt slabe, se pot face modificări, cum ar fi schimbarea solventului (benzen în loc de acetat de etil etc.), cu consimțământul părților implicate.
(5) Persistența culorii galbene indică un exces de diazometan, care este necesar pentru a asigura o metilare completă a probei.








