This document is an excerpt from the EUR-Lex website
Document 32017R0644
Commission Regulation (EU) 2017/644 of 5 April 2017 laying down methods of sampling and analysis for the control of levels of dioxins, dioxin-like PCBs and non-dioxin-like PCBs in certain foodstuffs and repealing Regulation (EU) No 589/2014 (Text with EEA relevance. )
Uredba Komisije (EU) 2017/644 z dne 5. aprila 2017 o določitvi metod vzorčenja in analitskih metod za nadzor vsebnosti dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB v nekaterih živilih ter razveljavitvi Uredbe (EU) št. 589/2014 (Besedilo velja za EGP. )
Uredba Komisije (EU) 2017/644 z dne 5. aprila 2017 o določitvi metod vzorčenja in analitskih metod za nadzor vsebnosti dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB v nekaterih živilih ter razveljavitvi Uredbe (EU) št. 589/2014 (Besedilo velja za EGP. )
C/2017/2185
UL L 92, 06/04/2017, p. 9–34
(BG, ES, CS, DA, DE, ET, EL, EN, FR, HR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
 In force
In force
|
6.4.2017 |
SL |
Uradni list Evropske unije |
L 92/9 |
UREDBA KOMISIJE (EU) 2017/644
z dne 5. aprila 2017
o določitvi metod vzorčenja in analitskih metod za nadzor vsebnosti dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB v nekaterih živilih ter razveljavitvi Uredbe (EU) št. 589/2014
(Besedilo velja za EGP)
EVROPSKA KOMISIJA JE –
ob upoštevanju Pogodbe o delovanju Evropske unije,
ob upoštevanju Uredbe (ES) št. 882/2004 Evropskega parlamenta in Sveta z dne 29. aprila 2004 o izvajanju uradnega nadzora, da se zagotovi preverjanje skladnosti z zakonodajo o krmi in živilih ter s pravili o zdravstvenem varstvu živali in zaščiti živali (1) ter zlasti člena 11(4) Uredbe,
ob upoštevanju naslednjega:
|
(1) |
Uredba Komisije (ES) št. 1881/2006 (2) določa mejne vrednosti za dioksinom nepodobne poliklorirane bifenile (PCB), dioksine in furane ter za vsoto dioksinov, furanov in dioksinom podobnih PCB v nekaterih živilih. |
|
(2) |
Priporočilo Komisije 2013/711/EU (3) določa prage ukrepanja, da bi se spodbudil proaktivni pristop za zmanjšanje prisotnosti polikloriranih dibenzo-para-dioksinov in polikloriranih dibenzofuranov (PCDD/F) ter dioksinom podobnih PCB v živilih. Navedeni pragi ukrepanja so orodje, s katerim pristojni organi in nosilci dejavnosti ugotavljajo, v katerih primerih je primerno določiti vir kontaminacije in sprejeti potrebne ukrepe za njeno zmanjšanje ali odpravo. |
|
(3) |
Uredba Komisije (EU) št. 589/2014 (4) vsebuje posebne določbe o postopku vzorčenja in analitskih metodah, ki jih je treba uporabiti za uradni nadzor vsebnosti dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB. |
|
(4) |
Določbe iz te uredbe se nanašajo samo na vzorčenje in analizo dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB za izvajanje Uredbe (ES) št. 1881/2006 in Priporočila 2013/711/EU. Ne vplivajo pa na strategijo, količine in pogostnost vzorčenja, kot so določeni v prilogah III in IV k Direktivi Sveta 96/23/ES (5). Ne vplivajo na ciljna merila za vzorčenje iz Odločbe Komisije 98/179/ES (6). |
|
(5) |
Primerno je zagotoviti, da nosilci živilske dejavnosti, ki izvajajo nadzor v skladu s členom 4 Uredbe (ES) št. 852/2004 Evropskega parlamenta in Sveta (7), uporabljajo postopke vzorčenja, enakovredne postopkom vzorčenja iz te uredbe, da se zagotovi reprezentativnost vzorcev, odvzetih za navedeni nadzor. Poleg tega je referenčni laboratorij Evropske unije za dioksine in PCB predložil dokaze, da rezultati analiz v nekaterih primerih niso zanesljivi, kadar laboratoriji, ki opravljajo analize vzorcev, ki jih odvzamejo nosilci živilske dejavnosti v okviru člena 4 Uredbe (ES) št. 852/2004, ne uporabljajo meril učinkovitosti iz te uredbe. Zato je primerno, da uporaba meril učinkovitosti postane obvezna tudi za analizo navedenih vzorcev. |
|
(6) |
Glede na to, da se pristop uporabe odločitvene meje za zagotovitev, da rezultat analize presega najvišjo raven z določeno verjetnostjo, kakor je določeno v Odločbi Komisije 2002/657/ES (8), ne uporablja več za analizo dioksinov in PCB v živilih, je primerno črtati ta pristop in ohraniti le pristop razširjene merilne negotovosti z uporabo faktorja zajetja 2, ki pomeni stopnjo zaupanja približno 95 %. |
|
(7) |
V skladu z zahtevami glede poročanja za bioanalitske presejalne metode je primerno določiti tudi fizikalno-kemijske metode za posebne zahteve glede poročanja v zvezi s presejanjem. |
|
(8) |
Glede na to, da analize dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB v večini primerov potekajo skupaj, je merila učinkovitosti za dioksinom nepodobne PCB primerno uskladiti z merili učinkovitosti za dioksine in dioksinom podobne PCB. To je poenostavitev brez pomembnih sprememb v praksi, saj v primeru dioksinom nepodobnih PCB relativni odziv potrditvenih ionov glede na ciljne ione znaša > 50 %. |
|
(9) |
Poleg tega se predlagajo še druge manjše spremembe sedanjih določb, zaradi katerih je potrebna razveljavitev Uredbe (EU) št. 589/2014 in njena nadomestitev z novo uredbo, da se ohrani berljivost besedila. |
|
(10) |
Ukrepi iz te uredbe so v skladu z mnenjem Stalnega odbora za rastline, živali, hrano in krmo – |
SPREJELA NASLEDNJO UREDBO:
Člen 1
V tej uredbi se uporabljajo opredelitve pojmov in okrajšave iz Priloge I.
Člen 2
Vzorčenje za uradni nadzor vsebnosti dioksinov, furanov, dioksinom podobnih PCB in dioksinom nepodobnih PCB v živilih, navedenih v oddelku 5 Priloge k Uredbi (ES) št. 1881/2006, se izvaja v skladu z metodami iz Priloge II k tej uredbi.
Člen 3
Priprava vzorcev in analize za nadzor vsebnosti dioksinov, furanov in dioksinom podobnih PCB v živilih, navedenih v oddelku 5 Priloge k Uredbi (ES) št. 1881/2006, se izvajajo v skladu z metodami iz Priloge III k tej uredbi.
Člen 4
Analize za nadzor vsebnosti dioksinom nepodobnih PCB v živilih, navedenih v oddelku 5 Priloge k Uredbi (ES) št. 1881/2006, se izvajajo v skladu z zahtevami za analitske postopke iz Priloge IV k tej uredbi.
Člen 5
Uredba (EU) št. 589/2014 se razveljavi.
Sklicevanja na razveljavljeno uredbo se štejejo za sklicevanja na to uredbo.
Člen 6
Ta uredba začne veljati dvajseti dan po objavi v Uradnem listu Evropske unije.
Ta uredba je v celoti zavezujoča in se neposredno uporablja v vseh državah članicah.
V Bruslju, 5. aprila 2017
Za Komisijo
Predsednik
Jean-Claude JUNCKER
(1) UL L 165, 30.4.2004, str. 1.
(2) Uredba Komisije (ES) št. 1881/2006 z dne 19. decembra 2006 o določitvi mejnih vrednosti nekaterih onesnaževal v živilih (UL L 364, 20.12.2006, str. 5).
(3) Priporočilo Komisije 2013/711/EU z dne 3. decembra 2013 za zmanjšanje prisotnosti dioksinov, furanov in PCB-jev v krmi in živilih (UL L 323, 4.12.2013, str. 37).
(4) Uredba Komisije (EU) št. 589/2014 z dne 2. junija 2014 o metodah vzorčenja in analitskih metodah za nadzor vsebnosti dioksinov, dioksinom podobnih PCB in dioksinom nepodobnih PCB v nekaterih živilih ter razveljavitvi Uredbe (EU) št. 252/2012 (UL L 164, 3.6.2014, str. 18).
(5) Direktiva Sveta 96/23/ES z dne 29. aprila 1996 o ukrepih za spremljanje nekaterih snovi in njihovih ostankov v živih živalih in v živalskih proizvodih ter razveljavitvi direktiv 85/358/EGS in 86/469/EGS in odločb 89/187/EGS in 91/664/EGS (UL L 125, 23.5.1996, str. 10).
(6) Odločba Komisije 98/179/ES z dne 23. februarja 1998 o podrobnih pravilih uradnega vzorčenja za spremljanje nekaterih snovi in njihovih ostankov v živih živalih in živalskih proizvodih (UL L 65, 5.3.1998, str. 31).
(7) Uredba Evropskega parlamenta in Sveta (ES) št. 852/2004 z dne 29. aprila 2004 o higieni živil (UL L 139, 30.4.2004, str. 1).
(8) Odločba Komisije 2002/657/ES z dne 14. avgusta 2002 o izvajanju Direktive Sveta 96/23/ES glede opravljanja analitskih metod in razlage rezultatov (UL L 221, 17.8.2002, str. 8).
PRILOGA I
OPREDELITEV POJMOV IN OKRAJŠAVE
I. OPREDELITEV POJMOV
V tej uredbi se uporabljajo opredelitve pojmov iz Priloge I k Odločbi 2002/657/ES.
Poleg navedenih opredelitev pojmov se v tej uredbi uporabljajo tudi naslednje opredelitve pojmov:
|
1.1 |
„Prag ukrepanja“ pomeni vrednost dane snovi, kot je določena v Prilogi k Priporočilu 2013/711/EU, pri kateri se sprožijo preiskave za ugotavljanje vira navedene snovi, če se odkrijejo njene povišane vrednosti. |
|
1.2 |
„Presejalne metode“ pomenijo metode za izbiro tistih vzorcev, katerih vsebnosti PCDD/F in dioksinom podobnih PCB presegajo mejne vrednosti ali prage ukrepanja. Omogočati morajo stroškovno učinkovito veliko prepustnost vzorcev in tako povečati možnosti za odkrivanje novih primerov, v katerih velika izpostavljenost lahko privede do tveganja za zdravje potrošnikov. Presejalne metode temeljijo na bioanalitskih metodah ali metodah GC-MS. Rezultati vzorcev, ki pri preverjanju skladnosti z mejno vrednostjo presegajo izločitveno vrednost, se preverijo s popolno ponovno analizo izvirnega vzorca s potrditveno metodo. |
|
1.3 |
„Potrditvene metode“ pomenijo metode, ki zagotavljajo celovite ali dopolnilne informacije za natančno opredelitev in količinsko določitev PCDD/F in dioksinom podobnih PCB pri mejni vrednosti ali po potrebi pri pragu ukrepanja. Pri takih metodah se uporablja plinska kromatografija/masna spektrometrija visoke ločljivosti (GC-HRMS) ali plinska kromatografija/tandemska masna spektrometrija (GC-MS/MS). |
|
1.4 |
„Bioanalitske metode“ pomenijo metode, ki temeljijo na uporabi bioloških načel, kot so testi na celični osnovi, testi na osnovi receptorjev ali imunološki testi. Te metode ne dajejo rezultatov na ravni kongenerjev, temveč zgolj pokažejo (1) vrednosti toksičnih ekvivalentov (TEQ), izražene v bioanalitskih ekvivalentih (BEQ), saj vse spojine, ki so prisotne v ekstraktu vzorca in pokažejo odziv pri preskusu, morda ne izpolnjujejo vseh zahtev načela TEQ. |
|
1.5 |
„Navidezni izkoristek pri bioloških testih“ pomeni vrednost BEQ, izračunano iz umeritvene krivulje na podlagi TCDD ali PCB 126, popravljene za slepe vrednosti in nato deljene z vrednostjo TEQ, določeno s potrditveno metodo. Njegov namen je popraviti vplive, kot so izguba PCDD/F in dioksinom podobnih spojin med postopki ekstrakcije in čiščenja, soekstrahirane spojine, ki povečujejo ali zmanjšujejo odziv (agonistični in antagonistični učinki), kakovost prilagajanja krivulje ali razlike med vrednostmi faktorja toksične ekvivalentnosti (TEF) in relativne učinkovitosti (REP). Navidezni izkoristek pri bioloških testih se izračuna iz ustreznih referenčnih vzorcev, ki imajo reprezentativno porazdelitev kongenerjev v območju mejne vrednosti ali praga ukrepanja. |
|
1.6 |
„Dvakratna analiza“ pomeni ločeno analizo predpisanih analitov z uporabo drugega alikvota istega homogeniziranega vzorca. |
|
1.7 |
„Sprejemljiva specifična meja določljivosti (2) posameznega kongenerja v vzorcu“ pomeni najmanjšo vsebnost analita, ki se lahko izmeri s sprejemljivo statistično gotovostjo, poleg tega pa morajo biti izpolnjeni tudi pogoji za določitev, kot so opisani v mednarodno priznanih standardih, kot je EN 16215:2012 (Krma – Določevanje dioksinov in dioksinu podobnih PCB z GC/HRMS in indikatorjev PCB z GC/HRMS), in/ali v metodah EPA 1613 in 1668, kot sta bili revidirani. Meja določljivosti posameznega kongenerja se lahko opredeli kot:
|
|
1.8 |
„Zgornja meja“ pomeni pojem, pri katerem se za izračun prispevka vsakega kongenerja, ki ni količinsko določen, uporablja vrednost meje določljivosti. |
|
1.9 |
„Spodnja meja“ pomeni pojem, pri katerem se za izračun prispevka vsakega kongenerja, ki ni količinsko določen, uporablja vrednost nič. |
|
1.10 |
„Srednja meja“ pomeni pojem, pri katerem se za izračun prispevka vsakega kongenerja, ki ni količinsko določen, uporablja polovična vrednost meje določljivosti. |
|
1.11 |
„Lot“ pomeni določljivo količino naenkrat dostavljenega živila, za katero pristojna oseba ugotovi skupne značilnosti, kot so poreklo, vrsta, vrsta pakiranja, izvajalec pakiranja, pošiljatelj ali oznake. Pri ribah ali ribiških proizvodih je tudi velikost rib primerljiva. Če velikost in/ali teža rib v pošiljki nista primerljivi, se lahko pošiljka še vedno šteje za lot, vendar je treba uporabiti poseben postopek vzorčenja. |
|
1.12 |
„Sublot“ pomeni določen del večjega lota, ki je določen za vzorčenje. Vsak sublot mora biti fizično ločen od preostalega dela lota in določljiv. |
|
1.13 |
„Primarni vzorec“ pomeni količino materiala, odvzetega z enega mesta v lotu ali sublotu. |
|
1.14 |
„Sestavljeni vzorec“ pomeni vzorec, sestavljen iz vseh primarnih vzorcev, odvzetih iz lota ali sublota. |
|
1.15 |
„Laboratorijski vzorec“ pomeni reprezentativen del/količino sestavljenega vzorca, namenjeno za laboratorijsko analizo. |
II. UPORABLJENE OKRAJŠAVE
|
BEQ |
bioanalitski ekvivalenti |
|
GC |
plinska kromatografija |
|
HRMS |
masna spektrometrija visoke ločljivosti |
|
LRMS |
masna spektrometrija nizke ločljivosti |
|
MS/MS |
tandemska masna spektrometrija |
|
PCB |
poliklorirani bifenil |
|
dioksinom nepodobni PCB |
PCB 28, PCB 52, PCB 101, PCB 138, PCB 153 in PCB 180 |
|
PCDD |
poliklorirani dibenzo-p-dioksini |
|
PCDF |
poliklorirani dibenzofurani |
|
QC |
nadzor kakovosti |
|
REP |
relativna učinkovitost |
|
TEF |
faktor toksične ekvivalentnosti |
|
TEQ |
toksični ekvivalenti |
|
TCDD |
2,3,7,8-tetraklorodibenzo-p-dioksin |
|
U |
razširjena merilna negotovost |
(1) Bioanalitske metode niso specifične za tiste kongenerje, ki so vključeni v shemo TEF. V ekstraktu vzorca so lahko prisotne druge strukturno povezane spojine, ki se vežejo na aromatski ogljikovodikov receptor (AhR), kar prispeva k celotnemu odzivu. Bioanalitski rezultati zato ne morejo dati ocene vsebnosti, temveč le nakažejo vsebnost TEQ v vzorcu.
(2) Kadar je primerno, se upoštevajo načela, kot so opisana v smernicah za ocenjevanje meje zaznavnosti (LOD) in meje določljivosti (LOQ) za meritve na področju onesnaževal v krmi in živilih [povezava na spletno stran].
(3) LOQ se izračuna iz točke najnižje koncentracije ob upoštevanju izkoristka internih standardov in količine vzorca.
PRILOGA II
METODE VZORČENJA ZA URADNI NADZOR VSEBNOSTI DIOKSINOV (PCDD/PCDF), DIOKSINOM PODOBNIH PCB IN DIOKSINOM NEPODOBNIH PCB V NEKATERIH ŽIVILIH
I. PODROČJE UPORABE
Odvzem vzorcev za uradni nadzor vsebnosti dioksinov (PCDD/F), dioksinom podobnih PCB in dioksinom nepodobnih PCB v živilih se izvaja v skladu z metodami, opisanimi v tej prilogi. Tako dobljeni sestavljeni vzorci se štejejo za reprezentativne vzorce lotov ali sublotov, iz katerih so vzeti. Skladnost z mejnimi vrednostmi, ki so določene v Uredbi (ES) št. 1881/2006, se ugotavlja na podlagi vrednosti, določenih v laboratorijskih vzorcih.
Za zagotovitev skladnosti z določbami člena 4 Uredbe (ES) št. 852/2004 nosilec živilske dejavnosti pri odvzemu vzorcev za nadzor vsebnosti dioksinov (PCDD/F), dioksinom podobnih PCB in dioksinom nepodobnih PCB odvzame vzorce v skladu z metodami, opisanimi v poglavju III te priloge, ali uporabi enakovreden postopek vzorčenja, za katerega je dokazana ista raven reprezentativnosti kot pri postopku vzorčenja, opisanem v poglavju III te priloge.
II. SPLOŠNE DOLOČBE
1. Osebje
Uradno vzorčenje opravi pooblaščena oseba, ki jo imenuje država članica.
2. Material za vzorčenje
Vsak lot ali sublot, ki ga je treba pregledati, se vzorči ločeno.
3. Previdnostni ukrepi
Med vzorčenjem in pripravo vzorcev so potrebni previdnostni ukrepi, da bi se izognili vsem spremembam, ki bi vplivale na vsebnost dioksinov in PCB, škodljivo vplivale na analitsko določanje ali povzročile nereprezentativnost sestavljenih vzorcev.
4. Primarni vzorci
Če je mogoče, se primarni vzorci odvzamejo na različnih mestih celotnega lota ali sublota. Odstopanje od tega postopka se zapiše v zapisnik iz točke II.8.
5. Priprava sestavljenega vzorca
Sestavljeni vzorec se pripravi tako, da se združijo primarni vzorci. Tehta najmanj 1 kg, razen če to ni izvedljivo, npr. če se vzorči en sam paket ali če ima proizvod zelo veliko tržno vrednost.
6. Enakovredni vzorci
Enakovredni vzorci za uradni nadzor, dopolnilno izvedensko mnenje in referenčne namene se odvzamejo iz homogeniziranega sestavljenega vzorca, razen če je ta postopek v nasprotju s pravili države članice o pravicah nosilca živilske dejavnosti. Velikost laboratorijskih vzorcev za uradni nadzor mora zadoščati za vsaj dvakratne analize.
7. Pakiranje in prenos vzorcev
Vsak vzorec se zapre v čisto posodo iz inertnih materialov, ki med prevozom omogoča primerno zaščito pred kontaminacijo, izgubo analitov z adsorpcijo na notranje stene posode in pred poškodbami. Sprejmejo se vsi potrebni previdnostni ukrepi, da se prepreči kakršna koli sprememba v sestavi vzorca, ki bi lahko nastala med prevozom ali skladiščenjem.
8. Pečatenje in označevanje vzorcev
Vsak vzorec, odvzet za uradno uporabo, se zapečati na mestu vzorčenja in označi v skladu s pravili držav članic.
O vsakem vzorčenju se napiše zapisnik, ki omogoča jasno identifikacijo vsakega lota, navedejo se datum in mesto vzorčenja ter vsi dodatni podatki, ki so analitiku lahko v pomoč.
III. NAČRT VZORČENJA
Z uporabljeno metodo vzorčenja se zagotovi, da je sestavljeni vzorec reprezentativen za (sub)lot, ki ga je treba preveriti.
1. Razdelitev lotov na sublote
Veliki loti se razdelijo na sublote, če je sublot mogoče fizično ločiti. Za proizvode, ki se tržijo v velikih nepakiranih pošiljkah (npr. rastlinska olja), se uporablja preglednica 1. Za druge proizvode se uporablja preglednica 2. Ob upoštevanju, da masa lota ni vedno natančen večkratnik mase sublotov, lahko masa sublota presega navedeno maso za največ 20 %.
Preglednica 1
Razdelitev lotov na sublote za proizvode, ki se tržijo v nepakiranih pošiljkah
|
Masa lota (v tonah) |
Masa ali število sublotov |
|
≥ 1 500 |
500 ton |
|
> 300 in < 1 500 |
3 subloti |
|
≥ 50 in ≤ 300 |
100 ton |
|
< 50 |
— |
Preglednica 2
Razdelitev lotov na sublote za druge proizvode
|
Masa lota (v tonah) |
Masa ali število sublotov |
|
≥ 15 |
15–30 ton |
|
< 15 |
— |
2. Število primarnih vzorcev
Sestavljeni vzorec, ki združuje vse primarne vzorce, tehta najmanj 1 kg (glej točko II.5).
Najmanjše število primarnih vzorcev, ki se odvzamejo iz lota ali sublota, je navedeno v preglednicah 3 in 4.
Za nepakirane tekoče proizvode se lot ali sublot čim bolj temeljito ročno ali mehansko premeša neposredno pred vzorčenjem, če to ne vpliva na kakovost proizvoda. V tem primeru se domneva, da je porazdelitev onesnaževal v zadevnem lotu ali sublotu homogena. Zato zadošča, da se za oblikovanje sestavljenega vzorca iz lota ali sublota odvzamejo trije primarni vzorci.
Primarni vzorci imajo podobno maso. Masa primarnega vzorca je najmanj 100 gramov.
Odstopanje od tega postopka je treba zapisati v zapisnik iz točke II.8 te priloge. V skladu z določbami Odločbe Komisije 97/747/ES (1) je velikost sestavljenega vzorca za kokošja jajca najmanj 12 jajc (za nepakirane lote in tudi za sublote, sestavljene iz posameznih pakiranj, se uporabljata preglednici 3 in 4).
Preglednica 3
Najmanjše število primarnih vzorcev, ki se odvzamejo iz lota ali sublota
|
Masa ali prostornina lota/sublota (v kg oziroma l) |
Najmanjše število primarnih vzorcev za odvzem |
|
< 50 |
3 |
|
50 do 500 |
5 |
|
> 500 |
10 |
Za lot ali sublot, ki je sestavljen iz posameznih pakiranj ali enot, je število pakiranj ali enot, ki se odvzamejo za oblikovanje sestavljenega vzorca, navedeno v preglednici 4.
Preglednica 4
Število pakiranj ali enot (primarnih vzorcev), ki se odvzamejo za oblikovanje sestavljenega vzorca, če je lot ali sublot sestavljen iz posameznih pakiranj ali enot
|
Število pakiranj ali enot v lotu/sublotu |
Število pakiranj ali enot za odvzem |
|
1 do 25 |
najmanj 1 pakiranje ali enota |
|
26 do 100 |
približno 5 %, najmanj 2 pakiranji ali enoti |
|
> 100 |
približno 5 %, največ 10 pakiranj ali enot |
3. Posebne določbe za vzorčenje lotov, ki vsebujejo cele ribe primerljive velikosti in teže
Ribe se štejejo za primerljive glede velikosti in teže, če razlika v velikosti in teži ni večja od približno 50 %.
Število primarnih vzorcev, ki se odvzamejo iz lota, je določeno v preglednici 3. Sestavljeni vzorec, ki združuje vse primarne vzorce, tehta najmanj 1 kg (glej točko II.5).
|
— |
Če lot za vzorčenje vsebuje majhne ribe (posamezne ribe, ki tehtajo manj kot približno 1 kg), se kot primarni vzorec vzame cela riba, da se oblikuje sestavljeni vzorec. Če tak sestavljeni vzorec tehta več kot 3 kg, lahko primarne vzorce sestavlja srednji del rib, ki tvorijo sestavljeni vzorec, pri čemer vsak primarni vzorec tehta najmanj 100 g. Celotni del, za katerega velja mejna vrednost, se uporabi za homogenizacijo vzorca. Srednji del ribe je tisti del ribe, v katerem je njeno težišče. V večini primerov se to nahaja pri hrbtni plavuti (če jo riba ima) ali v sredini med škržno odprtino in anusom. |
|
— |
Če lot za vzorčenje vsebuje večje ribe (posamezne ribe, ki tehtajo več kot približno 1 kg), primarni vzorec sestoji iz srednjega dela ribe. Vsak primarni vzorec tehta najmanj 100 g. Pri ribah srednje velikosti (približno 1 do 6 kg) se kot primarni vzorec vzame rezina od hrbtenice do trebuha iz srednjega dela ribe. Pri zelo velikih ribah (npr. > približno 6 kg) se kot primarni vzorec odvzame mišičnina iz srednjega dela ribe, in sicer iz desnega hrbtno-bočnega dela (pogled od spredaj). Če bi odvzem takšnega dela iz srednjega dela ribe povzročil pomembno gospodarsko škodo, zadošča odvzem treh primarnih vzorcev po najmanj 350 g, ne glede na velikost lota, lahko pa se primarni vzorec, ki je reprezentativen glede vsebnosti dioksinov v celi ribi, dobi tako, da se odvzame enakovredni del mišičnine iz predela v bližini repa in predela v bližini glave ene ribe. |
4. Vzorčenje lotov rib, ki vsebujejo cele ribe različne velikosti in/ali teže
|
— |
Za sestavljanje vzorca se uporabljajo določbe iz točke III.3. |
|
— |
Če prevladuje posamezen razred/kategorija velikosti ali teže (približno 80 % lota ali več), se odvzame vzorec rib s prevladujočo težo ali velikostjo. Tak vzorec se šteje za reprezentativen za celotni lot. |
|
— |
Če ne prevladuje noben razred/kategorija velikosti ali teže, potem je treba zagotoviti, da so ribe, izbrane za vzorec, reprezentativne za lot. Posebne smernice za take primere so navedene v smernicah za vzorčenje celih rib različnih velikosti in/ali teže (2). |
5. Vzorčenje na stopnji prodaje na drobno
Vzorčenje živil na stopnji prodaje na drobno se po možnosti izvede v skladu z določbami o vzorčenju iz točke III.2.
Če to ni mogoče, se lahko na stopnji prodaje na drobno uporablja nadomestna metoda vzorčenja, če zagotavlja, da je vzorčeni lot ali sublot dovolj reprezentativen.
IV. SKLADNOST LOTA ALI SUBLOTA S SPECIFIKACIJO
1. Glede dioksinom nepodobnih PCB
Lot je skladen, če rezultat analize za vsoto dioksinom nepodobnih PCB ne presega zadevne mejne vrednosti, določene v Uredbi (ES) št. 1881/2006, ob upoštevanju razširjene merilne negotovosti (3).
Lot ni v skladu z mejno vrednostjo iz Uredbe (ES) št. 1881/2006, če povprečje dveh rezultatov analiz na zgornji meji, pridobljenih z dvakratno analizo (4), ob upoštevanju razširjene merilne negotovosti nedvomno presega mejno vrednost.
Razširjena merilna negotovost se izračuna z uporabo faktorja zajetja 2, ki pomeni stopnjo zaupanja približno 95 %. Lot je neskladen, če je povprečje izmerjenih vrednosti, od katerega se odšteje razširjena negotovost povprečne vrednosti, nad določeno mejno vrednostjo.
Za rezultat analize, pridobljen na vzorcu za uradni nadzor, se uporabljajo pravila, navedena v odstavkih te točke. Pri analizi za dopolnilno izvedensko mnenje ali referenčne namene se uporabljajo nacionalna pravila.
2. Glede dioksinov (PCDD/F) in dioksinom podobnih PCB
Lot je skladen, če rezultat posamezne analize,
|
— |
opravljene s presejalno metodo, pri kateri je delež lažno skladnih rezultatov manjši kot 5 %, pokaže, da vsebnost ne presega zadevne mejne vrednosti PCDD/F ter vsote PCDD/F in dioksinom podobnih PCB iz Uredbe (ES) št. 1881/2006, |
|
— |
opravljene s potrditveno metodo, ne presega zadevne mejne vrednosti PCDD/F ter vsote PCDD/F in dioksinom podobnih PCB iz Uredbe (ES) št. 1881/2006, ob upoštevanju merilne negotovosti (5). |
Za presejalne teste se določi izločitvena vrednost za odločitev o skladnosti z zadevnimi mejnimi vrednostmi, določenimi za PCDD/F ali za vsoto PCDD/F in dioksinom podobnih PCB.
Lot ni v skladu z mejno vrednostjo iz Uredbe (ES) št. 1881/2006, če povprečje dveh rezultatov analiz na zgornji meji (dvakratna analiza (6)), pridobljenih z uporabo potrditvene metode, ob upoštevanju razširjene merilne negotovosti nedvomno presega mejno vrednost.
Razširjena merilna negotovost se izračuna z uporabo faktorja zajetja 2, ki pomeni stopnjo zaupanja približno 95 %. Lot je neskladen, če je povprečje izmerjenih vrednosti, od katerega se odšteje razširjena negotovost povprečne vrednosti, nad določeno mejno vrednostjo.
Vsoto ocenjene razširjene negotovosti ločenih rezultatov analize vsebnosti PCDD/F in dioksinom podobnih PCB je treba uporabiti za ocenjeno razširjeno negotovost vsote PCDD/F in dioksinom podobnih PCB.
Za rezultat analize, pridobljen na vzorcu za uradni nadzor, se uporabljajo pravila, navedena v odstavkih te točke. Pri analizi za dopolnilno izvedensko mnenje ali referenčne namene se uporabljajo nacionalna pravila.
V. PRESEGANJE PRAGOV UKREPANJA
Pragovi ukrepanja so orodje za izbiro vzorcev v tistih primerih, ko je primerno določiti vir kontaminacije in sprejeti ukrepe za njeno zmanjšanje ali odpravo. S presejalnimi metodami se določijo ustrezne izločitvene vrednosti za izbiro navedenih vzorcev. Če so za določitev vira in zmanjšanje ali odpravo kontaminacije potrebna precejšnja prizadevanja, je morda primerno, da se preseganje praga ukrepanja potrdi z dvakratno analizo s potrditveno metodo ob upoštevanju razširjene merilne negotovosti (7).
(1) Odločba Komisije 97/747/ES z dne 27. oktobra 1997 o obsegu in pogostnosti vzorčenja, predvidenega v Direktivi Sveta 96/23/ES za nadzor nekaterih snovi in njihovih ostankov v nekaterih živalskih proizvodih (UL L 303, 6.11.1997, str. 12).
(2) https://ec.europa.eu/food/sites/food/files/safety/docs/cs_contaminants_catalogue_dioxins_guidance-sampling_exemples-dec2006_en.pdf
(3) Kadar je primerno, se upoštevajo načela, kot so opisana v smernicah o merilni negotovosti za laboratorije, ki opravljajo analize vsebnosti PCDD/F in PCB z uporabo izotopske razredčitve – masne spektrometrije [povezava na spletno stran].
(4) Dvakratna analiza je potrebna, če je rezultat prvega določanja neskladen. Dvakratna analiza je potrebna za izključitev možnosti notranje navzkrižne kontaminacije ali naključne zamenjave vzorcev. Kadar se analiza izvaja med kontaminacijo, se lahko izpusti potrjevanje z dvakratno analizo, če so vzorci, izbrani za analizo, s sledljivostjo povezani s kontaminacijo, ugotovljena vsebnost pa bistveno presega mejno vrednost.
(5) Smernice o merilni negotovosti za laboratorije, ki opravljajo analize vsebnosti PCDD/F in PCB z uporabo izotopske razredčitve – masne spektrometrije [povezava na spletno stran], smernice za ocenjevanje meje zaznavnosti (LOD) in meje določljivosti (LOQ) za meritve na področju onesnaževal v krmi in živilih [povezava na spletno stran].
(6) Dvakratna analiza je potrebna, če je rezultat prvega določanja s potrditveno metodo z uporabo 13C-označenih internih standardov za zadevne analite neskladen. Dvakratna analiza je potrebna za izključitev možnosti notranje navzkrižne kontaminacije ali naključne zamenjave vzorcev. Kadar se analiza izvaja med kontaminacijo, se lahko izpusti potrjevanje z dvakratno analizo, če so vzorci, izbrani za analizo, s sledljivostjo povezani s kontaminacijo, ugotovljena vsebnost pa bistveno presega mejno vrednost.
(7) Enaka razlaga in zahteve za dvakratno analizo za nadzor pragov ukrepanja kot v opombi 6 za mejne vrednosti.
PRILOGA III
PRIPRAVA VZORCA IN ZAHTEVE ZA ANALITSKE METODE ZA NADZOR VSEBNOSTI DIOKSINOV (PCDD/F) IN DIOKSINOM PODOBNIH PCB V NEKATERIH ŽIVILIH
1. PODROČJE UPORABE
Zahteve, določene v tej prilogi, se uporabijo, kadar se živila analizirajo za uradni nadzor vsebnosti 2,3,7,8-substituiranih polikloriranih dibenzo-p-dioksinov in polikloriranih dibenzofuranov (PCDD/F) ter dioksinom podobnih polikloriranih bifenilov (dioksinom podobnih PCB), in za pripravo vzorcev in analitske zahteve za druge regulativne namene, vključno z nadzorom, ki ga izvajajo nosilci živilske dejavnosti za zagotovitev skladnosti z določbami člena 4 Uredbe (ES) št. 852/2004.
Prisotnost PCDD/F in dioksinom podobnih PCB v živilih se lahko spremlja z dvema različnima vrstama analitskih metod:
(a) Presejalne metode
Cilj presejalnih metod je izbor tistih vzorcev, katerih vsebnosti PCDD/F in dioksinom podobnih PCB presegajo mejne vrednosti ali prage ukrepanja. Presejalne metode omogočajo stroškovno učinkovito veliko prepustnost vzorcev in tako povečujejo možnosti za odkrivanje novih primerov, ko velika izpostavljenost lahko privede do tveganja za zdravje potrošnikov. Z njihovo uporabo naj bi se izognili lažno skladnim rezultatom. Vključujejo lahko bioanalitske metode in metode GC/MS.
Presejalne metode temeljijo na primerjavi rezultata analize z izločitveno vrednostjo in omogočajo odločitev da/ne glede mogočega preseganja mejne vrednosti ali praga ukrepanja. Koncentracijo PCDD/F ter vsoto PCDD/F in dioksinom podobnih PCB v vzorcih, za katere se domneva, da niso v skladu z mejno vrednostjo, je treba določiti/potrditi s potrditveno metodo.
Poleg tega lahko presejalne metode nakažejo vsebnost PCDD/F in dioksinom podobnih PCB v vzorcu. V primeru uporabe bioanalitskih presejalnih metod se rezultat izrazi v bioanalitskih ekvivalentih (BEQ), v primeru uporabe fizikalno-kemijskih metod GC-MS pa v toksičnih ekvivalentih (TEQ). Številčno navedeni rezultati presejalnih metod so primerni za dokazovanje skladnosti ali domnevne neskladnosti ali preseganja pragov ukrepanja ter nakažejo območje vrednosti v primeru spremljanja s potrditvenimi metodami. Presejalne metode pa niso primerne za namene, kot so ocena ravni prisotnosti, ocena vnosa, spremljanje časovnih gibanj vrednosti ali ponovna ocena pragov ukrepanja in mejnih vrednosti.
(b) Potrditvene metode
Potrditvene metode omogočajo nedvoumno identifikacijo in količinsko določanje PCDD/F in dioksinom podobnih PCB, prisotnih v vzorcu, ter zagotavljajo celovite informacije na podlagi kongenerja. Zato te metode omogočajo nadzor mejnih vrednosti in pragov ukrepanja, vključno s potrditvijo rezultatov, pridobljenih s presejalnimi metodami. Poleg tega se rezultati lahko uporabljajo za druge namene, na primer za določitev nizkih ravni prisotnosti pri nadzoru živil, spremljanje časovnih gibanj, oceno izpostavljenosti prebivalstva in vzpostavljanje zbirke podatkov za morebitno ponovno oceno pragov ukrepanja in mejnih vrednosti. Te metode so pomembne tudi za določitev vzorcev kongenerjev za ugotovitev vira mogoče kontaminacije. Take metode uporabljajo GC-HRMS. Za potrditev skladnosti ali neskladnosti z mejno vrednostjo se lahko uporabi tudi GC-MS/MS.
2. OZADJE
Za izračun koncentracij TEQ se koncentracije posameznih snovi v danem vzorcu pomnožijo z njihovim ustreznim TEF, kot ga je določila Svetovna zdravstvena organizacija in je naveden v Dodatku k tej prilogi, ter se nato seštejejo, da se dobi skupna koncentracija dioksinom podobnih spojin, izraženih v TEQ.
Presejalne in potrditvene metode se lahko uporabijo za nadzor določene matrice le, če so metode dovolj občutljive, da se z njimi zanesljivo odkrijejo vsebnosti pri mejni vrednosti ali pragu ukrepanja.
3. ZAHTEVE ZA ZAGOTAVLJANJE KAKOVOSTI
|
— |
Sprejeti je treba ukrepe za preprečitev navzkrižne kontaminacije na vseh stopnjah vzorčenja in analitskega postopka. |
|
— |
Vzorce je treba hraniti in prevažati v steklenih, aluminijastih, polipropilenskih ali polietilenskih posodah, ki so primerne za shranjevanje brez vplivanja na vsebnost PCDD/F in dioksinom podobnih PCB v vzorcih. Iz posode za vzorce morajo biti odstranjeni sledovi papirnega prahu. |
|
— |
Vzorce je treba hraniti in prevažati tako, da se ohrani neoporečnost vzorca živila. |
|
— |
Če je ustrezno, se vsak laboratorijski vzorec drobno zmelje in temeljito premeša po postopku, s katerim se dokazano doseže popolna homogenizacija (npr. zmleto tako, da se preseje z 1-milimetrskim sitom); če je vsebnost vlage previsoka, je treba vzorce pred mletjem posušiti. |
|
— |
Nadzor reagentov, steklovine in opreme zaradi mogočega vpliva na rezultate, izražene v TEQ ali BEQ, je splošno pomemben. |
|
— |
Slepa analiza se opravi z izvedbo celotnega analitskega postopka, iz katerega se izpusti le vzorec. |
|
— |
Pri bioanalitskih metodah je zelo pomembno testirati, da steklovina in topila, ki se uporabljajo za analizo, ne vsebujejo spojin, ki vplivajo na ugotavljanje ciljnih spojin v delovnem območju. Steklovina se spere s topili in/ali segreje do temperatur, primernih za odstranitev sledi PCDD/F, dioksinom podobnih spojin in motečih spojin z njene površine. |
|
— |
Količina vzorca, uporabljenega za ekstrakcijo, mora biti zadostna, da so izpolnjene zahteve glede dovolj nizkega delovnega območja, vključno s koncentracijami mejnih vrednosti ali pragov ukrepanja. |
|
— |
Posebni postopki za pripravo vzorca, ki se uporabljajo za obravnavane proizvode, so skladni z mednarodno sprejetimi smernicami. |
|
— |
Pri ribah je treba odstraniti kožo, saj mejna vrednost velja za mišičnino brez kože. Vendar je treba vso preostalo mišičnino in maščobno tkivo na notranji strani kože temeljito in popolnoma odstraniti s kože ter dodati vzorcu za analizo. |
4. ZAHTEVE ZA LABORATORIJE
|
— |
V skladu z določbami Uredbe (ES) št. 882/2004 laboratorije akreditirajo priznani organi, ki delujejo v skladu z zahtevami vodnika ISO 58, s čimer je zagotovljeno, da izvajajo analitsko zagotavljanje kakovosti. Laboratoriji se akreditirajo po standardu EN ISO/IEC 17025. Kadar je primerno, se upoštevajo načela, kot so opisana v tehničnih smernicah za oceno merilne negotovosti in mej določljivosti za analizo vsebnosti PCDD/F in PCB (1). |
|
— |
Sposobnost laboratorijev se dokazuje z nenehnim uspešnim sodelovanjem v medlaboratorijskih študijah za določanje PCDD/F in dioksinom podobnih PCB v ustreznih matricah živil in območjih koncentracij. |
|
— |
Laboratoriji, ki izvajajo presejalne metode za rutinski nadzor vzorcev, vzpostavijo tesno sodelovanje z laboratoriji, ki izvajajo potrditveno metodo, da se zagotovi nadzor kakovosti in potrdi rezultat analize sumljivih vzorcev. |
5. OSNOVNE ZAHTEVE ZA ANALITSKE POSTOPKE ZA DIOKSINE (PCDD/F) IN DIOKSINOM PODOBNE PCB
5.1 Nizko delovno območje in meje določljivosti
|
— |
Za PCDD/F morajo biti zaradi izredne toksičnosti nekaterih od teh spojin zaznavne količine v zgornjem femtogramskem območju (10– 15 g). Za večino kongenerjev PCB je meja določljivosti v nanogramskem območju (10– 9 g) že zadostna. Vendar mora za merjenje bolj toksičnih dioksinom podobnih kongenerjev PCB (zlasti neorto substituiranih kongenerjev) spodnji del delovnega območja doseči spodnje pikogramsko območje (10– 12 g). |
5.2 Velika selektivnost (specifičnost)
|
— |
Ločevati je treba med PCDD/F in dioksinom podobnimi PCB ter številnimi drugimi spojinami, ki se ekstrahirajo hkrati in so morda moteče ter so prisotne v koncentracijah, ki so do več velikostnih razredov višje od koncentracij predpisanih analitov. Za metode plinske kromatografije/masne spektrometrije (GC-MS) je treba ločevati med različnimi kongenerji, na primer med toksičnimi (npr. sedemnajst 2,3,7,8-substituiranih PCDD/F in dvanajst dioksinom podobnih PCB) in drugimi kongenerji. |
|
— |
Bioanalitske metode omogočajo ugotavljanje ciljnih spojin kot vsote PCDD/F in/ali dioksinom podobnih PCB. Vzorec se očisti, da se odstranijo spojine, ki povzročajo lažno neskladne rezultate, ali spojine, ki lahko zmanjšajo odziv in povzročijo lažno skladne rezultate. |
5.3 Velika točnost (pravilnost in natančnost, navidezni izkoristek pri bioloških testih)
|
— |
Pri metodah GC-MS določanje zagotovi veljavno oceno pravih koncentracij v vzorcu. Velika točnost (točnost meritve: tesno ujemanje merilnega rezultata s pravo ali dogovorjeno vrednostjo merjene veličine) je potrebna, da se prepreči zavrnitev rezultata analize vzorca zaradi nizke zanesljivosti ugotovljene vrednosti TEQ. Točnost se izrazi kot pravilnost (razlika med izmerjeno povprečno vrednostjo analita v certificiranem materialu in njegovo certificirano vrednostjo, izražena kot delež te vrednosti) in natančnost (relativni standardni odmik (RSDR), izračunan iz rezultatov, pridobljenih pri pogojih obnovljivosti). |
|
— |
Pri bioanalitskih metodah se določi navidezni izkoristek pri bioloških testih. |
5.4 Validacija v območju mejne vrednosti in splošni ukrepi za nadzor kakovosti
|
— |
Laboratoriji dokažejo učinkovitost metode v območju mejne vrednosti, npr. 0,5-kratna, 1-kratna in 2-kratna mejna vrednost s sprejemljivim koeficientom variacije za ponovljene analize, med postopkom validacije in/ali rutinsko analizo. |
|
— |
Redne slepe kontrole in preskusi z dodatkom ali analize kontrolnih vzorcev (če je na voljo, je zaželen certificiran referenčni material) se izvajajo kot notranji nadzorni ukrepi za zagotavljanje kakovosti. Za slepe kontrole, preskuse z dodatkom ali analize kontrolnih vzorcev se vodijo in preverjajo karte za nadzor kakovosti, s čimer se zagotovi, da je analitska učinkovitost v skladu z zahtevami. |
5.5 Meja določljivosti
|
— |
Za bioanalitsko presejalno metodo določitev LOQ ni nujna zahteva, vendar je treba dokazati, da lahko metoda razlikuje med slepo vrednostjo in izločitveno vrednostjo. Pri določanju vrednosti BEQ se določi prag poročanja zaradi obravnave vzorcev, pri katerih je odziv pod tem pragom. Za prag poročanja je treba dokazati, da se najmanj za trikrat razlikuje od postopka s slepimi vzorci, pri katerih je odziv pod delovnim območjem. Zato se izračuna iz vzorcev, ki vsebujejo ciljne spojine blizu zahtevane najnižje vrednosti, ne pa iz razmerja med signalom in šumom ali slepega testa. |
|
— |
Meja določljivosti za potrditveno metodo je približno ena petina mejne vrednosti. |
5.6 Merila za analizo
|
— |
Za zanesljive rezultate potrditvenih ali presejalnih metod morajo biti izpolnjena naslednja merila v območju mejnih vrednosti glede vrednosti TEQ oziroma vrednosti BEQ, ki je določena kot skupna vrednost TEQ ali skupna vrednost BEQ (kot vsota PCDD/F in dioksinom podobnih PCB) ali posebej za PCDD/F in dioksinom podobne PCB. |
|
|
Presejanje z bioanalitskimi ali fizikalno-kemijskimi metodami |
Potrditvene metode |
|
Delež lažno skladnih rezultatov (*1) |
< 5 % |
|
|
Pravilnost |
|
– 20 % do + 20 % |
|
Ponovljivost (RSDr) |
< 20 % |
|
|
Srednja natančnost (RSDR) |
< 25 % |
< 15 % |
5.7 Posebne zahteve za presejalne metode
|
— |
Pri presejanju se lahko uporabijo metode GC-MS in bioanalitske metode. Za metode GC/MS se uporabljajo zahteve iz točke 6. Za bioanalitske metode na celični osnovi so posebne zahteve določene v točki 7. |
|
— |
Laboratoriji, ki izvajajo presejalne metode za rutinski nadzor vzorcev, vzpostavijo tesno sodelovanje z laboratoriji, ki izvajajo potrditveno metodo. |
|
— |
Med rutinsko analizo je treba opraviti preverjanje učinkovitosti presejalne metode z analitskim nadzorom kakovosti in nenehno validacijo metod. Nenehno je treba izvajati program nadzora nad skladnimi rezultati. |
|
— |
Preverjanje mogočega zmanjšanja celične odzivnosti in citotoksičnosti. 20 % ekstraktov vzorcev se izmeri med rutinskim presejanjem brez TCDD in z dodanim TCDD, ki ustreza mejni vrednosti ali pragu ukrepanja, da se preveri, ali je morda odziv zmanjšan zaradi motečih snovi v ekstraktu vzorca. Izmerjena koncentracija vzorca z dodatkom se primerja z vsoto koncentracije ekstrakta brez dodatka in koncentracije z dodatkom. Če je ta izmerjena koncentracija za več kot 25 % nižja od izračunane (vsote) koncentracije, to kaže na mogoče zmanjšanje signala, zato je za zadevni vzorec treba opraviti potrditveno analizo. Rezultati se spremljajo v kartah za nadzor kakovosti. |
|
— |
Nadzor kakovosti skladnih vzorcev Približno od 2 % do 10 % skladnih vzorcev, odvisno od matrice vzorca in laboratorijskih izkušenj, je treba potrditi. |
|
— |
Določanje deleža lažno skladnih rezultatov na podlagi podatkov nadzora kakovosti Določi se delež lažno skladnih rezultatov pri presejanju vzorcev pod mejno vrednostjo ali pragom ukrepanja in nad njima. Dejanski delež lažno skladnih rezultatov je manjši kot 5 %. Ko je po nadzoru kakovosti skladnih vzorcev na voljo najmanj 20 potrjenih rezultatov na matrico/skupino matric, se na podlagi te zbirke podatkov pripravijo ugotovitve o deležu lažno skladnih rezultatov. Rezultati vzorcev, analiziranih s krožnimi preskusi ali med kontaminacijami, ki zajemajo območje koncentracije do npr. dvakratne mejne vrednosti, so prav tako lahko vključeni v kvoto najmanj 20 rezultatov za oceno deleža lažno skladnih rezultatov. Vzorci zajemajo najpogostejše vzorce kongenerjev, ki predstavljajo različne vire. Čeprav je glavni namen presejalnih testov odkrivanje vzorcev, ki presegajo pragove ukrepanja, je merilo za določanje deleža lažno skladnih rezultatov mejna vrednost, ob upoštevanju razširjene merilne negotovosti potrditvene metode. |
|
— |
Morebitni neskladni rezultati presejanja se vedno preverijo s celovito ponovno analizo izvirnega vzorca s potrditveno metodo. Ti vzorci se lahko uporabijo tudi za oceno deleža lažno neskladnih rezultatov. Pri presejalnih metodah je delež lažno neskladnih rezultatov delež rezultatov, za katere je s potrditveno analizo potrjeno, da so skladni, čeprav se je pri predhodnem presejanju pri vzorcu pokazal sum na neskladnost. Vendar ocena koristnosti presejalne metode temelji na primerjavi lažno neskladnih vzorcev in celotnega števila pregledanih vzorcev. Ta delež je dovolj majhen, da je uporaba presejalnega orodja koristna. |
|
— |
Bioanalitske metode vsaj pri pogojih validacije veljavno nakažejo vrednost TEQ, ki je izračunana in izražena kot BEQ. |
|
— |
Tudi pri bioanalitskih metodah, opravljenih pri pogojih ponovljivosti, je interna laboratorijska obnovljivost RSDr običajno manjša od obnovljivosti RSDR. |
6. POSEBNE ZAHTEVE ZA METODE GC-MS ZA PRESEJALNE IN POTRDITVENE NAMENE
6.1 Sprejemljive razlike med vrednostmi WHO-TEQ na zgornji in spodnji meji
|
— |
Razlika med vrednostjo na zgornji in spodnji meji ne presega 20 % za potrditev preseganja mejne vrednosti ali po potrebi pragov ukrepanja. |
6.2 Nadzor izkoristkov
|
— |
Dodajanje 13C-označenih 2,3,7,8-klor substituiranih internih standardov za PCDD/F in 13C-označenih internih standardov za dioksinom podobne PCB je treba izvesti na samem začetku analitske metode, npr. pred ekstrakcijo, da se validira analitski postopek. Dodati je treba vsaj en kongener za vsako od tetra- do okta-kloriranih homolognih skupin za PCDD/F in vsaj en kongener za vsako od homolognih skupin za dioksinom podobne PCB (ali vsaj en kongener za vsak masnospektrometričen izbran ion s funkcijo evidentiranja, ki se uporablja za spremljanje PCDD/F in dioksinom podobnih PCB). Pri potrditvenih metodah se uporablja vseh 17 13C-označenih 2,3,7,8-substituiranih internih standardov za PCDD/F in vseh 12 13C-označenih internih standardov za dioksinom podobne PCB. |
|
— |
Prav tako se določijo relativni odzivni faktorji za tiste kongenerje, za katere ni dodan noben od 13C-označenih analogov z uporabo ustreznih raztopin za umerjanje. |
|
— |
Za živila rastlinskega izvora in živila živalskega izvora, ki vsebujejo manj kot 10 % maščob, je dodatek internih standardov pred ekstrakcijo obvezen. Za živila živalskega izvora, ki vsebujejo več kot 10 % maščob, se lahko interni standardi dodajo pred ekstrakcijo maščob ali po njej. Izvede se ustrezna validacija učinkovitosti ekstrakcije, ki je odvisna od faze, pri kateri se dodajo interni standardi, in od tega, ali se o rezultatih poroča na podlagi proizvoda ali maščob. |
|
— |
Pred analizo GC-MS je treba dodati 1 ali 2 (nadomestna) standarda za izračun izkoristka. |
|
— |
Potreben je nadzor izkoristka. Pri potrditvenih metodah so izkoristki posameznih internih standardov v območju od 60 % do 120 %. Manjši ali večji izkoristki za posamezne kongenerje, zlasti za nekatere hepta- in okta-klorirane dibenzo-p-dioksine in dibenzofurane, so sprejemljivi, če njihov prispevek k vrednosti TEQ ne presega 10 % skupne vrednosti TEQ (na podlagi vsote PCDD/F in dioksinom podobnih PCB). Pri presejalnih metodah GC-MS so izkoristki v območju 30 % do 140 %. |
6.3 Odstranitev motečih snovi
|
— |
PCDD/F se od motečih kloriranih spojin, kot so dioksinom nepodobni PCB in klorirani difenil etri, ločijo z ustreznimi kromatografskimi tehnikami (prednost imajo florisil, koloni iz aluminijevega oksida in/ali ogljikovi koloni). |
|
— |
Zadostuje plinsko kromatografsko ločevanje izomerov (< 25 % od vrha do vrha med 1,2,3,4,7,8-HxCDF in 1,2,3,6,7,8-HxCDF). |
6.4 Umerjanje s standardno krivuljo
|
— |
Obseg umeritvene krivulje zajema ustrezno območje mejnih vrednosti ali pragov ukrepanja. |
6.5 Posebna merila za potrditvene metode
|
— |
Za GC-HRMS:
|
|
— |
Za GC-MS/MS:
|
7. POSEBNE ZAHTEVE ZA BIOANALITSKE METODE
Bioanalitske metode so metode, ki temeljijo na uporabi bioloških načel, kot so testi na celični osnovi, testi na osnovi receptorjev ali imunološki testi. V tej točki so določene splošne zahteve za bioanalitske metode.
S presejalno metodo se načeloma vzorec razvrsti kot skladen ali kot vzorec s sumom na neskladnost. V ta namen se izračunana vrednost BEQ primerja z izločitveno vrednostjo (glej točko 7.3). Vzorci pod izločitveno vrednostjo se ugotovijo za skladne, za tiste na tej meji ali nad njo pa se sumi, da niso skladni, zato jih je treba analizirati s potrditveno metodo. V praksi se vrednost BEQ, ki ustreza dvema tretjinama mejne vrednosti, lahko uporabi kot izločitvena vrednost, če sta zagotovljena delež lažno skladnih rezultatov, ki je manjši kot 5 %, in sprejemljiv delež lažno neskladnih rezultatov. Ker so mejne vrednosti ločene za PCDD/F ter za vsoto PCDD/F in dioksinom podobnih PCB, so za preverjanje skladnosti vzorcev brez frakcioniranja potrebne ustrezne izločitvene vrednosti za PCDD/F pri bioloških testih. Za preverjanje vzorcev, ki presegajo pragove ukrepanja, bi bil kot izločitvena vrednost primeren ustrezen delež zadevnega praga ukrepanja.
Če je okvirna vrednost izražena v BEQ, morajo biti rezultati vzorca v delovnem območju in presegati prag poročanja (glej točki 7.1.1 in 7.1.6).
7.1 Ocena odzivnosti preskusa
7.1.1 Splošne zahteve
|
— |
Kadar se koncentracije izračunajo iz umeritvene krivulje TCDD, vrednosti na zgornjem koncu krivulje pokažejo veliko razliko (visok koeficient variacije (KV)). Delovno območje je območje, v katerem je KV manjši od 15 %. Spodnji del delovnega območja (prag poročanja) je treba določiti precej nad postopkom s slepimi vzorci (najmanj trikrat višje). Zgornji del delovnega območja običajno predstavlja vrednost EC70 (70 % največje učinkovite koncentracije), vendar je ta nižje, če je KV v tem območju večji od 15 %. Delovno območje se določi med validacijo. Izločitvene vrednosti (glej točko 7.3) morajo biti znotraj delovnega območja. |
|
— |
Standardne raztopine in ekstrakti vzorcev se testirajo s trikratno ali vsaj dvakratno analizo. Kadar se uporabijo dvakratne analize, standardne raztopine ali ekstrakti kontrolnih vzorcev, testirani v 4 do 6 jamicah, razporejenih po plošči, pokažejo odziv ali koncentracijo (mogoče le v delovnem območju) na podlagi KV < 15 %. |
7.1.2 Umerjanje
7.1.2.1 Umerjanje s standardno krivuljo
|
— |
Vrednosti v vzorcih se lahko ocenijo tako, da se primerja odzivnost preskusa z umeritveno krivuljo TCDD (ali PCB 126 ali standardne mešanice PCDD/F in dioksinom podobnih PCB) za izračun vrednosti BEQ v ekstraktu in pozneje v vzorcu. |
|
— |
Umeritvena krivulja vsebuje 8 do 12 koncentracij (vsaj v dvojnikih), z zadostnimi koncentracijami v spodnjem delu krivulje (delovno območje). Posebna pozornost se nameni kakovosti prilagajanja krivulje v delovnem območju. Tako vrednost R2 malo ali sploh ne pripomore k ocenjevanju ustreznosti prilagajanja pri nelinearni regresiji. Boljše prilagajanje bo doseženo z zmanjšanjem razlike med izračunanimi in ugotovljenimi vrednostmi v delovnem območju krivulje (na primer z zmanjšanjem vsote kvadratov ostankov). |
|
— |
Ocenjena vrednost v ekstraktu vzorca se nato popravi glede na vrednost BEQ, izračunano za slepi vzorec matrice ali topila (da se upoštevajo nečistoče iz uporabljenih topil in kemikalij), in navidezen izkoristek (izračunan iz vrednosti BEQ ustreznih referenčnih vzorcev z reprezentativnimi vzorci kongenerjev v območju mejne vrednosti ali praga ukrepanja). Za popravek izkoristka mora biti navidezni izkoristek vedno v zahtevanem območju (glej točko 7.1.4.). Referenčni vzorci, ki se uporabijo za popravek izkoristka, morajo izpolnjevati zahteve iz točke 7.2. |
7.1.2.2 Umerjanje z referenčnimi vzorci
Druga možnost je, da se uporabi umeritvena krivulja, pripravljena iz vsaj štirih referenčnih vzorcev (glej točko 7.2): ene slepe matrice ter treh referenčnih vzorcev z 0,5-kratno, 1-kratno in 2-kratno mejno vrednostjo ali pragom ukrepanja, zaradi česar popravek slepih vrednosti in izkoristka ni več potreben, če se lastnosti matrice referenčnih vzorcev ujemajo z lastnostmi matrice neznanih vzorcev. V tem primeru se lahko odzivnost preskusa, ki ustreza dvema tretjinama mejne vrednosti (glej točko 7.3), izračuna neposredno iz teh vzorcev in uporabi kot izločitvena vrednost. Za preverjanje vzorcev, ki presegajo pragove ukrepanja, bi bil kot izločitvena vrednost primeren ustrezen delež teh pragov ukrepanja.
7.1.3 Ločeno določanje PCDD/F in dioksinom podobnih PCB
Ekstrakti se lahko razdelijo v frakcije, ki vsebujejo PCDD/F in dioksinom podobne PCB, kar omogoča ločeno navedbo vrednosti TEQ za PCDD/F in dioksinom podobne PCB (v BEQ). Po možnosti se uporabi standardna umeritvena krivulja PCB 126 za oceno rezultatov za frakcijo, ki vsebuje dioksinom podobne PCB.
7.1.4 Navidezni izkoristki pri bioloških testih
„Navidezni izkoristek pri bioloških testih“ se izračuna iz ustreznih referenčnih vzorcev z reprezentativnimi vzorci kongenerjev blizu mejne vrednosti ali praga ukrepanja in se izrazi kot delež vrednosti BEQ v primerjavi z vrednostjo TEQ. Odvisno od uporabljene vrste testa in TEF (2) lahko razlike med faktorji TEF in REP za dioksinom podobne PCB povzročijo majhne navidezne izkoristke za dioksinom podobne PCB v primerjavi s PCDD/F. Če se izvaja ločeno določanje PCDD/F in dioksinom podobnih PCB, navidezni izkoristki pri bioloških testih znašajo: za dioksinom podobne PCB od 20 % do 60 %, za PCDD/F od 50 % do 130 % (območja veljajo za umeritveno krivuljo TCDD). Ker se lahko prispevek dioksinom podobnih PCB k vsoti PCDD/F in dioksinom podobnih PCB razlikuje pri različnih matricah in vzorcih, se pri navideznih izkoristkih pri bioloških testih za vsoto parametrov upoštevajo ta območja in znašajo od 30 % do 130 %.
7.1.5 Nadzor nad izkoristkom pri čiščenju
Izguba spojin pri čiščenju se preveri med validacijo. Za slepi vzorec z dodatkom mešanice različnih kongenerjev se opravi čiščenje (najmanj n = 3), nato pa se s potrditveno metodo preverita izkoristek in variabilnost. Izkoristek znaša od 60 % do 120 %, zlasti za kongenerje, ki k vrednosti TEQ v različnih mešanicah prispevajo več kot 10 %.
7.1.6 Prag poročanja
Za poročanje o vrednostih BEQ se prag poročanja določi na podlagi ustreznih vzorcev matric, ki vključujejo značilne vzorce kongenerjev, ne pa na podlagi umeritvene krivulje standardov zaradi manjše natančnosti v njenem spodnjem delu. Upoštevati je treba učinke ekstrakcije in čiščenja. Prag poročanja je treba določiti precej nad postopkom s slepimi vzorci (najmanj trikrat višje).
7.2 Uporaba referenčnih vzorcev
|
— |
Referenčni vzorci predstavljajo matrico vzorca, vzorce kongenerjev in območja koncentracij za PCDD/F in dioksinom podobne PCB blizu mejne vrednosti ali praga ukrepanja. |
|
— |
V vsako preskusno serijo je treba vključiti postopek s slepimi vzorci ali po možnosti slepo matrico in referenčni vzorec pri mejni vrednosti ali pragu ukrepanja. Te vzorce je treba ekstrahirati in testirati hkrati in pod enakimi pogoji. Referenčni vzorec mora kazati izrazito večji odziv v primerjavi s slepim vzorcem, kar zagotavlja ustreznost preskusa. Navedeni vzorci se lahko uporabijo za popravek slepih vrednosti in izkoristka. |
|
— |
Referenčni vzorci, ki se izberejo za popravek izkoristka, so reprezentativni za preskusne vzorce, kar pomeni, da vzorci kongenerjev ne povzročijo prenizke ocene vrednosti. |
|
— |
Vključijo se lahko dodatni referenčni vzorci z npr. 0,5-kratno in 2-kratno mejno vrednostjo ali pragom ukrepanja, da se dokaže primerna učinkovitost preskusa v območju predpisane vrednosti za nadzor mejne vrednosti ali praga ukrepanja. Ti vzorci se lahko skupaj uporabijo za izračun vrednosti BEQ v preskusnih vzorcih (glej točko 7.1.2.2). |
7.3 Določitev izločitvenih vrednosti
Določi se razmerje med bioanalitskimi rezultati v BEQ in rezultati potrditvenih metod v TEQ (npr. z umeritvenimi preskusi v matrici, ki vključujejo referenčne vzorce z dodatkom pri 0-kratni, 0,5-kratni, 1-kratni in 2-kratni mejni vrednosti s 6 ponovitvami na vsaki ravni (n = 24)). Na podlagi tega razmerja se lahko ocenijo korekcijski faktorji (za slepe vrednosti in izkoristek), vendar se preverijo v vsaki preskusni seriji z vključitvijo postopka s slepimi vzorci/slepih matric in vzorcev izkoristka (glej točko 7.2).
Izločitvene vrednosti se določijo za sprejetje odločitve o skladnosti vzorca z mejnimi vrednostmi ali za nadzor pragov ukrepanja, če je to relevantno, glede na zadevne mejne vrednosti ali prage ukrepanja, določene za PCDD/F in za dioksinom podobne PCB posebej ali za vsoto PCDD/F in dioksinom podobnih PCB. Prikazuje jih spodnja končna točka porazdelitve bioanalitskih rezultatov (s popravkom slepih vrednosti in izkoristka), ki ustreza odločitveni meji potrditvene metode na podlagi 95-odstotne stopnje zaupanja, kar pomeni, da je delež lažno skladnih rezultatov < 5 %, in na podlagi RSDR < 25 %. Odločitvena meja potrditvene metode je mejna vrednost ob upoštevanju razširjene merilne negotovosti.
V praksi se lahko izločitvena vrednost (v BEQ) izračuna na naslednje načine (glej sliko 1):
7.3.1 Uporaba spodnjega razpona 95-odstotnega napovednega intervala pri odločitveni meji potrditvene metode
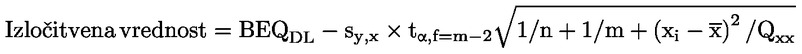 ,
,
pri čemer je:
|
BEQDL |
BEQ, ki ustreza odločitveni meji potrditvene metode, ki je mejna vrednost ob upoštevanju razširjene merilne negotovosti |
|
sy,x |
standardni odmik ostankov |
|
tα,f = m–2 |
Studentov faktor (α = 5 %, f = prostostne stopnje, enostranske) |
|
m |
skupno število umeritvenih točk (indeks j) |
|
n |
število ponovitev na vsaki stopnji |
|
xi |
koncentracija vzorca (v TEQ) umeritvene točke I, določena s potrditveno metodo |
|
|
povprečje koncentracij (v TEQ) vseh umeritvenih vzorcev |
 parameter vsote kvadratov
parameter vsote kvadratov
|
i |
= |
indeks za umeritveno točko i |
7.3.2 Izračun na podlagi bioanalitskih rezultatov (s popravkom slepih vrednosti in izkoristka) večkratnih analiz vzorcev (n > 6), kontaminiranih pri odločitveni meji potrditvene metode, kot spodnja končna točka porazdelitve podatkov pri ustrezni povprečni vrednosti BEQ:
Izločitvena vrednost = BEQDL – 1,64 × SDR,
pri čemer je:
|
SDR |
standardni odmik rezultatov bioloških testov pri BEQDL, izmerjen pri pogojih interne laboratorijske obnovljivosti |
7.3.3 Izračun kot povprečna vrednost bioanalitskih rezultatov (v BEQ, s popravkom slepih vrednosti in izkoristka) večkratnih analiz vzorcev (n ≥ 6), kontaminiranih pri dveh tretjinah mejne vrednosti ali praga ukrepanja. To temelji na ugotovitvi, da bo ta vrednost blizu izločitvene vrednosti iz točke 7.3.1 ali 7.3.2.
Izračun izločitvenih vrednosti na podlagi 95-odstotne stopnje zaupanja, kar pomeni, da je delež lažno skladnih rezultatov < 5 %, in na podlagi RSDR < 25 %:
|
1. |
na podlagi spodnjega razpona 95-odstotnega napovednega intervala pri odločitveni meji potrditvene metode, |
|
2. |
na podlagi večkratnih analiz vzorcev (n ≥ 6), kontaminiranih pri odločitveni meji potrditvene metode, kot spodnja končna točka porazdelitve podatkov (na sliki prikazana s krivuljo v obliki zvonca) pri ustrezni povprečni vrednosti BEQ. |
Slika 1

7.3.4 Omejitve izločitvenih vrednosti:
Izločitvene vrednosti na podlagi BEQ, izračunane iz RSDR, dosežene med validacijo z uporabo omejenega števila vzorcev z različnimi vzorci matric/kongenerjev, so lahko višje od mejnih vrednosti ali praga ukrepanja na podlagi TEQ zaradi večje natančnosti, kot jo je mogoče doseči rutinsko, ko je treba nadzirati neznani spekter mogočih vzorcev kongenerjev. V takih primerih se izločitvene vrednosti izračunajo iz RSDR = 25 %, ali pa se da prednost dvema tretjinama mejne vrednosti ali praga ukrepanja.
7.4 Značilnosti učinkovitosti metode
|
— |
Ker se pri bioanalitskih metodah ne morejo uporabiti interni standardi, se opravijo preskusi ponovljivosti, da se pridobijo informacije o standardnem odmiku v preskusnih serijah in med njimi. Ponovljivost je pod 20 %, interna laboratorijska obnovljivost pa pod 25 %. To temelji na izračunanih vrednosti v BEQ po popravku slepih vrednosti in izkoristka. |
|
— |
V postopku validacije je treba dokazati, da preskus razlikuje med slepim vzorcem in vsebnostjo pri izločitveni vrednosti ter omogoča identifikacijo vzorcev nad ustrezno izločitveno vrednostjo (glej točko 7.1.2). |
|
— |
Opredelijo se ciljne spojine, mogoči moteči vplivi in mejne sprejemljive slepe vrednosti. |
|
— |
Odstotni standardni odmik v odzivu ali koncentracija, izračunana iz odziva (mogoče le v delovnem območju), pri trikratnem določanju ekstrakta vzorca ne presega 15 %. |
|
— |
Nepopravljeni rezultati referenčnih vzorcev, izraženi v BEQ (slepa vrednost in mejna vrednost ali prag ukrepanja), se uporabijo za oceno učinkovitosti bioanalitske metode v stalnem časovnem presledku. |
|
— |
Za postopke s slepimi vzorci in vsako vrsto referenčnega vzorca se vodijo in preverjajo karte za nadzor kakovosti, s čimer se zagotovi, da je analitska učinkovitost v skladu z zahtevami, zlasti pri postopkih s slepimi vzorci glede zahtevane najmanjše razlike do spodnjega dela delovnega območja in pri referenčnih vzorcih glede interne laboratorijske obnovljivosti. Postopke s slepimi vzorci je treba strogo nadzorovati, da bi se izognili lažno skladnim rezultatom pri odštevanju. |
|
— |
Rezultati analiz s potrditveno metodo sumljivih vzorcev in od 2 % do 10 % skladnih vzorcev (najmanj 20 vzorcev na matrico) se zberejo in uporabijo za oceno učinkovitosti presejalne metode ter razmerja med BEQ in TEQ. Ta zbirka podatkov se lahko uporabi za ponovno oceno izločitvenih vrednosti, ki se uporabljajo za rutinske vzorce pri validiranih matricah. |
|
— |
Uspešnost metode se lahko dokaže tudi s sodelovanjem v krožnih preskusih. Rezultati iz vzorcev, analiziranih s krožnimi preskusi, ki zajemajo območje koncentracije do npr. dvakratne mejne vrednosti, se prav tako lahko vključijo v oceno deleža lažno skladnih rezultatov, če laboratorij lahko dokaže svojo učinkovitost. Vzorci zajemajo najpogostejše vzorce kongenerjev, ki predstavljajo različne vire. |
|
— |
Med incidenti se izločitvene vrednosti lahko ponovno ocenijo, pri čemer se upoštevajo posebni vzorci matric in kongenerjev v zadevnem incidentu. |
8. POROČANJE O REZULTATIH
Potrditvene metode
|
— |
Analitski rezultati vsebujejo vrednosti posameznih kongenerjev PCDD/F in dioksinom podobnih PCB, vrednosti TEQ pa se sporočijo kot vrednosti na spodnji meji, zgornji meji in srednji meji, da se v poročilo o rezultatih vključi čim več podatkov in tako omogoči razlaga rezultatov glede na posebne zahteve. |
|
— |
Poročilo vključuje tudi metodo, uporabljeno za ekstrakcijo PCDD/F, dioksinom podobnih PCB in lipidov. Vsebnost lipidov v vzorcu se določi in sporoči za matrice živil z mejnimi vrednostmi, izraženimi na podlagi maščob, in pričakovano koncentracijo maščob v razponu 0–2 % (v skladu z veljavno zakonodajo). Za druge vzorce pa je določitev vsebnosti lipidov neobvezna. |
|
— |
Izkoristki posameznih internih standardov morajo biti na voljo, če so zunaj območja iz točke 6.2, če je presežena mejna vrednost (v tem primeru izkoristki za eno od dveh dvakratnih analiz), in na zahtevo tudi v drugih primerih. |
|
— |
Ker je treba pri odločanju o skladnosti vzorca upoštevati razširjeno merilno negotovost, mora biti na voljo tudi ta parameter. Rezultat analize je zato izražen kot x +/– U, pri čemer je x rezultat analize, U pa razširjena merilna negotovost, kar pri faktorju zajetja 2 pomeni približno 95-odstotno stopnjo zaupanja. Pri ločenem določanju PCDD/F in dioksinom podobnih PCB je treba vsoto ocenjene razširjene negotovosti ločenih rezultatov analize vsebnosti PCDD/F in dioksinom podobnih PCB uporabiti za vsoto PCDD/F in dioksinom podobnih PCB. |
|
— |
Rezultati se izrazijo z istimi enotami in z enakim številom signifikantnih števk kot pri mejnih vrednostih iz Uredbe (ES) št. 1881/2006. |
Bioanalitske presejalne metode
|
— |
Rezultat presejanja se navede kot skladen ali pa kot rezultat s sumom na neskladnost („sumljiv“). |
|
— |
Poleg tega se lahko navede okvirni rezultat za PCDD/F in/ali dioksinom podobne PCB, izražen v BEQ (ne TEQ) (glej točko 1). Za vzorce, pri katerih je odziv pod pragom poročanja, se navede, da so pod pragom poročanja. Za vzorce, pri katerih je odziv nad delovnim območjem, se navede, da presegajo delovno območje, vrednost, ki ustreza zgornjemu delu delovnega območja, pa se navede v BEQ. |
|
— |
Za vsako vrsto matrice vzorca se v poročilu navede mejna vrednost ali prag ukrepanja, na katerem temelji ocena. |
|
— |
V poročilu se navedejo vrsta uporabljenega preskusa, osnovno načelo preskusa in vrsta umerjanja. |
|
— |
Poročilo vključuje tudi metodo, uporabljeno za ekstrakcijo PCDD/F, dioksinom podobnih PCB in lipidov. Vsebnost lipidov v vzorcu se določi in sporoči za matrice živil z mejnimi vrednostmi, izraženimi na osnovi maščob, in pričakovano koncentracijo maščob v razponu 0–2 % (v skladu z veljavno zakonodajo). Za druge vzorce pa je določitev vsebnosti lipidov neobvezna. |
|
— |
Če obstaja sum, da vzorci niso skladni, mora poročilo vključevati navodilo glede potrebnih ukrepov. Koncentracijo PCDD/F ter vsote PCDD/F in dioksinom podobnih PCB v navedenih vzorcih s povišanimi vsebnostmi je treba določiti/potrditi s potrditveno metodo. |
|
— |
Neskladni rezultati se sporočijo samo po potrditveni analizi. |
Fizikalno-kemijske presejalne metode
|
— |
Rezultat presejanja se navede kot skladen ali pa kot rezultat s sumom na neskladnost („sumljiv“). |
|
— |
Za vsako vrsto matrice vzorca se v poročilu navede mejna vrednost ali prag ukrepanja, na katerem temelji ocena. |
|
— |
Poleg tega se lahko navedejo vrednosti posameznih kongenerjev PCDD/F in dioksinom podobnih PCB ter vrednosti TEQ, ki se sporočijo kot vrednosti na spodnji meji, zgornji meji in srednji meji. Rezultati se izrazijo z istimi enotami in z (vsaj) enakim številom signifikantnih števk kot pri mejnih vrednostih iz Uredbe (ES) št. 1881/2006. |
|
— |
Izkoristki posameznih internih standardov morajo biti na voljo, če so zunaj območja iz točke 6.2, in na zahtevo tudi v drugih primerih. |
|
— |
V poročilu se navede uporabljena metoda GC-MS. |
|
— |
Poročilo vključuje tudi metodo, uporabljeno za ekstrakcijo PCDD/F, dioksinom podobnih PCB in lipidov. Vsebnost lipidov v vzorcu se določi in sporoči za matrice živil z mejnimi vrednostmi, izraženimi na osnovi maščob, in pričakovano koncentracijo maščob v razponu 0–2 % (v skladu z veljavno zakonodajo). Za druge vzorce pa je določitev vsebnosti lipidov neobvezna. |
|
— |
Če obstaja sum, da vzorci niso skladni, mora poročilo vključevati navodilo glede potrebnih ukrepov. Koncentracijo PCDD/F ter vsote PCDD/F in dioksinom podobnih PCB v navedenih vzorcih s povišanimi vsebnostmi je treba določiti/potrditi s potrditveno metodo. |
|
— |
Odločitev o neskladnosti se lahko sprejme samo po potrditveni analizi. |
(1) Smernice o merilni negotovosti za laboratorije, ki opravljajo analize vsebnosti PCDD/F in PCB z uporabo izotopske razredčitve – masne spektrometrije [povezava na spletno stran], smernice za ocenjevanje meje zaznavnosti (LOD) in meje določljivosti (LOQ) za meritve na področju onesnaževal v krmi in živilih [povezava na spletno stran].
(*1) Glede na mejne vrednosti.
(2) Sedanje zahteve temeljijo na TEF, ki so objavljeni v: M. Van den Berg in drugi, Toxicological Sciences 93 (2), str. 223–241 (2006).
Dodatek
TEF Svetovne zdravstvene organizacije (SZO) za oceno tveganja za zdravje ljudi na podlagi sklepov SZO – strokovnega srečanja mednarodnega programa za kemijsko varnost (IPCS) junija 2005 v Ženevi (1)
|
Kongener |
Vrednost TEF |
Kongener |
Vrednost TEF |
||
|
Dibenzo-p-dioksini („PCDD“) |
„Dioksinom podobni“ PCB: neorto PCB + monoorto PCB |
||||
|
2,3,7,8-TCDD |
1 |
|
|
||
|
1,2,3,7,8-PeCDD |
1 |
Neorto PCB |
|
||
|
1,2,3,4,7,8-HxCDD |
0,1 |
PCB 77 |
0,0001 |
||
|
1,2,3,6,7,8-HxCDD |
0,1 |
PCB 81 |
0,0003 |
||
|
1,2,3,7,8,9-HxCDD |
0,1 |
PCB 126 |
0,1 |
||
|
1,2,3,4,6,7,8-HpCDD |
0,01 |
PCB 169 |
0,03 |
||
|
OCDD |
0,0003 |
|
|
||
|
Dibenzofurani (PCDF) |
Monoorto PCB |
||||
|
2,3,7,8-TCDF |
0,1 |
PCB 105 |
0,00003 |
||
|
1,2,3,7,8-PeCDF |
0,03 |
PCB 114 |
0,00003 |
||
|
2,3,4,7,8-PeCDF |
0,3 |
PCB 118 |
0,00003 |
||
|
1,2,3,4,7,8-HxCDF |
0,1 |
PCB 123 |
0,00003 |
||
|
1,2,3,6,7,8-HxCDF |
0,1 |
PCB 156 |
0,00003 |
||
|
1,2,3,7,8,9-HxCDF |
0,1 |
PCB 157 |
0,00003 |
||
|
2,3,4,6,7,8-HxCDF |
0,1 |
PCB 167 |
0,00003 |
||
|
1,2,3,4,6,7,8-HpCDF |
0,01 |
PCB 189 |
0,00003 |
||
|
1,2,3,4,7,8,9-HpCDF |
0,01 |
|
|
||
|
OCDF |
0,0003 |
|
|
||
|
|||||
(1) Martin van den Berg in drugi, Ponovna ocena faktorjev toksične ekvivalentnosti za dioksine in dioksinom podobne spojine pri ljudeh in sesalcih, Svetovna zdravstvena organizacija, 2005 (The 2005 World Health Organization Re-evaluation of Human and Mammalian Toxic Equivalency Factors for Dioxins and Dioxin-like Compounds). Toxicological Sciences 93(2), str. 223–241 (2006).
PRILOGA IV
PRIPRAVA VZORCA IN ZAHTEVE ZA ANALITSKE METODE ZA NADZOR VSEBNOSTI DIOKSINOM NEPODOBNIH PCB V NEKATERIH ŽIVILIH
Zahteve, določene v tej prilogi, se uporabijo, kadar se živila analizirajo za uradni nadzor vsebnosti dioksinom nepodobnih PCB, in za pripravo vzorcev in analitske zahteve za druge regulativne namene, vključno z nadzorom, ki ga izvajajo nosilci živilske dejavnosti za zagotovitev skladnosti z določbami člena 4 Uredbe (ES) št. 852/2004.
Določbe o pripravi vzorcev iz točke 3 Priloge III k tej uredbi se uporabljajo tudi za nadzor vsebnosti dioksinom nepodobnih PCB v živilih.
1. Metode ugotavljanja, ki se uporabljajo
Plinska kromatografija/detekcija zajetja elektronov (GC-ECD), GC-LRMS, GC-MS/MS, GC-HRMS ali enakovredne metode.
2. Identifikacija in potrditev predpisanih analitov
|
— |
Relativni retencijski čas glede na interne standarde ali referenčne standarde (sprejemljivi odmik +/– 0,25 %). |
|
— |
Plinsko kromatografsko ločevanje dioksinom nepodobnih PCB (od motečih snovi, zlasti sočasno eluiranih PCB, še posebej če so vrednosti vzorcev v območju zakonsko dovoljenih mej in je treba potrditi neskladnost (1)). |
|
— |
Za tehnike GC-MS:
|
|
— |
Za GC-ECD: Potrditev rezultatov, ki presegajo mejno vrednost, z dvema kolonama GC s stacionarnimi fazami različne polarnosti. |
3. Dokazovanje učinkovitosti metode
Validacija v območju mejne vrednosti (0,5-kratna do 2-kratna mejna vrednost) s sprejemljivim koeficientom variacije za ponovljene analize (glej zahteve za srednjo natančnost v točki 8).
4. Meja določljivosti
Vsota LOQ (2) dioksinom nepodobnih PCB ne sme presegati tretjine mejne vrednosti (3).
5. Nadzor kakovosti
Redne slepe kontrole, analize vzorcev z dodatkom, vzorci za nadzor kakovosti, sodelovanje v medlaboratorijskih študijah z relevantnimi matricami.
6. Nadzor izkoristkov
|
— |
Uporaba primernih internih standardov s fizikalno-kemijskimi lastnostmi, ki so primerljive s tistimi, ki jih imajo predpisani analiti. |
|
— |
Dodajanje internih standardov:
|
|
— |
Zahteve za metode, pri katerih se uporablja vseh šest izotopsko označenih kongenerjev dioksinom nepodobnih PCB:
|
|
— |
Zahteve za metode, pri katerih se ne uporablja vseh šest izotopsko označenih internih standardov ali drugi interni standardi:
|
|
— |
Izkoristek neoznačenih kongenerjev se preveri z analizo vzorcev z dodatkom ali vzorcev za nadzor kakovosti s koncentracijami v območju mejne vrednosti. Sprejemljivi izkoristek za te kongenerje je med 60 % in 120 %. |
7. Zahteve za laboratorije
V skladu z določbami Uredbe (ES) št. 882/2004 laboratorije akreditirajo priznani organi, ki delujejo v skladu z zahtevami vodnika ISO 58, s čimer je zagotovljeno, da izvajajo analitsko zagotavljanje kakovosti. Laboratoriji se akreditirajo po standardu EN ISO/IEC 17025. Poleg tega se, kadar je primerno, upoštevajo načela, kot so opisana v tehničnih smernicah za oceno merilne negotovosti in mej določljivosti za analizo vsebnosti PCB (4).
8. Značilnosti učinkovitosti metode: merila za vsoto dioksinom nepodobnih PCB pri mejni vrednosti:
|
|
Izotopska razredčitev – masna spektrometrija (*1) |
Druge tehnike |
|
Pravilnost |
– 20 % do + 20 % |
– 30 % do + 30 % |
|
Srednja natančnost (RSDR) |
≤ 15 % |
≤ 20 % |
|
Razlika med izračunom zgornje in spodnje meje |
≤ 20 % |
≤ 20 % |
9. Poročanje o rezultatih
|
— |
Analitski rezultati vsebujejo vrednosti posameznih kongenerjev dioksinom nepodobnih PCB ter vsote dioksinom nepodobnih PCB, sporočijo pa se kot vrednosti na spodnji meji, zgornji meji in srednji meji, da se v poročilo o rezultatih vključi čim več podatkov in tako omogoči razlaga rezultatov glede na posebne zahteve. |
|
— |
Poročilo vključuje tudi metodo, uporabljeno za ekstrakcijo PCB in lipidov. Vsebnost lipidov v vzorcu se določi in sporoči za matrice živil z mejnimi vrednostmi, izraženimi na osnovi maščob, in pričakovano koncentracijo maščob v razponu 0–2 % (v skladu z veljavno zakonodajo). Za druge vzorce pa je določitev vsebnosti lipidov neobvezna. |
|
— |
Izkoristki posameznih internih standardov morajo biti na voljo, če so zunaj območja iz točke 6, če je presežena mejna vrednost, in na zahtevo tudi v drugih primerih. |
|
— |
Ker je treba pri odločanju o skladnosti vzorca upoštevati razširjeno merilno negotovost, mora biti na voljo tudi navedeni parameter. Rezultat analize je zato izražen kot x +/– U, pri čemer je x rezultat analize, U pa razširjena merilna negotovost, kar pri faktorju zajetja 2 pomeni približno 95-odstotno stopnjo zaupanja. |
|
— |
Rezultati se izrazijo z istimi enotami in z enakim številom signifikantnih števk kot pri mejnih vrednostih iz Uredbe (ES) št. 1881/2006. |
(1) Kongenerji, za katere je pogosto ugotovljeno, da se sočasno eluirajo, so npr. PCB 28/31, PCB 52/69 in PCB 138/163/164. Pri GC-MS je treba upoštevati tudi mogoče moteče vplive fragmentov višjih kloriranih kongenerjev.
(2) Kadar je primerno, se upoštevajo načela, kot so opisana v smernicah za ocenjevanje meje zaznavnosti (LOD) in meje določljivosti (LOQ) za meritve na področju onesnaževal v krmi in živilih [povezava na spletno stran].
(3) Zelo priporočljivo je, da je prispevek slepega reagenta k vsebnosti onesnaževala v vzorcu manjši. Laboratorij je odgovoren za nadzor spreminjanja slepih vrednosti, zlasti če se slepe vrednosti odštejejo.
(4) Smernice o merilni negotovosti za laboratorije, ki opravljajo analize vsebnosti PCDD/F in PCB z uporabo izotopske razredčitve – masne spektrometrije [povezava na spletno stran], smernice za ocenjevanje meje zaznavnosti (LOD) in meje določljivosti (LOQ) za meritve na področju onesnaževal v krmi in živilih [povezava na spletno stran].
(*1) Potrebna je uporaba vseh šestih 13C-označenih analogov kot internih standardov.