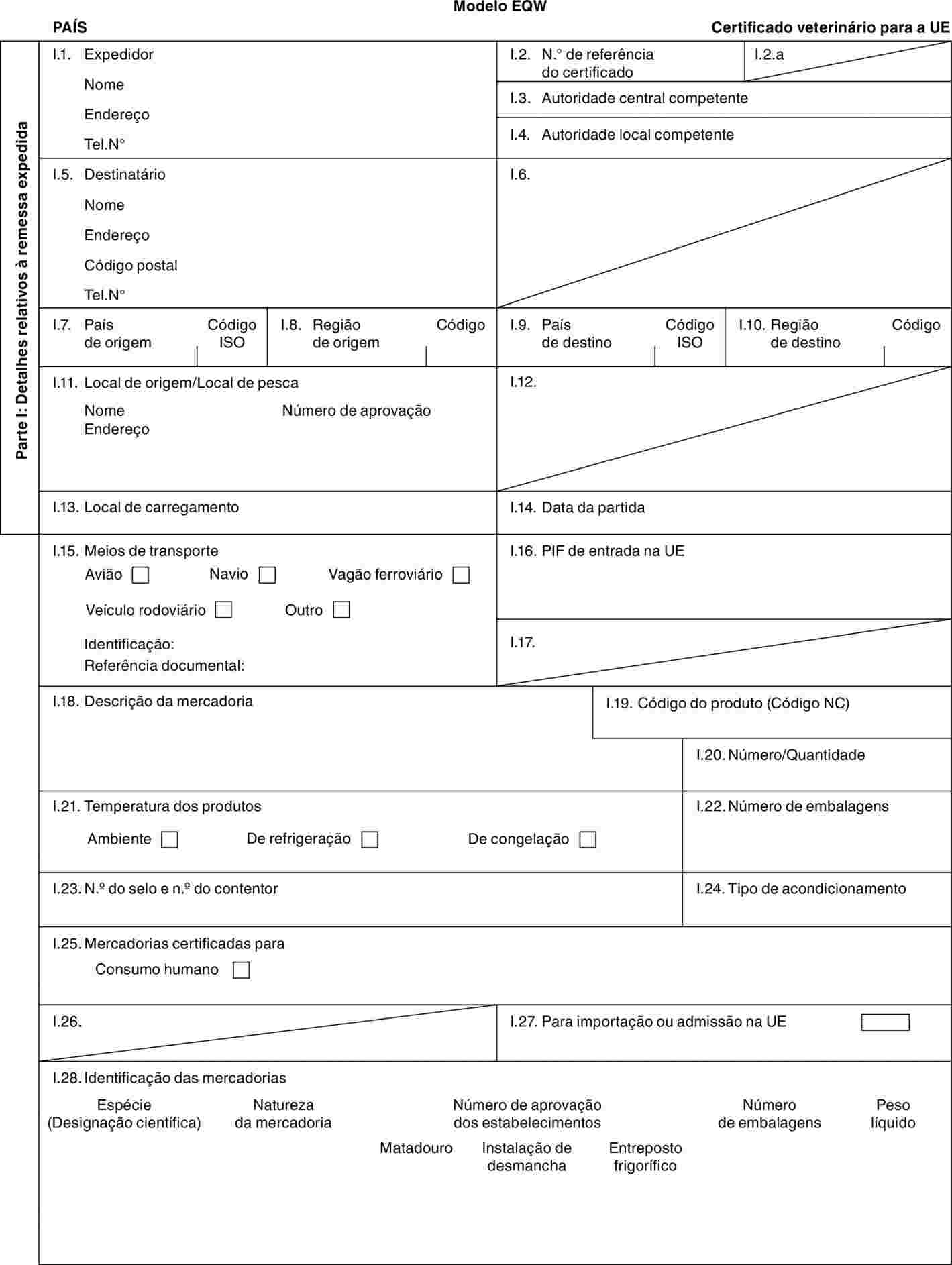
ANEXO I
UNGULADOS
PARTE 1
Lista de países terceiros, territórios ou partes destes (21)
|
Código ISO e nome do país terceiro |
Código do território |
Descrição do país terceiro, território ou parte destes |
Certificado veterinário |
Condições específicas |
|||||||
|
Modelo(s) |
GS |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
||||||
|
CA – Canadá |
CA-0 |
Todo o país |
POR-X |
|
IVb IX |
||||||
|
CA-1 |
Todo o país, excepto a região do vale de Okanagan, na Colúmbia Britânica, a seguir descrita:
|
BOV-X, OVI-X, OVI-Y RUM (22) |
A |
||||||||
|
CH – Suíça |
CH-0 |
Todo o país |
|
|
|||||||
|
CL – Chile |
CL-0 |
Todo o país |
BOV-X, OVI-X, RUM |
|
|
||||||
|
POR-X, SUI |
B |
|
|||||||||
|
GL – Gronelândia |
GL-0 |
Todo o país |
OVI-X, RUM |
|
V |
||||||
|
HR – Croácia |
HR-0 |
Todo o país |
BOV-X, BOV-Y, RUM, |
|
|
||||||
|
IS – Islândia |
IS-0 |
Todo o país |
OVI-X, OVI-Y BOV-X, BOV-Y RUM, OVI-X, OVI-Y |
|
|
||||||
|
POR-X, POR-Y |
B |
||||||||||
|
ME – Montenegro |
ME-0 |
Todo o país |
|
|
I |
||||||
|
MK – antiga República jugoslava da Macedónia (24) |
MK-0 |
Todo o país |
|
|
I |
||||||
|
NZ – Nova Zelândia |
NZ-0 |
Todo o país |
BOV-X, BOV-Y, RUM, POR-X, POR-Y OVI-X, OVI-Y |
|
III V |
||||||
|
PM – São Pedro e Miquelon |
PM-0 |
Todo o país |
BOV-X, BOV-Y, RUM, OVI-X, OVI-Y CAM |
|
|
||||||
|
RS – Sérvia (25) |
RS-0 |
Todo o país |
|
|
I |
||||||
Condições específicas (ver notas-de-rodapé em cada certificado):
|
«I» |
: |
para trânsito, através do território de um país terceiro, de animais vivos para abate imediato ou de bovinos vivos para engorda que são expedidos de um Estado-Membro e se destinam a outro Estado-Membro em camiões que foram selados com um selo numerado sequencialmente. O número de selo deve ser inscrito no certificado sanitário emitido em conformidade com o modelo estabelecido no anexo F da Directiva 64/432/CEE (26), para os bovinos vivos para abate e engorda, e em conformidade com o modelo I do anexo E da Directiva 91/68/CEE (27), para ovinos e caprino para abates. Além disso, o selo deve estar intacto à chegada ao posto de inspecção fronteiriço designado de entrada na União e o número de selo registado no sistema informático veterinário integrado da União (TRACES). O certificado deve ser carimbado no ponto de saída da União pela autoridade veterinária competentes antes do trânsito através de um ou mais países terceiros com a seguinte menção «APENAS PARA TRÂNSITO ENTRE PARTES DIFERENTES DA UNIÃO EUROPEIA ATRAVÉS DA ANTIGA REPÚBLICA JUGOSLAVA DA MACEDÓNIA/DO MONTENEGRO/DA SÉRVIA (28) (29)». Os bovinos para engorda devem ser transportados directamente para a exploração de destino designada pela autoridade veterinária competente de destino. Esses animais só podem sair dessa exploração para abate imediato. |
|
«II» |
: |
território com um estatuto oficial reconhecido de indemnidade de tuberculose para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado BOV-X. |
|
«III» |
: |
território com um estatuto oficial reconhecido de indemnidade de brucelose para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado BOV-X. |
|
«IVa» |
: |
território com um estatuto oficial reconhecido de indemnidade de leucose bovina enzoótica para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado BOV-X. |
|
«IVb» |
: |
território com explorações aprovadas com um estatuto oficial reconhecido de indemnidade de leucose bovina enzoótica para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado BOV-X. |
|
«V» |
: |
território com um estatuto oficial reconhecido de indemnidade de brucelose para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado OVI-X. |
|
«VI» |
: |
restrições geográficas. |
|
«VII» |
: |
território com um estatuto oficial reconhecido de indemnidade de tuberculose para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado RUM. |
|
«VIII» |
: |
território com um estatuto oficial reconhecido de indemnidade de brucelose para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado RUM. |
|
«IX» |
: |
território com um estatuto oficial reconhecido de indemnidade da doença de Aujeszky para efeitos da exportação para a União de animais vivos certificados segundo o modelo de certificado POR-X. |
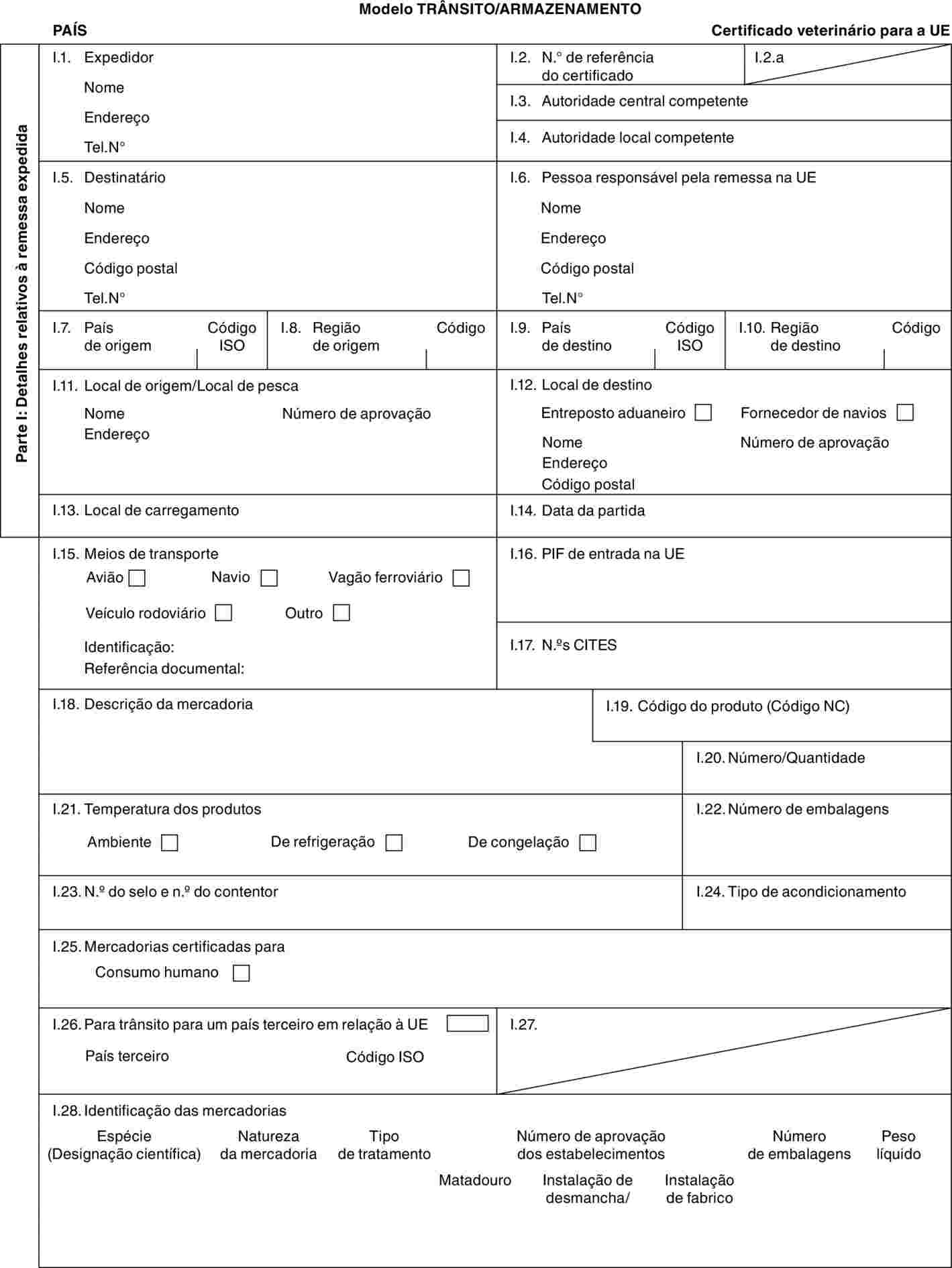
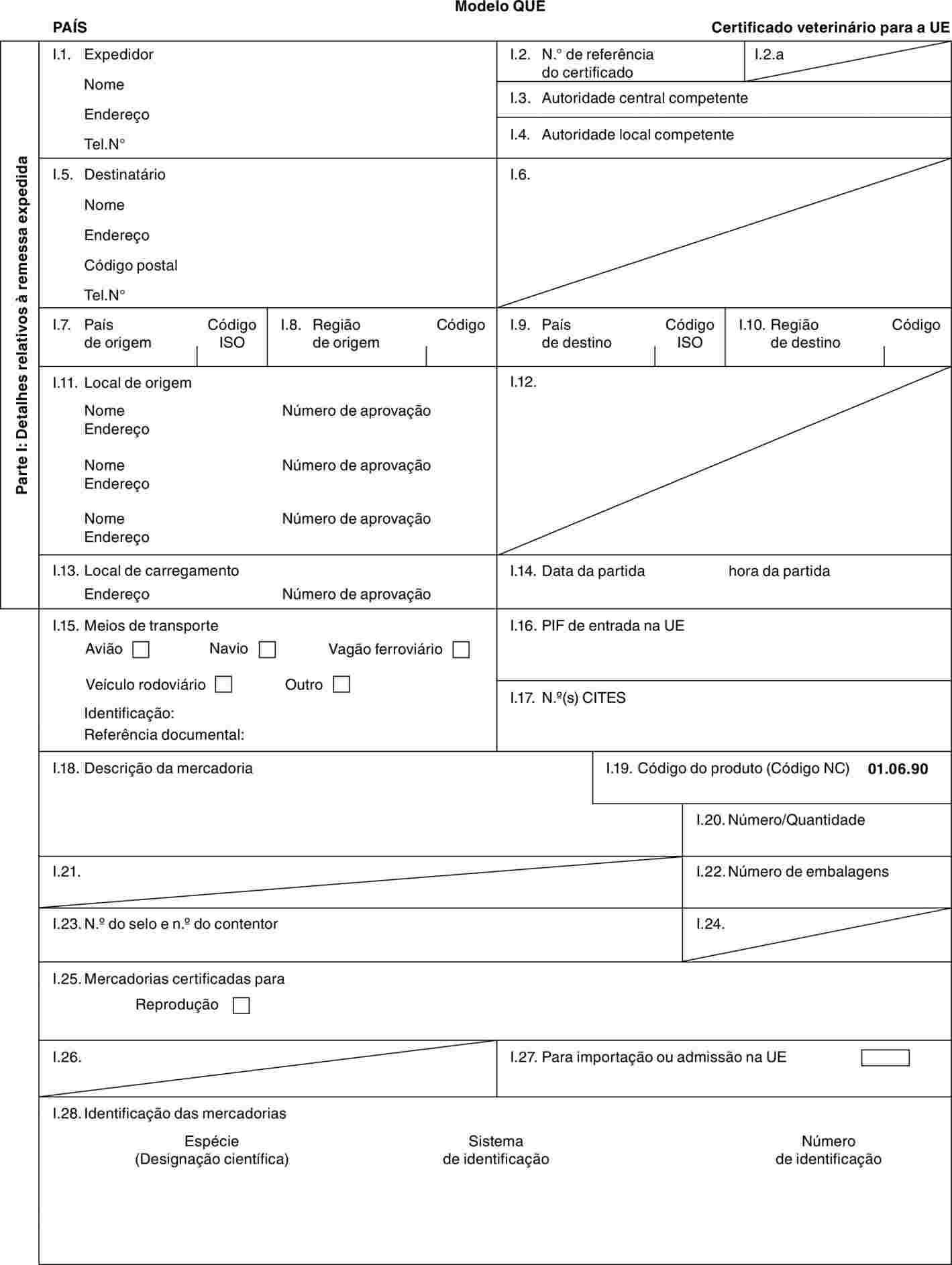
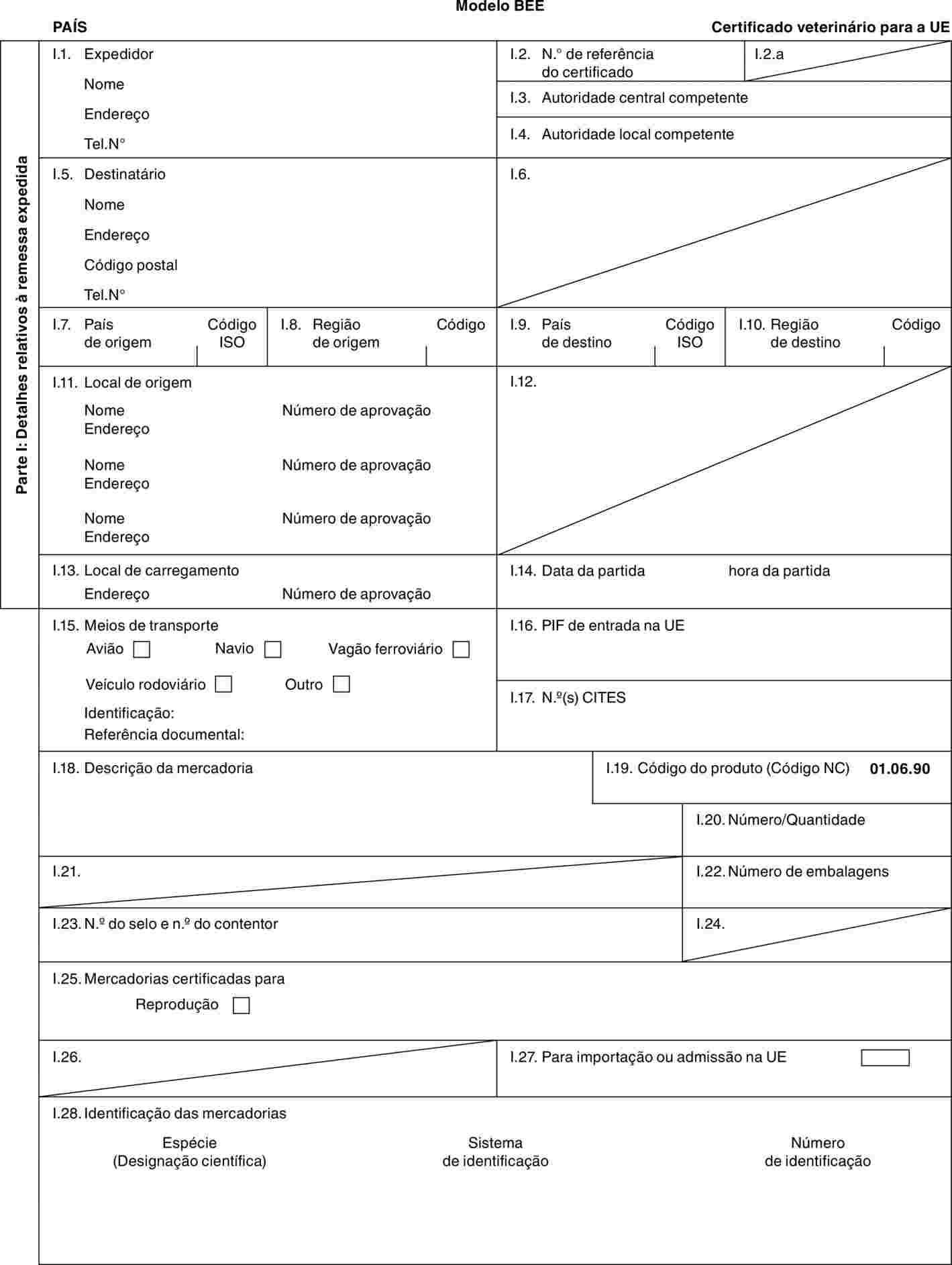
PARTE 2
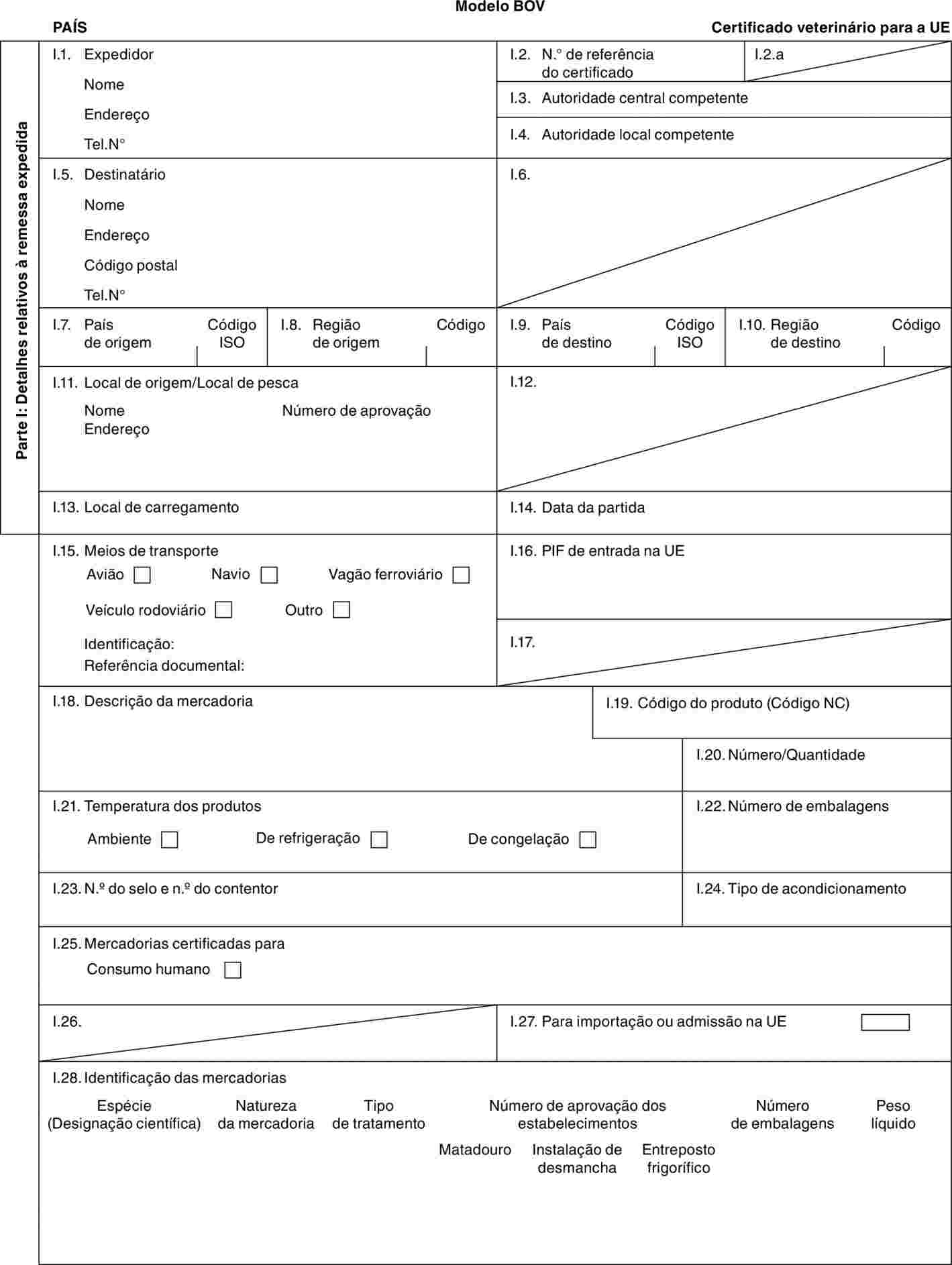
Modelos de certificados veterinários
Modelos:
|
«BOV-X» |
: |
modelo de certificado veterinário para bovinos domésticos (incluindo as espécies Bubalus e Bison e respectivos cruzamentos) destinados a reprodução e/ou rendimento após a importação. |
|
«BOV-Y» |
: |
modelo de certificado veterinário para bovinos domésticos (incluindo as espécies Bubalus e Bison e respectivos cruzamentos) destinados a abate imediato após a importação. |
|
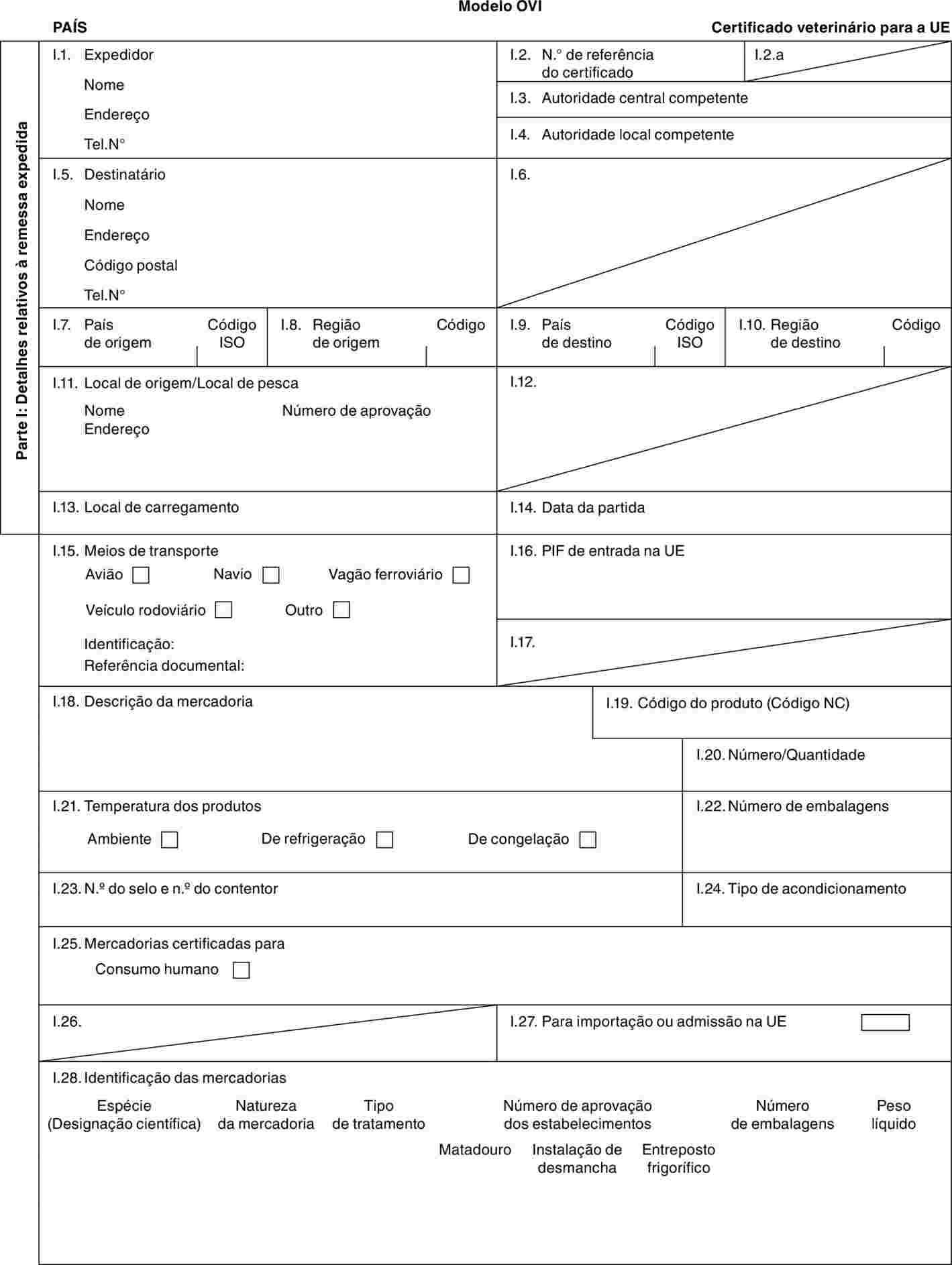
«OVI-X» |
: |
modelo de certificado veterinário para ovinos domésticos (Ovis aries) e caprinos domésticos (Capra hircus) destinados a reprodução e/ou rendimento após a importação. |
|
«OVI-Y» |
: |
modelo de certificado veterinário para ovinos domésticos (Ovis aries) e caprinos domésticos (Capra hircus) destinados a abate imediato após a importação. |
|
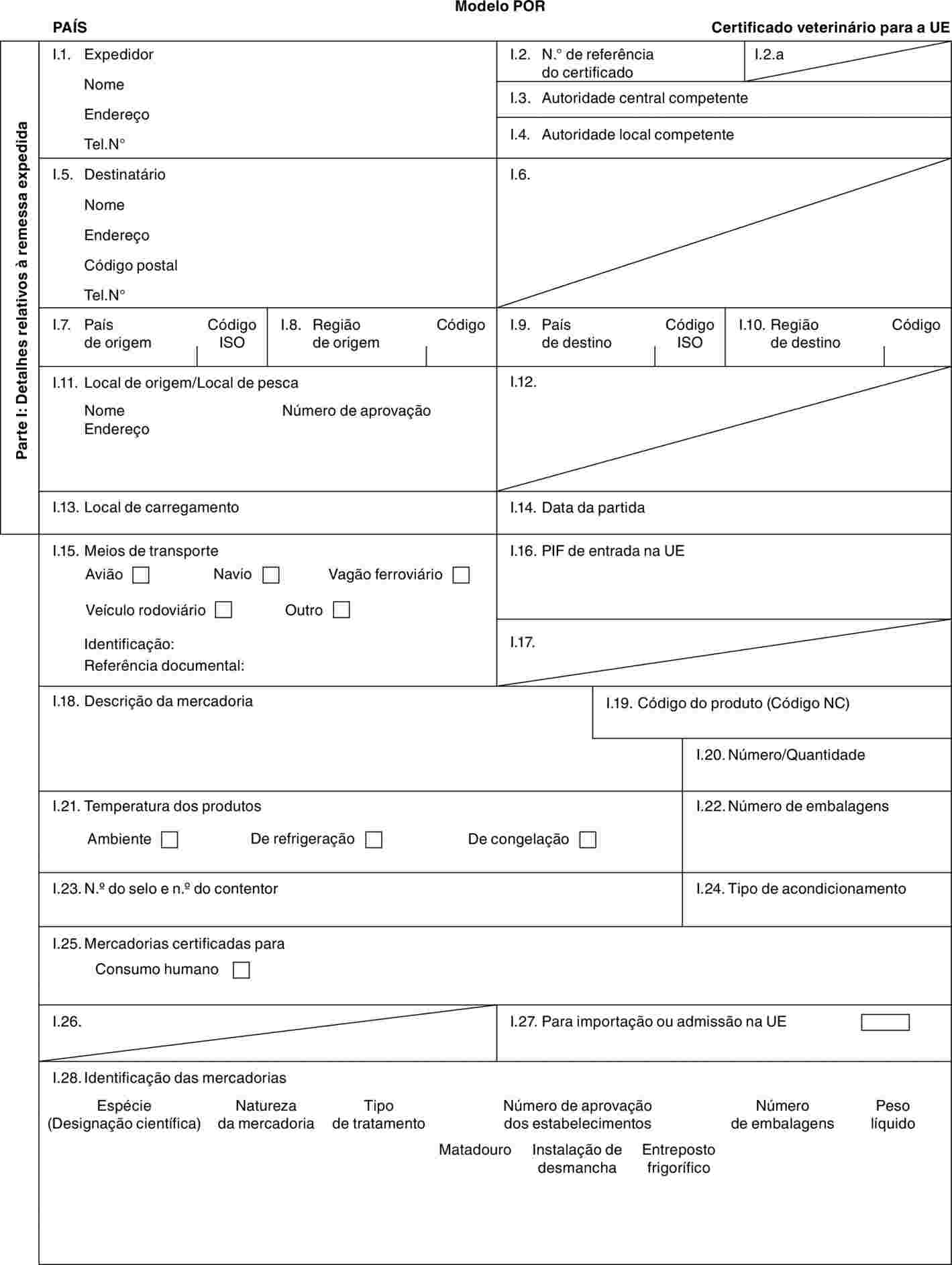
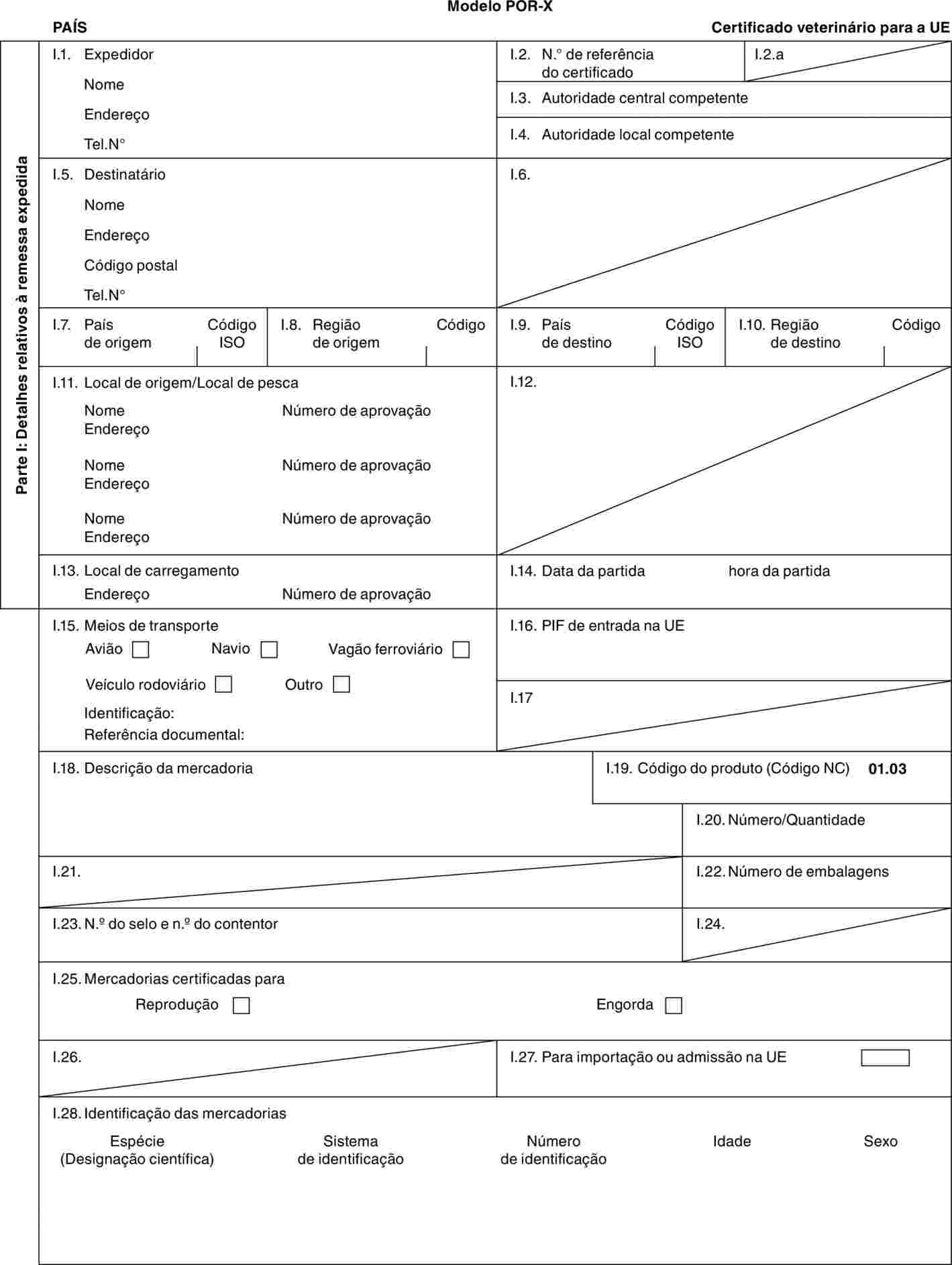
«POR-X» |
: |
modelo de certificado veterinário para suínos domésticos (Sus scrofa) destinados a reprodução e/ou rendimento após a importação. |
|
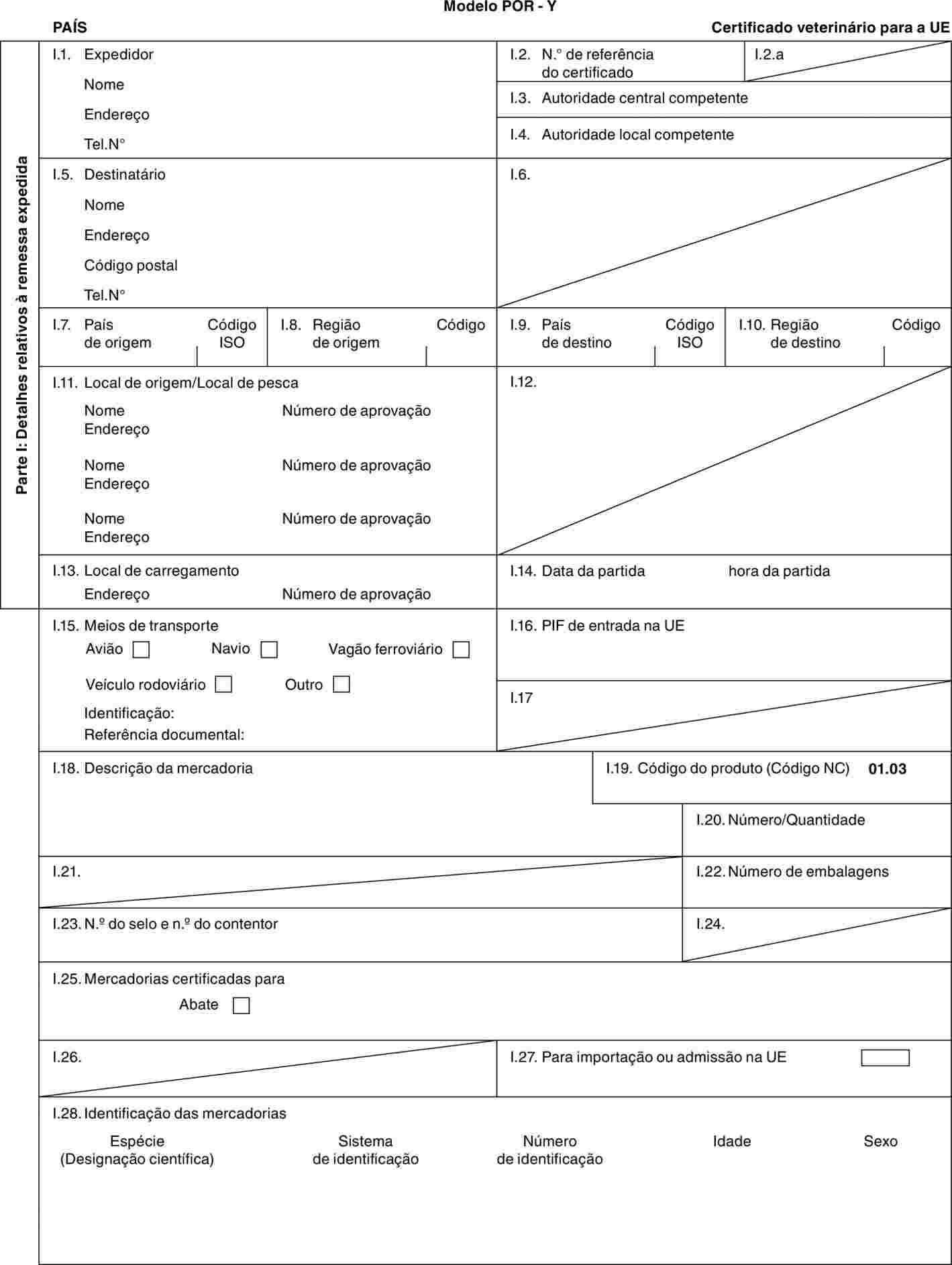
«POR-Y» |
: |
modelo de certificado veterinário para suínos domésticos (Sus scrofa) destinados a abate imediato após a importação. |
|
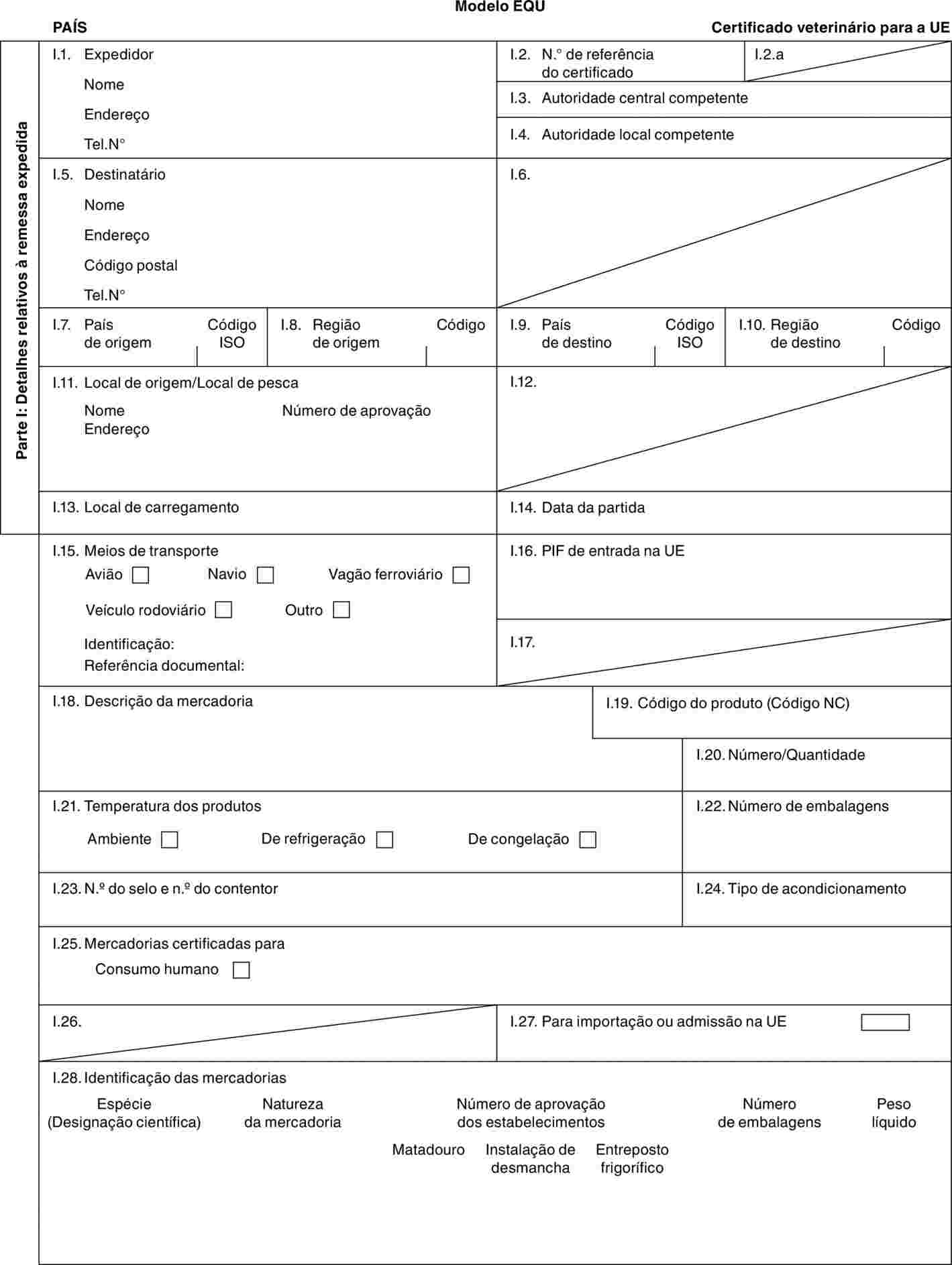
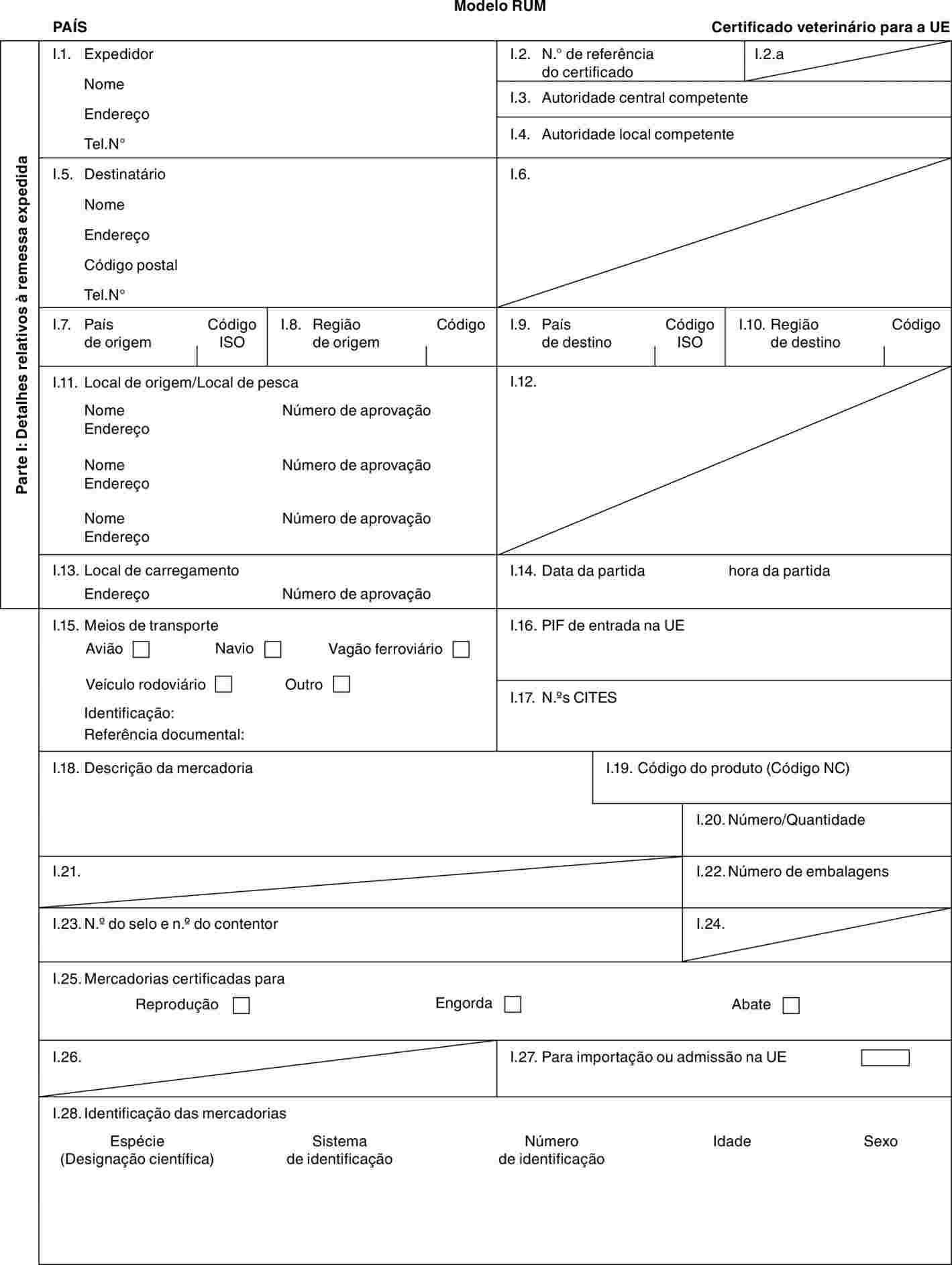
«RUM» |
: |
modelo de certificado veterinário para animais da ordem Artiodactyla [excluindo bovinos (incluindo as espécies Bubalus e Bison e respectivos cruzamentos), Ovis aries, Capra hircus, Suidae e Tayassuidae], e das famílias Rhinocerotidae e Elephantidae. |
|
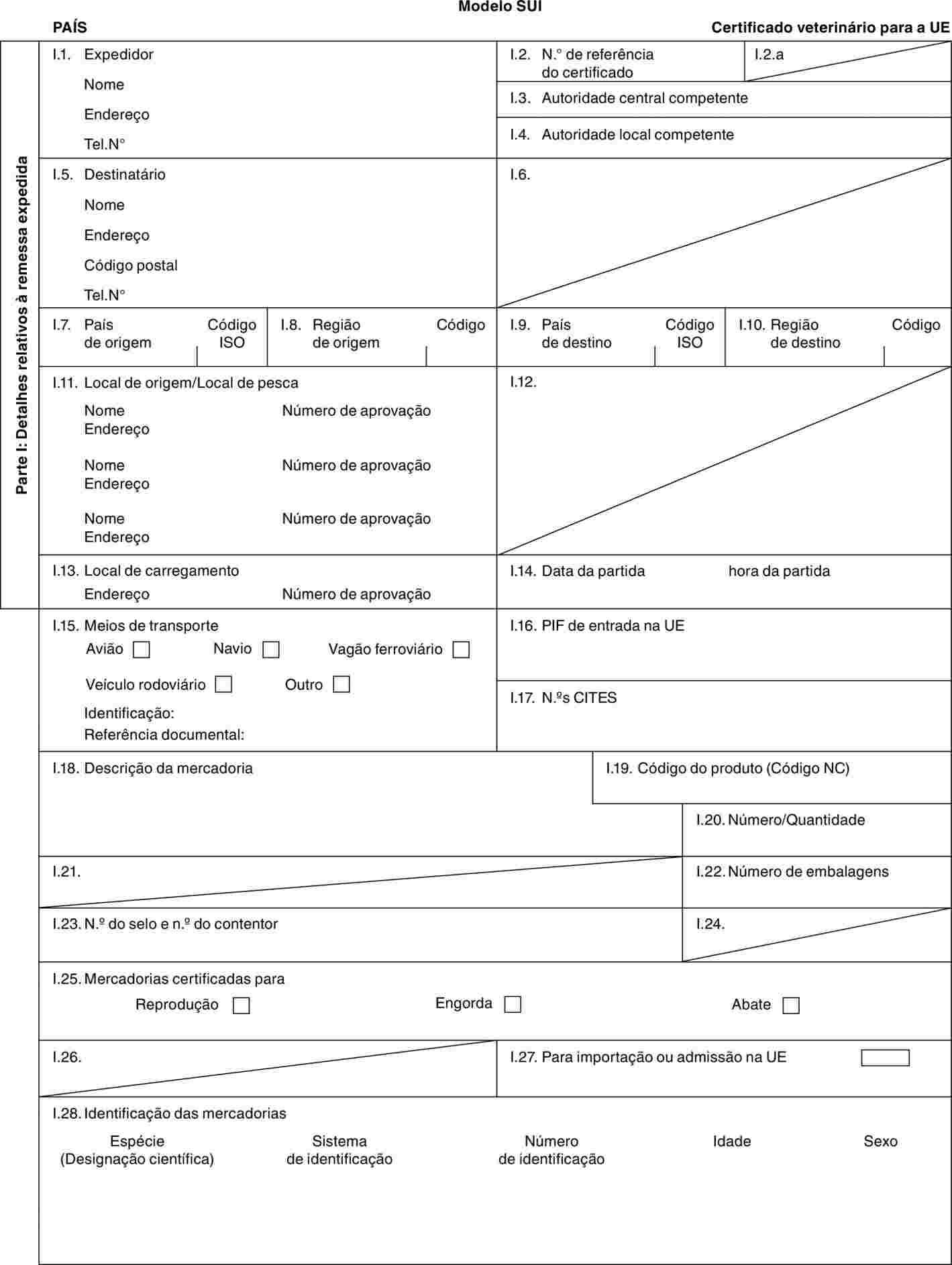
«SUI» |
: |
modelo de certificado veterinário para Suidae, Tayassuidae e Tapiridae não domésticos. |
|
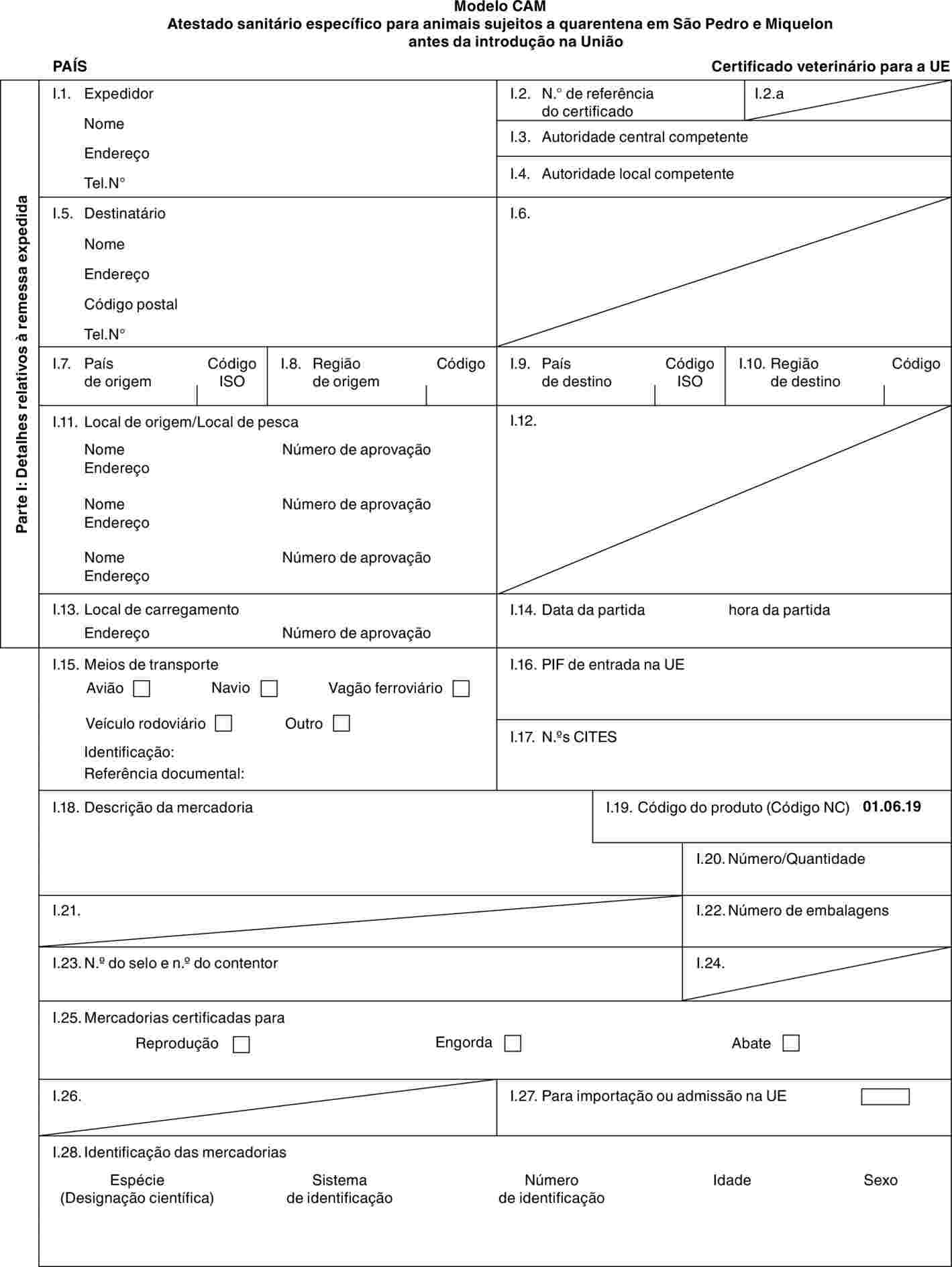
«CAM» |
: |
modelo de atestado específico para animais importados de São Pedro e Miquelon nas condições previstas na parte 7 do anexo I. |
GS (Garantias suplementares):
|
«A» |
: |
garantias relativas aos testes de detecção da febre catarral ovina e da doença hemorrágica epizoótica nos animais certificados segundo os modelos de certificado BOV-X (ponto II.2.8 B), OVI-X (ponto II.2.6 D) e RUM (ponto II.2.6). |
|
«B» |
: |
garantias relativas aos testes de detecção da doença vesiculosa dos suínos e da peste suína clássica nos animais certificados segundo os modelos de certificado POR-X (ponto II.2.4 B) e SUI (ponto II.2.4 B). |
|
«C» |
: |
garantias relativas aos testes de detecção da brucelose nos animais certificados segundo os modelos de certificado POR-X (ponto II.2.4 C) e SUI (ponto II.2.4 C). |































PARTE 3
Adenda para o transporte de animais por via marítima
(A preencher e anexar ao certificado veterinário quando o transporte até à fronteira da União incluir, ainda que só em parte do percurso, o transporte por navio)
|
Declaração do comandante do navio |
|
|
O abaixo assinado, comandante do navio (nome …), declara que os animais referidos no certificado veterinário anexo n.o … permaneceram a bordo do navio durante a viagem de … em … (país de exportação) para …, na União, e que o navio não fez escala em porto algum fora de … (país de exportação) durante o percurso até à União, a não ser: … (portos de escala). Além disso, durante a viagem, os animais não estiveram em contacto, a bordo, com animais de estatuto sanitário inferior. Feito em …, em … |
|
|
(porto de chegada) |
(data de chegada) |
|
(carimbo) |
(assinatura do comandante) |
|
(nome em maiúsculas e cargo) |
|
PARTE 4
Adenda para o transporte de animais por via aérea
(A preencher e anexar ao certificado veterinário quando o transporte até à fronteira da União incluir, ainda que só em parte do percurso, o transporte por avião)
|
Declaração do comandante do avião |
|
|
O abaixo assinado, comandante do avião (nome …), declara que a grade ou contentor e a zona circundante onde se encontram os animais referidos no certificado veterinário anexo n.o … foram pulverizadas com insecticida antes da partida. Feito em …, em … |
|
|
(aeroporto de partida) |
(data de partida) |
|
(carimbo) |
(assinatura do comandante) |
|
(nome em maiúsculas e cargo) |
|
PARTE 5
Condições para a aprovação de centros de agrupamento (como referido no artigo 4.o)
Para serem aprovados, os centros de agrupamento devem satisfazer os seguintes requisitos:
|
I. |
Devem estar sob a supervisão de um veterinário oficial. |
|
II. |
Devem situar-se no centro de uma área com, pelo menos, 20 km de diâmetro na qual, de acordo com verificações oficiais, não tenha ocorrido qualquer caso de febre aftosa durante um período de pelo menos 30 dias antes de serem utilizados como centros de agrupamento aprovados. |
|
III. |
Devem, antes da sua utilização como centros de agrupamento aprovados, ser limpos e desinfectados com um desinfectante oficialmente aprovado no país de exportação como eficaz no controlo da febre aftosa. |
|
IV. |
Devem, atendendo à sua capacidade, dispor de:
|
|
V. |
Os centros devem dispor, para o seu funcionamento, de veterinários suficientes para realizar todas as tarefas indicadas na parte 5. |
|
VI. |
Só devem, a fim de garantir a rastreabilidade, admitir animais que estejam individualmente identificados. Para esse efeito, aquando da admissão de animais, o proprietário ou o responsável do centro deve certificar-se de que os animais se encontram devidamente identificados e acompanhados dos documentos ou dos certificados sanitários correspondentes à espécie e à categoria em causa. Além disso, o proprietário ou o responsável do centro de agrupamento deve registar, num registo ou numa base de dados, e conservar durante pelo menos três anos, o nome do proprietário, a origem dos animais, as datas de entrada e saída, o número de identificação dos animais ou o número de registo do efectivo de origem e da exploração de destino e, ainda, o número de registo do transportador e o número de registo do camião que entrega ou recolhe os animais nesse centro de agrupamento. |
|
VII. |
Todos os animais que passem pelos centros de agrupamento aprovados devem satisfazer as condições sanitárias estabelecidas para a introdução na União de animais dessa categoria. |
|
VIII. |
Os animais a introduzir na União que passam por um centro de agrupamento aprovado devem, no prazo de seis dias após a chegada ao centro do agrupamento, ser carregados e expedidos directamente para a fronteira do país de exportação:
|
|
IX. |
Sempre que as condições para a exportação de animais para a União imponham a realização de um teste dentro de um determinado prazo antes do carregamento, esse prazo deve incluir qualquer período de agrupamento, até seis dias, desde a data de chegada dos animais ao centro de agrupamento aprovado. |
|
X. |
O país terceiro de exportação deve designar os centros que são aprovados para animais de reprodução e rendimento e os centros que são aprovados para animais destinados ao abate e deve notificar a Comissão e as autoridades centrais competentes dos Estados-Membros dos nomes e endereços desses centros. Estes dados devem ser actualizados periodicamente. |
|
XI. |
O país terceiro de exportação deve determinar o processo de supervisão oficial dos centros de agrupamento aprovados e deve assegurar a realização dessa supervisão. |
|
XII. |
Os centros de agrupamento aprovados devem ser inspeccionados regularmente pela autoridade competente do país terceiro a fim de se verificar que os requisitos para a aprovação estabelecidos nos pontos I a XI continuam a ser respeitados. Se essas inspecções mostrarem que as condições já não são respeitadas, a aprovação do centro deve ser suspensa. A aprovação só pode ser restabelecida quando a autoridade competente do país terceiro considerar que o centro satisfaz integralmente as disposições referidas nos pontos I a XI. |
PARTE 6
Protocolos de normalização das matérias utilizadas e das técnicas de execução dos testes
(referidos no artigo 5.o)
Tuberculose (TBL)
Intradermotuberculinização simples com tuberculina bovina: a executar de acordo com o anexo B da Directiva 64/432/CEE. No caso dos Suidae, intradermotuberculinização simples com tuberculina aviária: a executar de acordo com o anexo B da Directiva 64/432/CEE; no entanto, a injecção deve ser dada numa prega de pele na base da orelha.
Brucelose (Brucella abortus) (BRL)
Prova de seroaglutinação, prova da reacção de fixação do complemento, prova do antigénio brucélico tamponado e provas de imunoabsorção enzimática (ELISA): a executar de acordo com o anexo C da Directiva 64/432/CEE.
Brucelose (Brucella melitensis) (BRL)
Provas a executar de acordo com o anexo C da Directiva 91/68/CEE.
Leucose bovina enzoótica (LBE)
Prova de imunodifusão em gel de ágar e prova de imunoabsorção enzimática (ELISA): a executar de acordo com o capítulo II, partes A e C, do anexo D da Directiva 64/432/CEE.
Febre catarral ovina (FCO)
Prova ELISA de bloqueio ou competitiva: a executar de acordo com o seguinte protocolo:
A prova ELISA competitiva realizada com o anticorpo monoclonal 3-17-A3 permite detectar anticorpos de todos os serótipos conhecidos do vírus da febre catarral ovina (VFCO).
O fundamento da prova é a interrupção da reacção entre o antigénio do VFCO e um anticorpo monoclonal específico de grupo (3-17-A3) por adição de soro de ensaio. Os anticorpos do VFCO presentes no soro de ensaio bloqueiam a reactividade do anticorpo monoclonal (AMC), o que origina uma redução do desenvolvimento esperado da cor resultante da adição de anticorpo anti-rato marcado com enzima e de cromogénio/substrato. Podem utilizar-se soros com uma diluição única de 1:5 (ensaio pontual - apêndice 1) ou, em alternativa, diluir-se sucessivamente a amostra para determinar o título final (titulação do soro - apêndice 2). São considerados positivos os valores de inibição superiores a 50 %.
Material e reagentes:
|
1. |
Placas de microtítulo ELISA adequadas. |
|
2. |
Antigénio: fornecido como um concentrado de extracto de células, preparado como seguidamente descrito e armazenado a –20 °C ou –70 °C. |
|
3. |
Tampão de bloqueio: tampão fosfato salino (PBS) com 0,3 % de soro de bovino adulto negativo para o VFCO, 0,1 % (v/v) Tween-20 (fornecido em xarope de monolaurato de polioxietilenossorbitano) em PBS. |
|
4. |
Anticorpo monoclonal: 3-17-A3 (fornecido na forma de sobrenadante da cultura de tecidos de hibridoma) dirigido contra o polipeptídeo VP7 específico do grupo, armazenado a –20 °C ou liofilizado, diluído a 1/100 com um tampão de bloqueio antes da utilização. |
|
5. |
Conjugado: globulina de coelho anti-rato (adsorvida e eluída), conjugada com peroxidase de rábano silvestre e mantida ao abrigo da luz a 4 °C. |
|
6. |
Cromogénio e substrato: ortofenileno diamina (cromogénio OPD) a uma concentração final de 0,4 mg/ml em água destilada e esterilizada. Peróxido de hidrogénio (30 % p/v de substrato) 0,05 % v/v adicionado imediatamente antes da utilização (5μl H2 O2 por 10 ml de OPD). (Manipular cuidadosamente o OPD - utilizar luvas de borracha - suspeita de efeito mutagénico). |
|
7. |
Ácido sulfúrico 1 molar: 26,6 ml de ácido, adicionados a 473,4 ml de água destilada. (Não esquecer - adicionar sempre o ácido à água, nunca a água ao ácido.) |
|
8. |
Agitador orbital. |
|
9. |
Leitor de placas ELISA (a prova pode ser lida visualmente). |
Formato de ensaio
Cc: controlo do conjugado (sem soro/sem anticorpo monoclonal); C++: controlo do soro fortemente positivo; C+: controlo do soro fracamente positivo; C-: controlo do soro negativo; Cm: controlo do anticorpo monoclonal (sem soro).
APÊNDICE 1
Formato da diluição única (1:5) (40 soros/placa)
|
|
Controlos |
Soros de ensaio |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
|
A |
Cc |
C- |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
B |
Cc |
C- |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
C |
C++ |
C++ |
|
|
|
|
|
|
|
|
|
|
|
D |
C++ |
C++ |
|
|
|
|
|
|
|
|
|
|
|
E |
C+ |
C+ |
|
|
|
|
|
|
|
|
|
|
|
F |
C+ |
C+ |
|
|
|
|
|
|
|
|
|
|
|
G |
Cm |
Cm |
|
|
|
|
|
|
|
|
|
40 |
|
H |
Cm |
Cm |
|
|
|
|
|
|
|
|
|
40 |
APÊNDICE 2
Formato da titulação do soro (10 soros/placa)
|
|
Controlos |
Soros de ensaio |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
|
A |
Cc |
C- |
1:5 |
|
|
|
|
|
|
|
|
1:5 |
|
B |
Cc |
C- |
1:10 |
|
|
|
|
|
|
|
|
1:10 |
|
C |
C++ |
C++ |
1:20 |
|
|
|
|
|
|
|
|
1:20 |
|
D |
C++ |
C++ |
1:40 |
|
|
|
|
|
|
|
|
1:40 |
|
E |
C+ |
C+ |
1:80 |
|
|
|
|
|
|
|
|
1:80 |
|
F |
C+ |
C+ |
1:160 |
|
|
|
|
|
|
|
|
1:160 |
|
G |
Cm |
Cm |
1:320 |
|
|
|
|
|
|
|
|
1:320 |
|
H |
Cm |
Cm |
1:640 |
|
|
|
|
|
|
|
|
1:640 |
Protocolo de ensaio:
|
Controlo do conjugado (Cc) |
: |
Os alvéolos 1A e 1B representam um controlo em branco que compreende o antigénio do VFCO e um conjugado. Pode ser utilizado para aferir o leitor ELISA. |
|
Controlo do AMC (Cm) |
: |
As colunas 1 e 2, linhas G e H, representam o controlo do AMC e contêm o antigénio do VFCO, o AMC e o conjugado. Estes alvéolos representam a coloração máxima. A média dos valores da densidade óptica deste controlo corresponde ao valor de inibição de 0 %. |
|
Controlo positivo (C++, C+) |
: |
Colunas 1 e 2, linhas C-D-E-F. Estes alvéolos contêm o antigénio do VFCO, antissoros forte e fracamente positivos, respectivamente, AMC e conjugado. |
|
Controlo negativo (C-) |
: |
Os alvéolos 2A e 2B constituem os controlos negativos, que contêm antigénio do VFCO, antissoro negativo para o VFCO, AMC e conjugado. |
|
Soros em análise |
: |
Para estudos serológicos em grande escala e controlo rápido, os soros podem ser ensaiados a uma diluição única de 1:5 (apêndice 1). Em alternativa, podem ser ensaiados 10 soros com uma gama de diluições de 1:5 a 1:640 (apêndice 2). Obter-se-ão, desta forma, informações relativas ao título do anticorpo nos soros de ensaio. |
Técnica:
|
1. |
Diluir o antigénio do VFCO à concentração pré-titulada em STF. Proceder à dissociação ultrassónica para dispersar os agregados do vírus (não dispondo do aparelho necessário, pipetar vigorosamente) e adicionar 50 µl a todos os alvéolos da placa ELISA. Bater ligeiramente nos bordos da placa para dispersar o antigénio. |
|
2. |
Incubar a 37 °C durante 60 minutos num agitador orbital. Lavar as placas passando-as três vezes por água e esvaziando os alvéolos com PBS não estéril e secar com um papel absorvente. |
|
3. |
Alvéolos de controlo: adicionar 100 μl de tampão de bloqueio aos alvéolos Cc. Adicionar 50 μl de soros de controlo positivo e negativo a uma diluição de 1:5 (10 µl soro +40 μl tampão de bloqueio) aos respectivos alvéolos C-, C+ e C++. Adicionar 50 μl de tampão de bloqueio aos alvéolos de controlo AMC. Método de titulação pontual: distribuir, em alvéolos repetidos das colunas 3 a 12, diluições a 1:5 de cada soro de ensaio em tampão de bloqueio (10 µl soro +40 µl tampão de bloqueio), ou Método de titulação do soro: distribuir, em oito alvéolos de cada uma das colunas 3 a 12, uma dupla série de diluições de cada amostra de ensaio (1:5 a 1:640) em tampão de bloqueio. |
|
4. |
Imediatamente após a adição dos soros de ensaio, diluir a 1:100 o AMC em tampão de bloqueio e adicionar 50 μl a todos os alvéolos da placa, excepto ao controlo em branco. |
|
5. |
Incubar a 37° C durante 60 minutos num agitador orbital. Lavar três vezes com PBS e secar com um papel absorvente. |
|
6. |
Diluir o concentrado de coelho anti-rato a 1/5 000 num tampão de bloqueio e adicionar 50 μl a todos os alvéolos da placa. |
|
7. |
Incubar a 37° C durante 60 minutos num agitador orbital. Lavar três vezes com PBS e secar com um papel absorvente. |
|
8. |
Descongelar o dicloridrato de o-fenilenodiamina (OPD) e imediatamente antes da utilização adicionar 5 µl de peróxido de hidrogénio a 30 % a cada 10 ml de OPD. Adicionar 50 μl a todos os alvéolos da placa. Aguardar que a cor se desenvolva durante aproximadamente 10 minutos e parar a reacção com ácido sulfúrico 1 molar (50 µl por alvéolo). A cor deve desenvolver-se nos alvéolos de controlo AMC e nos alvéolos que contêm soros sem anticorpos do VFCO. |
|
9. |
Examinar e registar as placas, visualmente ou com recurso a um leitor espectrofotométrico. |
Análise dos resultados:
Com recurso a um programa informático, obter os valores da densidade óptica (DO) e inibição percentual (IP) correspondentes aos soros de ensaio e aos soros de controlo, com base nos valores médios registados nos alvéolos de controlo do antigénio. Os valores DO e IP são utilizados para determinar se os resultados se situam num intervalo aceitável. Os limites superiores e inferiores de controlo para o controlo do AMC (antigénio mais AMC na ausência de soros de ensaio) situam-se entre 0,4 e 1,4 para a DO. As placas que não sejam conformes aos referidos critérios deverão ser rejeitadas.
Se não se dispuser de um programa informático, imprimir os valores DO por meio do leitor ELISA (impressora). Calcular o valor médio da DO para os alvéolos de controlo do antigénio, que é equivalente ao valor 100 %. Determinar o valor DO 50 % e calcular manualmente a positividade e negatividade de cada amostra.
Valor de inibição percentual (IP) = 100 – (DO de cada controlo / DO média do Cm) × 100.
Os alvéolos repetidos com soro de controlo negativo e os alvéolos repetidos do ensaio em branco devem apresentar valores IP compreendidos entre +25 % e –25 % e entre +95 % e + 105 %, respectivamente. Se tal não suceder, não deverá rejeitar-se a placa, havendo contudo que ter em conta a possibilidade de estar a desenvolver-se uma coloração de fundo. Os soros de controlo forte e fracamente positivos devem registar valores IP compreendidos entre +81 % e + 100 % e entre +51 % e +80 %, respectivamente.
O limiar de diagnóstico para os soros de ensaio é de 50 % (IP 50 % ou DO 50 %). As amostras que apresentem valores IP superiores a 50 % são consideradas negativas. As amostras que apresentem, nos alvéolos repetidos, valores IP superiores e inferiores ao limiar são consideradas duvidosas, podendo ser objecto de nova análise pelo método de ensaio pontual e/ou por titulação. Poderão também titular-se as amostras positivas, de forma a obter indicações quanto ao grau de positividade.
Leitura visual: as amostras positivas e negativas são facilmente visíveis a olho nu; as amostras fracamente positivas ou fortemente negativas podem ser mais difíceis de interpretar a olho nu.
Preparação do antigénio do VFCO para o método ELISA:
|
1. |
Lavar três vezes 40-60 roux de células BHK-21 confluentes com um meio Eagle isento de soro e infectar com o serótipo 1 do vírus da febre catarral ovina num meio Eagle isento de soro. |
|
2. |
Incubar a 37 °C e examinar diariamente o efeito citopático (ECP). |
|
3. |
Quando o ECP estiver completo em 90 % a 100 % da camada de células de cada roux, recolher o vírus por agitação destacando as células aderentes ao vidro. |
|
4. |
Centrifugar a 2 000 a 3 000 rpm para agregar as células. |
|
5. |
Deitar fora a fracção sobrenadante e colocar novamente as células em suspensão em aproximadamente 30 ml de PBS que contenha 1 % de Sarkosyl e 2 ml de fluoreto de fenilmetilsulfonil (lise). Isto pode provocar uma gelificação das células, podendo adicionar-se mais lise para reduzir esse efeito. (NB: o fluoreto de fenilmetilsulfonil é uma substância perigosa - manipular com muito cuidado.) |
|
6. |
Proceder à dissociação das células durante 60 segundos utilizando uma sonda ultrassónica a uma amplitude de 30 mícrons. |
|
7. |
Centrifugar a 10 000 rpm durante 10 minutos. |
|
8. |
Reservar a fracção sobrenadante a +4 °C e ressuspender o agregado de células remanescente em 10 a 20 ml de lise. |
|
9. |
Proceder à dissociação ultrassónica e clarificar, reservando a fracção sobrenadante em cada fase, num total de três vezes. |
|
10. |
Reunir as fracções sobrenadantes e centrifugar a 24 000 rpm (100,000 g) durante 120 minutos a uma temperatura de +4 °C sobre uma almofada de 5 ml de sacarose a 40 % (p/v em PBS) utilizando tubos de centrifugação Beckmann de 30 ml e um rotor SW 28. |
|
11. |
Eliminar a fracção sobrenadante, escorrer cuidadosamente os tubos e suspender novamente o agregado em PBS por dissociação ultrassónica. Reservar o antigénio em alíquotas a –20 °C. |
Titulação do antigénio do VFCO para o método ELISA:
A titulação do antigénio da febre catarral ovina para o método ELISA é feita pelo método indirecto ELISA. Titulação de uma dupla série de diluições do antigénio relativamente a uma diluição constante (1/100) de anticorpo monoclonal 3-17-A3. O protocolo é o seguinte:
|
1. |
Titular uma diluição 1:20 do antigénio do VFCO em PBS ao longo de uma placa de microtítulo numa dupla série de diluições (50 µl/alvéolo) utilizando uma pipeta de canais múltiplos. |
|
2. |
Incubar a 37 °C durante 1 hora, utilizando um agitador orbital. |
|
3. |
Lavar três vezes as placas com PBS. |
|
4. |
Adicionar 50 μl de anticorpo monoclonal 3-17-A3 (diluído a 1/100) a cada um dos alvéolos da placa de microtítulo. |
|
5. |
Incubar a 37 °C durante 1 hora, utilizando um agitador orbital. |
|
6. |
Lavar três vezes as placas com PBS. |
|
7. |
Adicionar 50 μl de globulina de coelho anti-rato conjugada com peroxidase de rábano silvestre, diluída numa concentração pré-titulada óptima, a cada alvéolo da placa de microtítulo. |
|
8. |
Incubar a 37 °C durante 1 hora, utilizando um agitador orbital. |
|
9. |
Adicionar substrato e cromogénio como indicado atrás. Parar a reacção após 10 minutos por meio da adição de ácido sulfúrico 1 molar (50 μl por alvéolo). |
No ensaio competitivo, o anticorpo monoclonal deve encontrar-se em excesso, devendo por essa razão ser escolhida uma diluição de antigénio que se encontre na curva de titulação (e não na zona de planalto) que resulte numa densidade óptica de aproximadamente 0,8 após 10 minutos.
Prova de imunodifusão em gel de ágar a executar de acordo com o protocolo seguinte:
Antigénio:
Preparar o antigénio precipitante num qualquer sistema de cultura de células compatível com a multiplicação rápida de uma estirpe de referência do vírus da febre catarral ovina. São recomendadas as células BHK ou Vero. O antigénio está presente no fluido sobrenadante no termo do crescimento do vírus, mas, para ser eficaz, a sua concentração deve ser 50 a 100 vezes superior. Esta concentração obtém-se através de qualquer método padrão de concentração de proteínas; o vírus do antigénio pode ser inactivado por meio da adição de beta-propiolactona 0,3 % (v/v).
Soro de controlo positivo conhecido:
Utilizando o soro internacional de referência e o antigénio, é produzido um soro-tipo nacional, padronizado para obtenção de uma proporção óptima relativamente ao soro internacional de referência, liofilizado e utilizado como soro de controlo conhecido em cada ensaio.
Soro de ensaio
|
Técnica |
: |
Deitar agarose a 1 % preparada num tampão de borato ou de barbitol de sódio, com um pH entre 8,5 e 9,0 numa placa de Petri a uma profundidade mínima de 3,0 mm. Criar no ágar uma estrutura de sete alvéolos isentos de humidade, cada um com 5,0 mm de diâmetro. A estrutura consiste num alvéolo central e seis alvéolos dispostos num círculo com um raio de 3 cm. Preencher o alvéolo central com o antigénio padrão. Os alvéolos circundantes 2, 4 e 6 são preenchidos com soro positivo conhecido e os alvéolos 1, 3 e 5 com o soro de ensaio. O sistema é colocado em incubação durante um período que pode ir até 72 horas à temperatura ambiente numa câmara húmida fechada. |
|
Interpretação |
: |
Um soro de ensaio é positivo caso resulte na formação de uma linha de precipitina específica com o antigénio e numa linha de identidade total com o soro de controlo. Um soro de ensaio é negativo caso não forme uma linha específica com o antigénio e não deforme a linha do soro de controlo. As placas de Petri devem ser examinadas contra um fundo escuro e com uma iluminação indirecta. |
Doença hemorrágica epizoótica (DHE)
Prova de imunodifusão em gel de ágar a executar de acordo com o protocolo seguinte:
Antigénio:
Preparar o antigénio precipitante num qualquer sistema de cultura de células compatível com a multiplicação rápida do(s) serótipo(s) adequado(s) do vírus da doença hemorrágica epizoótica. São recomendadas as células BHK ou Vero. O antigénio está presente no fluido sobrenadante no termo do crescimento do vírus, mas, para ser eficaz, a sua concentração deve ser 50 a 100 vezes superior. Esta concentração obtém-se através de qualquer método padrão de concentração de proteínas; o vírus do antigénio pode ser inactivado por meio da adição de beta-propiolactona 0,3 % (v/v).
Soro de controlo positivo conhecido:
Utilizando o soro internacional de referência e o antigénio, é produzido um soro-tipo nacional, padronizado para obtenção de uma proporção óptima relativamente ao soro internacional de referência, liofilizado e utilizado como soro de controlo conhecido em cada ensaio.
Soro de ensaio
|
Técnica |
: |
Deitar agarose a 1 % preparada num tampão de borato ou de barbitol de sódio, com um pH entre 8,5 e 9,0 numa placa de Petri a uma profundidade mínima de 3,0 mm. Criar no ágar uma estrutura de sete alvéolos isentos de humidade, cada um com 5,0 mm de diâmetro. A estrutura consiste num alvéolo central e seis alvéolos dispostos num círculo com um raio de 3 cm. Preencher o alvéolo central com o antigénio padrão. Os alvéolos circundantes 2, 4 e 6 são preenchidos com soro positivo conhecido e os alvéolos 1, 3 e 5 com o soro de ensaio. O sistema é colocado em incubação durante um período que pode ir até 72 horas à temperatura ambiente numa câmara húmida fechada. |
|
Interpretação |
: |
Um soro de ensaio é positivo caso resulte na formação de uma linha de precipitina específica com o antigénio e numa linha de identidade total com o soro de controlo. Um soro de ensaio é negativo caso não forme uma linha específica com o antigénio e não deforme a linha do soro de controlo. As placas de Petri devem ser examinadas contra um fundo escuro e com uma iluminação indirecta. |
Rinotraqueíte infecciosa dos bovinos (RIB)/vulvovaginite pustulosa infecciosa (VPI)
(A) Prova de seroneutralização a executar de acordo com o protocolo seguinte:
|
Soro |
: |
Todos os soros são inactivados pelo calor, a 56 °C durante 30 minutos antes da utilização. |
|
Técnica |
: |
A prova da seroneutralização com quantidade de vírus constante e diluição variável em placas de microtítulo utiliza células MDBK ou outras células susceptíveis. As estirpes Colorado, Oxford ou qualquer outra estirpe de referência do vírus devem ser utilizadas a 100 TCID50 por 0,025 ml; misturar as amostras de soro inactivado e não diluído com igual volume (0,025 ml) de suspensão do vírus. Incubar as misturas vírus/soro durante 24 horas a 37 °C nas placas de microtítulo, antes de adicionar as células MDBK. Utilizar as células a uma concentração tal que leve à formação de uma camada simples completa após 24 horas. |
|
Controlos |
: |
i) Ensaio de infecciosidade do vírus; ii) Controlos de toxicidade do soro; iii) Controlos de cultura de células não inoculadas; iv) Antissoros de referência. |
|
Interpretação |
: |
Registar os resultados da prova de neutralização e o título do vírus utilizado na prova após três a seis dias de incubação a 37 °C. Os títulos do soro consideram-se negativos se não houver neutralização a uma diluição de 1/2 (soro não diluído). |
(B) Qualquer outro teste reconhecido no âmbito da Decisão 2004/558/CE (30).
Febre aftosa (FA)
(A) Colheita de amostras do esófago/faringe e prova a executar de acordo com o protocolo seguinte:
|
Reagentes |
: |
Antes de colher as amostras, preparar o meio para transporte. Distribuir volumes de 2 ml por tantos recipientes quantos os animais testados. Os recipientes devem ser resistentes à congelação em CO2 sólido ou azoto líquido. As amostras são colhidas com uma sonda esofágica, especialmente concebida para a colheita do escarro. Para colher uma amostra, passar o copo da sonda esofágica através da boca, sobre a língua, até à parte superior do esófago. Por meio de movimentos orientados lateral e superiormente, tentar raspar o epitélio superficial da parte superior do esófago e da faringe. Retirar então a sonda, se possível após o animal ter engolido. O copo deve estar cheio e conter uma mistura de muco, saliva, fluido esofágico e detritos celulares. Deve assegurar-se que cada espécime contenha algum material celular visível. O manuseamento muito brusco, que provoque sangramento, deve ser evitado. As amostras provenientes de alguns animais podem estar fortemente contaminadas com o conteúdo do rúmen. Essas amostras devem ser rejeitadas e a boca do animal lavada com água ou, de preferência, soro fisiológico antes de a colheita ser repetida. |
|
Tratamento das amostras |
: |
Examinar cada uma das amostras colhidas no copo da sonda esofágica relativamente à qualidade e adicionar 2 ml a igual volume de meio para transporte num recipiente que possa resistir à congelação. Fechar firmemente, selar, desinfectar e rotular esses recipientes. Manter as amostras a baixa temperatura (+4 °C) e examiná-las após três a quatro horas ou colocá-las sobre gelo seco (–69 °C) ou azoto líquido, mantendo-as congeladas até serem examinadas. Após utilização em cada animal, desinfectar e lavar a sonda por três vezes, sempre em água limpa. |
|
Pesquisa do vírus da febre aftosa |
: |
Inocular as amostras em culturas de células primárias de tiróide de bovino, utilizando pelo menos três tubos por amostra. Embora possam ser utilizadas outras células susceptíveis, como por exemplo células primárias de rim de bovino ou suíno, é necessário não esquecer que, para algumas estirpes do vírus da FA, essas células são menos sensíveis. Colocar os tubos em incubação num agitador do tipo rotativo, a 37 °C, e examinar diariamente, durante 48 horas, para detecção do efeito citopático (ECP). Caso o efeito não seja detectado, inocular casualmente as culturas em novas culturas e reexaminar durante 48 horas. A especificidade de qualquer ECP tem que ser confirmada. |
Meios para transporte recomendados:
|
1. |
Tampão fosfato 0,08 M com pH 7,2 que contenha albumina de soro de bovino a 0,01 %, vermelho de fenol a 0,002 % e antibióticos. |
|
2. |
Meio de cultura de tecidos (por exemplo, MEM Eagle) que contenha solução tampão HEPES 0,04 M, albumina de soro de bovino a 0,01 % e antibióticos, e que tenha pH 7,2. |
|
3. |
Adicionar antibióticos (por ml de solução final) ao meio para transporte, por exemplo: penicilina - 1 000 UI; sulfato de neomicina - 100 UI; sulfato de polimixina B - 50 UI; micostatina - 100 UI. |
(B) Prova de neutralização do vírus a executar de acordo com o protocolo seguinte:
|
Reagentes |
: |
Preparar o antigénio de base do vírus da febre aftosa em culturas de células ou em línguas dos animais e armazená-lo a –70 °C, ou menos, ou a –20 °C após adição de glicerol a 50 %. Este antigénio constitui o antigénio de base. O vírus da febre aftosa é estável nestas condições e os títulos sofrem pouca variação durante meses. |
|
Técnica |
: |
A prova é realizada em placas de microtítulo de fundo plano, com células susceptíveis como as IB-RS-2, BHK-21 ou células de rim de vitelo. Diluir os soros de ensaio a 1/4 num meio de cultura de células isento de soro, adicionando neomicina 100 UI/ml ou outros antibióticos adequados. Inactivar os soros a 56 °C durante 30 minutos e utilizar quantidades de 0,05 ml para preparar uma dupla série de diluições em placas de microtítulo, utilizando ansas de diluição de 0,05 ml. Adicionar então a cada alvéolo vírus pré-titulado diluído também em meio de cultura isento de soro e com 100 TCID50/0,05 ml. Incubar a 37 °C durante 1 hora de forma a permitir que a neutralização se dê e, em seguida, adicionar a cada alvéolo 0,05 ml de células em suspensão com 0,5 a 1,0 × 106 células por ml num meio de cultura de células com soro isento de anticorpos da febre aftosa. Selar em seguida as placas. Incubar as placas a 37 °C. As camadas simples tornam-se normalmente confluentes em 24 horas. O efeito citopático está habitualmente suficientemente avançado em 48 horas para permitir uma leitura microscópica da prova. Pode então ser feita uma leitura microscópica final ou uma fixação e coloração das placas para uma leitura macroscópica utilizando, por exemplo, uma solução de soro fisiológico e formol a 10 % e azul de metileno a 0,05 %. |
|
Controlos |
: |
Em cada prova os controlos incluem antissoro homólogo de título conhecido, um controlo de células, um controlo da toxicidade do soro, um controlo do meio e uma titulação do vírus a partir da qual é calculada a quantidade de vírus presente na prova. |
|
Interpretação |
: |
Consideram-se infectados os alvéolos onde se verificou o ECP e os títulos de neutralização são expressos como o recíproco da diluição final de soro presente nas misturas soro/vírus na fase terminal de 50 % calculada pelo método Spearman-Karber. (Karber, G., 1931, Archiv fuer Experimentelle Pathologie und Pharmakologie, 162, 480). Os ensaios são considerados válidos quando a quantidade de vírus utilizada por alvéolo no ensaio se situa entre 101,5 e 102,5 TCID50 e quando o título do soro de referência não exceder o dobro do título esperado, estimado a partir do valor da moda de titulações prévias. Se os controlos estiverem fora destes limites, o ensaios têm que ser repetidos. Um título, na fase terminal, de 1/11 ou menos é considerado negativo. |
(C) Detecção e quantificação do anticorpo pelo método ELISA a executar de acordo com o protocolo seguinte:
|
Reagentes |
: |
Antissoros de coelho para o antigénio 146S de 7 tipos de vírus da febre aftosa (VFA) a uma concentração pré-determinada óptima em solução tampão de carbonato/bicarbonato, com pH 9,6. Os antigénios são preparados a partir de estirpes seleccionadas de vírus cultivadas em camadas simples de células BHK-21. Os sobrenadantes não purificados são utilizados e pré-titulados de acordo com o protocolo mas sem soro, de forma a obter uma diluição tal que, após a adição de igual volume de PBST (tampão fosfato salino com 0,05 % de Tween-20 e o indicador vermelho de fenol), tenha uma densidade óptica entre 1,2 e 1,5. Podem ser utilizados vírus inactivados. O PBST é utilizado como diluente. Os antissoros de porco-da-índia são preparados através da inoculação de porcos-da-índia com antigénio 146S de cada serótipo. Prepara-se uma concentração pré-determinada óptima em PBST que contenha 10 % de soro normal de bovino e 5 % de soro normal de coelho. Utiliza-se imunoglobulina de coelho anti-porco-da-índia conjugada com peroxidase de rábano silvestre com uma concentração óptima pré-determinada em PBST que contenha 10 % de soro normal de bovino e 5 % de soro normal de coelho. Os soros de ensaio são diluídos em PBST. |
Técnica:
|
1. |
Revestir as placas ELISA com 50 μl de soros antivíricos de coelho e colocá-las durante uma noite numa câmara húmida, à temperatura ambiente. |
|
2. |
Preparar 50 microlitros em duplicado, de uma dupla série de diluições de cada soro de ensaio, começando com 1/4, em placas multi-alvéolos com base em forma de U (placas portadoras). Adicionar 50 microlitros de uma dose constante de antigénio a cada alvéolo e deixar as misturas em repouso durante uma noite a 4 °C. A adição do antigénio reduz a diluição inicial do soro para 1/8. |
|
3. |
Lavar cinco vezes as placas ELISA com PBST. |
|
4. |
Transferir então 50 microlitros das misturas soro/antigénio das placas portadoras para as placas ELISA revestidas com soro de coelho e incubar a 37 °C durante uma hora num agitador do tipo rotativo. |
|
5. |
Depois da lavagem, adicionar a cada alvéolo 50 µl de antissoro de porco-da-índia ao antigénio utilizado no ponto 4. Incubar as placas a 37 °C durante uma hora num agitador do tipo rotativo. |
|
6. |
Lavar as placas e adicionar a cada alvéolo 50 µl de imunoglobulina de coelho anti-porco-da-índia conjugada com peroxidase de rábano silvestre. Incubar as placas durante 1 hora a 37 °C num agitador do tipo rotativo. |
|
7. |
Lavar as placas e adicionar a cada alvéolo 50 µl de ortofenileno diamina com 0,05 % de H2O2 (30 %) p/v. |
|
8. |
Parar a reacção após 15 minutos com H2SO4 1,25 M. |
A leitura das placas é feita espectrofotometricamente a 492 nm num leitor ELISA ligado a um microcomputador.
|
Controlos |
: |
Por cada antigénio utilizado existem 40 alvéolos que não contêm soro, mas que contêm antigénio diluído em PBST. Uma dupla série, em duplicado, de diluições de antissoro de bovino de referência homólogo. Uma dupla série, em duplicado, de diluições de soro negativo de bovino. |
|
Interpretação |
: |
Os títulos de anticorpos são expressos em termos da diluição final do soro dos ensaios que tenham 50 % do valor da DO (densidade óptica) média registada nos alvéolos de controlo do vírus onde não existe soro. Consideram-se positivos os títulos superiores a 1/40. |
|
Referências |
: |
Hamblin C., Barnett ITR e Hedger RS (1986) «A new enzymelinked immunosorbent assay (ELISA) for the detection of antibodies against foot-and-mouth disease virus. I. Development and method of ELISA» Journal of Immunological Methods, 93, 115 a 121.11. |
Doença de Aujeszky (DAJ)
(A) Prova de seroneutralização a executar de acordo com o protocolo seguinte:
|
Soro |
: |
Todos os soros são inactivados pelo calor, a 56 °C durante 30 minutos antes da utilização. |
|
Técnica |
: |
A prova da seroneutralização com quantidade de vírus constante e diluição variável em placas de microtítulo utiliza células Vero ou outro sistema de células sensíveis. O vírus da doença de Aujeszky deve ser utilizado a 100 TCID50 por 0,025 ml; misturar as amostras de soro inactivado e não diluído com igual volume (0,025 ml) de suspensão do vírus. Incubar as misturas vírus/soro durante 2 horas a 37 °C nas placas de microtítulo, antes de adicionar as células adequadas. Utilizar as células a uma concentração tal que leve à formação de uma camada simples completa após 24 horas. |
|
Controlos |
: |
i) Ensaio de infecciosidade do vírus; ii) Controlos de toxicidade do soro; iii) Controlos de cultura de células não inoculadas; iv) Antissoros de referência. |
|
Interpretação |
: |
Registar os resultados da prova de neutralização e o título do vírus utilizado na prova após três a sete dias de incubação a 37 °C. Consideram-se negativos títulos do soro inferiores a 1/2 (soro não diluído). |
(B) Qualquer outro teste reconhecido no âmbito da Decisão 2008/185/CE (31).
Gastrenterite transmissível (GET)
Prova de seroneutralização a executar de acordo com o protocolo seguinte:
|
Soro |
: |
Todos os soros são inactivados pelo calor, a 56 °C durante 30 minutos antes da utilização. |
|
Técnica |
: |
A prova da seroneutralização com quantidade de vírus constante e diluição variável em placas de microtítulo utiliza células A72 (tumor de cão) ou outro sistema de células sensíveis. O vírus da gastrenterite transmissível deve ser utilizado a 100 TCID50 por 0,025 ml; misturar as amostras de soro inactivado e não diluído com igual volume (0,025 ml) de suspensão do vírus. Incubar as misturas vírus/soro durante 30 a 60 minutos a 37 °C nas placas de microtítulo, antes de adicionar as células adequadas. Utilizar as células a uma concentração tal que leve à formação de uma camada simples completa após 24 horas. Cada célula recebe 0,1 ml de suspensão de células. |
|
Controlos |
: |
i) Ensaio de infecciosidade do vírus; ii) Controlos de toxicidade do soro; iii) Controlos de cultura de células não inoculadas; iv) Antissoros de referência. |
|
Interpretação |
: |
Registar os resultados da prova de neutralização e o título do vírus utilizado na prova após três a cinco dias de incubação a 37 °C. Consideram-se negativos títulos do soro inferiores a 1/2 (diluição final). Se as amostras de soro não diluídas forem tóxicas para as culturas de tecidos, estes soros podem ser diluídos a 1/2 antes de serem utilizados na prova. Isto é equivalente a 1/4 da diluição final do soro. Os títulos do soro inferiores a 1/4 (diluição final) são considerados negativos nestes casos. |
Doença vesiculosa dos suínos (DVS)
Testes de detecção da doença vesiculosa dos suínos (DVS): a executar de acordo com a Decisão 2000/428/CE (32).
Peste suína clássica (PSC)
Testes de detecção da peste suína clássica (PSC): a executar de acordo com a Decisão 2002/106/CE (33).
Os testes de detecção da peste suína clássica devem respeitar as directrizes do capítulo pertinente do Manual de Testes de Diagnóstico e Vacinas para Animais Terrestres da OIE.
A avaliação da sensibilidade e especificidade da prova serológica de detecção da PSC devem ser determinadas num laboratório nacional que disponha de um sistema de garantia da qualidade. Os testes utilizados devem poder reconhecer uma gama de soros de referência fraca e fortemente positivos e permitir a detecção dos anticorpos numa fase inicial e na convalescença.
PARTE 7
Condições sanitárias de importação e quarentena aplicáveis aos animais importados para São Pedro e Miquelon num período inferior a seis meses antes da sua introdução na União
(referidas no artigo 6.o)
Espécies animais abrangidas
|
Taxon |
||
|
ORDEM |
FAMÍLIA |
GÉNERO E ESPÉCIE |
|
Artiodactyla |
Camelidae |
Camelus spp., Lama spp., Vicugna spp. |
CAPÍTULO 1
Permanência e quarentena
1. Os animais importados para São Pedro e Miquelon devem permanecer numa estação de quarentena autorizada, durante um período mínimo de 60 dias antes de serem expedidos para introdução na União. Este período pode ser aumentado devido a requisitos de ensaio para espécies individuais. Além disso, os animais devem cumprir os seguintes requisitos:
|
a) |
Podem entrar na estação de quarentena remessas separadas. No entanto, à entrada da estação de quarentena, todos os animais da mesma espécie que se encontrem na instalação de quarentena devem ser considerados como um único grupo e referidos como tal. O período de quarentena deve começar para o grupo inteiro no momento em que o último animal entra na instalação de quarentena. |
|
b) |
Dentro da estação de quarentena, cada grupo específico de animais deve ser mantido em isolamento, sem contacto directo ou indirecto com quaisquer outros animais, incluindo animais de outras remessas que possam estar presentes. Cada remessa deve ser mantida na estação de quarentena aprovado e protegida de insectos-vectores. |
|
c) |
Se, durante o período de quarentena, o isolamento de um grupo de animais não for mantido e houver contacto com outros animais, o período de quarentena deve recomeçar com a mesma duração do inicialmente prescrito à entrada na estação de quarentena. |
|
d) |
Os animais a introduzir na União que passam pela estação de quarentena devem ser carregados e expedidos directamente para a União:
|
2. Os locais de quarentena devem respeitar, pelo menos, as normas mínimas estabelecidas no anexo B da Directiva 91/496/CEE (34), bem como as seguintes condições:
|
a) |
Devem estar sob a supervisão de um veterinário oficial; |
|
b) |
Devem situar-se no centro de uma área de, pelo menos, 20 km de diâmetro na qual, de acordo com verificações oficiais, pelo menos 30 dias antes da sua utilização enquanto estação de quarentena, não tenha ocorrido qualquer caso de febre aftosa; |
|
c) |
Devem, antes de ser utilizados como estação de quarentena, ser limpos e desinfectados com um desinfectante oficialmente aprovado em São Pedro e Miquelon como eficaz no controlo das doenças referidas no capítulo 2; |
|
d) |
Devem, atendendo à sua capacidade, dispor de:
|
|
e) |
Devem dispor, para o seu funcionamento, de veterinários suficientes para realizar todas as tarefas; |
|
f) |
Só devem admitir animais que estejam individualmente identificados, a fim de garantir a rastreabilidade. Para esse efeito, aquando da admissão de animais, o proprietário ou o responsável pela estação de quarentena deve certificar-se de que os animais se encontram devidamente identificados e acompanhados dos certificados sanitários correspondentes à espécie e à categoria em causa. Além disso, o proprietário ou o responsável pela estação de quarentena deve registar, num registo ou numa base de dados, e conservar durante pelo menos três anos, o nome do proprietário, a origem dos animais que constituem a remessa, as datas de entrada e saída desses animais, o seu número de identificação e o seu local de destino; |
|
g) |
A autoridade competente deve determinar o processo de supervisão oficial da estação de quarentena e deve assegurar a realização dessa supervisão; esta supervisão incluirá inspecções regulares, para verificar se as condições de aprovação continuam a ser observadas. Em caso de incumprimento e suspensão, a aprovação só pode ser restabelecida quando a autoridade competente considerar que os locais de quarentena satisfazem integralmente todas as condições referidas na alíneas a) a g). |
CAPÍTULO 2
Testes sanitários
1. REQUISITOS GERAIS
Devem efectuar-se os seguintes testes com amostras de sangue dos animais colhidas, salvo indicação em contrário, decorridos pelo menos 21 dias após o início do período de isolamento.
Os testes laboratoriais devem ser realizados num laboratório aprovado na União, devendo todos os testes laboratoriais e respectivos resultados, as vacinações e os tratamentos ser anexados ao certificado sanitário.
De modo a reduzir ao mínimo as intervenções nos animais, a colheita de amostras, os testes e quaisquer vacinações devem ser agrupados o mais possível, embora respeitando os intervalos mínimos requeridos pelos protocolos dos testes indicados na parte 2 do presente capítulo.
2. REQUISITOS ESPECÍFICOS
2.1 CAMELIDAE
2.1.1 Tuberculose
|
a) |
Teste a utilizar: teste intradérmico de reacção comparativo utilizando derivados proteicos purificados (PPD) bovinos e aviários conformes com as normas para o fabrico de tuberculinas bovinas e aviárias, como descrito no ponto 2.1.2 do anexo B da Directiva 64/432/CEE. O teste tem de ser executado na zona atrás do ombro (região axilar), seguindo a técnica descrita no ponto 2.2.4 do anexo B da Directiva 64/432/CEE. |
|
b) |
Calendário: os animais têm de ser testados no prazo de dois dias após a sua chegada à estação de quarentena e 42 dias depois do primeiro teste. |
|
c) |
Interpretação dos testes: A reacção deve ser considerada:
|
|
d) |
Opções de acção depois dos testes: Se um animal apresentar um resultado positivo à reacção intradérmica aos PPD bovinos, o animal será excluído do grupo e os outros animais devem ser submetidos a novo teste, pelo menos 42 dias depois da realização do primeiro teste positivo, devendo este teste ser considerado como o primeiro teste descrito em b). Se mais de um animal do grupo apresentar um resultado positivo, o grupo na sua totalidade será rejeitado para efeitos de exportação para a União. Se um ou mais animais do mesmo grupo apresentarem uma reacção inconclusiva, todo o grupo será submetido a novo teste pelo menos 42 dias depois da realização do primeiro teste, devendo este teste ser considerado como o primeiro teste descrito em b). |
2.1.2 Brucelose
|
a) |
Teste a utilizar:
|
|
b) |
Calendário: os animais têm de ser testados no prazo de dois dias após a sua chegada à estação de quarentena e 42 dias depois do primeiro teste. |
|
c) |
Interpretação dos testes: Uma reacção positiva aos testes será a definida no anexo C da Directiva 64/432/CEE. |
|
d) |
Opções de acção depois dos testes: Os animais que apresentarem um resultado positivo a um dos testes serão excluídos do grupo e os outros animais devem ser submetidos a novo teste, pelo menos 42 dias depois da realização do primeiro teste positivo, devendo este teste ser considerado como o primeiro teste descrito em b). Apenas os animais que apresentarem resultados negativos a dois testes consecutivos realizados como descrito em b) serão autorizados para introdução na União. |
2.1.3 Febre catarral ovina e doença hemorrágica epizoótica (DHE)
|
a) |
Teste a utilizar: ensaio de imunodifusão em ágar-gel (AGID), tal como descrito na parte 6 do anexo I do Regulamento (UE) n.o 206/2010. Em caso de reacção positiva, os animais devem ser submetidos a uma prova ELISA competitiva, tal como descrita na parte 6 do anexo I do Regulamento (UE) n.o 206/2010 para fazer uma distinção entre as duas doenças. |
|
b) |
Calendário: Os animais têm de ser testados com resultados negativos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 21 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes:
|
2.1.4 Febre aftosa (FA)
|
a) |
Teste a utilizar: testes de diagnóstico (com a sonda esofágica ou serologia) utilizando as técnicas ELISA e NV (neutralização do vírus), segundo os protocolos descritos na parte 6 do anexo I do Regulamento (UE) n.o 206/2010. |
|
b) |
Calendário: os animais devem ser testados com resultados negativos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar um resultado positivo ao vírus da febre aftosa, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. Nota: qualquer detecção de anticorpos a proteínas estruturais ou não estruturais do vírus da febre aftosa será considerada como resultado de uma infecção prévia com a febre aftosa independentemente do estatuto de vacinação. |
2.1.5 Peste bovina
|
a) |
Teste a utilizar: prova ELISA competitiva, como descrita no Manual de Testes de Diagnóstico e Vacinas para Animais Terrestres da OIE, última versão, é o teste previsto para o comércio internacional e é o teste de opção. Podem igualmente utilizar-se a prova de seroneutralização ou outros testes reconhecidos em conformidade com os protocolos descritos nas secções pertinentes do manual da OIE. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar um resultado positivo ao vírus da peste bovina, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. |
2.1.6 Estomatite vesiculosa
|
a) |
Teste a utilizar: prova ELISA, uma prova de neutralização do vírus ou outro teste reconhecido em conformidade com os protocolos descritos nas secções pertinentes do manual da OIE. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar um resultado positivo ao vírus da estomatite vesiculosa, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. |
2.1.7 Febre do vale do Rift
|
a) |
Teste a utilizar: prova ELISA, uma prova de neutralização do vírus ou outro teste reconhecido em conformidade com os protocolos descritos nas secções pertinentes do manual da OIE. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar indícios de exposição ao agente da febre do vale do Rift, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. |
2.1.8 Dermatite nodular contagiosa
|
a) |
Teste a utilizar: serologia, utilizando a prova ELISA, uma prova de neutralização do vírus ou outro teste reconhecido em conformidade com os protocolos descritos nas secções pertinentes do manual da OIE. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar indícios de exposição à dermatite nodular contagiosa, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. |
2.1.9 Vírus da febre hemorrágica da Crimeia/Congo
|
a) |
Teste a utilizar: prova ELISA, prova de neutralização do vírus, teste de imunofluorescência ou outro teste reconhecido. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar indícios de exposição ao vírus da febre hemorrágica da Crimeia/Congo, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. |
2.1.10 Surra (Trypanosoma evansi (T. evansi))
|
a) |
Teste a utilizar: o agente parasitário pode ser identificado em amostras de sangue concentrado, em conformidade com os protocolos descritos nas secções pertinentes do manual da OIE. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se se detectar T. evansi em qualquer animal da remessa, esse animal será considerado não elegível para efeitos de introdução na União. Os restantes elementos do grupo devem ser submetidos a um tratamento antiparasitário interno e externo, utilizando os agentes eficazes contra T. evansi. |
2.1.11 Febre catarral maligna
|
a) |
Teste a utilizar: detecção do ADN viral, com base na identificação por imunofluorescência ou imunocitoquímica, utilizando os protocolos descritos nas secções pertinentes do manual da OIE. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: se qualquer animal apresentar indícios de exposição à febre catarral maligna, todos os animais presentes na estação de quarentena são considerados não elegíveis para efeitos de introdução na União. |
2.1.12 Raiva
Vacinação: a vacinação contra a raiva pode ser realizada quando solicitada pelo Estado-Membro de destino, devendo ser colhida uma amostra de sangue do animal e realizada uma prova de seroneutralização para pesquisa de anticorpos.
2.1.13 Leucose bovina enzoótica (apenas no caso de os animais se destinarem a um Estado-Membro ou região oficialmente indemnes de leucose bovina enzoótica, tal como referido no artigo 2.o, n.o 2, alínea k), da Directiva 64/432/CEE).
|
a) |
Teste a utilizar: AGID ou prova ELISA de bloqueio, em conformidade com os protocolos descritos no manual da OIE, última versão. |
|
b) |
Calendário: os animais devem ser submetidos a dois testes: o primeiro, no prazo de dois dias após a data da sua chegada à estação de quarentena e, o segundo, 42 dias, pelo menos, depois da data do primeiro teste. |
|
c) |
Opções de acção depois dos testes: os animais que apresentarem um resultado positivo ao teste descrito na alínea a) serão excluídos do grupo de animais na instalação de quarentena e os outros animais devem ser submetidos a novo teste, pelo menos 21 dias depois da realização do primeiro teste positivo, devendo este teste ser considerado como o primeiro teste descrito na alínea b). Apenas os animais que apresentarem resultados negativos a dois testes consecutivos realizados como descrito na alínea b) serão considerados como elegíveis para efeitos de introdução na União. |