EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32012D0726
2012/726/EU: Commission Implementing Decision of 22 November 2012 authorising the placing on the market of dihydrocapsiate as a novel food ingredient under Regulation (EC) No 258/97 of the European Parliament and of the Council (notified under document C(2012) 8391)
2012/726/ЕС: Решение за изпълнение на Комисията от 22 ноември 2012 година за разрешаване на пускането на пазара на дихидрокапсиат като нова хранителна съставка съгласно Регламент (ЕО) № 258/97 на Европейския парламент и на Съвета (нотифицирано под номер C(2012) 8391)
2012/726/ЕС: Решение за изпълнение на Комисията от 22 ноември 2012 година за разрешаване на пускането на пазара на дихидрокапсиат като нова хранителна съставка съгласно Регламент (ЕО) № 258/97 на Европейския парламент и на Съвета (нотифицирано под номер C(2012) 8391)
OB L 327, 27.11.2012, p. 49–51
(BG, ES, CS, DA, DE, ET, EL, EN, FR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
 In force
In force
|
27.11.2012 |
BG |
Официален вестник на Европейския съюз |
L 327/49 |
РЕШЕНИЕ ЗА ИЗПЪЛНЕНИЕ НА КОМИСИЯТА
от 22 ноември 2012 година
за разрешаване на пускането на пазара на дихидрокапсиат като нова хранителна съставка съгласно Регламент (ЕО) № 258/97 на Европейския парламент и на Съвета
(нотифицирано под номер C(2012) 8391)
(само текстът на английски език е автентичен)
(2012/726/ЕС)
ЕВРОПЕЙСКАТА КОМИСИЯ,
като взе предвид Договора за функционирането на Европейския съюз,
като взе предвид Регламент (ЕО) № 258/97 на Европейския парламент и на Съвета от 27 януари 1997 г. относно нови храни и нови хранителни съставки (1), и по-специално член 7 от него,
като има предвид, че:
|
(1) |
На 6 август 2010 г. дружеството Ajinomoto Co. Inc., Япония, отправи искане до компетентните органи на Обединеното кралство за пускане на пазара на дихидрокапсиат като нова хранителна съставка. |
|
(2) |
На 10 март 2011 г. компетентният орган на Обединеното кралство за оценка на храните представи доклада си за първоначална оценка. В доклада се прави заключението, че дихидрокапсиатът няма да представлява риск за здравето на потребителите. |
|
(3) |
На 13 април 2011 г. Комисията изпрати доклада за първоначална оценка до всички държави членки. |
|
(4) |
В 60-дневния срок, установен в член 6, параграф 4 от Регламент (ЕО) № 258/97, бяха повдигнати обосновани възражения в съответствие със същата разпоредба. |
|
(5) |
Поради това на 9 ноември 2011 г. бе потърсено становището на Европейския орган за безопасност на храните (ЕОБХ). |
|
(6) |
На 28 юни 2012 г. в своето „Научно становище относно дихидрокапсиат“ (2) ЕОБХ стигна до заключението, че дихидрокапсиатът е безопасен при предложените видове употреба и нива на употреба. |
|
(7) |
Дихидрокапсиатът отговаря на критериите, определени в член 3, параграф 1 от Регламент (ЕО) № 258/97. |
|
(8) |
Мерките, предвидени в настоящото решение, са в съответствие със становището на Постоянния комитет по хранителната верига и здравето на животните, |
ПРИЕ НАСТОЯЩОТО РЕШЕНИЕ:
Член 1
Дихидрокапсиат съгласно спецификациите в приложение I може да бъде пуснат на пазара като нова хранителна съставка за посочените видове употреба и при максималните нива, посочени в приложение II, без да се засягат разпоредбите на Регламент (ЕО) № 1925/2006 на Европейския парламент и на Съвета (3) и директиви 2009/39/ЕО (4) и 2009/54/ЕО (5) на Европейския парламент и на Съвета.
Член 2
Означението на разрешения с настоящото решение дихидрокапсиат върху етикета на храните, в чийто състав е вложен, е „дихидрокапсиат“.
Член 3
Адресат на настоящото решение е дружеството Ajinomoto Co. Inc., 15-1, Kyobashi, Chuo-ku, 1-choume, 104-8315, Токио, Япония.
Съставено в Брюксел на 22 ноември 2012 година.
За Комисията
Maroš ŠEFČOVIČ
Заместник-председател
(1) ОВ L 43, 14.2.1997 г., стр. 1.
(2) Бюлетин на ЕОБХ (EFSA Journal), 2012 г.; 10(7):2812.
(3) ОВ L 404, 30.12.2006 г., стр. 26.
(4) ОВ L 124, 20.5.2009 г., стр. 21.
(5) ОВ L 164, 26.6.2009 г., стр. 45.
ПРИЛОЖЕНИЕ I
СПЕЦИФИКАЦИИ НА ДИХИДРОКАПСИАТ
Определение
Дихидрокапсиатът се синтезира чрез естерификация на ванилилов алкохол и 8-метилнонанова киселина с катализатор ензим. След естерификацията с помощта на n-хексан се извлича дихидрокапсиат.
Ензимът „Lipozyme 435“ е одобрен от Датската служба за ветеринарен и хранителен контрол.
Описание: вискозна безцветна до жълтеникава течност
Химична формула: C18H28O4
Структурна формула:
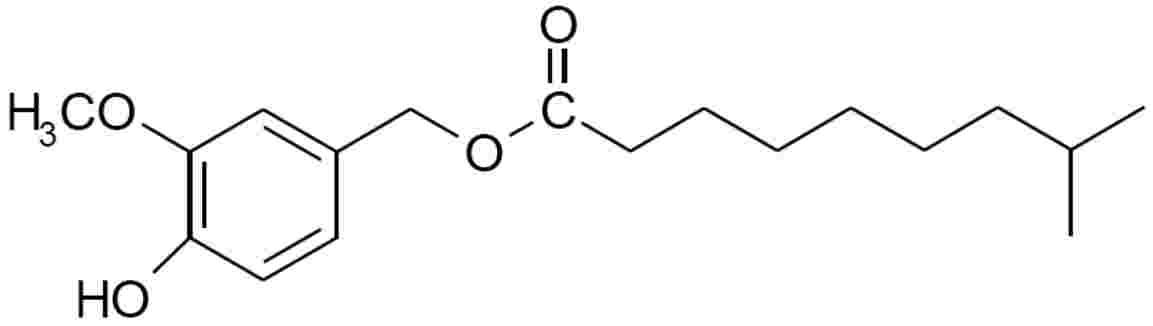
CAS №: 205687-03-2
Физико-химични свойства на дихидрокапсиат
|
Дихидрокапсиат |
повече от 94 % |
|
8-метилнонанова киселина |
под 6 % |
|
Ванилилов алкохол |
под 1 % |
|
Свързани със синтеза вещества |
под 2 % |
ПРИЛОЖЕНИЕ II
УПОТРЕБА НА ДИХИДРОКАПСИАТ
|
Категория храна |
Максимални нива на употреба |
|
Зърнени блокчета |
9 mg/100 g |
|
Бисквити, курабии и солени бисквити |
9 mg/100 g |
|
Оризови закуски |
12 mg/100 g |
|
Газирани напитки, разреждащи се напитки, напитки на основата на плодов сок |
1,5 mg/100 ml |
|
Зеленчукови напитки |
2 mg/100 ml |
|
Напитки на основата на кафе, напитки на основата на чай |
1,5 mg/100 ml |
|
Овкусена вода — негазирана |
1 mg/100 ml |
|
Предварително сварена овесена каша |
2,5 mg/100 g |
|
Други зърнени закуски |
4,5 mg/100 g |
|
Сладолед, млечни десерти |
4 mg/100 g |
|
Смеси за кремове (за директна консумация) |
2 mg/100 g |
|
Продукти на основата на кисело мляко |
2 mg/100 g |
|
Шоколадови изделия |
7,5 mg/100 g |
|
Твърди бонбони |
27 mg/100 g |
|
Дъвки без захар |
115 mg/100 g |
|
Сметана на немлечна основа за напитки |
40 mg/100 g |
|
Подсладители |
200 mg/100 g |
|
Супи (за директна консумация) |
1,1 mg/100 g |
|
Заливки за салата |
16 mg/100 g |
|
Растителни протеини |
5 mg/100 g |
|
Готови за консумация ястия Заместители на цяло хранене |
3 mg/ястие |
|
Напитки, заместващи цяло хранене |
1 mg/100ml |

