ISSN 1977-0820
Europeiska unionens
officiella tidning
L 126

Svensk utgåva
Lagstiftning
59 årgången
14 maj 2016
|
ISSN 1977-0820 |
||
|
Europeiska unionens officiella tidning |
L 126 |
|

|
||
|
Svensk utgåva |
Lagstiftning |
59 årgången |
|
|
|
|
|
(1) Text av betydelse för EES |
|
SV |
De rättsakter vilkas titlar är tryckta med fin stil är sådana rättsakter som har avseende på den löpande handläggningen av jordbrukspolitiska frågor. De har normalt en begränsad giltighetstid. Beträffande alla övriga rättsakter gäller att titlarna är tryckta med fetstil och föregås av en asterisk. |
II Icke-lagstiftningsakter
FÖRORDNINGAR
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/1 |
KOMMISSIONENS DELEGERADE FÖRORDNING (EU) 2016/757
av den 3 februari 2016
om fastställande av de åtgärder för tillämpningen av jordbrukslagstiftningen som kräver att uppgifter införs i Tullinformationssystemet
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DENNA FÖRORDNING
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av rådets förordning (EG) nr 515/97 av den 13 mars 1997 om ömsesidigt bistånd mellan medlemsstaternas administrativa myndigheter och om samarbete mellan dessa och kommissionen för att säkerställa en korrekt tillämpning av tull- och jordbrukslagstiftningen (1), särskilt artikel 23.4, och
av följande skäl:
|
(1) |
Ändamålet med Tullinformationssystemet (TIS) är att hjälpa de behöriga myndigheterna att förebygga, utreda och beivra överträdelser av tull- eller jordbrukslagstiftningen. För att TIS fortsatt ska möta de behöriga myndigheternas behov är det nödvändigt att uppdatera förteckningen över åtgärder för tillämpningen av jordbrukslagstiftningen som bör införas i systemet. |
|
(2) |
Uppgifter som förs in i TIS om åtgärder för tillämpningen av jordbrukslagstiftningen bör begränsas till de produkter som omfattas av kapitlen 1–24 i Kombinerade nomenklaturen. |
|
(3) |
Spårning av varurörelser som omfattas av jordbrukslagstiftningen är av yttersta vikt för att de behöriga myndigheterna snabbt ska kunna reagera på hälsorisker. För att se till att sådana varurörelser följs och spåras i alla stadier bör uppgifter lämnas om import, export, transitering, tillfällig lagring och flyttning inom EU. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
De åtgärder för tillämpningen av jordbrukslagstiftningen som enligt artikel 23.4 i förordning (EG) nr 515/97 kräver att uppgifter införs i TIS ska vara de som gäller för följande:
|
a) |
Import från tredjeland av produkter som omfattas av bestämmelser som antagits inom ramen för den gemensamma jordbrukspolitiken och den särskilda lagstiftning som antagits med avseende på varor som framställts genom bearbetning av jordbruksprodukter. |
|
b) |
Export till tredjeland av produkter som omfattas av bestämmelser som antagits inom ramen för den gemensamma jordbrukspolitiken och den särskilda lagstiftning som antagits med avseende på varor som framställts genom bearbetning av jordbruksprodukter. |
|
c) |
Varurörelser avseende produkter som omfattas av bestämmelser som antagits inom ramen för den gemensamma jordbrukspolitiken och den särskilda lagstiftning som antagits med avseende på varor som framställts genom bearbetning av jordbruksprodukter, inom ramen för ett förfarande för gemensam eller extern transitering samt verksamhet som omfattar tillfällig lagring i unionen av sådana produkter vid återexport från unionen till ett tredjeland. |
|
d) |
Unionsinterna varurörelser avseende produkter som omfattas av begränsningar eller förbud som grundar sig på bestämmelser som antagits inom ramen för den gemensamma jordbrukspolitiken och de särskilda bestämmelser som antagits med avseende på varor som framställts genom bearbetning av jordbruksprodukter, eller som åtnjuter EU-stöd. |
Artikel 2
Kommissionens förordning (EG) nr 696/98 (2) ska upphöra att gälla.
Artikel 3
Denna förordning träder i kraft den tjugonde dagen efter det att den har offentliggjorts i Europeiska unionens officiella tidning.
Den ska tillämpas från och med den 1 september 2016.
Denna förordning är till alla delar bindande och direkt tillämplig i alla medlemsstater.
Utfärdad i Bryssel den 3 februari 2016.
På kommissionens vägnar
Jean-Claude JUNCKER
Ordförande
(1) EGT L 82, 22.3.1997, s. 1.
(2) Kommissionens förordning (EG) nr 696/98 av den 27 mars 1998 om tillämpning av rådets förordning (EG) nr 515/97 av den 13 mars 1997 om ömsesidigt bistånd mellan medlemsstaternas administrativa myndigheter och om samarbete mellan dessa och kommissionen för att säkerställa en korrekt tillämpning av tull- och jordbrukslagstiftningen (EGT L 96, 28.3.1998, s. 22).
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/3 |
KOMMISSIONENS DELEGERADE FÖRORDNING (EU) 2016/758
av den 4 februari 2016
om ändring av Europaparlamentets och rådets förordning (EU) nr 1315/2013 i syfte att anpassa dess bilaga III
(Text av betydelse för EES)
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DENNA FÖRORDNING
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av Europaparlamentets och rådets förordning (EU) nr 1315/2013 av den 11 december 2013 om unionens riktlinjer för utbyggnad av det transeuropeiska transportnätet och om upphävande av beslut nr 661/2010/EU (1), särskilt artikel 49.6, och
av följande skäl:
|
(1) |
Förordning (EU) nr 1315/2013 ger möjlighet att anpassa de vägledande kartorna över det transeuropeiska transportnätet (TEN-T) som utvidgats till att omfatta vissa grannländer på grundval av avtal på hög nivå om transportinfrastrukturnät mellan unionen och de berörda grannländerna. |
|
(2) |
Vid toppmötet för västra Balkan (sexländersgruppen) i Wien godkändes den 27 augusti 2015 ett avtal på hög nivå mellan unionen och västra Balkanländerna Albanien, Bosnien och Hercegovina, Kosovo, f.d. jugoslaviska republiken Makedonien, Montenegro och Serbien om anpassning av den vägledande utvidgningen av de övergripande TEN-T-kartorna och om identifiering av stomnätsanslutningar på kartorna över det övergripande nätet. Detta avtal avser linjer i järnvägs- och vägnäten samt hamnar och flygplatser. Anpassningen av de vägledande kartorna över det övergripande nätet och, framförallt, identifieringen av det vägledande stomnätet kommer att göra det möjligt för unionen att bättre samordna sitt samarbete, vilket inbegriper ekonomiska stöd, med västra Balkan. |
|
(3) |
Inom ramen för den gemensamma kommitté som inrättats genom avtalet om Europeiska ekonomiska samarbetsområdet ingicks den 30 oktober 2015 ett avtal på hög nivå mellan unionen och Island och Norge om anpassning av den vägledande utvidgningen av de övergripande TEN-T-kartorna för dessa länder. Anpassningen rör ett begränsat antal justeringar av kartorna över väg-, hamn-, och flygplatsnäten som syftar till att bättre avspegla de vägledande TEN-T-näten i förhållande till TEN-T-metoden (2). |
|
(4) |
Förordning (EU) nr 1315/2013 bör därför ändras i enlighet med detta. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
Bilaga III till förordning (EU) nr 1315/2013 ska ändras i enlighet med bilagan till den här förordningen.
Artikel 2
Denna förordning träder i kraft den tjugonde dagen efter det att den har offentliggjorts i Europeiska unionens officiella tidning.
Denna förordning är till alla delar bindande och direkt tillämplig i alla medlemsstater.
Utfärdat i Bryssel den 4 februari 2016.
På kommissionens vägnar
Jean-Claude JUNCKER
Ordförande
(1) EUT L 348, 20.12.2013, s. 1.
(2) SWD(2013) 542 final.
BILAGA
Bilaga III till förordning (EU) nr 1315/2013 ska ändras på följande sätt:
|
(1) |
Punkt 11.1 ska ersättas med följande: ”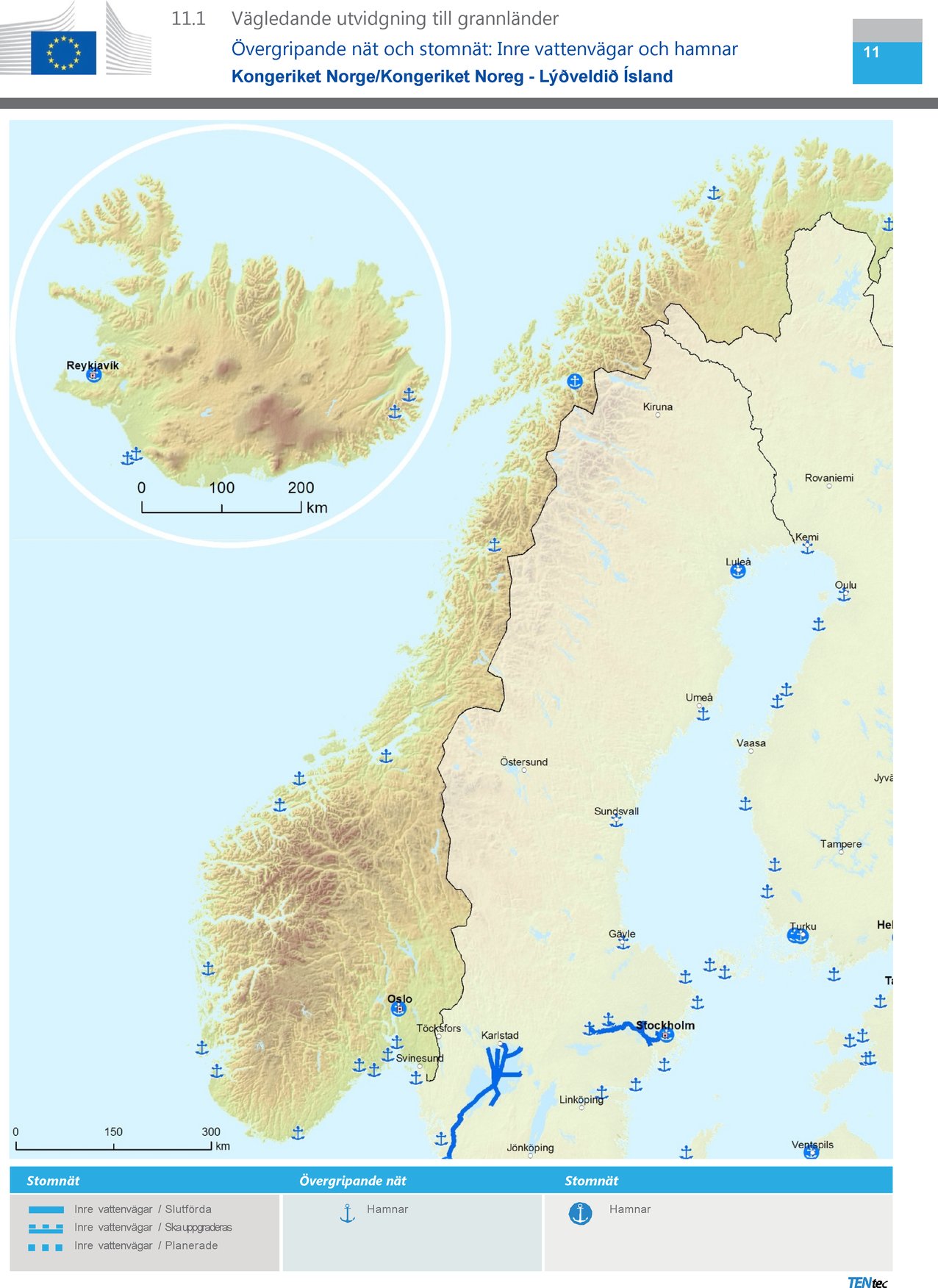 ” ” |
|
(2) |
Punkt 11.2 ska ersättas med följande: ” ” ” |
|
(3) |
Punkt 11.3 ska ersättas med följande: ”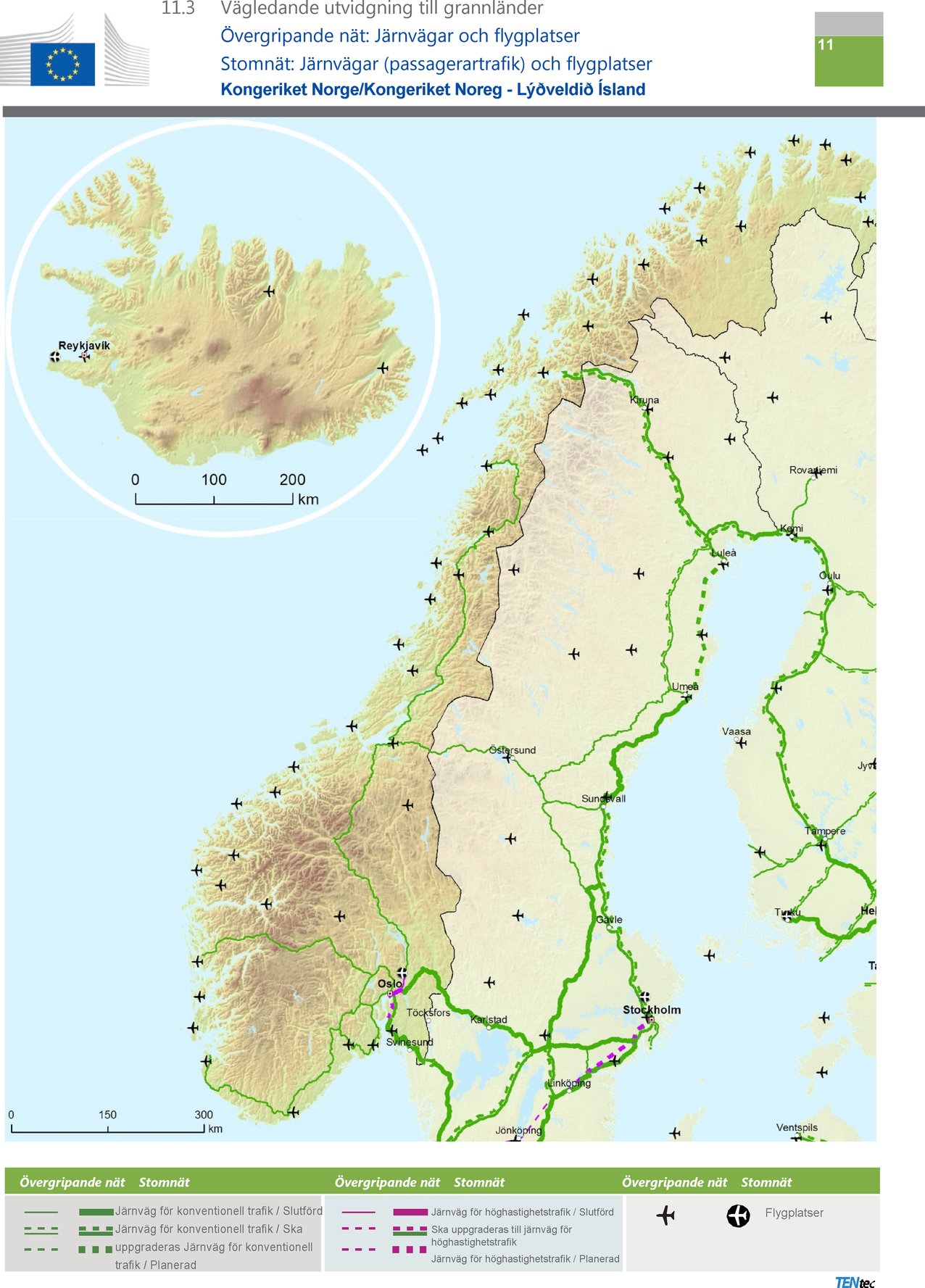 ” ” |
|
(4) |
Punkt 11.4 ska ersättas med följande: ”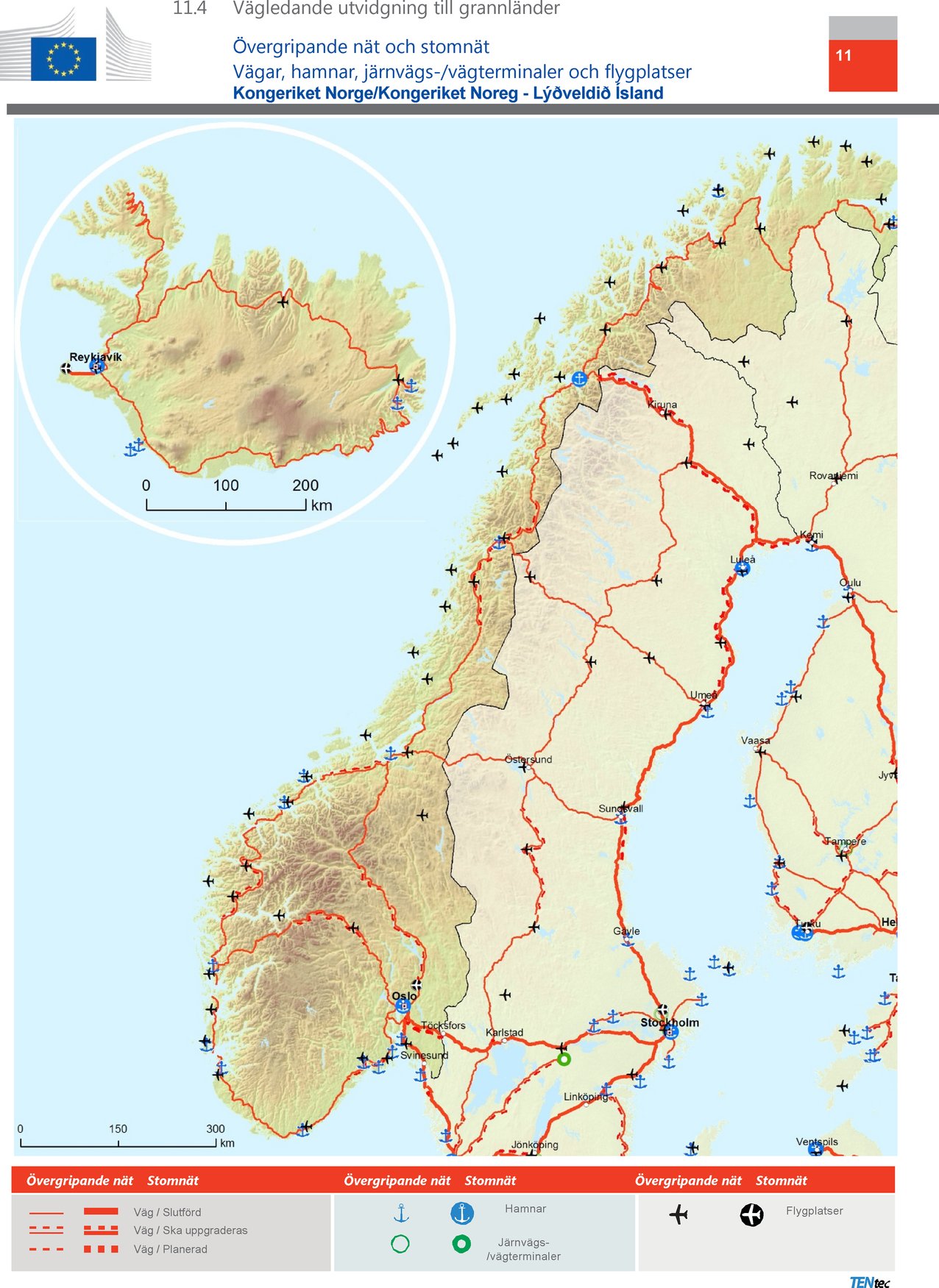 ” ” |
|
(5) |
Punkt 13.1 ska ersättas med följande: ” ” ” |
|
(6) |
Punkt 13.2 ska ersättas med följande: ” ” ” |
|
(7) |
Punkt 13.3 ska ersättas med följande: ”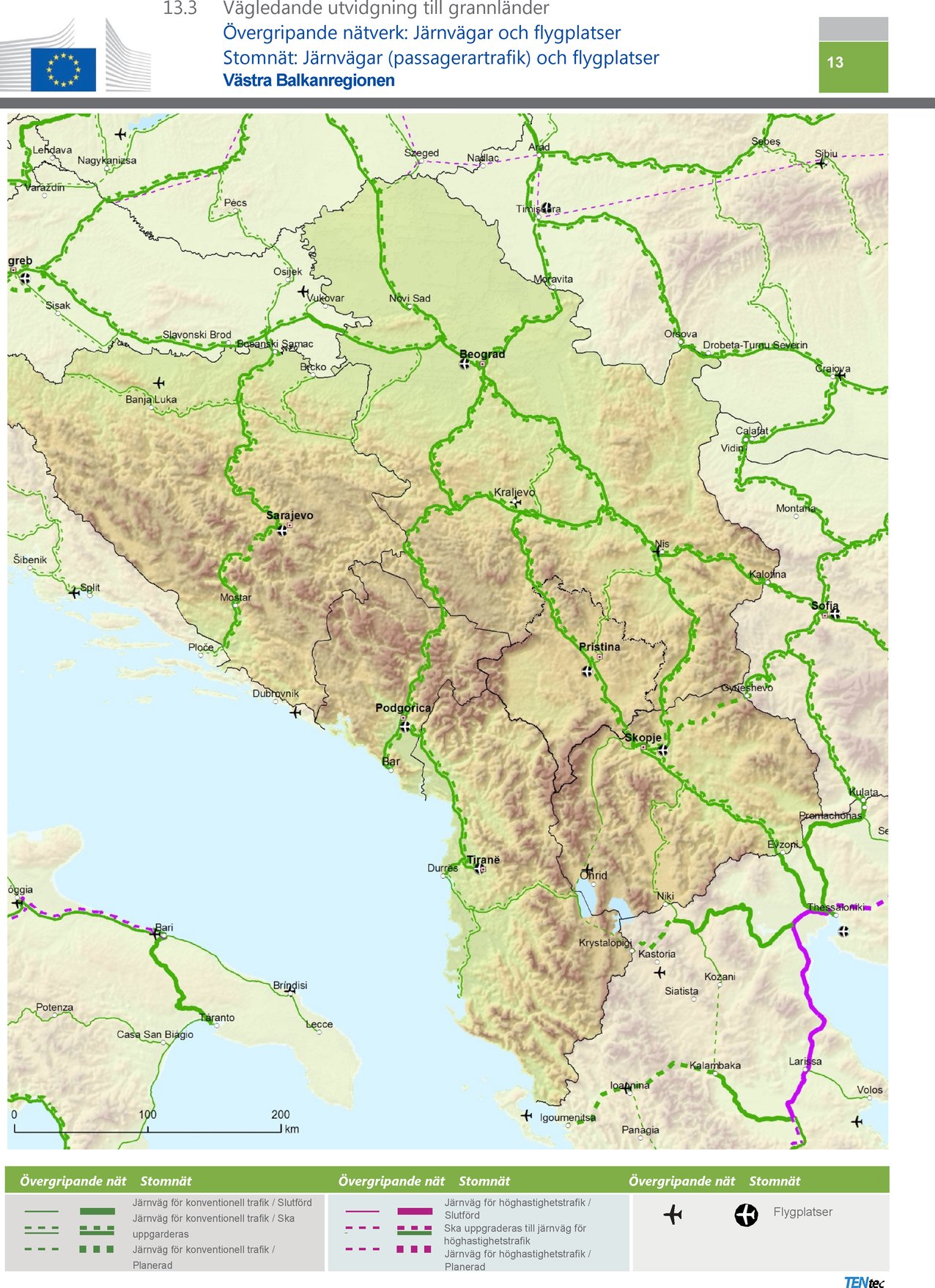 ” ” |
|
(8) |
Punkt 13.4 ska ersättas med följande: ” ” ” |
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/13 |
KOMMISSIONENS GENOMFÖRANDEFÖRORDNING (EU) 2016/759
av den 28 april 2016
om upprättande av förteckningar över tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta införsel till unionen av vissa produkter av animaliskt ursprung avsedda att användas som livsmedel, om fastställande av intygskrav, om ändring av förordning (EG) nr 2074/2005 och om upphävande av beslut 2003/812/EG
(Text av betydelse för EES)
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DENNA FÖRORDNING
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av rådets direktiv 2002/99/EG av den 16 december 2002 om fastställande av djurhälsoregler för produktion, bearbetning, distribution och införsel av produkter av animaliskt ursprung avsedda att användas som livsmedel (1), särskilt artiklarna 8.1 och 9.4,
med beaktande av Europaparlamentets och rådets förordning (EG) nr 854/2004 av den 29 april 2004 om fastställande av särskilda bestämmelser för genomförandet av offentlig kontroll av produkter av animaliskt ursprung avsedda att användas som livsmedel (2), särskilt artikel 11.1, och
av följande skäl:
|
(1) |
Enligt förordning (EG) nr 854/2004 får produkter av animaliskt ursprung endast importeras från ett tredjeland eller en del av ett tredjeland som finns med i en förteckning som upprättats enligt den förordningen. |
|
(2) |
I kommissionens beslut 2003/812/EG (3) upprättas förteckningar över tredjeländer från vilka medlemsstaterna ska tillåta import av vissa produkter avsedda att användas som livsmedel enligt rådets direktiv 92/118/EEG (4). Dessa förteckningar innehåller en förteckning över tredjeländer eller delar av tredjeländer från vilka det är tillåtet att importera gelatin avsett att användas som livsmedel. Det finns dock ingen förteckning som omfattar kollagen eller råvaror för framställning av gelatin och kollagen avsett att användas som livsmedel. Sådana förteckningar bör upprättas. |
|
(3) |
I enlighet med Europaparlamentets och rådets förordning (EG) nr 853/2004 (5) ska livsmedelsföretagare som importerar produkter av animaliskt ursprung se till att de dokument som åtföljer sändningen uppfyller kraven i artikel 14 i förordning (EG) nr 854/2004. I kommissionens förordning (EG) nr 2074/2005 (6) fastställs förlagor till intyg för import av vissa produkter av animaliskt ursprung avsedda att användas som livsmedel. Dessa förlagor till intyg innehåller föråldrade hänvisningar till tidigare lagstiftning som behöver uppdateras. |
|
(4) |
De tredjeländer, delar av tredjeländer och områden som förtecknas i bilaga II till kommissionens beslut 2006/766/EG (7), i del 1 i bilaga I till kommissionens förordning (EG) nr 798/2008 (8), i del 1 i bilaga I till kommissionens förordning (EG) nr 119/2009 (9) eller i del 1 i bilaga II till kommissionens förordning (EU) nr 206/2010 (10) uppfyller unionskraven för import av färskt kött och vissa fiskeriprodukter. Dessa förteckningar kan också användas vid import av råvaror för framställning av gelatin och kollagen. Mindre strikta krav bör dock tillämpas om dessa råvaror har genomgått vissa behandlingar som föreskrivs i avsnitten XIV och XV i bilaga III till förordning (EG) nr 853/2004. |
|
(5) |
De råvaror för framställning av gelatin och kollagen, även behandlade, som förs in till unionen för transitering till ett tredjeland utgör en försumbar risk för folkhälsan. Dessa råvaror, även behandlade, bör dock uppfylla de tillämpliga djurhälsokraven. Därmed bör en förteckning över tredjeländer, delar av tredjeländer och områden upprättas och förlagor till intyg för transitering, och lagring före transitering, av råvaror och behandlade råvaror för framställning av gelatin och kollagen fastställas. |
|
(6) |
På grund av Kaliningrads geografiska läge bör speciella djurhälsovillkor fastställas för transitering via unionen av sändningar av råvaror och behandlade råvaror för framställning av gelatin eller kollagen till och från Ryssland, vilket endast berör transitering genom Lettland, Litauen och Polen. |
|
(7) |
För att förtydliga och förenkla unionslagstiftningen, och utan att det påverkar tillämpningen av kommissionens beslut 2003/863/EG (11), bör de förteckningar över tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta införsel av grodlår, snäckor, gelatin, kollagen, råvaror och behandlade råvaror för framställning av gelatin och kollagen och införsel av honung, bidrottninggelé och andra biodlingsprodukter avsedda att användas som livsmedel samt förlagorna till intyg för dessa produkter fastställas i en bilaga till denna förordning. Följaktligen bör de motsvarande befintliga intygen utgå från bilaga VI till förordning (EG) nr 2074/2005. |
|
(8) |
För att säkerställa säkerheten hos vissa högförädlade produkter av animaliskt ursprung har särskilda krav införts i bilaga III till förordning (EG) nr 853/2004. Det är därför lämpligt att upprätta en förteckning över de länder från vilka dessa produkter får importeras och att fastställa en förlaga till intyg för dessa produkter. |
|
(9) |
Eftersom förteckningar över tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta import av köttprodukter av hägnat pälsvilt och hägnat fjädervilt samt kött och köttprodukter av harar och kaniner (Leporidae) fastställs i kommissionens beslut 2007/777/EG (12) respektive i förordning (EG) nr 119/2009, är beslut 2003/812/EG överflödigt och bör upphävas. |
|
(10) |
En övergångsperiod bör medges så att medlemsstaterna och livsmedelsföretagarna kan anpassa sig till de nya kraven i denna förordning. |
|
(11) |
De åtgärder som föreskrivs i denna förordning är förenliga med yttrandet från ständiga kommittén för växter, djur, livsmedel och foder. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
KAPITEL 1
IMPORT AV VISSA PRODUKTER AV ANIMALISKT URSPRUNG
Artikel 1
Förteckningar över tredjeländer, delar av tredjeländer och områden
De tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta import av följande produkter av animaliskt ursprung avsedda att användas som livsmedel fastställs i de tillämpliga delarna av bilaga I:
|
a) |
Grodlår, del I. |
|
b) |
Snäckor, del II. |
|
c) |
Gelatin och kollagen, del III. |
|
d) |
Råvaror för framställning av gelatin och kollagen, del IV. |
|
e) |
Behandlade råvaror för framställning av gelatin och kollagen, del V. |
|
f) |
Honung, bidrottninggelé och andra biodlingsprodukter, del VI. |
|
g) |
Följande högförädlade produkter, del VII:
|
Artikel 2
Förlagor till intyg
1. Förlagorna till intyg för import till unionen av de produkter som avses i artikel 1 fastställs i bilaga II enligt följande:
|
a) |
Grodlår, del I. |
|
b) |
Snäckor, del II. |
|
c) |
Gelatin, del III. |
|
d) |
Kollagen, del IV. |
|
e) |
Råvaror för framställning av gelatin och kollagen, del V. |
|
f) |
Behandlade råvaror för framställning av gelatin och kollagen, del VI. |
|
g) |
Honung, bidrottninggelé och andra biodlingsprodukter, del VII. |
|
h) |
Följande högförädlade produkter, del VIII:
|
Dessa intyg ska fyllas i i enlighet med anvisningarna i bilaga IV och anmärkningarna i de tillämpliga intygen.
2. Elektroniska intyg och andra system som unionen och det berörda tredjelandet kommit överens om får användas.
KAPITEL 2
TRANSITERING AV VISSA PRODUKTER AV ANIMALISKT URSPRUNG
Artikel 3
Förteckningar över tredjeländer, delar av tredjeländer och områden
I delarna IV och V i bilaga I till denna förordning fastställs de tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta transitering genom unionen till ett tredjeland, antingen direkt eller efter lagring i unionen, av råvaror respektive behandlade råvaror för framställning av gelatin och kollagen avsett att användas som livsmedel, i enlighet med artiklarna 12.4 och 13 i rådets direktiv 97/78/EG (14).
Artikel 4
Förlaga till intyg
1. Förlagan till intyg för transitering genom unionen av de råvaror och behandlade råvaror som avses i artikel 3 fastställs i bilaga III.
Detta intyg ska fyllas i i enlighet med anvisningarna i bilaga IV och anmärkningarna i den tillämpliga förlagan till intyg.
2. Elektroniska intyg och andra system som harmoniserats på unionsnivå får användas.
Artikel 5
Undantag för transitering genom Lettland, Litauen och Polen
1. Genom undantag från artikel 3 ska man tillåta transitering på landsväg eller järnväg mellan de specifika, utsedda gränskontrollstationer i Lettland, Litauen och Polen som förtecknas med anmärkning 13 i bilaga I till kommissionens beslut 2009/821/EG (15) av sändningar av de råvaror eller behandlade råvaror som avses i artikel 3 i denna förordning och som kommer från och är destinerade till Ryssland, direkt eller via ett annat tredjeland, om följande villkor är uppfyllda:
|
a) |
Den officiella veterinären vid gränskontrollstationen för införsel har förseglat sändningen med en försegling som är försedd med ett löpnummer. |
|
b) |
De dokument som enligt artikel 7 i direktiv 97/78/EG ska åtfölja sändningen har på varje sida märkts med ”Only for transit to Russia via the EU” av den officiella veterinären vid gränskontrollstationen för införsel. |
|
c) |
Formföreskrifterna i artikel 11 i direktiv 97/78/EG är uppfyllda. |
|
d) |
Det anges på den gemensamma veterinärhandlingen vid införsel som utfärdats av den officiella veterinären vid gränskontrollstationen för införsel att sändningen är godkänd för transitering. |
2. De sändningar som avses i punkt 1 får inte lastas av eller lagras i unionen på det sätt som avses i artikel 12.4 eller 13 i direktiv 97/78/EG.
3. Den behöriga myndigheten ska göra regelbundna kontroller för att se till att antalet sändningar enligt punkt 1 och motsvarande mängd produkter som lämnar unionen motsvarar det antal och den mängd som har förts in i unionen.
KAPITEL 3
SLUTBESTÄMMELSER
Artikel 6
Ändringar
Bilaga VI till förordning (EG) nr 2074/2005 ska ändras på följande sätt:
|
1. |
I avsnitt I ska kapitlen I, II, III och VI utgå. |
|
2. |
Tilläggen I, II, III och VI ska utgå. |
Artikel 7
Upphävande
Beslut 2003/812/EG ska upphöra att gälla.
Artikel 8
Övergångsbestämmelser
De sändningar av produkter av animaliskt ursprung för vilka de tillämpliga intygen har utfärdats i enlighet med förordning (EG) nr 2074/2005 får fortsätta att föras in till unionen under förutsättning att intyget undertecknades före den 3 december 2016.
Artikel 9
Ikraftträdande
Denna förordning träder i kraft den tjugonde dagen efter det att den har offentliggjorts i Europeiska unionens officiella tidning.
Denna förordning är till alla delar bindande och direkt tillämplig i alla medlemsstater.
Utfärdad i Bryssel den 28 april 2016.
På kommissionens vägnar
Jean-Claude JUNCKER
Ordförande
(1) EGT L 18, 23.1.2003, s. 11.
(2) EUT L 139, 30.4.2004, s. 206.
(3) Kommissionens beslut 2003/812/EG av den 17 november 2003 om upprättande av en förteckning över tredje länder från vilka medlemsstaterna skall tillåta import av vissa produkter avsedda som livsmedel enligt rådets direktiv 92/118/EEG (EUT L 305, 22.11.2003, s. 17).
(4) Rådets direktiv 92/118/EEG av den 17 december 1992 om djurhälso- och hygienkrav för handel inom gemenskapen med produkter, som inte omfattas av sådana krav i de särskilda gemenskapsbestämmelser som avses i bilaga A.I till direktiv 89/662/EEG och, i fråga om patogener, i direktiv 90/425/EEG, samt för import till gemenskapen av sådana produkter (EGT L 62, 15.3.1993, s. 49).
(5) Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55).
(6) Kommissionens förordning (EG) nr 2074/2005 av den 5 december 2005 om tillämpningsåtgärder för vissa produkter enligt Europaparlamentets och rådets förordning (EG) nr 853/2004 och för genomförandet av offentliga kontroller enligt Europaparlamentets och rådets förordningar (EG) nr 854/2004 och (EG) nr 882/2004, om undantag från Europaparlamentets och rådets förordning (EG) nr 852/2004 och om ändring av förordningarna (EG) nr 853/2004 och (EG) nr 854/2004 (EUT L 338, 22.12.2005, s. 27).
(7) Kommissionens beslut 2006/766/EG av den 6 november 2006 om fastställande av en förteckning över de tredjeländer och delar av tredjeländer från vilka import av musslor, tagghudingar, manteldjur, marina snäckor och fiskeriprodukter är tillåten (EUT L 320, 18.11.2006, s. 53).
(8) Kommissionens förordning (EG) nr 798/2008 av den 8 augusti 2008 om fastställande av en förteckning över tredjeländer, områden, zoner eller delområden från vilka fjäderfä och fjäderfäprodukter får importeras till och transiteras genom gemenskapen samt kraven för veterinärintyg (EUT L 226, 23.8.2008, s. 1).
(9) Kommissionens förordning (EG) nr 119/2009 av den 9 februari 2009 om fastställande av en förteckning över tredjeländer och delar av tredjeländer för import till eller transitering genom gemenskapen av kött av vilda harar och kaniner, vissa vilda landlevande däggdjur och hägnade kaniner samt om kraven för veterinärintyg (EUT L 39, 10.2.2009, s. 12).
(10) Kommissionens förordning (EU) nr 206/2010 av den 12 mars 2010 om fastställande av förteckningar över tredjeländer, områden eller delar därav från vilka det är tillåtet att föra in vissa djur och färskt kött till Europeiska unionen samt kraven för veterinärintyg (EUT L 73, 20.3.2010, s. 1).
(11) Kommissionens beslut 2003/863/EG av den 2 december 2003 om hälsointyg för import av animaliska produkter från Förenta staterna (EUT L 325, 12.12.2003, s. 46).
(12) Kommissionens beslut 2007/777/EG av den 29 november 2007 om djur- och folkhälsovillkor och förlagor till hälsointyg för import från tredjeländer av vissa köttprodukter och behandlade magar, blåsor och tarmar avsedda att användas som livsmedel och om upphävande av beslut 2005/432/EG (EUT L 312, 30.11.2007, s. 49).
(13) Europaparlamentets och rådets förordning (EG) nr 1333/2008 av den 16 december 2008 om livsmedelstillsatser (EUT L 354, 31.12.2008, s. 16).
(14) Rådets direktiv 97/78/EG av den 18 december 1997 om principerna för organisering av veterinärkontroller av produkter från tredje land som förs in i gemenskapen (EGT L 24, 30.1.1998, s. 9).
(15) Kommissionens beslut 2009/821/EG av den 28 september 2009 om upprättande av en förteckning över godkända gränskontrollstationer, om fastställande av vissa regler för inspektioner som utförs av kommissionens veterinärexperter och om fastställande av veterinärenheter i Traces (EUT L 296, 12.11.2009, s. 1).
BILAGA I
Förteckningar över de tredjeländer, delar av tredjeländer och områden som avses i artikel 1
DEL I
GRODLÅR
De tredjeländer och områden som förtecknas i kolumnen ”Land” i bilaga II till beslut 2006/766/EG, utom de för vilka en begränsning anges i kolumnen ”Begränsningar” i den bilagan, och följande länder eller områden:
|
LAND ISO-KOD |
LAND/OMRÅDE |
|
MK (*1) |
f.d. jugoslaviska republiken Makedonien |
DEL II
SNÄCKOR
De tredjeländer och områden som förtecknas i kolumnen ”Land” i bilaga II till beslut 2006/766/EG, utom de för vilka en begränsning anges i kolumnen ”Begränsningar” i den bilagan, och följande länder eller områden:
|
LAND ISO-KOD |
LAND/OMRÅDE |
|
MD |
Moldavien |
|
MK (*2) |
f.d. jugoslaviska republiken Makedonien |
|
SY |
Syrien |
DEL III
GELATIN OCH KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL
AVSNITT A
Gelatin och kollagen som härrör från nötkreatur, får, getter, svin och hästdjur, såväl hägnade som frilevande
De tredjeländer och områden som förtecknas i kolumn 1 i del 1 i bilaga II till förordning (EU) nr 206/2010 och följande länder eller områden:
|
LAND ISO-KOD |
LAND/OMRÅDE |
|
KR |
Republiken Korea |
|
MY |
Malaysia |
|
PK |
Pakistan |
|
TW |
Taiwan |
AVSNITT B
Gelatin och kollagen som härrör från fjäderfä, inklusive ratiter och fjädervilt
De tredjeländer och områden som förtecknas i kolumn 1 i del 1 i bilaga I till förordning (EG) nr 798/2008.
AVSNITT C
Gelatin och kollagen som härrör från fiskeriprodukter
Alla tredjeländer och områden som förtecknas i kolumnen ”Land” i bilaga II till beslut 2006/766/EG, oberoende av om en begränsning anges i kolumnen ”Begränsningar” i den bilagan.
AVSNITT D
Gelatin och kollagen som härrör från harar och kaniner (Leporidae) och de vilda landlevande däggdjur som inte avses i avsnitt A
De tredjeländer som förtecknas i kolumn 1 i del 1 i bilaga I till förordning (EG) nr 119/2009.
DEL IV
RÅVAROR FÖR FRAMSTÄLLNING AV GELATIN OCH KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL
AVSNITT A
Råvaror från nötkreatur, får, getter, svin och hästdjur, såväl hägnade som frilevande
De tredjeländer, områden och delar därav som förtecknas i del 1 i bilaga II till förordning (EU) nr 206/2010 från vilka det är tillåtet att till unionen föra in denna kategori av färskt kött från respektive art enligt vad som anges i den delen av den bilagan, såvida inte en sådan införsel begränsas av tilläggsgaranti A eller F enligt kolumn 5.
AVSNITT B
Råvaror från fjäderfä, inklusive ratiter och fjädervilt
De tredjeländer, delar av tredjeländer och områden som förtecknas i del 1 i bilaga I till förordning (EG) nr 798/2008 från vilka det är tillåtet att importera färskt fjäderfäkött från respektive art enligt vad som anges i den delen av den bilagan.
AVSNITT C
Råvaror från fiskeriprodukter
De tredjeländer och områden som förtecknas i kolumnen ”Land” i bilaga II till beslut 2006/766/EG och som omfattas av de begränsningar som anges i kolumnen ”Begränsningar” i den bilagan.
AVSNITT D
Råvaror från harar och kaniner (Leporidae) och de vilda landlevande däggdjur som inte avses i avsnitt A
De tredjeländer som förtecknas i kolumn 1 i del 1 i bilaga I till förordning (EG) nr 119/2009 från vilka det är tillåtet att importera färskt kött från respektive art enligt vad som anges i den delen av den bilagan.
DEL V
BEHANDLANDE RÅVAROR FÖR FRAMSTÄLLNING AV GELATIN OCH KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL
AVSNITT A
Behandlade råvaror från nötkreatur, får, getter, svin och hästdjur, såväl hägnade som frilevande
De tredjeländer, områden och delar därav som förtecknas i kolumn 1 i del 1 i bilaga II till förordning (EU) nr 206/2010 och följande länder eller områden:
|
LAND ISO-KOD |
LAND/OMRÅDE |
|
KR |
Republiken Korea |
|
MY |
Malaysia |
|
PK |
Pakistan |
|
TW |
Taiwan |
AVSNITT B
Behandlade råvaror från fjäderfä, inklusive ratiter och fjädervilt
De tredjeländer och områden som förtecknas i kolumn 1 i del 1 i bilaga I till förordning (EG) nr 798/2008.
AVSNITT C
Behandlade råvaror från fiskeriprodukter
Alla tredjeländer och områden som förtecknas i kolumnen ”Land” i bilaga II till beslut 2006/766/EG, oberoende av om en begränsning anges i kolumnen ”Begränsningar” i den bilagan.
AVSNITT D
Behandlade råvaror från harar och kaniner (Leporidae) och de vilda landlevande däggdjur som inte avses i avsnitt A
De tredjeländer som förtecknas i kolumn 1 i del 1 i bilaga I till förordning (EG) nr 119/2009.
AVSNITT E
De behandlade råvaror som avses i avsnitt XIV kapitel I punkt 4 b iii och avsnitt XV kapitel I punkt 4 b iii i bilaga III till förordning (EG) nr 853/2004
De tredjeländer, delar av tredjeländer och områden som avses i del IV i denna bilaga.
DEL VI
HONUNG, BIDROTTNINGGELÉ OCH ANDRA BIODLINGSPRODUKTER AVSEDDA ATT ANVÄNDAS SOM LIVSMEDEL
De tredjeländer och områden som förtecknas i kolumnen ”Land” i bilagan till kommissionens beslut 2011/163/EU (1) och som har ett X i kolumnen ”Honung” i den bilagan.
DEL VII
HÖGFÖRÄDLAT KONDROITINSULFAT, HÖGFÖRÄDLAD HYALURONSYRA, HÖGFÖRÄDLADE ANDRA HYDROLYSERADE BROSKPRODUKTER, HÖGFÖRÄDLAT KITOSAN, GLUKOSAMIN, LÖPE OCH HUSBLOSS SAMT HÖGFÖRÄDLADE AMINOSYROR AVSEDDA ATT ANVÄNDAS SOM LIVSMEDEL
|
a) |
När det gäller råvaror som härrör från hov- och klövdjur, inklusive hästdjur, de tredjeländer och områden som förtecknas i kolumn 1 i del 1 i bilaga II till förordning (EU) nr 206/2010 och följande länder eller områden:
|
|
b) |
När det gäller råvaror som härrör från fiskeriprodukter, alla tredjeländer och områden som förtecknas i kolumnen ”Land” i bilaga II till beslut 2006/766/EG, oberoende av om en begränsning anges i kolumnen ”Begränsningar” i den bilagan. |
|
c) |
När det gäller råvaror som härrör från fjäderfä, de tredjeländer och områden som förtecknas i kolumn 1 i del 1 i bilaga I till förordning (EG) nr 798/2008. |
(*1) F.d. jugoslaviska republiken Makedonien. Koden föregriper inte den definitiva beteckningen för detta land, vilken kommer att fastställas efter det att de nuvarande förhandlingarna i Förenta nationerna om detta har slutförts.
(*2) F.d. jugoslaviska republiken Makedonien. Koden föregriper inte den definitiva beteckningen för detta land, vilken kommer att fastställas efter det att de nuvarande förhandlingarna i Förenta nationerna om detta har slutförts.
(1) Kommissionens beslut 2011/163/EU av den 16 mars 2011 om godkännande av planer som lagts fram av tredjeländer i enlighet med artikel 29 i rådets direktiv 96/23/EG (EUT L 70, 17.3.2011, s. 40).
BILAGA II
De förlagor till intyg som avses i artikel 2
DEL I
FÖRLAGA TILL INTYG FÖR IMPORT AV KYLDA, FRYSTA ELLER BEREDDA GRODLÅR AVSEDDA ATT ANVÄNDAS SOM LIVSMEDEL

LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Fartyg
I.19 Varukod (HS)
02.08.90
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Typ av behandling
Godkännande-nummer för anläggningar
Tillverkningsan-läggning
Antal förpackningar
Nettovikt

LAND
Förlaga FRG Grodlår
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1) och Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och att de ovan beskrivna grodlåren har producerats i enlighet med kraven i dessa förordningar, särskilt när det gäller följande:
— De kommer från en anläggning (anläggningar) som genomför ett program grundat på HACCP-principerna i enlighet med artikel 5 i förordning (EG) nr 852/2004.
— De kommer från grodor som har tappats på blod, beretts och, i förekommande fall, kylts, frysts, bearbetats, emballerats och lagrats under hygieniska förhållanden i enlighet med kraven i avsnitt XI i bilaga III till förordning (EG) nr 853/2004.
Anmärkningar
Del I:
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).
— Fält I.28: Typ av behandling: Färska, behandlade.
Del II:
— Underskriften och stämpeln ska ha en annan färg än övriga uppgifter i intyget.
Del II: Intyg
Officiell inspektör
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL II
FÖRLAGA TILL INTYG FÖR IMPORT AV KYLDA, FRYSTA, SKALADE, KOKTA, BEREDDA ELLER KONSERVERADE SNÄCKOR AVSEDDA ATT ANVÄNDAS SOM LIVSMEDEL

LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter (vetenskapligt namn)
Typ av behandling
Godkännandenummer för anläggningar
Antal förpackningar
Nettovikt
Tillverkningsanläggning

LAND
Förlaga SNS Snäckor
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1) och Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och att de ovan beskrivna snäckorna har producerats i enlighet med kraven i dessa förordningar, särskilt när det gäller följande:
— De kommer från en anläggning (anläggningar) som genomför ett program grundat på HACCP-principerna i enlighet med artikel 5 i förordning (EG) nr 852/2004.
— De har hanterats och, i förekommande fall, skalats, kokats, beretts, konserverats, frysts, emballerats och lagrats under hygieniska förhållanden i enlighet med kraven i avsnitt XI i bilaga III till förordning (EG) nr 853/2004.
Anmärkningar
Del I:
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubriker: 03.07, 16.05.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).
— Fält I.28: Typ av behandling: Färska, behandlade.
Del II:
— Underskriften och stämpeln ska ha en annan färg än övriga uppgifter i intyget.
Del II: Intyg
Officiell inspektör
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL III
FÖRLAGA TILL INTYG FÖR IMPORT AV GELATIN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL

LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Framställnings-datum
(dd/mm/åååå)
Godkännande-nummer för anläggningar
Tillverkningsan-läggning
Antal förpackningar
Nettovikt

LAND
Förlaga GEL Gelatin avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1) och Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och att det ovan beskrivna gelatinet har producerats i enlighet med kraven i dessa förordningar, särskilt när det gäller följande:
— Det kommer från en anläggning (anläggningar) som genomför ett program grundat på HACCP-principerna i enlighet med artikel 5 i förordning (EG) nr 852/2004.
— Det har producerats av råvaror som uppfyller kraven i avsnitt XIV kapitlen I och II i bilaga III till förordning (EG) nr 853/2004.
— Det har framställts i enlighet med villkoren i avsnitt XIV kapitel III i bilaga III till förordning (EG) nr 853/2004.
— Det uppfyller kriterierna i avsnitt XIV kapitel IV i bilaga III till förordning (EG) nr 853/2004 och i kommissionens förordning (EG) nr 2073/2005 av den 15 november 2005 om mikrobiologiska kriterier för livsmedel (EUT L 338, 22.12.2005, s. 1).
Om gelatinet kommer från idisslare, med undantag för gelatin som härrör från hudar och skinn från idisslare, ska dessutom följande gälla:
(1) antingen
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i Europaparlamentets och rådets förordning (EG) nr 999/2001 av den 22 maj 2001 om fastställande av bestämmelser för förebyggande, kontroll och utrotning av vissa typer av transmissibel spongiform encefalopati (EGT L 147, 31.5.2001, s. 1) har klassificerats som ett land eller en region med försumbar BSE-risk.
— De djur från vilka gelatinet härrör är födda, oavbrutet uppfödda och slaktade i landet med försumbar BSE-risk och har genomgått besiktning före och efter slakt.
— Om det har förekommit inhemska fall av BSE i landet eller regionen
i) kommer det från djur som föddes efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, eller
ii) innehåller produkterna från nötkreatur, får och getter inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk.
— De djur från vilka gelatinet härrör har genomgått besiktning före och efter slakt.
— De djur från vilka gelatinet avsett för export härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Gelatinet innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001), eller maskinurbenat kött från ben av nötkreatur, får och getter.]
Del II: Intyg

LAND
Förlaga GEL Gelatin avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
(1) eller
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med försumbar BSE-risk.
— Gelatinet härrör från djur som har genomgått besiktning före och efter slakt.
— Gelatinet härrör både från djur som är födda, oavbrutet uppfödda och slaktade i ett land eller en region med försumbar BSE-risk i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 och som, om det har förekommit inhemska fall av BSE i landet eller regionen, är födda efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, och från djur som är födda i ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk, och dessa djur har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Gelatinet innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001), eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med ej fastställd BSE-risk.
— De djur från vilka gelatinet härrör har inte utfodrats med kött- och benmjöl eller fettgrevar från idisslare och har genomgått besiktning före och efter slakt.
— De djur från vilka gelatinet härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Gelatinet härrör inte från
i) specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001,
ii) nerv- och lymfvävnad som frilagts under urbeningen,
iii) maskinurbenat kött från ben från nötkreatur, får eller getter.]
Anmärkningar
Del I:
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubrik: 35.03.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).

LAND
Förlaga GEL Gelatin avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
Del II:
(1) Stryk det som inte är tillämpligt.
— Underskriften och stämpeln ska ha en annan färg än övriga uppgifter i intyget.
Officiell veterinär Namn (med versaler):
Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL IV
FÖRLAGA TILL INTYG FÖR IMPORT AV KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL
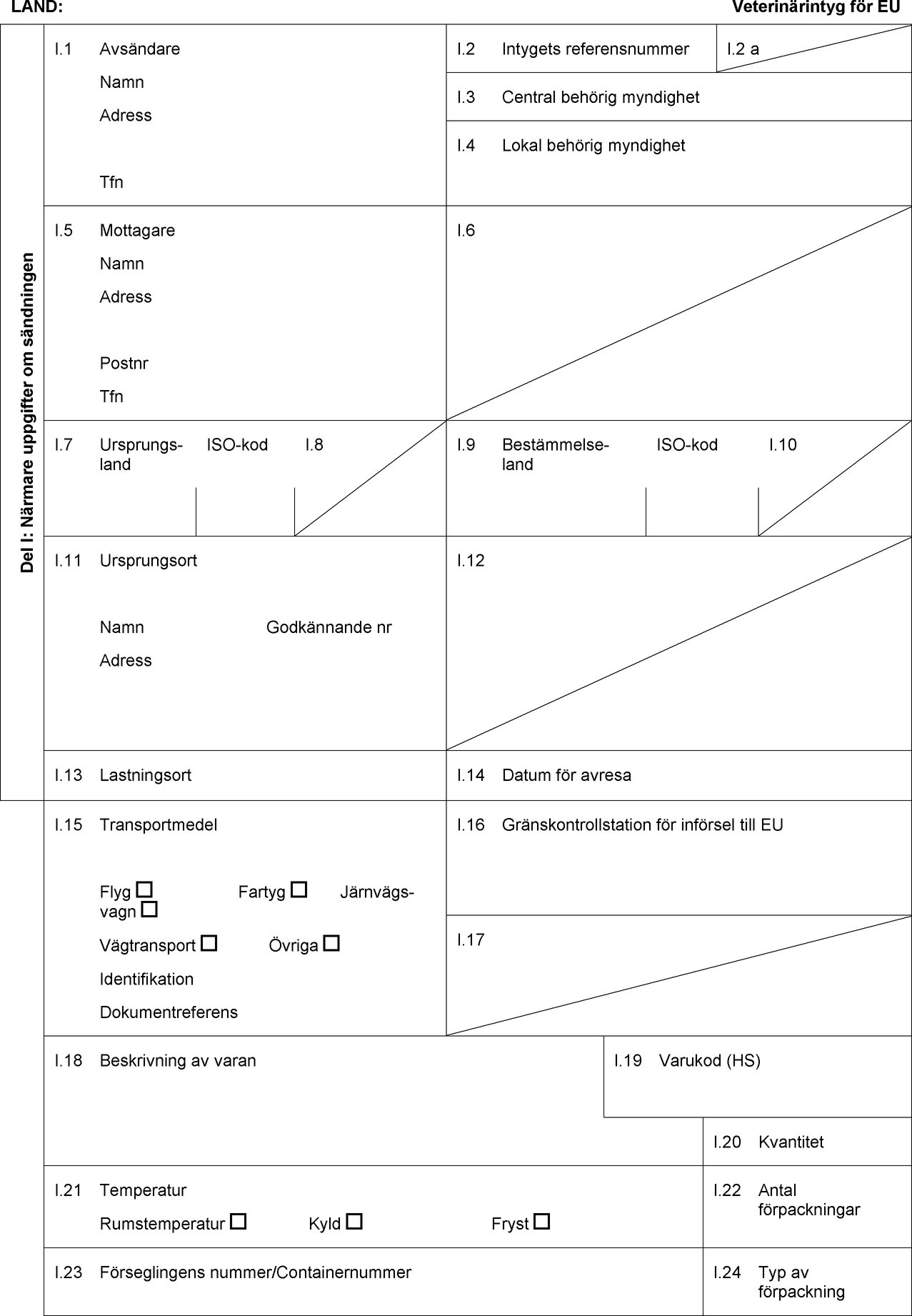
LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägs-vagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Framställnings-datum
(dd/mm/åååå)
Godkännande-nummer för anläggningar
Tillverkningsan-läggning
Antal förpackningar
Nettovikt

LAND
Förlaga COL Kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1) och Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och att det ovan beskrivna kollagenet har producerats i enlighet med kraven i dessa förordningar, särskilt när det gäller följande:
— Det kommer från en anläggning (anläggningar) som genomför ett program grundat på HACCP-principerna i enlighet med artikel 5 i förordning (EG) nr 852/2004.
— Det har producerats av råvaror som uppfyller kraven i avsnitt XV kapitlen I och II i bilaga III till förordning (EG) nr 853/2004.
— Det har framställts i enlighet med villkoren i avsnitt XV kapitel III i bilaga III till förordning (EG) nr 853/2004.
— Det uppfyller kriterierna i avsnitt XV kapitel IV i bilaga III till förordning (EG) nr 853/2004 och i kommissionens förordning (EG) nr 2073/2005 av den 15 november 2005 om mikrobiologiska kriterier för livsmedel (EUT L 338, 22.12.2005, s. 1).
Om kollagenet kommer från idisslare, med undantag för kollagen som härrör från hudar och skinn från idisslare, ska dessutom följande gälla:
(1) antingen
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i Europaparlamentets och rådets förordning (EG) nr 999/2001 av den 22 maj 2001 om fastställande av bestämmelser för förebyggande, kontroll och utrotning av vissa typer av transmissibel spongiform encefalopati (EGT L 147, 31.5.2001, s. 1) har klassificerats som ett land eller en region med försumbar BSE-risk.
— De djur från vilka kollagenet härrör är födda, oavbrutet uppfödda och slaktade i landet med försumbar BSE-risk och har genomgått besiktning före och efter slakt.
— Om det har förekommit inhemska fall av BSE i landet eller regionen
i) kommer det från djur som föddes efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, eller
ii) innehåller produkterna från nötkreatur, får och getter inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk.
— De djur från vilka kollagenet härrör har genomgått besiktning före och efter slakt.
— De djur från vilka kollagenet avsett för export härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Kollagenet innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001), eller maskinurbenat kött från ben av nötkreatur, får och getter.]
Del II: Intyg

LAND
Förlaga COL Kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
(1) eller
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med försumbar BSE-risk.
— Kollagenet härrör från djur som har genomgått besiktning före och efter slakt.
— Kollagenet härrör både från djur som är födda, oavbrutet uppfödda och slaktade i ett land eller en region med försumbar BSE-risk i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 och som, om det har förekommit inhemska fall av BSE i landet eller regionen, är födda efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, och från djur som är födda i ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk, och dessa djur har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Kollagenet innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001), eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [Det kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med ej fastställd BSE-risk.
— De djur från vilka kollagenet härrör har inte utfodrats med kött- och benmjöl eller fettgrevar från idisslare och har genomgått besiktning före och efter slakt.
— De djur från vilka kollagenet härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Kollagenet härrör inte från
i) specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001,
ii) nerv- och lymfvävnad som frilagts under urbeningen,
iii) maskinurbenat kött från ben från nötkreatur, får eller getter.]
Anmärkningar
Del I:
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.18: Detta intyg får också användas för import av naturtarm av kollagen.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubrik: 35.04 eller 39.17.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).

LAND
Förlaga COL Kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
Del II:
(1) Stryk det som inte är tillämpligt.
— Underskriften och stämpeln ska ha en annan färg än övriga uppgifter i intyget.
Officiell veterinär
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL V
FÖRLAGA TILL INTYG FÖR IMPORT AV RÅVAROR FÖR FRAMSTÄLLNING AV GELATIN/KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL (1)
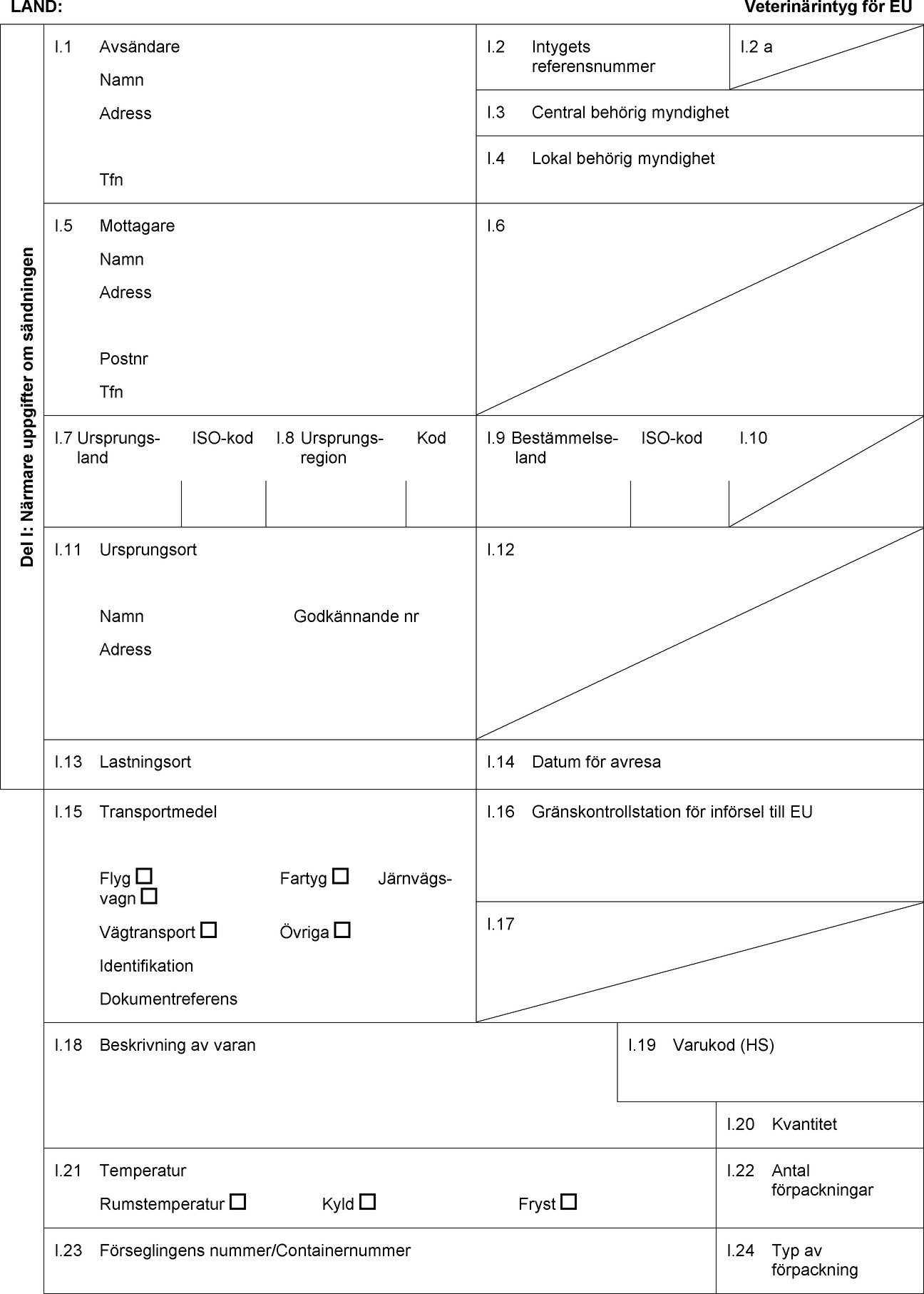
LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8 Ursprungs-region
Kod
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägs-vagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Framställning av gelatin/kollagen avsett att användas som livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Typ av vara
Godkännande-nummer för anläggningar
Tillverkningsan-läggning
Antal förpackningar
Nettovikt

LAND
Förlaga RCG Råvaror för framställning av gelatin/ kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1), Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och Europaparlamentets och rådets förordning (EG) nr 854/2004 av den 29 april 2004 om fastställande av särskilda bestämmelser för genomförandet av offentlig kontroll av produkter av animaliskt ursprung avsedda att användas som livsmedel (EUT L 139, 30.4.2004, s. 206) och att de ovan beskrivna råvarorna uppfyller kraven i dessa förordningar, särskilt när det gäller följande:
— (1) [De ben, hudar och skinn från tama och hägnade idisslare, svin och fjäderfä samt de ligament och senor som beskrivs ovan härrör från djur som har slaktats på ett slakteri och vars slaktkroppar vid en besiktning före och efter slakt har befunnits tjänliga som livsmedel.]
och/eller
— (1) [De hudar, skinn och ben från frilevande vilt som beskrivs ovan härrör från nedlagda djur vars slaktkroppar vid en besiktning efter slakt har befunnits tjänliga som livsmedel.]
och/eller
— (1) [De fiskskinn och fiskben som beskrivs ovan härrör från anläggningar som tillverkar fiskeriprodukter avsedda att användas som livsmedel och är godkända för export.]
(1) och
[Om råvarorna kommer från idisslare, med undantag för hudar och skinn från idisslare, ska dessutom följande gälla:
(1) antingen
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i Europaparlamentets och rådets förordning (EG) nr 999/2001 av den 22 maj 2001 om fastställande av bestämmelser för förebyggande, kontroll och utrotning av vissa typer av transmissibel spongiform encefalopati (EGT L 147, 31.5.2001, s. 1) har klassificerats som ett land eller en region med försumbar BSE-risk.
— De djur från vilka råvarorna från nötkreatur, får och getter härrör är födda, oavbrutet uppfödda och slaktade i landet med försumbar BSE-risk och har genomgått besiktning före och efter slakt.
— Om det har förekommit inhemska fall av BSE i landet eller regionen
i) föddes djuren efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, eller
ii) innehåller råvarorna från nötkreatur, får och getter inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk.
— De djur från vilka råvarorna från nötkreatur, får och getter härrör har genomgått besiktning före och efter slakt.
Del II: Intyg

LAND
Förlaga RCG Råvaror för framställning av gelatin/ kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
— De djur från vilka råvarorna från nötkreatur, får och getter som är avsedda för export härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Råvarorna från nötkreatur, får och getter innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med försumbar BSE-risk.
— De djur från vilka råvarorna från nötkreatur, får och getter härrör har genomgått besiktning före och efter slakt.
— Råvarorna från nötkreatur, får och getter som är avsedda för export härrör både från djur som är födda, oavbrutet uppfödda och slaktade i ett land eller en region med försumbar BSE-risk i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 och som, om det har förekommit inhemska fall av BSE i landet eller regionen, är födda efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, och från djur som är födda i ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk, och dessa djur har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Råvarorna från nötkreatur, får och getter innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med ej fastställd BSE-risk.
— De djur från vilka råvarorna från nötkreatur, får och getter härrör har inte utfodrats med kött- och benmjöl eller fettgrevar från idisslare och har genomgått besiktning före och efter slakt.
— De djur från vilka råvarorna från nötkreatur, får och getter härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— Råvarorna från nötkreatur, får och getter härrör inte från
i) specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001,
ii) nerv- och lymfvävnad som frilagts under urbeningen,
iii) maskinurbenat kött från ben från nötkreatur, får eller getter.]]

LAND
Förlaga RCG Råvaror för framställning av gelatin/ kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
(1) [II.2 Djurhälsointyg
I egenskap av officiell veterinär intygar jag följande om de råvaror som beskrivs ovan:
II.2.1 De består av animaliska produkter som uppfyller de djurhälsokrav som anges nedan.
II.2.2 De har erhållits i området [ ] (1) eller [ ] (2) (3) (4) från
(1) antingen [II.2.2.1 djur som kommer från anläggningar och som har vistats i detta område sedan födseln eller åtminstone under de sista tre månaderna före slakt och för vilka följande gäller:
(1) antingen [i) De är av de arter som avses i kommissionens förordning (EU) nr 206/2010 av den 12 mars 2010 om fastställande av förteckningar över tredjeländer, områden eller delar därav från vilka det är tillåtet att föra in vissa djur och färskt kött till Europeiska unionen samt kraven för veterinärintyg (EUT L 73, 20.3.2010, s. 1), de uppfyller alla relevanta djurhälsokrav vid import enligt den förordningen och de slaktades för att användas som livsmedel vid en tidpunkt då import till Europeiska unionen av färskt kött från djur av dessa arter var tillåten från landet eller området därav i enlighet med kolumn 8 i del 1 i bilaga II till den förordningen.]
(1) eller [ii) De är av de arter som avses i kommissionens förordning (EG) nr 119/2009 av den 9 februari 2009 om fastställande av en förteckning över tredjeländer och delar av tredjeländer för import till eller transitering genom gemenskapen av kött av vilda harar och kaniner, vissa vilda landlevande däggdjur och hägnade kaniner samt om kraven för veterinärintyg (EUT L 39, 10.2.2009, s. 12) och de uppfyller alla relevanta djurhälsokrav vid import enligt den förordningen.]]
(1) eller [II.2.2.1 fjäderfä som har vistats i det området sedan kläckningen eller som har importerats som dagsgamla kycklingar eller slaktfjäderfän från ett tredjeland/tredjeländer som förtecknas för denna vara i del 1 i bilaga I till kommissionens förordning (EG) nr 798/2008 av den 8 augusti 2008 om fastställande av en förteckning över tredjeländer, områden, zoner eller delområden från vilka fjäderfä och fjäderfäprodukter får importeras till och transiteras genom gemenskapen samt kraven för veterinärintyg (EUT L 226, 23.8.2008, s. 1) under villkor som minst motsvarar villkoren i den förordningen och som härrör från de arter som anges i den förordningen samt uppfyller alla relevanta djurhälsokrav vid import enligt den förordningen, och de slaktades för att användas som livsmedel vid en tidpunkt då import till Europeiska unionen av färskt kött från djur av dessa arter var tillåten från landet eller området därav i enlighet med kolumn 6 B i del 1 i bilaga I till den förordningen.]
(1) eller [II.2.2.1 djur som har nedlagts i vilt tillstånd inom detta område (5), samt fångats in och nedlagts inom ett område
i) i vilket det inom en radie av 25 km inte har förekommit något fall/utbrott av någon av följande sjukdomar för vilka djuren är mottagliga: mul- och klövsjuka, boskapspest, Newcastlesjuka eller högpatogen aviär influensa under de senaste 30 dagarna, eller klassisk svinpest eller afrikansk svinpest under de senaste 40 dagarna, och
ii) som är beläget minst 20 km från gränsen till ett annat område i ett land eller en del därav från vilket det vid tidpunkten i fråga inte är tillåtet att exportera dessa råvaror till Europeiska unionen, och
iii) där djuren inom tolv timmar efter nedläggning transporterades för kylning antingen till en uppsamlingscentral och omedelbart därefter till en viltanläggning, eller direkt till en viltanläggning.]

LAND
Förlaga RCG Råvaror för framställning av gelatin/ kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
II.2.3 De har erhållits på en anläggning där det inom en radie på 10 km inte har förekommit något fall/utbrott av någon av följande sjukdomar för vilka djuren är mottagliga: mul- och klövsjuka, boskapspest, Newcastlesjuka, högpatogen aviär influensa, klassisk svinpest eller afrikansk svinpest under de senaste 30 dagarna, eller om sjukdomsfall har förekommit har beredning av råvaror för export till Europeiska unionen tillåtits först efter det att allt kött har avlägsnats och anläggningen har genomgått fullständig rengöring och desinfektion under överinseende av en officiell veterinär.
II.2.4 De har erhållits och beretts utan att komma i kontakt med andra råvaror som inte uppfyller villkoren ovan, och de har hanterats för att förhindra kontaminering med patogena agens.
II.2.5 De har transporterats i rena och förseglade containrar eller lastbilar.]
Anmärkningar
Del I:
— Fält I.8: Ange områdets beteckning enligt bilaga II till kommissionens beslut 2006/766/EG av den 6 november 2006 om fastställande av en förteckning över de tredjeländer och delar av tredjeländer från vilka import av musslor, tagghudingar, manteldjur, marina snäckor och fiskeriprodukter är tillåten (EUT L 320, 18.11.2006, s. 53) och/eller del 1 i bilaga I till förordning (EG) nr 798/2008 eller i del 1 i bilaga I till förordning (EG) nr 119/2009 och/eller del 1 i bilaga II till förordning (EU) nr 206/2010.
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress. I tillämpliga fall registrerings- eller godkännandenummer.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubriker: 02.08, 03.05, 05.05, 05.06, 05.11.91, 05.11.99, 41.01, 41.02, 41.03.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).
— Fält I.28: Typ av vara: Hudar, skinn, ben, ligament och senor.
Godkännandenummer för anläggningar: I tillämpliga fall registrerings- eller godkän-nandenummer.
Tillverkningsanläggning: Innefattar slakteri, fabriksfartyg, styckningsanläggning, vilt-hanteringsanläggning och bearbetningsanläggning.
Del II:
(1) Stryk det som inte är tillämpligt. När det gäller produkter som härrör från fiskeriprodukter bör hela avsnitt II.2 strykas.
(2) Det exporterande landets eller områdets eller den exporterande zonens namn och ISO-kod enligt bestämmelserna i
— bilagorna till beslut 2006/766/EG,
— bilaga I till förordning (EG) nr 798/2008,

LAND
Förlaga RCG Råvaror för framställning av gelatin/ kollagen avsett att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
— del 1 i bilaga II till förordning (EG) nr 119/2009,
— del 1 i bilaga II till förordning (EU) nr 206/2010.
(3) Om delar av råvarorna härrör från djur som härrör från ett (annat) av de tredjeländer som förtecknas i bilaga II till förordning (EU) nr 206/2010 för import av den varan till unionen, anges koden/koderna för landet/länderna eller området/områdena och för det tredjeland där djuren slaktas (råvarorna får inte komma från ett land eller område som har tilläggsgaranti A eller F enligt kolumn 5 i den bilagan).
(4) Om råvarorna härrör från slaktfjäderfä som härrör från ett (annat) av de tredjeländer som förtecknas i del 1 i bilaga I till förordning (EG) nr 798/2008 för import av den varan till unionen, anges koden/koderna för landet/länderna eller området/områdena och för det tredjeland där fjäderfäna slaktas.
(5) Gäller endast länder från vilka det är tillåtet att importera viltkött avsett att användas som livsmedel av samma djurart till Europeiska unionen.
— Underskriften och stämpeln ska ha en annan färg än den tryckta texten.
OBS: Meddelande till person med ansvar för sändningen i EU: Detta intyg är avsett endast för veterinära ändamål och ska åtfölja sändningen till dess att den når gränskontrollstationen. Sändningen ska transporteras direkt till den mottagande tillverkningsanläggningen.
Officiell veterinär
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL VI
FÖRLAGA TILL INTYG FÖR IMPORT AV BEHANDLADE RÅVAROR FÖR FRAMSTÄLLNING AV GELATIN/KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL
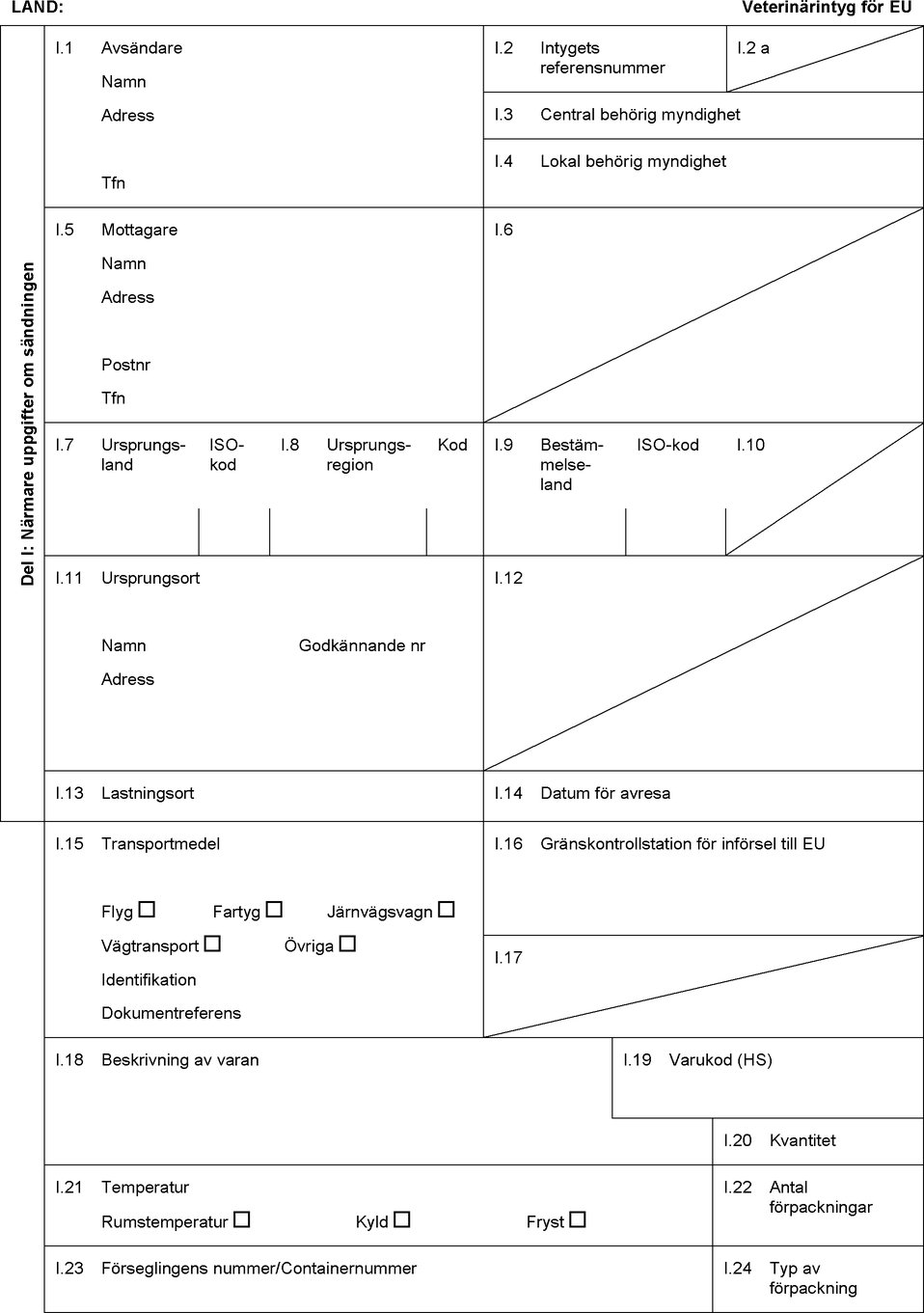
LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8 Ursprungs-region
Kod
I.9 Bestäm-melse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Framställning av gelatin/kollagen avsett att användas som livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Typ av vara
Godkännandenum-mer för anläggningar
Tillverkningsanlägg-ning
Antal förpackningar
Nettovikt

LAND
Förlaga TCG Behandlade råvaror för framställning av gelatin och kollagen
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att de behandlade råvaror som beskrivs ovan uppfyller följande krav:
— De härrör från anläggningar som står under den behöriga myndighetens kontroll och har förtecknats av den.
och
— (1) [De ben, hudar och skinn från tama och hägnade idisslare, svin och fjäderfä som beskrivs ovan härrör från djur som har slaktats på ett slakteri och vars slaktkroppar vid en besiktning före och efter slakt har befunnits tjänliga som livsmedel.]
(1) och/eller
— [De hudar, skinn och ben från frilevande vilt som beskrivs ovan härrör från nedlagda djur vars slaktkroppar vid en besiktning efter slakt har befunnits tjänliga som livsmedel.]
(1) och/eller
— [De fiskskinn och fiskben som beskrivs ovan härrör från anläggningar som tillverkar fiskeriprodukter avsedda att användas som livsmedel och är godkända för export.]
och
(1) antingen [De är torkade ben från nötkreatur, får, getter, svin och hästdjur, såväl hägnade som frilevande, samt fjäderfä, inklusive ratiter och fjädervilt, för framställning av kollagen eller gelatin, och de härrör från friska djur som slaktats i ett slakteri och de har behandlats enligt följande:
(1) antingen [Fördelning till bitar på ca 15 mm och avfettning med hett vatten med en minimitemperatur på 70 °C i minst 30 minuter, på 80 °C i minst 15 minuter eller på 90 °C i minst 10 minuter, avskiljning och därefter tvättning och torkning i minst 20 minuter i en ström av varmluft med en ingångstemperatur på minst 350 °C eller i 15 minuter i en ström av varmluft med en ingångstemperatur på över 700 °C.]
(1) eller [Soltorkning i minst 42 dagar vid en genomsnittstemperatur på minst 20 °C.]
(1) eller [Syrabehandling som säkerställer att pH-värdet är lägre än 6 i hela materialet i minst en timme före torkning.]]
(1) eller [De är hudar och skinn från hägnade idisslare, svinhudar, skinn från fjäderfä eller hudar och skinn från frilevande vilt, och de härrör från friska djur och de har behandlats enligt följande:
(1) antingen [Alkalibehandling som säkerställer att pH-värdet är högre än 12 i hela materialet och därefter saltning i minst sju dagar.]
(1) eller [Torkning i minst 42 dagar vid en temperatur på minst 20 °C.]
(1) eller [Syrabehandling som säkerställer att pH-värdet är lägre än 5 i hela materialet i minst en timme.]
(1) eller [Alkalibehandling som säkerställer att pH-värdet är högre än 12 i hela materialet i minst åtta timmar.]]
(1) eller [De är sådana ben, hudar och skinn från hägnade idisslare, svinhudar, skinn från fjäderfä, fiskskinn samt hudar och skinn från frilevande vilt från tredjeländer, delar av tredjeländer och områden som avses i del IV i bilaga I till den här förordningen som har genomgått någon annan behandling än de som förtecknas ovan och som kommer från anläggningar som är registrerade eller godkända enligt förordning (EG) nr 852/2004 eller (EG) nr 853/2004,
och
(1) [om råvarorna kommer från idisslare, med undantag för hudar och skinn från idisslare, ska dessutom följande gälla:
Del II: Intyg

LAND
Förlaga TCG Behandlade råvaror för framställning av gelatin och kollagen
II. Hälsoinformation
II a Intygets referensnummer
II b
(1) antingen
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i Europaparlamentets och rådets förordning (EG) nr 999/2001 av den 22 maj 2001 om fastställande av bestämmelser för förebyggande, kontroll och utrotning av vissa typer av transmissibel spongiform encefalopati (EGT L 147, 31.5.2001, s. 1) har klassificerats som ett land eller en region med försumbar BSE-risk.
— De djur från vilka de behandlade råvarorna från nötkreatur, får och getter härrör är födda, oavbrutet uppfödda och slaktade i landet med försumbar BSE-risk och har genomgått besiktning före och efter slakt.
— Om det har förekommit inhemska fall av BSE i landet eller regionen
i) föddes djuren efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, eller
ii) innehåller de behandlade råvarorna från nötkreatur, får och getter inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk.
— De djur från vilka de behandlade råvarorna från nötkreatur, får och getter härrör har genomgått besiktning före och efter slakt.
— De djur från vilka de behandlade råvarorna från nötkreatur, får och getter som är avsedda för export härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— De behandlade råvarorna från nötkreatur, får och getter innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med försumbar BSE-risk.
— De djur från vilka de behandlade råvarorna från nötkreatur, får och getter härrör har genomgått besiktning före och efter slakt.
— De behandlade råvarorna från nötkreatur, får och getter som är avsedda för export härrör både från djur som är födda, oavbrutet uppfödda och slaktade i ett land eller en region med försumbar BSE-risk i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 och som, om det har förekommit inhemska fall av BSE i landet eller regionen, är födda efter det att förbudet mot utfodring av idisslare med kött- och benmjöl och fettgrevar som härrör från idisslare började gälla, och från djur som är födda i ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med kontrollerad BSE-risk, och dessa djur har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.

LAND
Förlaga TCG Behandlade råvaror för framställning av gelatin och kollagen
II. Hälsoinformation
II a Intygets referensnummer
II b
— De behandlade råvarorna från nötkreatur, får och getter innehåller inte och härrör inte från specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001, eller maskinurbenat kött från ben av nötkreatur, får och getter.]
(1) eller
— [De kommer från ett land eller en region som i enlighet med artikel 5.2 i förordning (EG) nr 999/2001 har klassificerats som ett land eller en region med ej fastställd BSE-risk.
— De djur från vilka de behandlade råvarorna från nötkreatur, får och getter härrör har inte utfodrats med kött- och benmjöl eller fettgrevar från idisslare och har genomgått besiktning före och efter slakt.
— De djur från vilka de behandlade råvarorna från nötkreatur, får och getter härrör har inte slaktats efter bedövning genom insprutning av gas i hjärnskålen eller avlivats med samma metod och heller inte slaktats efter bedövning genom laceration av vävnad i centrala nervsystemet med ett avlångt, stavformigt instrument som förs in i hjärnskålen.
— De behandlade råvarorna från nötkreatur, får och getter härrör inte från
i) specificerat riskmaterial enligt definitionen i bilaga V till förordning (EG) nr 999/2001,
ii) nerv- och lymfvävnad som frilagts under urbeningen,
iii) maskinurbenat kött från ben från nötkreatur, får eller getter.]]]
(1) [II.2 Djurhälsointyg
I egenskap av officiell veterinär intygar jag följande om de behandlade råvaror som beskrivs ovan:
II.2.1 De består av animaliska produkter som uppfyller de djurhälsokrav som anges nedan.
II.2.2 De har erhållits i området (1) [ ] (1) eller [ ] (2) (3).
II.2.3 De har erhållits och beretts utan att komma i kontakt med andra råvaror som inte uppfyller villkoren ovan, och de har hanterats för att förhindra kontaminering med patogena agens.
II.2.4 De har transporterats i rena och förseglade containrar eller lastbilar.]
Anmärkningar
Del I:
— Fält I.8: Områdets beteckning enligt bilaga II till kommissionens beslut 2006/766/EG av den 6 november 2006 om fastställande av en förteckning över de tredjeländer och delar av tredjeländer från vilka import av musslor, tagghudingar, manteldjur, marina snäckor och fiskeriprodukter är tillåten (EUT L 320, 18.11.2006, s. 53) eller del 1 i bilaga I till kommissionens förordning (EG) nr 798/2008 av den 8 augusti 2008 om fastställande av en förteckning över tredjeländer, områden, zoner eller delområden från vilka fjäderfä och fjäderfäprodukter får importeras till och transiteras genom gemenskapen samt kraven för veterinärintyg (EUT L 226, 23.8.2008, s. 1) eller del 1 i bilaga I till kommissionens förordning (EG) nr 119/2009 av den 9 februari 2009 om fastställande av en förteckning över tredjeländer och delar av tredjeländer för import till eller transitering genom gemenskapen av kött av vilda harar och kaniner, vissa vilda landlevande däggdjur och hägnade kaniner samt om kraven för veterinärintyg (EUT L 39, 10.2.2009, s. 12) eller del 1 i bilaga II till kommissionens förordning (EU) nr 206/2010 av den 12 mars 2010 om fastställande av förteckningar över tredjeländer, områden eller delar därav från vilka det är tillåtet att föra in vissa djur och färskt kött till Europeiska unionen samt kraven för veterinärintyg (EUT L 73, 20.3.2010, s. 1).
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress samt godkännandenummer eller i tillämpliga fall det identifieringsnummer som den behöriga myndigheten tilldelat anläggningen.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.

LAND
Förlaga TCG Behandlade råvaror för framställning av gelatin och kollagen
II. Hälsoinformation
II a Intygets referensnummer
II b
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubriker: 03.05, 05.05, 05.06, 05.11.91, 05.11.99, 41.01, 41.02, 41.03.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).
— Fält I.28: Typ av vara: Hudar, skinn, ben, ligament och senor.
Godkännandenummer för anläggningar: Godkännandenummer eller i tillämpliga fall det identifieringsnummer som den behöriga myndigheten tilldelat anläggningen.
Tillverkningsanläggning: Innefattar slakteri, fabriksfartyg, styckningsanläggning, vilt-hanteringsanläggning och bearbetningsanläggning.
Godkännandenummer: I tillämpliga fall.
Del II:
(1) Stryk det som inte är tillämpligt. När det gäller produkter som härrör från fiskeriprodukter bör hela avsnitt II.2 strykas.
(2) Det exporterande landets eller områdets eller den exporterande zonens namn och ISO-kod enligt bestämmelserna i
— del 1 i bilaga II till förordning (EU) nr 206/2010,
— bilaga I till förordning (EG) nr 798/2008,
— del 1 i bilaga II till förordning (EG) nr 119/2009.
(3) Om delar av råvarorna härrör från djur som härrör från ett (annat) av de tredjeländer som förtecknas i bilaga I till kommissionens genomförandeförordning (EU) 2016/759 av den 28 april 2016 om upprättande av förteckningar över tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta införsel till unionen av vissa produkter av animaliskt ursprung avsedda att användas som livsmedel, om fastställande av intygskrav, om ändring av förordning (EG) nr 2074/2005 och om upphävande av beslut 2003/812/EG (EUT L 126, 14.5.2016, s. 13) anges koden/koderna för landet/länderna eller området/områdena.
— Underskriften och stämpeln ska ha en annan färg än den tryckta texten.
OBS: Meddelande till person med ansvar för sändningen i EU: Detta intyg är avsett endast för veterinära ändamål och ska åtfölja sändningen till dess att den når gränskontrollstationen. Sändningen ska transporteras direkt till den mottagande tillverkningsanläggningen.
— Transporttiden får ingå i behandlingstidens längd.
Officiell veterinär
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL VII
FÖRLAGA TILL INTYG FÖR IMPORT AV HONUNG, BIDROTTNINGGELÉ OCH ANDRA BIODLINGSPRODUKTER AVSEDDA ATT ANVÄNDAS SOM LIVSMEDEL
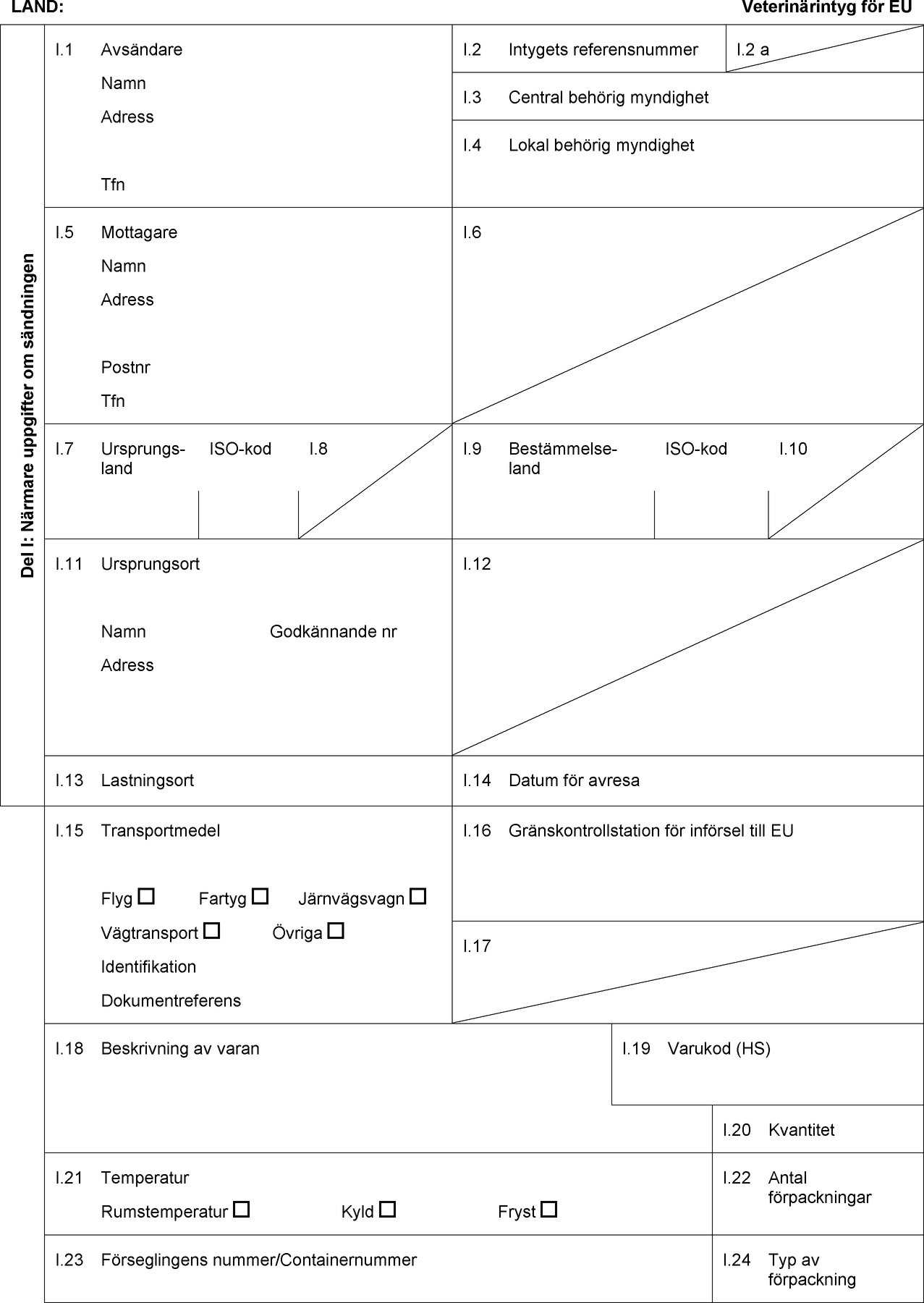
LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Typ av behandling
Godkännandenum-mer för anläggningar
Tillverkningsanlägg-ning
Antal förpackningar
Nettovikt

LAND
Förlaga HON Honung, bidrottninggelé och andra biodlingsprodukter
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1) och Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och att den ovan beskrivna honungen och bidrottninggelén och de ovan beskrivna andra biodlingsprodukterna har producerats i enlighet med kraven i dessa förordningar, särskilt när det gäller följande:
— De kommer från en anläggning (anläggningar) som genomför ett program grundat på HACCP-principerna i enlighet med förordning (EG) nr 852/2004.
— De har hanterats och, i förekommande fall, beretts, emballerats och lagrats under hygieniska förhållanden i enlighet med kraven i bilaga II till förordning (EG) nr 852/2004.
— De uppfyller de garantier för levande djur och produkter framställda av dessa som föreskrivs i de program för påvisande av restsubstanser som lämnats in enligt rådets direktiv 96/23/EG av den 29 april 1996 om införande av kontrollåtgärder för vissa ämnen och restsubstanser av dessa i levande djur och i produkter framställda därav och om upphävande av direktiv 85/358/EEG och 86/469/EEG samt beslut 89/187/EEG och 91/664/EEG (EGT L 125, 23.5.1996, s. 10), särskilt artikel 29.
Anmärkningar
Del I:
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress. Godkännandenummer innebär registreringsnummer.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubriker: 04.09, 04.10.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).
— Fält I.28: Typ av behandling: Ange sonikering, homogenisering, ultrafiltrering, pastörisering eller ingen värmebehandling.
Godkännandenummer för anläggningar: Godkännandenummer eller i tillämpliga fall det identifieringsnummer som den behöriga myndigheten tilldelat anläggningen.
Del II:
— Underskriften och stämpeln ska ha en annan färg än övriga uppgifter i intyget.
Del II: Intyg
Officiell inspektör
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
DEL VIII
FÖRLAGA TILL INTYG FÖR IMPORT AV HÖGFÖRÄDLAT KONDROITINSULFAT, HÖGFÖRÄDLAD HYALURONSYRA, HÖGFÖRÄDLADE ANDRA HYDROLYSERADE BROSKPRODUKTER, HÖGFÖRÄDLAT KITOSAN, GLUKOSAMIN, LÖPE OCH HUSBLOSS SAMT HÖGFÖRÄDLADE AMINOSYROR AVSEDDA ATT ANVÄNDAS SOM LIVSMEDEL

LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6
I.7 Ursprungs-land
ISO-kod
I.8
I.9 Bestämmelse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn Godkännande nr
Adress
I.12
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning
I.25 Varorna intygas vara avsedda som/för:
Livsmedel
I.26
I.27 För import och införsel till EU
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Framställningsda-tum
(dd/mm/åååå)
Godkännandenum-mer för anläggningar
Tillverkningsanlägg-ning
Antal förpackningar
Nettovikt

LAND
Förlaga HRP Högförädlat kondroitinsulfat, högförädlad hyaluronsyra, högförädlade andra hydrolyserade broskprodukter, högförädlat kitosan, glukosamin, löpe och husbloss samt högförädlade aminosyror avsedda att användas som livsmedel
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Folkhälsointyg
Jag intygar att jag är förtrogen med de tillämpliga bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 178/2002 av den 28 januari 2002 om allmänna principer och krav för livsmedelslagstiftning, om inrättande av Europeiska myndigheten för livsmedelssäkerhet och om förfaranden i frågor som gäller livsmedelssäkerhet (EGT L 31, 1.2.2002, s. 1), Europaparlamentets och rådets förordning (EG) nr 852/2004 av den 29 april 2004 om livsmedelshygien (EUT L 139, 30.4.2004, s. 1) och Europaparlamentets och rådets förordning (EG) nr 853/2004 av den 29 april 2004 om fastställande av särskilda hygienregler för livsmedel av animaliskt ursprung (EUT L 139, 30.4.2004, s. 55) och att de ovan beskrivna högförädlade produkterna har producerats i enlighet med kraven i dessa förordningar, särskilt när det gäller följande:
— De kommer från en anläggning (anläggningar) som genomför ett program grundat på HACCP-principerna i enlighet med förordning (EG) nr 852/2004.
— De har hanterats och, i förekommande fall, beretts, emballerats och lagrats under hygieniska förhållanden i enlighet med kraven i bilaga II till förordning (EG) nr 852/2004.
— De uppfyller kraven i avsnitt XVI i bilaga III till förordning (EG) nr 853/2004.
— (1) [När det gäller aminosyror
i) har människohår inte använts vid tillverkningen, och
ii) de uppfyller bestämmelserna i Europaparlamentets och rådets förordning (EG) nr 1333/2008 av den 16 december 2008 om livsmedelstillsatser (EUT L 354, 31.12.2008, s. 16).
Anmärkningar
Del I:
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Särskilda uppgifter ska lämnas vid eventuell ur- och omlastning.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubrik: 21.06.90, 29.22, 29.30, 29.32, 35.07, 35.03 eller 39.13.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: Identifiering av container/förseglingsnummer (i tillämpliga fall).
Del II:
(1) Stryk det som inte är tillämpligt.
— Underskriften och stämpeln ska ha en annan färg än övriga uppgifter i intyget.
Del II: Intyg
Officiell veterinär Namn (med versaler):
Befattning och titel:
Datum: Underskrift:
Stämpel:
(1) Om de inte omfattas av del VI.
BILAGA III
FÖRLAGA TILL INTYG FÖR TRANSITERING GENOM UNIONEN, ANTINGEN DIREKT ELLER EFTER LAGRING, AV RÅVAROR ELLER BEHANDLADE RÅVAROR FÖR FRAMSTÄLLNING AV GELATIN/KOLLAGEN AVSETT ATT ANVÄNDAS SOM LIVSMEDEL

LAND:
Veterinärintyg för EU
Del I: Närmare uppgifter om sändningen
I.1 Avsändare
Namn
Adress
Tfn
I.2 Intygets referensnummer
I.2 a
I.3 Central behörig myndighet
I.4 Lokal behörig myndighet
I.5 Mottagare
Namn
Adress
Postnr
Tfn
I.6 Person med ansvar för sändningen i EU
Namn
Adress
Postnr
Tfn
I.7 Ursprungs-land
ISO-kod
I.8 Ursprungs-region
Kod
I.9 Bestäm-melse-land
ISO-kod
I.10
I.11 Ursprungsort
Namn
Adress
I.12 Bestämmelseort
Tullager Leverantör till fartyg
Namn Godkännande nr
Adress
Postnr
I.13 Lastningsort
I.14 Datum för avresa
I.15 Transportmedel
Flyg Fartyg Järnvägsvagn
Vägtransport Övriga
Identifikation
Dokumentreferens
I.16 Gränskontrollstation för införsel till EU
I.17
I.18 Beskrivning av varan
I.19 Varukod (HS)
I.20 Kvantitet
I.21 Temperatur
Rumstemperatur Kyld Fryst
I.22 Antal förpackningar
I.23 Förseglingens nummer/Containernummer
I.24 Typ av förpackning

I.25 Varorna intygas vara avsedda som/för:
Framställning av gelatin/kollagen avsett att användas som livsmedel
I.26 För transit till tredjeland i förh. till EU
Tredjeland ISO-kod
I.27
I.28 Identifiering av varorna
Arter
(Vetenskapligt namn)
Tillverkningsanläggning
Antal förpackningar
Nettovikt

LAND
Förlaga TRANSITERING/LAGRING
II. Hälsoinformation
II a Intygets referensnummer
II b
II.1 Djurhälsointyg
I egenskap av officiell veterinär intygar jag följande om de råvaror eller behandlade råvaror som beskrivs i del I:
II.1.1 De kommer från ett land eller ett område som godkänts för import till unionen enligt del 1 i bilaga I till kommissionens förordning (EG) nr 798/2008 av den 8 augusti 2008 om fastställande av en förteckning över tredjeländer, områden, zoner eller delområden från vilka fjäderfä och fjäderfäprodukter får importeras till och transiteras genom gemenskapen samt kraven för veterinärintyg (EUT L 226, 23.8.2008, s. 1) eller kommissionens förordning (EG) nr 119/2009 av den 9 februari 2009 om fastställande av en förteckning över tredjeländer och delar av tredjeländer för import till eller transitering genom gemenskapen av kött av vilda harar och kaniner, vissa vilda landlevande däggdjur och hägnade kaniner samt om kraven för veterinärintyg (EUT L 39, 10.2.2009, s. 12) eller del 1 i bilaga II till kommissionens förordning (EU) nr 206/2010 av den 12 mars 2010 om fastställande av förteckningar över tredjeländer, områden eller delar därav från vilka det är tillåtet att föra in vissa djur och färskt kött till Europeiska unionen samt kraven för veterinärintyg (EUT L 73, 20.3.2010, s. 1).
II.1.2 De uppfyller de relevanta djurhälsovillkoren i förlagan till djurhälsointyg i del V eller VI i bilaga II till kommissionens genomförandeförordning (EU) 2016/759 av den 28 april 2016 om upprättande av förteckningar över tredjeländer, delar av tredjeländer och områden från vilka medlemsstaterna ska tillåta införsel till unionen av vissa produkter av animaliskt ursprung avsedda att användas som livsmedel, om fastställande av intygskrav, om ändring av förordning (EG) nr 2074/2005 och om upphävande av beslut 2003/812/EG (EUT L 126, 14.5.2016, s. 13).
Anmärkningar
Detta intyg är avsett för transitering och lagring i enlighet med artikel 12.4 eller 13 i rådets direktiv 97/78/EG av den 18 december 1997 om principerna för organisering av veterinärkontroller av produkter från tredje land som förs in i gemenskapen (EGT L 24, 30.1.1998, s. 9) av råvaror eller behandlade råvaror för framställning av gelatin/kollagen avsett som livsmedel från
1. tamdjur av nötkreatur (inklusive arter av Bison och Bubalus samt korsningar av dessa),
2. tamfår (Ovis aries) eller tamget (Capra hircus),
3. tamsvin (Sus scrofa),
4. tama hästdjur (Equus caballus, Equus asinus samt korsningar av dessa),
5. hägnade icke-domesticerade djur av ordningen Artiodactyla (utom nötkreatur [inklusive arter av Bison och Bubalus samt korsningar av dessa], Ovis aries, Capra hircus, Suidae och Tayassuidae) och av familjerna Rhinocerotidae och Elephantidae,
6. frilevande icke-domesticerade djur av ordningen Artiodactyla (utom nötkreatur [inklusive arter av Bison och Bubalus samt korsningar av dessa], Ovis aries, Capra hircus, Suidae och Tayassuidae) och av familjerna Rhinocerotidae och Elephantidae,
7. hägnade icke-domesticerade djur av familjerna Suidae, Tayassuidae eller Tapiridae,
8. frilevande icke-domesticerade djur av familjerna Suidae, Tayassuidae eller Tapiridae,
9. frilevande hästdjur av undersläktet Hippotigris (zebra),
10. frilevande harar och kaniner (Leporidae),
11. andra frilevande landlevande däggdjur än hov- och klövdjur, harar och kaniner,
12. hägnade kaniner,
13. fjäderfä,
14. hägnade ratiter,
15. frilevande vilt,
16. fisk.
Del II: Intyg

LAND
Förlaga TRANSITERING/LAGRING
II. Hälsoinformation
II a Intygets referensnummer
II b
Del I:
— Fält I.8: Områdets beteckning enligt del 1 i bilaga II till förordning (EU) nr 206/2010 eller del 1 i bilaga I till förordning (EG) nr 119/2009 eller del 1 i bilaga I till förordning (EG) nr 798/2008 eller bilaga II till kommissionens beslut 2006/766/EG av den 6 november 2006 om fastställande av en förteckning över de tredjeländer och delar av tredjeländer från vilka import av musslor, tagghudingar, manteldjur, marina snäckor och fiskeriprodukter är tillåten (EUT L 320, 18.11.2006, s. 53).
— Fält I.11: Ursprungsort: Den avsändande anläggningens namn och adress.
— Fält I.12: Adress (och godkännandenummer om det är känt) till ett lager i en frizon, ett frilager, ett tullager eller en skeppshandlare.
— Fält I.15: Registreringsnummer (järnvägsvagn eller containrar och lastbilar), flightnummer (flyg) eller namn (fartyg). Vid eventuell ur- och omlastning ska avsändaren underrätta gränskontrollstationen för införsel till EU.
— Fält I.19: Ange lämplig kod enligt Harmoniserade systemet (HS) under följande rubrik: 02.08, 03.05, 05.04, 05.05, 05.06, 05.11.91, 05.11.99, 41.01, 41.02 eller 41.03.
— Fält I.20: Ange total bruttovikt och total nettovikt.
— Fält I.23: För containrar eller lådor anges även containerns nummer och (i tillämpliga fall) förseglingens nummer.
— Fält I.28: Tillverkningsanläggning: Ange anläggningens registreringsnummer, godkännandenummer eller i tillämpliga fall det identifieringsnummer som den behöriga myndigheten tilldelat anläggningen. Innefattar slakteri, fabriksfartyg, styckningsanläggning, vilthanteringsanläggning och bearbetningsanläggning.
Officiell veterinär eller officiell inspektör
Namn (med versaler): Befattning och titel:
Datum: Underskrift:
Stämpel:
BILAGA IV
ANVISNINGAR FÖR IFYLLANDE AV INTYG
(som avses i artiklarna 2.1 och 4.1)
|
a) |
Intyg ska utfärdas av det exporterande tredjelandet på grundval av förlagorna i bilagorna II och III, i enlighet med förlagan för respektive produkt av animaliskt ursprung. De ska innehålla, i den nummerordning som anges i förlagan, de intyganden som krävs för alla tredjeländer och, i tillämpliga fall, de tilläggsgarantier som krävs för det exporterande tredjelandet eller en del därav. Om bestämmelsemedlemsstaten kräver att de berörda produkterna av animaliskt ursprung ska uppfylla extra intygskrav, ska det i originalet till intyget även intygas att dessa krav uppfylls. |
|
b) |
Om det i intygsförlagan anges att ej tillämpliga förklaringar ska strykas, får intygsutfärdaren stryka över, parafera och stämpla förklaringar som inte är relevanta eller stryka dem ur intyget. |
|
c) |
Ett separat och unikt intyg ska utfärdas för de produkter av animaliskt ursprung som exporteras från ett område (områden) eller en zon (zoner) i samma exportland som förtecknas eller avses i bilaga I och som har samma bestämmelseort och transporteras i samma järnvägsvagn, lastbil, flygplan eller fartyg. |
|
d) |
Originalet till varje intyg ska bestå av ett enda blad eller, om mer text krävs, utformas på ett sådant sätt att alla blad som behövs utgör en enda odelbar enhet. |
|
e) |
Intyget ska vara avfattat på minst ett av de officiella språken i den medlemsstat där gränskontrollstationen för införsel av sändningen till EU är belägen och på minst ett av de officiella språken i bestämmelsemedlemsstaten. Dessa medlemsstater kan dock tillåta att intyget avfattas på det officiella språket i en annan medlemsstat och vid behov åtföljs av en officiell översättning. |
|
f) |
Om det för identifiering av varorna i sändningen (schemat i punkt I.28 i förlagan till intyg) bifogas ytterligare blad till intyget, ska även dessa blad betraktas som en del av originalintyget och intygsutfärdaren ska underteckna och stämpla på varje sida. |
|
g) |
Om intyget, med de ytterligare blad som avses i led f, består av mer än en sida, ska varje sida numreras – (sidans nummer) av (det totala antalet sidor) – längst ned på sidan, medan intygets referensnummer, som fastställts av den behöriga myndigheten, ska anges högst upp på sidan. |
|
h) |
Originalintyget ska fyllas i och undertecknas av en officiell veterinär eller av en annan utsedd officiell inspektör då detta föreskrivs i förlagan till intyg. De behöriga myndigheterna i det exporterande tredjelandet ska se till att de bestämmelser om utfärdande av intyg som följs är likvärdiga med dem som anges i rådets direktiv 96/93/EG (1). Underskriften ska ha en annan färg än den tryckta texten. Detta gäller även för stämplar, med undantag för präglade stämplar och vattenstämplar. |
|
i) |
Intygets referensnummer som anges i fälten I.2 och II a ska tilldelas av den behöriga myndigheten. |
(1) Rådets direktiv 96/93/EG av den 17 december 1996 om certifiering av djur och animaliska produkter (EGT L 13, 16.1.1997, s. 28).
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/63 |
KOMMISSIONENS GENOMFÖRANDEFÖRORDNING (EU) 2016/760
av den 13 maj 2016
om undantagsåtgärder till stöd för sektorn för ägg och fjäderfäkött i Italien
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DENNA FÖRORDNING
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av Europaparlamentets och rådets förordning (EU) nr 1308/2013 av den 17 december 2013 om upprättande av en samlad marknadsordning för jordbruksprodukter och om upphävande av rådets förordningar (EEG) nr 922/72, (EEG) nr 234/79, (EG) nr 1037/2001 och (EG) nr 1234/2007 (1), särskilt artikel 220.1 a, och
av följande skäl:
|
(1) |
Den 15 december 2014 bekräftade och anmälde Italien högpatogen aviär influensa av subtyp H5N8. Utbrottet av sjukdomen bekräftades i en kommersiell anläggning som håller slaktkalkoner av hankön i kommunen Porto Viro, provinsen Rovigo, regionen Venetien i Italien. |
|
(2) |
Italien vidtog snabbt och effektivt alla nödvändiga djurhälsoåtgärder och veterinära åtgärder som krävs i enlighet med rådets direktiv 2005/94/EG (2). |
|
(3) |
I synnerhet vidtog de italienska myndigheterna bekämpningsåtgärder, övervakningsåtgärder och förebyggande åtgärder och upprättade skydds- och övervakningszoner i enlighet med kommissionens genomförandebeslut 2014/936/EU (3). De kunde på så vis snabbt utplåna hotet. Unionens djurhälsoåtgärder, nationella djurhälsoåtgärder och veterinära åtgärder tillämpades fram till och med den 16 februari 2015 i samtliga anläggningar utom i anläggningar som håller slaktkalkoner av hankön, där åtgärder tillämpades fram till och med den 25 februari 2015. |
|
(4) |
Den 23 juni 2015 informerade de italienska myndigheterna kommissionen om att de nödvändiga djurhälsoåtgärder och veterinära åtgärder som vidtagits för att innesluta och utplåna virusets spridning hade påverkat vissa aktörer och att dessa drabbats av inkomstförluster som inte berättigar till ekonomiskt bidrag från unionen enligt Europaparlamentets och rådets förordning (EU) nr 652/2014 (4). |
|
(5) |
Den 23 juni 2015 mottog kommissionen en formell begäran från de italienska myndigheterna om medfinansiering av vissa undantagsåtgärder till stöd för marknaden i enlighet med artikel 220.3 i förordning (EU) nr 1308/2013. De italienska myndigheterna förtydligade sin begäran den 11 och 27 januari 2016. |
|
(6) |
Till följd av djurhälsoåtgärderna och de veterinära åtgärderna försenades utsläppandet av fåglar till anläggningar för slaktuppfödning av kapuner, majskycklingar, standardkycklingar och kalkoner i skydds- och övervakningszonerna, och en anläggning för avelskalkoner i sådana zoner kunde inte producera kläckägg. Detta ledde till en produktionsförlust av kött från kapuner, majskycklingar, standardkycklingar och kalkoner som föds upp för slakt och en produktionsförlust av kläckägg från avelskalkoner under den period då djurhälsoåtgärderna och de veterinära åtgärderna var i kraft. Förlusterna bör därför kompenseras. |
|
(7) |
Till följd av de djurhälsoåtgärder och sanitära åtgärder som tillämpades slaktades kycklingar med ursprung från flera anläggningar belägna i skyddszonen omedelbart och köttet från dessa kycklingar antingen värmebehandlades i enlighet med artikel 23 i direktiv 2005/94/EG eller frystes för att underlätta en gradvis försäljning av det frysta fjäderfäköttet i skyddszonen. Förlusterna på grund av skillnaden i värde mellan färskt fjäderfäkött och värmebehandlat eller fryst fjäderfäkött bör därför kompenseras. |
|
(8) |
I enlighet med artikel 220.5 i förordning (EU) nr 1308/2013 ska unionen medfinansiera motsvarande 50 % av Italiens utgifter för undantagsåtgärder till stöd för marknaden. De maximala kvantiteter som berättigar till finansiering för varje undantagsåtgärd till stöd för marknaden bör fastställas av kommissionen efter en granskning av Italiens begäran. |
|
(9) |
För att undvika risken för överkompensation bör ett schablonbelopp för medfinansiering fastställas på en lämplig nivå för varje produkt. |
|
(10) |
De arter som berörs är kycklingar (kapuner, majskycklingar och standardkycklingar) och kalkoner (båda könen) som föds upp för köttproduktion, kläckägg av kalkon och värmebehandlat eller fryst kycklingkött. |
|
(11) |
För att undvika risken för dubbelfinansiering bör förlusterna inte ha kompenserats genom statligt stöd eller försäkringar och unionens medfinansiering enligt denna förordning bör begränsas till stödberättigande produkter för vilka ekonomiskt stöd från unionen inte har erhållits enligt förordning (EU) nr 652/2014. |
|
(12) |
Omfattningen och varaktigheten av undantagsåtgärderna enligt denna förordning bör begränsas till vad som är absolut nödvändigt för att stödja marknaden i fråga. |
|
(13) |
För att garantera en sund budgetförvaltning för dessa exceptionella stödåtgärder bör endast de utbetalningar av stöd som Italien gjort till mottagarna senast den 30 september 2016 berättiga till medfinansiering från unionen. Artikel 5.2 i kommissionens delegerade förordning (EU) nr 907/2014 (5) bör inte tillämpas. |
|
(14) |
För att säkerställa att utbetalningarna är stödberättigande och korrekta bör de italienska myndigheterna göra förhandskontroller. |
|
(15) |
För att göra det möjligt för unionen att fullgöra sin ekonomiska kontroll bör de italienska myndigheterna lämna in räkenskapsavslutningen för betalningarna till kommissionen. |
|
(16) |
För att säkerställa att dessa åtgärder genomförs omedelbart av Italien, bör denna förordning träda i kraft dagen efter det att den har offentliggjorts. |
|
(17) |
De åtgärder som föreskrivs i denna förordning är förenliga med yttrandet från kommittén för den samlade marknadsordningen inom jordbruket. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
Unionen ska medfinansiera motsvarande 50 % av Italiens utgifter, för att stödja marknaden för kläckägg och fjäderfäkött som allvarligt drabbats av det utbrott av högpatogen aviär influensa av subtyp H5N8 som upptäcktes och anmäldes av Italien mellan den 15 december 2014 och med anledning av vilket unionens och nationella djurhälsoåtgärder och veterinära åtgärder var tillämpliga till och med den 16 februari 2015 på samtliga anläggningar utom anläggningar som håller slaktkalkoner av hankön, där åtgärderna tillämpades till och med den 25 februari 2015.
Utgifterna ska berättiga till medfinansiering från unionen endast om Italien har betalat ut stödet till stödmottagarna senast den 30 september 2016. Artikel 5.2 i delegerad förordning (EU) nr 907/2014 ska inte tillämpas.
Artikel 2
Den högsta nivån för unionens medfinansiering ska uppgå till följande:
|
a) |
För förlust av produktion av kläckägg av avelskalkoner inom övervakningszonen, ska ett schablonbelopp på 0,42 euro per kläckägg av kalkon enligt KN-nummer 0407 19 11 gälla för högst 313 560 stycken. |
|
b) |
För förlust av produktion av fjäderfäkött på grund av förseningar i samband med djurhälsoåtgärder och veterinära åtgärder avseende kapuner, majskycklingar, standardkycklingar och kalkoner av han- och honkön som föds upp för slakt på de anläggningar som är belägna i skydds- och övervakningszonerna, ska följande schablonbelopp gälla:
|
|
c) |
För förlust av värdet mellan färskt och värmebehandlat kycklingkött från standardkycklingar som omedelbart slaktades i skyddszonen, ska schablonbeloppet vara 0,3761 euro per kg levande vikt upp till ett totalt belopp på 98 297,50 euro. |
|
d) |
För förlust av värdet mellan färskt och fryst kycklingkött från standardkycklingar som omedelbart slaktades i skyddszonen, ska schablonbeloppet vara 0,04 euro per kg kycklingkött upp till ett totalt belopp på 3 402,44 euro. |
Artikel 3
Unionens medfinansiering i enlighet med denna förordning ska begränsas till produkter som inte ersätts genom statligt stöd eller försäkringar och för vilka inga ekonomiska bidrag från unionen har erhållits enligt förordning (EU) nr 652/2014.
Artikel 4
Innan stödet utbetalas ska Italien genomföra omfattande administrativa och fysiska kontroller för att säkerställa att denna förordning efterlevs.
De italienska myndigheterna ska kontrollera följande:
|
a) |
Att den stödmottagare som lämnat in ansökan om stöd är stödberättigad. |
|
b) |
För varje stödberättigad aktör: stödberättigandet, kvantitet och faktisk förlust av produktion av kläckägg av avelskalkoner. |
|
c) |
För varje stödberättigande aktör: stödberättigande, kvantitet och faktisk förlust av produktion av kyckling- och kalkonkött på grund av förseningar i utsläppandet på anläggningar belägna i skydds- och övervakningszonerna av kapuner, majskycklingar, standardkycklingar och kalkoner som föds upp för slakt, under den tid då djurhälsoåtgärderna och de veterinära åtgärderna tillämpades. |
|
d) |
För varje stödberättigande aktör: stödberättigande, kvantitet och faktisk förlust i värde mellan färskt och värmebehandlat kycklingkött från standardkycklingar som omedelbart slaktades i skyddszonen under den tid då djurhälsoåtgärderna och de veterinära åtgärderna tillämpades. |
|
e) |
För varje stödberättigad aktör: stödberättigande, kvantitet och faktisk förlust i värde mellan färskt och fryst kycklingkött från standardkycklingar som omedelbart slaktades i skyddszonen under den tid då djurhälsoåtgärderna och de veterinära åtgärderna tillämpades. |
|
f) |
Att finansiering inte har mottagits av någon stödberättigad aktör från någon annan källa i syfte att kompensera de förluster som avses i artikel 2. |
Artikel 5
De italienska myndigheterna ska underrätta kommissionen om räkenskapsavslutningen för betalningarna.
Artikel 6
Denna förordning träder i kraft dagen efter det att den har offentliggjorts i Europeiska unionens officiella tidning.
Denna förordning är till alla delar bindande och direkt tillämplig i alla medlemsstater.
Utfärdad i Bryssel den 13 maj 2016.
På kommissionens vägnar
Jean-Claude JUNCKER
Ordförande
(1) EUT L 347, 20.12.2013, s. 671.
(2) Rådets direktiv 2005/94/EG av den 20 december 2005 om gemenskapsåtgärder för bekämpning av aviär influensa och om upphävande av direktiv 92/40/EEG (EUT L 10, 14.1.2006, s. 16).
(3) Kommissionens genomförandebeslut 2014/936/EU av den 17 december 2014 om vissa skyddsåtgärder i samband med högpatogen aviär influensa av subtyp H5N8 i Italien (EUT L 365, 19.12.2014, s. 160).
(4) Europaparlamentets och rådets förordning (EU) nr 652/2014 av den 15 maj 2014 om fastställande av bestämmelser för förvaltningen av utgifter för livsmedelskedjan, djurhälsa, djurskydd, växtskydd och växtförökningsmaterial, och om ändring av rådets direktiv 98/56/EG, 2000/29/EG och 2008/90/EG, Europaparlamentets och rådets förordningar (EG) nr 178/2002, (EG) nr 882/2004 och (EG) nr 396/2005, Europaparlamentets och rådets direktiv 2009/128/EG samt Europaparlamentets och rådets förordning (EG) nr 1107/2009, och om upphävande av rådets beslut 66/399/EEG, 76/894/EEG och 2009/470/EG (EUT L 189, 27.6.2014, s. 1).
(5) Kommissionens delegerade förordning (EU) nr 907/2014 av den 11 mars 2014 om komplettering av Europaparlamentets och rådets förordning (EU) nr 1306/2013 vad gäller utbetalande organ och andra organ, ekonomisk förvaltning, avslutande av räkenskaper, säkerheter och användning av euron (EUT L 255, 28.8.2014, s. 18).
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/67 |
KOMMISSIONENS GENOMFÖRANDEFÖRORDNING (EU) 2016/761
av den 13 maj 2016
om undantag från genomförandeförordning (EU) nr 809/2014 vad gäller sista inlämningsdag för den samlade ansökan, stödansökningar eller stödanspråk, sista dag för meddelande om ändringar av den samlade ansökan eller stödanspråk och sista dag för ansökningar om tilldelning av stödrättigheter eller ökning av stödrättigheters värde inom ramen för ordningen för grundstöd för år 2016
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DENNA FÖRORDNING
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av Europaparlamentets och rådets förordning (EU) nr 1306/2013 av den 17 december 2013 om finansiering, förvaltning och övervakning av den gemensamma jordbrukspolitiken och om upphävande av rådets förordningar (EEG) nr 352/78, (EG) nr 165/94, (EG) nr 2799/98, (EG) nr 814/2000, (EG) nr 1290/2005 och (EG) nr 485/2008 (1), särskilt artikel 78 första stycket led b och andra stycket, och
av följande skäl:
|
(1) |
Genomförandeförordning (EU) nr 809/2014 (2) fastställer sista inlämningsdag för den samlade ansökan, stödansökningar eller stödanspråk, sista dag för meddelande om ändringar av den samlade ansökan eller stödanspråk och sista dag för ansökningar om tilldelning av stödrättigheter eller ökning av stödrättigheters värde inom ramen för ordningen för grundstöd. |
|
(2) |
På grund av de administrativa svårigheter som uppstått under det första året av genomförandet av den nya rättsliga ramen för direktstödssystemet och av de åtgärder för de landsbygdsutvecklingsåtgärder som fortfarande förekommer i vissa medlemsstater samt de nya inslagen med anknytning till utarbetande av ansökningsprocessen för ansökningsåret 2016, har förvaltningen av den samlade ansökan, stödansökningarna och stödanspråken samt ansökningarna om tilldelning av stödrättigheter eller ökningen av stödrättigheternas värde inom ramen för ordningen för grundstöd försenats i vissa medlemsstater. Dessa svårigheter uppstår i samband med den generellt allvarliga ekonomiska situationen i vissa jordbrukssektorer. |
|
(3) |
Denna situation har inverkat på stödmottagarnas möjligheter att lämna in den samlade ansökan, stödansökningar eller stödanspråk, ansökningar om tilldelning av stödrättigheter eller ökning av stödrättigheters värde inom ramen för ordningen för grundstöd inom de tidsfrister som fastställs i artiklarna 13.1 och 22.1 i genomförandeförordning (EU) nr 809/2014. |
|
(4) |
Med hänsyn till denna situation är det lämpligt att föreskriva ett undantag från artiklarna 13.1 och 22.1 i genomförandeförordning (EU) nr 809/2014 som tillåter medlemsstaterna att för år 2016 fastställa en sista dag för inlämnande av den samlade ansökan, stödansökningar eller stödanspråk, ansökningar om tilldelning av stödrättigheter eller ökning av stödrättigheters värde inom ramen för ordningen för grundstöd, som infaller efter den dag som fastställs i de artiklarna. Eftersom de dagar och perioder som avses i artiklarna 11.4, 15.2 och 15.2a i genomförandeförordning (EU) nr 809/2014 hänvisar till är kopplade till den sista dag som fastställs i artikel 13.1 i den förordningen, ska ett liknande undantag föreskrivas för meddelandet om ändringar av den samlade ansökan eller stödanspråk och ändringar till följd av de preliminära kontrollerna. |
|
(5) |
Eftersom dessa undantag bör omfatta den samlade ansökan, stödansökningar och stödanspråk, ändringar av den samlade ansökan eller stödanspråk och ansökningar om tilldelning av stödrättigheter för år 2016, är det lämpligt att denna förordning tillämpas på ansökningar och stödanspråk som rör år 2016. |
|
(6) |
De åtgärder som föreskrivs i denna förordning är förenliga med yttrandet från förvaltningskommittén för direktstöd och landsbygdsutvecklingskommittén. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
Genom undantag från artikel 13.1 första stycket i genomförandeförordning (EU) nr 809/2014, ska för år 2016 de sista datum för inlämning av den samlade ansökan, stödansökningar eller stödanspråk som ska fastställas av medlemsstaterna inte infalla senare än den 15 juni.
Artikel 2
Genom undantag från artikel 15.2 i genomförandeförordning (EU) nr 809/2014 och i det fall medlemsstaterna utnyttjar undantaget som föreskrivs i artiklarna 1 och 3 i denna förordning, ska för år 2016 de ändringar som görs av den samlade ansökan eller stödanspråk i enlighet med artikel 15.1 i genomförandeförordning (EU) nr 809/2014 meddelas till behörig myndighet senast den 15 juni.
Det undantag som avses i artikel 1 i denna förordning och i första stycket i denna artikel ska även tillämpas vid beräkning av de tidsperioder på 26, 35 respektive 10 kalenderdagar efter sista dagen för inlämning av den samlade ansökan, stödansökningar eller stödanspråk och sista datum för meddelande om ändringar som avses i artiklarna 11.4 och 15.2a i genomförandeförordning (EU) nr 809/2014.
Artikel 3
Genom undantag från artikel 22.1 i genomförandeförordning (EU) nr 809/2014, ska, för år 2016, den dag som medlemsstaterna fastställer för inlämnande av ansökningar om tilldelning av stödrättigheter eller ökning av stödrättigheters värde inom ramen för ordningen för grundstöd inte infalla senare än den 15 juni.
Artikel 4
Denna förordning träder i kraft samma dag som den offentliggörs i Europeiska unionens officiella tidning.
Den ska tillämpas på ansökningar och stödanspråk som gäller år 2016.
Denna förordning är till alla delar bindande och direkt tillämplig i alla medlemsstater.
Utfärdad i Bryssel den 13 maj 2016.
På kommissionens vägnar
Jean-Claude JUNCKER
Ordförande
(1) EUT L 347, 20.12.2013, s. 549.
(2) Kommissionens genomförandeförordning (EU) nr 809/2014 av den 17 juli 2014 om regler för tillämpningen av Europaparlamentets och rådets förordning (EU) nr 1306/2013 vad gäller det integrerade administrations- och kontrollsystemet, landsbygdsutvecklingsåtgärder och tvärvillkor (EUT L 227, 31.7.2014, s. 69).
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/69 |
KOMMISSIONENS GENOMFÖRANDEFÖRORDNING (EU) 2016/762
av den 13 maj 2016
om fastställande av schablonimportvärden för bestämning av ingångspriset för vissa frukter och grönsaker
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DENNA FÖRORDNING
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av Europaparlamentets och rådets förordning (EU) nr 1308/2013 av den 17 december 2013 om upprättande av en samlad marknadsordning för jordbruksprodukter och om upphävande av rådets förordningar (EEG) nr 922/72, (EEG) nr 234/79, (EG) nr 1037/2001 och (EG) nr 1234/2007 (1),
med beaktande av kommissionens genomförandeförordning (EU) nr 543/2011 av den 7 juni 2011 om tillämpningsföreskrifter för rådets förordning (EG) nr 1234/2007 vad gäller sektorn för frukt och grönsaker och sektorn för bearbetad frukt och bearbetade grönsaker (2), särskilt artikel 136.1, och
av följande skäl:
|
(1) |
I genomförandeförordning (EU) nr 543/2011 fastställs, i enlighet med resultatet av de multilaterala handelsförhandlingarna i Uruguayrundan, kriterierna för kommissionens fastställande av schablonvärden vid import från tredjeländer, för de produkter och de perioder som anges i del A i bilaga XVI till den förordningen. |
|
(2) |
Varje arbetsdag fastställs ett schablonimportvärde i enlighet med artikel 136.1 i genomförandeförordning (EU) nr 543/2011 med hänsyn till varierande dagliga uppgifter. Denna förordning bör därför träda i kraft samma dag som den offentliggörs i Europeiska unionens officiella tidning. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
De schablonimportvärden som avses i artikel 136 i genomförandeförordning (EU) nr 543/2011 fastställs i bilagan till denna förordning.
Artikel 2
Denna förordning träder i kraft samma dag som den offentliggörs i Europeiska unionens officiella tidning.
Denna förordning är till alla delar bindande och direkt tillämplig i alla medlemsstater.
Utfärdad i Bryssel den 13 maj 2016.
På kommissionens vägnar
För ordföranden
Jerzy PLEWA
Generaldirektör för jordbruk och landsbygdsutveckling
(1) EUT L 347, 20.12.2013, s. 671.
(2) EUT L 157, 15.6.2011, s. 1.
BILAGA
Schablonimportvärden för bestämning av ingångspriset för vissa frukter och grönsaker
|
(euro/100 kg) |
||
|
KN-nummer |
Kod för tredjeland (1) |
Schablonimportvärde |
|
0702 00 00 |
MA |
95,5 |
|
TR |
75,0 |
|
|
ZZ |
85,3 |
|
|
0707 00 05 |
TR |
116,3 |
|
ZZ |
116,3 |
|
|
0709 93 10 |
TR |
137,6 |
|
ZZ |
137,6 |
|
|
0805 10 20 |
EG |
45,4 |
|
IL |
88,6 |
|
|
MA |
55,4 |
|
|
TR |
31,5 |
|
|
ZA |
78,5 |
|
|
ZZ |
59,9 |
|
|
0805 50 10 |
ZA |
168,2 |
|
ZZ |
168,2 |
|
|
0808 10 80 |
AR |
111,7 |
|
BR |
98,2 |
|
|
CL |
123,9 |
|
|
CN |
61,7 |
|
|
NZ |
155,0 |
|
|
US |
162,5 |
|
|
ZA |
95,9 |
|
|
ZZ |
115,6 |
|
(1) Landsbeteckningar som fastställs i kommissionens förordning (EU) nr 1106/2012 av den 27 november 2012 om tillämpning av Europaparlamentets och rådets förordning (EG) nr 471/2009 om gemenskapsstatistik över utrikeshandeln med icke-medlemsstater vad gäller uppdateringen av nomenklaturen avseende länder och territorier (EUT L 328, 28.11.2012, s. 7). Koden ZZ står för ”övrigt ursprung”.
BESLUT
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/71 |
RÅDETS BESLUT (EU) 2016/763
av den 13 maj 2016
om fastställande av den ståndpunkt som ska intas på Europeiska unionens vägnar i kommittén för offentlig upphandling vad gäller utkastet till beslut om skiljedomsförfaranden i enlighet med artikel XIX.8 i det reviderade avtalet om offentlig upphandling
EUROPEISKA UNIONENS RÅD HAR ANTAGIT DETTA BESLUT
med beaktande av fördraget om Europeiska unionens funktionssätt, särskilt artikel 207.4 första stycket jämfört med artikel 218.9,
med beaktande av Europeiska kommissionens förslag, och
av följande skäl:
|
(1) |
I det reviderade avtalet om offentlig upphandling (nedan kallat det reviderade GPA-avtalet), som trädde i kraft den 6 april 2014, fastställs ett nytt regelverk som parterna i det reviderade GPA-avtalet ska tillämpa på den upphandling som omfattas av avtalet. I det reviderade GPA-avtalet föreskrivs att parterna i det reviderade GPA-avtalet får använda skiljedomsförfaranden i fall då invändningar mot föreslagna korrigeringar, överföringar av en enhet från en bilaga till en annan, borttagande av en enhet eller andra ändringar av en parts bilagor till tillägg I inte har kunnat lösas genom samråd. |
|
(2) |
I enlighet med artikel XIX.8 i det reviderade GPA-avtalet ska kommittén för offentlig upphandling anta bestämmelser om skiljedomsförfaranden för att underlätta lösning av frågor som rör sådana invändningar. |
|
(3) |
Parterna i det reviderade GPA-avtalet har fört ingående diskussioner om innehållet i sådana bestämmelser om skiljedomsförfaranden när det gäller olika alternativ som ska tillämpas vid invändningar mot en föreslagen ändring av en parts upphandlingstäckning. Parterna i det reviderade GPA-avtalet har kunnat enas i frågan. |
|
(4) |
De bestämmelser om skiljedomsförfaranden som man enats om anges i ett utkast till beslut om skiljedomsförfaranden i enlighet med artikel XIX.8 i det reviderade GPA-avtalet. |
|
(5) |
I utkastet till beslut om skiljedomsförfaranden fastställs de villkor som ska uppfyllas för att skiljedomsförfaranden ska kunna användas samt regler för utnämning av skiljemän, tredje parters medverkan i skiljedomsförfaranden, genomförandet av förfarandet och skiljemännens avgörande. |
|
(6) |
Antagandet av utkastet till beslutet om skiljedomsförfaranden förväntas bidra positivt till det befintliga regelverket efter det reviderade GPA-avtalet, eftersom syftet är att underlätta lösning av frågor som rör invändningar mot föreslagna korrigeringar, överföringar av en enhet från en bilaga till en annan, borttagande av en enhet eller andra ändringar av en parts bilagor till tillägg I till det reviderade GPA-avtalet. |
|
(7) |
Det är därför lämpligt att fastställa den ståndpunkt vad gäller utkastet till beslut om skiljedomsförfaranden som ska intas på unionens vägnar i kommittén för offentlig upphandling. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
Den ståndpunkt som ska intas på unionens vägnar i kommittén för offentlig upphandling ska vara att godkänna antagandet av utkastet till beslut om skiljedomsförfaranden i enlighet med artikel XIX.8 i det reviderade avtalet om offentlig upphandling.
Utkastet till beslut om skiljedomsförfarande åtföljer detta beslut.
Artikel 2
Detta beslut träder i kraft samma dag som det antas.
Utfärdat i Bryssel den 13 maj 2016.
På rådets vägnar
E.M.J. PLOUMEN
Ordförande
UTKAST TILL BESLUT OM SKILJEFÖRFARANDEN I ENLIGHET MED ARTIKEL XIX.8 I DET REVIDERADE GPA-AVTALET
Kommittén för offentlig upphandling (nedan kallad kommittén), som
noterar att det följer av artikel XIX.8 i det reviderade avtalet om offentlig upphandling (nedan kallat avtalet) att kommittén ska utarbeta skiljedomsförfaranden för att underlätta lösning av frågor som rör invändningar enligt artikel XIX.2 i avtalet, och
bekräftar vikten av artikel XIX.8 b och c i avtalet för sådana skiljedomsförfaranden och upprepar parternas åtagande att anta beslut i enlighet med artikel XIX.8 b och c i avtalet,
härmed antar följande bestämmelser om skiljedomsförfaranden för att underlätta lösning av frågor som rör invändningar enligt artikel XIX.2 i avtalet:
Åberopande av skiljedomsförfarande
|
1. |
I enlighet med artikel XIX.7 i avtalet får den ändrande parten eller en invändande part, när den ändrande parten och en invändande part inte kan lösa en fråga som rör en invändning mot en föreslagen ändring enligt artikel XIX.1 i avtalet, hänskjuta den föreslagna ändringen till ett skiljedomsförfarande, med angivande av skälen till begäran, genom att underrätta kommittén tidigast 45 dagar efter den dag då meddelandet om den föreslagna ändringen enligt artikel XIX.1 i avtalet sändes ut. |
|
2. |
Om två eller flera parter hänskjuter samma föreslagna ändring till skiljedomsförfarande innan samtliga skiljemän utsetts, ska den ändrande parten och alla invändande parter enas om ett enda skiljedomsförfarande som behandlar alla invändningar mot samma föreslagna ändring. Om ytterligare hänskjutningar av samma föreslagna ändring görs efter det att samtliga skiljemän har utnämnts, ska den ändrande parten och alla invändande parter om möjligt komma överens om ett enda skiljedomsförfarande. |
Utnämning av skiljemän
|
3. |
Skiljedomsförfaranden ska genomföras av skiljemän. Om inte parterna i skiljedomsförfarandet enas om något annat, ska det finnas tre skiljemän. Skiljemännen ska uppfylla kraven för panelmedlemmar enligt artikel 8.1, 8.2 och 8.9 i överenskommelsen om regler och förfaranden för tvistlösning. |
|
4. |
Kommitténs sekretariat ska, på begäran av en part i skiljedomsförfarandet, föreslå nomineringar till skiljemän. Parterna i skiljedomsförfarandet får inte motsätta sig nomineringar annat än om tvingande skäl föreligger. Medborgare i parterna i skiljedomsförfarandet och tredje parters regeringstjänstemän får inte utses till skiljemän, såvida inte parterna i skiljedomsförfarandet enas om något annat. |
|
5. |
Om parterna i skiljedomsförfarandet inte kan enas om vilka som bör utses till skiljemän inom 20 dagar efter det att den föreslagna ändringen hänskjutits till skiljedomsförfarande, ska generaldirektören, på begäran av en part i skiljedomsförfarandet, utse skiljemännen inom 10 dagar, efter samråd med parterna i skiljedomsförfarandet och kommitténs ordförande. |
Medverkan av tredje part
|
6. |
En part i avtalet som har ett väsentligt intresse av en föreslagen ändring som hänskjutits till skiljedomsförfarande och som underrättat kommittén om detta intresse (nedan kallad tredje part) inom 10 dagar efter det att den föreslagna ändringen hänskjutits till skiljeförfarande ska uppmanas att lämna in en skriftlig inlaga, delta i sammanträden i sakfrågan mellan skiljemännen och parterna i skiljedomsförfarandet, göra muntliga framställningar och ha rätt att besvara frågor från skiljemännen. |
Förfaranden
|
7. |
Skiljemännen ska vid skiljedomsförfarandet tillämpa relevanta bestämmelser i avtalet och låta sig vägledas av det beslut som antagits av kommittén i enlighet med artikel XIX.8 b i avtalet, när det har antagits. Därutöver ska följande arbetsförfaranden tillämpas:
|
|
8. |
Uppförandereglerna enligt överenskommelsen om regler och förfaranden för tvistlösning ska gälla varje person som tjänstgör som skiljeman i dessa förfaranden och, enligt vad som anges i uppförandereglerna och tillämpliga bestämmelser i tjänsteföreskrifterna, de personer i sekretariatet som bistår skiljemännen. |
|
9. |
Om parterna i skiljedomsförfarandet enas om en lösning med avseende på invändningar mot den föreslagna ändringen ska de utan dröjsmål underrätta skiljemännen. Efter att ha mottagit underrättelsen ska skiljemännen avsluta förfarandet för dessa parter. De närmare detaljerna i sådana lösningar ska anmälas till kommittén, där alla parter i avtalet får lämna synpunkter. |
Skiljemännens avgörande
|
10. |
Skiljemännens mandat ska innehålla krav på att skiljemännen ska avgöra,
|
|
11. |
Skiljemännen ska avge en rapport med sitt motiverade avgörande till parterna i skiljedomsförfarandet inom 90 dagar eller, om skiljemännen ändrar tidsplanen, senast 120 dagar
Den tidsperiod som fastställs i den här punkten får förlängas genom överenskommelse mellan parterna i skiljedomsförfarandet. Kommitténs sekretariat ska utan dröjsmål skicka rapporten till parterna i avtalet efter översättning. |
|
12. |
Om skiljemännen fäller ett negativt avgörande enligt punkt 10 a och de inte har fastställt någon kompensationsjustering enligt punkt 10 b, får vilken part som helst i skiljedomsförfarandet, tidigast 30 och senast 60 dagar efter det att skiljemännens rapport har skickats ut, begära att samma skiljemän, om de är tillgängliga, fastställer den kompensationsjustering som skulle leda till en likvärdig nivå på täckningen och bibehålla balansen mellan rättigheter och skyldigheter enligt avtalet. För detta ändamål ska skiljemännen låta sig vägledas av det beslut som antagits av kommittén i enlighet med artikel XIX.8 c i avtalet, när det har antagits. Om någon av de ursprungliga skiljemännen inte är tillgänglig ska en ersättare utses i enlighet med punkterna 3–5. |
Genomförande
|
13. |
Parterna i skiljedomsförfarandet ska godta skiljemännens avgörande som slutgiltigt. |
|
14. |
Vid tillämpning av artikel XIX.7 b i) i avtalet ska skiljedomsförfarandet anses slutfört
|
BILAGA
FÖRSLAG TILL TIDSPLAN FÖR SKILJEDOMSFÖRFARANDET
Skiljemännen ska basera den tidsplan som antas enligt punkt 7 a på följande:
|
a. |
Mottagande av skriftliga inlagor från parterna i skiljedomsförfarandet: |
|
|
|
- - - - - - - - - - 2 veckor |
||
|
- - - - - - - - - - 2 veckor |
||
|
b. |
Mottagande av inlagor från tredje part: |
- - - - - - - - - - 1 vecka |
|
|
c. |
Sammanträde i sakfrågan med skiljemännen: |
- - - - - - - - - - 1-2 veckor |
|
|
d. |
Svar på frågor till parterna och tredje parter i skiljedomsförfarandet: |
- - - - - - - - - - 1-2 veckor |
|
|
e. |
Avgivande och utskick av skiljemännens rapport om avgörandet: |
- - - - - - - - - - 4 veckor |
Skiljemännen får i enlighet med bestämmelserna i punkt 11 ändra ovanstående tidsplan och planera ytterligare sammanträden med parterna i skiljedomsförfarandet efter samråd med dessa.
|
14.5.2016 |
SV |
Europeiska unionens officiella tidning |
L 126/77 |
KOMMISSIONENS GENOMFÖRANDEBESLUT (EU) 2016/764
av den 12 maj 2016
om ändring av genomförandebeslut (EU) 2015/789 om åtgärder för att förhindra introduktion i och spridning inom unionen av Xylella fastidiosa (Wells et al.)
[delgivet med nr C(2016) 2731]
EUROPEISKA KOMMISSIONEN HAR ANTAGIT DETTA BESLUT
med beaktande av fördraget om Europeiska unionens funktionssätt,
med beaktande av rådets direktiv 2000/29/EG av den 8 maj 2000 om skyddsåtgärder mot att skadegörare på växter eller växtprodukter förs in till gemenskapen och mot att de sprids inom gemenskapen (1), särskilt artikel 16.3 fjärde meningen, och
av följande skäl:
|
(1) |
Från det att kommissionens genomförandebeslut (EU) 2015/789 (2) antogs och fram till och med februari 2016 har Italien till kommissionen anmält flera utbrott av Xylella fastidiosa (Wells et al.) (nedan kallad den angivna skadegöraren) i olika delar av det område som omger provinsen Lecce. Utbrotten har ägt rum i flera olika kommuner i provinserna Taranto och Brindisi. Kommissionens senaste revision i november 2015 bekräftade dessutom att de undersökningar som krävs enligt genomförandebeslut (EU) 2015/789 endast hade genomförts i mycket begränsad utsträckning i området som omger provinsen Lecce (i regionen Apulien, Italien). Revisionen bekräftade också att det nuvarande undersökningsprogrammet fortfarande inte säkerställer att nya utbrott upptäcks i tid eller att den faktiska omfattningen av den angivna skadegörarens spridning i området kan fastställas exakt. |
|
(2) |
Den senaste revisionen bekräftade risken för att den angivna skadegöraren snabbt sprids till resten av det berörda området. Av detta skäl och med tanke på områdets storlek bör den angripna zonen där inneslutningsåtgärder kan vidtas utvidgas så att den sträcker sig utanför provinsen Lecces gräns, och förflyttning av angivna växter från området bör endast tillåtas på mycket stränga villkor. En sådan utvidgning bör ske utan dröjsmål med beaktande av att risken för att den angivna skadegöraren sprids till resten av unionens territorium ökar när insektsvektorns flygsäsong börjar tidigt på våren. Den angripna zonen bör därför utvidgas till att även omfatta de kommuner, eller delar av vissa kommuner, i provinserna Brindisi och Taranto där det har förekommit utbrott av den angivna skadegöraren eller där det är sannolikt att den skadegöraren redan har spridits och är etablerad. Den angripna zonen bör dock inte omfatta det område som av Italien har förklarats vara fritt från den angivna skadegöraren innan detta beslut antas. |
|
(3) |
För att rättsläget ska vara klart bör artikel 7.2 c formuleras om så att det tydligt framgår att de åtgärder som ska vidtas i enlighet med den artikeln gäller i den angripna zonen och inte utanför den. |
|
(4) |
För att säkerställa att resten av unionens territorium effektivt skyddas mot den angivna skadegöraren, och med beaktande av inneslutningsområdets utvidgning, bör övervakningszonen ersättas med nya krav för undersökningar i inneslutningsområdet. Dessa krav bör gälla i ett 20 km brett område från gränsen till buffertzonen och in i inneslutningsområdet, och i den omgivande buffertzonen på 10 km. |
|
(5) |
Sedan genomförandebeslut (EU) 2015/789 antogs har det visat sig att det är oproportionerligt att tillämpa samma krav för förflyttning av angivna växter inom de angripna zonerna som för förflyttning av dem från de angripna zonerna till buffertzonerna, eftersom den angivna skadegöraren redan är etablerad i dessa angripna zoner. |
|
(6) |
Sedan genomförandebeslut (EU) 2015/789 antogs har det bekräftats att angivna växter som under hela produktionscykeln odlas in vitro i ett sterilt medium inte utgör någon risk för spridning av den angivna skadegöraren, eftersom det odlingssättet undanröjer risken för infektion genom att det förhindrar kontakt med den angivna skadegörarens vektorer. Därför bör förflyttning inom och införsel till unionen av dessa angivna växter tillåtas på vissa villkor. |
|
(7) |
Sedan genomförandebeslut (EU) 2015/789 antogs har de officiella kontrollerna gett vid handen att angivna växter med ursprung i områden som är fria från den angivna skadegöraren bör omfattas av samma krav som angivna växter med ursprung i tredjeländer där den angivna skadegöraren inte förekommer när det gäller officiella kontroller vid införsel till unionen. |
|
(8) |
Bilaga I bör ändras så att den omfattar alla växtarter som sedan kommissionens genomförandebeslut (EU) 2015/2417 (3) antogs har identifierats som angivna växter av kommissionen. |
|
(9) |
De åtgärder som föreskrivs i detta beslut är förenliga med yttrandet från ständiga kommittén för växter, djur, livsmedel och foder. |
HÄRIGENOM FÖRESKRIVS FÖLJANDE.
Artikel 1
Ändringar av genomförandebeslut (EU) 2015/789
Genomförandeförordning (EU) 2015/789 ska ändras på följande sätt:
|
1. |
I artikel 4.2 ska tredje stycket ersättas med följande: ”När det gäller förekomsten av den angivna skadegöraren i provinsen Lecce och i de kommuner som förtecknas i bilaga II ska den angripna zonen omfatta åtminstone den provinsen och de kommunerna eller, i förekommande fall, fastighetsområdena (Fogli) i dessa kommuner.” |
|
2. |
Artikel 7 ska ändras på följande sätt:
|
|
3. |
Artikel 8 ska utgå. |
|
4. |
I artikel 9 ska punkt 1 ersättas med följande: ”1. Denna artikel ska tillämpas på andra angivna växter än sådana som under hela produktionscykeln odlats in vitro. Det ska vara förbjudet att från de avgränsade områdena, och från de angripna zonerna till buffertzonerna, förflytta angivna växter som har odlats under åtminstone en del av sin livstid i ett avgränsat område som upprättats i enlighet med artikel 4.” |
|
5. |
Följande artikel ska införas som artikel 9a: ”Artikel 9a Förflyttning inom unionen av angivna växter som har odlats in vitro 1. Angivna växter som under hela produktionscykeln har odlats in vitro, och under åtminstone en del av sin livstid i ett avgränsat område som upprättats i enlighet med artikel 4, får endast förflyttas ut från de avgränsade områdena, och från de angripna zonerna till buffertzonerna, om villkoren i punkterna 2–5 är uppfyllda. 2. De angivna växter som avses i punkt 1 har odlats på en plats som uppfyller samtliga följande villkor:
3. De angivna växter som avses i punkt 1 har odlats i en transparent behållare under sterila förhållanden och uppfyller ett av följande krav:
4. De angivna växter som avses i punkt 1 ska transporteras i en transparent behållare under sterila förhållanden så att de inte kan infekteras med den angivna skadegöraren genom dess vektorer. 5. De ska åtföljas av ett växtpass som har utarbetats och utfärdats i enlighet med direktiv 92/105/EEG.” |
|
6. |
Artikel 17 ska ändras på följande sätt:
|
|
7. |
I artikel 18 ska punkterna 2, 3 och 4 ersättas med följande: ”2. När det gäller angivna växter med ursprung i ett tredjeland där den angivna skadegöraren inte förekommer, eller i ett område som avses i artikel 17.2, ska det ansvariga officiella organet utföra följande kontroller:
3. När det gäller angivna växter med ursprung i ett område där det är känt att den angivna skadegöraren förekommer, ska det ansvariga officiella organet utföra följande kontroller:
4. De prover som avses i punkterna 2 b och 3 b ska ha en storlek som gör det möjligt att med 99 % tillförlitlighet identifiera en förekomst av angripna växter av minst 1 %, med beaktande av ISPM nr 31. Första stycket ska inte tillämpas på angivna växter som under hela produktionscykeln har odlats in vitro och transporteras i transparenta behållare under sterila förhållanden.” |
|
8. |
Bilaga I ska ändras i enlighet med bilaga I till detta beslut. |
|
9. |
Bilagan i bilaga II till detta beslut ska läggas till som bilaga II. |
Artikel 2
Adressater
Detta beslut riktar sig till medlemsstaterna.
Utfärdat i Bryssel den 12 maj 2016.
På kommissionens vägnar
Vytenis ANDRIUKAITIS
Ledamot av kommissionen
(1) EGT L 169, 10.7.2000, s. 1.
(2) Kommissionens genomförandebeslut (EU) 2015/789 av den 18 maj 2015 om åtgärder för att förhindra introduktion i och spridning inom unionen av Xylella fastidiosa (Wells et al.) (EUT L 125, 21.5.2015, s. 36).
(3) Kommissionens genomförandebeslut (EU) 2015/2417 av den 17 december 2015 om ändring av kommissionens genomförandebeslut (EU) 2015/789 om åtgärder för att förhindra introduktion i och spridning inom unionen av Xylella fastidiosa (Wells et al.) (EUT L 333, 19.12.2015, s. 143).
BILAGA I
Bilaga I till genomförandebeslut (EU) 2015/789 ska ändras på följande sätt:
|
1. |
Följande poster ska införas i alfabetisk ordning:
|
|
2. |
Följande poster ska utgå:
|
|
3. |
Posten ”Cytisus racemosus Broom” ska ersättas med följande: ”Genista x spachiana (syn. Cytisus racemosus Broom)”. |
BILAGA II
Följande bilaga II ska läggas till i genomförandebeslut (EU) 2015/789:
”BILAGA II
FÖRTECKNING ÖVER DE KOMMUNER SOM AVSES I ARTIKEL 4.2
|
1. |
Kommuner i provinsen Brindisi:
|
|
2. |
Kommuner i provinsen Taranto:
|