ISSN 1725-5244
Uradni list
Evropske unije
C 276

Slovenska izdaja
Informacije in objave
Zvezek 51
31. oktober 2008
|
ISSN 1725-5244 |
||
|
Uradni list Evropske unije |
C 276 |
|

|
||
|
Slovenska izdaja |
Informacije in objave |
Zvezek 51 |
|
Obvestilo št. |
Vsebina |
Stran |
|
|
IV Informacije |
|
|
|
INFORMACIJE INSTITUCIJ IN ORGANOV EVROPSKE UNIJE |
|
|
|
Komisija |
|
|
2008/C 276/01 |
||
|
2008/C 276/02 |
||
|
2008/C 276/03 |
||
|
|
INFORMACIJE DRŽAV ČLANIC |
|
|
2008/C 276/04 |
||
|
2008/C 276/05 |
Podatki, ki jih predložijo države članice o državni pomoči, dodeljeni na podlagi Uredbe Komisije (ES) št. 70/2001 o uporabi členov 87 in 88 Pogodbe ES pri pomoči za majhna in srednje velika podjetja ( 1 ) |
|
|
2008/C 276/06 |
Podatki, ki jih predložijo države članice o državni pomoči, dodeljeni na podlagi Uredbe Komisije (ES) št. 70/2001 o uporabi členov 87 in 88 Pogodbe ES pri pomoči za majhna in srednje velika podjetja ( 1 ) |
|
|
|
V Objave |
|
|
|
UPRAVNI POSTOPKI |
|
|
|
Komisija |
|
|
2008/C 276/07 |
Javni razpis, ki ga je objavila Italija na podlagi člena 4(1)(d) Uredbe Sveta (EGS) št. 2408/92, za opravljanje rednih zračnih prevozov na progi Albenga–Rim Fiumicino in v obratni smeri ( 1 ) |
|
|
2008/C 276/08 |
Javni razpis, ki ga je objavila Italija v skladu s členom 4(1)(d) Uredbe Sveta (EGS) št. 2408/92 za opravljanje rednih zračnih prevozov na progi Crotone–Milano Linate in v obratni smeri ( 1 ) |
|
|
2008/C 276/09 |
Javni razpis, ki ga je objavila Italija v skladu s členom 4(1)(d) Uredbe Sveta (EGS) št. 2408/92 za opravljanje rednih zračnih prevozov na progi Crotone–Roma Fiumicino in v obratni smeri ( 1 ) |
|
|
2008/C 276/10 |
||
|
|
POSTOPKI V ZVEZI Z IZVAJANJEM KONKURENČNE POLITIKE |
|
|
|
Komisija |
|
|
2008/C 276/11 |
Predhodna priglasitev koncentracije (Št. primera COMP/M.5368 – MidAmerican/Constellation) – Zadeva, primerna za obravnavo po poenostavljenem postopku ( 1 ) |
|
|
|
||
|
2008/C 276/12 |
||
|
|
|
|
|
(1) Besedilo velja za EGP |
|
SL |
|
IV Informacije
INFORMACIJE INSTITUCIJ IN ORGANOV EVROPSKE UNIJE
Komisija
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/1 |
Menjalni tečaji eura (1)
30. oktobra 2008
(2008/C 276/01)
1 euro=
|
|
Valuta |
Menjalni tečaj |
|
USD |
ameriški dolar |
1,3035 |
|
JPY |
japonski jen |
128,73 |
|
DKK |
danska krona |
7,4478 |
|
GBP |
funt šterling |
0,7907 |
|
SEK |
švedska krona |
9,811 |
|
CHF |
švicarski frank |
1,48 |
|
ISK |
islandska krona |
305 |
|
NOK |
norveška krona |
8,52 |
|
BGN |
lev |
1,9558 |
|
CZK |
češka krona |
24,48 |
|
EEK |
estonska krona |
15,6466 |
|
HUF |
madžarski forint |
257,24 |
|
LTL |
litovski litas |
3,4528 |
|
LVL |
latvijski lats |
0,7093 |
|
PLN |
poljski zlot |
3,565 |
|
RON |
romunski leu |
3,6375 |
|
SKK |
slovaška krona |
30,39 |
|
TRY |
turška lira |
1,9842 |
|
AUD |
avstralski dolar |
1,9204 |
|
CAD |
kanadski dolar |
1,5697 |
|
HKD |
hongkonški dolar |
10,1052 |
|
NZD |
novozelandski dolar |
2,2015 |
|
SGD |
singapurski dolar |
1,9141 |
|
KRW |
južnokorejski won |
1 665,72 |
|
ZAR |
južnoafriški rand |
13,0194 |
|
CNY |
kitajski juan |
8,9133 |
|
HRK |
hrvaška kuna |
7,1699 |
|
IDR |
indonezijska rupija |
13 914,86 |
|
MYR |
malezijski ringit |
4,6046 |
|
PHP |
filipinski peso |
63,09 |
|
RUB |
ruski rubelj |
34,7912 |
|
THB |
tajski bat |
45,381 |
|
BRL |
brazilski real |
2,7521 |
|
MXN |
mehiški peso |
16,6978 |
Vir: referenčni menjalni tečaj, ki ga objavlja ECB.
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/2 |
Povzetek odločb Skupnosti o dovoljenjih za promet z zdravili od 1. septembra 2008 do 30. septembra 2008
(Objavljeno v skladu s členom 13 ali členom 38 Uredbe (ES) št. 726/2004 Evropskega parlamenta in Sveta (1) )
(2008/C 276/02)
— Izdaja dovoljenja za promet (člen 13 Uredbe (ES) št. 726/2004): Odobrena
|
Datum sprejetja odločbe |
Ime zdravila |
INN (mednarodno nelastniško ime) |
Imetnik dovoljenja za promet |
Registracijska številka v registru Skupnosti |
Farmacevtska oblika |
Oznaka ATC (anatomsko terapevtsko kemijska oznaka) |
Datum obvestila |
|||
|
12.9.2008 |
Oprymea |
pramipeksol |
|
EU/1/08/469/001-025 |
Tableta |
NO4BC05 |
15.9.2008 |
|||
|
15.9.2008 |
Tevagrastim |
Filgrastim |
|
EU/1/08/445/001-008 |
Raztopina za injiciranje ali infundiranje |
L03AA02 |
17.9.2008 |
|||
|
15.9.2008 |
Biograstim |
Filgrastim |
|
EU/1/08/450/001-008 |
Raztopina za injiciranje ali infundiranje |
L03AA02 |
17.9.2008 |
|||
|
15.9.2008 |
Ratiograstim |
Filgrastim |
|
EU/1/08/444/001-008 |
Raztopina za injiciranje ali infundiranje |
L03AA02 |
17.9.2008 |
|||
|
15.9.2008 |
Filgrastim ratiopharm |
Filgrastim |
|
EU/1/08/449/001-008 |
Raztopina za injiciranje ali infundiranje |
L03AA02 |
17.9.2008 |
|||
|
26.9.2008 |
Prepandemic influenza vaccine (H5N1) (split virion inactivated adjuvanted) GlaxoSmithKline Biologicals |
Prepandemično cepivo proti gripi (H5N1) z delci virionov, inaktivirano (z adjuvansom) A/VietNam/1194/2004 NIBRG |
|
EU/1/08/478/001 |
Suspenzija in emulzija za emulzijo za injiciranje |
J07BB02 |
30.9.2008 |
|||
|
30.9.2008 |
Xarelto |
rivaroksaban |
|
EU/1/08/472/001-008 |
Filmsko obložena tableta |
B01AX06 |
2.10.2008 |
— Sprememba dovoljenja za promet (člen 13 Uredbe (ES) št. 726/2004): Odobrena
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik dovoljenja za promet |
Registracijska številka v registru Skupnosti |
Datum obvestila |
|||||
|
1.9.2008 |
Aranesp |
|
EU/1/01/185/001-073 |
3.9.2008 |
|||||
|
1.9.2008 |
Adenuric |
|
EU/1/08/447/001-004 |
3.9.2008 |
|||||
|
3.9.2008 |
||||||||
|
1.9.2008 |
Rotarix |
|
EU/1/05/330/001-011 |
3.9.2008 |
|||||
|
1.9.2008 |
Zostavax |
|
EU/1/06/341/001-013 |
3.9.2008 |
|||||
|
2.9.2008 |
Ziagen |
|
EU/1/99/112/001-002 |
4.9.2008 |
|||||
|
2.9.2008 |
Lucentis |
|
EU/1/06/374/001 |
4.9.2008 |
|||||
|
2.9.2008 |
Olanzapine Neopharma |
|
EU/1/07/426/001-011 |
4.9.2008 |
|||||
|
2.9.2008 |
SonoVue |
|
EU/1/01/177/002 |
4.9.2008 |
|||||
|
2.9.2008 |
Gardasil |
|
EU/1/06/357/001-021 |
5.9.2008 |
|||||
|
2.9.2008 |
Viramune |
|
EU/1/97/055/001-003 |
4.9.2008 |
|||||
|
2.9.2008 |
Ventavis |
|
EU/1/03/255/001-006 |
4.9.2008 |
|||||
|
2.9.2008 |
Silgard |
|
EU/1/06/358/001-021 |
4.9.2008 |
|||||
|
2.9.2008 |
Cetrotide |
|
EU/1/99/100/001-003 |
5.9.2008 |
|||||
|
2.9.2008 |
Olanzapine Teva - |
|
EU/1/07/427/001-057 |
4.9.2008 |
|||||
|
2.9.2008 |
Elaprase |
|
EU/1/06/365/001-003 |
4.9.2008 |
|||||
|
3.9.2008 |
Tysabri |
|
EU/1/06/346/001 |
8.9.2008 |
|||||
|
3.9.2008 |
Comtess |
|
EU/1/98/082/001-003 EU/1/98/082/005 |
8.9.2008 |
|||||
|
3.9.2008 |
Aldara |
|
EU/1/98/080/001 |
5.9.2008 |
|||||
|
3.9.2008 |
Tamiflu |
|
EU/1/02/222/001-004 |
5.9.2008 |
|||||
|
3.9.2008 |
Mirapexin |
|
EU/1/97/051/001-006 EU/1/97/051/009-012 |
5.9.2008 |
|||||
|
3.9.2008 |
Aldara |
|
EU/1/98/080/001 |
5.9.2008 |
|||||
|
3.9.2008 |
Comtan |
|
EU/1/98/081/001-004 |
8.9.2008 |
|||||
|
3.9.2008 |
Cialis |
|
EU/1/02/237/001-008 |
5.9.2008 |
|||||
|
5.9.2008 |
Mircera |
|
EU/1/07/400/017-021 |
9.9.2008 |
|||||
|
5.9.2008 |
Herceptin |
|
EU/1/00/145/001 |
9.9.2008 |
|||||
|
5.9.2008 |
Puregon |
|
EU/1/96/008/038-041 |
9.9.2008 |
|||||
|
5.9.2008 |
Epivir |
|
EU/1/96/015/001-005 |
9.9.2008 |
|||||
|
8.9.2008 |
Evra |
|
EU/1/02/223/001-003 |
10.9.2008 |
|||||
|
9.9.2008 |
Herceptin |
|
EU/1/00/145/001 |
11.9.2008 |
|||||
|
12.9.2008 |
Viread |
|
EU/1/01/200/001-002 |
15.9.2008 |
|||||
|
15.9.2008 |
Sustiva |
|
EU/1/99/110/001-009 |
17.9.2008 |
|||||
|
15.9.2008 |
Glubrava |
|
EU/1/07/421/001-009 |
17.9.2008 |
|||||
|
15.9.2008 |
Stalevo |
|
EU/1/03/260/001-023 |
17.9.2008 |
|||||
|
16.9.2008 |
Combivir |
|
EU/1/98/058/001-002 |
18.9.2008 |
|||||
|
17.9.2008 |
Optisulin |
|
EU/1/00/133/001-008 |
19.9.2008 |
|||||
|
17.9.2008 |
Lantus |
|
EU/1/00/134/001-037 |
19.9.2008 |
|||||
|
22.9.2008 |
Emtriva |
|
EU/1/03/261/001-003 |
24.9.2009 |
|||||
|
22.9.2008 |
Emend |
|
EU/1/03/262/001-008 |
24.9.2008 |
|||||
|
26.9.2008 |
Aclasta |
|
EU/1/05/308/001-002 |
30.9.2008 |
|||||
|
26.9.2008 |
Thelin |
|
EU/1/06/353/001-005 |
30.9.2008 |
|||||
|
29.9.2008 |
Mycamine |
|
EU/1/08/448/001-002 |
1.10.2008 |
|||||
|
1.10.2008 |
— Umik dovoljenja za promet (člen 13 Uredbe (ES) št. 726/2004)
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik dovoljenja za promet |
Registracijska številka v registru Skupnosti |
Datum obvestila |
|||||
|
26.9.2008 |
Exubera |
|
EU/1/05/327/001-018 |
30.9.2008 |
— Izdaja dovoljenja za promet (Člen 38 Uredbe (ES) št. 726/2004): Odobrena
|
Datum sprejetja odločbe |
Ime zdravila |
INN (mednarodno nelastniško ime) |
Imetnik dovoljenja za promet |
Registracijska številka v registru Skupnosti |
Farmacevtska oblika |
Oznaka ATC (anatomsko terapevtsko kemijska oznaka) |
Datum obvestila |
|||||
|
9.9.2008 |
Trocoxil |
Mavacoxib |
|
EU/2/08/084/001-005 |
Žvečljive tablete |
QM01AH92 |
11.9.2008 |
— Sprememba dovoljenja za promet (člen 38 Uredbe (ES) št. 726/2004): Odobrena
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik dovoljenja za promet |
Registracijska številka v registru Skupnosti |
Datum obvestila |
|||||
|
2.9.2008 |
Advocate |
|
EU/2/03/039/001-030 |
4.9.2008 |
|||||
|
4.9.2008 |
||||||||
|
5.9.2008 |
Profender |
|
EU/2/05/054/001-031 |
9.9.2008 |
|||||
|
9.9.2008 |
||||||||
|
15.9.2008 |
Oxyglobin |
|
EU/2/99/015/002 |
17.9.2008 |
|||||
|
19.9.2008 |
DRAXXIN |
|
EU/2/03/041/001-005 |
23.9.2008 |
|||||
|
26.9.2008 |
PRAC-TIC |
|
EU/2/06/066/001-012 |
30.9.2008 |
— Sprememba dovoljenja za promet (člen 38 Uredbe (ES) št. 726/2004): Zavrnjena
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik dovoljenja za promet |
Registracijska številka v registru Skupnosti |
Datum obvestila |
||||
|
26.9.2008 |
Porcilis Pesti |
|
EU/2/99/016/001-006 |
30.9.2008 |
Kdor želi dobiti vpogled v javno poročilo o oceni zadevnih zdravil ter o zadevnih odločb zdravil, se lahko obrne na naslov:
|
The European Medicines Agency |
|
7 Westferry Circus |
|
Canary Wharf |
|
London E14 4HB |
|
United Kingdom |
(1) UL L 136, 30.4.2004, str 1.
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/9 |
Povzetek odločb Skupnosti o dovoljenjih za promet z zdravili od 1. septembra 2008 do 30. septembra 2008
(Odločbe, sprejete na podlagi člena 34 Direktive 2001/83/ES Evropskega parlamenta in Sveta (1) oziroma člena 38 Direktive 2001/82/ES Evropskega parlamenta in Sveta (2) )
(2008/C 276/03)
— Izdaja, ohranjanje ali sprememba nacionalnega dovoljenja za promet
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik(i) dovoljenja za promet |
Zadevne države članice |
Datum obvestila |
|||||
|
3.9.2008 |
Cozaar |
Glej Prilogo I |
Glej Prilogo I |
8.9.2008 |
|||||
|
3.9.2008 |
Cozaar Comp |
Glej Prilogo II |
Glej Prilogo II |
8.9.2008 |
|||||
|
9.9.2008 |
Arcoxia |
Glej Prilogo III |
Glej Prilogo III |
11.9.2008 |
|||||
|
9.9.2008 |
Etoricoxib |
Glej Prilogo IV |
Glej Prilogo IV |
11.9.2008 |
|||||
|
11.9.2008 |
Activelle |
Glej Prilogo V |
Glej Prilogo V |
15.9.2008 |
|||||
|
11.9.2008 |
Rapinyl |
Glej Prilogo VI |
Glej Prilogo VI |
15.9.2008 |
|||||
|
15.9.2008 |
Remeron |
Glej Prilogo VII |
Glej Prilogo VII |
17.9.2008 |
|||||
|
23.9.2008 |
Gemzar |
Glej Prilogo VIII |
Glej Prilogo VIII |
24.9.2008 |
|||||
|
26.9.2008 |
Natrijev salicilat |
Glej Prilogo IX |
Glej Prilogo IX |
29.9.2008 |
|||||
|
26.9.2008 |
Toltrazuril |
Glej Prilogo X |
Glej Prilogo X |
29.9.2008 |
|||||
|
26.9.2008 |
Aclasta |
|
Ta odločba je naslovljena na države članice |
29.9.2008 |
— Ukinitev nacionalnega dovoljenja za promet
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik(i) dovoljenja za promet |
Zadevne države članice |
Datum obvestila |
|
9.9.2008 |
Pulairmax |
Glej Prilogo XI |
Glej Prilogo XI |
11.9.2008 |
— Preklic ukinitve nacionalnega dovoljenja za promet
|
Datum sprejetja odločbe |
Ime zdravila |
Imetnik(i) dovoljenja za promet |
Zadevne države članice |
Datum obvestila |
|
5.9.2008 |
Suramox 15 % LA — Stabox 15 % LA |
Glej Prilogo XII |
Glej Prilogo XII |
9.9.2008 |
(1) UL L 311, 28.11.2001, str. 67.
(2) UL L 311, 28.11.2001, str. 1.
DODATEK I
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, PREDLAGATELJEV, IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
Izmišljeno ime Kalijev losartanat |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
||||||
|
Avstrija |
|
Cosaar 12,5 mg — Filmtabletten |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Avstrija |
|
Cosaar 50 mg — Filmtabletten |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Avstrija |
|
Cosaar 100 mg — Filmtabletten |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Cozaar 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Cozaar 50 MG |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Cozaar 12,5 mg |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Cozaar Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Loortan 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Loortan 50 mg |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Loortan 12,50 mg |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Belgija |
|
Loortan Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Bolgarija |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Ciper |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Ciper |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Danska |
|
Cozaar |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Danska |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Danska |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Danska |
|
Cozaar Startpakke |
12,5 mg + 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Estonija |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Estonija |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Estonija |
|
Cozaar 12,5 mg |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Finska |
|
Cozaar |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Finska |
|
Cozaar |
12,5 mg and 50 mg (initiation pack) |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Finska |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Finska |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Francija |
|
Cozaar 100 mg film-coated tablets |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Francija |
|
Cozaar 50 mg scored coated tablets |
50 mg |
Filmsko obložena tableta z zarezo |
Peroralna uporaba |
||||||
|
Nemčija |
|
Cardopal Start 12,5 mg Filmtabletten |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Lorzaar 100 mg Filmtabletten |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Lorzaar 50 mg Filmtabletten |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Lorzaar Protect 100 mg Filmtabletten |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Lorzaar Protect 50 mg Filmtabletten |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Lorzaar Start 12,5 mg Filmtabletten |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Pinzaar 100 mg Filmtabletten |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Pinzaar 50 mg Filmtabletten |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nemčija |
|
Lorzaar Varipharmstart 12,5 mg Filmtabletten |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Grčija |
|
Cozaar |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Grčija |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Grčija |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Madžarska |
|
Cozaar |
12,5 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Madžarska |
|
Cozaar |
50 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Madžarska |
|
Cozaar |
100 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Irska |
|
Cozaar 50 mg Film-coated tablets |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Irska |
|
Cozaar 100 mg Film-coated tablets |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Irska |
|
Cozaar 12,5 mg Film-coated tablets |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Lortaan 50 mg compresse rivestite con film |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Lortaan 12,5 mg compresse rivestite con film |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Lortaan 100 mg compresse rivestite con film |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Neo-Lotan 50 mg compresse rivestite con film |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Neo-Lotan 12,5 mg compresse rivestite con film |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Neo-Lotan 100 mg compresse rivestite con film |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Losaprex 50 mg compresse rivestite con film |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Losaprex 12,5 mg compresse rivestite con film |
12.5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Italija |
|
Losaprex 100 mg compresse rivestite con film |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Latvija |
|
Cozaar 50 mg film-coated tablets |
50 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Latvija |
|
Cozaar 100 mg film-coated tablets |
100 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Litva |
|
Cozaar (Losartan) |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Litva |
|
Cozaar (Losartan) |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Litva |
|
Cozaar (Losartan) |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Cozaar 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Cozaar 50 MG |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Cozaar 12,5 mg |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Cozaar Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Loortan 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Loortan 50 mg |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Loortan 12,50 mg |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Loortan Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Malta |
|
“Cozaar 100 mg” pilloli miksija b'rita |
10 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Malta |
|
“Cozaar 50 mg” pilloli miksija b'rita |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nizozemska |
|
Cozaar 50 |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Nizozemska |
|
Cozaar 100 |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Poljska |
|
Cozaar |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Poljska |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Poljska |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Cozaar 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Cozaar IC |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Cozaar IC — Titulação |
12,5 mg + 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Lortaan IC |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Lortaan IC — Titulação |
12,5 mg + 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Lortaan |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Portugalska |
|
Lortaan 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Romunija |
|
Cozaar, comprimate filmate, 50 mg |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Slovenija |
|
Cozaar 12,5 mg filmsko obložene tablete |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Slovenija |
|
Cozaar 50 mg filmsko obložene tablete |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Slovenija |
|
Cozaar 100 mg filmsko obložene tablete |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Španija |
|
Cozaar 12,5 mg Inicio |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Španija |
|
Cozaar 50 mg |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Španija |
|
Cozaar 100 mg |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Švedska |
|
Cozaar 12,5 mg filmdragerade tabletter |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Švedska |
|
Cozaar 12,5 mg + 50 mg filmdragerade tabletter |
12,5 + 50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Švedska |
|
Cozaar 50 mg filmdragerade tabletter |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Švedska |
|
Cozaar 100 mg filmdragerade tabletter |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Združeno kraljestvo |
|
Cozaar 50 mg Film-coated tablets |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Združeno kraljestvo |
|
Cozaar 25 mg Film-coated tablets |
25 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Združeno kraljestvo |
|
Cozaar 100 mg Film-coated tablets |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Islandija |
|
Cozaar |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Islandija |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Islandija |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Norveška |
|
Cozaar |
12,5 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Norveška |
|
Cozaar |
50 mg |
Filmsko obložena tableta |
Peroralna uporaba |
||||||
|
Norveška |
|
Cozaar |
100 mg |
Filmsko obložena tableta |
Peroralna uporaba |
DODATEK II
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, PREDLAGATELJEV, IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
Izmišljeno ime Kalijev losartanat in hidroklorotiazid |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
|||||||
|
Avstrija |
|
Cosaar Plus — Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Avstrija |
|
Fortzaar-Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Belgija |
|
Cozaar Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Belgija |
|
Cozaar Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Belgija |
|
Loortan Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Belgija |
|
Loortan Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Bolgarija |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Ciper |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Ciper |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Danska |
|
Cozaar Comp. |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Danska |
|
Cozaar Comp. Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Danska |
|
Cozaar Comp. 100 mg/12,5 mg |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Danska |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Estonija |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Estonija |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Finska |
|
Cozaar Comp |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Finska |
|
Cozaar Comp |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Finska |
|
Cozaar Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Francija |
|
Fortzaar 100 mg/25 mg comprimé pelliculé |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Francija |
|
Hyzaar 100 mg/25 mg comprimé pelliculé |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Francija |
|
Fortzaar 50 mg/12,5 mg comprimé pelliculé |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Francija |
|
Hyzaar 50 mg/12,5 mg comprimé pelliculé |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Francija |
|
Fortzaar 100 mg/12,5 mg comprimé pelliculé |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Lorzaar Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Cardopal Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Lorzaar Varipharm Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Fortzaar 100/25 mg Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Fortzaar Varipharm 100/25 mg Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Lorzaar Plus Forte 100/12,5 mg Filmtabletten |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Grčija |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Grčija |
|
Hyzaar 100/25 |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Madžarska |
|
Hyzaar 50/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Madžarska |
|
Hyzaar Forte 100/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Irska |
|
Cozaar' Comp 50 mg/12,5 mg film-coated tablets |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Irska |
|
Cozaar' Comp 100 mg/25 mg film-coated tablets |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Hizaar 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Hizaar 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Forzaar 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Neo-Lotan Plus 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Neo-Lotan Plus 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Losazid 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Italija |
|
Losazid 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Latvija |
|
Hyzaar 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Latvija |
|
Fortzaar 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Litva |
|
Fortzaar (Losartan/Hydrochlorothiazide) |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Litva |
|
Hyzaar (Losartan/Hydrochlorothiazide) |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Luksemburg |
|
Cozaar Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Luksemburg |
|
Cozaar Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Luksemburg |
|
Loortan Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Luksemburg |
|
Loortan Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Malta |
|
“Cozaar Comp” 50/12,5 mg pilloli miksija b'rita |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Malta |
|
“Cozaar Comp” 100/25 mg pilloli miksija b'rita |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Malta |
|
“Cozaar Comp” 100/12,5 mg pilloli miksija b'rita |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nizozemska |
|
Cozaar Plus 100/12,5 |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nizozemska |
|
Fortzaar 100/25 |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Nizozemska |
|
Hyzaar 50/12,5 |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Poljska |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Poljska |
|
Hyzaar Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Cozaar Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Cozaar Plus |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Siaara |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Lortaan Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Lortaan Plus |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Losartan + Hidroclorotiazida Frosst |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Romunija |
|
Hyzaar® 50 mg/12,5 mg comprimate filmate |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Romunija |
|
Fortzaar® 100/25 mg comprimate filmate |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Slovenija |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Slovenija |
|
Hyzaar |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Slovenija |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Španija |
|
Cozaar Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Španija |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Švedska |
|
Cozaar Comp 50 mg/12,5 mg filmdragerade tabletter |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Švedska |
|
Cozaar Comp 100 mg/12,5 mg filmdragerade tabletter |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Švedska |
|
Cozaar Comp Forte 100 mg/25 mg filmdragerade tabletter |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Združeno kraljestvo |
|
Cozaar-Comp 50/12,5 mg film-coated tablets |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Združeno kraljestvo |
|
Cozaar-Comp 100/25 mg film-coated tablets |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Združeno kraljestvo |
|
Cozaar-Comp 100 mg/12,5 mg film-coated tablets |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Islandija |
|
Cozaar-Comp 50/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Islandija |
|
Cozaar-Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Islandija |
|
Cozaar-Comp 100/12,5 mg |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Norveška |
|
Cozaar Comp |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Norveška |
|
Cozaar Comp |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
|||||||
|
Norveška |
|
Cozaar Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmsko obložena tableta |
Peroralna uporaba |
DODATEK III
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, PREDLAGATELJEV/IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
Izmišljeno ime |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
||||||
|
Avstrija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Belgija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Češka republika |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Ciper |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Danska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Estonija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Finska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Francija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Nemčija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Grčija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Madžarska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Islandija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Irska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Italija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Latvija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Litva |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Luksemburg |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Malta |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Nizozemska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Norveška |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Poljska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Portugalska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Slovaška |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Slovenija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Španija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Švedska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
||||||
|
Združeno kraljestvo |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
DODATEK IV
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, PREDLAGATELJEV/IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
Izmišljeno ime |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
|||||||
|
Avstrija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Auxib |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Belgija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Ranacox |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Bolgarija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Češka republika |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Ciper |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Danska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Estonija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Finska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Turox |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Francija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Nemčija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Grčija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Madžarska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Islandija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Irska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Italija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Italija |
|
Algix |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Italija |
|
Recoxib |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Italija |
|
Tauxib |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Latvija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Litva |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Luksemburg |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Ranacox |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Malta |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Nizozemska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Auxib |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Norveška |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Poljska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Exxiv |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Portugalska |
|
Turox |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Romunija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Slovaška |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Slovenija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Španija |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Španija |
|
Exxiv |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Švedska |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Turox |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Združeno kraljestvo |
|
Arcoxia |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||
|
Auxib 90 |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Exxiv 90 |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|||||||||
|
Turox 90 |
90 mg |
Filmsko obložene tablete |
Peroralna uporaba |
DODATEK V
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, PREDLAGATELJEV/IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
Predlagatelj |
Izmišljeno ime |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
|||||
|
Avstrija |
|
|
Noviana 0,5 mg/0,1 mg Filmtabletten |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Belgija |
|
|
Activelle minor comprimés pelliculés |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Bolgarija |
|
|
Eviana филмирани таблетки |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Češka republika |
|
|
Noviana potahované tablety |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Danska |
|
|
Activelle low filmovertrukne tabletter |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Estonija |
|
|
Activelle |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Finska |
|
|
Activelle 0,5 mg/0,1 mg tabl. |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Francija |
|
|
Activelle 0,5 mg/0,1 mg, comprimé pelliculé |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Nemčija |
|
|
Noviana |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Madžarska |
|
|
Noviana filmtabletta |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Islandija |
|
|
Activelle low 0,5 mg/0,1 mg tablets filmuhúðaðar töflur |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Irska |
|
|
Activelle Tablets |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Italija |
|
|
Activelle 0,5 mg/0,1 mg compresse film-rivestite |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Latvija |
|
|
Noviana 0,5 mg/0,1 mg apvalkotās tabletes |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Litva |
|
|
Activelle |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Luksemburg |
|
|
Activelle comprimés pelliculés |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Nizozemska |
|
|
Activelle filmomhulde tabletten |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Norveška |
|
|
Noviana 0,5 mg/0,1 mg tablett filmdrasjert |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Portugalska |
|
|
Activelle |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Romunija |
|
|
Noviana comprimate filmate |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Slovaška |
|
|
Noviana |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Slovenija |
|
|
Noviana filmsko obložene tablete |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Španija |
|
|
Activelle 0,5 mg/ 0,1 mg comprimidos recubiertos de película |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Švedska |
|
|
Activelle |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
|||||
|
Združeno kraljestvo |
|
|
Noviana film-coated tablets |
0,5 mg estradiola (v obliki hemihidrata) + 0,1 mg noretisteronacetata |
Filmsko obložene tablete |
Peroralna uporaba |
DODATEK VI
SEZNAM IMEN, FARMACEVTSKE OBLIKE, JAKOSTI ZDRAVILA, POSTOPKA UPORABE, PROSILCA IN IMETNIKA DOVOLJENJA ZA PROMET V DRŽAVI ČLANICI
|
Država članica |
Imetnik dovoljenja za promet z zdravilom: |
Predlagatelj |
(Izmišljeno ime) ime |
Jakost |
Farmacevtska oblika |
Postopek uporabe zdravila |
||||
|
Avstrija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Belgija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Ciper |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Češka republika |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Danska |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Estonija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Finska |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Francija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Nemčija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Grčija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Madžarska |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Islandija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Ireland |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Italija |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Latvija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Litva |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Luksemburg |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Norveška |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Poljska |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Portugalska |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Slovaška republika |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Slovenija |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Španija |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Švedska |
|
|
Abstral |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
||||
|
Združeno kraljestvo |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Podjezična tableta |
Sublingvalna uporaba |
(1) Odobritev imena v postopku.
DODATEK VII
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet |
INN |
Izmišljeno ime |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
Vsebina (koncentracija) |
|||||||
|
Avstrija |
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Belgija |
Delegation of power:
|
Mirtazapine |
Remergon |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remergon |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Ciper |
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Češka republika |
|
Mirtazapine |
REMERON 15 MG |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
REMERON 30 MG |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON 45 MG |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 15 MG |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 30 MG |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 45 MG |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Danska |
|
Mirtazapine |
Mitazon Smelt |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Mitazon Smelt |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mitazon Smelt |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mitazon |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
||||||||
|
Mirtazapine |
Remeron Smelt |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Oral, opløsning |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Estonija |
|
Mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Finska |
|
Mirtazapine |
Remeron Soltab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron Soltab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Soltab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Perorala raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazon |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
||||||||
|
Mirtazapine |
Mirtazon Smelt |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazon Smelt |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazon Smelt |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Francija |
|
Mirtazapine |
Norset |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Norset |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Norset |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Norset |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Norset |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Norset |
15 mg/ml |
Perorala raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Nemčija |
|
Mirtazapine |
Remergil |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remergil |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergil |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergil |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazapin STADA |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
||||||||
|
Mirtazapine |
Mirtazapin STADA |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapin STADA |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Grčija |
|
Mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Madžarska |
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Islandija |
|
Mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron 15 mg/ml |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Irska |
|
Mirtazapine |
Zispin® film-coated tablets |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Zispin® film-coated tablets |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Zispin® film-coated tablets |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Zispin® oral solution |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Italija |
|
mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Latvija |
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Litva |
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron Sol Tab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Sol Tab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron Sol Tab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Luksemburg |
Delegation of power:
|
Mirtazapine |
Remergon |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remergon |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remergon |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Nizozemska |
|
Mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron drank |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Norveška |
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron mikstur, oppløsning |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Polska |
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Portugalska |
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Perorala raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazon |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
||||||||
|
Mirtazapine |
Mirtazon |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazon |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Romunija |
|
Mirtazapine |
Remeron SolTab 15 mg |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron SolTab 30 mg |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron SolTab 45 mg |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Slovaška republika |
|
Mirtazapine |
REMERON 15 mg |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
REMERON 30 mg |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON 45 mg |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 15 mg |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 30 mg |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 45 mg |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Španija |
|
Mirtazapine |
Rexer |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Rexer |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Rexer |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Rexer |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
||||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Švedska |
|
Mirtazapine |
Remeron |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron-S |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron-S |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Remeron-S |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Združeno kraljestvo |
|
Mirtazapine |
Mirtazapine 15 mg tablets |
15 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||
|
Mirtazapine |
Mirtazapine 30 mg tablets |
30 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapine 45 mg tablets |
45 mg |
Filmsko obložene tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Mirtazapine 15 mg/ml oral solution |
15 mg/ml |
Peroralna raztopina |
Peroralna uporaba |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Zispin SolTab 15 mg orodispersible tablet |
15 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Zispin SolTab 30 mg orodispersible tablet |
30 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
|||||||||
|
Mirtazapine |
Zispin SolTab 45 mg orodispersible tablet |
45 mg |
Orodisperzibilne tablete |
Peroralna uporaba |
|
DODATEK VIII
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, POTI UPORABE ZDRAVILA, PREDLAGATELJEV IN IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
(Izmišljeno) ime |
Jakost |
Farmacevtska oblika |
Pot uporabe zdravila |
||||||
|
Avstrija |
|
Gemzar 200 mg — Trockensubstanz zur Infusionsbereitung |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Avstrija |
|
Gemzar 1 g — Trockensubstanz zur Infusionsbereitung |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Belgija |
|
Gemzar 1000 |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Belgija |
|
Gemzar 200 |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Bolgarija |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Bolgarija |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Češka republika |
|
Gemzar 1 g |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Češka republika |
|
Gemzar 200 mg |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Ciper |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Ciper |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Danska |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Danska |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Estonija |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Estonija |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Finska |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Finska |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Francija |
|
Gemzar 1 000 mg, poudre pour solution pour perfusion |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Francija |
|
Gemzar 200 mg, poudre pour solution pour perfusion |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Nemčija |
|
Gemzar 200 mg Pulver zur Herstellung einer Infusionslösung |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Nemčija |
|
Gemzar 1 g Pulver zur Herstellung einer Infusionslösung |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Grčija |
|
ΓΚΕΜΖΑΡ |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Grčija |
|
ΓΚΕΜΖΑΡ |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Madžarska |
|
Gemzar 1 g powder for injection |
1 g |
Prašek za injiciranje |
Intravenska uporaba |
||||||
|
Madžarska |
|
Gemzar 200 mg powder for injection |
200 mg |
Prašek za injiciranje |
Intravenska uporaba |
||||||
|
Irska |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Irska |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Islandija |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Islandija |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Italija |
|
Gemzar 200 mg powder for solution for infusion and intravesical instillation |
200 mg |
Prašek za raztopino za infundiranje in intravezikalno vstavitev |
Intravenska uporaba in intravezikalna uporaba |
||||||
|
Italija |
|
Gemzar 1 g powder for solution for infusion and intravesical instillation |
1 g |
Prašek za raztopino za infundiranje in intravezikalno vstavitev |
Intravenska uporaba in intravezikalna uporaba |
||||||
|
Latvija |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Latvija |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Litva |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Litva |
|
Gemzar |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Luksemburg |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Luksemburg |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Malta |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Malta |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Nizozemska |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Nizozemska |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Norveška |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Norveška |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Poljska |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Poljska |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Portugalska |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Portugalska |
|
Gemzar |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Romunija |
|
Gemzar 1 g |
1 000 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Romunija |
|
Gemzar 200 mg |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Slovaška |
|
Gemzar 1 g |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Slovaška |
|
Gemzar 200 mg |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Slovenija |
|
Gemzar 200 mg prašek za raztopino za infundiranje |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Slovenija |
|
Gemzar 1 g prašek za raztopino za infundiranje |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Španija |
|
Gemzar 1 g powder for solution for injection |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Španija |
|
Gemzar 200 mg powder for solution for injection |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Švedska |
|
Gemzar |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Švedska |
|
Gemzar |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Združeno kraljestvo |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
||||||
|
Združeno kraljestvo |
|
Gemzar 1g powder for solution for infusion |
1 g |
Prašek za raztopino za infundiranje |
Intravenska uporaba |
DODATEK IX
IME, FARMACEVTSKA OBLIKA, JAKOST ZDRAVILA, ŽIVALSKE VRSTE, POTI UPORABE ZDRAVILA IN IMETNIK DOVOLJENJA ZA PROMET/PREDLAGATELJ
|
Država članica/številka dovoljenja za promet |
Imetnik dovoljenja za promet |
Izmišljeno ime zdravila |
Farmacevtska oblika |
Jakost/zdravilna učinkovina (INN) |
Živalske vrste |
|
Avstrija (8-00694) |
Chevita Tierarzneimittel Ges.m.b.H. |
Asprimax 850 mg/g |
Prašek za peroralno raztopino |
Natrijev salicilat |
Prašiči |
|
Nizozemska (REG NL 8913) |
Dopharma Research B.V. |
NA-SALICYLAAT, 100 %, prašek za peroralno raztopino |
Prašek za peroralno raztopino |
Natrijev salicilat |
Teleta in prašiči |
|
Nizozemska (REG NL 10411) |
Dopharma Research B.V. |
NA-SALICYLAAT, 80 % WSP |
Prašek za peroralno raztopino |
Natrijev salicilat |
Teleta in prašiči |
|
Decentralizirani postopek na podlagi napotitve v skladu s členom 33 (CD 17. aprila 2008) |
Eurovet Animal Health B.V. |
SOLACYL 100 %, prašek za peroralno raztopino za teleta in prašiče |
Prašek za peroralno raztopino |
|
Teleta in prašiči |
DODATEK X
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI VETERINARSKEGA ZDRAVILA, ŽIVALSKIH VRST, NAČINOV UPORABE ZDRAVILA, IMETNIKOV DOVOLJENJA ZA PROMET Z ZDRAVILOM V DRŽAVAH ČLANICAH
|
Država članica |
Izmišljeno ime |
Imetnik dovoljenja za promet z zdravilom Ime in naslov družbe |
Živalske vrste |
Farmacevtska oblika |
Jakost |
Indikacije |
||||||||
|
Avstrija |
Baycox 25 mg/ml Lösung zum Eingeben für Hühner und Puten |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Belgija |
Baycox 2,5 % orale oplossing |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Bolgarija |
Baycox 2,5 % solution |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Bolgarija |
Cevazuril oral solution |
|
Pitovni piščanci, rejenci, kokoši in purani |
Peroralna raztopina |
25 mg/ml |
Preprečevanje in zdravljenje kokcidioze |
||||||||
|
Ciper |
Baycox 2,5 % oral solution |
|
Pitovni piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Češka republika |
Baycox 2,5 % sol. ad us. vet. |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Francija |
Baycox 2,5 % |
|
Piščanci: pitovni piščanci, kokoši in rejenci |
Peroralna raztopina |
25 mg/ml |
Preprečevanje in zdravljenje kokcidioze |
||||||||
|
Francija |
CEVAZURIL |
|
Piščanci: pitovni piščanci, kokoši in rejenci |
Peroralna raztopina |
25 mg/ml |
Preprečevanje in zdravljenje kokcidioze |
||||||||
|
Nemčija |
Baycox 2,5 % |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Grčija |
Baycox 2,5 % oral solution |
|
Pitovni piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Madžarska |
Baycox 2,5 % solution A.U.V. |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Irska |
Baycox 2,5 % Solution |
|
Piščanci |
Peroralna raztopina |
25 mg/ml |
Zdravljenje in spremljanje kokcidioze |
||||||||
|
Italija |
Baycox soluzione 2,5 % |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Italija |
Cevazuril (1) |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Poljska |
Baycox 2,5 % |
|
Pitovni piščanci, rejenci, purani in golobi |
Peroralna raztopina |
25 mg/ml |
Piščanci in purani: zdravljenje kokcidioze Golobi: zdravljenje in preprečevanje kokcidioze |
||||||||
|
Portugalska |
Baycox 2,5 % oral solution |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Romunija |
Cevazuril |
|
Pitovni piščanci, rejenci, kokoši in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Slovaška |
Baycox 2,5 % sol. a.u.v. |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Slovenija |
Baycox 2,5 % w/v oral solution |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Nizozemska |
Baycox 2,5 % |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Nizozemska |
Baycox oplossing 2,5 % |
|
Piščanci in purani |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
||||||||
|
Združeno kraljestvo |
Baycox 2,5 % oral solution |
|
Pitovni piščanci in rejenci pitovnih piščancev |
Peroralna raztopina |
25 mg/ml |
Zdravljenje kokcidioze |
(1) Dovoljenje za promet z zdravilom je bilo preklicano dne 12. junija 2007.
DODATEK XI
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI ZDRAVILA, NAČINOV UPORABE, PREDLAGATELJEV, IMETNIKOV DOVOLJENJA ZA PROMET V DRŽAVI ČLANICI
|
Država članica |
Imetnik dovoljenja za promet v državi članici |
Predlagatelj |
Izmišljeno ime |
Jakost |
Farmacevtska oblika |
Način uporabe |
Vsebina (koncentracija) |
||||||
|
Avstrija |
|
|
Pulairmax 100 μg/Dosis Pulver zur Inhalation |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg/Dosis Pulver zur Inhalation |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg/Dosis Pulver zur Inhalation |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Belgija |
|
|
Pulairmax 100 μg inhalatiepoeder |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg inhalatiepoeder |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg inhalatiepoeder |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Ciper |
|
|
Pulairmax 100 μg Σκόνη για εισπνοή |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg Σκόνη για εισπνοή |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg Σκόνη για εισπνοή |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Češka republika |
|
|
Pulmax 100 μg Prášek k inhalaci |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulmax 200 μg Prášek k inhalaci |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulmax 400 μg Prášek k inhalaci |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Danska |
|
|
Pulairmax |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Estonija |
|
|
Pulairmax |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Finska |
|
|
Pulairmax 100 μg inhalaatiojauhe |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg inhalaatiojauhe |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg inhalaatiojauhe |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Nemčija |
|
|
Pulairmax 100 Mikrogramm/Dosis Pulver zur Inhalation |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 Mikrogramm/Dosis Pulver zur Inhalation |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 Mikrogramm/Dosis Pulver zur Inhalation |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Grčija |
|
|
Pulairmax 100 μg Κόνις για εισπνοή |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg Κόνις για εισπνοή |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg Κόνις για εισπνοή |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Irska |
|
|
Pulairmax 100 μg Inhalation Powder |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg Inhalation Powder |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg Inhalation Powder |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Italija |
|
|
Pulairmax 100 polvere per inalazione |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 mcg polvere per inalazione |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 mcg polvere per inalazione |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Latvija |
|
|
Pulairmax |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Litva |
|
|
Pulairmax |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Luksemburg |
|
|
Pulairmax 100 μg poudre pour inhalation |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg poudre pour inhalation |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg poudre pour inhalation |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Malta |
|
|
Pulairmax 100 μg Trab li jittiehed bin-nifs |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg Trab li jittiehed bin-nifs |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg Trab li jittiehed bin-nifs |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Nizozemska |
|
|
Pulmax 100 mg, inhalatiepoeder |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulmax 200 mg, inhalatiepoeder |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulmax 400 mg, inhalatiepoeder |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Norveška |
|
|
Pulairmax 100 μg inhalasjonspulver |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax 200 μg inhalasjonspulver |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax 400 μg inhalasjonspulver |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Poljska |
|
|
Pulmax 100 μg proszek do inhalacji |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulmax 200 μg proszek do inhalacji |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulmax 400 μg proszek do inhalacji |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Portugalska |
|
|
Pulmax, 100 μg pó para inalação |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulmax, 200 μg pó para inalação |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulmax, 400 μg pó para inalação |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Slovaška |
|
|
Pulmax 100 mcg Inhalačný prášok |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulmax 200 mcg Inhalačný prášok |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulmax 400 mcg Inhalačný prášok |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Španija |
|
|
Budesonida TEVA 100 microgramos polvo para inhalación EFG |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Budesonida TEVA 200 microgramos polvo para inhalación EFG |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Budesonida TEVA 400 microgramos polvo para inhalación EFG |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
|||||||||
|
Švedska |
|
|
Pulairmax |
100 μg |
Prašek za inhalacijo |
Inhalacija |
100 mikrogramov |
||||||
|
Pulairmax |
200 μg |
Prašek za inhalacijo |
Inhalacija |
200 mikrogramov |
|||||||||
|
Pulairmax |
400 μg |
Prašek za inhalacijo |
Inhalacija |
400 mikrogramov |
DODATEK XII
SEZNAM IMEN, FARMACEVTSKIH OBLIK, JAKOSTI, ŽIVALSKIH VRST, POGOSTOSTI IN NAČINOV UPORABE ZDRAVILA, PRIPOROČENIH ODMERKOV, KARENCE IN IMETNIKOV DOVOLJENJA ZA PROMET V DRŽAVAH ČLANICAH, NA KATERE SE NAPOTITVENI POSTOPEK NANAŠA
|
Država članica |
Imetnik dovoljenja za promet z zdravilom |
Izmišljeno ime izdelka |
Farmacevtska oblika |
Jakost |
Živalska vrsta |
Pogostost in način uporabe zdravila |
Priporočeni odmerek |
Karenca (meso in mleko) |
||||
|
Češka republika |
|
Suramox 15 % LA |
Suspenzija za injiciranje |
150 mg/ml |
Govedo, prašiči |
Dve injekciji intramuskularno z vmesnim intervalom 48 ur |
15 mg amoksicilina/kg tt (enakovredno 1ml/10 kg) |
Meso in drobovina: Govedo: 58 dni Prašiči: 35 dni Mleko: 2,5 dni |
||||
|
Španija (1) |
|
Stabox 15 % LA |
Suspenzija za injiciranje |
150 mg/ml |
Govedo, prašiči |
Dve injekciji intramuskularno z vmesnim intervalom 48 ur |
15 mg amoksicilina/kg tt (enakovredno 1ml/10 kg) |
Meso in drobovina: Govedo: 58 dni Prašiči: 35 dni Mleko: 2,5 dni |
||||
|
Italija |
|
Stabox 15 % LA |
Suspenzija za injiciranje |
150 mg/ml |
Govedo, prašiči |
Dve injekciji intramuskularno z vmesnim intervalom 48 ur |
15 mg amoksicilina/kg tt (enakovredno 1ml/10 kg) |
Meso in drobovina: Govedo: 58 dni Prašiči: 35 dni Mleko: 2,5 dni |
||||
|
Francija (2) |
|
Suramox 15 % LA |
Suspenzija za injiciranje |
150 mg/ml |
Govedo, prašiči |
Dve injekciji intramuskularno z vmesnim intervalom 48 ur |
15 mg amoksicilina/kg tt (enakovredno 1ml/10 kg) |
Meso in drobovina: Govedo: 58 dni Prašiči: 35 dni Mleko: 2,5 dni |
(1) Brez dovoljenja za promet.
(2) Referenčna država članica za postopek medsebojnega priznavanja.
INFORMACIJE DRŽAV ČLANIC
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/74 |
Izvleček iz ukrepa prenehanja v skladu s členom 9 Direktive 2001/24/ES Evropskega parlamenta in Sveta o reorganizaciji in prenehanju kreditnih institucij, ki zadeva Kaupthing Bank Luxembourg S.A.
(2008/C 276/04)
ODLOŽITEV PLAČILA
S sodbo z dne 9. oktobra 2008 ob 17. uri je luksemburško okrožno sodišče, ki ima sedež v Luxembourgu in je pristojno za gospodarske zadeve, odobrilo, da lahko delniška družba Kaupthing Bank Luxembourg S.A., vpisana v register gospodarskih družb pod št. 63997 oddelka B, s sedežem na naslovu 35a, avenue J-F Kennedy, L-1855 Luxembourg, uporabi postopek odložitve plačila, kot je določen v delu IV zakona z dne 5. aprila 1993 o finančnem sektorju, kot je bil spremenjen, ter da se uporablja člen 60-2(15) navedenega zakona, na podlagi katerega se zahteva pisna odobritev upraviteljev za vse akte in odločitve Kaupthing Bank Luxembourg S.A. (če se ta odobritev ne predloži, se štejejo akti in odločitve za nične) ter v skladu s katerim lahko upravitelji poslovodnim organom družbe Kaupthing Bank Luxembourg S.A. v razpravo predložijo vse predloge, ki se jim zdijo primerni. Upravitelji so lahko prisotni na razpravah skupščine delničarjev ter upravnih, vodstvenih, poslovodnih ali nadzornih organov Kaupthing Bank Luxembourg S.A.
Ista sodba pooblašča družbo z omejeno odgovornostjo PricewaterhouseCoopers S.à.r.l., ki jo zastopata ga. Emmanuelle Caruel-Henniaux in g. Franz Fayot, kot upravitelja za nadzor nad upravljanjem sredstev delniške družbe Kaupthing Bank Luxembourg S.A. ter za postopek odložitve plačila določa rok šestih mesecev.
Komisija za nadzor finančnega sektorja in delniška družba Kaupthing Bank Luxembourg S.A. lahko vložita pritožbo v petnajstih dneh po uradnem obvestilu o sodbi v skladu z odstavkom 9 člena 60-2 zakona z dne 5. aprila 1993 o finančnem sektorju, kot je bil spremenjen, tj. potem, ko sodna pisarna luksemburškega okrožnega sodišča, ki ima sedež v Luxembourgu in je pristojno za gospodarske zadeve, v obliki priporočenega pisma pošlje uradno obvestilo o navedeni sodbi. Pritožba se v obliki pisne izjave predloži navedeni sodni pisarni.
Zoper sodbo ni mogoče vložiti pritožbe niti pritožbe tretjih strank.
V potrditev pravilnosti izvlečka sodbe,
Upravitelji
PricewaterhouseCoopers S.à.r.l., ki jo zastopata ga. Emmanuelle Caruel-Henniaux in g. Franz Fayot
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/75 |
Podatki, ki jih predložijo države članice o državni pomoči, dodeljeni na podlagi Uredbe Komisije (ES) št. 70/2001 o uporabi členov 87 in 88 Pogodbe ES pri pomoči za majhna in srednje velika podjetja
(Besedilo velja za EGP)
(2008/C 276/05)
|
Številka pomoči |
XS 193/08 |
||||||||||
|
Država članica |
Republika Bolgarija |
||||||||||
|
Regija |
Območje po členu 87(3)(a) Pogodbe ES |
||||||||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
Shema dodelitve nepovratne pomoči v okviru ukrepa „Dodajanje vrednosti kmetijskim in gozdarskim proizvodom“ v zvezi s programom razvoja podeželja za obdobje 2007-2013 za:
|
||||||||||
|
Pravna podlaga |
Zakonodaja EU:
Zakonodaja Republike Bolgarije:
|
||||||||||
|
Načrtovani letni izdatki po shemi ali skupni znesek individualne pomoči, dodeljene podjetju |
Shema pomoči |
Skupni letni znesek |
34,4 mio EUR (1) |
||||||||
|
Zavarovana posojila |
|
||||||||||
|
Individualna pomoč |
Skupni znesek pomoči |
|
|||||||||
|
Zavarovana posojila |
|
||||||||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
Da (največ 50 %) |
|||||||||
|
Datum začetka izvajanja |
Po soglasju Evropske komisije k spremembi poglavja 9 („Elementi, potrebni za oceno po pravilih konkurence, in seznam shem pomoči, odobrenih v skladu s členi 87, 88 in 89 Pogodbe“) programa razvoja podeželja za obdobje 2007-2013 in vključitvi registrske številke te državne pomoči v poglavje 9 |
||||||||||
|
Trajanje sheme ali individualne pomoči |
Do 31.12.2013 |
||||||||||
|
Cilj pomoči |
Pomoč majhnim in srednje velikim podjetjem (MSP) |
Da |
|||||||||
|
Zadevni gospodarski sektorji |
Pomoč je omejena na posebne sektorje |
Da |
|||||||||
|
Druge predelovalne dejavnosti |
Da (2) |
||||||||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
||||||||||
|
|||||||||||
|
Individualne pomoči v visokih zneskih |
V skladu s členom 6 Uredbe |
Ne |
|||||||||
|
Številka pomoči |
XS 201/08 |
||||||
|
Država članica |
Italija |
||||||
|
Regija |
Sardegna |
||||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
Contributi per impianti fotovoltaici |
||||||
|
Pravna podlaga |
Articolo 24, L.R. 29 maggio 2007, n. 2 Deliberazioni Giunta Regionale n. 21/37 del 8.4.2008 e n. 34/22 del 19.6.2008 DDS n. 366 del 25.6.2008 |
||||||
|
Vrsta ukrepa |
Shema pomoči |
||||||
|
Proračun |
Načrtovani letni izdatki: 10 mio EUR |
||||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe: Pomoč, odobrena podjetjem, ki se nahajajo v delih regije, ki so upravičeni do pomoči v skladu s Karto regionalnih državnih pomoči 2007-2013, objavljeno v UL C 90, 11.4.2008, je sestavljena iz dodeljenih sredstev, ki ne presegajo 20 % upravičenih stroškov postavitve fotovoltaičnega elektroenergetskega sistema. Za podjetja, ki se nahajajo v posebnih katastrskih oddelkih regije, ki niso upravičeni do pomoči in ki so navedeni v Karti regionalnih državnih pomoči 2007-2013, je največja intenzivnost pomoči omejena na:
Pomoč se odobri pod pogojem, da naložba ostane v regiji vsaj pet let in da lastna sredstva upravičenca znašajo vsaj 25 % upravičene naložbe. Pomoč je v skladu z ukrepi za spodbujanje proizvodnje električne energije z uporabo fotovoltaičnih elektroenergetskih sistemov, določenih v D.M. z dne 28. julija 2005, kakor je bil spremenjen z D.M. z dne 6. februarja 2006 in D.M. z dne 19. februarja 2007 („energetski račun“). Ta pomoč se ne sme kumulirati z nobeno drugo regionalno in državno pomočjo ter pomočjo Skupnosti |
||||||
|
Datum začetka izvajanja |
18.7.2008 |
||||||
|
Trajanje sheme ali individualne pomoči |
18.9.2008 |
||||||
|
Cilj pomoči |
MSP |
||||||
|
Zadevni gospodarski sektorji |
Vsi sektorji, upravičeni do pomoči za MSP |
||||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
||||||
|
Drugi podatki |
Ukrep se izvaja preko javnega razpisa s postopkom, ki temelji na oceni in razvrščanju zahtevkov. Prednost bodo imeli zahtevki, ki bodo potrebovali manj javne pomoči, kot jo je največ mogoče pridobiti, to je 20 %. Za podjetja, ki se nahajajo v predelih, ki niso upravičeni do regionalne pomoči, je zmanjšanje intenzivnosti pomoči v skladu z zgornjo mejo, ki jo določa Uredba (ES) št. 70/2001 |
|
Št. pomoči |
XS 209/08 |
|||||||||
|
Država članica |
Grčija |
|||||||||
|
Regija |
— |
|||||||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
«ΕΝΙΣΧΥΣΗ ΤΗΣ ΑΝΤΑΓΩΝΙΣΤΙΚΟΤΗΤΑΣ ΚΑΙ ΤΗΣ ΚΑΙΝΟΤΟΜΙΑΣ ΤΩΝ ΜΙΚΡΟΜΕΣΑΙΩΝ ΕΠΙΧΕΙΡΗΣΕΩΝ ΣΤΟΥΣ ΤΟΜΕΙΣ ΤΗΣ ΜΕΤΑΠΟΙΗΣΗΣ ΚΑΙ ΤΟΥ ΤΟΥΡΙΣΜΟΥ» (3η προκήρυξη) [«ENISHYSI TIS ANTAGONISTIKOTITAS KAI TIS KAINOTOMIAS TON MIKROMESAION EPIHEIRISEON STOYS TOMEIS TIS METAPOIISIS KAI TOY TOYRISMOY» (3i prokiryksi)] |
|||||||||
|
Pravna podlaga |
Άρθρο 35 του Ν. 3016/2002 (ΦΕΚ 110 Α'/17-05-2002) ΥΑ 41630/ΕΥΣ9450/7.11.2005 (ΦΕΚ 1651/B'/29.11.05) ΚΥΑ 14871/EYΣ3047/20.4.2005 (ΦΕΚ 575/ΤΒ/28.04.2005) ΥΑ 39059/ΕΥΣ9047/14.10.2005 (ΦΕΚ 1539/Β/8.11.2005) ΚΥΑ 1707/ΕΥΣ443/17.01.2006 (ΦΕΚ 42/Β/19.01.2006) |
|||||||||
|
Vrsta ukrepa |
Shema pomoči |
|||||||||
|
Proračun |
Načrtovani letni izdatki: 400 mio EUR |
|||||||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
|||||||||
|
Datum začetka izvajanja |
15.3.2006 |
|||||||||
|
Trajanje |
30.6.2007 |
|||||||||
|
Cilj |
Mala in srednja podjetja |
|||||||||
|
Gospodarski sektorji |
Vse predelovalne dejavnosti, turizem |
|||||||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
|
Št. pomoči |
XS 211/08 |
|||
|
Država članica |
Nemčija |
|||
|
Regija |
Freie und Hansestadt Hamburg |
|||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
|
|||
|
Pravna podlaga |
Verordnung (EG) Nr. 70/2001 der Kommission vom 12. Januar 2001 über die Anwendung der Artikel 87 und 88 EG-Vertrag auf staatliche Beihilfen an kleine und mittlere Unternehmen (ABl. EG 13.1.2001 L 10/33 verlängert durch ABl. EU 23.12.2006 L 368/85); Gesetz über die Kreditkommission vom 29.4.1997 (Hamburgisches Gesetz- und Verordnungsblatt 1997, Nr. 18, S. 133) |
|||
|
Vrsta ukrepa |
Ad hoc |
|||
|
Proračun |
Skupni znesek načrtovane pomoči: 3 450 EUR |
|||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
|||
|
Datum začetka izvajanja |
14.8.2008 |
|||
|
Trajanje |
14.2.2009 |
|||
|
Cilj |
Mala in srednja podjetja |
|||
|
Gospodarski sektorji |
Druge storitve |
|||
|
Naziv in naslov organa, ki dodeli pomoč |
|
|
Št. pomoči |
XS 212/08 |
|||
|
Država članica |
Nemčija |
|||
|
Regija |
Freie und Hansestadt Hamburg |
|||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
|
|||
|
Pravna podlaga |
Verordnung (EG) Nr. 70/2001 der Kommission vom 12. Januar 2001 über die Anwendung der Artikel 87 und 88 EG-Vertrag auf staatliche Beihilfen an kleine und mittlere Unternehmen (ABl. EG 13.1.2001 L 10/33 verlängert durch ABl. EU 23.12.2006 L 368/85); Gesetz über die Kreditkommission vom 29.4.1997 (Hamburgisches Gesetz- und Verordnungsblatt 1997, Nr. 18, S. 133) |
|||
|
Vrsta ukrepa |
Ad hoc |
|||
|
Proračun |
Skupni znesek načrtovane pomoči: 6 750 EUR |
|||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
|||
|
Datum začetka izvajanja |
31.7.2008 |
|||
|
Trajanje |
31.1.2009 |
|||
|
Cilj |
Mala in srednja podjetja |
|||
|
Gospodarski sektorji |
Druge storitve |
|||
|
Naziv in naslov organa, ki dodeli pomoč |
|
(1) Letni znesek je okviren in izračunan na osnovi sredstev, predvidenih za ukrep 123 „Dodajanje vrednosti kmetijskim in gozdarskim proizvodom“ v zvezi s programom razvoja podeželja za obdobje 2007–2013 (241 mio EUR v tekočih cenah).
(2) Do pomoči so upravičeni naslednji sektorji, ki se ukvarjajo s predelavo in/ali trženjem proizvodov, določenih v Prilogi I k Pogodbi ES:
|
— |
mleko in mlečni izdelki (predvsem NACE 15.5), |
|
— |
meso in mesni izdelki (predvsem NACE 15.1), |
|
— |
sadje in vrtnine, vključno z gobami (predvsem NACE 15.3), |
|
— |
predelava medu (ni jasne klasifikacije NACE, lahko pa se nanaša na NACE 15.89), |
|
— |
žita, proizvodi mlinske industrije in škrobni izdelki (predvsem NACE 15.6), |
|
— |
rastlinska in živalska olja in maščobe (predvsem NACE 15.4), |
|
— |
predelava industrijskih in zdravilnih rastlin, vključno z vrtnicami, ki vsebujejo olje, zelišči in nepredelanim tobakom (ni jasne klasifikacije NACE, delno pa spada pod NACE 24.63), |
|
— |
krmila (krma) (predvsem NACE 15.71), |
|
— |
grozdni mošt, vino in kis (predvsem NACE 15.87 in 15.93). |
Do pomoči so upravičeni vsi sektorji, ki se ukvarjajo s proizvodnjo energije iz rastlinskih in živalskih proizvodov primarne in sekundarne biomase, določenih v Prilogi I k Pogodbi ES, razen ribjih proizvodov (ni jasne klasifikacije NACE).
|
— |
Sektorji, ki se ukvarjajo s predelavo in/ali trženjem gozdarskih proizvodov, razen pohištvene industrije (predvsem NACE 20.10, 20.30, 20.40, 20.51). |
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/79 |
Podatki, ki jih predložijo države članice o državni pomoči, dodeljeni na podlagi Uredbe Komisije (ES) št. 70/2001 o uporabi členov 87 in 88 Pogodbe ES pri pomoči za majhna in srednje velika podjetja
(Besedilo velja za EGP)
(2008/C 276/06)
|
Št. pomoči |
XS 213/08 |
||||||
|
Država članica |
Združeno kraljestvo |
||||||
|
Regija |
East Midlands |
||||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
Hathersage Developments Ltd |
||||||
|
Pravna podlaga |
RDA Act 1998 |
||||||
|
Vrsta ukrepa |
Ad hoc |
||||||
|
Proračun |
Skupni znesek načrtovane pomoči: 0,33 mio GBP |
||||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
||||||
|
Datum začetka izvajanja |
14.1.2008 |
||||||
|
Trajanje |
31.3.2009 |
||||||
|
Cilj |
Mala in srednja podjetja |
||||||
|
Gospodarski sektorji |
Strokovne, znanstvene in tehnične dejavnosti |
||||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
|
Št. pomoči |
XS 214/08 |
||||
|
Država članica |
Združeno kraljestvo |
||||
|
Regija |
North East England |
||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
Python Properties |
||||
|
Pravna podlaga |
Industrial Development Act 1982 sections 7 and 11 Local Government Act 2000 section 2 |
||||
|
Vrsta ukrepa |
Shema pomoči |
||||
|
Proračun |
Načrtovani letni izdatki: 0,3 mio GBP |
||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
||||
|
Datum začetka izvajanja |
3.3.2008 |
||||
|
Trajanje |
31.12.2008 |
||||
|
Cilj |
Mala in srednja podjetja |
||||
|
Gospodarski sektorji |
Vse predelovalne dejavnosti, druge storitve |
||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
|
Št. pomoči |
XS 215/08 |
||||||
|
Država članica |
Združeno kraljestvo |
||||||
|
Regija |
West Midlands |
||||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
Premium Vehicles Centres of Excellence Projects — Warwick University |
||||||
|
Pravna podlaga |
Regional Development Agencies Act 1998 |
||||||
|
Vrsta ukrepa |
Shema pomoči |
||||||
|
Proračun |
Načrtovani letni izdatki: 2,2 mio GBP |
||||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
||||||
|
Datum začetka izvajanja |
15.8.2008 |
||||||
|
Trajanje |
31.12.2013 |
||||||
|
Cilj |
Mala in srednja podjetja |
||||||
|
Gospodarski sektorji |
Vse predelovalne dejavnosti |
||||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
|
Št. pomoči |
XS 219/08 |
||||
|
Država članica |
Nizozemska |
||||
|
Regija |
— |
||||
|
Naziv sheme pomoči ali ime podjetja, ki prejme individualno pomoč |
Subsidieregeling innovatiekredieten-module van de Experimentele kaderregeling subsidies innovatieprojecten |
||||
|
Pravna podlaga |
Kaderwet EZ subsidies |
||||
|
Vrsta ukrepa |
Shema pomoči |
||||
|
Proračun |
Načrtovani letni izdatki: 20,3 mio EUR |
||||
|
Največja intenzivnost pomoči |
V skladu s členom 4(2)–(6) in členom 5 Uredbe |
||||
|
Datum začetka izvajanja |
5.7.2008 |
||||
|
Trajanje |
5.7.2012 |
||||
|
Cilj |
Mala in srednja podjetja |
||||
|
Gospodarski sektorji |
Vsi sektorji, upravičeni do pomoči za MSP |
||||
|
Naziv in naslov organa, ki dodeli pomoč |
|
V Objave
UPRAVNI POSTOPKI
Komisija
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/82 |
Javni razpis, ki ga je objavila Italija na podlagi člena 4(1)(d) Uredbe Sveta (EGS) št. 2408/92, za opravljanje rednih zračnih prevozov na progi Albenga–Rim Fiumicino in v obratni smeri
(Besedilo velja za EGP)
(2008/C 276/07)
UVOD
Italijanska vlada (Ministrstvo za infrastrukturo in promet) je na podlagi člena 4 Uredbe (EGS) št. 2408/92 in v skladu z odločitvami uradnega srečanja pristojnih služb, ki je potekalo pri upravi dežele Ligurija, odobrila ta javni razpis za dodelitev koncesije za opravljanje zračnega prevoza na progi: Albenga–Rim Fiumicino in v obratni smeri
Standardi, ki izhajajo iz obveznosti javne službe, so bili objavljeni v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008.
Če se v 30 dneh od objave navedene obveznosti ne prijavi noben letalski prevoznik, ki bi začel zračne prevoze na omenjeni progi v skladu z obveznostmi javne službe brez dodatnega finančnega nadomestila, je italijanska vlada (Ministrstvo za infrastrukturo in promet) v skladu s postopkom iz člena 4(1)(d) Uredbe (EGS) št. 2408/92 sklenila, da bo omogočila dostop do te proge samo enemu prevozniku in mu na podlagi javnega razpisa dodelila pravico do opravljanja teh prevozov po navedeni uredbi.
SPLOŠNE DOLOČBE
Ta javni razpis določa predmet razpisa, pravila sodelovanja na razpisu, pravila glede trajanja, spremembe ali izteka veljavnosti pogodbe, kazni zaradi neizpolnjevanja pogodbenih določil ter glede jamstva za resnost ponudbe in garancije za dobro izvedbo pogodbenih obveznosti.
Pravica do opravljanja prevozov na navedeni progi bo z javnim razpisom dodeljena ponudniku, ki bo cenovno najugodnejši glede na znesek finančnega nadomestila, določenega v točki 6 tega razpisa.
1. Predmet javnega razpisa
Opravljanje rednih letalskih prevozov na progi Albenga–Rim Fiumicino in v obratni smeri v skladu z obveznostjo javne službe, objavljene v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008 na podlagi določb Uredbe (EGS) št. 2408/92.
2. Sodelovanje na javnem razpisu
Ponudbe lahko predložijo vsi letalski prevozniki iz Skupnosti, kot so opredeljeni v členu 2(b) Uredbe (EGS) št. 2408/92 in izpolnjujejo naslednje zahteve:
Splošne zahteve
|
1. |
niso v stečaju ali v postopku prisilne likvidacije, niso sklenili dogovora z upniki ter niso v postopku za ugotovitev česa od navedenega; |
|
2. |
ni jim bilo s sodbo prepovedano opravljanje dejavnosti v skladu s členom 9(2) Zakonodajnega dekreta št. 231/2001 in ni jim bilo prepovedano sklepati pogodb z javno upravo; |
|
3. |
izpolnjujejo obveznosti glede plačevanja prispevkov za socialno varnost; |
|
4. |
niso prijavili lažnih podatkov glede izpolnjevanja zahtev za sodelovanje na drugih javnih razpisih za opravljanje rednih zračnih prevozov na podlagi obveznosti javne službe. |
Kandidat dokaže, da izpolnjuje navedene pogoje tako, da za točko 3 predloži potrdilo o rednem plačevanju prispevkov, ki ga izda INPS ali INAIL, in potrdilo iz člena 17 Zakona št. 68 z dne 12. marca 1999 o pravicah invalidnih oseb do dela; za točke 1, 2 in 4 pa predloži izjavo, ki nadomešča potrdilo o izpolnjevanju pogojev v skladu s členoma 46 in 47 Predsedniškega dekreta št. 445 z dne 28. decembra 2000.
Kandidati, ki imajo sedež v drugih državah članicah Evropske unije in ne v Italiji, morajo predložiti potrdila ali dokazila, ki jih izdajo uprave ali organi v državi porekla, skupaj s prevodom v italijanski jezik, ki ga overi italijanski konzulat in potrdi, da prevod ustreza izvirniku.
Tehnične zahteve
|
1. |
operativna licenca, podeljena v skladu z Uredbo (EGS) št. 2407/92; |
|
2. |
obvezno zavarovanje za primer nesreče, zlasti za zavarovanje potnikov, prtljage, blaga, ki se prevaža, in tretjih oseb v skladu z Uredbo (ES) št. 785/2004; |
|
3. |
spričevalo letalskega prevoznika (COA) v skladu z zakonodajo Skupnosti; |
|
4. |
ne smejo biti na t. i. „črnem seznamu“ letalskih prevoznikov, ki ne izpolnjujejo evropskih varnostnih standardov, kakor je objavljen na spletni strani: http://ec.europa.eu/transport/air-ban; |
|
5. |
sistem stroškovnega računovodstva, ki omogoča razčlenitev zadevnih stroškov (vključno s stalnimi stroški in prihodki). |
Letalski prevozniki, ki po predložitvi ponudbe ne izpolnjujejo več navedenih pogojev, so samodejno izločeni iz postopka ocenjevanja.
Če letalski prevoznik po sklenitvi pogodbe ne izpolnjuje več pogojev iz točke 5, se uporabijo določbe iz točke 14 in predzadnjega odstavka točke 15 tega javnega razpisa.
3. Postopek
Za ta javni razpis veljajo določbe člena 4(1)(d), (e), (f), (h) in (i) Uredbe Sveta (EGS) št. 2408/92.
4. Razpisna dokumentacija
Celotna razpisna dokumentacija s posebnimi pravili, ki se uporabljajo za razpis, vključno z veljavnostjo ponudb in z vsemi drugimi informacijami, ki so lahko koristne, je sestavni del tega razpisa skupaj z vzorcem pogodbe iz točke 5 in jo je mogoče brezplačno zahtevati na naslovu: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio, 118, I-00185 Roma, ali na elektronskem naslovu: trasporto.aereo@enac.rupa.it.
5. Pogodba o opravljanju prevozov
Opravljanje prevozov bo urejala pogodba med letalskim prevoznikom in ENAC, sestavljena na podlagi vzorca pogodbe, ki je del razpisne dokumentacije.
6. Finančno nadomestilo
Najvišji znesek finančnega nadomestila, ki je na voljo po razpisu za dodelitev koncesije za opravljanje zračnega prevoza na zadevni progi, je 979 112,85 EUR (devetsto devetinsedemdeset tisoč sto dvanajst/85) letno vključno z DDV.
Ponudbe je treba sestaviti v skladu z razpisno dokumentacijo, v obrazcu za finančni del ponudbe pa je treba izrecno navesti zahtevani znesek nadomestila za opravljanje zadevnih prevozov, ki ne presega navedenega zneska.
Natančen znesek nadomestila se ob koncu leta veljavnosti Pogodbe določi za nazaj glede na dejanske odhodke in prihodke, nastale z opravljanjem prevozov, na podlagi predloženih dokazil in v mejah zneska, navedenega v ponudbi, kakor je določeno v razpisni dokumentaciji.
Letalski prevoznik v nobenem primeru ne more zahtevati finančnega nadomestila, ki presega zgornjo mejo iz pogodbe, ker plačilo ni povračilo, temveč nadomestilo za opravljanje prevozov v skladu z obveznostmi javne službe.
Plačila za leto, ko je pogodba veljavna, se izplačajo s predplačili in poračunom v skladu z določbami razpisne dokumentacije brez poseganja v preglede, ki jih izvaja ENAC, da ugotovi dejansko namenskost nadomestila in izpolnjevanje zahtev s strani letalskega prevoznika. Končni znesek se plača po natančnem pregledu računovodskih izkazov, ki jih prevoznik predloži za zadevno progo, in po ugotovitvi, da se prevozi opravljajo v skladu s pogodbo.
7. Cene
V predloženih ponudbah je treba navesti cene prevozov, ki so določene v obvestilu o uvedbi obveznosti javne službe, objavljenem v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008.
8. Začetek opravljanja prevozov
Prevozi se začnejo izvajati 15 (petnajst) dni po sklenitvi pogodbe, začetek opravljanja prevozov pa se potrdi z ustreznim zapisnikom, ki ga podpišeta letalski prevoznik in ENAC.
9. Trajanje pogodbe
Pogodba traja eno leto od dneva, ko se dejansko začnejo zračni prevozi na zadevni progi.
Letalski prevoznik mora dati ENAC na voljo osebje, tehnično in računovodsko dokumentacijo, naprave in vse drugo, kar je potrebno za spremljanje in nadzor pravilnega izpolnjevanja, uporabe in izvajanja določb iz obvestila Komisije, dekreta o uvedbi obveznosti, tega razpisa, pogodbe in razpisne dokumentacije.
Za neizpolnjevanje navedenih obveznosti so določene kazni v skladu s točko 11 tega javnega razpisa.
10. Odpoved pogodbe
Pogodbeni stranki lahko pogodbo pred običajnim iztekom njene veljavnosti prekineta s šestmesečnim odpovednim rokom.
Kadar prevoznik preneha izpolnjevati obveznosti javne službe, se šteje, da je od pogodbe odstopil brez odpovednega roka, razen če ponovno ne začne leteti v skladu z obveznostmi javne službe najpozneje 30 dni od prejema zadevnega opomina ENAC.
Če prevoznik odstopi od pogodbe, si ENAC pridržuje pravico, da ustrezno oceni, ali naj Ministrstvu za infrastrukturo in promet predlaga sklenitev nove pogodbe z naslednjim najvišje uvrščenim prevoznikom na razpisu. Pogoji izvajanja obveznosti in sorazmernost nadomestila so enaki kot pri prvi dodelitvi obveznosti javne službe.
11. Neizpolnjevanje obveznosti in kazni
Prevoznik ne krši pogodbe, če prevoze preneha opravljati zaradi naslednjih razlogov:
|
— |
nevarnih vremenskih razmer, |
|
— |
zaprtja enega od letališč iz delovnega programa, |
|
— |
težav, povezanih z varnostjo, |
|
— |
stavk, |
|
— |
višje sile. |
Pri prekinitvi opravljanja zračnih prevozov iz navedenih razlogov se znesek finančnega nadomestila sorazmerno zmanjša glede na število odpovedanih letov.
Pri neizpolnjevanju nalog in obveznosti, prevzetih s pogodbo, lahko ENAC naloži letalskemu prevozniku plačilo kazni, ki je sorazmerna s številom kršitev, kot je določeno v vzorcu pogodbe.
Kazen v nobenem primeru ne sme biti višja od 50 % najvišjega zneska finančnega nadomestila iz točke 6 tega razpisa, pri čemer ima ENAC v primeru preseganja navedene meje pravico do odpovedi pogodbe zaradi neizpolnjevanja obveznosti, s čimer takoj preneha tudi obveznost plačila nezapadlih zneskov nadomestila.
Letno število odpovedanih letov iz razlogov, za katere je neposredno odgovoren prevoznik, ne sme preseči 2 % števila predvidenih letov.
Pri preseganju omenjenega števila mora prevoznik plačati ENAC kazen v višini 3 000,00 EUR (tri tisoč) za vsak odpovedani let nad mejo 2 %, in sicer na podlagi uradnega obvestila, ki se prevozniku pošlje najpozneje 10 dni po seznanitvi z dogodkom. Prevoznik lahko predloži morebitne pripombe najpozneje v sedmih dneh.
ENAC poleg tega popravi tudi znesek nadomestila sorazmerno s številom opravljenih letov. Zneski, prejeti iz tega naslova, bodo namenjeni izboljšanju prometne povezanosti mesta Albenga.
Neupoštevanje odpovednega roka iz točke 10 se kaznuje z zneskom, ki se izračuna na podlagi predvidenega nadomestila in števila zamujenih dni odpovednega roka od dneva prenehanja prevozov z obveznostjo javne službe, pod pogoji iz točke 10 in po enačbi:
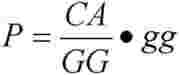
Pri čemer je:
|
P |
= |
znesek kazni |
|
CA |
= |
znesek letnega nadomestila |
|
GG |
= |
število dni zadevnega leta (365 ali 366) |
|
gg |
= |
število zamujenih dni odpovednega roka |
Kazni iz te točke se lahko seštevajo s kaznimi, ki jih določajo predpisi Skupnosti in nacionalni predpisi.
12. Jamstvo za resnost ponudbe
Da bi dokazali resnost in zanesljivost ponudbe, morajo prevozniki, ki sodelujejo na razpisu, položiti jamstvo v višini 2 % skupnega zneska nadomestila iz točke 6 bodisi v obliki varščine bodisi v obliki zavarovalnega ali bančnega jamstva.
Načini predložitve navedenega jamstva so določeni v razpisni dokumentaciji in so lahko navedeni tudi v pogodbi.
Jamstvo mora biti veljavno najmanj 180 (sto osemdeset) dni po izteku roka za oddajo ponudb, prevozniki pa se morajo zavezati, da bodo njegovo veljavnost med razpisnim postopkom na zahtevo ENAC podaljšali, če se ta ne konča pred iztekom veljavnosti jamstva.
Ko ENAC prevoznike obvesti, da niso bili izbrani na razpisu, se jamstvo sprosti.
13. Jamstvo za dobro izvedbo pogodbenih obveznosti in zavarovalno kritje
Prevoznik, ki mu je bilo dodeljeno opravljanje zračnih prevozov v skladu z obveznostmi javne službe s tem razpisom, mora predložiti bančno ali zavarovalno jamstvo v višini 400 000,00 EUR (štiristo tisoč) v korist ENAC, ki si pridržuje pravico do njene uporabe za zagotovitev neprekinjenega izvajanja obveznosti javne službe.
Jamstvo se samodejno sprosti brez odobritve ENAC, če je izid pregleda iz zadnjega odstavka točke 6 pozitiven.
14. Izguba pravice do finančnega nadomestila
Če letalski prevoznik kadar koli po sklenitvi pogodbe ne izpolnjuje splošnih in tehničnih pogojev iz točke 2 tega razpisa in zahtev iz razpisne dokumentacije, izgubi pravico do opravljanja prevozov na zadevni progi in pravico do finančnega nadomestila, vrniti pa mora tudi vse neupravičeno prejete zneske, vključno z zamudnimi obrestmi.
Po prenehanju pravice do opravljanja prevozov na zadevni progi lahko Ministrstvo za infrastrukturo in promet pooblasti ENAC, da sklene drugo pogodbo za preostalo obdobje opravljanja prevozov z naslednjim najvišje uvrščenim prevoznikom na razpisu.
V tem primeru velja pogodba od dneva začetka opravljanja prevozov do datuma, ko naj bi se v razdrti pogodbi nehali prevozi, v skladu z delovnim načrtom, ki je bil odobren, ko je bila ocenjena ponudba najugodnejšega ponudnika.
15. Razdrtje pogodbe
Če prevoznik ne izpolnjuje določbe obvestila o uvedbi obveznosti, objavljenega v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008, zadevnega dekreta o uvedbi obveznosti, pogodbe, razpisa in razpisne dokumentacije, lahko ENAC na podlagi člena 1454 Civilnega zakonika pošlje pisno obvestilo prevozniku, ta pa ima 15 (petnajst) dni časa po prejemu takega obvestila, da odpravi neizpolnjevanje določb.
Če tega ne naredi v navedenem roku, ENAC lahko šteje, da je pogodbo razdrl, trajno zadrži znesek jamstva iz točke 13 in od prevoznika zahteva nadomestilo za nastalo škodo.
Poleg tega ima ENAC po členu 1456 Civilnega zakonika pravico, da razdre pogodbo s pisnim obvestilom prevozniku, če ta ne izpolnjuje obveznosti in nalog iz pogodbe, s tega razpisa in razpisne dokumentacije.
Pri razdrtju pogodbe lahko Ministrstvo za infrastrukturo in promet pooblasti ENAC, da sklene novo pogodbo za preostalo obdobje opravljanja zračnih prevozov z naslednjim najvišje uvrščenim prevoznikom na razpisu.
V tem primeru velja pogodba od dneva začetka opravljanja prevozov do datuma, ko naj bi se v razdrti pogodbi nehali prevozi, v skladu z delovnim načrtom, ki je bil odobren, ko je bila ocenjena ponudba najugodnejšega ponudnika.
16. Predložitev ponudb
Ponudbe, sestavljene v skladu z razpisno dokumentacijo, sicer se izločijo iz postopka, je treba v 30 (tridesetih) dneh od objave tega javnega razpisa v Uradnem listu Evropske unije poslati s priporočeno pošiljko s povratnico ali vročiti osebno s potrdilom o prejemu na naslov: ENAC, Direzione Generale, viale del Castro Pretorio, 118, I-00185 Roma.
Ponudbe morajo biti v zaprti in zapečateni ovojnici, sicer se izločijo iz postopka.
Zunanja ovojnica, ki je zaprta, zapečatena in parafirana na obeh straneh in po robovih, mora vsebovati dve notranji ovojnici, prav tako zapečateni in parafirani, opremljeni z naslednjim pripisom: „Offerta per la gara in oneri di servizio pubblico sulla rotta Albenga-Roma Fiumicino e viceversa“.
Dokumenti, ki jih morata vsebovati navedeni ovojnici, so navedeni v razpisni dokumentaciji iz točke 4 tega javnega razpisa.
Razume se, da je izključno pošiljatelj odgovoren, če ovojnica iz kakršnega koli razloga ne prispe na naslov prejemnika do navedenega roka.
Če bo predložena samo ena veljavna ponudba, se razpisni postopek izvede.
17. Čas veljavnosti ponudb
180 (sto osemdeset) dni po roku za oddajo ponudb.
18. Oddaja naročila
Razpis izvede ENAC s komisijo, ki jo sestavljajo vodstveni uslužbenec ENAC, ki ga pooblasti generali direktor, izvedenec, ki ga imenuje dežela Ligurija, in predsednik, ki ga sporazumno imenujeta ENAC in dežela Ligurija; naloge tajništva opravlja ENAC.
19. Obdelava osebnih podatkov
Vsi osebni podatki se bodo uporabljali in obdelovali izključno za uradne potrebe, ob tem pa bosta zagotovljena njihovo varstvo in zaupnost v skladu z veljavnimi predpisi. V ta namen bo izbrani prevoznik dal pisno dovoljenje za obdelavo osebnih podatkov v skladu z Zakonodajnim dekretom št. 196/2003, kakor je bil spremenjen in dopolnjen.
20. Obdelava občutljivih podatkov
Občutljivi podatki, ki jih vsebujejo ponudbe prevoznikov, se bodo obdelovali v skladu s pravilnikom „Regolamento per il trattamento dei dati sensibili e giudiziari“ (pravilnik o obdelavi občutljivih in sodnih podatkov), ki ga je na seji 2. marca 2006 potrdil upravni odbor ENAC in je na voljo na spletni strani ENAC: http://enac-italia.it
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/86 |
Javni razpis, ki ga je objavila Italija v skladu s členom 4(1)(d) Uredbe Sveta (EGS) št. 2408/92 za opravljanje rednih zračnih prevozov na progi Crotone–Milano Linate in v obratni smeri
(Besedilo velja za EGP)
(2008/C 276/08)
UVOD
Italijanska vlada (Ministrstvo za infrastrukturo in promet) je na podlagi člena 4 Uredbe (EGS) št. 2408/92 in v skladu z odločitvami uradnega srečanja pristojnih služb, ki je potekalo pri upravi dežele Calabria, odobrila ta javni razpis za dodelitev koncesije za opravljanje zračnega prevoza na progi Crotone–Milano Linate in v obratni smeri.
Standardi, ki izhajajo iz obveznosti javne službe, so bili objavljeni v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008.
Če se v 30 dneh od objave navedene obveznosti ne prijavi noben letalski prevoznik, ki bi začel zračne prevoze na omenjeni progi v skladu z obveznostmi javne službe brez dodatnega finančnega nadomestila, je italijanska vlada (Ministrstvo za infrastrukturo in promet) v skladu s postopkom iz člena 4(1)(d) Uredbe (EGS) št. 2408/92 sklenila, da bo omogočila dostop do te proge samo enemu prevozniku in mu na podlagi javnega razpisa dodelila pravico do opravljanja teh prevozov po navedeni uredbi.
SPLOŠNE DOLOČBE
Ta javni razpis določa predmet razpisa, pravila sodelovanja na razpisu, pravila glede trajanja, spremembe ali izteka veljavnosti pogodbe, kazni zaradi neizpolnjevanja pogodbenih določil ter glede jamstva za resnost ponudbe in garancije za dobro izvedbo pogodbenih obveznosti.
Pravica do opravljanja prevozov na navedeni progi bo z javnim razpisom dodeljena ponudniku, ki bo cenovno najugodnejši glede na znesek finančnega nadomestila, določenega v točki 6 tega razpisa.
1. Predmet javnega razpisa
Opravljanje rednih letalskih prevozov na progi Crotone–Milano Linate in v obratni smeri v skladu z obveznostmi javne službe, objavljenimi v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008 na podlagi določb Uredbe (EGS) št. 2408/92.
2. Udeležba
Ponudbe lahko predložijo vsi letalski prevozniki iz Skupnosti, kot so opredeljeni v členu 2(b) Uredbe (EGS) št. 2408/92 in ki izpolnjujejo naslednje zahteve:
Splošne zahteve
|
1. |
niso v stečaju ali v postopku prisilne likvidacije, niso sklenili dogovora z upniki ter niso v postopku za ugotovitev česa od navedenega; |
|
2. |
ni jim bilo s sodbo prepovedano opravljanje dejavnosti v skladu s členom 9(2) Zakonodajnega odloka št. 231/2001 in ni jim bilo prepovedano sklepati pogodb z javno upravo; |
|
3. |
izpolnjujejo obveznosti glede plačevanja prispevkov za socialno varnost; |
|
4. |
niso prijavili lažnih podatkov glede izpolnjevanja zahtev za sodelovanje na drugih javnih razpisih za opravljanje rednih zračnih prevozov na podlagi obveznosti javne službe. |
Kandidat dokaže, da izpolnjuje navedene pogoje tako, da za točko 3 predloži potrdilo o rednem plačevanju prispevkov, ki ga izda INPS ali INAIL, in potrdilo iz člena 17 Zakona št. 68 z dne 12. marca 1999 o pravicah invalidnih oseb do dela. Za točke 1, 2 in 4 kandidat predloži izjavo, ki nadomešča potrdilo o izpolnjevanju pogojev v skladu s členoma 46 in 47 Predsedniškega odloka št. 445 z dne 28. decembra 2000.
Kandidati, ki imajo sedež v drugih državah članicah Evropske unije in ne v Italiji, morajo predložiti potrdila ali dokazila, ki jih izdajo uprave ali organi v državi porekla, skupaj s prevodom v italijanski jezik, ki ga overi italijanski konzulat in potrdi, da prevod ustreza izvirniku.
Tehnične zahteve
|
1. |
operativna licenca, podeljena v skladu z Uredbo (EGS) št. 2407/1992; |
|
2. |
obvezno zavarovanje za primer nesreče, zlasti za zavarovanje potnikov, prtljage, blaga, ki se prevaža, in tretjih oseb v skladu z Uredbo (ES) št. 785/2004; |
|
3. |
spričevalo letalskega prevoznika (COA) v skladu z zakonodajo Skupnosti; |
|
4. |
kandidati ne smejo biti na t. i. „črnem seznamu“ letalskih prevoznikov, ki ne izpolnjujejo evropskih varnostnih standardov, kakor je objavljen na spletni strani: http://ec.europa.eu/transport/air-ban; |
|
5. |
sistem stroškovnega računovodstva, ki omogoča razčlenitev zadevnih stroškov (vključno s stalnimi stroški in prihodki). |
Letalski prevozniki, ki po predložitvi ponudbe ne izpolnjujejo več navedenih pogojev, so samodejno izločeni iz postopka ocenjevanja.
Če letalski prevoznik po sklenitvi pogodbe ne izpolnjuje več pogojev iz točke 5, se uporabijo določbe iz točke 14 in predzadnjega odstavka točke 15 tega javnega razpisa.
3. Postopek
Za ta javni razpis veljajo določbe člena 4(1)(d), (e), (f), (h) in (i) Uredbe Sveta (EGS) št. 2408/1992.
4. Razpisna dokumentacija
Celotna razpisna dokumentacija s posebnimi pravili, ki se uporabljajo za razpis, vključno z veljavnostjo ponudb in vsemi drugimi informacijami, ki so lahko koristne, je sestavni del tega razpisa skupaj z vzorcem pogodbe iz točke 5 in jo je mogoče brezplačno zahtevati na naslovu: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio, 118, I-00185 Roma ali na elektronskem naslovu: trasporto.aereo@enac.rupa.it.
5. Pogodba o izvajanju storitve
Opravljanje prevozov bo urejala pogodba med letalskim prevoznikom in ENAC, sestavljena na podlagi vzorca pogodbe, ki je del razpisne dokumentacije.
6. Finančno nadomestilo
Najvišji znesek finančnega nadomestila, ki je na voljo po razpisu za dodelitev koncesije za opravljanje zračnega prevoza na zadevni progi, je 1 258 178,33 EUR letno (vključno z DDV).
Ponudbe je treba sestaviti v skladu z razpisno dokumentacijo, v obrazcu za finančni del ponudbe z letno razčlenitvijo stroškov pa je treba izrecno navesti zahtevani znesek nadomestila za opravljanje zadevnih prevozov, ki ne presega navedenega zneska.
Natančen znesek nadomestila se vsako leto določi za nazaj glede na dejanske odhodke in prihodke, nastale z opravljanjem prevozov, na podlagi predloženih dokazil in v mejah zneska, navedenega v ponudbi, kakor je določeno v razpisni dokumentaciji.
Letalski prevoznik v nobenem primeru ne more zahtevati finančnega nadomestila, ki presega zgornjo mejo iz pogodbe, ker plačilo ni povračilo, temveč nadomestilo za opravljanje prevozov v skladu z obveznostmi javne službe.
Letna plačila se izplačajo s predplačili in poračunom v skladu z določbami razpisne dokumentacije brez poseganja v preglede, ki jih izvaja ENAC, da ugotovi dejansko namenskost nadomestila in izpolnjevanje zahtev s strani letalskega prevoznika. Končni znesek se plača po natančnem pregledu računovodskih izkazov, ki jih prevoznik predloži za zadevno progo, in po ugotovitvi, da se prevozi opravljajo v skladu s pogodbo.
7. Cene prevozov
V predloženih ponudbah je treba navesti cene prevozov, ki so določene v obvestilu o uvedbi obveznosti javne službe, objavljenem v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008.
8. Začetek opravljanja prevozov
Prevozi se začnejo izvajati 15 dni po sklenitvi pogodbe, začetek opravljanja prevozov pa se potrdi z ustreznim zapisnikom, ki ga podpišeta letalski prevoznik in ENAC.
9. Trajanje pogodbe
Pogodba traja dve leti od dneva, ko se dejansko začnejo zračni prevozi na zadevni progi.
Letalski prevoznik mora dati ENAC na voljo osebje, tehnično in računovodsko dokumentacijo, naprave in vse drugo, kar je potrebno za spremljanje in nadzor pravilnega izpolnjevanja, uporabe in izvajanja določb iz obvestila Komisije, odloka o uvedbi obveznosti, tega razpisa, pogodbe in razpisne dokumentacije.
Za neizpolnjevanje navedenih obveznosti so določene kazni v skladu s točko 11 tega javnega razpisa.
10. Odpoved pogodbe
Katera koli stranka lahko predčasno odstopi od pogodbe s šestmesečnim odpovednim rokom brez obveznosti plačila nadomestila ali odškodnine, vendar ne prej kot v 12 mesecih po začetku opravljanja prevozov.
Kadar prevoznik preneha izpolnjevati obveznosti javne službe, se šteje, da je od pogodbe odstopil brez odpovednega roka, razen če ponovno ne začne opravljati prevozov v skladu z obveznostmi javne službe najpozneje 30 dni od prejema zadevnega opomina ENAC.
Če prevoznik odstopi od pogodbe, si ENAC pridržuje pravico, da ustrezno oceni, ali naj Ministrstvu za infrastrukturo in promet predlaga sklenitev nove pogodbe z naslednjim najvišje uvrščenim prevoznikom na razpisu. Pogoji izvajanja obveznosti in sorazmernost nadomestila so enaki kot pri prvi dodelitvi obveznosti javne službe.
11. Neizvajanje storitev in kazni
Prevoznik ne krši pogodbe, če prevoze preneha opravljati iz naslednjih razlogov:
|
— |
nevarnih vremenskih razmer, |
|
— |
zaprtja enega od letališč iz delovnega programa, |
|
— |
težav, povezanih z varnostjo, |
|
— |
stavk, |
|
— |
višje sile. |
Pri prekinitvi opravljanja zračnih prevozov iz navedenih razlogov se znesek finančnega nadomestila sorazmerno zmanjša glede na število odpovedanih letov.
Pri neizpolnjevanju nalog in obveznosti, prevzetih s pogodbo, lahko ENAC letalskemu prevozniku naloži plačilo kazni, ki je sorazmerna s številom kršitev, kot je določeno v vzorcu pogodbe.
Kazen v nobenem primeru ne sme biti višja od 50 % največjega zneska finančnega nadomestila iz točke 6 tega razpisa, pri čemer ima ENAC v primeru preseganja navedene meje pravico do odpovedi pogodbe zaradi neizpolnjevanja obveznosti, s čimer takoj preneha tudi obveznost plačila nezapadlih zneskov nadomestila.
Letno število odpovedanih letov iz razlogov, za katere je neposredno dogovoren prevoznik, ne sme preseči 2 % števila predvidenih letov.
Pri preseganju omenjenega števila mora prevoznik plačati ENAC kazen v višini 3 000,00 EUR za vsak odpovedani let nad mejo 2 %, in sicer na podlagi uradnega obvestila, ki se prevozniku pošlje najpozneje 10 dni po seznanitvi z dogodkom. Prevoznik lahko predloži morebitne pripombe najpozneje v sedmih dneh.
ENAC poleg tega popravi tudi znesek nadomestila sorazmerno s številom opravljenih letov. Zneski, prejeti iz tega naslova, bodo namenjeni izboljšanju prometne povezanosti mesta Crotone.
Neupoštevanje odpovednega roka iz točke 10 se kaznuje z zneskom, ki se izračuna na podlagi letnega nadomestila in števila zamujenih dni odpovednega roka od dneva prenehanja prevozov z obveznostjo javne službe, pod pogoji iz točke 10 in po enačbi:
P = CA/GG × gg
kjer je:
|
P |
= |
kazenski |
|
CA |
= |
znesek letnega nadomestila |
|
GG |
= |
število dni zadevnega leta (365 ali 366) |
|
gg |
= |
število zamujenih dni odpovednega roka |
Kazni iz te točke se lahko seštevajo s kaznimi, ki jih določajo predpisi Skupnosti in nacionalni predpisi.
12. Jamstvo za resnost ponudbe
Da bi dokazali resnost in zanesljivost ponudbe, morajo prevozniki, ki sodelujejo na razpisu, položiti jamstvo v višini 2 % skupnega zneska nadomestila iz točke 6 bodisi v obliki varščine bodisi v obliki zavarovalnega ali bančnega jamstva.
Načini predložitve navedenega jamstva so določeni v razpisni dokumentaciji in so lahko navedeni tudi v pogodbi.
Jamstvo mora biti veljavno najmanj 180 dni po izteku roka za oddajo ponudb, prevozniki pa se morajo zavezati, da bodo njegovo veljavnost med razpisnim postopkom na zahtevo ENAC podaljšali, če se ta ne konča pred iztekom veljavnosti jamstva.
Ko ENAC prevoznike obvesti, da niso bili izbrani na razpisu, se jamstvo sprosti.
13. Jamstvo za dobro izvedbo pogodbenih obveznosti in zavarovalno kritje
Prevoznik, ki mu je bilo s tem razpisom dodeljeno opravljanje zračnih prevozov v skladu z obveznostmi javne službe, mora predložiti bančno ali zavarovalno jamstvo v višini 700 000,00 EUR v korist ENAC, ki si pridržuje pravico do njegove uporabe za zagotovitev neprekinjenega izvajanja obveznosti javne službe.
Jamstvo se samodejno sprosti brez odobritve ENAC, če je izid pregleda iz zadnjega odstavka točke 6 pozitiven.
14. Izguba pravice do finančnega nadomestila
Če letalski prevoznik kadar koli po sklenitvi pogodbe ne izpolnjuje splošnih in tehničnih pogojev iz točke 2 tega razpisa in zahtev iz razpisne dokumentacije, izgubi pravico do opravljanja prevozov na zadevni progi in pravico do finančnega nadomestila, vrniti pa mora tudi vse neupravičeno prejete zneske, vključno z zamudnimi obrestmi.
Po prenehanju pravice do opravljanja prevozov na zadevni progi lahko Ministrstvo za infrastrukturo in promet pooblasti ENAC, da sklene drugo pogodbo za preostalo obdobje opravljanja prevozov z naslednjim najvišje uvrščenim prevoznikom na razpisu.
V tem primeru velja pogodba od dneva začetka opravljanja prevozov do datuma, ko naj bi se v razdrti pogodbi nehali prevozi, v skladu z delovnim načrtom, ki je bil odobren, ko je bila ocenjena ponudba najugodnejšega ponudnika.
15. Razdrtje pogodbe
Če prevoznik ne izpolnjuje določb obvestila o uvedbi obveznosti, objavljenega v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008, zadevnega odloka o uvedbi obveznosti, pogodbe, razpisa in razpisne dokumentacije, lahko ENAC na podlagi člena 1454 Civilnega zakonika pošlje pisno obvestilo prevozniku, v skladu s katerim mora ta v 15 dneh po prejemu takega obvestila odpraviti neizpolnjevanje določb.
Če tega ne stori v navedenem roku, ENAC lahko šteje, da je pogodbo razdrl, trajno zadrži znesek jamstva iz točke 13 in od prevoznika zahteva nadomestilo za nastalo škodo.
Poleg tega ima ENAC po členu 1456 Civilnega zakonika pravico, da razdre pogodbo s pisnim obvestilom prevozniku, če ta ne izpolnjuje obveznosti in nalog iz pogodbe, tega razpisa in razpisne dokumentacije.
Pri razdrtju pogodbe lahko Ministrstvo za infrastrukturo in promet pooblasti ENAC, da sklene novo pogodbo za preostalo obdobje opravljanja zračnih prevozov z naslednjim najvišje uvrščenim prevoznikom na razpisu za dodelitev zadevne proge.
V tem primeru velja pogodba od dneva začetka opravljanja prevozov do datuma, ko naj bi se v razdrti pogodbi nehali prevozi, v skladu z delovnim načrtom, ki je bil odobren, ko je bila ocenjena ponudba najugodnejšega ponudnika.
16. Predložitev ponudb
Ponudbe, ki morajo biti sestavljene v skladu z razpisno dokumentacijo, sicer se izločijo iz postopka, je treba v 30 dneh od objave tega javnega razpisa v Uradnem listu Evropske unije poslati s priporočeno pošiljko s povratnico ali vročiti osebno s potrdilom o prejemu na naslov: ENAC, Direzione Generale, Viale del Castro Pretorio, 118, I-00185 Roma.
Ponudbe morajo prispeti v treh zaprtih in zapečatenih ovojnicah, sicer se izločijo iz postopka.
Zunanja ovojnica, ki je zaprta, zapečatena in parafirana na obeh straneh in po robovih, mora vsebovati dve notranji ovojnici, prav tako zapečateni in parafirani, opremljeni z naslednjim pripisom: „Offerta per la gara in oneri di servizio pubblico sulla rotta Crotone-Milano Linate e viceversa“ (Ponudba za razpis za obveznosti javne službe za redne zračne prevoze na progi Crotone–Milano Linate in v obratni smeri).
Dokumenti, ki jih morajo vsebovati navedene tri ovojnice, so navedeni v razpisni dokumentaciji iz točke 4 tega javnega razpisa.
Razume se, da je izključno pošiljatelj odgovoren, če ovojnica iz kakršnega koli razloga ne prispe na naslov prejemnika do navedenega roka.
Razpisni postopek se izvede, tudi če bo predložena samo ena veljavna ponudba.
17. Čas veljavnosti ponudbe
180 dni po roku za oddajo ponudb.
18. Oddaja naročila
Razpis izvede ENAC s komisijo, ki jo sestavljajo vodstveni uslužbenec ENAC, ki ga pooblasti generalni direktor, izvedenec, ki ga imenuje dežela Calabria, in predsednik, ki ga sporazumno imenujeta ENAC in dežela Calabria; naloge tajništva opravlja ENAC.
19. Obdelava osebnih podatkov
Vsi osebni podatki se bodo uporabljali in obdelovali izključno za uradne potrebe, ob tem pa bosta zagotovljena njihova varstvo in zaupnost v skladu z veljavnimi predpisi. V ta namen bo izbrani prevoznik dal pisno dovoljenje za obdelavo osebnih podatkov v skladu z Zakonodajnim odlokom št. 196/2003, kakor je bil spremenjen in dopolnjen.
20. Obdelava občutljivih podatkov
Občutljivi podatki, ki jih vsebujejo ponudbe prevoznikov, se bodo obdelovali v skladu s pravilnikom „Regolamento per il trattamento dei dati sensibili e giudiziari“ (pravilnik o obdelavi občutljivih in sodnih podatkov), ki ga je na seji 2. marca 2006 potrdil upravni odbor ENAC in je na voljo na spletni strani ENAC: http://enac-italia.it
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/90 |
Javni razpis, ki ga je objavila Italija v skladu s členom 4(1)(d) Uredbe Sveta (EGS) št. 2408/92 za opravljanje rednih zračnih prevozov na progi Crotone–Roma Fiumicino in v obratni smeri
(Besedilo velja za EGP)
(2008/C 276/09)
UVOD
Italijanska vlada (Ministrstvo za infrastrukturo in promet) je na podlagi člena 4 Uredbe (EGS) št. 2408/92 in v skladu z odločitvami uradnega srečanja pristojnih služb, ki je potekalo pri upravi dežele Calabria, odobrila ta javni razpis za dodelitev koncesije za opravljanje zračnega prevoza na progi Crotone–Roma Fiumicino in v obratni smeri.
Standardi, ki izhajajo iz obveznosti javne službe, so bili objavljeni v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008.
Če se v 30 dneh od objave navedene obveznosti ne prijavi noben letalski prevoznik, ki bi začel zračne prevoze na omenjeni progi v skladu z obveznostmi javne službe brez dodatnega finančnega nadomestila, je italijanska vlada (Ministrstvo za infrastrukturo in promet) v skladu s postopkom iz člena 4(1)(d) Uredbe (EGS) št. 2408/92 sklenila, da bo omogočila dostop do te proge samo enemu prevozniku in mu na podlagi javnega razpisa dodelila pravico do opravljanja teh prevozov po navedeni uredbi.
SPLOŠNE DOLOČBE
Ta javni razpis določa predmet razpisa, pravila sodelovanja na razpisu, pravila glede trajanja, spremembe ali izteka veljavnosti pogodbe, kazni zaradi neizpolnjevanja pogodbenih določil ter glede jamstva za resnost ponudbe in garancije za dobro izvedbo pogodbenih obveznosti.
Pravica do opravljanja prevozov na navedeni progi bo z javnim razpisom dodeljena ponudniku, ki bo cenovno najugodnejši glede na znesek finančnega nadomestila, določenega v točki 6 tega razpisa.
1. Predmet javnega razpisa
Opravljanje rednih letalskih prevozov na progi Crotone–Roma Fiumicino in v obratni smeri v skladu z obveznostmi javne službe, objavljenimi v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008 na podlagi določb Uredbe (EGS) št. 2408/92.
2. Udeležba
Ponudbe lahko predložijo vsi letalski prevozniki iz Skupnosti, kot so opredeljeni v členu 2(b) Uredbe (EGS) št. 2408/92 in ki izpolnjujejo naslednje zahteve:
Splošne zahteve
|
1. |
niso v stečaju ali v postopku prisilne likvidacije, niso sklenili dogovora z upniki ter niso v postopku za ugotovitev česa od navedenega; |
|
2. |
ni jim bilo s sodbo prepovedano opravljanje dejavnosti v skladu s členom 9(2) Zakonodajnega odloka št. 231/2001 in ni jim bilo prepovedano sklepati pogodb z javno upravo; |
|
3. |
izpolnjujejo obveznosti glede plačevanja prispevkov za socialno varnost; |
|
4. |
niso prijavili lažnih podatkov glede izpolnjevanja zahtev za sodelovanje na drugih javnih razpisih za opravljanje rednih zračnih prevozov na podlagi obveznosti javne službe. |
Kandidat dokaže, da izpolnjuje navedene pogoje tako, da za točko 3 predloži potrdilo o rednem plačevanju prispevkov, ki ga izda INPS ali INAIL, in potrdilo iz člena 7 Zakona št. 68 z dne 12. marca 1999 o pravicah invalidnih oseb do dela. Za točke 1, 2 in 4 kandidat predloži izjavo, ki nadomešča potrdilo o izpolnjevanju pogojev v skladu s členoma 46 in 47 Predsedniškega odloka št. 445 z dne 28. decembra 2000.
Kandidati, ki imajo sedež v drugih državah članicah Evropske unije in ne v Italiji, morajo predložiti potrdila ali dokazila, ki jih izdajo uprave ali organi v državi porekla, skupaj s prevodom v italijanski jezik, ki ga overi italijanski konzulat in potrdi, da prevod ustreza izvirniku.
Tehnične zahteve
|
1. |
operativna licenca, podeljena v skladu z Uredbo (EGS) št. 2407/1992; |
|
2. |
obvezno zavarovanje za primer nesreče, zlasti za zavarovanje potnikov, prtljage, blaga, ki se prevaža, in tretjih oseb v skladu z Uredbo (ES) št. 785/2004; |
|
3. |
spričevalo letalskega prevoznika (COA) v skladu z zakonodajo Skupnosti; |
|
4. |
kandidati ne smejo biti na t. i. „črnem seznamu“ letalskih prevoznikov, ki ne izpolnjujejo evropskih varnostnih standardov, kakor je objavljen na spletni strani: http://ec.europa.eu/transport/air-ban; |
|
5. |
sistem stroškovnega računovodstva, ki omogoča razčlenitev zadevnih stroškov (vključno s stalnimi stroški in prihodki). |
Letalski prevozniki, ki po predložitvi ponudbe ne izpolnjujejo več navedenih pogojev, so samodejno izločeni iz postopka ocenjevanja.
Če letalski prevoznik po sklenitvi pogodbe ne izpolnjuje več pogojev iz točke 5, se uporabijo določbe iz točke 14 in predzadnjega odstavka točke 15 tega javnega razpisa.
3. Postopek
Za ta javni razpis veljajo določbe člena 4(1)(d), (e), (f), (h) in (i) Uredbe Sveta (EGS) št. 2408/1992.
4. Razpisna dokumentacija
Celotna razpisna dokumentacija s posebnimi pravili, ki se uporabljajo za razpis, vključno z veljavnostjo ponudb in vsemi drugimi informacijami, ki so lahko koristne, je sestavni del tega razpisa skupaj z vzorcem pogodbe iz točke 5 in jo je mogoče brezplačno zahtevati na naslovu: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio, 118, I-00185 Roma ali na elektronskem naslovu: trasporto.aereo@enac.rupa.it.
5. Pogodba o izvajanju storitve
Opravljanje prevozov bo urejala pogodba med letalskim prevoznikom in ENAC, sestavljena na podlagi vzorca pogodbe, ki je del razpisne dokumentacije.
6. Finančno nadomestilo
Najvišji znesek finančnega nadomestila, ki je na voljo po razpisu za dodelitev koncesije za opravljanje zračnega prevoza na zadevni progi, je 1 724 666 EUR letno (vključno z DDV).
Ponudbe je treba sestaviti v skladu z razpisno dokumentacijo, v obrazcu za finančni del ponudbe z letno razčlenitvijo stroškov pa je treba izrecno navesti zahtevani znesek nadomestila za opravljanje zadevnih prevozov, ki ne presega navedenega zneska.
Natančen znesek nadomestila se vsako leto določi za nazaj glede na dejanske odhodke in prihodke, nastale z opravljanjem prevozov, na podlagi predloženih dokazil in v mejah zneska, navedenega v ponudbi, kakor je določeno v razpisni dokumentaciji.
Letalski prevoznik v nobenem primeru ne more zahtevati finančnega nadomestila, ki presega zgornjo mejo iz pogodbe, ker plačilo ni povračilo, temveč nadomestilo za opravljanje prevozov v skladu z obveznostmi javne službe.
Letna plačila se izplačajo s predplačili in poračunom v skladu z določbami razpisne dokumentacije brez poseganja v preglede, ki jih izvaja ENAC, da ugotovi dejansko namenskost nadomestila in izpolnjevanje zahtev s strani letalskega prevoznika. Končni znesek se plača po natančnem pregledu računovodskih izkazov, ki jih prevoznik predloži za zadevno progo, in po ugotovitvi, da se prevozi opravljajo v skladu s pogodbo.
7. Cene prevozov
V predloženih ponudbah je treba navesti cene prevozov, ki so določene v obvestilu o uvedbi obveznosti javne službe, objavljenem v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008.
8. Začetek opravljanja prevozov
Prevozi se začnejo izvajati 15 dni po sklenitvi pogodbe, začetek opravljanja prevozov pa se potrdi z ustreznim zapisnikom, ki ga podpišeta letalski prevoznik in ENAC.
9. Trajanje pogodbe
Pogodba traja dve leti od dneva, ko se dejansko začnejo zračni prevozi na zadevni progi.
Letalski prevoznik mora dati ENAC na voljo osebje, tehnično in računovodsko dokumentacijo, naprave in vse drugo, kar je potrebno za spremljanje in nadzor pravilnega izpolnjevanja, uporabe in izvajanja določb iz obvestila Komisije, odloka o uvedbi obveznosti, tega razpisa, pogodbe in razpisne dokumentacije.
Za neizpolnjevanje navedenih obveznosti so določene kazni v skladu s točko 11 tega javnega razpisa.
10. Odpoved pogodbe
Katera koli stranka lahko predčasno odstopi od pogodbe s šestmesečnim odpovednim rokom brez obveznosti plačila nadomestila ali odškodnine, vendar ne prej kot v 12 mesecih po začetku opravljanja prevozov.
Kadar prevoznik preneha izpolnjevati obveznosti javne službe, se šteje, da je od pogodbe odstopil brez odpovednega roka, razen če ponovno ne začne opravljati prevozov v skladu z obveznostmi javne službe najpozneje 30 dni od prejema zadevnega opomina ENAC.
Če prevoznik odstopi od pogodbe, si ENAC pridržuje pravico, da ustrezno oceni, ali naj Ministrstvu za infrastrukturo in promet predlaga sklenitev nove pogodbe z naslednjim najvišje uvrščenim prevoznikom na razpisu. Pogoji izvajanja obveznosti in sorazmernost nadomestila so enaki kot pri prvi dodelitvi obveznosti javne službe.
11. Neizvajanje storitev in kazni
Prevoznik ne krši pogodbe, če prevoze preneha opravljati iz naslednjih razlogov:
|
— |
nevarnih vremenskih razmer, |
|
— |
zaprtja enega od letališč iz delovnega programa, |
|
— |
težav, povezanih z varnostjo, |
|
— |
stavk, |
|
— |
višje sile. |
Pri prekinitvi opravljanja zračnih prevozov iz navedenih razlogov se znesek finančnega nadomestila sorazmerno zmanjša glede na število odpovedanih letov.
Pri neizpolnjevanju nalog in obveznosti, prevzetih s pogodbo, lahko ENAC letalskemu prevozniku naloži plačilo kazni, ki je sorazmerna s številom kršitev, kot je določeno v vzorcu pogodbe.
Kazen v nobenem primeru ne sme biti višja od 50 % največjega zneska finančnega nadomestila iz točke 6 tega razpisa, pri čemer ima ENAC v primeru preseganja navedene meje pravico do odpovedi pogodbe zaradi neizpolnjevanja obveznosti, s čimer takoj preneha tudi obveznost plačila nezapadlih zneskov nadomestila.
Letno število odpovedanih letov iz razlogov, za katere je neposredno dogovoren prevoznik, ne sme preseči 2 % števila predvidenih letov.
Pri preseganju omenjenega števila mora prevoznik plačati ENAC kazen v višini 3 000,00 EUR za vsak odpovedani let nad mejo 2 %, in sicer na podlagi uradnega obvestila, ki se prevozniku pošlje najpozneje 10 dni po seznanitvi z dogodkom. Prevoznik lahko predloži morebitne pripombe najpozneje v sedmih dneh.
ENAC poleg tega popravi tudi znesek nadomestila sorazmerno s številom opravljenih letov. Zneski, prejeti iz tega naslova, bodo namenjeni izboljšanju prometne povezanosti mesta Crotone.
Neupoštevanje odpovednega roka iz točke 10 se kaznuje z zneskom, ki se izračuna na podlagi letnega nadomestila in števila zamujenih dni odpovednega roka od dneva prenehanja prevozov z obveznostjo javne službe, pod pogoji iz točke 10 in po enačbi:
P = CA/GG × gg
kjer je:
|
P |
= |
kazenski |
|
CA |
= |
znesek letnega nadomestila |
|
GG |
= |
število dni zadevnega leta (365 ali 366) |
|
gg |
= |
število zamujenih dni odpovednega roka |
Kazni iz te točke se lahko seštevajo s kaznimi, ki jih določajo predpisi Skupnosti in nacionalni predpisi.
12. Jamstvo za resnost ponudbe
Da bi dokazali resnost in zanesljivost ponudbe, morajo prevozniki, ki sodelujejo na razpisu, položiti jamstvo v višini 2 % skupnega zneska nadomestila iz točke 6 bodisi v obliki varščine bodisi v obliki zavarovalnega ali bančnega jamstva.
Načini predložitve navedenega jamstva so določeni v razpisni dokumentaciji in so lahko navedeni tudi v pogodbi.
Jamstvo mora biti veljavno najmanj 180 dni po izteku roka za oddajo ponudb, prevozniki pa se morajo zavezati, da bodo njegovo veljavnost med razpisnim postopkom na zahtevo ENAC podaljšali, če se ta ne konča pred iztekom veljavnosti jamstva.
Ko ENAC prevoznike obvesti, da niso bili izbrani na razpisu, se jamstvo sprosti.
13. Jamstvo za dobro izvedbo pogodbenih obveznosti in zavarovalno kritje
Prevoznik, ki mu je bilo s tem razpisom dodeljeno opravljanje zračnih prevozov v skladu z obveznostmi javne službe, mora predložiti bančno ali zavarovalno jamstvo v višini 700 000,00 EUR v korist ENAC, ki si pridržuje pravico do njegove uporabe za zagotovitev neprekinjenega izvajanja obveznosti javne službe.
Jamstvo se samodejno sprosti brez odobritve ENAC, če je izid pregleda iz zadnjega odstavka točke 6 pozitiven.
14. Izguba pravice do finančnega nadomestila
Če letalski prevoznik kadar koli po sklenitvi pogodbe ne izpolnjuje splošnih in tehničnih pogojev iz točke 2 tega razpisa in zahtev iz razpisne dokumentacije, izgubi pravico do opravljanja prevozov na zadevni progi in pravico do finančnega nadomestila, vrniti pa mora tudi vse neupravičeno prejete zneske, vključno z zamudnimi obrestmi.
Po prenehanju pravice do opravljanja prevozov na zadevni progi lahko Ministrstvo za infrastrukturo in promet pooblasti ENAC, da sklene drugo pogodbo za preostalo obdobje opravljanja prevozov z naslednjim najvišje uvrščenim prevoznikom na razpisu.
V tem primeru velja pogodba od dneva začetka opravljanja prevozov do datuma, ko naj bi se v razdrti pogodbi nehali prevozi, v skladu z delovnim načrtom, ki je bil odobren, ko je bila ocenjena ponudba najugodnejšega ponudnika.
15. Razdrtje pogodbe
Če prevoznik ne izpolnjuje določb obvestila o uvedbi obveznosti, objavljenega v Uradnem listu Evropske unije C 241 z dne 20. septembra 2008, zadevnega odloka o uvedbi obveznosti, pogodbe, razpisa in razpisne dokumentacije, lahko ENAC na podlagi člena 1454 Civilnega zakonika pošlje pisno obvestilo prevozniku, v skladu s katerim mora ta v 15 dneh po prejemu takega obvestila odpraviti neizpolnjevanje določb.
Če tega ne stori v navedenem roku, ENAC lahko šteje, da je pogodbo razdrl, trajno zadrži znesek jamstva iz točke 13 in od prevoznika zahteva nadomestilo za nastalo škodo.
Poleg tega ima ENAC po členu 1456 Civilnega zakonika pravico, da razdre pogodbo s pisnim obvestilom prevozniku, če ta ne izpolnjuje obveznosti in nalog iz pogodbe, tega razpisa in razpisne dokumentacije.
Pri razdrtju pogodbe lahko Ministrstvo za infrastrukturo in promet pooblasti ENAC, da sklene novo pogodbo za preostalo obdobje opravljanja zračnih prevozov z naslednjim najvišje uvrščenim prevoznikom na razpisu za dodelitev zadevne proge.
V tem primeru velja pogodba od dneva začetka opravljanja prevozov do datuma, ko naj bi se v razdrti pogodbi nehali prevozi, v skladu z delovnim načrtom, ki je bil odobren, ko je bila ocenjena ponudba najugodnejšega ponudnika.
16. Predložitev ponudb
Ponudbe, ki morajo biti sestavljene v skladu z razpisno dokumentacijo, sicer se izločijo iz postopka, je treba v 30 dneh od objave tega javnega razpisa v Uradnem listu Evropske unije poslati s priporočeno pošiljko s povratnico ali vročiti osebno s potrdilom o prejemu na naslov: ENAC, Direzione Generale, Viale del Castro Pretorio, 118, I-00185 Roma.
Ponudbe morajo prispeti v treh zaprtih in zapečatenih ovojnicah, sicer se izločijo iz postopka.
Zunanja ovojnica, ki je zaprta, zapečatena in parafirana na obeh straneh in po robovih, mora vsebovati dve notranji ovojnici, prav tako zapečateni in parafirani, opremljeni z naslednjim pripisom: „Offerta per la gara in oneri di servizio pubblico sulla rotta Crotone-Roma Fiumicino e viceversa“ (Ponudba za razpis za obveznosti javne službe za redne zračne prevoze na progi Crotone–Roma Fiumicino in v obratni smeri).
Dokumenti, ki jih morajo vsebovati navedene tri ovojnice, so navedeni v razpisni dokumentaciji iz točke 4 tega javnega razpisa.
Razume se, da je izključno pošiljatelj odgovoren, če ovojnica iz kakršnega koli razloga ne prispe na naslov prejemnika do navedenega roka.
Razpisni postopek se izvede, tudi če bo predložena samo ena veljavna ponudba.
17. Čas veljavnosti ponudbe
180 dni po roku za oddajo ponudb.
18. Oddaja naročila
Razpis izvede ENAC s komisijo, ki jo sestavljajo vodstveni uslužbenec ENAC, ki ga pooblasti generalni direktor, izvedenec, ki ga imenuje dežela Calabria, in predsednik, ki ga sporazumno imenujeta ENAC in dežela Calabria; naloge tajništva opravlja ENAC.
19. Obdelava osebnih podatkov
Vsi osebni podatki se bodo uporabljali in obdelovali izključno za uradne potrebe, ob tem pa bosta zagotovljena njihova varstvo in zaupnost v skladu z veljavnimi predpisi. V ta namen bo izbrani prevoznik dal pisno dovoljenje za obdelavo osebnih podatkov v skladu z Zakonodajnim odlokom št. 196/2003, kakor je bil spremenjen in dopolnjen.
20. Obdelava občutljivih podatkov
Občutljivi podatki, ki jih vsebujejo ponudbe prevoznikov, se bodo obdelovali v skladu s pravilnikom „Regolamento per il trattamento dei dati sensibili e giudiziari“ (pravilnik o obdelavi občutljivih in sodnih podatkov), ki ga je na seji 2. marca 2006 potrdil upravni odbor ENAC in je na voljo na spletni strani ENAC: http://enac-italia.it
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/94 |
RAZPIS ZA ZBIRANJE PREDLOGOV – EACEA/29/08
Evropska združenja, ki na evropski ravni delujejo na področju izobraževanja in usposabljanja
(2008/C 276/10)
1. Cilji in opis
Namen tega razpisa za zbiranje predlogov je podpreti evropska združenja, ki delujejo na področju izobraževanja in usposabljanja ali si prizadevajo za dosego cilja, ki je del politike Evropske unije.
Pravna podlaga sta akcijski program na področju vseživljenjskega učenja (program „Vseživljenjsko učenje“) (1) in zlasti njegov podprogram „Jean Monnet“.
Na podlagi izvajanja tretje ključne dejavnosti programa „Jean Monnet“ so cilji tega razpisa:
|
— |
podpreti obstoj visokokakovostnih evropskih združenj, ki delujejo na področju izobraževanja in usposabljanja, |
|
— |
podpreti evropska združenja, ki prispevajo k izvajanju delovnega programa „Izobraževanje in usposabljanje 2010“ (2), |
|
— |
podpreti evropska združenja, ki prek izobraževanja in usposabljanja prispevajo k povečevanju znanja in ozaveščenosti o evropskem integracijskem procesu. |
Financiranje, ki ga zagotavlja Skupnost na podlagi tega razpisa, ima obliko enoletnih dotacij za poslovanje za leto 2009, s katerimi se podpirajo določeni operativni in administrativni stroški izbranih evropskih združenj.
Izvajalska agencija za izobraževanje, avdiovizualno področje in kulturo („Agencija“), ki deluje po pooblastilu Evropske komisije („Komisija“), je odgovorna za vodenje tega razpisa za zbiranje predlogov.
2. Upravičeni prosilci
Določeno evropsko združenje je upravičeno, če izpolnjuje naslednje pogoje. Organizacija:
|
— |
je neprofitna organizacija, |
|
— |
ima vsaj dve leti (na dan 23. decembra 2008) pravno osebnost in sedež v eni od upravičenih držav (države članice EU-27, Islandija, Lihtenštajn, Norveška in Turčija), |
|
— |
večino svojih dejavnosti izvaja v državah članicah Evropske unije, državah, ki spadajo v Evropski gospodarski prostor, in/ali državah kandidatkah, |
|
— |
je organ, ki si prizadeva za dosego cilja v splošnem evropskem interesu, kot je opredeljen v členu 162 pravil za izvajanje finančne uredbe, določenih v Uredbi Komisije (ES, Euratom) št. 2342/2002 (3), kakor je bila nazadnje spremenjena z Uredbo (ES) št. 478/2007, |
|
— |
deluje na področju izobraževanja in usposabljanja na evropski ravni in si prizadeva za dosego jasnih in natančno opredeljenih ciljev, določenih v členih njenega statuta, |
|
— |
izvaja dejavnosti, ki so skladne s prednostnimi nalogami delovnega programa „Izobraževanje in usposabljanje 2010“, in/ali prek izobraževanja in usposabljanja prispeva k povečevanju znanja in ozaveščenosti o evropskem integracijskem procesu, |
|
— |
vključuje članske organizacije, ki imajo sedež v vsaj 12 različnih državah članicah EU (4). Take članske organizacije morajo imeti status „polnopravne članice“ (pridružene članice in opazovalke ne štejejo kot „polnopravne članice“) na nadnacionalni, nacionalni, regionalni ali lokalni ravni. |
Opozorilo: fizične osebe, posamezni pogodbeniki, posamezne visokošolske ustanove ali javni organi in ustanove, ki so del upravne strukture držav članic, se ne štejejo za „združenja“.
3. Merila za dodelitev
Vloge, ki izpolnjujejo pogoje, bodo ocenjene na podlagi kakovosti podrobnega 12-mesečnega delovnega programa za leto 2009, pri čemer bodo uporabljena naslednja merila za dodelitev:
|
— |
ustreznost, jasnost in skladnost kratkoročnih ciljev (12 mesecev), |
|
— |
kakovost vodenja delovnega programa (jasnost in skladnost dejavnosti in predlaganega proračuna za dosego ciljev, časovnega okvira), |
|
— |
verjetni učinek dejavnosti na izobraževanje in/ali usposabljanje na evropski ravni (zlasti v kakšnem obsegu evropska združenja, ki so prosilci, prispevajo k izvajanju delovnega programa Izobraževanje in usposabljanje 2010 in/ali povečevanju znanja in ozaveščenosti o evropskem integracijskem procesu). |
Podrobnejši opis informacij, ki jih morajo prosilci predložiti za vsako merilo za dodelitev, je na voljo na spletnem naslovu: http://eacea.ec.europa.eu/index.htm in ga je treba pozorno prebrati.
4. Proračun in trajanje projekta
Skupni okvirni proračun Skupnosti, namenjen sofinanciranju evropskih združenj na podlagi tega razpisa, znaša 600 000 EUR.
Najvišja dotacija za poslovanje, dodeljena vsakemu združenju za 12-mesečni letni delovni program (ki ustreza enemu proračunskemu letu), ne sme presegati 100 000 EUR.
Organizacije prosilke lahko izbirajo med dvema sistemoma sofinanciranja:
|
(a) |
proračunskim financiranjem: tradicionalno financiranje upravičenih stroškov, pri katerem finančna podpora Skupnosti ne sme presegati 75 % skupnih upravičenih stroškov, navedenih v proračunu za delovni program združenja; |
|
(b) |
pavšalnim financiranjem: financiranje na podlagi pavšalnega zneska, pri katerem finančna podpora Skupnosti ne sme presegati 75 % povzetka začasnega poročila o izdatkih in prihodkih za zadevno leto. |
Obdobje upravičenosti stroškov za delovni program za največ 12 mesecev se začne med 1. januarjem 2009 in 1. aprilom 2009 ter ne sme trajati več kot do konca proračunskega leta upravičenca.
5. Rok in oddaja predlogov
Rok za oddajo vlog je 23. decembra 2008 (datum poštnega žiga). Vloge je treba poslati na naslov:
|
Education, Audiovisual and Culture Executive Agency |
|
Lifelong Learning: Erasmus, Jean Monnet |
|
Call for Proposal EACEA/29/08 |
|
Mr. Ralf RAHDERS |
|
Office: BOUR 2/61 |
|
Avenue du Bourget 1 |
|
B-1140 Brussels |
Sprejete bodo le na uradnem obrazcu oddane vloge,, podpisane s strani oseb, ki imajo pravico sklepati pravno zavezujoče zadeve v imenu organizacije prosilke. Hkrati morajo vloge vsebovati vse informacije in priloge, določene v razpisu in smernicah za kandidate. Vloge, poslane po telefaksu ali elektronski pošti, bodo zavrnjene.
6. Dodatne informacije
Navodila za prosilce in obrazci za vloge so na voljo na spletni strani agencije: http://eacea.ec.europa.eu.
Za dodatne informacije je na voljo:
|
Izvajalska agencija za izobraževanje, avdiovizualno področje in kulturo |
|
Ga. Ilona POKORNA |
|
E-mail: Ilona.Pokorna@ec.europa.eu |
|
Tel. (direktna številka): (32-2) 295 83 94 |
(1) Glej Sklep št. 1720/2006/ES Evropskega parlamenta in Sveta z dne 15. novembra 2006 o uvedbi akcijskega programa na področju vseživljenjskega učenja.
http://eur-lex.europa.eu/LexUriServ/site/en/oj/2006/c_327/c_32420061230en00590067.pdf
(2) Glej http://ec.europa.eu/education/policies/2010/et_2010_en.html
(3) Po tej opredelitvi je organizacija, ki si prizadeva za dosego cilja v splošnem evropskem interesu:
|
— |
evropski organ za izobraževanje, usposabljanje, obveščanje ali raziskovanje in študij evropskih politik ali evropski organ za standardizacijo, ali |
|
— |
evropsko omrežje, ki predstavlja neprofitne organe držav članic ali držav kandidatk in ki pospešuje uporabo načel in politik, ki so skladne s cilji pogodb. |
(4) Poleg tega lahko evropsko združenje vključuje članske organizacije s sedežem v drugih državah, ki sodelujejo v programu Vseživljenjsko učenje (države, ki niso članice EU).
POSTOPKI V ZVEZI Z IZVAJANJEM KONKURENČNE POLITIKE
Komisija
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/97 |
Predhodna priglasitev koncentracije
(Št. primera COMP/M.5368 – MidAmerican/Constellation)
Zadeva, primerna za obravnavo po poenostavljenem postopku
(Besedilo velja za EGP)
(2008/C 276/11)
|
1. |
Komisija je 23. oktobra 2008 prejela priglasitev predlagane koncentracije v skladu s členom 4 Uredbe Sveta (ES) št. 139/2004 (1), s katero podjetje MidAmerican Energy Holdings Company („MidAmerican“, ZDA), ki je pod nadzorom podjetja Berkshire Hathaway, z nakupom delnic pridobi nadzor nad skupino Constellation Energy group Inc. („Constellation“, ZDA) v smislu člena 3(1)(b) Uredbe Sveta. |
|
2. |
Poslovne dejavnosti zadevnih podjetij so:
|
|
3. |
Po predhodnem pregledu Komisija ugotavlja, da bi priglašena transakcija lahko spadala v področje uporabe Uredbe (ES) št. 139/2004. Vendar končna odločitev o tej točki še ni sprejeta. Na podlagi Obvestila Komisije o poenostavljenem postopku obravnave določenih koncentracij v okviru Uredbe Sveta (ES) št. 139/2004 (2) je treba opozoriti, da je ta zadeva primerna za obravnavo po postopku, določenem v Obvestilu. |
|
4. |
Komisija zainteresirane tretje osebe poziva, naj ji predložijo svoje morebitne pripombe glede predlagane transakcije. Komisija mora prejeti pripombe najpozneje v 10 dneh po datumu te objave. Pripombe lahko pošljete Komisiji po telefaksu (št. telefaksa: (32-2) 296 43 01 ali 296 72 44) ali po pošti z navedbo sklicne številke COMP/M.5368 – MidAmerican/Constellation na naslov:
|
(1) UL L 24, 29.1.2004, str. 1.
(2) UL C 56, 5.3.2005, str. 32.
|
31.10.2008 |
SL |
Uradni list Evropske unije |
C 276/s3 |
OPOMBA BRALCU
Institucije so se odločile, da v svojih besedilih ne bodo več navajale zadnje spremembe navedenih besedil.
Če ni navedeno drugače, se akti iz objavljenih besedil sklicujejo na akte v trenutno veljavni različici.