EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32010D0472
2010/472/EU: Commission Decision of 26 August 2010 on imports of semen, ova and embryos of animals of the ovine and caprine species into the Union (notified under document C(2010) 5780) Text with EEA relevance
2010/472/UE: Decizia Comisiei din 26 august 2010 privind importurile de material seminal, ovule și embrioni de animale din speciile ovină și caprină în Uniune [notificată cu numărul C(2010) 5780] Text cu relevanță pentru SEE
2010/472/UE: Decizia Comisiei din 26 august 2010 privind importurile de material seminal, ovule și embrioni de animale din speciile ovină și caprină în Uniune [notificată cu numărul C(2010) 5780] Text cu relevanță pentru SEE
OJ L 228, 31.8.2010, p. 74–93
(BG, ES, CS, DA, DE, ET, EL, EN, FR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
Special edition in Croatian: Chapter 03 Volume 059 P. 140 - 159
 No longer in force, Date of end of validity: 20/04/2021; abrogat prin 32021R0404
No longer in force, Date of end of validity: 20/04/2021; abrogat prin 32021R0404
- Date of document:
- 26/08/2010
- Date of effect:
- 01/09/2010; Punere în aplicare a se vedea articolul 7
- Date of effect:
- 31/08/2011; Punere în aplicare cel târziu intră în vigoare parţial a se vedea articolul 6
- Date of notification:
- 31/08/2010; Actul a fost notificat, dar data notificării nu este disponibilă pe EUR-Lex. Se folosește, în schimb, data publicării.
- Date of end of validity:
- 20/04/2021; abrogat prin 32021R0404
- Author:
- Comisia Europeană
- Form:
- Decizie
- Addressee:
- Cele douăzeci și șapte de state membre: Belgia, Bulgaria, Republica Cehă, Danemarca, Germania, Estonia, Irlanda, Grecia, Spania, Franţa, Italia, Cipru, Letonia, Lituania, Luxemburg, Ungaria, Malta, Ţările de Jos, Austria, Polonia, Portugalia, România, Slovenia, Slovacia, Finlanda, Suedia, Regatul Unit
- Additional information:
- relevanţă pentru SEE
- Treaty:
- Tratat privind funcţionarea Uniunii Europene
- Legal basis:
-
- 31990L0425 - A17P2PTB) 31990L0425 - A18P1L1 31990L0425 - A19PTB)
- 31992L0065
- Link
- Link
- Link
- Select all documents mentioning this document No data available in the table
- Modifies:
-
Relation Act Comment Subdivision concerned From To Repeal 32008D0635 01/09/2010
No data available in the table
- Modified by:
-
Relation Act Comment Subdivision concerned From To Modified by 32012D0411 înlocuire anexă III 01/01/2013 Modified by 32012D0411 modificare anexă I 01/01/2013 Modified by 32012D0411 înlocuire anexă II P. 2 SECTION A 01/01/2013 Modified by 32012D0411 înlocuire anexă IV P. 2 01/01/2013 Modified by 32013D0470 înlocuire anexă II P.2 SECTION A Modified by 32013D0470 înlocuire anexă IV P.2 Modified by 32013R0519 modificare anexă III 01/07/2013 Modified by 32013R0519 modificare anexă I 01/07/2013 Modified by 32014D0802 înlocuire anexă IV P.2 01/01/2015 Modified by 32016D2002 înlocuire anexă II p. 2 SECTION A 09/11/2016 Modified by 32019D0604 adăugare anexă III tabel text Modified by 32019D0604 adăugare anexă I tabel text Modified by 32019D1767 adăugare anexă III tabel text Modified by 32019D1767 adăugare anexă I tabel text Modified by 32020D2217 adăugare anexă III text 01/01/2021 Modified by 32020D2217 adăugare anexă I text 01/01/2021 Repealed by 32021R0404 21/04/2021 - Instruments cited:
- Link
- EUROVOC descriptor:
- Subject matter:
- Directory code:
|
31.8.2010 |
RO |
Jurnalul Oficial al Uniunii Europene |
L 228/74 |
DECIZIA COMISIEI
din 26 august 2010
privind importurile de material seminal, ovule și embrioni de animale din speciile ovină și caprină în Uniune
[notificată cu numărul C(2010) 5780]
(Text cu relevanță pentru SEE)
(2010/472/UE)
COMISIA EUROPEANĂ,
având în vedere Tratatul privind funcționarea Uniunii Europene,
având în vedere Directiva 92/65/CEE a Consiliului din 13 iulie 1992 de definire a cerințelor de sănătate animală care reglementează schimburile și importurile în Comunitate de animale, material seminal, ovule și embrioni care nu se supun, în ceea ce privește cerințele de sănătate animală, reglementărilor comunitare speciale prevăzute în anexa A punctul I la Directiva 90/425/CEE (1), în special articolul 17 alineatul (2) litera (b) și articolul 17 alineatul (3), articolul 18 alineatul (1) prima liniuță și articolul 19 teza introductivă și litera (b),
întrucât:
|
(1) |
Directiva 92/65/CEE definește condițiile de sănătate animală care reglementează importurile în Uniune de material seminal, ovule și embrioni de animale din speciile ovină și caprină (denumite în continuare „produsele”). Aceasta prevede că pot fi importate în Uniune numai produsele care provin dintr-o țară terță inclusă pe o listă de țări terțe, stabilită în conformitate cu directiva respectivă și însoțite de un certificat de sănătate corespunzător unui model care este, de asemenea, întocmit în conformitate cu directiva respectivă. Certificatul de sănătate trebuie să certifice că produsele provin din centre de colectare și de depozitare aprobate sau de la echipe de colectare și de producție care oferă garanții cel puțin echivalente cu cele prevăzute în anexa D capitolul I la directiva respectivă. |
|
(2) |
Decizia 2008/635/CE a Comisiei din 22 iulie 2008 privind importurile în Comunitate de material seminal, ovule și embrioni de animale din speciile ovină și caprină, în ceea ce privește lista țărilor terțe, lista centrelor de colectare a materialului seminal și echipele de recoltare a embrionilor, precum și cerințele de certificare (2) stabilește în prezent lista țărilor terțe din care statele membre urmează să autorizeze importurile produselor. |
|
(3) |
Directiva 92/65/CEE, astfel cum a fost modificată prin Directiva 2008/73/CE a Consiliului (3), a introdus o procedură simplificată pentru enumerarea centrelor de colectare și depozitare a materialului seminal și a echipelor de colectare și producție de embrioni din țări terțe aprobate pentru importurile produselor în Uniune. |
|
(4) |
În plus, anexa D la Directiva 92/65/CEE, astfel cum a fost modificată prin Regulamentul (UE) nr. 176/2010 al Comisiei (4), stabilește anumite cerințe noi pentru produse, care urmează să se aplice de la 1 septembrie 2010. Aceasta introduce reguli privind centrele de depozitare a materialului seminal și condiții detaliate pentru aprobarea și supravegherea lor. De asemenea, stabilește condiții detaliate pentru aprobarea și supravegherea echipelor de colectare și producție de embrioni, pentru colectarea și tratarea embrionilor obținuți in vivo, producția și tratarea embrionilor fertilizați in vitro și a embrionilor micromanipulați. De asemenea, a modificat condițiile care urmează să fie aplicate animalelor donatoare de material seminal, ovule și embrioni de animale din speciile ovină și caprină. |
|
(5) |
În consecință, este necesar să se stabilească noi certificate de sănătate pentru importurile produselor în Uniune, ținând cont de modificările aduse Directivei 92/65/CEE prin Directiva 2008/73/CE și Regulamentul (UE) nr. 176/2010. |
|
(6) |
În plus, se recomandă ca transporturile de produse importate în Uniune din Elveția să fie însoțite de un certificat de sănătate întocmit în conformitate cu modelele utilizate pentru schimburile comerciale în interiorul Uniunii cu material seminal, ovule și embrioni de animale din speciile ovină și caprină, stabilite în Decizia 2010/470/UE a Comisiei din 26 august 2010 de stabilire a modelelor de certificate de sănătate pentru schimburile comerciale în interiorul Uniunii de material seminal, ovule și embrioni de animale din speciile ecvină, ovină și caprină și de ovule și embrioni de animale din specia porcină (5), cu adaptările stabilite la punctul 7 din anexa 11 apendicele 2 capitolul IX litera (B) din Acordul dintre Comunitatea Europeană și Confederația Elvețiană privind comerțul cu produse agricole, astfel cum a fost aprobat prin Decizia 2002/309/CE a Consiliului și a Comisiei privind Acordul de cooperare științifică și tehnologică din 4 aprilie 2002 privind încheierea a șapte acorduri cu Confederația Elvețiană (6). |
|
(7) |
În aplicarea prezentei decizii, ar trebui să se ia în considerare cerințele specifice de certificare și modelele de atestare de sănătate animală care pot fi stabilite în conformitate cu Acordul dintre Comunitatea Europeană și Guvernul Canadei cu privire la măsurile sanitare pentru protecția sănătății publice și animale în comerțul cu animale vii și produse de origine animală (7), astfel cum a fost aprobat prin Decizia 1999/201/CE a Consiliului (8). |
|
(8) |
În aplicarea prezentei decizii, ar trebui să se ia în considerare, de asemenea, cerințele specifice de certificare și modelele de atestare de sănătate animală care pot fi stabilite în conformitate cu Acordul dintre Comunitatea Europeană și Noua Zeelandă privind măsurile sanitare aplicabile în comerțul cu animale vii și produse de origine animală (9), astfel cum a fost aprobat prin Decizia 97/132/CE a Consiliului (10). |
|
(9) |
Din motive de claritate și de coerență a legislației Uniunii, Decizia 2008/635/CE ar trebui abrogată și înlocuită cu prezenta decizie. |
|
(10) |
Pentru a se evita perturbarea schimburilor comerciale, folosirea certificatelor de sănătate emise în conformitate cu Decizia 2008/635/CE ar trebui autorizată pentru o perioadă de tranziție, cu anumite condiții. |
|
(11) |
Măsurile prevăzute în prezenta decizie sunt conforme cu avizul Comitetului permanent pentru lanțul alimentar și sănătatea animală, |
ADOPTĂ PREZENTA DECIZIE:
Articolul 1
Obiect
Prezenta decizie stabilește o listă de țări terțe sau părți ale acestora din care statele membre urmează să autorizeze importul în Uniune de transporturi de material seminal, ovule și embrioni de animale din speciile ovină și caprină.
De asemenea, ea stabilește cerințele de certificare pentru importul acelor produse în Uniune.
Articolul 2
Importurile de material seminal
Statele membre autorizează importurile transporturilor de material seminal de animale din speciile ovină și caprină cu condiția să respecte următoarele condiții:
|
(a) |
provin dintr-o țară terță sau dintr-o parte a unei țări terțe menționate în anexa I; |
|
(b) |
provin dintr-un centru aprobat de colectare sau de depozitare a materialului seminal, enumerat în conformitate cu articolul 17 alineatul (3) litera (b) din Directiva 92/65/CEE; |
|
(c) |
sunt însoțite de un certificat de sănătate întocmit în conformitate cu următoarele modele de certificate de sănătate prezentate în partea 2 din anexa II și completate conform notelor explicative cuprinse în partea 1 a anexei respective:
Cu toate acestea, atunci când sunt prevăzute cerințe specifice de certificare în acorduri bilaterale între Uniune și țările terțe, se aplică cerințele respective; |
|
(d) |
respectă cerințele prevăzute în certificatele de sănătate menționate la litera (c). |
Articolul 3
Importurile de ovule și embrioni
Statele membre autorizează importurile transporturilor de ovule și embrioni de animale din speciile ovină și caprină cu condiția să respecte următoarele condiții:
|
(a) |
provin dintr-o țară terță sau dintr-o parte a unei țări terțe menționate în anexa III; |
|
(b) |
provin de la o echipă aprobată de colectare sau de producere a embrionilor, enumerată în conformitate cu articolul 17 alineatul (3) litera (b) din Directiva 92/65/CEE; |
|
(c) |
sunt însoțite de un certificat de sănătate întocmit în conformitate cu modelul prezentat în partea 2 din anexa IV și completat conform notelor explicative cuprinse în partea 1 a anexei respective. Cu toate acestea, atunci când sunt prevăzute cerințe specifice de certificare în acorduri bilaterale între Uniune și țările terțe, trebuie să se aplice cerințele respective. |
|
(d) |
respectă cerințele prevăzute în certificatul de sănătate menționate la litera (c). |
Articolul 4
Condiții generale privind transporturile de material seminal, ovule și embrioni către Uniune
(1) Transporturile de material seminal, ovule și embrioni de animale din speciile ovină și caprină nu se transportă în același container cu alte transporturi de material seminal, ovule și embrioni care:
|
(a) |
nu sunt destinate introducerii în Uniune; sau |
|
(b) |
au o stare de sănătate inferioară. |
(2) În cursul transportului către Uniunea Europeană, transporturile de material seminal, ovule și embrioni se plasează în containere închise și sigilate, iar sigiliul trebuie să rămână intact pe durata transportului.
Articolul 5
Abrogare
Decizia 2008/635/CE se abrogă.
Articolul 6
Dispoziții tranzitorii
Pentru o perioadă de tranziție de până la 31 august 2011, statele membre autorizează importurile din țări terțe de stocuri din următoarele produse:
|
(a) |
material seminal de animale din speciile ovină și caprină care a fost colectat, tratat și depozitat în conformitate cu Directiva 92/65/CEE până la 31 august 2010 și care este însoțit de un certificat de sănătate emis cel târziu la 31 mai 2011 în conformitate cu modelul prezentat în anexa II la Decizia 2008/635/CE; |
|
(b) |
ovule și embrioni de animale din speciile ovină și caprină care au fost colectați sau produși, tratați și depozitați în conformitate cu Directiva 92/65/CEE până la 31 august 2010 și care sunt însoțiți de un certificat de sănătate emis cel târziu la 31 mai 2011 în conformitate cu modelul prezentat în anexa VI la Decizia 2008/635/CE. |
Articolul 7
Aplicabilitate
Prezenta decizie se aplică de la 1 septembrie 2010.
Articolul 8
Destinatari
Prezenta decizie se adresează statelor membre.
Adoptată la Bruxelles, 26 august 2010.
Pentru Comisie
John DALLI
Membru al Comisiei
(1) JO L 268, 14.9.1992, p. 54.
(2) JO L 206, 2.8.2008, p. 17.
(3) JO L 219, 14.8.2008, p. 40.
(5) A se vedea pagina 15 din prezentul Jurnal Oficial.
(6) JO L 114, 30.4.2002, p. 1.
(10) JO L 57, 26.2.1997, p. 4.
ANEXA I
Lista țărilor terțe sau a părților acestora din care statele membre urmează să autorizeze importurile de transporturi de material seminal de animale din speciile ovină și caprină
|
Codul ISO |
Numele țării terțe |
Observații |
|
|
Descrierea teritoriului (dacă este cazul) |
Garanții suplimentare |
||
|
AU |
Australia |
|
Garanțiile suplimentare în ceea ce privește testarea, stabilite la punctele II.4.9 și II.4.10 din certificatul de sănătate prezentat în anexa II partea 2 secțiunea A sunt obligatorii. |
|
CA |
Canada |
Teritoriu, astfel cum este descris în partea 1 a anexei I la Regulamentul (UE) nr. 206/2010 al Comisiei (1). |
Garanția suplimentară în ceea ce privește testarea, stabilită la punctul II.4.9 din certificatul de sănătate prezentat în secțiunea A din partea 2 a anexei II este obligatorie. |
|
CH |
Elveția (2) |
|
|
|
CL |
Chile |
|
|
|
GL |
Groenlanda |
|
|
|
HR |
Croația |
|
|
|
IS |
Islanda |
|
|
|
NZ |
Noua Zeelandă |
|
|
|
PM |
Saint Pierre și Miquelon |
|
|
|
US |
Statele Unite |
|
Garanția suplimentară în ceea ce privește testarea, stabilită la punctul II.4.9 din certificatul de sănătate prezentat în secțiunea A din partea 2 a anexei II este obligatorie. |
(2) Certificate în conformitate cu Acordul dintre Comunitatea Europeană și Confederația Elvețiană privind comerțul cu produse agricole, astfel cum a fost aprobat prin Decizia 2002/309/CE a Consiliului și a Comisiei privind Acordul de cooperare științifică și tehnologică din 4 aprilie 2002 privind încheierea a șapte acorduri cu Confederația Elvețiană (JO L 114, 30.4.2002, p. 132).
ANEXA II
PARTEA 1
Note explicative pentru certificare
|
(a) |
Certificatele de sănătate se emit de către autoritatea competentă din țara terță exportatoare, în conformitate cu modelul prezentat în partea 2 din anexa II. În cazul în care statul membru de destinație solicită cerințe suplimentare de certificare, atestări care să certifice faptul că aceste cerințe sunt îndeplinite se adaugă, de asemenea, în formularul original al certificatului de sănătate. |
|
(b) |
Originalul certificatului de sănătate este compus dintr-o singură foaie de hârtie, sau, în cazul în care nu este suficient, trebuie prezentat astfel încât toate foile de hârtie necesare să facă parte dintr-un tot integrat și indivizibil. |
|
(c) |
Atunci când modelul de certificat de sănătate indică alegerea mențiunii adecvate, mențiunile irelevante pot fi tăiate cu o linie și parafate și apoi ștampilate de inspectorul autorizat sau eliminate complet din certificat. |
|
(d) |
Certificatul de sănătate se întocmește în cel puțin una dintre limbile oficiale ale statului membru al punctului de control la frontiera de intrare în Uniunea Europeană și în limba statului membru de destinație. Totuși, statele membre în cauză pot autoriza elaborarea certificatului în limba oficială a altui stat membru, însoțit, dacă este necesar, de o traducere oficială. |
|
(e) |
În cazul în care se anexează foi suplimentare la certificatul de sănătate, din motive de identificare a diferitelor elemente ale transportului (tabelul de la rubrica I.28 din modelul de certificat de sănătate), aceste foi se consideră, de asemenea, ca făcând parte din originalul certificatului de sănătate prin aplicarea, pe fiecare pagină, a semnăturii și a ștampilei inspectorului autorizat. |
|
(f) |
În cazul în care certificatul de sănătate, inclusiv tabelele suplimentare prevăzute la litera (e), se compune din mai multe pagini, fiecare pagină se numerotează în josul paginii – (numărul paginii) din (numărul total de pagini) – și este prevăzută, sus, cu numărul de referință al certificatului atribuit de autoritatea competentă. |
|
(g) |
Originalul certificatului de sănătate trebuie completat și semnat de către un medic veterinar oficial în cursul ultimei zile lucrătoare care precedă încărcarea transportului pentru export către Uniunea Europeană. Autoritățile competente din țara terță exportatoare asigură respectarea cerințelor de certificare echivalente cu cele stabilite în Directiva 96/93/CE a Consiliului (1). Culoarea semnăturii și ștampilei veterinarului oficial trebuie să fie diferită de cea a textului tipărit pe certificatul de sănătate. Această cerință se aplică, de asemenea, ștampilelor, cu excepția timbrelor seci sau a securizării cu filigran. |
|
(h) |
Originalul certificatului de sănătate trebuie să însoțească transportul până la punctul de control la frontiera de intrare în Uniunea Europeană. |
|
(i) |
Numărul de referință al certificatului menționat la rubricile I.2 și II.a ale modelului de certificat de sănătate trebuie să fie emis de către autoritatea competentă din țara terță exportatoare. |
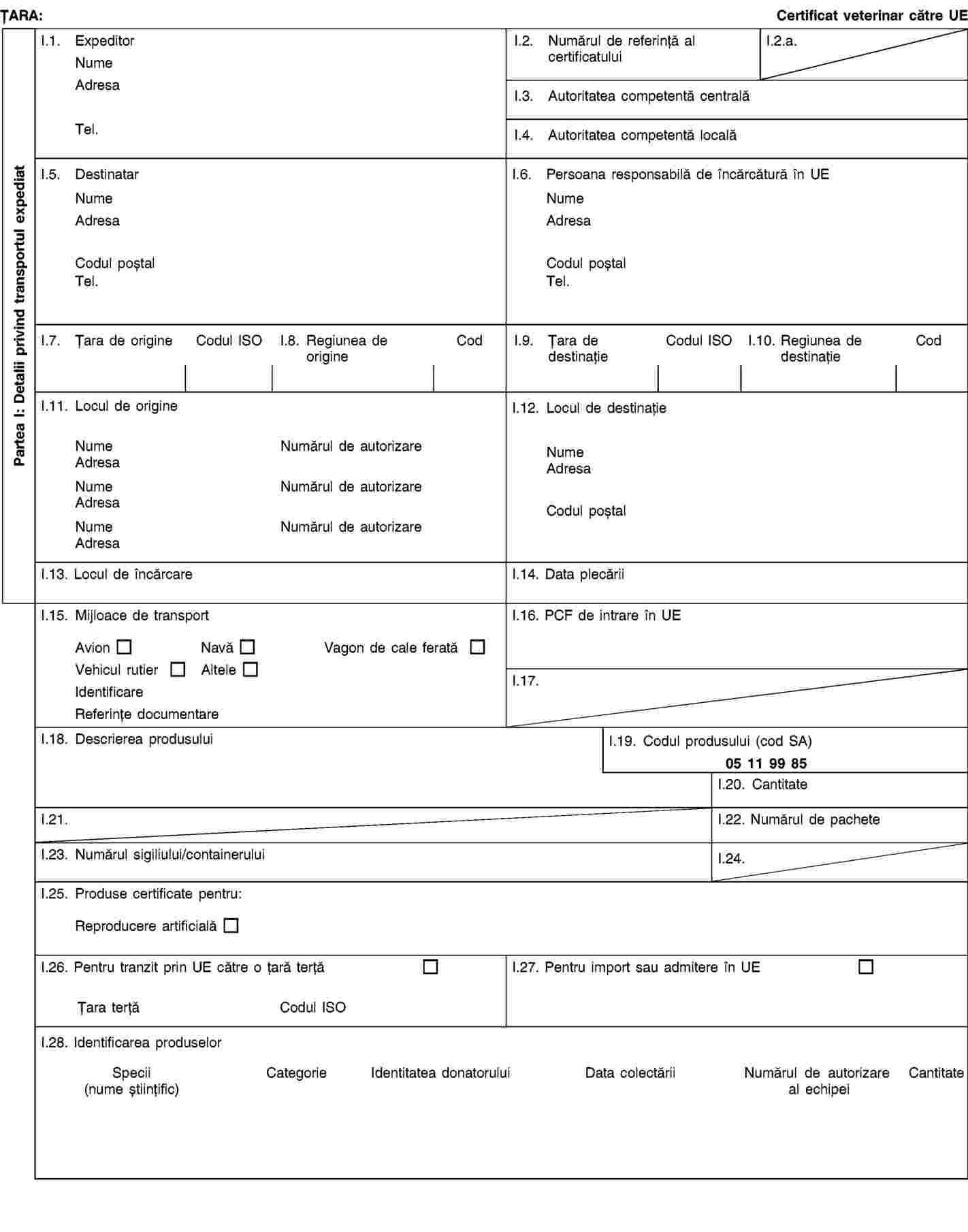
PARTEA 2
Modele de certificate de sănătate pentru importurile transporturilor de material seminal de animale din speciile ovină și caprină
Secțiunea A
|
MODELUL 1 – |
Certificat de sănătate pentru materialul seminal expediat dintr-un centru aprobat de colectare a materialului seminal care este locul de origine a materialului seminal |





Secțiunea B
|
MODELUL 2 – |
Certificat de sănătate pentru materialul seminal expediat dintr-un centru aprobat de depozitare a materialului seminal |



ANEXA III
Lista țărilor terțe sau a părților acestora din care statele membre urmează să autorizeze importurile de transporturi de ovule și embrioni de animale din speciile ovină și caprină
|
Codul ISO |
Numele țării terțe |
Observații |
|
|
Descrierea teritoriului (dacă este cazul) |
Garanții suplimentare |
||
|
AU |
Australia |
|
Garanțiile suplimentare în ceea ce privește testarea, stabilite la punctele II.2.6 și II.2.7 din certificatul de sănătate prezentat în partea 2 a anexei IV sunt obligatorii. |
|
CA |
Canada |
Teritoriu, astfel cum este descris în partea 1 a anexei I la Regulamentul (UE) nr. 206/2010 al Comisiei (1), astfel cum a fost modificat ultima dată. |
Garanția suplimentară în ceea ce privește testarea, stabilită la punctul II.2.7 din certificatul de sănătate prezentat în partea 2 a anexei IV este obligatorie. |
|
CH |
Elveția (2) |
|
|
|
CL |
Chile |
|
|
|
GL |
Groenlanda |
|
|
|
HR |
Croația |
|
|
|
IS |
Islanda |
|
|
|
NZ |
Noua Zeelandă |
|
|
|
PM |
Saint Pierre și Miquelon |
|
|
|
US |
Statele Unite |
|
Garanția suplimentară în ceea ce privește testarea, stabilită la punctul II.2.7 din certificatul de sănătate prezentat în partea 2 a anexei IV este obligatorie. |
(2) Certificate în conformitate cu Acordul dintre Comunitatea Europeană și Confederația Elvețiană privind comerțul cu produse agricole, astfel cum a fost aprobat prin Decizia 2002/309/CE a Consiliului și a Comisiei privind Acordul de cooperare științifică și tehnologică din 4 aprilie 2002 privind încheierea a șapte acorduri cu Confederația Elvețiană (JO L 114, 30.4.2002, p. 132).
ANEXA IV
PARTEA 1
Note explicative pentru certificare
|
(a) |
Certificatele de sănătate se emit de către autoritatea competentă din țara terță exportatoare, în conformitate cu modelul prezentat în partea 2 din anexa IV. În cazul în care statul membru de destinație solicită cerințe suplimentare de certificare, atestări care să certifice faptul că aceste cerințe sunt îndeplinite se adaugă, de asemenea, în formularul original al certificatului de sănătate. |
|
(b) |
Originalul certificatului de sănătate este compus dintr-o singură foaie de hârtie, sau, în cazul în care nu este suficient, trebuie prezentat astfel încât toate foile de hârtie necesare să facă parte dintr-un tot integrat și indivizibil. |
|
(c) |
Atunci când modelul de certificat de sănătate indică alegerea mențiunii adecvate, mențiunile irelevante pot fi tăiate cu o linie și parafate și apoi ștampilate de inspectorul autorizat sau eliminate complet din certificat. |
|
(d) |
Certificatul de sănătate se întocmește în cel puțin una din limbile oficiale ale statului membru al punctului de control la frontiera de intrare în Uniunea Europeană și în limba statului membru de destinație. Totuși, statele membre în cauză pot autoriza elaborarea certificatului în limba oficială a altui stat membru, însoțit, dacă este necesar, de o traducere oficială. |
|
(e) |
În cazul în care se anexează foi suplimentare la certificatul de sănătate, din motive de identificare a diferitelor elemente ale transportului (tabelul de la rubrica I.28 din modelul de certificat de sănătate), aceste foi se consideră, de asemenea, ca făcând parte din originalul certificatului de sănătate prin aplicarea, pe fiecare pagină, a semnăturii și a ștampilei inspectorului autorizat. |
|
(f) |
În cazul în care certificatul de sănătate, inclusiv tabelele suplimentare prevăzute la litera (e), se compune din mai multe pagini, fiecare pagină se numerotează în josul paginii – (numărul paginii) din (numărul total de pagini) – și este prevăzută, sus, cu numărul de referință al certificatului atribuit de autoritatea competentă. |
|
(g) |
Originalul certificatului de sănătate trebuie completat și semnat de către un medic veterinar oficial în cursul ultimei zile lucrătoare care precedă încărcarea transportului pentru export către Uniunea Europeană. Autoritățile competente din țara terță exportatoare asigură respectarea cerințelor de certificare echivalente cu cele stabilite în Directiva 96/93/CE a Consiliului (1). Culoarea semnăturii și ștampilei veterinarului oficial trebuie să fie diferită de cea a textului tipărit pe certificatul de sănătate. Această cerință se aplică, de asemenea, ștampilelor, cu excepția timbrelor seci sau a securizării cu filigran. |
|
(h) |
Originalul certificatului de sănătate trebuie să însoțească transportul până la punctul de control la frontiera de intrare în Uniunea Europeană. |
|
(i) |
Numărul de referință al certificatului menționat la rubricile I.2 și II.a ale modelului de certificat de sănătate trebuie să fie emis de către autoritatea competentă din țara terță exportatoare. |
PARTEA 2
Modele de certificate de sănătate pentru importurile transporturilor de ovule și embrioni de animale din speciile ovină și caprină