1964L0432 — PT — 27.05.2015 — 019.002
Este texto constitui um instrumento de documentação e não tem qualquer efeito jurídico. As Instituições da União não assumem qualquer responsabilidade pelo respetivo conteúdo. As versões dos atos relevantes que fazem fé, incluindo os respetivos preâmbulos, são as publicadas no Jornal Oficial da União Europeia e encontram-se disponíveis no EUR-Lex. É possível aceder diretamente a esses textos oficiais através das ligações incluídas no presente documento
|
►B
|
DIRECTIVA DO CONSELHO
de 26 de Junho de 1964
relativa a problemas de fiscalização sanitária em matéria de comércio intracomunitário de animais das espécies bovina e suína
(64/432/CEE)
(JO P 121 de 29.7.1964, p. 1977)
|
Alterado por:
Alterado por:
|
A1
|
ACTO relativo às condições de adesão e às adaptações dos Tratados
|
L 73
|
14
|
27.3.1972
|
|
|
|
L 002
|
1
|
..
|
|
A2
|
ACTO relativo às condições de adesão da República Helénica e às adaptações dos Tratados
|
L 291
|
17
|
19.11.1979
|
|
A3
|
ACTO relativo às condições de adesão do Reino da Noruega, da República da Áustria, da República da Finlândia e do Reino da Suécia e às adaptações dos Tratados em que se funda a União Europeia (94/C 241/08)
|
C 241
|
21
|
29.8.1994
|
|
|
|
L 001
|
1
|
..
|
|
►A4
|
ACTO relativo às condições de adesão da República Checa, da República da Estónia, da República de Chipre, da República da Letónia, da República da Lituânia, da República da Hungria, da República de Malta, da República da Polónia, da República da Eslovénia e da República Eslovaca e às adaptações dos Tratados em que se funda a União Europeia
|
L 236
|
33
|
23.9.2003
|
Rectificado por:
|
(*)
|
Este acto não existe em língua portuguesa.
|
▼B
DIRECTIVA DO CONSELHO
de 26 de Junho de 1964
relativa a problemas de fiscalização sanitária em matéria de comércio intracomunitário de animais das espécies bovina e suína
(64/432/CEE)
▼M42
Artigo 1.o
A presente directiva é aplicável ao comércio intracomunitário de bovinos e de suínos com excepção dos suínos selvagens, definidos na alínea e) do artigo 2.o da Directiva 80/217/CEE (
4
), sem prejuízo do disposto nas Directivas 80/215/CEE (
5
), 85/511/CEE, 88/407/CEE (
6
), 89/608/CEE (
7
), 90/425/CEE, 90/429/CEE (
8
), 90/667/CEE (
9
), 91/496/CEE, 91/628/CEE (
10
), 92/102/CEE, 92/119/CEE (
11
) e na Decisão 90/424/CEE (
12
).
Artigo 2.o
1. São aplicáveis as definições dadas no artigo 2.o da Directiva 90/425/CEE e na Directiva 91/628/CE.
2. Além disso, para efeitos da presente directiva, entende-se por:
a)
Efectivo: animal ou conjunto de animais mantidos numa exploração [na acepção da alínea b) do artigo 2.o da Directiva 92/102/CEE] como unidade epidemiológica; se existir mais do que um efectivo numa exploração, devem formar uma unidade distinta com o mesmo estatuto sanitário;
b)
Animal para abate: bovino (incluindo as espécies Bison bison, e Bubalus bubalus ou porcino destinado a um matadouro ou a um mercado a partir do qual só pode ser transportado para efeitos de abate;
c)
Animal para reprodução ou produção: bovino (incluindo as espécies Bison bison e Bubalus bubalus) ou suíno não abrangido pela alínea b), destinado à reprodução, à produção de leite ou de carne, a trabalhar como animal de tiro, ou a exposições ou concursos com excepção dos animais que participem em acontecimentos culturais e desportivos;
d)
Efectivo bovino oficialmente indemne de tuberculose: efectivo bovino que satisfaz as condições definidas na
►
secção I, pontos 1 e 2 do anexo A ◄ ;
e)
Estado-membro ou região de um Estado-membro oficialmente indemne de tuberculose: Estado-membro ou parte de um Estado-membro que satisfaz as condições definidas na
►
secção I, pontos 4 e 5 do Anexo A ◄ ;
f)
Efectivo bovino oficialmente indemne de brucelose: efectivo bovino que satisfaz as condições definidas na
►
secção II, pontos 1 e 2 do Anexo A ◄ ;
g)
Região oficialmente indemne de brucelose: região de um Estado-membro que satisfaz as condições definidas na secção II, pontos 7, 8 e 9, do anexo A;
h)
Estado-membro oficialmente indemne de brucelose: Estado-membro que satisfaz as condições definidas na
►
secção II, pontos 7, 8 e 9 do anexo A ◄ ;
i)
Efectivo bovino indemne de brucelose: efectivo bovino que satisfaz as condições definidas na
►
secção II, pontos 4 e 5 do anexo A ◄ ;
j)
Efectivo oficialmente indemne de leucose bovina enzoótica: efectivo que satisfaz as condições definidas na capitulo I, partes A e B, do anexo D;
k)
Estado-membro ou região indemne de leucose bovina enzoótica: região ou Estado-membro que satisfaz as condições definidas no
►
capítulo I, partes E e F, do anexo D ◄ ;
l)
Veterinário oficial: o veterinário designado pela autoridade central competente;
m)
Veterinário autorizado: veterinário aprovado pela autoridade veterinária competente de acordo com o disposto no n.o 4, alínea b), do artigo 14.o;
n)
Doenças de comunicação obrigatória: as doenças referidas na alínea i) do anexo E (I);
o)
Centro de agrupamento: qualquer local, incluindo explorações, centros de recolha e mercados, onde são agrupados bovinos e suínos provenientes de diferentes explorações de origem com vista à constituição de lotes de animais destinados ao comércio. Estes centros de agrupamento devem ser aprovados para fins comerciais e satisfazer as exigências estabelecidas no artigo 11.o;
p)
Região: a parte do território de um Estado-membro cuja superfície seja de pelo menos 2 000 km2 e sujeita a inspecção pelas autoridades competentes e que inclui pelo menos uma das seguintes regiões administrativas:
|
— Bélgica:
|
provinceprovincie,
|
|
— Alemanha:
|
Regierungsbezirk,
|
|
— Dinamarca:
|
amt ou ilha,
|
|
— França:
|
département,
|
|
— Itália:
|
provincia,
|
|
— Luxemburgo:
|
—,
|
|
— Países Baixos:
|
rvv-kring,
|
|
— Reino Unido:
|
Inglaterra, País de Gales e Irlanda do Norte: county; Escócia: district ou island area,
|
|
— Irlanda:
|
county,
|
|
— Grécia:
|
νομός,
|
|
— Espanha:
|
provincia,
|
|
— Portugal:
|
continente: distrito; outras partes do território português: região autónoma,
|
|
— Áustria:
|
Bezirk,
|
|
— Suécia:
|
ian,
|
|
— Finlândia:
|
lääni/iän,
|
|
▼A4
|
|
— República Checa:
|
kraj,
|
|
— Estónia:
|
maakond,
|
|
— Chipre:
|
επαρχία (distrito),
|
|
— Letónia:
|
rajons,
|
|
— Lituânia:
|
apskritis,
|
|
— Hungria:
|
megye,
|
|
— Malta:
|
—,
|
|
— Polónia:
|
powiat,
|
|
— Eslovénia:
|
območje,
|
|
— Eslováquia:
|
kraj,
|
|
▼M53
|
|
— Bulgária:
|
област,
|
|
— Roménia:
|
județ,
|
|
▼M58
|
|
— Croácia:
|
županija;
|
|
▼M42
|
q)
Comerciante: pessoa singular ou colectiva que compra e vende, directa ou indirectamente, animais para fins comerciais, que tem uma rotação regular desses animais, que, no prazo máximo de 30 dias a contar da aquisição dos animais, os revende ou transfere das primeiras instalações para outras que não são da sua propriedade, que se encontra registada e que satisfaz as condições estabelecidas no artigo 13.o
Artigo 3.o
1. Cada Estado-membro assegurará que apenas sejam enviados a partir do seu território para o território de outro Estado-membro os animais que satisfaçam as condições pertinentes, definidas na presente directiva.
2. Os bovinos e suínos abrangidos pela presente directiva devem:
a) Ser sujeitos:
— a um controlo de identidade e
— a um exame clínico nas 24 horas anteriores à partida realizado por um veterinário oficial, não apresentando qualquer sinal clínico de doença;
b) Ser provenientes de uma exploração ou de uma área que não seja objecto, por motivos sanitários, de qualquer proibição ou restrição que afecte as espécies em questão, de acordo com a legislação comunitária e/ou nacional;
▼C1
c) Ser identificados como previsto na Directiva 92/102/CEE, no caso dos animais da espécie suína, e como previsto no Regulamento (CE) n.o 1760/2000, no caso dos animais da espécie bovina;
▼M42
d) Não ser destinados ao abate ou a quarentena no âmbito de um programa de erradicação de uma doença contagiosa ou infecciosa em aplicação num Estado-membro ou região;
e) Satisfazer o disposto nos artigos 4.o e 5.o
Artigo 4.o
1. Os bovinos e suínos abrangidos pela presente directiva não devem, em momento algum, desde a saída da exploração de origem até à chegada ao local de destino noutro Estado-membro, ter estado em contacto com outros animais artiodáctilos que não tenham o mesmo estatuto sanitário.
2. Os bovinos e suínos abrangidos pela presente directiva devem ser transportados em meios de transporte que satisfaçam o disposto na Directiva 91/628/CEE e as disposições adicionais previstas no artigo 12.o
3. As regras que regem as condições de aprovação dos locais onde pode ser efectuada a limpeza e desinfecção serão determinadas de acordo com o mecanismo previsto no artigo 17.o
Artigo 5.o
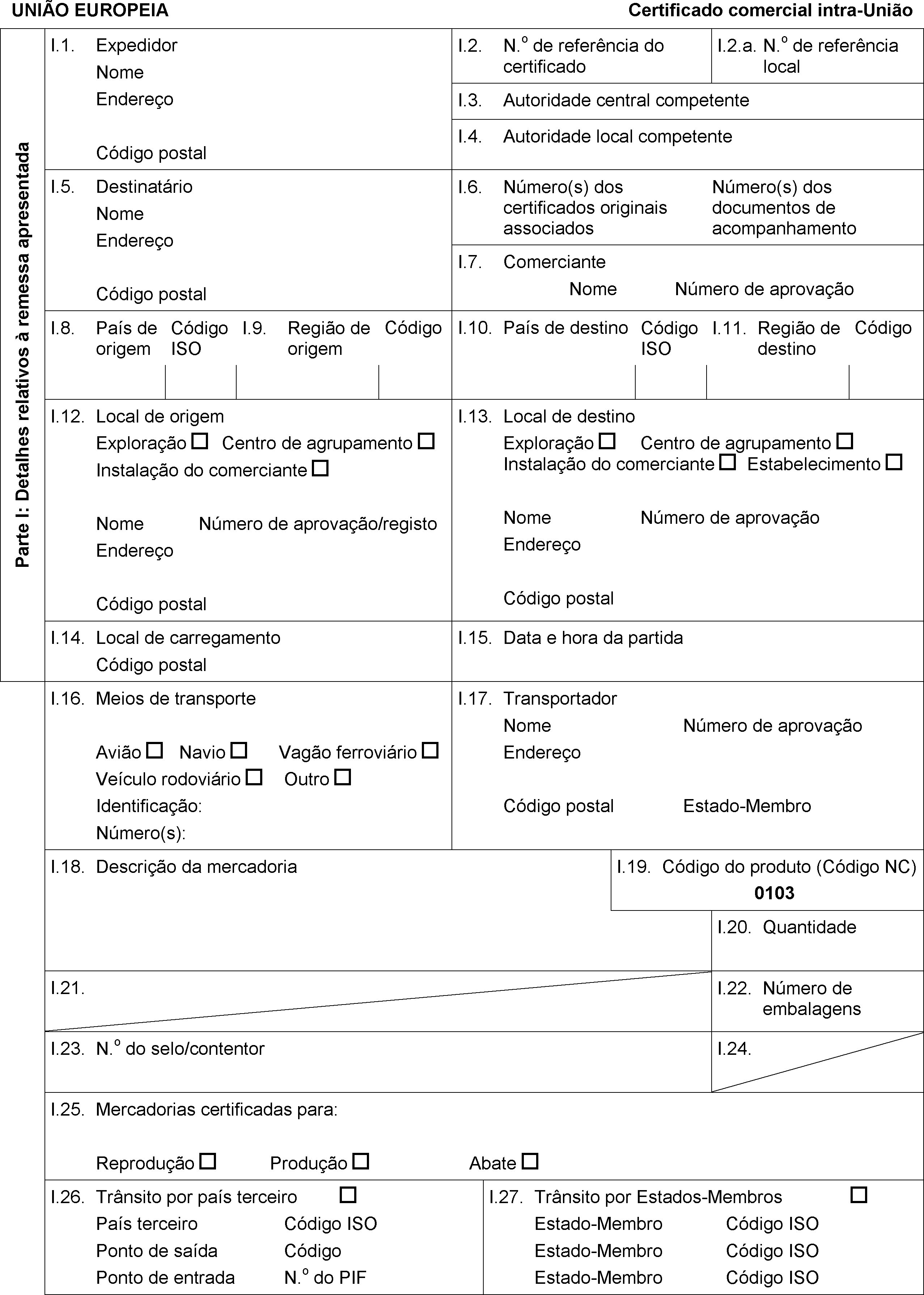
1. Durante o transporte para o local de destino, os bovinos e suínos abrangidos pela presente directiva devem ser acompanhados de um
►
certificado sanitário conforme com o modelo aplicável, (1 ou 2) constante do anexo F ◄ . O certificado consistirá numa única folha ou, nos casos em que seja necessária mais que uma folha, deverá ser constituído de maneira a que todas as folhas façam parte de um conjunto integrado e indivisível, e deve conter um número de série. Deve ser emitido no dia da inspecção sanitária, pelo menos numa das línguas oficiais do país de destino. O certificado será válido durante 10 dias a contar da data da inspecção sanitária.
2. As inspecções sanitárias para a emissão do certificado sanitário (incluindo as garantias adicionais) para uma remessa de animais podem ter lugar na exploração de origem ou num centro de agrupamento. Para o efeito, a autoridade competente velará por que os certificados sanitários sejam estabelecidos pelo veterinário oficial após as inspecções, visitas e controlos previstas pela presente directiva.
Todavia, no que se refere:
a) Aos animais provenientes de centros de agrupamento aprovados, esse certificado pode ser estabelecido:
— com base no documento oficial relativo às informações necessárias preenchido pelo veterinário oficial responsável pela exploração de origem ou
— com base no
►
certificado conforme com o modelo aplicável (1 ou 2) reproduzido no anexo F ◄ e cujas partes A e B serão devidamente preenchidas e comprovadas pelo veterinário oficial responsável pela exploração de origem;
b) Aos animais provenientes de uma exploração qualificada nos termos da rede prevista no artigo 14.o, esse certificado pode ser estabelecido:
— com base no documento oficial relativo às informações necessárias preenchido pelo veterinário autorizado responsável pela exploração de origem ou
— com base no
►
certificado conforme com o modelo aplicável (1 ou 2) reproduzido no anexo F ◄ e cujas partes A e B serão devidamente preenchidas e comprovadas pelo veterinário autorizado responsável pela exploração de origem.
Na mesma ocasião, o veterinário oficial garantirá, se necessário, o respeito das garantias adicionais previstas pela legislação comunitária.
3. O veterinário oficial responsável pelo centro de agrupamento realizará todas as verificações necessárias nos animais logo após a chegada destes.
4. O veterinário oficial que preencha
►
a parte C do certificado conforme com o modelo aplicável (1 ou 2) reproduzido no anexo F ◄ deverá assegurar o registo do transporte dos animais no sistema ANIMO no dia da emissão do certificado.
5. Os animais visados pela presente directiva podem transitar por um centro de agrupamento situado num Estado-membro que não seja o de destino. Nesse caso, o
►
certificado conforme com o modelo aplicável (1 ou 2) reproduzido no anexo F ◄
►
(incluindo a parte C) ◄ deve ser preenchido pelo veterinário oficial responsável do Estado-membro de origem dos animais. O veterinário oficial responsável pelo centro de agrupamento fornece um comprovativo para o Estado-membro de destino mediante a emissão de um segundo
►
certificado conforme com o modelo aplicável (1 ou 2) reproduzido no anexo F ◄ , no qual aporá o número de série do certificado original, e que juntará ao certificado original ou a uma cópia autenticada do mesmo. Nesse caso, o período de validade combinada do certificado não pode exceder o período de validade previsto no n.o 1.
Artigo 6.o
1. Para além de satisfazerem as exigências constantes dos artigos 3.o, 4.o e 5.o, os animais para reprodução ou produção devem:
— ter permanecido numa única exploração durante um período de 30 dias antes do carregamento, ou desde o nascimento na exploração de origem, caso tenham menos de 30 dias. O veterinário oficial deve certificar-se, com base na identificação oficial prevista no n.o 2, alínea c), do artigo 3.o e nos registos oficiais, de que os animais satisfazem esta condição e de que, além disso, são originários de um país da Comunidade ou foram importados de um país terceiro em conformidade com a legislação comunitária em matéria de sanidade animal.
— Contudo, para os animais que transitam por um centro de agrupamento autorizado situado no Estado-membro de origem, a duração do agrupamento dos mesmos animais fora da exploração de origem não poderá exceder seis dias,
— no que respeita aos animais importados de um país terceiro para um Estado-membro que não seja o de destino final devem ser transportados para o Estado-membro de destino tão rapidamente quanto possível, ao abrigo do certificado emitido nos termos do artigo 7.o da Directiva 91/496/CEE,
— no caso de animais importados de um país terceiro, à chegada ao local de destino e antes de qualquer outro transporte, satisfazer as exigências da presente directiva e, em especial, a exigência relativa à permanência prevista no primeiro parágrafo, não podendo ser integrados no efectivo enquanto o veterinário responsável pela exploração não confirmar que os animais em questão não são susceptíveis de pôr em risco o estatuto sanitário da exploração.
— Se um animal proveniente de um país terceiro for introduzido numa exploração, esta não poderá transaccionar qualquer dos seus animais durante um período de 30 dias a contar dessa introdução, salvo se o animal importado se encontrar completamente isolado dos restantes animais da exploração.
2. Para além de satisfazerem as exigências constantes dos artigos 3.o, 4.o e 5.o, os bovinos para reprodução e produção devem ainda:
a)
►M55
pertençam a um efectivo bovino oficialmente indemne de tuberculose e, se tiverem mais de seis semanas, apresentem uma reacção negativa a uma prova intradérmica de tuberculina efectuada nos termos do ponto 2.2 do anexo B, quer nos 30 dias anteriores à saída do efectivo de origem, quer num lugar e em condições a definir nos termos do artigo 17.o
◄
Esta prova intradérmica de tuberculina não é exigida no caso de os animais serem originários de um Estado-membro, ou de uma parte de um Estado-membro, considerado/a oficialmente indemne de tuberculose ou de um Estado-membro, ou de uma parte de um Estado-membro que faça parte de uma rede de vigilância reconhecida;
b) No caso dos animais não castrados provenientes de um efectivo bovino oficialmente indemne de brucelose e com mais de 12 meses de idade, ter apresentado uma contagem brucélica inferior a 30 unidades internacionais de aglutinação por mililitro numa prova de sero-aglutinação (ou em qualquer prova aprovada de acordo com o procedimento do Comité veterinário permanente (CVP) na sequência da adopção dos protocolos pertinentes) realizada no período de 30 dias imediatamente anterior à saída do efectivo de origem e efectuada em conformidade com o disposto na secção A do anexo C.
Esta prova de sero-aglutinação (ou qualquer prova aprovada de acordo com o procedimento do CVP na sequência da adopção dos protocolos pertinentes) não é exigida se os animais forem originários de um Estado-membro, ou de uma parte de um Estado-membro, considerado/a oficialmente indemne de brucelose ou de um Estado-membro, ou de uma parte de um Estado-membro que faça parte de uma rede de vigilância reconhecida;
c) Ser provenientes de um efectivo oficialmente indemne de leucose bovina enzoótica e, caso se trate de animais com mais de 12 meses de idade, ter reagido negativamente a uma prova individual realizada durante os 30 dias anteriores à sua saída do efectivo de origem, em conformidade com as disposições do anexo D.
Esta prova não é exigida se os animais forem originários de um Estado-membro, ou de uma parte de um Estado-membro, considerado/a oficialmente indemne de leucose bovina enzoótica ou de um Estado-membro, ou de uma parte de um Estado-membro que faça parte de uma rede de vigilância reconhecida;
d) Não ter estado em contacto, desde a saída da exploração de origem até à chegada ao local de destino, com animais que apenas satisfaçam as exigências do n.o 3 enunciadas;
▼M46
e) Não ter, até 31 de Dezembro de 2000, sido submetidos às provas previstas nas alíneas a) e b), no caso dos bovinos com menos de 30 meses destinados à produção de carne que:
— provenham de uma exploração bovina oficialmente indemne de tuberculose e de brucelose,
— estejam acompanhados de um certificado sanitário conforme com o ponto 7 do modelo 1, secção A do anexo F, devidamente preenchido,
— permaneçam sob supervisão até ao abate,
— durante o transporte não tenham estado em contacto com bovinos que não sejam provenientes de efectivos oficialmente indemnes dessas doenças,
desde que:
— essas disposições se limitem ao comércio entre Estados-Membros ou regiões dos Estados-Membros com o mesmo estatuto sanitário em relação à tuberculose ou à brucelose,
— o Estado-Membro de destino tome todas as medidas necessárias para evitar qualquer contaminação de efectivos indígenas,
— os Estados-Membros ponham em prática um sistema adequado de verificações por sondagem, inspecção e controlo destinado a garantir uma aplicação eficaz da presente regulamentação,
— a Comissão controle a aplicação correcta da presente directiva a fim de garantir o pleno respeito da regulamentação pelos Estados-Membros.
▼M42
3. Para além de satisfazerem as exigências dos artigos 3.o, 4.o e 5.o, os bovinos para abate devem ser provenientes de efectivos oficialmente indemnes de tuberculose ou de leucose bovina enzoótica; os bovinos não castrados devem ainda ser provenientes de efectivos oficialmente indemnes de brucelose.
Todavia, até
►M46
31 de Dezembro de 2000 ◄ , os países destinatários podem conceder à Espanha autorizações gerais ou limitadas de introdução nos respectivos territórios de animais para abate da espécie bovina provenientes de efectivos não oficialmente indemnes de tuberculose, de leucose bovina enzoótica e de brucelose, desde que esses animais:
— tenham sido submetidos com resultado negativo, nos trinta dias que precedem o embarque, às provas adequadas prescritas nos anexos B, C e D,
— sejam directamente conduzidos, assim que cheguem ao país de destino, para um matadouro e nele serem abatidos o mais rapidamente possível e o mais tardar 72 horas após a chegada, de acordo com os requisitos em matéria de polícia sanitária.
▼M55
Artigo 6.o-A
Os Estados-Membros devem designar os organismos oficiais e laboratórios nacionais de referência responsáveis pela coordenação das normas e métodos de diagnóstico referidos nos anexos A e D. Devem manter listas actualizadas destas instituições e disponibilizá-las aos demais Estados-Membros e ao público.
As tarefas e responsabilidades desses organismos oficiais e laboratórios nacionais de referência encontram-se estabelecidas nos anexos B e C e no capítulo II do anexo D.
Podem ser aprovadas nos termos do n.o 2 do artigo 17.o regras de execução para uma aplicação uniformizada do presente artigo.
▼M42
Artigo 7.o
Os animais para abate que à chegada ao país de destino tenham sido conduzidos:
— para um matadouro, deverão ser abatidos o mais rapidamente possível e o mais tardar 72 horas após a chegada, de acordo com os requisitos em matéria de sanidade animal,
— ou para um centro de agrupamento autorizado, devem ser conduzidos após o mercado para um matadouro para aí serem abatidos o mais rapidamente possível e o mais tardar nos três dias úteis após a chegada ao centro de agrupamento, de acordo com os requisitos em matéria de sanidade animal. Em momento algum, entre a sua chegada ao centro de agrupamento e a sua chegada ao matadouro, podem entrar em contacto com animais artiodáctilos que não os que preenchem as condições requeridas pela presente directiva.
Artigo 8.o
Os Estados-membros assegurarão que a suspeita de presença de uma das doenças enumeradas no anexo E(I) seja imediata e obrigatoriamente notificada à autoridade competente.
Cada Estado-membro enviará à Comissão, até 31 de Maio de cada ano e pela primeira vez em 1999 um balanço pormenorizado dos casos de doenças referidas no capítulo I do Anexo E(I) ou de qualquer outra doença sujeita a garantias adicionais previstas pela legislação comunitária no seu território ao longo do ano transcorrido, bem como um balanço detalhado sobre os programas de inspecção ou de erradicação em curso. Essas informações basear-se-ão em critérios uniformes a estabelecer de acordo com o procedimento previsto no artigo 17.o A Comissão apresentará essas informações aos Estados-membros no âmbito do CVP e, em especial, pode utilizá-las em relação às decisões referidas nos anexos A e D.
Artigo 9.o
1. Um Estado-membro que tenha um programa nacional obrigatório de luta contra uma das doenças contagiosas enumeradas no capítulo II do anexo E(II), aplicável na totalidade ou em parte do seu território, deve apresentar o referido programa à Comissão, indicando, nomeadamente:
— a distribuição da doença no seu território,
— a justificação do programa, atendendo à importância da doença e as vantagens esperadas do programa em relação aos seus custos,
— a zona geográfica em que o programa vai ser aplicado,
— os diferentes estatutos aplicáveis aos estabelecimentos envolvidos e as normas que devem ser respeitadas em cada categoria, bem como os métodos a utilizar para a realização das provas,
— os processos de vigilância do programa, cujos resultados devem ser enviados, pelo menos anualmente, à Comissão,
— as conclusões a tirar se, por qualquer motivo, um estabelecimento perder o seu estatuto,
— as medidas a adoptar se forem positivos os resultados das provas realizadas em conformidade com as disposições do programa.
2. A Comissão examinará os programas apresentados pelos Estados-membros. Os programas referidos no n.o 1 podem ser aprovados em conformidade com os critérios definidos no n.o 1, de acordo com o procedimento previsto no artigo 17.o De acordo com o mesmo procedimento serão definidas, simultaneamente ou o mais tardar três meses após a aprovação dos programas, as garantias suplementares, gerais ou limitadas, que podem ser exigidas no comércio intracomunitário. Essas garantias não podem ser superiores às que os Estados-membros exigem no âmbito nacional.
3. Os programas apresentados pelos Estado-membros podem ser alterados ou completados de acordo com o procedimento previsto no artigo 17.o De acordo com o mesmo procedimento, podem ser aprovadas alterações ou complementos a programas previamente aprovados, ou às garantias definidas de acordo com o n.o 2.
Artigo 10.o
1. Um Estado-membro que considere que o seu território, ou parte dele, está indemne de uma das doenças enumeradas no capítulo II do anexo E(II), apresentará à Comissão documentos comprovativos adequados, indicando, nomeadamente:
— a natureza da doença e o historial da sua ocorrência no território,
— os resultados das provas de vigilância, baseados numa pesquisa serológica, microbiológica, patológica ou epidemiológica e no facto de a doença ser de notificação obrigatória às autoridades competentes,
— o período durante o qual foi feita a vigilância,
— se aplicável, o período durante o qual foi proibida a vacinação contra a doença e a zona geográfica abrangida por essa proibição,
— as normas que permitem o controlo da ausência da doença.
2. A Comissão examinará a documentação apresentada pelos Estados-membros. As garantias suplementares, gerais ou limitadas, que podem ser exigidas no comércio intracomunitário, podem ser definidas de acordo com o procedimento previsto no artigo 17.o Essas garantias não devem ser superiores às que os Estados-membros exigem no âmbito nacional.
3. O Estado-membro em causa notificará a Comissão de qualquer alteração dos pormenores referidos no n.o 1 respeitantes à doença, e em especial de quaisquer novos surtos da doença. À luz dessas informações, as garantias definidas em conformidade com o n.o 2 podem ser alteradas ou suprimidas de acordo com o procedimento previsto no artigo 17.o
Artigo 11.o
1. Os Estados-membros velarão por que, os centros de agrupamento satisfaçam pelo menos as seguintes condições para serem autorizados pela autoridade competente:
a) Estarem sob a supervisão de um veterinário oficial que garanta, em especial, o cumprimento do disposto nos n.os 1 e 2 do artigo 4.o;
b) Estarem localizados numa zona não sujeita a proibição ou restrição nos termos da legislação comunitária aplicável ou da legislação nacional;
c) Serem limpos e desinfectados antes de cada utilização, de acordo com as instruções do veterinário oficial;
d) Estarem dotados, em função da capacidade de acolhimento:
— de instalações reservadas exclusivamente para esse fim, quando utilizados como centros de agrupamento,
— de instalações apropriadas que permitam carregar, descarregar e acomodar convenientemente os animais, abeberá-los, alimentá-los e administrar-lhes todos os tratamentos necessários; essas instalações devem ser fáceis de limpar e desinfectar,
— de infra-estruturas de inspecção adequadas,
— de infra-estruturas de isolamento adequadas,
— de equipamentos apropriados para a limpeza e desinfecção das instalações e camiões,
— de uma área de armazenagem adequada para a forragem, camas e estrume,
— de um sistema adequado de recolha das águas usadas,
— de um gabinete ou instalações para o veterinário oficial;
e) Só admitirem animais identificados e provenientes de efectivos oficialmente indemnes de tuberculose, brucelose e leucose, ou animais de abate que satisfaçam as condições previstas na presente directiva e em especial as do n.o 3 do artigo 6.o Para o efeito, quando os animais são admitidos, o proprietário ou o responsável do centro procederá ou mandará proceder à verificação das marcas de identificação dos animais e dos documentos sanitários ou outros documentos de acompanhamento específicos da espécie ou categoria em questão;
▼M51
ee) Cumprirem as disposições da Directiva 98/58/CE e do Regulamento (CE) n.o 1/2005 (
13
) que lhes são aplicáveis;
▼M42
f) Serem periodicamente inspeccionados a fim de se verificar se continuam a ser preenchidas as condições que permitiram a sua aprovação.
2. O proprietário ou o responsável do centro de agrupamento é obrigado, com base no documento de acompanhamento, ou com base nos números ou marcas de identificação dos animais, a inscrever num registo ou suporte informático e a conservar durante pelo menos três anos as seguintes informações:
— o nome do proprietário, a origem, a data de entrada, a data de saída, o número e a identificação dos animais das espécies bovina ou o número de registo da exploração de origem ou do efectivo de origem dos suínos chegados ao centro e o seu destino previsto,
— o número de registo do transportador e a matrícula do camião que descarrega ou carrega os animais no centro.
▼M55
3. A autoridade competente emite um número de aprovação para cada centro de agrupamento aprovado. As autorizações dos centros de agrupamento podem ser limitadas a uma determinada espécie, a animais destinados à reprodução e produção, ou a animais destinados ao abate.
A autoridade competente elabora e mantém actualizada uma lista de centros de agrupamento aprovados e respectivos números de autorização e disponibiliza-a aos demais Estados-Membros e ao público.
▼M51
4. A autoridade competente pode suspender ou retirar a autorização em caso de incumprimento do presente artigo ou de outras disposições da presente directiva ou do Regulamento (CE) n.o 1/2005 ou de outra legislação comunitária no domínio veterinário enumerada no capítulo 1 do anexo A da Directiva 90/425/CEE (
14
). A autorização pode ser restituída depois de a autoridade competente se certificar de que o centro de agrupamento satisfaz integralmente todas as disposições pertinentes referidas no presente número.
▼M42
5. A autoridade competente deve garantir que os centros de agrupamento, quando em funcionamento, dispõem de um número suficiente de veterinários oficiais para executar todas as suas atribuições.
6. As eventuais regras de aplicação necessárias à aplicação uniforme do presente artigo serão fixadas de acordo com o procedimento previsto no artigo 17.o
▼M51
Artigo 12.o
1. Os Estados-Membros devem assegurar que os transportadores observem as seguintes condições adicionais:
a) Devem utilizar, para o transporte dos animais, meios de transporte que sejam:
i) construídos de modo a que as fezes, a cama ou a forragem dos animais não possam verter ou cair para fora do veículo; e
ii) limpos e desinfectados com desinfectantes autorizados pela autoridade competente, imediatamente depois de cada transporte de animais ou de qualquer outro produto que possa afectar a saúde animal, e se necessário antes de novo carregamento de animais;
b) Devem:
i) dispor de instalações adequadas de limpeza e desinfecção aprovadas pela autoridade competente, incluindo instalações de armazenagem de material de cama e de estrume; ou
ii) comprovar que essas operações são efectuadas por terceiros aprovados pela autoridade competente.
2. O transportador deve, em relação a cada veículo destinado ao transporte de animais, assegurar a manutenção de um registo contendo, pelo menos, as seguintes informações, que devem ser conservadas por um período mínimo de três anos:
a) Local, data e hora do carregamento, nome ou razão social e endereço da exploração ou do centro de agrupamento onde os animais foram carregados;
b) Local, data e hora de entrega, nome ou razão social e endereço do ou dos destinatários;
c) Espécie e número de animais transportados;
d) Data e local de desinfecção;
e) Indicação pormenorizada da documentação de acompanhamento, incluindo o número;
f) Duração prevista de cada viagem.
3. Os transportadores devem assegurar que os animais transportados não entrem em contacto com animais de estatuto inferior em momento algum da viagem, desde a saída da exploração ou do centro de agrupamento de origem até à chegada ao respectivo destino.
4. Os Estados-Membros devem assegurar que os transportadores cumpram o disposto no presente artigo no que se refere à documentação adequada que deve acompanhar os animais.
5. O presente artigo não é aplicável às pessoas que transportem animais até uma distância máxima de 65 km, a contar do local de partida até ao local de destino.
6. Em caso de incumprimento do disposto no presente artigo, são aplicáveis, mutatis mutandi, as disposições relativas às infracções e à notificação de infracções previstas no artigo 26.o do Regulamento (CE) n.o 1/2005 no respeitante à saúde animal.
▼M42
Artigo 13.o
1. Os Estados-membros assegurarão que todos os comerciantes estejam registados, aprovados e possuam um número de autorização atribuído pela autoridade competente, e que satisfaçam pelo menos as seguintes condições:
a) Negociarem apenas em animais identificados e provenientes de efectivos oficialmente indemnes de tuberculose, brucelose e leucose, ou animais de abate que satisfaçam as condições fixadas na presente directiva e em especial as previstas no n.o 3 do artigo 6.o Para o efeito, os comerciantes devem assegurar que os animais estejam devidamente identificados e acompanhados dos documentos sanitários específicos das espécies em causa.
No entanto, a autoridade competente pode autorizar a comercialização de animais identificados que não satisfaçam as condições previstas no primeiro parágrafo, desde que esses animais sejam conduzidos imediatamente a um matadouro no Estado-membro de origem sem transitar pela respectivas instalações, para serem abatidos nesse matadouro o mais rapidamente possível a fim de evitar a propagação de doenças. Deverão ser tomadas as disposições necessárias para que, ao chegarem ao matadouro, esses animais não possam entrar em contacto com outros animais e para que sejam abatidos separadamente dos restantes animais;
b) O comerciante é obrigado, com base no documento de acompanhamento dos animais, ou com base nos números ou marcas de identificação dos animais, a inscrever num registo ou suporte informático e a conservar durante pelo menos três anos as seguintes informações:
— o nome do proprietário, a origem, a data de compra, as categorias, o número e a identificação dos animais da espécie bovina ou o número de registo da exploração de origem ou do efectivo de origem dos suínos comprados,
— o número de registo do transportador e/ou o número de licença do camião que entrega e transporta os animais,
— o nome e o endereço do comprador e o destino dos animais,
— cópias dos itinerários seguidos e/ou o número de série dos certificados sanitários;
c) Caso o comerciante detenha animais nas suas instalações, deverá assegurar que:
— seja dada formação específica ao pessoal responsável pelos animais no que se refere à aplicação dos requisitos da presente directiva e ao tratamento e bem-estar dos animais,
— o veterinário oficial realize inspecções e eventualmente análises periódicas aos animais e que sejam tomadas todas as medidas necessárias para evitar a propagação de doenças.
2. Os Estados-membros assegurarão que cada instalação utilizada pelos comerciantes no exercício da sua actividade esteja registada e possua um número de autorização fornecido pela autoridade competente, e que satisfaça pelo menos as seguintes condições:
a) Estar sob a supervisão de um veterinário oficial;
b) Estar situada numa zona não sujeita a proibição ou restrição em conformidade com a legislação comunitária pertinente ou com a legislação nacional;
c) Ser dotada:
— de instalações adequadas com capacidade suficiente e em particular infra-estruturas de inspecção adequadas e infra-estruturas de isolamento de modo a poder isolar todos os animais caso ocorra uma doença contagiosa,
— de instalações apropriadas para descarregar os animais e, se necessário, os acomodar convenientemente, abeberá-los, alimentá-los e prestar-lhes todos os tratamentos que requeiram; essas instalações devem ser fáceis de limpar e desinfectar,
— de uma área de recolha adequada para camas e estrume,
— de um sistema adequado de recolha das águas usadas.
d) Ter sido previamente limpa e desinfectada antes de cada utilização de acordo com as instruções do veterinário oficial.
3. A autoridade competente pode suspender ou revogar a autorização em caso de incumprimento do presente artigo ou de outras disposições da presente directiva ou de qualquer outra directiva pertinente em matéria de sanidade animal. A autorização pode ser retribuída depois de a autoridade competente se certificar de que o negociante cumpre as disposições pertinentes da presente directiva.
4. A autoridade competente efectuará inspecções periódicas para verificar o cumprimento dos requisitos pertinentes do presente artigo.
▼M55
5. Os Estados-Membros elaboram e mantêm actualizada uma lista dos negociantes aprovados e das instalações registadas utilizadas pelos negociantes no contexto do seu negócio e respectivos números de autorização, disponibilizando essa lista aos demais Estados-Membros e ao público.
6. Podem ser aprovadas nos termos do n.o 2 do artigo 17.o regras de execução para uma aplicação uniformizada do n.o 5.
▼M42
Artigo 14.o
1. A autoridade competente de um Estado-membro pode instalar um sistema de redes de vigilância.
O sistema de redes de vigilância deve ser constituído, pelo menos:
— pelo proprietário da exploração ou qualquer pessoa singular ou colectiva responsável pela mesma,
— pelo veterinário autorizado ou pelo veterinário oficial responsável pela exploração,
— pelo veterinário autorizado responsável pela exploração,
— pelo serviço veterinário oficial do Estado-membro,
— pelos laboratórios oficiais de diagnóstico veterinário ou qualquer outro laboratório autorizado pela autoridade competente,
— por uma base de dados informatizada.
Os veterinários oficiais dos matadouros e centros de agrupamento aprovados serão associados ao sistema de redes.
2. Esse sistema de redes de vigilância tem como objectivos principais a classificação oficial das explorações, a manutenção dessa classificação através de inspecções periódicas, a recolha de dados epidemiológicos e a vigilância das doenças por forma a garantir o respeito de todas as normas da presente directiva ou de qualquer outra directiva pertinente em matéria de sanidade animal.
Esse sistema de redes de vigilância é obrigatório em todas as exploração do território do Estado-membro que o criou. No entanto, a autoridade competente pode autorizar a instalação desse sistema numa parte do território constituída por uma ou várias regiões adjacentes, tal como definidas no n.o 2, alínea p), do artigo 2.o No caso de ser concedida essa derrogação, o transporte de animais para essa parte do território em proveniência de outras regiões que não façam parte do sistema de redes será sujeito ao disposto na presente directiva.
A autoridade competente estabelecerá os direitos e obrigações a respeitar pelos veterinários autorizados, pelos responsáveis pelas explorações ou pelos seus proprietários, e ainda por quaisquer outros participantes no sistema, incluindo a pessoa responsável pela concessão do certificado sanitário.
A autoridade competente velará por que as obrigações referidas no n.o 2 sejam pelo menos as seguintes:
A. O proprietário de uma exploração ou a pessoa por ela responsável deve:
i) Garantir por contrato ou acto jurídico os serviços de um veterinário autorizado pela autoridade competente;
ii) Recorrer imediatamente ao veterinário autorizado responsável pela exploração logo que suspeite da existência de uma doença contagiosa ou de qualquer doença de notificação obrigatória;
iii) Informar o veterinário autorizado sobre a introdução de quaisquer animais na sua exploração;
iv) Isolar os animais antes de os introduzir na exploração a fim de permitir ao veterinário autorizado verificar, mediante as provas adequadas, se o estatuto sanitário da mesma pode ser mantido.
B. O veterinário autorizado nos termos do n.o 2, alínea m), do artigo 2.o será sujeito ao controlo da autoridade competente e deve preencher os seguintes requisitos:
i) Satisfazer as condições necessárias ao exercício da profissão de veterinário;
ii) Não ter quaisquer laços familiares ou financeiros com o proprietário ou responsável da exploração;
iii) Possuir conhecimentos específicos no domínio da sanidade animal no que se refere aos animais da espécie em causa, o que significa que deve:
— actualizar regularmente os seus conhecimentos, especialmente sobre a regulamentação sanitária aplicável,
— satisfazer as exigências estabelecidas pela autoridade competente para assegurar o correcto funcionamento da rede,
— prestar informações e assistência ao proprietário ou ao responsável da exploração, por forma a que sejam tomadas todas as medidas para assegurar a manutenção da autorização desta última, inclusivamente com base em programas acordados com a autoridade competente,
— assegurar o cumprimento dos requisitos em matéria de:
—
i) identificação e certificação sanitária dos animas do efectivo, dos animais introduzidos na exploração e dos animais transaccionados,
ii) participação obrigatória das doenças infecciosas e de quaisquer outros factores de risco para a saúde e bem-estar dos animais e para a saúde humana,
iii) estabelecimento, na medida do possível, das causas de morte dos animais e do local para onde devem ser enviados,
iv) condições de higiene do efectivo e das unidades de produção pecuária.
— Se o correcto funcionamento do sistema o exigir, cada Estado-membro poderá limitar as responsabilidades do veterinário a um número limitado de explorações ou a uma determinada zona geográfica.
— A autoridade competente elaborará listas de veterinários autorizados e das explorações autorizadas que participam na rede. Se a autoridade competente verificar que um dos participantes na rede deixou de satisfazer as condições acima prescritas, suspenderá ou revogará a autorização, sem prejuízo de quaisquer sanções eventualmente aplicáveis.
C. A base de dados informatizada deve conter pelo menos as seguintes informações:
▼M59
1. Para cada animal:
— código ou códigos de identificação único(s), para os casos previstos no artigo 4.o, n.o 1, no artigo 4.o-B, no artigo 4.o-C, n.o 1, e no artigo 4.o-D do Regulamento (CE) n.o 1760/2000 do Parlamento Europeu e do Conselho (
15
),
— código de identificação da mãe ou, no caso de um animal importado de um país terceiro, o código de identificação único do meio de identificação individual atribuído ao animal pelo Estado-Membro de destino, nos termos do Regulamento (CE) n.o 1760/2000,
— número de identificação da exploração em que nasceu,
— números de identificação de todas as explorações em que permaneceu e datas de cada mudança de exploração,
— data da morte ou do abate,
— o tipo de identificador eletrónico, se aplicado ao animal.
▼M42
2. Para cada exploração:
— um número de identificação que consiste, além do código do país, num código que não exceda 12 caracteres,
— nome e endereço do proprietário.
3. A base de dados deverá permitir que se disponha, em qualquer momento, das seguintes informações:
— número de identificação de todos os bovinos presentes numa exploração e, no caso de grupo de suínos, o número de registo da exploração de origem ou do efectivo de origem bem como, quando for o caso, o número de certificado sanitário,
— lista de todos os transportes de cada bovino a partir da exploração em que nasceu ou, para os animais importados de países terceiros, da exploração de importação e, no caso de grupos de suínos, o número de registo da última exploração ou do último efectivo de origem e quando se tratar de animais importados de países terceiros, a exploração de importação.
Estas informações serão conservadas na base de dados até que tenham decorrido três anos consecutivos após a morte dos bovinos, ou até que tenham decorrido três anos consecutivos após o registo, no caso dos suínos.
Todavia, apenas as disposições dos pontos 2, 3 e 4 são aplicáveis aos animais da espécie suína.
▼M45
4. A fim de garantir o carácter operacional das bases de dados informatizadas nacionais relativas aos animais da espécie suína, as regras de execução necessárias, incluindo as informações que as bases de dados nacionais devem conter, serão adoptadas nos termos do artigo 17.o
▼M42
4. Todos os outros participantes da rede não referidos no n.o 3, partes A e B, operam sob a responsabilidade da autoridade competente. A autoridade competente de cada Estado-membro é responsável pela instalação da rede, e com vista ao seu bom funcionamento, deve proceder a inspecções periódicas da rede.
5. Os Estados-membros que instalem um sistema de rede de vigilância do tipo mencionado nos n.os 1 a 4, operacional durante um período de pelo menos 12 meses, deverão solicitar à Comissão a sua aprovação de acordo com o procedimento previsto no artigo 17.o
Para o efeito, a Comissão analisará a documentação apresentada pelos Estados-membros.
Os peritos da Comissão validarão os sistemas de redes através de um processo de auditoria.
No caso de o resultado desta auditoria ser favorável, a Comissão, no prazo de 90 dias a contar da recepção do pedido de aprovação, remeterá um relatório ao CVP, acompanhado das propostas adequadas.
No caso de constatação de infracções repetidas, a autorização do sistema de rede de vigilância pode ser suspendida de acordo com o procedimento previsto no artigo 17.o, a pedido da Comissão ou de um ou vários Estados-membros.
6. Os Estados-membros que tiverem instalado em todo o seu território um sistema de rede de vigilância reconhecido nos termos do presente artigo ficam autorizados a não aplicar o n.o 2, alínea a), segundo travessão do artigo 3.o aos transportes de animais visados pela presente directiva no interior do respectivo território.
7. Até 31 de Dezembro de 1999 o mais tardar, o Conselho, deliberando por maioria qualificada com base num relatório da Comissão acompanhado de propostas, procederá a uma revisão das disposições do presente artigo à luz da experiência adquirida, com o objectivo de as alterar, actualizar e, eventualmente, tornar extensivas a todos os Estados-membros.
8. O financiamento do sistema de redes de vigilância será abordado no âmbito da revisão do anexo B da Directiva 85/73/CEE (
16
), nos termos do artigo 8.o da Directiva 96/43/CE.
Artigo 15.o
1. Os Estados-membros tomarão as medidas específicas adequadas para sancionar qualquer infracção à presente directiva, por parte de uma pessoa singular ou de uma pessoa colectiva.
2. Caso se verifique que as disposições da presente directiva não foram ou não estão a ser respeitadas, a autoridade competente do local onde for verificado esse facto tomará todas as medidas adequadas para salvaguardar a saúde dos animais e para prevenir a difusão de doenças.
Consoante o caso, essas medidas da autoridade competente poderão ser as disposições necessárias para:
a) Terminar a viagem ou reenviar os animais ao seu local de partida através do itinerário mais directo, desde que essa medida não ponha em perigo a saúde ou o bem-estar dos animais;
b) Acomodar convenientemente os animais e dispensar-lhes os cuidados necessários, em caso de interrupção da viagem;
c) Determinar o abate dos animais. O destino e utilização das carcaças desses animais serão definidos:
— segundo as disposições previstas na Directiva 64/433/CEE (
17
) ou
— segundo as disposições previstas na Directiva 90/667/CEE se o estatuto sanitário dos animais não puder ser determinado ou se estes forem susceptíveis de representar um risco em matéria de saúde animal ou de saúde pública. Todavia, se for conveniente aplicar as disposições previstas na Directiva 90/667/CEE, deve ser concedido ao proprietário ou ao seu representante um prazo de regularização antes de recorrer a esta possibilidade. Neste caso, é aplicável o disposto no n.o 3 do presente artigo.
3. A autoridade competente do Estado-membro de destino avisará imediatamente a autoridade competente do Estado-membro de origem após ter constatado qualquer infracção à presente directiva.
Nos termos do disposto na Directiva 89/608/CEE, os Estados-membros prestar-se-ão mutuamente assistência na aplicação da presente directiva e mais particularmente com vista a assegurar o respeito das disposições previstas no presente artigo.
4. O presente artigo não afecta as regras nacionais aplicáveis em matéria de sanções penais.
▼M55
Artigo 16.o
O anexo A e o capítulo I do anexo D são alterados pelo Conselho, deliberando por maioria qualificada sob proposta da Comissão, com vista, nomeadamente, à sua adaptação ao progresso tecnológico e científico.
Os anexos B e C, o capítulo II do anexo D e os anexos E e F são alterados pela Comissão nos termos do artigo 17.o.
▼M46
Artigo 17.o
1. A Comissão é assistida pelo Comité Veterinário Permanente instituído pela Decisão 68/361/CEE, a seguir designado por «comité».
2. Sempre que se faça referência ao presente número, são aplicáveis os artigos 5.o e 7.o da Decisão 1999/468/CE.
O prazo previsto no n.o 6 do artigo 5.o da Decisão 1999/468/CE é de três meses.
3. O comité aprovará o seu regulamento interno.
▼M46
Artigo 17.oA
1. A Comissão é assistida pelo Comité Veterinário Permanente, instituído pela Decisão 68/361/CEE, a seguir designado por «comité».
2. Sempre que se faça referência ao presente número, são aplicáveis os artigos 5.o e 7.o da Decisão 1999/468/CE, tendo-se em conta o disposto no seu artigo 8.o
O prazo previsto no n.o 6 do artigo 5.o é de três meses.
3. O comité aprovará o seu regulamento interno.
▼M45
Artigo 18.o
Os Estados-Membros que não tenham criado um sistema de redes de vigilância autorizado assegurarão que esteja plenamente operacional uma base de dados informatizada que cumpra o disposto no artigo 14.o da seguinte forma:
a) No que se refere aos animais da espécie bovina, a partir de 31 de Dezembro de 1999;
b) No que se refere ao registo de explorações de animais da espécie suína que cumpram o disposto no ponto 2 da parte C do artigo 14.o, a partir de 31 de Dezembro de 2000;
c) No que respeita às deslocações de animais de espécie suína que cumpram o disposto no ponto 2 da parte C do artigo 14.o:
— desde as suas explorações de nascimento, o mais tardar em 31 de Dezembro de 2001,
— desde as outras explorações, o mais tardar em 31 de Dezembro de 2002.
Cada deslocação de animais da espécie suína dará lugar a um registo na base de dados. O registo incluirá, no mínimo, o número de suínos deslocados, o número de identificação da exploração ou da vara de origem, o número de identificação da exploração ou da vara de chegada, a data de partida e a data de chegada.
▼M42
Artigo 19.o
As normas da Directiva 90/425/CEE serão aplicáveis, em especial, aos controlos na origem, à organização e ao seguimento dos controlos a efectuar pelo país de destino e às medidas de salvaguarda a aplicar.
Artigo 20.o
Os Estados-membros são os destinatários da presente directiva.
▼M44
ANEXO A
I. Efectivo bovino oficialmente indemne de tuberculose
Para efeitos da presente secção, entende-se por «bovinos» todos os bovinos com excepção dos animais que participem em manifestações culturais ou desportivas.
1. Um efectivo bovino é oficialmente indemne de tuberculose se:
a) Todos os animais estiverem isentos de sinais clínicos de tuberculose;
b) Todos os bovinos com mais de seis semanas de idade tiverem reagido negativamente a pelo menos duas provas oficiais intradérmicas de tuberculina realizadas em conformidade com o anexo B, a primeira seis meses após a eliminação de qualquer infecção do efectivo e a segunda seis meses mais tarde; ou no caso de o efectivo ter sido constituído unicamente com animais provenientes de efectivos oficialmente indemnes de tuberculose, sendo a primeira prova realizada a partir do 60.o dia após a constituição do efectivo bovino e não sendo a segunda obrigatória;
c) Após a realização da primeira prova referida na alínea b), não tiver sido introduzido no efectivo qualquer bovino com mais de seis semanas, a não ser que tenha reagido negativamente a uma prova intradérmica de tuberculina realizada e avaliada em conformidade com o anexo B e efectuada nos 30 dias anteriores ou nos 30 dias posteriores à data da sua introdução no efectivo; neste último caso, o ou os animais em causa deverão permanecer isolados fisicamente dos outros animais do efectivo de uma forma que evite qualquer contacto directo ou indirecto com os outros animais até prova de reacção negativa.
Porém, a autoridade competente poderá não exigir que esta prova se realize em animais que se movimentem no seu território, se o animal for proveniente de um efectivo oficialmente indemne de tuberculose, excepto nos Estados-membros em que, em 1 de Janeiro de 1998 e até obtenção do estatuto de região oficialmente indemne de tuberculose, a autoridade competente exija que sejam realizadas essas provas nos animais que se movimentem entre efectivos participantes num sistema de redes, tal como definido no artigo 14.o
2. Um efectivo bovino conservará o estatuto de oficialmente indemne de tuberculose se:
a) Continuarem a ser satisfeitas as condições das alíneas a) e c) do ponto 1;
b) Todos os animais que entrarem na exporação forem provenientes de efectivos com estatuto de oficialmente indemnes de tuberculose;
c) Todos os animais da exploração, excluindo os vitelos com menos de seis semanas que tiverem nascido na exploração, forem sujeitos a uma prova de tuberculina de rotina, realizada anualmente, em conformidade com o anexo B.
No entanto, a autoridade competente de um Estado-membro pode, relativamente ao Estado-membro ou parte do Estado-membro onde todos os efectivos bovinos sejam sujeitos a um programa oficial de luta contra a tuberculose, alterar a frequência das provas de rotina do seguinte modo:
— se a média — determinada em 31 de Dezembro de cada ano — das percentagens anuais de efectivos bovinos confirmados como infectados com tuberculose não for superior a 1 % de todos os efectivos dentro da área definida durante os dois períodos de vigilância anuais mais recentes, o intervalo entre as provas de rotina do efectivo pode ser aumentado para dois anos e os machos destinados a engorda numa unidade epidemiológica isolada podem ser dispensados das provas de tuberculina, desde que sejam provenientes de efectivos oficialmente indemnes de tuberculose e que a autoridade competente garanta que os machos destinados a engorda não serão utilizados para reprodução e seguirão directamente para o abate;
— se a média — determinada em 31 de Dezembro de cada ano — das percentagens anuais de efectivos bovinos confirmados como infectados com tuberculose não for superior a 0,2 % de todos os efectivos dentro da área definido durante os dois períodos de vigilância bienais mais recentes, o intervalo entre as provas de rotina pode ser aumentado para três anos e/ou a idade com que os animais têm de ser sujeitos a essas provas pode ser aumentada para 24 meses;
— se a média — determinada em 31 de Dezembro de cada ano — das percentagens anuais de efectivos bovinos confirmados como infectados com tuberculose não for superior a 0,1 % de todos os efectivos dentro da área definida durante os dois períodos de vigilância trienais mais recentes, o intervalo entre as provas de rotina pode ser aumentado para quatro anos ou a autoridade competente pode dispensar os efectivos da prova de tuberculina, desde que as seguintes condições sejam satisfeitas:
—
1. Antes da sua introdução num efectivo, todos os bovinos sejam sujeitos, com resultados negativos, a uma prova intradérmica de tuberculina;
ou
2. Todos os bovinos abatidos sejam sujeitos a uma pesquisa de lesões de tuberculose, sendo estas sujeitas a um exame histopatológico e bacteriológico para pôr em evidência o bacilo da tuberculose.
A autoridade competente pode igualmente, relativamente ao Estado-membro ou parte deste, aumentar a frequência das provas de tuberculina de rotina, se o nível de incidência da doença tiver aumentado.
3A. O estatuto de oficialmente indemne de tuberculose de um efectivo será suspenso se:
a) As condições referidas no ponto 2 deixarem de ser respeitadas;
ou
b) Se considerar que um ou mais animais tiveram uma reacção positiva à prova de tuberculina ou se houver suspeita de um caso de tuberculose numa inspecção post mortem.
Se um animal for considerado como tendo reacção positiva à prova de tuberculina, será retirado do efectivo e abatido. Serão realizadas análises laboratoriais e epidemiológicas e inspecções post mortem adequadas ao animal com reacção positiva ou à carcaça do animal suspeito. O estatuto permanecerá suspenso até que sejam completadas todas as análises laboratoriais. Se não se confirmar a presença de tuberculose, poderá ser levantada a suspensão do estatuto de oficialmente indemne de tuberculose do efectivo de origem se uma prova efectuada a todos os animais com mais de seis semanas de idade der resultado negativo pelo menos 42 dias depois da eliminação do ou dos animais com reacção positiva;
ou
c) O efectivo contiver animais de estatuto indeterminado nos termos do anexo B. Neste caso, o estatuto do efectivo permanecerá suspenso até que o estatuto dos animais tenha sido esclarecido. Os animais nessas condições serão obrigatoriamente isolados dos restantes animais do efectivo até esclarecimento do seu estatuto, quer através de uma nova prova passados 42 dias quer através de uma inspecção post mortem e de análises laboratoriais;
d) Contudo, em derrogação dos requisitos da alínea c), nos Estados-membros em que a autoridade competente realize provas regulares aos efectivos utilizando a prova de tuberculina de comparação descrita no anexo B, e no caso de efectivos em que não tenham sido descobertos quaisquer animais com reacção positiva confirmada nos três anos anteriores, pelo menos, a autoridade competente poderá decidir não limitar as movimentações dos outros animais do efectivo, desde que o estatuto dos animais com reacção duvidosa seja esclarecido através de uma nova prova realizada passados 42 dias e que nenhum animal do efectivo tenha acesso ao circuito comercial intracomunitário até ter sido clarificado o estatuto dos animais com reacção duvidosa. Se, nesta nova prova, um animal apresentar reacção positiva ou continuar a apresentar uma reacção duvidosa, serão aplicáveis as condições previstas na alínea b). Se posteriormente for confirmada a presença da doença, todos os animais que tenham abandonado a exploração desde a última prova com resultado totalmente negativo deverão ser localizados e testados.
3B. O estatuto de oficialmente indemne de tuberculose do efectivo será retirado se a presença de tuberculose for confirmada através do isolamento da bactéria M bovis na análise laboratorial.
A autoridade competente poderá retirar o estatuto:
a) Se as condições descritas no ponto 2 deixarem de ser satisfeitas; ou
b) Se se constatarem lesões de tuberculose nos exames post-mortem;
c) Se um inquérito epidemiológico determinar a possibilidade de infecção; ou
d) Por quaisquer outros motivos considerados pertinentes para efeitos de luta contra a tuberculose bovina.
A autoridade competente procederá à localização e ao controlo de todos os efectivos considerados epidemiologicamente ligados. O estatuto de oficialmente indemne de tuberculose de um efectivo permanecerá retirado até que as instalações e os utensílios tenham sido completamente limpos e desinfectados e até que todos os animais com mais de seis semanas de idade tenham reagido negativamente a pelos menos duas provas de tuberculina consecutivas, a primeira no mínimo 60 dias e a segunda no mínimo 4 meses e no máximo 12 meses após a retirada do último animal com reacção positiva.
4. Com base nas informações fornecidas nos termos do artigo 8.o, um Estado-membro ou uma parte de um Estado-membro pode ser declarado oficialmente indemne de tuberculose nos termos do artigo 17.o, se satisfizer as seguintes condições:
a) A percentagem de efectivos bovinos confirmados como infectados com tuberculose não exceder 0,1 % por ano do total de efectivos durante seis anos consecutivos e pelo menos 99,99 % dos efectivos terem obtido o estatuto de oficialmente indemnes de tuberculose todos os anos durante um período de seis anos, devendo o cálculo desta última percentagem efectuar-se em 31 de Dezembro de cada ano civil;
▼M46
b) Cada bovino for identificado nos termos da legislação comunitária, e;
▼M44
c) Todos os bovinos abatidos serem sujeitos a uma inspecção oficial post mortem;
d) Terem sido cumpridos os procedimentos de suspensão e retirada do estatuto de oficialmente indemne de tuberculose.
5. Um Estado-membro ou uma parte de um Estado-membro conservará o estatuto de oficialmente indemne de tuberculose se continuarem a ser satisfeitas as condições das alíneas a) a d) do ponto 4. Contudo, caso existam indícios de uma mudança significativa da situação no que se refere à tuberculose num Estado-membro, ou numa parte de um Estado-membro, que tenha sido considerado oficialmente indemne de tuberculose, a Comissão pode, nos termos do artigo 17.o, tomar uma decisão de suspensão ou de revogação do estatuto até que tenham sido satisfeitos os requisitos da decisão.
II. Efectivo bovino indemne de brucelose e oficialmente indemne de brucelose
Para efeitos da presente secção, entende-se por «bovinos» todos os bovinos com excepção dos machos destinados a engorda, desde que sejam provenientes de um efectivo oficialmente indemne de brucelose e que a autoridade competente assegure que os machos destinados a engorda não serão usados para reprodução e seguirão directamente para o abate.
1. Um efectivo bovino é oficialmente indemne de brucelose se:
a) Não incluir bovinos vacinados contra a brucelose, excluindo as fêmeas vacinadas há pelo menos três anos;
b) Todos os bovinos estiverem isentos de sinais clínicos de brucelose há pelo menos seis meses;
c) Todos os bovinos com mais de 12 meses de idade tiverem sido sujeitos a um dos seguintes programas de provas, com resultados negativos, em conformidade com o anexo C:
i) duas provas serológicas especificadas no ponto 10, efectuadas com intervalos superiores a três meses e inferiores a 12 meses,
ii) três provas a amostras de leite, com intervalos de três meses, seguidas de uma prova serológica especificada no ponto 10 efectuada pelo menos seis semanas depois;
d) Todos os bovinos que tiverem entrado no efectivo forem provenientes de um efectivo com estatuto de oficialmente indemne de brucelose e, no caso dos animais com mais de 12 meses de idade, apresentarem um título brucélico inferior a 30 UI de aglutinação por mililitro aquando da realização de uma prova de seroaglutinação nos termos do anexo C, ou tiverem reagido negativamente a qualquer outra prova aprovada nos termos do artigo 17.o durante os 30 dias anteriores ou os 30 dias posteriores à data da sua introdução no efectivo: neste último caso, o ou os animais em causa deverão permanecer isolados fisicamente dos outros animais do efectivo de uma forma que evite qualquer contacto directo ou indirecto com os outros animais até prova de reacção negativa.
2. Um efectivo bovino conservará o estatuto de oficialmente indemne de brucelose se:
a) For realizado anualmente, com resultados negativos, segundo o anexo C, um dos seguintes programas de provas:
i) três provas do anel do leite realizadas com intervalos de, pelo menos, três meses,
ii) três provas ELISA do leite, realizados com intervalos de, pelo menos, três meses,
iii) três provas do anel do leite realizadas com um intervalo de, pelo menos, três meses, seguidas de uma das provas serológicas referidas no ponto 10, realizada pelo menos seis semanas depois,
iv) duas provas ELISA do leite, realizadas com um intervalo de, pelo menos, três meses, seguidas de uma das provas serológicas referidas no ponto 10, realizada pelo menos seis semanas depois,
v) duas provas serológicas realizadas com um intervalo de, pelo menos, três meses e não superior a 12 meses.
No entanto, a autoridade competente do Estado-membro pode, relativamente ao Estado-membro ou parte do Estado-membro não oficialmente indemne de brucelose mas em que todos os efectivos bovinos estejam sujeitos a um programa oficial de combate à brucelose, alterar a frequência das provas de rotina do seguinte modo:
— se a percentagem de efectivos bovinos infectados não for superior a 1 %, pode ser suficiente realizar, anualmente, duas provas do anel do leite ou duas provas ELISA do leite com um intervalo de pelo menos três meses, ou uma prova serológica,
— se pelo menos 99,8 % dos efectivos bovinos tiverem sido declarados oficialmente indemnes de brucelose durante, pelo menos, quatro anos, o intervalo entre os controlos pode ser alargado para dois anos se forem controlados todos os animais com mais de 12 meses de idade, ou o controlo pode limitar-se aos animais com mais de 24 meses de idade se os efectivos continuarem a ser controlados todos os anos. Os controlos devem ser realizados utilizando uma das provas serológicas referidas no ponto 10;
b) Todos os bovinos que entrarem no efectivo forem provenientes de efectivos com o estatuto de oficialmente indemnes de brucelose e, no caso dos bovinos com mais de doze meses de idade, apresentarem um título brucélico inferior a 30 UI de aglutinação por mililitro, aquando da realização de uma prova de seroaglutinação segundo o anexo C ou tiverem tido uma reacção negativa a qualquer outra prova aprovada nos termos do artigo 17.o durante os 30 dias anteriores ou os 30 dias posteriores à introdução no efectivo; neste último caso, o ou os animais em causa deverão permanecer isolados fisicamente dos outros animais do efectivo de uma forma que evite qualquer contacto directo ou indirecto com os outros animais até prova de reacção negativa.
No entanto, a prova referida na alínea b) poderá não ser exigida nos Estados-membros, ou regiões dos Estados-membros, em que, desde há pelo menos dois anos, a percentagem de efectivos bovinos infectados com brucelose não seja superior a 0,2 % e se os animais forem provenientes de um efectivo oficialmente indemne de brucelose nesse Estado-membro ou região e não tiverem estado em contacto, durante o transporte, com bovinos de estatuto inferior;
c) Em derrogação da alínea b), os bovinos provenientes de um efectivo bovino indemne de brucelose podem ser introduzidos num efectivo oficialmente indemne de brucelose se tiverem, pelo menos, 18 meses de idade e, no caso de terem sido vacinados contra a brucelose, a vacina tiver sido efectuada há mais de um ano.
Esses animais devem ter apresentado, nos 30 dias anteriores à introdução no efectivo, um título brucélico inferior a 30 UI de aglutinação por mililitro e um resultado negativo numa prova de fixação do complemento ou noutra prova aprovada nos termos do artigo 17.o
Se, no entanto, uma fêmea proveniente de um efectivo indemne de brucelose for introduzida num efectivo bovino oficialmente indemne de brucelose, nos termos do disposto no parágrafo acima, esse efectivo será considerado indemne de brucelose durante dois anos a contar da data de introdução do último animal vacinado.
3A. O estatuto de um efectivo oficialmente indemne de brucelose será suspenso ou retirado se:
a) As condições referidas nos pontos 1 e 2 não forem respeitadas; ou
b) Na sequência de provas laboratoriais ou por motivos clínicos se suspeitar de que um ou mais bovinos têm brucelose e os animais suspeitos tiverem sido abatidos ou isolados de uma forma que evite qualquer contacto directo ou indirecto com os outros animais.
Se o animal tiver sido abatido e já não puder ser submetido a provas, a suspensão pode ser levantada caso duas provas de seroaglutinação, realizadas segundo o anexo C, em todos os bovinos do efectivo com mais de 12 meses de idade, apresentem um título inferior a 30 UI de aglutinação por mililitro. A primeira prova deve ser realizada pelo menos 30 dias após a eliminação do animal e a segunda pelo menos 60 dias depois.
Se o animal tiver sido isolado em relação aos outros animais do efectivo, pode proceder-se à sua reintrodução no efectivo e o estatuto deste último pode ser restabelecido, se posteriormente:
a) Numa prova de seroaglutinação, apresentar um título inferior a 30 UI de aglutinação por mililitro e tiver apresentado um resultado negativo numa prova de fixação do complemento, ou
b) Tiver apresentado um resultado negativo em qualquer outro conjunto de provas aprovado para o efeito nos termos do artigo 17.o
3B. O estatuto de efectivo oficialmente indemne de brucelose será retirado se, na sequência de provas laboratoriais ou de investigação epidemiológicas, for confirmada no efectivo uma infecção com Brucella.
O estatuto do efectivo só poderá ser restabelecido quando todos os bovinos presentes no efectivo no momento da primeira manifestação da doença tiverem sido abatidos ou, em alternativa, o efectivo tiver sido sujeito a uma prova de controlo e todos os animais com mais de 12 meses de idade tiverem apresentado resultados negativos em duas provas consecutivas com intervalos de 60 dias, sendo a primeira efectuada pelo menos 30 dias após a retirada do ou dos animais positivos.
No caso das fêmeas que se encontravam prenhes no momento da primeira manifestação da doença, o controlo final será obrigatoriamente realizado a partir de 21.o dia após o parto do último animal prenhe no momento da primeira manifestação da doença.
4. Um efectivo bovino é indemne de brucelose se satisfizer as condições das alíneas b) e c) do ponto 1 e se tiver sido realizada a vacinação, do seguinte modo:
i) As fêmeas tiverem sido vacinadas:
— antes dos seis meses de idade com uma estirpe 19 da vacina viva, ou
— antes dos 15 meses de idade com uma vacina inactivada 45/20 adjuvante que tenha sido oficialmente controlada e aprovada, ou
— com outras vacinas aprovadas de acordo com o procedimento previsto no artigo 17.o;
ii) Os bovinos com menos de 30 meses que tenham sido vacinados com uma estirpe 19 da vacina viva podem apresentar um resultado na prova de seroaglutinação sueprior a 30 UI, mas inferior a 80 UI de aglutinação por mililitro desde que apresentem, na prova de fixação do complemento, um resultado inferior a 30 unidades CEE no caso das fêmeas vacinadas há menos de 12 meses ou inferior a 20 unidades CEE nos restantes casos.
5. Um efectivo bovino conservará o estatuto de indemne de brucelose se:
i) For objecto de um dos programas de provas enumerados na alínea a) do ponto 2;
ii) Os bovinos que entrarem no efectivo respeitarem as condições da alínea b) do ponto 2 ou
— forem provenientes de efectivos com o estatuto de indemnes de brucelose e, no caso dos bovinos com mais de 12 meses de idade, apresentarem, nos 30 dias anteriores à introdução no efectivo, ou em isolamento após essa introdução, menos de 30 UI de aglutinação por mililitro numa prova de seroaglutinação e um resultado negativo numa prova de fixação do complemento, segundo o anexo C, ou
— forem provenientes de efectivos com o estatuto de indemne de brucelose, a sua idade for inferior a 30 meses e tiverem sido vacinados com uma estirpe 19 de vacina viva, se numa prova de seroaglutinação apresentarem um resultado superior a 30 UI mas inferior a 80 UI de aglutinação por militlitro desde que, na prova de fixação do complemento, o resultado for inferior a 30 unidades CEE no caso das fêmeas vacinadas há menos de 12 meses ou inferior a 20 unidades CEE nos restantes casos.
6A. O estatuto de indemne de brucelose de um efectivo será suspenso se:
a) As condições definidas nos pontos 4 e 5 supra não forem respeitadas, ou
b) Na sequência de provas laboratoriais ou por motivos clínicos, se suspeitar da presença de brucelose num ou mais animais com idade superior a 30 meses e o animal ou animais suspeitos tiverem sido abatidos ou isolados de uma forma que evite qualquer contacto directo ou indirecto com os outros animais.
Se o animal tiver sido isolado, pode proceder-se à sua reintrodução no efectivo e o estatuto deste último pode ser restabelecido se, posteriormente, o animal apresentar numa prova de seroaglutinação um título inferior a 30 UI de aglutinação por mililitro e tiver apresentado um resultado negativo numa prova de fixação do complemento ou noutra prova aprovada nos termos do artigo 17.o
Se o animal tiver sido abatido e já não puder ser sumetido a provas, a suspensão pode ser levantada caso duas provas de seroaglutinação, realizadas segundo o anexo C, em todos os bovinos do efectivo com mais de 12 meses de idade, apresentem um título inferior a 30 UI de aglutinação por mililitro. A primeira prova deve ser realizada pelo menos 30 dias após a eliminação do animal e a segunda pelo menos 60 dias depois.
Se os animais a controlar ao abrigo dos dois parágrafos anteriores tiverem menos de 30 meses de idade e tiverem sido vacinados com uma estirpe 19 da vacina viva, pode considerar-se que tiveram reacção negativa se apresentarem um resultado na prova de seroaglutinação superior a 30 UI, mas inferior a 80 UI de aglutinação por mililitro desde que, na prova de fixação do complemento, apresentem um resultado inferior a 30 unidades CEE no caso das fêmeas vacinadas há menos de 12 meses ou inferior a 20 unidades CEE nos restantes casos.
6B. O estatuto de efectivo indemne de brucelose será retirado se, na sequência de provas laboratoriais ou de investigações epidemiológicas, for confirmada no efectivo uma infecção com Brucella.
O estatuto do efectivo só poderá ser restabelecido quando todos os bovinos presentes no efectivo no momento da primeira manifestação da doença tiverem sido abatidos ou, em alternativa, o efectivo tiver sido sujeito a uma prova de controlo e todos os animais não vacinados com mais de 12 meses de idade tiverem apresentado resultados negativos em duas provas consecutivas com intervalos de 60 dias, sendo a primeira efectuada pelo menos 30 dias após a eliminação do ou dos animais positivos.
Se todos os animais a controlar referidos no parágrafo anterior tiverem menos de 30 meses de idade e tiverem sido vacinados com uma estirpe 19 da vacina viva, podem ser considerados como negativos se apresentarem um título brucélico superior a 30 UI mas inferior a 80 UI aglutinantes por mililitro, desde que apresentem, na prova de fixação do complemento, um título inferior a 30 unidades CEE no caso das fêmeas vacinadas há menos de doze meses ou um título inferior a 20 unidades CEE nos restantes casos.
No caso das fêmeas que se encontravam prenhes no momento da primeira manifestação da doença, o controlo final deverá ser realizado pelo menos 21 dias após o parto do último animal prenhe no momento da primeira manifestação da doença.
7. Um Estado-membro ou uma região de um Estado-membro pode ser declarado oficialmente indemne de brucelose nos termos do artigo 17.o se satisfizer as seguintes condições:
a) Não ter sido registado qualquer caso de aborto devido à infecção com Brucella nem de isolamento de B abortus pelo menos nos últimos três anos e no mínimo 99.8 % dos efectivos terem conseguido alcançar o estatuto de oficialmente indemnes de brucelose todos os anos, durante cinco anos consecutivos, devendo o cálculo desta percentagem efectuar-se em 31 de Dezembro de cada ano civil. Contudo, caso a autoridade competente adopte uma política de abate de todo o efectivo, os incidentes isolados evidenciados por inquérito epidemiológico que se devam à introdução de animais de fora do Estado-membro ou de parte do Estado-membro e os efectivos cujo estatuto de oficialmente indemne de brucelose tenha sido suspenso ou retirado por razões que não a suspeita de doença, poderão ser ignorados para efeitos do cálculo acima referido, desde que a autoridade central competente do Estado-membro afectado por estes incidentes elabore um registo anual e o envie à Comissão, nos termos do n.o 2 do artigo 8.o, e
▼M46
b) Cada bovino for identificado nos termos da legislação comunitária, e
▼M44
c) Os casos de aborto serem de notificação obrigatória e objecto de investigação pela autoridade competente.
8. Sem prejuízo do ponto 9, um Estado-membro ou uma região de um Estado-membro declarado oficialmente indemne de brucelose manterá este estatuto se:
a) Continuarem a ser satisfeitas as condições fixadas no ponto 7, alíneas a) e b), e se os casos de aborto suspeitos de serem devidos à brucelose forem de notificação obrigatória e objecto de investigação pela autoridade competente;
b) Todos os anos, durante os cinco primeiros anos após obtenção do estatuto, todos os bovinos com mais de 24 meses de idade em pelo menos 20 % dos efectivos tiverem sido sujeitos e tiverem tido reacção negativa a uma prova serológica efectuada de acordo com o anexo C ou, no caso dos efectivos leiteiros, por análise de amostras de leite de acordo com o anexo C;
c) Forem notificados à autoridade competente todos os casos de bovinos suspeitos de estar infectados com Brucella, sendo esses animais submetidos a uma investigação epidemiológica oficial relativamente à brucelose, que deverá incluir, pelo menos, duas provas serológicas de sangue, incluindo uma prova de fixação do complemento, bem como um exame microbiológico de amostras adequadas;
d) Durante o período de suspeita, que se manterá até à obtenção de resultados negativos nas provas previstas na alínea c), for suspenso o estatuto de oficialmente indemne de brucelose do efectivo de origem ou de trânsito do bovino suspeito e dos efectivos epidemiologicamente associados;
e) Em caso de um foco de brucelose evolutiva, todos os bovinos tiverem sido abatidos. Os restantes animais de espécies sensíveis serão submetidos às provas adequadas, e as instalações e o material serão limpos e desinfectados.
9. Um Estado-membro ou uma região de um Estado-membro declarado oficialmente indemne de brucelose notificará a Comissão de todas as ocorrências de casos de brucelose. Caso existam indícios de uma mudança significativa da situação no que se refere à brucelose num Estado-membro, ou numa parte de um Estado-membro, que tenha sido reconhecido como oficialmente indemne de brucelose, a Comissão pode, nos termos do artigo 17.o, propor a suspensão ou revogação do estastuto até que sejam satisfeitos os requisitos da decisão.
10. Para efeitos da presente secção II entende-se por «prova serológica» uma prova de seroaglutinação, uma prova de antigénio brucélico tamponado, uma prova de fixação do complemento, uma prova de plasmoaglutinação, uma prova do anel em plasma, uma prova de mciroaglutinação ou uma prova ELISA individual em sangue, como descrito no anexo C. Para efeitos da secção II, será igualmente aceite qualquer outra prova diagnóstica aprovada nos termos do artigo 17.o e descrita no anexo C. Por «prova do anel» entende-se uma prova do anel do leite ou uma prova ELISA do leite de acordo com o anexo C.
▼M49
ANEXO B
TUBERCULOSE
1. IDENTIFICAÇÃO DO AGENTE
A presença de Mycobacterium bovis (M. bovis), agente da tuberculose bovina, em amostras clínicas ou post mortem pode ser demonstrada pela observação de esfregaços corados ou por técnicas de imunoperoxidase, e confirmada por cultura do organismo num meio de isolamento primário.
O material anatomopatológico para confirmação da presença de M. bovis deve ser colhido em gânglios linfáticos anormais e em órgãos parenquimatosos tais como os pulmões, o fígado, o baço, etc. Caso o animal não apresente lesões patológicas, dever-se-ão colher para observação e cultura amostras dos gânglios linfáticos retrofaríngeos, brônquicos, mediastínicos, supramamários e mandibulares, e de alguns gânglios linfáticos mesentéricos, bem como do fígado.
A identificação de isolados pode ser feita geralmente por determinação das propriedades culturais e bioquímicas. A polimerização em cadeia (PCR) também pode ser utilizada na detecção do complexo M. tuberculosis. As técnicas de análise do ADN podem revelar-se mais rápidas e fiáveis que os métodos bioquímicos, para distinguir a M. bovis de outros membros do complexo M. tuberculosis. A identificação genética permite distinguir entre diversas estirpes de M. bovis e tornará possível a descrição de padrões de origem, transmissão e disseminação de M. bovis.
A técnica e meios utilizados, a sua normalização e a interpretação dos resultados devem ser conformes às especificações do capítulo 2.3.3 (tuberculose bovina) da quarta edição (de 2000) do Manual de normas aplicáveis aos testes para diagnóstico e às vacinas, do OIE.
2. PROVA CUTÂNEA DE TUBERCULINA
Em provas cutâneas de tuberculina oficiais utilizar-se-ão, de acordo com o método referido no ponto 2.2, derivados proteicos purificados («Purified Protein Derivatives, PPD») da tuberculina conformes às normas estabelecidas no ponto 2.1.
2.1. Normas relativas à tuberculina (bovina e aviária)
2.1.1. Definição
O derivado proteico purificado da tuberculina (tuberculina PPD, bovina e aviária) é um preparado obtido a partir dos produtos do crescimento e lise de Mycobacterium bovis ou de Mycobacterium avium, conforme o caso, tratados termicamente, capazes de revelar uma hipersensibilidade retardada num animal sensibilizado a microrganismos da mesma espécie.
2.1.2. Produção
É obtido a partir das fracções hidrossolúveis preparadas por aquecimento em vapor livre e posterior filtração de culturas de M. bovis ou de M. avium (conforme o caso) em meio sintético líquido. A fracção activa do filtrado, constituída principalmente por proteína, é isolada por precipitação, lavada e de novo dissolvida. Pode ser adicionado um conservante antimicrobiano que não dê origem a falsas reacções positivas, tal como o fenol. O preparado final estéril, isento de micobactérias, é depositado assepticamente em recipientes de vidro estéreis e invioláveis, que serão em seguida fechados de forma a impedir contaminações. O preparado pode ser liofilizado.
2.1.3. Identificação do produto
Injectar por via intradérmica uma série progressiva de doses em diferentes sítios, em cobaias albinas convenientemente sensibilizadas, de peso não inferior a 250 g. Após 24 a 28 horas, surgem reacções sob forma de inchaços edematosos com eritema, com ou sem necrose no ponto de injecção. A extensão e severidade das reacções variam em função da dose. As cobaias não sensibilizadas não apresentam reacção a injecções semelhantes.
2.1.4. Controlos
2.1.4.1. pH: O pH é de 6,5 a 7,5.
2.1.4.2. Fenol: Caso o preparado a examinar contenha fenol, a sua concentração não deverá exceder 5 g/l.
2.1.4.3. Efeito de sensibilização: utilizar um grupo de três cobaias que não tenham sido previamente tratadas com qualquer material que venha a interferir com o controlo. Injectar por via intradérmica em cada cobaia, por três vezes e com intervalos de cinco dias, uma dose do preparado a examinar equivalente a 500 UI em 0,1 ml. 15 a 21 dias após a terceira injecção, injectar por via intradérmica a mesma dose (500 UI) nestes animais e num grupo testemunha de três cobaias com a mesma massa, que não tenham recebido previamente injecções de tuberculina. 24 a 28 horas após as últimas injecções, as reacções dos dois grupos não apresentam diferença significativa.
2.1.4.4. Toxicidade: utilizar duas cobaias, cada uma com 250 g, no mínimo, que não tenham sido previamente tratadas com qualquer material que venha a interferir com o controlo. Injectar, por via subcutânea, em cada cobaia 0,5 ml do preparado a examinar. Observar os animais durante sete dias. Não ocorrem quaisquer efeitos anormais durante o período de observação.
2.1.4.5. Esterilidade: satisfaz o controlo de esterilidade prescrito na monografia sobre vacinas de uso veterinário da quarta edição (de 2002) da Farmacopeia Europeia.
2.1.5. Actividade
A actividade do derivado proteico purificado da tuberculina (bovina ou aviária) é determinada por comparação das reacções produzidas em cobaias sensibilizadas por injecção, por via intradérmica, de uma série de diluições do preparado a examinar com as reacções produzidas por concentrações conhecidas de um preparado de referência de derivado proteico purificado da tuberculina (bovina ou aviária, conforme o caso), aferido em unidades internacionais.
Para controlar a actividade, sensibilizar pelo menos nove cobaias albinas, cada uma com um peso de 400 a 600 g, por injecção intramuscular profunda de 0,0001 mg (massa húmida) de M. bovis viva da estirpe AN5, suspendidos em 0,5 ml de uma solução de 9 g/l de cloreto de sódio R, para a tuberculina bovina, ou de uma dose adequada de M. avium inactivada ou viva, para a tuberculina aviária. Quatro semanas, pelo menos, após a sensibilização das cobaias, raspar-lhes os pêlos dos flancos, numa área suficiente para quatro injecções de cada lado, no máximo. Fazer diluições do preparado a examinar e do preparado de referência em solução-tampão de fosfatos isotónica (pH 6,5-7,5) com 0,005 g/l de polissorbato 80 R. Utilizar pelo menos três doses do preparado de referência e pelo menos três doses do preparado a examinar. Escolher as doses de forma a que o diâmetro das lesões produzidas não seja inferior a 8 mm nem superior a 25 mm. Atribuir de forma aleatória as diluições aos sítios de injecção, segundo o método do quadrado latino. Injectar cada dose por via intradérmica, num volume constante de 0,1 ou 0,2 ml. Medir o diâmetro das lesões após 24 a 28 horas e calcular o resultado do teste utilizando os métodos estatísticos habituais, admitindo que o diâmetro das lesões é directamente proporcional ao logaritmo da concentração das tuberculinas.
O teste só é válido se os limites do intervalo de confiança (P = 0,95) não forem, respectivamente, inferior a 50 por cento e superior a 200 por cento da actividade estimada. Para a tuberculina bovina, a actividade estimada não é inferior a 66 por cento, nem superior a 150 por cento, da actividade declarada. Para a tuberculina aviária, a actividade estimada não é inferior a 75 por cento, nem superior a 133 por cento, da actividade declarada. Para ambas as tuberculinas (bovina e aviária), a actividade declarada não é inferior a 20 000 UI/ml.
2.1.6. Armazenagem
Conservar ao abrigo da luz, à temperatura de 5 ± 3 oC.
2.1.7. Rotulagem
O rótulo indica:
— a actividade em unidades internacionais por mililitro,
— a denominação e a quantidade de qualquer substância adicionada,
— para os preparados liofilizados:
—
— a denominação e o volume do líquido de reconstituição a adicionar,
— que o produto deve ser utilizado imediatamente após a reconstituição.
2.2. Métodos para a realização das provas
2.2.1. Consideram-se provas oficiais de tuberculina:
— a intradermotuberculinização simples: esta prova exige uma única injecção de tuberculina bovina;
— a intradermotuberculinização de comparação: esta prova exige uma só injecção de tuberculina bovina e uma só injecção de tuberculina aviária, administradas simultaneamente.
2.2.2. A dose de tuberculina injectada será:
— 2 000 UI, no mínimo, de tuberculina bovina,
— 2 000 UI, no mínimo, de tuberculina aviária.
2.2.3. O volume de cada dose injectada não deverá exceder 0,2 ml.
2.2.4. As provas de tuberculina devem ser realizadas por injecção da ou das tuberculinas na pele do pescoço. Os pontos de injecção situar-se-ão no limite entre os terços anterior e médio do pescoço. Caso sejam injectadas no mesmo animal tuberculinas aviária e bovina, o ponto de injecção da tuberculina aviária deve situar-se a cerca de 10 cm da linha superior do pescoço e o ponto de injecção da tuberculina bovina deve situar-se 12,5 cm abaixo, numa linha mais ou menos paralela à linha da espádua, ou em lados diferentes do pescoço; nos animais jovens, em que ainda não seja possível separar suficientemente os pontos de injecção de um dos lados do pescoço, será aplicada uma injecção de cada lado em sítios idênticos, no centro do terço médio do pescoço.
2.2.5. A técnica de administração da tuberculina e a interpretação das reacções serão as seguintes:
2.2.5.1.
Técnica
Nas zonas de injecção os pêlos devem ser cortados, e a pele limpa. Segura-se uma prega da pele de cada zona em que os pêlos foram cortados, entre o indicador e o polegar, mede-se com uma craveira e anota-se o resultado. Injectar em seguida a dose de tuberculina, por um método que assegure a sua administração por via intradérmica. Poderá ser utilizada uma pequena agulha estéril ligada a uma seringa graduada contendo tuberculina, que se introduzirá obliquamente nas camadas mais profundas da pele com o bordo biselado voltado para o exterior. Uma injecção bem dada provocará, à palpação, um ligeiro inchaço com as dimensões de uma ervilha em cada ponto de injecção. A espessura da prega de pele em cada ponto de injecção voltará a ser medida e registada 72 horas (+/- 4 h) depois da injecção.
2.2.5.2.
Interpretação das reacções
A interpretação das reacções basear-se-á na observação clínica e no aumento ou aumentos registados na espessura da prega de pele nos pontos de injecção, 72 horas depois da injecção da ou das tuberculinas.
a) Reacção negativa: se apenas se observar um inchaço limitado, com um aumento máximo de 2 mm de espessura da prega da pele, sem sinais clínicos tais como edema difuso ou extenso, exsudação, necrose, dor ou reacção inflamatória dos canais linfáticos da região ou dos gânglios;
b) Reacção duvidosa: se não se observar nenhum dos sinais clínicos indicados na alínea a), mas o aumento de espessura da prega da pele for superior a 2 mm e inferior a 4 mm;
c) Reacção positiva: se se observarem os sinais clínicos indicados na alínea a) ou um aumento de espessura da prega de pele de 4 mm ou mais no sítio da injecção.
2.2.5.3. A interpretação das provas oficiais de tuberculina é a seguinte:
2.2.5.3.1. Intradermotuberculinização simples:
a) Positiva: reacção tal como definida na alínea c) do ponto 2.2.5.2;
b) Duvidosa: reacção idêntica à definida na alínea b) do ponto 2.2.5.2;
c) Negativa: reacção tal como definida na alínea a) do ponto 2.2.5.2.
Os animais em que a intradermotuberculinização simples tenha dado resultados duvidosos serão submetidos a uma outra tuberculinização passado um prazo mínimo de 42 dias.
Os animais em que esta segunda prova não dê resultados negativos devem ser considerados como tendo reagido positivamente à prova de tuberculina.
Os animais com resultados positivos na prova intradérmica simples podem ser submetidos a uma intradermotuberculinização de comparação, caso haja suspeitas de falsas reacções positivas ou de reacções de interferência.
2.2.5.3.2. Intradermotuberculinização de comparação para a determinação e manutenção do estatuto de efectivo oficialmente indemne de tuberculose:
a) Positiva: reacção bovina superior em mais de 4 mm à reacção aviária ou presença de sinais clínicos;
b) Duvidosa: reacção bovina positiva ou duvidosa e superior em 1 a 4 mm à reacção aviária, e ausência de sinais clínicos;
c) Negativa: reacção bovina negativa ou reacção bovina positiva ou duvidosa mas igual ou inferior a uma reacção aviária positiva ou duvidosa e ausência de sinais clínicos nos dois casos.
Os animais em que a intradermotuberculinização de comparação tenha dado resultados duvidosos devem ser submetidos a uma outra prova de tuberculina passado um prazo mínimo de 42 dias. Os animais em que esta segunda prova não dê resultados negativos devem ser considerados como tendo reagido positivamente à prova de tuberculina.
2.2.5.3.3. O estatuto de efectivo oficialmente indemne de tuberculose pode ser suspenso, ficando os animais do efectivo excluídos do comércio intracomunitário, até estar regularizado o estatuto dos animais seguintes:
a) Animais considerados como tendo tido uma reacção duvidosa à prova de tuberculina simples;
b) Animais considerados como tendo reagido positivamente à prova de tuberculina simples mas que devem ser submetidos a uma prova de tuberculina de comparação;
c) Animais considerados como tendo tido uma reacção duvidosa à prova de tuberculina de comparação.
2.2.5.3.4. Nos casos em que a legislação comunitária exige que os animais sejam submetidos a uma prova intradérmica antes da sua deslocação, a prova deve ser interpretada de forma a que sejam excluídos do comércio intracomunitário os animais em que o aumento de espessura da prega de pele seja superior a 2 mm, ou em que se verifique a presença de sinais clínicos.
2.2.5.3.5. Para permitir a detecção de um número máximo de animais infectados e doentes num efectivo ou região, os Estados-Membros podem alterar os critérios de interpretação da prova de forma a melhorar a sua sensibilidade, considerando como reacções positivas todas as reacções duvidosas referidas na alínea b) do ponto 2.2.5.3.1 e na alínea b) do ponto 2.2.5.3.2.
3. PROVA SUPLEMENTAR
Para permitir a detecção de um número máximo de animais infectados e doentes num efectivo ou região, os Estados-Membros podem autorizar a utilização, além da prova de tuberculina, do ensaio de interferão-gama referido no capítulo 2.3.3 (tuberculose bovina) da quarta edição (de 2000) do Manual de normas aplicáveis aos testes para diagnóstico e às vacinas, do OIE.
4. ORGANISMOS OFICIAIS E LABORATÓRIOS NACIONAIS DE REFERÊNCIA
▼M55
4.1. Tarefas e responsabilidades
Os organismos oficiais e laboratórios nacionais de referência designados em conformidade com o artigo 6.o-A devem ser encarregados do controlo oficial, nos respectivos Estados-Membros, das tuberculinas e reagentes indicados nos pontos 2 e 3, a fim de garantir a conformidade de cada um deles com as normas indicadas respectivamente no ponto 2.1 e no ponto 3.
▼M55 —————
▼M56
ANEXO C
BRUCELOSE
1. IDENTIFICAÇÃO DO AGENTE
A demonstração, através de coloração ácido-resistente modificada ou imunospecífica, de organismos com a morfologia da Brucella em material de aborto, corrimentos vaginais ou no leite constitui um dado sugestivo de brucelose, especialmente se for corroborada por testes serológicos. Os métodos de polimerização em cadeia (PCR) constituem também meios adicionais de detecção.
Sempre que possível, a Brucella spp. deve ser isolada com recurso a meios simples ou selectivos por cultura de corrimentos uterinos, fetos abortados, secreções do úbere ou tecidos seleccionados, tais como nódulos linfáticos e órgãos reprodutores masculinos e femininos.
Após o isolamento, há que identificar a espécie e biovar, através de lise com fagos e/ou de testes do metabolismo oxidativo ou critérios de cultura, bioquímicos e serológicos. A PCR pode constituir um método quer complementar quer de biotipagem, com base em sequências genómicas específicas.
A técnica e meios utilizados, a sua normalização e a interpretação dos resultados devem ser conformes às especificações dos capítulos 2.4.3 (brucelose bovina), 2.7.2 (brucelose ovina e caprina) e 2.8.5 (brucelose suína) da sexta edição (2008) do Manual de testes de diagnóstico e vacinas da OIE.
2. TESTES IMUNOLÓGICOS
2.1. Normas
|
2.1.1.
|
Para a preparação de todo o antigénio utilizado nos testes do Rosa Bengala (RBT), de sero-aglutinação (SAT), de fixação do complemento (CFT) e do anel em leite (MRT) deve usar-se a estirpe n.o 99 (Weybridge) ou 1119-3 (USDA) da Brucella abortus biovar 1.
|
|
2.1.2.
|
O soro-padrão de referência para os testes RBT, SAT, CFT e MRT é o soro-padrão de referência internacional do OIE (OIEISS), anteriormente designado segundo soro-padrão anti-Brucella abortus da OMS (ISAbS).
|
|
2.1.3.
|
Os soros-padrão de referência para os ensaios de imunoabsorção enzimática (ELISA) são os seguintes:
— o soro-padrão ELISA fracamente positivo do OIE (OIEELISAWPSS),
— o soro-padrão ELISA fortemente positivo do OIE (OIEELISASPSS),
— o soro-padrão ELISA negativo do OIE (OIEELISANSS).
|
|
2.1.4.
|
Os soros-padrão de referência para os ensaios com fluorescência polarizada (FPA) são os seguintes:
— o soro-padrão ELISA fracamente positivo do OIE (OIEELISAWPSS),
— o soro-padrão ELISA fortemente positivo do OIE (OIEELISASPSS),
— o soro-padrão ELISA negativo do OIE (OIEELISANSS).
|
|
2.1.5.
|
Os soros-padrão enumerados nos pontos 2.1.3 e 2.1.4 encontram-se disponíveis no laboratório comunitário de referência para a brucelose ou na Veterinary Laboratories Agency (VLA) de Weybridge (Reino Unido).
|
|
2.1.6.
|
O OIEISS, o OIEELISAWPSS, o OIEELISASPSS e o OIEELISANSS são padrões primários internacionais, a partir dos quais devem ser estabelecidos padrões secundários de referência nacionais de soros («padrões de trabalho») para cada um dos testes referidos no ponto 2.1.1 em cada um dos Estados-Membros.
|
2.2. Ensaios de imunoabsorção enzimática (ELISA) ou outras provas de aglutinação para a detecção da brucelose bovina no soro ou no leite.
2.2.1. Material e reagentes
A técnica utilizada e a interpretação dos resultados devem ter sido validadas em conformidade com os princípios estabelecidos no capítulo 1.1.4 da sexta edição (2008) do Manual de testes de diagnóstico e vacinas da OIE e tem de, no mínimo, abranger testes laboratoriais e de diagnóstico.
2.2.2. Normalização do teste
|
2.2.2.1.
|
Normalização do procedimento de teste de amostras séricas específicas:
a) uma pré-diluição de 1:150 (
18
) do OIEISS, de 1:2 do OIEELISAWPSS ou de 1:16 do OIEELISASPSS utilizando-se um soro negativo (ou um agregado de soros negativos) tem de apresentar uma reacção positiva;
b) Uma pré-diluição de 1:600 do OIEISS, de 1:8 do OIEELISAWPSS ou de 1:64 do OIEELISASPSS utilizando-se um soro negativo (ou um agregado de soros negativos) tem de apresentar uma reacção negativa;
c) O OIEELISANSS tem de apresentar sempre uma reacção negativa.
|
|
2.2.2.2.
|
Normalização do procedimento de teste de amostras de agregados de soro:
a) Uma pré-diluição de 1:150 do OIEISS, de 1:2 do OIEELISAWPSS ou de 1:16 do OIEELISASPSS utilizando-se um soro negativo (ou um agregado de soros negativos), subsequentemente diluída em soros negativos o número de vezes correspondente ao número de amostras que compõem o agregado, tem de apresentar uma reacção positiva;
b) O OIEELISANSS tem de apresentar sempre uma reacção negativa;
c) O teste deve ser adequado para detectar dados sugestivos de infecção num só animal de um grupo de animais cujas amostras de soro foram agregadas.
|
|
2.2.2.3.
|
Normalização do procedimento de teste de amostras de agregados de leite ou soro de leite:
a) uma pré-diluição de 1:1 000 do OIEISS, de 1:16 do OIEELISAWPSS ou de 1:125 do OIEELISASPSS utilizando-se um soro negativo (ou um agregado de soros negativos), subsequentemente diluída a 1:10 em leite negativo, tem de apresentar uma reacção positiva;
b) O OIEELISANSS diluído a 1:10 em leite negativo tem de apresentar sempre uma reacção negativa;
c) O teste deve ser adequado para detectar dados sugestivos de infecção num só animal de um grupo de animais cujas amostras de soro foram agregadas.
|
2.2.3. Condições de utilização do teste ELISA no diagnóstico da brucelose bovina
|
2.2.3.1.
|
Nas condições de calibração indicadas nos pontos 2.2.2.1 e 2.2.2.2 para os testes ELISA de amostras séricas, a sensibilidade diagnóstica dos testes ELISA deve ser superior ou igual à dos testes RBT ou CFT, tendo em conta a situação epidemiológica em que são utilizados.
|
|
2.2.3.2.
|
Nas condições de calibração indicadas no ponto 2.2.2.3 para os testes ELISA de amostras de agregados de leite, a sensibilidade diagnóstica dos testes ELISA deve ser superior ou igual à dos testes MRT, tendo em conta não só a situação epidemiológica, como também os sistemas de criação médios e extremos previstos.
|
|
2.2.3.3.
|
Se os testes ELISA forem utilizados para efeitos de certificação, em conformidade com o disposto no n.o 1 do artigo 6.o, ou para a determinação e manutenção do estatuto dos efectivos, em conformidade com o disposto no ponto II.10 do anexo A, a agregação de amostras séricas deve efectuar-se de molde a que os resultados dos testes possam ser indubitavelmente relacionados com o animal específico incluído no agregado. Os testes de confirmação devem ser efectuados em amostras séricas de animais específicos.
|
|
2.2.3.4.
|
O teste ELISA pode ser utilizado numa amostra de leite retirada de uma colheita de leite proveniente de uma exploração com pelo menos 30 % das vacas leiteiras em lactação. Se se recorrer àquele método, têm de ser tomadas medidas que garantam que as amostras recolhidas para análise possam ser indubitavelmente relacionadas com os animais de que o leite provém. Os testes de confirmação devem ser efectuados em amostras séricas de animais específicos.
|
2.3. Teste de fixação do complemento (CFT)
|
2.3.1.
|
O antigénio é constituído por uma suspensão bacteriana em fenol-soro fisiológico [NaCl a 0,85 % (m/v) e fenol a 0,5 % (v/v)] ou num tampão veronal. Os antigénios podem ser fornecidos concentrados, desde que o factor de diluição a utilizar esteja indicado no rótulo do frasco. O antigénio deve ser conservado a 4 oC e não deve ser congelado.
|
|
2.3.2.
|
Os soros devem ser inactivados do seguinte modo:
— soro de bovino: 56 a 60 oC durante 30 a 50 minutos;
— soro de suíno: 60 oC durante 30 a 50 minutos.
|
|
2.3.3.
|
Para que haja uma reacção genuína no âmbito do teste, deve-se utilizar uma dose complementar superior à dose mínima necessária para a hemólise total.
|
|
2.3.4.
|
O teste de fixação do complemento deve ser sempre acompanhado dos seguintes controlos:
a) Controlo do efeito anticomplementar do soro;
b) Controlo do antigénio;
c) Controlo dos eritrócitos sensibilizados;
d) Controlo do complemento;
e) Controlo da sensibilidade no início da reacção, utilizando-se um soro positivo;
f) Controlo da especificidade da reacção, utilizando-se um soro negativo.
|
|
2.3.5.
|
Cálculo dos resultados O OIEISS contém 1 000 unidades internacionais CFT (ICFTU) por ml. Se, num dado método, o OIEISS for testado, o resultado deve ser apresentado sob a forma de título (ou seja, a diluição directa mais elevada do OIEISS dando 50 % de hemólise, TOIEISS). O resultado do soro testado, apresentado sob a forma de título (Tsoro testado), deve ser expresso em ICFTU por ml. Para converter o título em ICFTU, o factor (F) necessário para a conversão em ICFTU do título de soro testado (Tsoro testado) por tal método é dado pela seguinte fórmula:
F = 1 000 × 1/TOIEISS
e o teor de unidades internacionais CFT por ml de soro testado (ICFTUsoro testado) é dado pelo seguinte fórmula:
ICFTUSORO TESTADO = F × TSORO TESTADO
|
|
2.3.6.
|
Interpretação dos resultados É considerado positivo um soro com 20 ou mais UI por ml.
|
2.4. Teste do anel em leite (MRT)
|
2.4.1.
|
O antigénio é constituído por uma suspensão bacteriana em fenol-soro fisiológico [NaCl a 0,85 % (m/v) e fenol a 0,5 % (v/v)] corada com hematoxilina. O antigénio deve ser conservado a 4 oC e não deve ser congelado.
|
|
2.4.2.
|
A sensibilidade do antigénio tem de ser normalizada tomando como padrão o OIEISS, por forma a que o antigénio produza uma reacção positiva numa diluição a 1:500 do OIEISS em leite negativo e uma reacção negativa numa diluição a 1:1 000 .
|
|
2.4.3.
|
Devem ser submetidas à prova do anel amostras representativas do conteúdo de cada batedeira ou de cada cisterna de leite da exploração.
|
|
2.4.4.
|
As amostras de leite não devem ter sido congeladas, aquecidas ou sujeitas a agitação violenta.
|
|
2.4.5.
|
A reacção deve efectuar-se de acordo com um dos seguintes métodos:
— numa coluna de leite de, pelo menos, 25 mm de altura e com um volume de leite de 1 ml, ao qual se adicionaram 0,03 ou 0,05 ml de um dos antigénios corados padronizados,
— numa coluna de leite de, pelo menos, 25 mm de altura e com um volume de leite de 2 ml, ao qual se adicionaram 0,05 ml de um dos antigénios corados padronizados,
— num volume de leite de 8 ml ao qual se adicionaram 0,08 ml de um dos antigénios corados padronizados.
|
|
2.4.6.
|
A mistura de leite e antigénio deve ser incubada a 37 oC durante 60 minutos, junto com padrões de trabalho positivos e negativos. A incubação a 4 oC 16 a 24 horas depois aumenta a sensibilidade do teste.
|
|
2.4.7.
|
Interpretação dos resultados:
a) Reacção negativa: leite corado e nata não corada;
b) Reacção positiva:
— leite e nata com coloração idêntica, ou
— leite não corado e nata corada.
|
2.5. Teste do antigénio brucélico tamponado [teste do Rosa Bengala (RBT)]
|
2.5.1.
|
O antigénio é constituído por uma suspensão bacteriana num diluente de antigénio brucélico tamponado com pH de 3,65 ± 0,05, corada com o corante Rosa Bengala. O antigénio deve ser fornecido pronto a ser utilizado e deve ser armazenado a 4 oC, sem ser congelado.
|
|
2.5.2.
|
O antigénio deve ser preparado sem referência à concentração de células, devendo a sua sensibilidade ser aferida por comparação com o OIEISS, por forma a que o antigénio produza uma reacção positiva com uma diluição sérica de 1:45 e uma reacção negativa com uma diluição de 1:55.
|
|
2.5.3.
|
O teste RBT deve ser efectuado do seguinte modo:
a) Misturam-se volumes iguais (20-30 μl) de soro e antigénio numa placa de porcelana ou esmaltada, por forma a criar uma zona com aproximadamente 2 cm de diâmetro. A mistura é agitada suavemente durante quatro minutos à temperatura ambiente, pesquisando-se então a aglutinação com uma boa fonte de luz;
b) Podem ser utilizados métodos automatizados, desde que sejam pelo menos tão sensíveis e precisos como o método manual.
|
|
2.5.4.
|
Interpretação dos resultados Considera-se positiva qualquer reacção visível, a menos que se verifique dessecação excessiva na periferia.
Todas as séries de testes devem incluir padrões de trabalho positivos e negativos.
|
2.6. Teste de sero-aglutinação (SAT)
|
2.6.1.
|
O antigénio é uma suspensão bacteriana em fenol-soro fisiológico [NaCl a 0,85 % (m/v) e fenol a 0,5 % (v/v)].
Não deve ser utilizado formaldeído.
Os antigénios podem ser fornecidos concentrados, desde que o factor de diluição a utilizar esteja indicado no rótulo do frasco.
Pode adicionar-se EDTA à suspensão de antigénio, até uma diluição final de 5 mM, para diminuir o número de falsos positivos no teste de sero-aglutinação. Subsequentemente, a suspensão bacteriana deve ser reajustada para um pH de 7,2.
|
|
2.6.2.
|
O OIEISS contém 1 000 unidades internacionais de aglutinação.
|
|
2.6.3.
|
O antigénio deve ser preparado sem referência à concentração de células, devendo a sua sensibilidade ser aferida por comparação com o OIEISS, por forma a que o antigénio produza uma aglutinação de 50 % com uma diluição sérica final de 1:600 a 1:1 000 , ou uma aglutinação de 75 % com uma diluição sérica final de 1:500 a 1:750.
Pode ser igualmente aconselhável comparar a reactividade dos novos lotes de antigénio com a dos já anteriormente padronizados, através de um painel de soros bem definidos.
|
|
2.6.4.
|
O teste deve ser efectuado em tubos ou em microplacas. A mistura de diluições de antigénio e soro deve ser incubada durante 16 a 24 horas a 37 oC.
Devem ser preparadas pelo menos três diluições para cada soro. As diluições do soro suspeito devem ser feitas de forma a que a leitura da reacção no limite de positividade seja feita no tubo mediano (ou poço, caso seja utilizada uma microplaca).
|
|
2.6.5.
|
Interpretação dos resultados O grau de aglutinação brucélica do soro deve ser expresso em UI por ml.
É considerado positivo um soro com 30 ou mais UI por ml.
|
2.7. Ensaio com fluorescência polarizada (FPA)
|
2.7.1.
|
O FPA pode ser efectuado em tubos de vidro ou numa placa de 96 poços. A técnica utilizada, a sua normalização e a interpretação dos resultados têm de ser conformes às especificações do capítulo 2.4.3 (brucelose bovina) da sexta edição (2008) do Manual de testes de diagnóstico e vacinas da OIE.
|
|
2.7.2.
|
Normalização do teste O FPA deve ser normalizado de forma a que:
a) O OIEELISASPSS e o OIEELISAWPSS apresentem resultados positivos de forma coerente;
b) Uma pré-diluição de 1:8 do OIEELISAWPSS ou de 1:64 do OIEELISASPSS utilizando-se um soro negativo (ou um agregado de soros negativos) apresentem sempre uma reacção negativa;
c) O OIEELISANSS apresente sempre uma reacção negativa.
Devem incluir-se em cada lote de testes: um soro fortemente positivo, um soro fracamente positivo e um soro-padrão de trabalho negativo (calibrados em função dos soros padrão ELISA da OIE).
|
3. TESTES COMPLEMENTARES
3.1. Prova cutânea da brucelose (BST)
3.1.1. Condições de utilização da BST:
a) A prova cutânea da brucelose não deve ser utilizada na certificação com vista ao comércio intracomunitário;
b) A prova cutânea da brucelose é um dos testes mais específicos para a detecção de brucelose em animais não vacinados, no entanto, o diagnóstico não pode assentar apenas em provas intradérmicas positivas;
c) Devem ser considerados infectados ou suspeitos de estarem infectados os bovinos com resultados negativos num dos testes serológicos definidos no presente anexo e com resultado positivo na BST;
d) Os bovinos com um resultado positivo num dos testes serológicos definidos no presente anexo podem ser sujeitos à BST, para interpretar os resultados dos testes serológicos, nomeadamente se não puder ser excluída uma reacção cruzada com outras bactérias em efectivos bovinos oficialmente indemnes ou indemnes de brucelose.
|
3.1.2.
|
A prova deve utilizar uma preparação normalizada e definida de alérgeno da brucelose isenta de antigénio lipopolissacarídico (LPS) liso, visto que este pode causar reacções inflamatórias inespecíficas ou interferir com testes serológicos subsequentes.
Os requisitos para a produção de Brucellin devem cumprir o disposto na secção C.1 do capítulo 2.4.3 da sexta edição (2008) do Manual de testes de diagnóstico e vacinas da OIE.
|
|
3.1.3.
|
Procedimento de ensaio
|
3.1.3.1.
|
Injecta-se intradermicamente na prega caudal, na pele do flanco ou na parte lateral do pescoço 0,1 ml de alérgeno da brucelose.
|
|
3.1.3.2.
|
Procede-se à leitura dos resultados após 48-72 horas.
|
|
3.1.3.3.
|
Antes da injecção e aquando da repetição do exame, mede-se a espessura da pele no local de injecção com um compasso de Vernier.
|
|
3.1.3.4.
|
Interpretação dos resultados:
As reacções fortes são facilmente identificáveis pela tumefacção e endurecimento locais.
Na BST, um aumento da espessura da pele de 1,5 a 2 mm deve ser considerado uma reacção positiva.
|
|
3.2. Ensaio de imunoabsorção enzimática competitiva (cELISA)
3.2.1. Condições de utilização do ensaio cELISA
O ensaio cELISA não deve ser utilizado com vista à certificação para o comércio intracomunitário;
Os bovinos com um resultado positivo num dos testes serológicos definidos no presente anexo podem ser sujeitos a um ensaio cELISA, para confirmar a interpretação dos resultados dos testes serológicos, nomeadamente se não puder ser excluída uma reacção cruzada com outras bactérias em efectivos bovinos oficialmente indemnes ou indemnes de brucelose nem eliminar reacções devidas a anticorpos residuais produzidos em resposta à vacinação com S19.
3.2.2. Procedimento de ensaio
O ensaio deve ser efectuado em conformidade com o prescrito na secção B.2 do capítulo 2.4.3 da sexta edição (2008) do Manual de testes de diagnóstico e vacinas da OIE.
▼M48
4. LABORATÓRIOS NACIONAIS DE REFERÊNCIA
▼M56
4.1. Tarefas e responsabilidades
Incumbe aos laboratórios nacionais de referência:
a) A aprovação dos resultados dos testes de validação que comprovam a fiabilidade do método de teste utilizado no Estado-Membro;
b) A determinação do número máximo de amostras que podem ser agregadas nos kits ELISA utilizados;
c) A calibração de padrões de trabalho, tal como referido no ponto 2.1.6;
d) Controlos de qualidade de todos os lotes de antigénios e kits ELISA utilizados no Estado-Membro;
e) Cooperar com o laboratório comunitário de referência para a brucelose e seguir as suas recomendações.
▼M55 —————
▼M44
ANEXO D
CAPÍTULO I
EFECTIVOS, ESTADOS-MEMBROS E REGIÕES OFICIALMENTE INDEMNES DE LEUCOSE BOVINA ENZOÓTICA
A. Um efectivo é considerado oficialmente indemne de leucose bovina enzoótica se:
i) Não existirem indícios, quer clínicos quer laboratoriais, de qualquer caso de leucose bovina enzoótica no efectivo, nem tiver sido confirmado qualquer caso nos dois anos anteriores; e
ii) Todos os animais com idade superior a 24 meses tiverem sido submetidos, com reacções negativas, a duas provas realizadas nos 12 meses precedentes, segundo o presente anexo, com um intervalo de, pelo menos, quatro meses; ou
iii) Preencher as condições da alínea i) anterior e estiver situado num Estado-membro ou numa região de um Estado-membro oficialmente indemne de leucose bovina enzoótica.
B. Um efectivo manterá o estatuto de oficialmente indemne de leucose bovina enzoótica se:
i) Continuar a estar preenchida a condição prevista na alínea i) da parte A;
ii) Todos os animais introduzidos no efectivo forem provenientes de um efectivo oficialmente indemne de leucose bovina enzoótica;
iii) Todos os animais com idade superior a 24 meses continuarem a apresentar reacção negativa a provas realizadas, de três em três anos, de acordo com o capítulo II;
iv) Os animais destinados à reprodução que tenham sido introduzidos num efectivo e que sejam provenientes de um país terceiro tiverem sido importados nos termos da Directiva 72/462/CEE.
C. O estatuto de efectivo oficialmente indemne de leucose bovina enzoótica será suspenso caso deixem de estar preenchidas as condições especificadas na parte B ou se na sequência de provas laboratoriais ou por motivos clínicos se suspeitar de que um ou mais bovinos têm leucose bovina enzoótica e o ou os animais suspeitos forem imediatamente abatidos.
D. O estatuto permanecerá suspenso até que estejam preenchidas as seguintes condições:
1. Se, num efectivo oficialmente indemne de leucose bovina enzoótica, apenas um animal tiver apresentado reacção positiva a uma das provas referidas no capítulo II ou se, por outros motivos, houver suspeitas de infecção de um animal do efectivo:
i) O animal que tenha reagido positivamente e, no caso de uma vaca, todos os vitelos seus descendentes, devem ser retirados do efectivo e enviados para abate, sob o controlo das autoridades veterinárias;
ii) Todos os animais do efectivo com idade superior a doze meses devem ter apresentado reacção negativa a duas prova serológicas realizadas (com um intervalo de pelo menos quatro meses e de no máximo doze meses) de acordo com o capítulo II pelo menos três meses após a retirada dos animais positivos e dos seus eventuais descendentes;
iii) Deve ter sido realizado um inquérito epidemiológico com resultados negativos e os efectivos epidemiologicamente ligados ao efectivo infectado devem ter sido submetidos às medidas referidas na alínea ii).
A autoridade competente pode, no entanto, conceder uma derrogação da obrigação de abate do vitelo de uma vaca infectada, desde que este tenha sido separado da mãe imediatamente após o parto. Neste caso, o vitelo deve ser sujeito às condições previstas na alínea iii) do ponto 2.
2. Caso mais de um animal do efectivo oficialmente indemne de leucose bovina enzoótica tenha apresentado reacção positiva a uma das provas referidas no capítulo II, ou caso haja, por outros motivos, suspeitas de infecção em mais do que um animal do efectivo:
i) Todos os animais que apresentaram uma reacção positiva e os respectivos vitelos, se se tratar de vacas, devem ser retirados para abate sob controlo das autoridades veterinárias;
ii) Todos os animais do efectivo com idade superior a 12 meses devem ter sido submetidos, com reacção negativa, a duas provas realizadas de acordo com o capítulo II, com um intervalo mínimo de quatro meses e máximo de 12 meses;
iii) Os restantes animais do efectivo devem, depois de identificados, permanecer na exploração até terem idade superior a 24 meses e ter sido submetidos a provas de acordo com o capítulo II após atingirem essa idade, a não ser que a autoridade competente permita que esses animais sigam directamente para abate sob controlo oficial;
iv) Deve ter sido realizado um inquérito epidemiológico com resultados negativos e os efectivos epidemiologicamente ligados ao efectivo infectado devem ter sido submetidos às medidas referidas na alínea ii).
A autoridade competente pode, no entanto, conceder uma derrogação da obrigação de abate do vitelo de uma vaca infectada, desde que este tenha sido separado da mãe imediatamente após o parto. Neste caso, o vitelo deve ser submetido às condições previstas na alínea iii) do ponto 2.
E. Nos termos do artigo 17.o e com base em informações fornecidas segundo o artigo 8.o, um Estado-membro ou parte de um Estado-membro pode ser oficialmente considerado indemne de leucose bovina enzoótica se:
a) Todas as condições do ponto A forem satisfeitas e pelo menos 99,8 % dos efectivos bovinos estiverem oficialmente indemnes de leucose bovina enzoótica;
ou
b) Não tiver sido confirmado qualquer caso de leucose bovina enzoótica no Estado-membro ou parte do Estado-membro durante os últimos três anos e a presença de tumores suspeitos de serem devidos à LBE for obrigatoriamente notificada, sendo as respectivas causas investigadas, e
no caso de um Estado-membro, todos os animais com idade superior a 24 meses em pelo menos 10 % dos efectivos, seleccionados aleatoriamente, tiverem sido submetidos com resultados negativos a provas de acordo com o capítulo II durante os 24 meses anteriores; ou
no caso de uma parte de um Estado-membro, todos os animais com idade superior a 24 meses tiverem sido submetidos a uma prova prevista no capítulo II durante os 24 meses anteriores;
ou
c) For demonstrado por qualquer outro método, com um nível de confiança de 99 %, que menos de 0,2 % dos efectivos foram infectados.
F. Um Estado-membro ou uma região de um Estado-membro manterão o estatuto de oficialmente indemnes de leucose bovina enzoótica se:
a) Todos os bovinos abatidos no território desse Estado-membro ou região forem submetidos a uma inspecção oficial post mortem no qual todos os tumores que poderiam ser devidos ao vírus da LBE são objecto de um exame laboratorial; e
b) O Estado-membro informar a Comissão da ocorrência de todos os casos de leucose bovina enzoótica na região;
c) Todos os bovinos com reacção positiva a uma das provas previstas no capítulo II forem abatidos e o efectivo permanecer submetido a restrições até ao restabelecimento do seu estatuto segundo a parte D;
d) Todos os bovinos com mais de dois anos de idade tiverem sido controlados, quer uma vez durante os primeiros cinco anos após obterem o estatuto segundo o capítulo II, quer no decurso dos cinco primeiros anos após a obtenção do estatuto por outro procedimento que demonstre, com um grau de confiança de 99 %, que menos de 0,2 % dos efectivos foram infectados. Contudo, se não se tiver registado nenhum caso de leucose bovina enzoótica no Estado-membro ou numa região de um Estado-membro numa proporção de um efectivo para 10 000 durante pelo menos três anos, pode ser tomada, nos termos do artigo 17.o, a decisão de diminuir a pesquisa serológica sistemática desde que todos os bovinos com mais de 12 meses de idade em pelo menos 1 % dos efectivos, seleccionados aleatoriamente todos os anos, tenham sido sujeitos a uma prova realizada segundo o capítulo II.
G. O estatuto de oficialmente indemne de leucose bovina enzoótica de um Estado-membro ou de uma parte de um Estado-membro será suspenso, nos termos do artigo 17.o, se, em resultado das pesquisas realizadas de acordo com o ponto F supra, houver indícios de uma significativa alteração da situação no que se refere à leucose bovina enzoótica num Estado-membro ou parte de um Estado-membro que tenha sido reconhecido como oficialmente indemne de leucose bovina enzoótica.
O estatuto de oficialmente indemne de leucose bovina enzoótica pode ser restabelecido, nos termos do artigo 17.o, quando os critérios determinados de acordo com o mesmo procedimento forem cumpridos.
▼M57
CAPÍTULO II
PROVAS PARA PESQUISA DE LEUCOSE BOVINA ENZOÓTICA
A pesquisa de leucose bovina enzoótica efectua-se mediante a prova de imunodifusão em ágar nas condições descritas nas partes A e B, ou mediante a prova de imunoabsorção enzimática (Elisa) nas condições descritas na parte C. O método de imunodifusão só se aplica às provas individuais. No caso de os resultados das provas serem objecto de uma contestação devidamente fundamentada, efectuar-se-á uma prova de imunodifusão como controlo complementar.
As provas de imunodifusão e Elisa devem ser padronizados em relação ao soro E05, que é o soro-padrão oficial da UE, fornecido por:
Friedrich-Loeffler-Institut
Federal Research Institute for Animal Health
OIE Reference Laboratory for Enzootic Bovine Leukosis (EBL)
Südufer 10
17493 Greifswald — Insel Riems
Alemanha.
A.
Provas de imunodifusão sobre placas de ágar para pesquisa de leucose bovina enzoótica
1. O antigénio a utilizar nesta prova deve conter a glicoproteína do vírus da leucose bovina. O antigénio deve ser padronizado em relação ao soro E05.
2. Os organismos oficiais e laboratórios nacionais de referência designados em conformidade com o disposto no artigo 6.oA para a coordenação dos padrões e dos métodos de diagnóstico da leucose bovina enzoótica devem ser encarregados da calibração do antigénio-padrão de trabalho em relação ao soro E05.
3. Os antigénios-padrão utilizados no laboratório devem ser apresentados pelo menos uma vez por ano aos organismos oficiais ou laboratórios nacionais de referência designados em conformidade com o artigo 6.oA, para aí serem testados por comparação com o soro E05. Independentemente desta padronização, o antigénio utilizado pode ser calibrado de acordo com o método descrito na parte B.
4. Na prova serão utilizados os reagentes seguintes:
a) Antigénio: o antigénio deve conter a glicoproteína específica do vírus da leucose bovina enzoótica padronizado por comparação com o soro E05;
c) Um soro de controlo positivo conhecido;
d) Ágar:
— tampão Tris 0,05 M, pH 7,2,
— devem colocar-se 15 ml deste ágar numa placa de Petri de 85 mm de diâmetro, o que dá uma altura de 2,6 mm de ágar.
5. Preparar um dispositivo experimental de sete cavidades isentas de humidade por perfuração do ágar até ao fundo da placa; a rede assim obtida deverá ser constituída por uma cavidade central em torno da qual se ordenam seis cavidades periféricas dispostas em círculo.
Diâmetro da cavidade central: 4 mm;
Diâmetro das cavidades periféricas: 6 mm;
Distância entre a cavidade central e as cavidades periféricas: 3 mm.
6. Encher a cavidade central com o antigénio-padrão. As cavidades periféricas 1 e 4 – ver esquema no ponto 3 da parte B – são enchidas com o soro positivo conhecido e as cavidades 2, 3, 5 e 6 com os soros a testar. As cavidades devem ser enchidas até ao desaparecimento do menisco.
7. As quantidades obtidas são as seguintes:
— antigénio: 32 microlitros,
— soro de controlo: 73 microlitros,
— soro a testar: 73 microlitros.
8. A incubação deve durar 72 horas à temperatura ambiente (20-27 °C) em atmosfera húmida e fechada.
9. A prova pode ser lida passadas 24 horas e passadas 48 horas, mas não se pode obter qualquer resultado final antes de passarem 72 horas:
a) Um soro a testar é positivo se formar uma curva de precipitação específica com o antigénio do vírus da leucose bovina e se essa curva coincidir com a do soro de controlo;
b) Um soro a testar é negativo se não formar uma curva de precipitação específica com o antigénio do vírus da leucose bovina e se não inflectir a curva do soro de controlo;
c) A reacção não pode ser considerada concludente se:
i) inflectir a curva do soro de controlo para a cavidade do antigénio do vírus da leucose bovina sem formar uma curva de precipitação visível com o antigénio, ou
ii) não for possível interpretá-la como negativa ou como positiva.
No caso de as reacções não serem concludentes, pode repetir-se a prova e utilizar soro concentrado.
10. Pode ser utilizada qualquer outra configuração ou distribuição das cavidades, desde que permita detectar como positiva uma diluição do soro E05 em soro negativo a 1/10.
B.
Método de padronização do antigénio
1. Soluções e materiais necessários
a) 40 ml de ágar a 1,6 % num tampão Tris/HCl 0,05 M, pH 7,2, com 8,5 % de NaCl;
b) 15 ml de um soro de leucose bovina que só tenha anticorpos em relação às glicoproteínas do vírus da leucose bovina, diluído a 1/10 num tampão Tris/HCl 0,05 M, pH 7,2, com 8,5 % de NaCl;
c) 15 ml de um soro de leucose bovina que só tenha anticorpos em relação às glicoproteínas do vírus da leucose bovina, diluído a 1/5 num tampão Tris/HCl 0,05 M, pH 7,2, com 8,5 % de NaCl;
d) Quatro placas de Petri de plástico, com 85 mm de diâmetro;
e) Punção com 4 a 6 mm de diâmetro;
f) Antigénio de referência;
g) Antigénio a padronizar;
2. Modo de execução
Dissolver o ágar (1,6 %) no tampão Tris/HCl aquecendo com cuidado até 100 °C. Pôr no banho-maria a 56 °C durante cerca de 1 hora. Colocar também as diluições do soro de leucose bovina no banho-maria a 56 °C.
Misturar em seguida 15 ml de solução de agarose a 56 °C com os 15 ml de soro de leucose bovina (1:10), agitar rapidamente e deitar em duas placas de Petri, à razão de 15 ml por placa. Repetir as operações atrás descritas com o soro de leucose bovina diluído a 1/5.
Quando a agarose tiver endurecido, fazer as cavidades do seguinte modo:
3. Adição de antigénio
a) Placas de Petri n.os 1 e 3:
i) cavidade A — antigénio de referência não diluído,
ii) cavidade B — antigénio de referência diluído a 1/2,
iii) cavidades C e E — antigénio de referência,
iv) cavidade D — antigénio a testar, não diluído.
b) Placas de Petri n.os 2 e 4:
i) cavidade A — antigénio a testar, não diluído,
ii) cavidade B — antigénio a testar, diluído a 1/2,
iii) cavidade C — antigénio a testar, diluído a 1/4,
iv) cavidade D — antigénio a testar, diluído a 1/8.
4. Instruções complementares
a) A prova deve ser efectuada com dois graus de diluição do soro (1/5 e 1/10) a fim de obter a precipitação óptima;
b) Se o diâmetro de precipitação for muito pequeno para cada um dos dois graus de diluição, deve fazer-se uma diluição suplementar do soro;
c) Se o diâmetro de precipitação for excessivo para ambos os graus de diluição e se o precipitado for ténue, deve-se escolher um grau de diluição mais fraco para o soro;
d) A concentração final de ágar deve ser de 0,8 % e a dos soros de 5 % e de 10 %, respectivamente;
e) Anotar os diâmetros medidos no gráfico seguinte. A diluição de trabalho é aquela em que se registar o mesmo diâmetro para o antigénio a testar e para o antigénio de referência.

C.
Prova de imunoabsorção enzimática (Elisa) para a pesquisa de leucose bovina enzoótica
1. São os seguintes os materiais e reagentes a utilizar:
a) Microplacas para fase sólida, tinas ou qualquer outra fase sólida;
b) Antigénio fixado à fase sólida com ou sem a ajuda de anticorpos de captação policlonais ou monoclonais. Se o antigénio for directamente aplicado à fase sólida, todas as amostras que apresentem reacções positivas devem ser testadas de novo em relação ao antigénio de controlo. Este deve ser idêntico ao antigénio testado, mas sem os antigénios do vírus da leucose bovina. Se os anticorpos de captação forem aplicados à fase sólida, os anticorpos devem reagir apenas aos antigénios do vírus da leucose bovina;
c) Fluido biológico a examinar;
d) Controlos positivos e negativos correspondentes;
f) Substrato adaptado à enzima utilizada;
g) Solução de paragem, se necessário;
h) Soluções para a diluição das amostras de ensaio, para a preparação dos reagentes e para a lavagem;
i) Sistema de leitura adequado ao substrato utilizado.
2. Normalização e sensibilidade do teste
A sensibilidade da prova Elisa utilizada deve ser de um nível tal que o soro E05 seja positivo quando diluído 10 vezes (amostras de soro) ou 250 vezes (amostras de leite) mais do que uma diluição obtida a partir de amostras agregadas. Em provas em que as amostras (soro e leite) sejam examinadas individualmente, o soro E05, diluído à razão de 1 para 10 (para o soro negativo) ou à razão de 1 para 250 (para o leite negativo), deve dar uma reacção positiva quando for examinado na mesma diluição que é utilizada para os ensaios individuais. Os organismos públicos indicados no ponto 2 da parte A são responsáveis pelo controlo da qualidade do método Elisa, nomeadamente para determinar, para cada lote de produção, o número de amostras a agregar, com base na contagem obtida com o soro E05.
3. Condições de utilização do teste Elisa para a pesquisa de leucose bovina enzoótica
a) O método Elisa pode ser utilizado em amostras de leite ou de soro.
b) Se os testes Elisa forem utilizados para efeitos de certificação, em conformidade com o disposto no n.o 2, alínea c), do artigo 6.o, ou para a determinação e manutenção do estatuto dos efectivos, em conformidade com o disposto no capítulo I do anexo D, a agregação de amostras de soro ou de leite deve efectuar-se de molde a que as amostras colhidas para exame possam ser indubitavelmente relacionadas com os animais incluídos no agregado. Os testes de confirmação devem ser efectuados em amostras colhidas de animais específicos.
c) Sempre que o teste Elisa for utilizado numa amostra de leite a granel, esta amostra deve ter sido retirada de uma colheita de leite proveniente de um efectivo com pelo menos 30 % das vacas leiteiras em lactação. Os testes de confirmação devem ser efectuados em amostras de soro ou leite colhidas de animais específicos.
▼M42
ANEXO E (I)
a) Doenças dos bovinos
— Peripneumonia contagiosa dos bovinos
— Leucose bovina enzoótica
b) Doenças dos suínos
— Doença vesiculosa do suíno
ANEXO E (II)
— Rinotraqueíte infecciosa dos bovinos
— Infecção por Brucella suis
— Gastroenterite transmissível
▼M61
ANEXO F
MODELO 1
Certificado sanitário para bovinos de reprodução/produção/abate
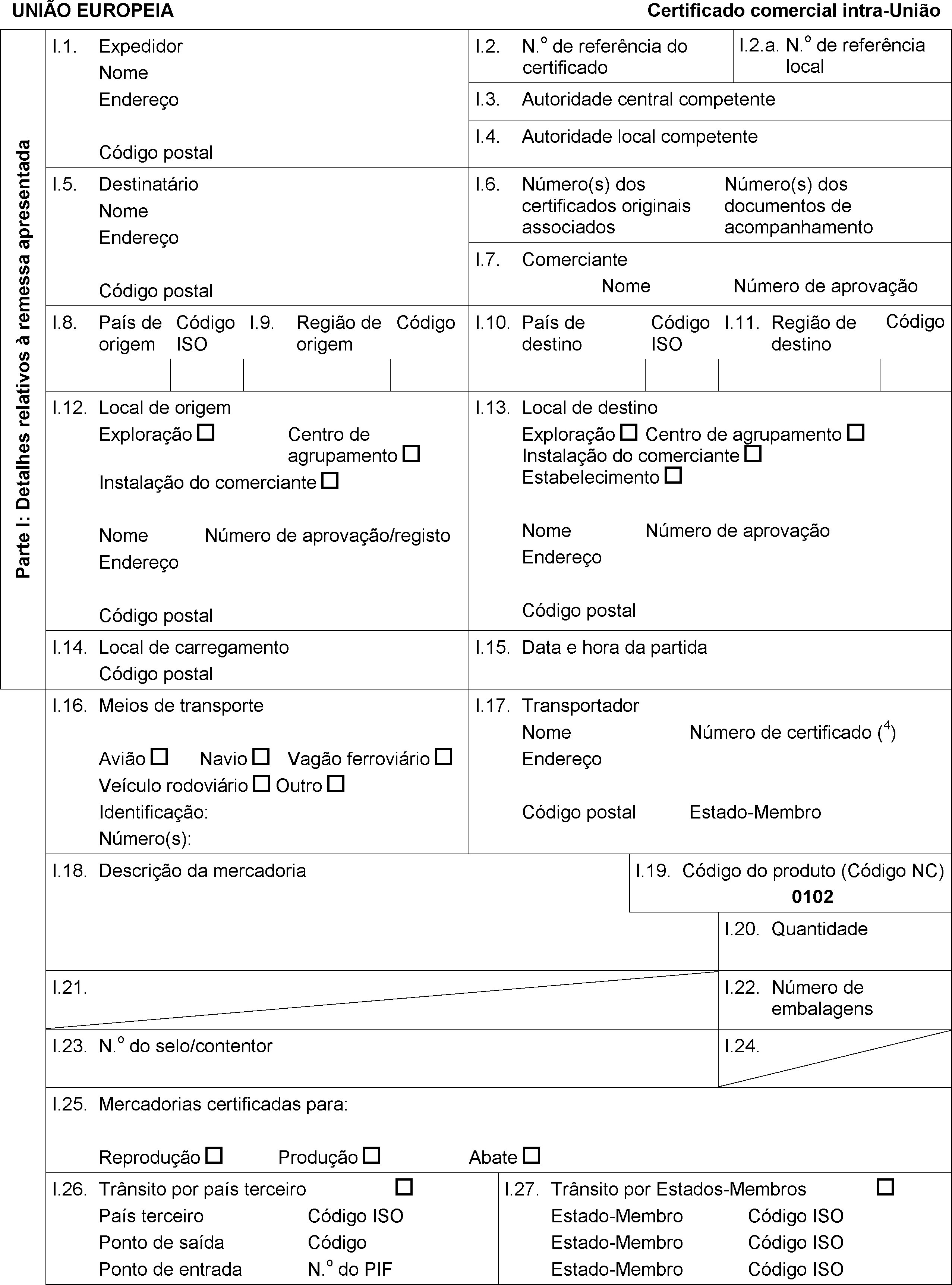





MODELO 2
Certificado sanitário para suínos de reprodução/produção/abate