EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32009D0365
2009/365/EC: Commission Decision of 28 April 2009 authorising the placing on the market of lycopene from Blakeslea trispora as a novel food ingredient under Regulation (EC) No 258/97 of the European Parliament and of the Council (notified under document number C(2009) 3039)
2009/365/EB: 2009 m. balandžio 28 d. Komisijos sprendimas, kuriuo leidžiama tiekti rinkai likopeną iš Blakeslea trispora kaip naują maisto sudedamąją dalį pagal Europos Parlamento ir Tarybos reglamentą (EB) Nr. 258/97 (pranešta dokumentu Nr. C(2009) 3039)
2009/365/EB: 2009 m. balandžio 28 d. Komisijos sprendimas, kuriuo leidžiama tiekti rinkai likopeną iš Blakeslea trispora kaip naują maisto sudedamąją dalį pagal Europos Parlamento ir Tarybos reglamentą (EB) Nr. 258/97 (pranešta dokumentu Nr. C(2009) 3039)
OJ L 111, 5.5.2009, p. 31–34
(BG, ES, CS, DA, DE, ET, EL, EN, FR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
 In force
In force
|
5.5.2009 |
LT |
Europos Sąjungos oficialusis leidinys |
L 111/31 |
KOMISIJOS SPRENDIMAS
2009 m. balandžio 28 d.
kuriuo leidžiama tiekti rinkai likopeną iš Blakeslea trispora kaip naują maisto sudedamąją dalį pagal Europos Parlamento ir Tarybos reglamentą (EB) Nr. 258/97
(pranešta dokumentu Nr. C(2009) 3039)
(Tekstas autentiškas tik ispanų kalba)
(2009/365/EB)
EUROPOS BENDRIJŲ KOMISIJA,
atsižvelgdama į Europos Bendrijos steigimo sutartį,
atsižvelgdama į 1997 m. sausio 27 d. Europos Parlamento ir Tarybos reglamentą (EB) Nr. 258/97 dėl naujų maisto produktų ir naujų maisto komponentų (1), ypač į jo 7 straipsnį,
kadangi:
|
(1) |
2007 m. rugpjūčio 30 d. bendrovė Vitatene kompetentingoms Jungtinės Karalystės institucijoms pateikė prašymą leisti tiekti rinkai likopeną iš Blakeslea trispora kaip naują maisto sudedamąją dalį. 2007 m. spalio 17 d. kompetentinga Jungtinės Karalystės maisto vertinimo tarnyba pateikė pirminio vertinimo ataskaitą. Ataskaitoje padaryta išvada, kad atsižvelgiant į kitas nagrinėjamas su likopenu susijusias paraiškas, reikalingas papildomas vertinimas norint užtikrinti, kad leidimai naudoti įvairių rūšių likopenus kaip naujas maisto sudedamąsias dalis būtų suteikti tomis pačiomis sąlygomis. |
|
(2) |
2008 m. vasario 11 d. Komisija pirminio vertinimo ataskaitą išsiuntė visoms valstybėms narėms. |
|
(3) |
2008 m. konsultuotasi su Europos maisto saugos tarnyba, o 2008 m. gruodžio 4 d. ši pateikė savo nuomonę. |
|
(4) |
EMST savo nuomonėje padarė tokią išvadą: kadangi likopenas gali pakisti dėl oksidacijos, jis turi būti gaminamas kaip suspensijos valgomuosiuose aliejuose, tiesiogiai supresuoti arba disperguojantys vandenyje milteliai. Turi būti užtikrinta pakankama antioksidacinė apsauga. |
|
(5) |
EMST taip pat padarė išvadą, kad nors vidutinis vartotojas likopeno paprastai suvartos mažiau nei leistina paros dozė (LPD), kai kurie vartotojai gali jo suvartoti daugiau nei LPD. Todėl taip pat būtų tikslinga kelerius metus po leidimo suteikimo kaupti vartojimo duomenis, kad būtų galima peržiūrėti šį leidimą atsižvelgiant į papildomą informaciją apie likopeno saugumą ir jo suvartojimą. Visų pirma reikėtų kaupti duomenis apie likopeno kiekį pusryčių dribsniuose. Tačiau šio sprendimo reikalavimas taikomas tik jei likopenas naudojamas kaip nauja maisto sudedamoji dalis, o ne kaip maisto dažiklis; pastarajam taikoma 1988 m. gruodžio 21 d. Tarybos direktyva 89/107/EEB dėl valstybių narių įstatymų, reglamentuojančių maisto priedus, kuriuos leidžiama naudoti žmonėms vartoti skirtuose maisto produktuose, suderinimo (2). |
|
(6) |
Remiantis moksliniu vertinimu nustatyta, kad likopenas iš Blakeslea trispora atitinka Reglamento (EB) Nr. 258/97 3 straipsnio 1 dalyje nustatytus kriterijus. |
|
(7) |
Bendrovė Vitatene sutiko, kad Komisijos sprendimas 2006/721/EB (3) būtų panaikintas. |
|
(8) |
Šiame sprendime numatytos priemonės atitinka Maisto grandinės ir gyvūnų sveikatos nuolatinio komiteto nuomonę, |
PRIĖMĖ ŠĮ SPRENDIMĄ:
1 straipsnis
Bendrijos rinkai galima tiekti I priede nurodytą likopeną iš Blakeslea trispora (toliau – produktas) kaip naują maisto sudedamąją dalį naudoti II priede išvardytuose maisto produktuose.
2 straipsnis
Ženklinant maisto produktus, kuriuose yra naujos maisto sudedamosios dalies, kurią šiuo sprendimu leidžiama tiekti rinkai, nurodomas jos pavadinimas „likopenas“.
3 straipsnis
Bendrovė Vitatene, tiekdama produktą rinkai, parengia stebėsenos programą. Į šią programą įtraukiama informacija apie maisto produktuose naudojamus likopeno kiekius, kaip apibrėžta III priede.
Surinkti duomenys pateikiami Komisijai ir valstybėms narėms. Atsižvelgiant į naują informaciją ir į EMST ataskaitą, ne vėliau kaip 2014 m. likopeno kaip maisto sudedamosios dalies naudojimas turėtų būti peržiūrėtas.
4 straipsnis
Sprendimas 2006/721/EB panaikinamas.
5 straipsnis
Šis sprendimas skirtas Vitatene S.A.U. Avda. Antibióticos 59–61, E-24009 León, Ispanija.
Priimta Briuselyje, 2009 m. balandžio 28 d.
Komisijos vardu
Androulla VASSILIOU
Komisijos narė
(2) OL L 40, 1989 2 11, p. 27.
(3) OL L 296, 2006 10 26, p. 13.
I PRIEDAS
Likopeno iš Blakeslea trispora specifikacijos
APRAŠYMAS
Išgrynintasis likopenas iš Blakeslea trispora sudarytas iš ≥ 95 % likopeno ir ≤ 5 % kitų karotenoidų. Likopeno forma – milteliai atitinkamoje rišamojoje medžiagoje arba aliejinė dispersija. Spalva – tamsiai raudona arba rausvai violetinė. Turi būti užtikrinta antioksidacinė apsauga.
SPECIFIKACIJA
|
Cheminis pavadinimas |
: |
likopenas |
|
C.A.S. numeris |
: |
502–65–8 (visas trans-likopenas) |
|
Cheminė formulė |
: |
C40H56 |
|
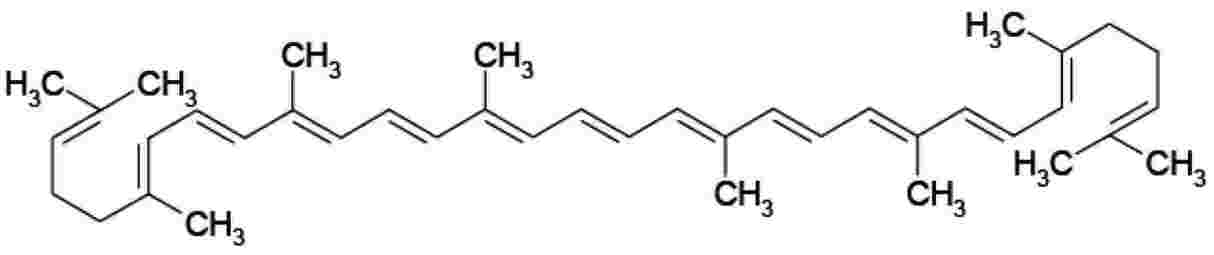
Struktūrinė formulė |
: |
|
|
Formulinė masė |
: |
536,85 |
II PRIEDAS
Maisto produktų, į kuriuos galima dėti likopeno iš Blakeslea trispora, sąrašas
|
Maisto kategorija |
Didžiausias leistinas likopeno kiekis |
|
Iš vaisių ir (arba) daržovių sulčių pagaminti gėrimai (įskaitant koncentratus) |
2,5 mg/100 g |
|
Gėrimai, skirti intensyviam raumenų darbui, ypač tinkantys sportininkams |
2,5 mg/100 g |
|
Maisto produktai, skirti vartoti laikantis sumažinto energijos kiekio dietų, kurių paskirtis – sumažinti svorį |
8 mg/pakaitiniame maiste |
|
Pusryčių dribsniai |
5 mg/100 g |
|
Riebalai ir padažai |
10 mg/100 g |
|
Sriubos, išskyrus pomidorų |
1 mg/100 g |
|
Duona (įskaitant traškią duoną) |
3 mg/100 g |
|
Specialios medicininės paskirties dietiniai maisto produktai |
Laikantis tam tikrų mitybos reikalavimų |
|
Maisto papildai |
15 mg paros dozėje, rekomenduojamoje gamintojo |
III PRIEDAS
Likopeno iš Blakeslea trispora stebėsena po leidimo suteikimo
KAUPTINA INFORMACIJA
Likopeno iš Blakeslea tripsora, kurį Vitatene tiekė savo klientams Europos Sąjungos rinkai tiektiniems galutiniams produktams gaminti, kiekis.
Produktų, kuriuose yra likopeno iš Blakeslea tripsora, teikimo rinkai paieškos duomenų bazėse rezultatai pagal valstybes nares, įskaitant kiekvieno pateikto maisto produkto papildymo lygį ir porcijos dydį.
INFORMACIJOS TEIKIMAS
2009 – 2012 m. informacija Europos Komisijai teikiama kasmet. Pirmiausiai 2010 m. spalio 31 d. pateikiama 2009 m. liepos 1 d. – 2010 m. birželio 30 d. laikotarpio informacija; atitinkamai kasmet teikiama kitų dvejų metų informacija tuo pačiu metiniu laikotarpiu.
PAPILDOMA INFORMACIJA
Jei reikia ir jei tokios informacijos yra, Vitatene turėtų pateikti tokią pat informaciją apie likopeno, naudojamo kaip maisto dažiklis, dozes.
Vitatene teikia naują mokslinę informaciją (jei tokios yra) dėl maksimalios saugios likopeno dozės persvarstymo.
LIKOPENO SUVARTOJIMO DOZĖS VERTINIMAS
Remdamasi sukaupta ir pateikta pirmiau nurodyta informacija Vitatene iš naujo įvertina likopeno suvartojimą.
PERŽIŪRA
2013 m. Komisija konsultuosis su EMST dėl pramonės atstovų pateiktos informacijos peržiūros.