EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 02005R2074-20190101
Commission Regulation (EC) No 2074/2005 of 5 December 2005 laying down implementing measures for certain products under Regulation (EC) No 853/2004 of the European Parliament and of the Council and for the organisation of official controls under Regulation (EC) No 854/2004 of the European Parliament and of the Council and Regulation (EC) No 882/2004 of the European Parliament and of the Council, derogating from Regulation (EC) No 852/2004 of the European Parliament and of the Council and amending Regulations (EC) No 853/2004 and (EC) No 854/2004 (Text with EEA relevance)Text with EEA relevance
Consolidated text: A Bizottság 2074/2005/EK rendelete (2005. december 5.) a 853/2004/EK európai parlamenti és tanácsi rendelet szerinti bizonyos termékekre és a 854/2004/EK és a 882/2004/EK európai parlamenti és tanácsi rendelet szerinti hatósági ellenőrzések megszervezésére vonatkozó végrehajtási intézkedések megállapításáról, a 852/2004/EK európai parlamenti és tanácsi rendelettől való eltérésről, valamint a 853/2004/EK és 854/2004/EK rendelet módosításáról (EGT vonatkozású szöveg)EGT-vonatkozású szöveg
A Bizottság 2074/2005/EK rendelete (2005. december 5.) a 853/2004/EK európai parlamenti és tanácsi rendelet szerinti bizonyos termékekre és a 854/2004/EK és a 882/2004/EK európai parlamenti és tanácsi rendelet szerinti hatósági ellenőrzések megszervezésére vonatkozó végrehajtási intézkedések megállapításáról, a 852/2004/EK európai parlamenti és tanácsi rendelettől való eltérésről, valamint a 853/2004/EK és 854/2004/EK rendelet módosításáról (EGT vonatkozású szöveg)EGT-vonatkozású szöveg
02005R2074 — HU — 01.01.2019 — 012.001
Ez a dokumentum kizárólag tájékoztató jellegű és nem vált ki joghatást. Az EU intézményei semmiféle felelősséget nem vállalnak a tartalmáért. A jogi aktusoknak – ideértve azok bevezető hivatkozásait és preambulumbekezdéseit is – az Európai Unió Hivatalos Lapjában közzétett és az EUR-Lex portálon megtalálható változatai tekintendők hitelesnek. Az említett hivatalos szövegváltozatok közvetlenül elérhetők az ebben a dokumentumban elhelyezett linkeken keresztül
|
A BIZOTTSÁG 2074/2005/EK rendelete (2005. december 5.) a 853/2004/EK európai parlamenti és tanácsi rendelet szerinti bizonyos termékekre és a 854/2004/EK és a 882/2004/EK európai parlamenti és tanácsi rendelet szerinti hatósági ellenőrzések megszervezésére vonatkozó végrehajtási intézkedések megállapításáról, a 852/2004/EK európai parlamenti és tanácsi rendelettől való eltérésről, valamint a 853/2004/EK és 854/2004/EK rendelet módosításáról (HL L 338, 2005.12.22., 27. o) |
Módosította:
|
|
|
Hivatalos Lap |
||
|
Szám |
Oldal |
Dátum |
||
|
L 320 |
13 |
18.11.2006 |
||
|
L 281 |
12 |
25.10.2007 |
||
|
L 277 |
18 |
18.10.2008 |
||
|
L 337 |
31 |
16.12.2008 |
||
|
L 6 |
3 |
11.1.2011 |
||
|
A BIZOTTSÁG 809/2011/EU VÉGREHAJTÁSI RENDELETE (2011. augusztus 11.) |
L 207 |
1 |
12.8.2011 |
|
|
A BIZOTTSÁG 1012/2012/EU VÉGREHAJTÁSI RENDELETE (2012. november 5.) |
L 306 |
1 |
6.11.2012 |
|
|
L 69 |
95 |
8.3.2014 |
||
|
A BIZOTTSÁG (EU) 2015/2295 VÉGREHAJTÁSI RENDELETE (2015. december 9.) |
L 324 |
5 |
10.12.2015 |
|
|
A BIZOTTSÁG (EU) 2016/759 VÉGREHAJTÁSI RENDELETE (2016. április 28.) |
L 126 |
13 |
14.5.2016 |
|
|
L 281 |
21 |
31.10.2017 |
||
|
L 285 |
8 |
1.11.2017 |
||
Helyesbítette:
A BIZOTTSÁG 2074/2005/EK rendelete
(2005. december 5.)
a 853/2004/EK európai parlamenti és tanácsi rendelet szerinti bizonyos termékekre és a 854/2004/EK és a 882/2004/EK európai parlamenti és tanácsi rendelet szerinti hatósági ellenőrzések megszervezésére vonatkozó végrehajtási intézkedések megállapításáról, a 852/2004/EK európai parlamenti és tanácsi rendelettől való eltérésről, valamint a 853/2004/EK és 854/2004/EK rendelet módosításáról
(EGT vonatkozású szöveg)
1. cikk
A 853/2004/EK és 854/2004/EK rendelet alkalmazásában az élelmiszerláncra vonatkozó információkkal kapcsolatos követelmények
A 853/2004/EK rendelet II. mellékletének III. szakaszában és a 854/2004/EK rendelet I. melléklete I. szakasza II. fejezetének A. pontjában említett élelmiszerláncra vonatkozó információkkal kapcsolatos követelményeket e rendelet I. melléklete állapítja meg.
2. cikk
A 853/2004/EK és 854/2004/EK rendelet alkalmazásában a halászati termékekre vonatkozó követelmények
A 853/2004/EK rendelet 11. cikkének (9) bekezdésében, valamint a 854/2004/EK rendelet 18. cikkének (14) és (15) bekezdésében említett halászati termékekre vonatkozó követelményeket e rendelet II. melléklete állapítja meg.
3. cikk
A 853/2004/EK és 854/2004/EK rendeletek alkalmazásában a tengeri biotoxinok elismert vizsgálati módszerei
A 853/2004/EK rendelet 11. cikkének (4) bekezdésében, valamint a 854/2004/EK rendelet 18. cikke (13) bekezdésének a) pontjában említett, a tengeri biotoxinok kimutatása tekintetében elismert vizsgálati módszereket e rendelet III. melléklete állapítja meg.
4. cikk
A 853/2004/EK rendelet alkalmazásában a csontokról mechanikusan lefejtett hús kalciumtartalma
A 853/2004/EK rendelet 11. cikkének (2) bekezdésében említett, a csontokról mechanikusan lefejtett hús kalciumtartalmát e rendelet IV. melléklete állapítja meg.
5. cikk
Létesítmények jegyzéke a 882/2004/EK rendelet alkalmazásában
A 882/2004/EK rendelet 31. cikke (2) bekezdésének f) pontjában említett létesítmények jegyzékére vonatkozó követelményeket e rendelet V. melléklete állapítja meg.
6. cikk
A 853/2004/EK és a 854/2004/EK rendelet alkalmazásában az egyes állati eredetű termékek behozatalára vonatkozó egészségügyi bizonyítványminták és okmányminták
1. A 853/2004/EK rendelet 6. cikke (1) bekezdésének d) pontjában említett, az e rendelet VI. mellékletében felsorolt állati eredetű termékek behozatalára vonatkozó egészségügyi bizonyítványmintákat és okmánymintákat az említett melléklet állapítja meg.
2. A kapitány által aláírandó okmány mintáját, amely a 854/2004/EK rendelet 15. cikkének (3) bekezdése értelmében, amennyiben a halászati termékek behozatala közvetlenül a fagyasztó hajóról történik, az említett rendelet 14. cikkében meghatározott okmány helyébe léphet, e rendelet VI. melléklete állapítja meg.
6a. cikk
Nyers- és hőkezelt tejre vonatkozó vizsgálati módszerek
A 853/2004/EK rendelet III. melléklete IX. szakasza I. fejezetének III. pontjában megállapított határértékeknek való megfelelés ellenőrzése és az ugyanazon rendelet III. melléklete IX. szakasza II. fejezetének II. pontjában említett, a tejtermékekre vonatkozó pasztőrözési eljárás megfelelő alkalmazásának biztosítása érdekében az e rendelet VIa. mellékletében megállapított vizsgálati módszereket a hatáskörrel rendelkező hatóságok és szükség szerint az élelmiszeripari vállalkozók alkalmazhatják.
6b. cikk
A húsvizsgálattal kapcsolatos hatósági ellenőrzésekre vonatkozó követelmények a 854/2004/EK rendelet alkalmazásában
A húsvizsgálattal kapcsolatos hatósági ellenőrzésekre vonatkozó követelményeket a VI. b. melléklet tartalmazza.
6c. cikk
A valamely tagállam lobogója alatt közlekedő halászhajók által kifogott és az Unió területére harmadik országokon keresztül tárolással vagy anélkül beszállított halászati termékek hatósági ellenőrzésére vonatkozó követelmények
(1) A valamely tagállam lobogója alatt közlekedő halászhajók által kifogott, az Unióba más szállítási eszközzel való behozatalt megelőzően egy harmadik országban tárolással vagy anélkül kirakodott, emberi fogyasztásra szánt halászati termékek mellé az adott harmadik országbeli illetékes hatóság által kibocsátott, a VI. melléklet VIII. függelékében meghatározott egészségügyi bizonyítványmintának megfelelően kitöltött egészségügyi bizonyítványt kell csatolni.
(2) Az átadás helyszínéül szolgáló harmadik országnak szerepelnie kell a 854/2004/EK rendelet 11. cikke (1) bekezdésében említett jegyzéken.
(3) Amennyiben az első bekezdésben említett halászati termékeket az ugyanazon bekezdésben említett harmadik országban lévő tárolólétesítményben rakodják ki vagy oda szállítják, a tárolólétesítménynek szerepelnie kell a 854/2004/EK rendelet 12. cikkében említett jegyzéken.
(4) Amennyiben az első bekezdésben említett halászati termékeket harmadik ország lobogója alatt hajózó halászhajóra rakodták be, a harmadik országnak szerepelnie kell a 854/2004/EK rendelet 11 cikke (1) bekezdésében említett jegyzéken, a halászhajónak pedig a 854/2004/EK rendelet 12. cikkében említett jegyzéken.
A korábban konténeres halászati termékeket szállító konténerhajókra nem vonatkoznak e követelmények.
7. cikk
Eltérés a 852/2004/EK rendelettől a hagyományos jellemzőkkel rendelkező élelmiszerek tekintetében
(1) E rendelet alkalmazásában a „hagyományos jellemzőkkel rendelkező élelmiszerek” olyan élelmiszerek, amelyek(et) abban a tagállamban, ahol azokat hagyományosan gyártják:
a) hagyományos termékekként történelmileg elismertek; vagy
b) a hagyományos eljárással kapcsolatos kodifikált vagy nyilvántartásba vett technikai referenciáknak megfelelően vagy a hagyományos előállítási módszereknek megfelelően gyártottak; vagy
c) hagyományos élelmiszer-ipari termékekként a közösségi, nemzeti, regionális vagy helyi jogszabályok oltalma alatt állnak.
(2) A tagállamok a hagyományos jellemzőkkel rendelkező élelmiszereket gyártó létesítményeknek egyéni vagy általános eltéréseket nyújthatnak az alábbiakban megállapított követelmények alól:
a) a 852/2004/EK rendelet II. melléklete II. fejezetének 1. pontja, az olyan helyiségek tekintetében, ahol az ilyen termékek a jellemzőik részleges kifejlődéséhez szükséges környezetnek vannak kitéve. Az ilyen helyiségek különösen nem sima, vízhatlan, nedvszívó vagy nem a korróziónak ellenálló anyagból készült falakból, mennyezetből és ajtókból, valamint természetes földtani falakból, mennyezetből és padlóból állnak;
b) a 852/2004/EK rendelet II. melléklete II. fejezetének 1. f) pontja, és II. melléklete V. fejezetének 1. pontja az anyagok olyan típusa tekintetében, amelyekből kifejezetten az e termékek előkészítéséhez, csomagolásához és gyűjtőcsomagolásához használt eszközök és felszerelések készülnek.
Az a) pontban említett üzemek tisztítására és fertőtlenítésére vonatkozó intézkedéseket, valamint ezek elvégzésének gyakoriságát a tevékenységhez kell igazítani a különleges környezeti flórájuk figyelembevétele érdekében.
A b) pontban említett eszközöket és felszereléseket mindenkor kielégítő higiéniai állapotban tartják, és rendszeresen tisztítják és fertőtlenítik.
(3) A (2) bekezdésben említett eltéréseket nyújtó tagállamok erről a Bizottságot és a többi tagállamot az egyéni vagy általános eltérések nyújtásától számított 12 hónapon belül értesítik. Minden értesítés:
a) tartalmazza a kiigazított követelmények rövid leírását;
b) leírja az érintett élelmiszereket és létesítményeket; és
c) megad minden más, vonatkozó információt.
8. cikk
A 853/2004/EK rendelet módosításai
A 853/2004/EK rendelet II. és III. melléklete e rendelet VII. mellékletével összhangban módosul.
9. cikk
A 854/2004/EK rendelet módosításai
A 854/2004/EK rendelet I., II. és III. melléklete e rendelet VIII. mellékletével összhangban módosul.
10. cikk
Hatálybalépés és alkalmazandóság
Ez a rendelet az Európai Unió Hivatalos Lapjában való kihirdetését követő huszadik napon lép hatályba.
Ezt a rendeletet 2006. január 1-jétől kell alkalmazni, kivéve az V. melléklet II. és III. fejezetét, amelyeket 2007. január 1-jétől kell alkalmazni.
Ez a rendelet teljes egészében kötelező és közvetlenül alkalmazandó valamennyi tagállamban.
I. MELLÉKLET
AZ ÉLELMISZERLÁNCRA VONATKOZÓ INFORMÁCIÓK
I. SZAKASZ
AZ ÉLELMISZER-IPARI VÁLLALKOZÓK KÖTELEZETTSÉGEI
A vágásra feladott állatokat tartó élelmiszer-ipari vállalkozók biztosítják, hogy a 853/2004/EK rendeletben említett, élelmiszerláncra vonatkozó információk megfelelően szerepelnek a feladott állatokkal kapcsolatos dokumentációban oly módon, hogy azokhoz az érintett vágóhíd üzemeltetője hozzáférhessen.
II. SZAKASZ
A HATÁSKÖRREL RENDELKEZŐ HATÓSÁGOK KÖTELEZETTSÉGEI
I. FEJEZET
AZ ÉLELMISZERLÁNCRA VONATKOZÓ INFORMÁCIÓ NYÚJTÁSA
1. A feladás helye szerinti, hatáskörrel rendelkező hatóság tájékoztatja a feladó élelmiszer-ipari vállalkozót a 853/2004/EK rendelet II. mellékletének III. szakaszával összhangban a vágóhíd számára nyújtandó, az élelmiszerláncra vonatkozó információ minimális elemeiről.
2.
A hatáskörrel rendelkező hatóság a vágás helyén igazolja, hogy:
a) az élelmiszerláncra vonatkozó információ következetesen és hatékonyan áramlik a feladást megelőzően az állatokat nevelő vagy tartó élelmiszer-ipari vállalkozó és a vágóhíd üzemeltetője között;
b) az élelmiszerláncra vonatkozó információ érvényes és megbízható;
c) adott esetben a vonatkozó információval kapcsolatban a gazdaság felé visszacsatolást nyújtanak.
3. Amennyiben más tagállamba küldenek állatokat levágásra, a feladás helye szerinti és a vágás helye szerinti, hatáskörrel rendelkező hatóságok együttműködnek annak biztosítása érdekében, hogy a feladó élelmiszer-ipari vállalkozó által nyújtott információhoz a fogadó vágóhíd üzemeltetője könnyen hozzáférjen.
II. FEJEZET
VISSZACSATOLÁS A SZÁRMAZÁSI GAZDASÁG FELÉ
1. A hatósági állatorvos használhatja az I. függelékben megállapított okmánymintát azon vonatkozó vizsgálati eredmények tekintetében, amelyeket a 854/2004/EK rendelet I. melléklete II. szakaszának I. fejezetével összhangban azzal a gazdasággal kell közölni, ahol az állatokat az ugyanabban a tagállamban történő levágás előtt nevelték.
2. A hatáskörrel rendelkező hatóság felelős a vonatkozó vizsgálati eredmények közléséért azokban az esetekben, amikor az állatokat egy másik tagállamban lévő gazdaságban nevelték, és a hatóságnak a függelékben megállapított okmányminta egy változatát kell használnia mind a feladó, mind a fogadó ország nyelvén.
Függelék az I. melléklethez
OKMÁNYMINTA
|
1. |
Azonosítási adatok |
||
|
|
1.1. |
származási gazdaság (pl. tulajdonos vagy vezető) |
|
|
|
|
név/szám |
|
|
|
|
teljes cím |
|
|
|
|
telefonszám |
|
|
|
1.2. |
azonosítószámok (külön jegyzéket kell mellékelni) |
|
|
|
|
az állatok összlétszáma (fajonként) |
|
|
|
|
azonosítási problémák (ha vannak) |
|
|
|
1.3. |
állomány/ketrec azonosítás (adott esetben) |
|
|
|
1.4. |
állatfajok |
|
|
|
1.5. |
egészségügyi bizonyítvány referenciaszáma |
|
|
2. |
Ante mortem megállapítások |
||
|
|
2.1. |
jóllét |
|
|
|
|
az érintett állatok száma |
|
|
|
|
típus/osztály/kor |
|
|
|
|
vizsgálatok (pl. farokharapás) |
|
|
|
2.2. |
az állatokat szennyezetten szállították |
|
|
|
2.3. |
klinikai diagnózis (betegség) |
|
|
|
|
az érintett állatok száma |
|
|
|
|
típus/osztály/kor |
|
|
|
|
megfigyelések |
|
|
|
|
vizsgálat időpontja |
|
|
|
2.4. |
laboratóriumi eredmények () |
|
|
3. |
Post mortem megállapítások |
||
|
|
3.1. |
(makroszkópikus) megállapítások |
|
|
|
|
az érintett állatok száma |
|
|
|
|
típus/osztály/kor |
|
|
|
|
az érintett állat(ok) szerve vagy része |
|
|
|
|
a levágás időpontja |
|
|
|
3.2. |
betegség (kódok használhatók ()) |
|
|
|
|
az érintett állatok száma |
|
|
|
|
típus/osztály/kor |
|
|
|
|
az érintett állat(ok) szerve vagy része |
|
|
|
|
részlegesen vagy teljesen visszautasított állati testek (indokolja) |
|
|
|
|
Levágás időpontja |
|
|
|
3.3. |
résultats de laboratoirelaboratóriumi eredmények () |
|
|
|
3.4. |
más eredmények (pl. paraziták, idegen testek stb.) |
|
|
|
3.5. |
jólléti megállapítások (pl. törött láb) |
|
|
4. |
Kiegészítő információk |
||
|
5. |
Kapcsolattartási adatok |
||
|
|
5.1. |
vágóhíd (jóváhagyási szám) |
|
|
|
|
név |
|
|
|
|
teljes cím |
|
|
|
|
telefonszám |
|
|
|
5.2 |
elektronikus cím, ha van |
|
|
6. |
Hatósági állatorvos (név nyomtatottan) |
||
|
|
|
aláírás és pecsét |
|
|
7. |
Dátum |
||
|
8. |
A nyomtatványhoz csatolt oldalak száma: |
||
|
(1) Mikrobiológiai, kémiai, szerológiai stb. (írja be az eredményeket a mellékletek szerint). (2) A hatáskörrel rendelkező hatóságok a következő kódokat használhatják: A kód az OIE által jegyzékbe vett betegségek esetében; B100 és B200 kód jólléti kérdésekben (a 854/2004/EK rendelet I. melléklete I. szakasza II. fejezetének C. pontja) és C100–C290 kódok a húsra vonatkozó határozatok tekintetében (854/2004/EK rendelet I. melléklete II. szakasza V. fejezetének 1. a)–u) pontja). A kódrendszer szükség esetén további albontásokat tartalmazhat (pl. C141 egy közepesen általános betegség esetében, C142 egy súlyosabb betegség esetében stb.). Ha kódokat használnak, azoknak a jelentésük megfelelő magyarázatával együtt elérhetőknek kell lenniük az élelmiszer-ipari vállalkozó számára. (3) Mikrobiológiai, kémiai, szerológiai stb. (írja be az eredményeket a mellékletek szerint). |
|||
II. MELLÉKLET
HALÁSZATI TERMÉKEK
I. SZAKASZ
AZ ÉLELMISZER-IPARI VÁLLALKOZÓK KÖTELEZETTSÉGEI
Ez a szakasz megállapítja a parazitáknak a halászati termékekben történő kimutatására irányuló szemrevételezéses vizsgálatokkal kapcsolatos részletes szabályokat.
I. FEJEZET
FOGALOMMEGHATÁROZÁSOK
1. „Látható parazita”: olyan parazita, vagy paraziták csoportja, ami méret, szín vagy mintázat alapján egyértelműen megkülönböztethető a halszövetektől.
2. „Szemrevételezéssel történő vizsgálat”: a hal vagy halászati termék roncsolásmentes, optikai nagyítóeszközök nélküli, jó látási viszonyok közötti megvizsgálása az emberi látás segítségével, beleértve – amennyiben szükséges – a lámpázást is.
3. „Lámpázás”: a lepényhal vagy halfilé esetében a paraziták kimutatása érdekében a halnak egy elsötétített szobában fény felé történő tartása.
II. FEJEZET
A SZEMREVÉTELEZÉSSEL TÖRTÉNŐ VIZSGÁLAT
1. A szemrevételezéssel történő vizsgálatot reprezentatív számú mintán kell elvégezni. A parti létesítményekért felelős személyek és az üzemhajó fedélzetén dolgozó szakemberek meghatározzák a vizsgálatok nagyságrendjét és gyakoriságát, figyelembe véve a halászati termékek jellegét, származási helyét és felhasználását. Az előállítás során a kizsigerelt hal szemrevételezéssel történő vizsgálatát szakemberek végzik a hasüregen és az emberi fogyasztásra szánt májon és halikrán. Az alkalmazott kizsigerelési módszer szerint a szemrevételezéssel történő vizsgálatot az alábbiak szerint végzik:
a) kézi kizsigerelés esetén a munkát végző személy folyamatosan a zsigerelés és a mosás során;
b) gépi kizsigerelés esetén a minimum tíz halból álló tételekből vett reprezentatív számú mintából való mintavétellel.
2. A halfilék, illetve halszeletek szemrevételezéssel történő vizsgálatát szakemberek végzik a hús filézését vagy szeletelését követő tisztogatása során. Ha darabonkénti vizsgálat nem lehetséges a filék nagysága vagy a filézési műveletek következtében, akkor mintavételi tervet kell készíteni, és a hatáskörrel rendelkező hatóság számára hozzáférhetővé tenni a 853/2004/EK rendelet III. melléklete VIII. szakasza II. fejezetének 4. pontjával összhangban. Amennyiben technikai szempontból szükséges a filék lámpázása, azt a mintavételi tervnek tartalmaznia kell.
II. SZAKASZ
A HATÁSKÖRREL RENDELKEZŐ HATÓSÁGOK KÖTELEZETTSÉGEI
I. FEJEZET
A HALÁSZATI TERMÉKEK EGYES KATEGÓRIÁIRA VONATKOZÓ ÖSSZES ILLÉKONY NITROGÉNBÁZIS (TVB-N) HATÁRÉRTÉKEI ÉS AZ ALKALMAZANDÓ VIZSGÁLATI MÓDSZEREK
1. A feldolgozatlan halászati termékeket emberi fogyasztásra alkalmatlannak kell tekinteni, amennyiben az érzékszervi vizsgálat kétségeket támaszt frissességükkel kapcsolatban, a kémiai ellenőrző vizsgálatok pedig az alábbi TVB-N-határértékek túllépésére utalnak:
a) 25 milligramm nitrogén/100 gramm hús a II. fejezet 1. pontjában említett fajokra vonatkozóan;
b) 30 milligramm nitrogén/100 gramm hús a II. fejezet 2. pontjában említett fajokra vonatkozóan;
c) 35 milligramm nitrogén/100 gramm hús a II. fejezet 3. pontjában említett fajokra vonatkozóan;
d) 60 milligramm nitrogén/100 g a 853/2004/EK rendelet III. melléklete VIII. szakaszának IV. fejezete B.1. részének második albekezdésében említett, emberi felhasználásra szánt halolaj közvetlen elkészítésére használt, nem darabolt halászati termékekre vonatkozóan; amennyiben azonban az alapanyag megfelel az említett fejezet B.1. része a), b) és c) pontja előírásainak, akkor a tagállamok – a különleges közösségi jogszabályok megállapításáig – bizonyos fajok esetében magasabb határértékeket is megállapíthatnak.
A TVB-N-határértékek ellenőrző vizsgálatához használandó referencia-módszer a III. fejezetben szereplő, perklórsavval proteinmentesített kivonat lepárlását magában foglaló módszer.
2. Az 1. pontban említett lepárlást olyan készülékkel kell elvégezni, amely megfelel a IV. fejezetben található ábra alapelveinek.
3. A TVB-N-határérték ellenőrző vizsgálatához használható rutinmódszerek a következők:
— a Conway és Byrne által leírt mikrodiffúziós módszer (1933),
— az Antonacopoulos által leírt közvetlen lepárlási módszer (1968),
— triklór-ecetsavval proteinmentesített kivonat lepárlása [a Codex Alimentarius halakkal és halászati termékekkel foglalkozó bizottsága (1968)].
4. A mintának legalább három különböző pontról vett, majd őrléssel összekevert, körülbelül 100 gramm húsból kell állnia.
A tagállamok a hatósági laboratóriumoknak rutineljárásként a fent említett referencia-módszer használatát ajánlják. A rutinmódszerek egyikével elvégzett vizsgálat eredményeinek kétségbevonása vagy az azokkal kapcsolatos vita esetén az eredmények ellenőrzésére csak a referencia-módszer használható.
II. FEJEZET
AZON FAJKATEGÓRIÁK, AMELYEK ESETÉBEN A TVB-N-HATÁRÉRTÉK RÖGZÍTÉSRE KERÜL
1. Sebastes spp., Helicolenus dactylopterus, Sebastichthys capensis.
2. A Pleuronectidae családhoz tartozó fajok (a laposhal kivételével: Hippoglossus spp.).
3. Salmo salar, a Merlucciidae családhoz tartozó fajok, a Gadidae családhoz tartozó fajok.
III. FEJEZET
A TVB-N KONCENTRÁCIÓJÁNAK MEGHATÁROZÁSA HALAKBAN ÉS HALÁSZATI TERMÉKEKBEN
Referenciaeljárás
1. Az alkalmazás célja és tárgya
Ez a módszer a halakban és halászati termékekben jelen levő TVB-N koncentrációjának azonosítására alkalmas referenciaeljárást írja le. Ez az eljárás a TVB-N-koncentráció 5 mg/100 g és legalább 100 mg/100 g közötti tartományában alkalmazható.
2. Meghatározás
A „TVB-N-koncentráció” alatt az illékony nitrogénbázis-vegyületeknek a leírt eljárással meghatározott nitrogéntartalma értendő.
A koncentráció mg/100 g-ban kerül meghatározásra.
3. Rövid leírás
Az illékony nitrogénbázis-vegyületeket 0,6 M-os perklórsavoldattal vonjuk ki a mintából. A lúgosítás után a kivonat gőzlepárlóba kerül, és az illékony bázisalkotórészeket savfelfogó tartály nyeli el. A TVB-N koncentrációja az elnyelt bázisok titrálásával kerül meghatározásra.
4. Vegyszerek
Eltérő megjelölés hiányában reagensfokozatú vegyszereket kell használni. A felhasznált víznek desztilláltnak vagy ioncseréltnek, és legalább ugyanolyan tisztaságúnak kell lennie. Eltérő megjelölés hiányában „oldat” alatt vizes oldatot kell érteni:
a) perklórsavoldat = 6 g/100 ml;
b) nátrium-hidroxid-oldat = 20 g/100 ml;
c) standard sósavoldat 0,05 mol/l ((0,05 N);
|
Megjegyzés: |
Automatikus lepárlókészülék használatakor a titrálást 0,01 mol/l ((0,01 N) koncentrációjú standard sósavoldattal kell végezni. |
d) bórsavoldat = 3 g/100 ml;
e) szilikon habzásgátló hatóanyag;
f) fenolftaleinoldat = 1 g/100 ml 95 % etanol;
g) indikátoroldat (Tashiro kevert indikátor) 2 g metilvörös és 1 g metilénkék 1 000 ml 95 %-os etanolban feloldva.
5. Eszközök és kellékek
a) Húsdaráló, kellően homogén halhúsminta előállításához.
b) 8 000 fordulat/perc és 45 000 fordulat/perc közötti nagysebességű keverőgép.
c) 150 mm átmérőjű bordázott szűrő, gyorsszűréshez.
d) 0,01 ml-es beosztású 5 ml-es büretta.
e) Gőzlepárló készülék. A készüléknek képesnek kell lennie különböző gőzmennyiségek szabályozására, valamint állandó mennyiségű gőz megadott időtartam alatt történő előállítására. A készüléknek biztosítania kell, hogy a lúgosító anyagok hozzáadása során a keletkező szabad bázisok ne távozhassanak a rendszerből.
6. Kivitelezés
Figyelmeztetés: Az erősen maró hatású perklórsavval történő munkavégzés során gondoskodni kell a szükséges elővigyázatossági és megelőző intézkedésekről. A mintákat – ha egyáltalán lehetséges – a következő utasításoknak megfelelően, beérkezésük után minél hamarabb el kell készíteni:
a)
Az elemzésre kerülő mintát az 5. a) pontban leírt módon húsdarálóval gondosan meg kell darálni. Pontosan 10 g ± 0,1 g ledarált mintát egy megfelelő edényben kell kimérni. Ezt a 4. a) pontban leírt 90,0 ml perklórsavoldattal kell összekeverni, két percig homogenizálni az 5. b) pontban leírt keverőgéppel, majd le kell szűrni.
Az így nyert kivonat körülbelül 2 oC és 6 oC közötti hőmérsékleten legalább hét napig eltartható.
b)
Az a) pontban leírtaknak megfelelően előállított 50,0 ml kivonatot az 5. e) pontban leírt gőzlepárló készülékbe kell helyezni. A kivonat megfelelő lúgosításának későbbi ellenőrzésére néhány csepp fenolftaleint a 4. f) pontban említett módon kell a kivonathoz adni. Néhány csepp szilikon habzásgátló hatóanyag hozzáadása után 6,5 ml nátrium-hidroxid-oldatot a 4. b) pontban leírt módon kell a kivonathoz adni, és a gőzlepárlás azonnal megkezdődik.
A gőzlepárlás beállítása következtében 10 percen belül körülbelül 100 ml párlat képződik. A lepárló kivezető csöve a 4. d) pontban leírt módon belemerül a 100 ml bórsavoldattal feltöltött savfelfogó tartályba, amelybe a 4. g) pont szerint 3–5 csepp indikátoroldat is került. Pontosan 10 perc múlva a lepárlás befejeződik. A lepárló kivezetőcsövét el kell távolítani a savfelfogó tartályból, és vízzel ki kell mosni. A savfelfogó oldatban lévő illékony bázisok standard sósavoldattal történő titrálással kerülnek meghatározásra a 4. c) pontban előírt módon.
A végpont pH-értékének 5,0 ± 0,1 -nek kell lennie.
c)
Két párhuzamos meghatározás szükséges. Az alkalmazott módszer akkor megfelelő, ha a párhuzamos mérések közötti különbség nem haladja meg a 2 mg/100 g értéket.
d)
A b) pontban leírt módon vakpróbát kell végezni. A kivonat helyett a 4. a) pontban meghatározottaknak megfelelően 50,0 ml perklórsavoldatot kell használni.
7. A TVB-N-érték kiszámítása
A savfelfogó oldat 4. c) pont szerinti sósavval történő titrálásával a TVB-N-koncentráció a következő egyenlet alapján számítható ki:

V1 = 0,01 M sósavoldat térfogata a minta ml-ében;
V0 = 0,01 M sósavoldat térfogata a vakminta ml-ében;
M = a minta súlya g-ban.
Megjegyzések
1. Két párhuzamos meghatározás szükséges. Az alkalmazott módszer akkor megfelelő, ha a párhuzamos mérések közötti különbség nem haladja meg a 2 mg/100 g értéket.
2. A berendezés 50 mg TVB-N/100 g-mal egyenértékű NH4Cl-oldatok lepárlásával ellenőrizhető.
3. A megismételhetőség standard eltérése Sr = 1,20 mg/100 g. A összehasonlíthatóság standard eltérése SR = 2,50 mg/100 g.
IV. FEJEZET
TVB-N GŐZLEPÁRLÓ KÉSZÜLÉK
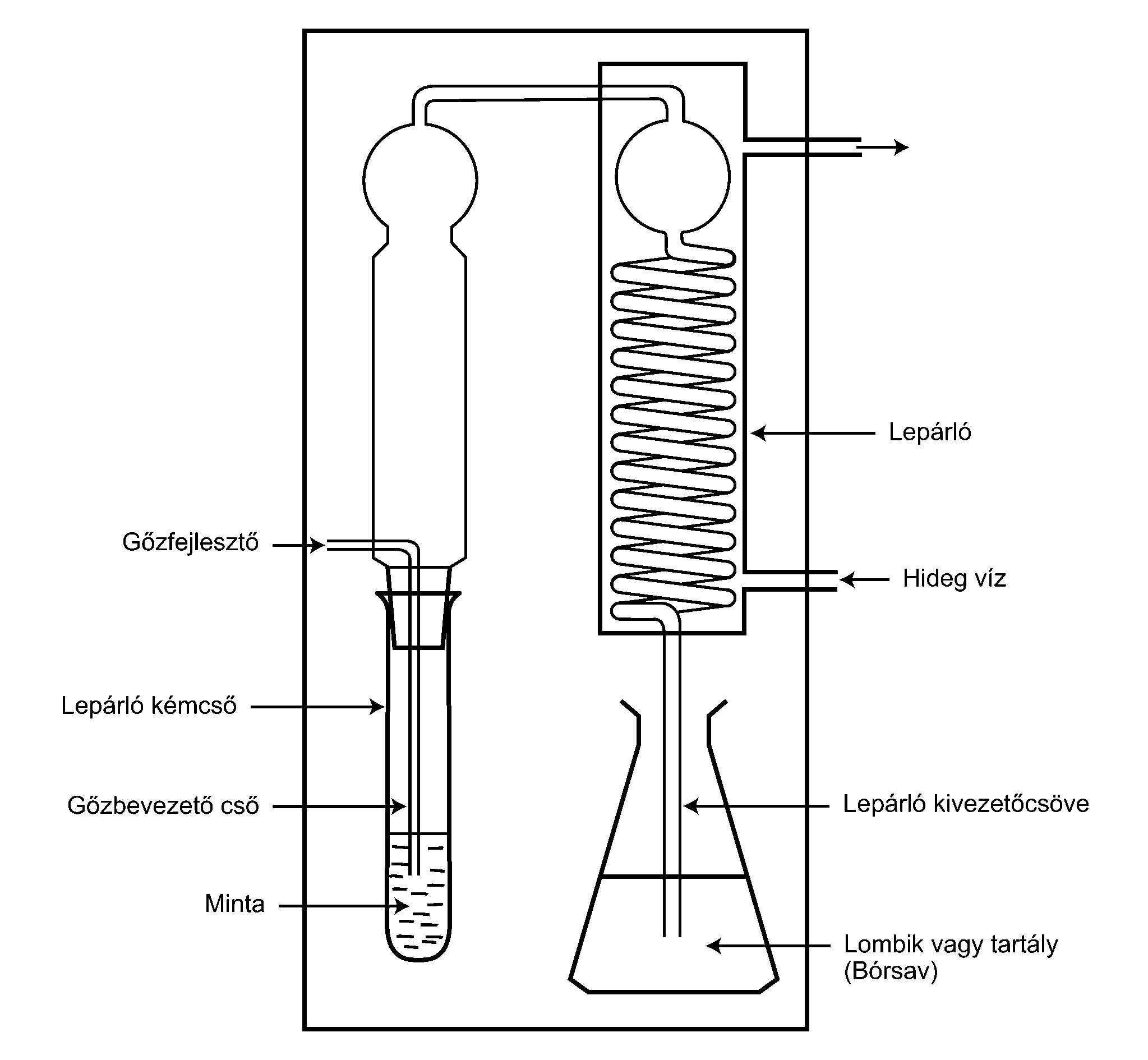
III. MELLÉKLET
A TENGERI BIOTOXINOK KIMUTATÁSA TEKINTETÉBEN ELISMERT VIZSGÁLATI MÓDSZEREK
A 853/2004/EK rendelet III. melléklete VII. szakasza V. fejezetének 2. pontjában megállapított határértékeknek való megfelelés ellenőrzése érdekében a hatáskörrel rendelkező hatóságok – és adott esetben az élelmiszer-ipari vállalkozók – a következő vizsgálati módszereket használhatják.
A 86/609/EGK tanácsi irányelv ( 1 ) 7. cikkének (2) és (3) bekezdésével összhangban a szubsztitúció, finomítás és a redukció elemeit a biológiai módszerek alkalmazásakor figyelembe kell venni.
I. FEJEZET
A BÉNULÁSOS KAGYLÓMÉREG (PSP) KIMUTATÁSÁRA IRÁNYULÓ MÓDSZER
1. A kagylók ehető részeinek (az egész test vagy bármely ehető rész külön) bénulásos kagylóméreg (PSP) tartalmát a biológiai vizsgálati módszerrel vagy bármely más nemzetközileg elismert módszerrel összhangban kell kimutatni.
2. Ha az eredmények bizonytalanok, az AOAC 2005.06. hivatalos módszerben (Paralytic Shellfish Poisoning Toxins in Shellfish) közzétett ún. Lawrence-módszer tekintendő referencia-módszernek.
II. FEJEZET
AZ AMNÉZIÁS KAGYLÓMÉREG (ASP) KIMUTATÁSÁRA IRÁNYULÓ MÓDSZER
A kagylók ehető részeinek (az egész test vagy bármely ehető rész külön) teljes amnéziás kagylóméreg (ASP) tartalmát nagy hatékonyságú folyadékkromatográfiás (HPLC) módszer vagy bármely más nemzetközileg elismert módszer alkalmazásával kell kimutatni.
Szűrési célból azonban az AOAC Journal 2006. júniusi számában publikált 2006.02 ASP ELISA módszer is alkalmazható a kagylók ehető részeinek teljes amnéziás kagylóméreg (ASP) tartalma kimutatására.
Ha az eredmények bizonytalanok, a referencia-módszer a HPLC-módszer.
III. FEJEZET
A LIPOFIL TOXIN KIMUTATÁSÁRA IRÁNYULÓ MÓDSZER
A. Kémiai módszer
1. A 853/2004/EK rendelet III. melléklete VII. szakasza V. fejezete 2. pontjának c), d) és e) alpontjában említett tengeri biotoxinok kimutatására a referencia-módszer az uniós referencialaboratórium folyadékkromatográfiás – tömegspektrometriás (LC-MS/MS) módszere. E módszert legalább az alábbi vegyületek kimutatására kell alkalmazni:
|
— |
az okadaic-sav csoportjába tartozó toxinok : OA, DTX1, DTX2,DTX3 és észtereik, |
|
— |
a pektenotoxinok csoportjába tartozó toxinok : PTX1 és PTX2, |
|
— |
a yessotoxinok csoportjába tartozó toxinok : YTX, 45 OH YTX, homo YTX és 45 OH homo YTX, |
|
— |
az azasprisavak csoportjába tartozó toxinok : AZA1, AZA2 és AZA3. |
2. A teljes toxicitási egyenértéket az EFSA ajánlásának megfelelően toxicitási egyenérték-tényezők használatával kell kiszámítani.
3. Amennyiben újabb, közegészségügyi szempontból fontos analógokat fedeznek fel, akkor azokat is be kell venni az elemzésbe. A teljes toxicitási egyenértéket az EFSA ajánlásának megfelelően toxicitási egyenérték-tényezők használatával kell kiszámítani.
4. Más módszerek, mint a folyadékkromatográfiás (LC) – tömegspektrometriás (MS) módszer, a megfelelő kimutatást lehetővé tévő nagyteljesítményű folyadékkromatográfia (HPLC), az immunpróbák és funkcionális próbák – mint például a foszfatázgátlási próba – az uniós referencialaboratórium LC-MS/MS módszere mellett alternatív vagy kiegészítő módszerként felhasználhatók a következő feltételekkel:
a) egyedül vagy kombinálva legalább az e fejezet A1. pontjában azonosított analógokat ki tudják mutatni; megfelelőbb kritériumok szükség esetén kidolgozhatók;
b) teljesítik az uniós referencialaboratórium által meghatározott, a módszer teljesítőképességére vonatkozó kritériumokat. Az ilyen módszereket laboratóriumon belül kell validálni, továbbá elismert jártassági vizsgálati rendszer szerint sikeresen kell tesztelni. Az uniós referencialaboratórium támogatja a technológia laboratóriumközi validálása irányába mutató tevékenységeket a hivatalos szabványosítás lehetővé tétele érdekében;
c) alkalmazásuk a referencia-módszer alkalmazásával egyenértékű közegészségügyi védelmet nyújt.
B. Biológiai módszerek
1. Annak érdekében, hogy a tagállamok módszereiket az e fejezet A1. pontjában meghatározott LC-MS/MS módszerhez igazíthassák, 2014. december 31-ig továbbra is alkalmazható a 853/2004/EK rendelet III. melléklete VII. szakaszának V. fejezete 2. pontjának c), d) és e) alpontjában említett tengeri toxinok kimutatására egéren végzett biológiai tesztek sorozata, amelyek a vizsgálati adag (hepatopancreas vagy az egész test), valamint az extrakciós és tisztítási lépésekhez használt oldószerek tekintetében térnek el egymástól.
2. Az érzékenység és a szelektivitás az extrakciós és tisztítási lépésekhez használt oldószerektől függ, és ezt az alkalmazni kívánt módszer kiválasztásakor figyelembe kell venni a toxinok teljes skálájának lefedése érdekében.
3. Az okadaic-sav, a dinofízistoxinok, az azaspirsavak, a pectenotoxinok és a yessotoxinok kimutatását egyetlen, acetonos extrakciót alkalmazó, egéren végzett biológiai teszttel is el lehet végezni. Az esetleges kölcsönhatások kiküszöbölése érdekében ezt a vizsgálati eljárást szükség esetén folyadék/folyadék megoszlási lépésekkel lehet kiegészíteni, etil-acetát/víz vagy diklór-metán/víz alkalmazásával.
4. Mindegyik teszthez három egeret kell használni. Ha a háromból két egér 24 órán belül elpusztul azt követően, hogy beoltották 5 g hepatopancreasnak vagy 25 g egész testnek megfelelő extraktummal, ezt pozitív eredménynek kell tekinteni a 853/2004/EK rendelet III. melléklete VII. szakaszának V. fejezete 2. pontjának c), d) és e) alpontjában említett toxinok közül egynek vagy többnek a megállapított szintek feletti mennyiségben való jelenléte szempontjából.
5. Az okadaic-sav, a dinofízistoxinok, a pectenotoxinok és az azaspirsavak kimutatására olyan, egéren végzett biológiai teszt alkalmazható, amelyben acetonos extrakciót alkalmaznak dietil-éteres folyadék/folyadék megoszlást követően, ez azonban nem alkalmas a yessotoxinok kimutatására, mivel a megoszlási lépés során e toxinok elveszhetnek. Mindegyik teszthez három egeret kell használni. Ha a háromból két egér 24 órán belül elpusztul azt követően, hogy beoltották 5 g hepatopancreasnak vagy 25 g egész testnek megfelelő extraktummal, ezt pozitív eredménynek kell tekinteni az okadaic-savnak, a dinofízistoxinoknak, a pectenotoxinoknak és az azaspirsavaknak a 853/2004/EK rendelet III. melléklete VII. szakaszának V. fejezete 2. pontjának c) és e) alpontjában említett szint feletti mennyiségben való jelenléte szempontjából.
6. Az okadaic-sav, a dinofízistoxinok és az azaspirsavak kimutatására patkányon végzett biológiai teszt alkalmazható. Mindegyik teszthez három patkányt kell használni. Ha a három patkány közül bármelyiknél hasmenéses reakció jelentkezik, azt pozitív eredménynek kell tekinteni az okadaic-savnak, a dinofízistoxinoknak és az azaspirsavaknak a 853/2004/EK rendelet III. melléklete VII. szakaszának V. fejezete 2. pontjának c) és e) alpontjában említett szint feletti mennyiségben való jelenléte szempontjából.
|
C. |
Az e fejezet B1. pontjában meghatározott időszakot követően az egéren végzett biológiai teszt a tagállamok által kidolgozott nemzeti ellenőrző programok keretében kizárólag a tenyésztési és átmosási területeken időszakosan végzett, új vagy ismeretlen tengeri toxinok kimutatására szolgáló monitoring során alkalmazható. |
IV. MELLÉKLET
A CSONTOKRÓL MECHANIKUSAN LEFEJTETT HÚS KALCIUMTARTALMA
A 853/2004/EK rendeletben említett MSM kalciumtartalma:
1. nem haladja meg a friss termék 0,1 %-át (= 100 mg/100 g vagy 1 000 ppm);
2. azt a szabványosított nemzetközi módszerrel határozzák meg.
V. MELLÉKLET
Az engedélyezett létesítmények jegyzékei
I. FEJEZET
AZ ENGEDÉLYEZETT ÉLELMISZER-IPARI LÉTESÍTMÉNYEK JEGYZÉKEIHEZ TÖRTÉNŐ HOZZÁFÉRÉS
Annak érdekében, hogy a Bizottság segítse a tagállamokat az engedélyezett élelmiszer-ipari létesítmények naprakész jegyzékeinek a többi tagállam és a nyilvánosság számára történő hozzáférhetővé tételében, a Bizottság internetes honlapot biztosít, amelyen minden egyes tagállam a saját nemzeti internetes honlapjához linket biztosít, illetve tájékoztatást nyújt, amennyiben a szóban forgó jegyzékek közzététele a TRACES rendszerrel történik.
II. FEJEZET
A NEMZETI INTERNETES HONLAPOK FORMÁTUMA
A. Összesített jegyzék
1. Minden tagállam a Bizottság rendelkezésére bocsátja azt az internetes címet, amelyen a 853/2004/EK rendelet I. mellékletének 8.1. pontjában meghatározott állati eredetű termékek tekintetében engedélyezett élelmiszer-ipari létesítmények jegyzékeinek összesített jegyzékét tartalmazó egyetlen nemzeti internetes honlap elérhető.
2. Az 1. pontban említett összesített jegyzék egyetlen lapból áll, és az az Unió egy vagy több hivatalos nyelvén tölthető ki.
B. Üzemeltetési táblázat
1. Az összesített jegyzéket tartalmazó internetes honlapot a hatáskörrel rendelkező hatóság vagy – adott esetben – a 882/2004/EK rendelet 4. cikkében említett, hatáskörrel rendelkező hatóságok valamelyike dolgozza ki.
2. Az összesített jegyzék az alábbiakhoz tartalmaz linkeket:
a) az ugyanazon internetes honlapon elhelyezett más internetes honlapok;
b) a többi hatáskörrel rendelkező hatóság, egység, vagy – adott esetben – testület által üzemeltetett internetes honlapok, amennyiben nem az 1. pontban említett hatáskörrel rendelkező hatóság tartja fenn az engedélyezett élelmiszer-ipari létesítmények egyes jegyzékeit.
C. Jegyzékek a TRACES rendszerben
Az A. és B. résztől eltérve a tagállamoknak lehetőségük van arra, hogy a jegyzékeket a TRACES rendszeren keresztül bocsássák rendelkezésre.
III. FEJEZET
ELRENDEZÉS ÉS AZ ENGEDÉLYEZETT LÉTESÍTMÉNYEK JEGYZÉKEINEK KÓDJAI
Az engedélyezett élelmiszer-ipari létesítményekre vonatkozó információk széles körű elérhetőségének biztosítása és a jegyzékek áttekinthetőségének javítása érdekében meg kell határozni az elrendezést, többek között az érintett információkra és kódokra vonatkozó követelményeket.
IV. FEJEZET
TECHNIKAI ELŐÍRÁSOK
A II. és III. fejezetben említett feladatokat és tevékenységeket a Bizottság által közzétett technikai előírásokkal összhangban kell elvégezni.
VI. MELLÉKLET
AZ ÁLLATI EREDETŰ TERMÉKEK BEHOZATALÁRA VONATKOZÓ EGÉSZSÉGÜGYI BIZONYÍTVÁNYMINTÁK ÉS OKMÁNYMINTÁK
I. SZAKASZ
▼M10 —————
IV. FEJEZET
HALÁSZATI TERMÉKEK
A 853/2004/EK rendelet 6. cikke (1) bekezdésének d) pontjában említett, a halászati termékek behozatalára vonatkozó egészségügyi bizonyítvány megfelel az e melléklet IV. függelékében megállapított mintának.
V. FEJEZET
ÉLŐ KÉTHÉJÚ KAGYLÓK
A 853/2004/EK rendelet 6. cikke (1) bekezdésének d) pontjában említett, az élő kéthéjú kagylók behozatalára vonatkozó egészségügyi bizonyítvány megfelel az e melléklet V. függelékében megállapított mintának.
▼M10 —————
II. SZAKASZ
A KAPITÁNY ÁLTAL ALÁÍRANDÓ OKMÁNY MINTÁJA
A kapitány által aláírandó okmány, amely a 854/2004/EK rendelet 15. cikkének (3) bekezdése értelmében, amenynyiben a fagyasztott halászati termékek behozatala közvetlenül a fagyasztó hajóról történik, az említett rendelet 14. cikkében meghatározott okmány helyébe léphet, megfelel az e melléklet VII. függelékében meghatározott mintának.
▼M10 —————
A VI. melléklet IV. függeléke
Az emberi fogyasztásra szánt halászati termékek behozatalára vonatkozó egészségügyi bizonyítványminta




A VI. melléklet V. függeléke
A. RÉSZ
AZ EMBERI FOGYASZTÁSRA SZÁNT ÉLŐ KÉTHÉJÚ KAGYLÓK, TÜSKÉSBŐRŰEK, ZSÁKÁLLATOK ÉS TENGERI HASLÁBÚAK BEHOZATALÁRA VONATKOZÓ EGÉSZSÉGÜGYI BIZONYÍTVÁNYMINTA



B. RÉSZ:
AZ ACANTHOCARDIA TUBERCULATUM FAJHOZ TARTOZÓ FELDOLGOZOTT KÉTHÉJÚ KAGYLÓKRA VONATKOZÓ KIEGÉSZÍTŐ ÁLLAT-EGÉSZSÉGÜGYI IGAZOLÁSMINTA
A hatósági ellenőr igazolja, hogy az Acanthocardia tuberculatum fajhoz tartozó és … hivatkozási számú egészségügyi bizonyítvánnyal tanúsított feldolgozott kéthéjú kagylókat:
1. a 2006/766/EK ( 2 ) bizottsági határozat alkalmazásában az illetékes hatóság által egyértelműen azonosított, ellenőrzött és engedélyezett tenyésztési területen takarították be, és ahol e kagylók ehető részében a PSP-szint alacsonyabb, mint 300 μg/100 g;
2. a hatáskörrel rendelkező hatóság által lezárt járműben vagy tartályban közvetlenül az alábbi létesítménybe szállították:
…
…
(a hatáskörrel rendelkező hatóság által kifejezetten a kezelésre jóváhagyott létesítmény neve és hatósági engedélyezési száma);
3. a létesítménybe történő szállítás során a hatáskörrel rendelkező hatóság által kiállított okmány kísérte, amely engedélyezi a szállítást, tartalmazza a termék jellegét, mennyiségét, a származási területet és a rendeltetési létesítmény nevét;
4. alávetették a 96/77/EK határozat mellékletében leírt hőkezelésnek;
5. nem tartalmaznak a biológiai tesztelési eljárással kimutatható PSP-szintet, melyet az ezen igazolás hatálya alá tartozó szállítmányban lévő minden tételen elvégzett vizsgálatról szóló mellékelt jelentés mutat ki.
A hatósági ellenőr igazolja, hogy az illetékes hatóság megerősítette, hogy a 2. pontban említett létesítményben végrehajtott egészségügyi önellenőrzéseket kifejezetten a 4. pontban említett hőkezelésre alkalmazzák.
Alulírott hatósági ellenőr kijelenti, hogy ismeri a 96/77/EK határozat rendelkezéseit, és hogy a mellékelt jelentés(ek) egyeznek a feldolgozást követően a termékeken végrehajtott vizsgálattal.
|
Hatósági ellenőr |
|
|
Név (nyomtatott betűvel): Képesítés és beosztás: Kelt: |
Aláírás: Bélyegző: |
▼M10 —————
A VI. melléklet VII. függeléke
MINTA A KAPITÁNY ÁLTAL ALÁÍRANDÓ, A KÖZVETLENÜL A FAGYASZTÓ HAJÓRÓL IMPORTÁLT FAGYASZTOTT HALÁSZATI TERMÉKEKET KÍSÉRŐ OKMÁNYHOZ



A VI. melléklet VIII. függeléke
A valamely uniós tagállam lobogója alatt közlekedő halászhajók által kifogott, harmadik országon keresztül tárolással vagy anélkül szállított, emberi fogyasztásra szánt halászati termékek egészségügyi bizonyítványmintája



VIA. MELLÉKLET
NYERS- ÉS HŐKEZELT TEJRE VONATKOZÓ VIZSGÁLATI MÓDSZEREK
I. FEJEZET
A CSÍRASZÁM ÉS A SZOMATIKUS SEJTSZÁM MEGHATÁROZÁSA
1. A 853/2004/EK rendelet III. melléklete IX. szakasza I. fejezetének III. pontjában megállapított kritériumoknak való megfelelés ellenőrzésekor a következő szabványokat kell referencia-módszerként alkalmazni:
a) EN/ISO 4833 az összcsíraszám esetében 30 oC-on;
b) ISO 13366-1 a szomatikus sejtszám esetében.
2. Alternatív analitikai módszerek a következő esetekben fogadhatók el:
a) az összcsíraszám esetében 30 oC-on, ha a módszereket az 1a) pontban említett referenciamódszer alapján validálják, összhangban a 16140 EN/ISO szabványban előírt protokollal vagy nemzetközileg elfogadott más hasonló protokollokkal.
Különösen az alternatív analitikai módszer és az 1a) pontban említett referenciamódszer közötti átváltási arányt határozzák meg az ISO 21187 szabvány szerint.
b) a szomatikus sejtszám esetében, ha a módszereket az 1b) pontban említett referenciamódszer alapján validálják, összhangban a 8196 ISO szabványban előírt protokollal, és a 13366-2 ISO szabvánnyal vagy nemzetközileg elfogadott más hasonló protokollokkal összhangban történő alkalmazás esetén.
II. FEJEZET
LÚGOS FOSZFATÁZAKTIVITÁS MEGHATÁROZÁSA
1. A lúgos foszfatázaktivitás meghatározásakor az ISO 11816-1 szabványt kell referenciamódszerként alkalmazni.
2. A lúgos foszfatázaktivitást enzimaktivitási miliegységek/literben (mU/l) fejezik ki. A lúgos foszfatázaktivitás egy egysége a lúgos foszfatázenzim azon mennyisége, amely percenként 1 mikromol alapréteg átalakítását katalizálja.
3. A lúgos foszfatáz-vizsgálat eredménye negatívnak tekintendő, ha a mért aktivitás a tehéntejben nem haladja meg a 350 mU/l-t.
4. Alternatív analitikai módszerek alkalmazása elfogadható, ha a módszereket az 1. pontban említett referenciamódszer alapján validálják, összhangban a nemzetközileg elfogadott protokollokkal.
VI. B. MELLÉKLET
A HÚSVIZSGÁLAT HATÓSÁGI ELLENŐRZÉSEIRE ALKALMAZANDÓ KÖVETELMÉNYEK
|
1. |
E melléklet alkalmazásában a következő fogalommeghatározásokat kell alkalmazni: a) ellenőrzött tartási feltételek mellett és integrált tenyésztési rendszerekben: olyan állattartástípus, ahol az állatokat a függelékben meghatározott feltételek mellett tartják; b) fiatal szarvasmarhaféle: bármilyen nemű, 8 hónapnál nem idősebb szarvasmarha; c) fiatal juhféle: bármilyen nemű, 12 hónapnál nem idősebb juhféle, amelynek állandó metszőfoga még nem törte át a fogínyt; d) fiatal kecskeféle: bármilyen nemű, 6 hónapnál nem idősebb kecskeféle; e) állomány: valamely gazdaságban tartott állat vagy állatcsoport, amely járványügyi egységet képez; ha egynél több állományt tartanak valamely gazdaságban, valamennyi állomány önálló járványügyi egységet képez; f) gazdaság: bármely olyan létesítmény, építmény vagy szabad ég alatti gazdaság esetén bármely olyan hely, amely ugyanazon tagállam területén található, ahol állatokat tartanak, gondoznak vagy feldolgoznak; g) nem folyamatos vágási vagy vadfeldolgozási tevékenységet folytató létesítmény: olyan, az illetékes hatóság által kockázatelemzés alapján kijelölt vágóhíd vagy vadfeldolgozó létesítmény, amelyben a vágási vagy vadfeldolgozási tevékenység nem a teljes munkanap folyamán vagy nem a hét egymást követő összes munkanapján történik. |
|
2. |
Levágást követő vizsgálatok a nem folyamatos vágási vagy vadfeldolgozási tevékenységet folytató létesítményekben.
|
|
3. |
A bemetszést nem alkalmazó, kockázatalapú húsvizsgálatra vonatkozó követelmények. ▼M8 —————
|
|
4. |
Az egypatás állatok levágást követő vizsgálatára vonatkozó kiegészítő követelmények.
|
Függelék a VI. b. melléklethez
E melléklet alkalmazásában az ellenőrzött tartási feltételek és integrált tenyésztési rendszerek azt jelenti, hogy az élelmiszer-ipari vállalkozónak az alábbi feltételeket teljesítenie kell:
a) minden takarmány olyan létesítményből származik, amely a takarmányt a 183/2005/EK európai parlamenti és tanácsi rendelet ( 3 ) 4. és 5. cikkében meghatározott követelményekkel összhangban termeli; az állatok számára takarmányként adott szálastakarmányt vagy terményeket megfelelően kezelni kell, és amennyiben lehetséges, szárítani és/vagy pelletálni;
b) az egyszerre betelepítés/egyszerre kitelepítés rendszerét kell alkalmazni, ahol lehetséges. Amennyiben az állományba új állatok kerülnek, azokat az állat-egészségügyi szolgálat által előírt ideig elkülönítve kell tartani a betegségek behurcolásának megelőzése érdekében;
c) az állatok egyike sem kerülhet kapcsolatba külső létesítményekkel, kivéve, ha az élelmiszer-ipari vállalkozó kockázatelemzés alapján az illetékes hatóság számára kielégítő módon képes bizonyítani, hogy a külső kapcsolat az adott időszakban, létesítményekben és körülmények között nem jár betegségek behurcolásának veszélyével;
d) a 853/2004/EK rendelet II. mellékletének III. szakaszában meghatározottak szerint az állatokról és tartásuk körülményeiről születésüktől kezdve a levágásukig részletes információ áll rendelkezésre;
e) ha almot biztosítanak az állatok részére, az alomanyagot megfelelően kezelni kell a betegségek elkerülése vagy a betegségek behurcolásának elkerülése érdekében;
f) a gazdaság személyzetének meg kell felelnie a 852/2004/EK rendelet I. mellékletében meghatározott általános higiéniai előírásoknak;
g) az állattartás helyszínének hozzáférésére vonatkozó ellenőrző eljárások vannak érvényben;
h) a gazdaság nem biztosít szállást turisták számára, illetve nem szolgál kempingként, kivéve, ha az élelmiszer-ipari vállalkozó kockázatelemzés alapján az illetékes hatóság számára kielégítő módon képes bizonyítani, hogy a létesítmények az állatok nevelésére szolgáló területtől megfelelően el vannak különítve és az emberek és állatok között közvetlen vagy közvetett kapcsolat nem lehetséges;
i) az állatok nem férnek hozzá a hulladéklerakókhoz vagy a háztartási szeméthez;
j) kártevők elleni védekezési terv van érvényben;
k) silótakarmányozást nem alkalmaznak, kivéve, ha az élelmiszer-ipari vállalkozó kockázatelemzés alapján az illetékes hatóság számára kielégítő módon képes bizonyítani, hogy a takarmány az állatokra nem jelent veszélyt;
l) szennyvíztisztító telepekről származó szennyvíz és üledék nem kerül az állatok által elérhető területekre, illetve azt nem alkalmazzák az állatok táplálására használt legelők növényeinek trágyázására, kivéve, ha azt megfelelő és az illetékes hatóság által elfogadott módon kezelik.
VII. MELLÉKLET
A 853/2004/EK RENDELET MÓDOSÍTÁSAI
A 853/2004/EK rendelet II. és III. melléklete a következőképpen módosul:
1. A II. melléklet I. szakaszának B. pontja a következőképpen módosul:
a) A 6. pont második albekezdése helyébe a következő szöveg lép:
„BE, CZ, DK, DE, EE, GR, ES, FR, IE, IT, CY, LV, LT, LU, HU, MT, NL, AT, PL, PT, SI, SK, FI, SE és UK.”
b) A 8. pont helyébe a következő szöveg lép:
„8. Amennyiben a jelölést egy, a Közösség területén lévő létesítményben helyezik fel, annak ovális alakúnak kell lennie, és tartalmaznia kell a következő rövidítések egyikét: CE, EC, EF, EG, EK, EY, ES, EÜ, EK, EB vagy WE.”
2. A III. melléklet a következőképpen módosul:
a) Az I. szakasz IV. fejezetének 8. pontja helyébe a következő szöveg lép:
„8. Az emberi fogyasztásra szánt állati testet vagy egyéb testrészeket teljesen le kell bőrözni, kivéve a sertésféléket és a juh- és kecskefélék fejét, a borjakat, valamint a szarvasmarha-, juh- és kecskefélék lábát. A fejeket és a lábakat úgy kell kezelni, hogy elkerüljék a többi hús szennyeződését.”
b) A II. szakasz a következő VII. fejezettel egészül ki:
„VII. FEJEZET: VÍZVISSZATARTÓ ÁGENSEK
Az élelmiszer-ipari vállalkozók biztosítják, hogy kifejezetten a vízvisszatartás elősegítése érdekében kezelt baromfihúst nem friss húsként hozzák forgalomba, hanem előkészített húsként, vagy azt feldolgozott termékek előállításához használják fel.”
c) A VIII. szakasz V. fejezetének E. 1. pontja helyébe a következő szöveg lép:
„1. A következő családokba tartozó mérgező halakból származó halászati termékeket nem lehet forgalomba hozni: Tetraodontidae, Molidae, Diodontidae és Canthigasteridae. A Gempylidae családba, különösen Ruvettus pretiosus-hoz és Lepidocybium flavobrunneum-hoz tartozó friss, előkészített és feldolgozott halászati termékek csak egyedi csomagolással/gyűjtőcsomagolással ellátott filé formájában hozhatók forgalomba, és azokat megfelelően kell címkézni, hogy ellássák a fogyasztót az elkészítéssel/főzéssel, valamint a káros emésztőszervi hatásokat okozó anyagok jelenlétére vonatkozó kockázatokkal kapcsolatos információkkal. A címkén a köznapi elnevezést kísérnie kell a tudományos névnek.”
d) A IX. szakasz a következőképpen módosul:
i. Az I. fejezet II.B.1. e) pontja helyébe a következő szöveg lép:
„e) hogy a tőgybimbók merítéses vagy permetező kezelését csak a biocid termékek forgalomba hozataláról szóló, 1998. február 16-i 98/8/EK európai parlamenti és tanácsi irányelvben ( *1 ) megállapított eljárásokkal összhangban történt engedélyezést vagy nyilvántartásba vételt követően használják.
ii. A II. fejezet II.1. pontja helyébe a következő szöveg lép:
„1. Amikor a nyers tej vagy a tejtermék hőkezelésen esik át, az élelmiszer-ipari vállalkozóknak biztosítaniuk kell, hogy az megfelel a 852/2004/EK rendelet II. melléklete XI. fejezete követelményeinek. Biztosítják különösen, hogy a következő eljárások alkalmazása során betartják az említett előírásokat:
a) A pasztőrözést a következőket tartalmazó kezeléssel érik el:
i. magas hőmérséklet rövid ideig (legalább 72 oC 15 másodpercig);
ii. alacsony hőmérséklet hosszú ideig (legalább 63 oC 30 percig); vagy
iii. az idő-hőmérséklet feltételek bármely más kombinációja az egyenértékű hatás elérése érdekében,
hogy a termékek adott esetben az ilyen kezelés után az alkalikus-foszfatáz-vizsgálatra negatív reakciót adjanak.
b) Az ultramagas hőmérsékleten történő hőkezelést (UHT) a következőket tartalmazó kezeléssel érik el:
i. magas hőmérsékleten rövid ideig történő a folyamatos hőhatás (135 oC-nál nem kevesebb hőmérsékleten, megfelelő idő kombinációjával), hogy ne legyenek olyan életképes mikroorganizmusok vagy spórák, amelyek a kezelt termékekben növekedésre képesek, amikor azt aszeptikus zárt tartályban szobahőmérsékleten tartják; és
ii. elegendő annak biztosításához, hogy a termékek mikrobiológiailag stabilak maradjanak, azt követően, hogy azokat zárt tartályban 15 napig 30 oC-on, vagy 7 napig 55 oC-on inkubálták, vagy bármely más olyan módszert követően, amely kimutatja, hogy megfelelő hőkezelést alkalmaztak.”
e) A X. szakasz II. fejezete a következőképpen módosul:
i. A III. rész 5. pontja helyébe a következő szöveg lép:
„5. A feltörés után a tojáslé minden részét a lehető leggyorsabban fel kell dolgozni a mikrobiológiai veszélyek elkerülése vagy azok elfogadható szintre való csökkentése érdekében. A nem megfelelően feldolgozott tétel azonnal ismét feldolgozható ugyanabban a létesítményben, ha a feldolgozás azt emberi fogyasztásra alkalmassá teszi. Amennyiben egy tételt emberi fogyasztásra alkalmatlannak találnak, azt denaturálni kell annak biztosítására, hogy nem kerül emberi fogyasztásra.”
ii. Az V. rész 2. pontja helyébe a következő szöveg lép:
„2. Tojáslé esetében az 1. pontban említett címkének a »nem pasztörizált tojáslé – a rendeltetési helyen kezelendő« szavakat is tartalmaznia kell, és meg kell jelölnie a feltörés dátumát és óráját is.”
f) A XIV. szakasz a következő V. fejezettel egészül ki:
„V. FEJEZET: CÍMKÉZÉS
A zselatint tartalmazó egyedi és gyűjtőcsomagolásnak az »emberi fogyasztásra alkalmas zselatin« szavakat is tartalmaznia kell, és meg kell jelölnie az előkészítés dátumát.”
VIII. MELLÉKLET
A 854/2004/EK RENDELET MÓDOSÍTÁSAI
A 854/2004/EK rendelet I., II. és III. melléklete a következőképpen módosul:
1. Az I. melléklet I. szakasza III. fejezetének 3. pontja a következőképpen módosul:
a) Az a) pont második albekezdése helyébe a következő szöveg lép:
„BE, CZ, DK, DE, EE, GR, ES, FR, IE, IT, CY, LV, LT, LU, HU, MT, NL, AT, PL, PT, SI, SK, FI, SE és UK.”
b) A c) pont helyébe a következő szöveg lép:
„c) a Közösségen belüli vágóhídon történő alkalmazás esetén a jelölésnek tartalmaznia kell a CE, EC, EF, EG, EK, EY, ES, EÜ, EK, EB vagy WE rövidítést.”
2. A II. melléklet II. fejezetének A.4. és A.5. pontja helyébe a következő szöveg lép:
„4. A hatáskörrel rendelkező hatóság a B. osztályba sorolhatja az olyan területeket, amelyekről az élő kagylók begyűjthetők, de a 3. pontban említett egészségügyi előírások betartása érdekében csak tisztító központban való kezelést, illetve átmosást követően lehet emberi fogyasztás céljára forgalomba hozni. Az ilyen területekről származó élő kagylóknál a hús és az intravalvularis folyadék 100 grammjában 4 600 E. coli-nál nem lehet több. E vizsgálat referencia-módszere az ISO 16649-3-ban meghatározott, ötcsöves háromszoros hígítású legvalószínűbb szám (MPN)-vizsgálat. Alternatív módszerek alkalmazhatók, ha azokat e referencia-módszerrel szemben az EN/ISO 16140-ben szereplő kritériumokkal összhangban validálták.
5. A hatáskörrel rendelkező hatóság C. osztályba sorolhatja az olyan területeket, amelyekről az élő kagylók begyűjthetők, de a 3. bekezdésben említett egészségügyi előírásoknak való megfelelés érdekében csak hosszan tartó átmosást követően lehet forgalomba hozni. Az ilyen területekről származó élő kagylóknál a hús és az intravalvularis folyadék 100 grammjában 46 000 E. coli-nál nem lehet több. E vizsgálat referencia-módszere az ISO 16649-3-ban meghatározott, ötcsöves háromszoros hígítású legvalószínűbb szám (MPN)-vizsgálat. Alternatív módszerek alkalmazhatók, ha azokat e referencia-módszerrel szemben az EN/ISO 16140-ben szereplő kritériumokkal összhangban validálták.”
3. A III. melléklet II. fejezetének G.1. pontja helyébe a következő szöveg lép:
„1. A következő családokba tartozó mérgező halakból származó halászati termékeket nem lehet forgalomba hozni: Tetraodontidae, Molidae, Diodontidae és Canthigasteridae. A Gempylidae családba, különösen Ruvettus pretiosus-hoz és Lepidocybium flavobrunneum-hoz tartozó friss, előkészített és feldolgozott halászati termékek csak védőcsomagolással/csomagolással ellátott filé formájában hozhatók forgalomba, és azokat megfelelően kell címkézni, hogy ellássák a fogyasztót az elkészítéssel/főzéssel, valamint a káros emésztőszervi hatásokat okozó anyagok jelenlétére vonatkozó kockázatokkal kapcsolatos információkkal. A címkén a köznapi elnevezést kísérnie kell a tudományos névnek.”
( ) HL L 358., 1986.12.18., 1. o.
( ) Lásd e Hivatalos Lap 53 oldalát.
( 1 ) HL L 35., 2005.2.8., 1. o.
( *1 ) HL L 123., 1998.4.24., 1. o.”


