ISSN 1977-0693
doi:10.3000/19770693.L_2013.021.fra
Journal officiel
de l'Union européenne
L 21

Édition de langue française
Législation
56e année
24 janvier 2013
|
ISSN 1977-0693 doi:10.3000/19770693.L_2013.021.fra |
||
|
Journal officiel de l'Union européenne |
L 21 |
|

|
||
|
Édition de langue française |
Législation |
56e année |
|
Sommaire |
|
I Actes législatifs |
page |
|
|
|
RÈGLEMENTS |
|
|
|
* |
|
|
|
III Autres actes |
|
|
|
|
ESPACE ÉCONOMIQUE EUROPÉEN |
|
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
||
|
|
* |
|
|
|
|
|
(1) Texte présentant de l'intérêt pour l'EEE |
|
FR |
Les actes dont les titres sont imprimés en caractères maigres sont des actes de gestion courante pris dans le cadre de la politique agricole et ayant généralement une durée de validité limitée. Les actes dont les titres sont imprimés en caractères gras et précédés d'un astérisque sont tous les autres actes. |
I Actes législatifs
RÈGLEMENTS
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/1 |
RÈGLEMENT (UE) N o 55/2013 DU CONSEIL
du 17 décembre 2012
portant extension du champ d’application du règlement (UE) no 1214/2011 du Parlement européen et du Conseil sur le transport transfrontalier professionnel d’euros en espèces par la route entre États membres dans la zone euro
LE CONSEIL DE L’UNION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne, et notamment son article 352,
vu la proposition de la Commission européenne,
vu l’approbation du Parlement européen,
après transmission du projet d’acte législatif aux parlements nationaux,
vu l’avis de la Banque centrale européenne (1),
statuant conformément à une procédure législative spéciale,
considérant ce qui suit:
|
(1) |
Le règlement (UE) no 1214/2011 du Parlement européen et du Conseil (2) vise à faciliter le transport transfrontalier d’euros en espèces entre les États membres. Cependant, ledit règlement s’applique uniquement sur le territoire des États membres qui ont adopté l’euro comme monnaie unique. |
|
(2) |
Durant la période précédant le passage à l’euro dans un État membre, il est nécessaire d’acheminer des euros en espèces depuis des États membres de la zone euro existante, étant donné que les billets en euros nécessaires à ce passage sont habituellement acheminés au départ de stocks situés dans la zone euro existante et que les pièces sont souvent entièrement ou partiellement frappées à l’étranger. |
|
(3) |
Il est donc nécessaire que le règlement (UE) no 1214/2011 s’applique également aux États membres qui se préparent à adopter l’euro. Il devrait s’appliquer à partir de la date de la décision du Conseil d’abroger la dérogation accordée aux États membres concernés en ce qui concerne leur participation à l’euro. |
|
(4) |
Étant donné que l’objectif du présent règlement, à savoir faciliter le transport professionnel transfrontalier d’euros en espèces par la route entre les États membres actuels de la zone euro et les États sur le point d’introduire l’euro, ne peut pas être réalisé de manière suffisante par les États membres, en raison de régimes réglementaires très complexes et très différents en la matière et peut donc, en raison des dimensions et des effets de cette action, être mieux réalisé au niveau de l’Union, celle-ci peut prendre des mesures conformément au principe de subsidiarité consacré à l’article 5 du traité sur l’Union européenne. Conformément au principe de proportionnalité tel qu’énoncé audit article, le présent règlement n’excède pas ce qui est nécessaire pour atteindre cet objectif, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
Le règlement (UE) no 1214/2011 s’applique au territoire d’un État membre qui n’a pas encore adopté l’euro à partir de la date de la décision du Conseil d’abroger la dérogation accordée aux États membres concernés en ce qui concerne leur participation à l’euro, prise en vertu de l’article 140, paragraphe 2, du traité sur le fonctionnement de l’Union européenne.
Article 2
Le présent règlement entre en vigueur douze mois après sa publication au Journal officiel de l’Union européenne.
Il est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 17 décembre 2012.
Par le Conseil
Le président
S. ALETRARIS
(1) Avis du 5 octobre 2010 (JO C 278 du 15.10.2010, p. 1).
(2) JO L 316 du 29.11.2011, p. 1.
II Actes non législatifs
RÈGLEMENTS
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/3 |
RÈGLEMENT (UE) N o 56/2013 DE LA COMMISSION
du 16 janvier 2013
modifiant les annexes I et IV du règlement (CE) no 999/2001 du Parlement européen et du Conseil fixant les règles pour la prévention, le contrôle et l’éradication de certaines encéphalopathies spongiformes transmissibles
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CE) no 999/2001 du Parlement européen et du Conseil du 22 mai 2001 fixant les règles pour la prévention, le contrôle et l’éradication de certaines encéphalopathies spongiformes transmissibles (1), et notamment son article 23, premier alinéa,
considérant ce qui suit:
|
(1) |
Le règlement (CE) no 999/2001 fixe les règles pour la prévention, le contrôle et l’éradication des encéphalopathies spongiformes transmissibles (EST) chez les animaux. Il s’applique à la production et à la mise sur le marché des animaux vivants et des produits d’origine animale et, dans certains cas spécifiques, à leurs exportations. |
|
(2) |
L’article 7, paragraphe 1, du règlement (CE) no 999/2001 dispose que l’utilisation de protéines animales dans l’alimentation des ruminants est interdite. Son article 7, paragraphe 2, étend cette interdiction aux animaux autres que les ruminants et la limite, en ce qui concerne l’alimentation de ces animaux avec des produits d’origine animale, conformément à l’annexe IV dudit règlement. |
|
(3) |
L’annexe IV du règlement (CE) no 999/2001 étend l’interdiction énoncée à l’article 7, paragraphe 1, à l’alimentation des animaux d’élevage non ruminants (à l’exception des animaux carnivores à fourrure) avec, entre autres, des protéines animales transformées (PAT). Par dérogation, et dans certaines conditions, l’annexe IV autorise toutefois certaines PAT dans l’alimentation des animaux d’élevage non ruminants. |
|
(4) |
L’article 11 du règlement (CE) no 1069/2009 du Parlement européen et du Conseil du 21 octobre 2009 établissant des règles sanitaires applicables aux sous-produits animaux et produits dérivés non destinés à la consommation humaine et abrogeant le règlement (CE) no 1774/2002 (règlement relatif aux sous-produits animaux) (2) interdit l’alimentation d’animaux terrestres d’une espèce donnée, autres que les animaux à fourrure, au moyen de PAT dérivées de corps ou de parties de corps d’animaux de la même espèce. Cet article interdit également l’alimentation des poissons d’élevage au moyen de PAT dérivées de corps ou de parties corporelles de poissons d’élevage de la même espèce. |
|
(5) |
La communication de la Commission au Parlement européen et au Conseil intitulée «Feuille de route no 2 pour les EST — Document de stratégie sur les encéphalopathies spongiformes transmissibles pour 2010-2015» (3) a été adoptée le 16 juillet 2010. Elle met en évidence les domaines dans lesquels des modifications pourraient être apportées à la législation de l’Union sur les EST. Elle souligne également que le réexamen de la réglementation sur les EST doit se fonder essentiellement sur des avis scientifiques et des aspects techniques relatifs au contrôle et à la mise en œuvre des nouvelles mesures. |
|
(6) |
Cette communication aborde notamment la révision des dispositions actuelles de la législation de l’Union concernant l’interdiction des protéines animales dans l’alimentation animale. Se fondant sur deux avis scientifiques émis le 24 janvier 2007 (4) et le 17 novembre 2007 (5) par le groupe scientifique sur les dangers biologiques (BIOHAZ) de l’Autorité européenne de sécurité des aliments (EFSA), la communication reconnaît qu’aucune EST n’a été décelée chez les animaux d’élevage non ruminants élevés dans des conditions naturelles et que le risque de transmission de l’encéphalopathie spongiforme bovine (ESB) entre non-ruminants est négligeable à condition que le recyclage intraspécifique soit évité. La communication conclut, par conséquent, qu’il serait envisageable de lever l’interdiction d’utiliser des PAT provenant de non-ruminants dans l’alimentation des non-ruminants, sans toutefois lever l’interdiction du recyclage intraspécifique et seulement s’il existe des techniques d’analyse validées qui permettent de déterminer l’espèce d’origine des PAT, ainsi qu’une canalisation correcte des PAT provenant de différentes espèces. |
|
(7) |
Le 29 novembre 2010, le Conseil a adopté des conclusions concernant cette communication (6). Dans ces conclusions, le Conseil reconnaît l’importance fondamentale de l’interdiction d’utiliser des PAT dans les aliments destinés aux animaux d’élevage pour la prévention de la transmission de l’ESB via la chaîne alimentaire, interdiction qui joue un rôle majeur dans la réduction de l’incidence de cette maladie dans la population bovine. En outre, le Conseil considère que toute éventuelle réintroduction de l’utilisation des PAT issues de non-ruminants dans l’alimentation d’autres espèces de non-ruminants est nécessairement subordonnée à la réalisation de tests efficaces et validés permettant d’établir une distinction entre les PAT issues d’espèces différentes ainsi qu’à une analyse approfondie des risques liés à l’assouplissement de la réglementation du point de vue de la santé publique et animale. |
|
(8) |
Le 9 décembre 2010, le groupe scientifique BIOHAZ de l’EFSA a adopté un avis sur la révision de l’évaluation quantitative des risques d’ESB liés aux PAT (7). Il a conclu que «sur la base des données de surveillance de l’ESB dans l’Union européenne en 2009 et conformément au modèle de l’EFSA pour l’évaluation quantitative des risques liés aux PAT, dans l’hypothèse d’une contamination de 0,1 % (limite de détection des PAT dans les aliments pour animaux) avec des PAT issues de non-ruminants, la moyenne estimée de la charge infectieuse totale d’ESB qui pourrait pénétrer annuellement dans l’alimentation des bovins dans l’Union serait équivalente à 0,2 dose infectieuse à 50 % par voie orale chez les bovins» et estimé que «cela correspondait, dans la population bovine de l’Union, à l’infection de moins d’un animal supplémentaire par an par l’ESB, avec une limite supérieure de confiance à 95 %». |
|
(9) |
Dans sa «Résolution du Parlement européen du 8 mars 2011 sur le déficit de l’Union en protéines végétales: quelle solution à un problème ancien?» (8), le Parlement européen invite la Commission à lui présenter, ainsi qu’au Conseil, une proposition législative visant à autoriser l’utilisation des PAT issues de résidus d’abattage pour la production d’aliments pour animaux monogastriques (porcs et volaille), sous réserve que les ingrédients proviennent de viandes déclarées propres à la consommation humaine et que l’interdiction du recyclage intraspécifique et du cannibalisme induit soit appliquée intégralement et contrôlée. |
|
(10) |
Dans sa «Résolution du Parlement européen du 6 juillet 2011 sur la législation de l’Union européenne sur les encéphalopathies spongiformes transmissibles et sur les contrôles des aliments pour animaux et des denrées alimentaires — Mise en œuvre et perspectives» (9), le Parlement est favorable, eu égard notamment au déficit actuel de l’Union en protéines, à la proposition de la Commission visant à supprimer les dispositions de la législation de l’Union qui interdisent de nourrir les non-ruminants avec des PAT, sous réserve qu’elle s’applique uniquement aux non-herbivores, et sous certaines conditions. |
|
(11) |
Le Parlement préconise dans sa résolution que les méthodes de production et de stérilisation utilisées pour les protéines animales transformées respectent les normes de sécurité les plus rigoureuses et les règles établies par le règlement (CE) no 1069/2009 et utilisent la technologie la plus récente et la plus sûre qui existe. Il demande que les interdictions existantes concernant le recyclage intra-espèce restent en place, que les chaînes de production de PAT à partir d’espèces différentes soient totalement séparées et que cette séparation soit contrôlée par les autorités compétentes dans les États membres et fasse l’objet d’un audit par la Commission. Le Parlement indique, en outre, qu’avant la mise en œuvre de la levée de l’interdiction, une méthode fiable propre à chaque espèce doit être adoptée pour identifier l’espèce d’origine des protéines contenues dans les produits pour l’alimentation animale contenant des PAT, de façon à pouvoir exclure le recyclage intra-espèce et la présence de PAT, que la production de PAT à partir de matériels des catégories 1 et 2 doit être interdite et que seuls les matériels de catégorie 3 propres à la consommation humaine doivent être utilisés pour la production de PAT. Enfin, il rejette l’utilisation de PAT provenant de non-ruminants ou de ruminants dans les aliments pour ruminants. |
|
(12) |
Le 9 mars 2012, le laboratoire de référence de l’Union européenne pour la détection de protéines animales dans l’alimentation animale (EURL-AP) a validé une nouvelle méthode de diagnostic fondée sur l’ADN permettant de détecter de très faibles niveaux de matériels provenant de ruminants, susceptibles de se trouver dans les aliments pour animaux (10). Cette méthode peut être utilisée pour effectuer des contrôles de routine sur les PAT et les aliments composés pour animaux contenant des PAT, afin de vérifier l’absence de protéines provenant de ruminants. |
|
(13) |
Actuellement, il n’existe aucune méthode de diagnostic validée permettant de déceler la présence de matériaux provenant de porcins ou de volailles dans les aliments pour animaux. Par conséquent, il ne serait pas possible de contrôler la bonne mise en œuvre de l’interdiction du recyclage intraspécifique si l’utilisation de PAT d’origine porcine dans l’alimentation des volailles et l’utilisation de PAT provenant de volailles dans l’alimentation porcine étaient de nouveau autorisées. |
|
(14) |
La production aquacole ne suscite aucune préoccupation quant au respect de l’interdiction du recyclage intraspécifique, dans la mesure où les exigences de canalisation actuellement en place pour l’utilisation des farines de poisson dans l’alimentation des animaux d’aquaculture ont déjà fait la preuve de leur efficacité. |
|
(15) |
À l’exception des farines de poisson et des aliments composés pour animaux contenant des farines de poisson, qui sont déjà autorisés pour l’alimentation des non-ruminants, il convient donc que les PAT provenant de non-ruminants et les aliments pour animaux contenant de telles PAT soient à nouveau autorisés pour l’alimentation des animaux d’aquaculture. Des conditions strictes de collecte, de transport et de transformation de ces produits doivent s’appliquer, de manière à éviter tout risque de contamination croisée avec des protéines provenant de ruminants. En outre, il convient de prélever et d’analyser régulièrement des échantillons des PAT et des aliments composés pour animaux contenant ces PAT, pour vérifier l’absence de contamination croisée avec des protéines provenant de ruminants. |
|
(16) |
Il convient donc de supprimer l’interdiction d’alimenter des animaux d’aquaculture avec des PAT provenant de non-ruminants, énoncée à l’annexe IV du règlement (CE) no 999/2001. Dans un souci de clarté de la législation de l’Union, il y a lieu de remplacer l’intégralité de l’annexe IV par l’annexe IV figurant à l’annexe du présent règlement. |
|
(17) |
Le point 1 de l’annexe I du règlement (CE) no 999/2001 fait référence à des définitions d’aliments pour animaux et de sous-produits animaux non destinés à la consommation humaine figurant dans des actes juridiques de l’Union qui ont depuis été abrogés. Dans un souci de clarté de la législation de l’Union, ces références doivent être remplacées par des références aux définitions respectives figurant dans les actes juridiques en vigueur. L’annexe I du règlement (CE) no 999/2001 doit donc être modifiée conformément à l’annexe du présent règlement. |
|
(18) |
Étant donné que les États membres et les opérateurs économiques du secteur de l’alimentation animale ont besoin de suffisamment de temps pour adapter leurs procédures de contrôle aux nouvelles exigences introduites par le présent règlement, celui-ci ne doit pas s’appliquer immédiatement après son entrée en vigueur. |
|
(19) |
Il convient dès lors de modifier le règlement (CE) no 999/2001 en conséquence. |
|
(20) |
Les mesures prévues au présent règlement sont conformes à l’avis du Comité permanent de la chaîne alimentaire et de la santé animale, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
Les annexes I et IV du règlement (CE) no 999/2001 sont modifiées conformément à l’annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l’Union européenne.
Il s’applique à compter du 1er juin 2013.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 16 janvier 2013.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 147 du 31.5.2001, p. 1.
(2) JO L 300 du 14.11.2009, p. 1.
(3) COM/2010/0384.
(4) «Opinion of the Scientific Panel on Biological Hazards on a request from the European Parliament on the assessment of the health risks of feeding of ruminants with fishmeal in relation to the risk of TSE», The EFSA Journal (2007) 443, p. 1.
(5) «Opinion of the Scientific Panel on Biological Hazards on a request from the European Parliament on Certain Aspects related to the Feeding of Animal Proteins to Farm Animals», The EFSA Journal (2007) 576, p. 1.
(6) http://register.consilium.europa.eu/pdf/fr/10/st13/st13889-ad01.fr10.pdf
(7) «Opinion of the Scientific Panel on Biological Hazards on a revision of the quantitative risk assessment (QRA) of the BSE risk posed by processed animal protein (PAPs)», The EFSA Journal (2011);9(1):1947.
(8) Texte adopté, P7_TA(2011)0084.
(9) Texte adopté, P7_TA(2011)0328.
(10) http://eurl.craw.eu/index.php?page=24&id=10
ANNEXE
Les annexes I et IV du règlement (CE) no 999/2001 sont modifiées comme suit:
|
1) |
Le point 1 de l’annexe I est remplacé par le texte suivant:
|
|
2) |
L’annexe IV est remplacée par le texte suivant: «ANNEXE IV ALIMENTATION DES ANIMAUX CHAPITRE I Extensions de l’interdiction énoncée à l’article 7, paragraphe 1 Conformément à l’article 7, paragraphe 2, l’interdiction énoncée à l’article 7, paragraphe 1, est étendue à l’utilisation:
CHAPITRE II Dérogations aux interdictions énoncées à l’article 7, paragraphe 1, et au chapitre I Conformément à l’article 7, paragraphe 3, premier alinéa, les interdictions énoncées à l’article 7, paragraphe 1, et au chapitre I ne s’appliquent pas à l’utilisation:
CHAPITRE III Conditions générales d’application de certaines dérogations prévues au chapitre II SECTION A Transport de matières premières pour aliments des animaux et d’aliments composés pour animaux destinés à être utilisés pour l’alimentation d’animaux d’élevage non ruminants
SECTION B Production d’aliments composés pour animaux destinés à être utilisés pour l’alimentation d’animaux d’élevage non ruminants
SECTION C Importation de matières premières pour aliments des animaux et d’aliments composés pour animaux destinés à être utilisés pour l’alimentation d’animaux d’élevage non ruminants autres que les animaux à fourrure Les importateurs veillent à ce qu’avant leur mise en libre pratique dans l’Union, les lots contenant les matières premières pour aliments des animaux et les aliments composés pour animaux suivants, destinés à l’alimentation des animaux d’élevage non ruminants autres que les animaux à fourrure conformément au chapitre II de la présente annexe, soient analysés conformément aux méthodes d’analyse applicables en matière d’identification des constituants d’origine animale pour le contrôle de l’alimentation animale figurant à l’annexe VI du règlement (CE) no 152/2009, afin de vérifier l’absence de constituants d’origine animale non autorisés:
SECTION D Utilisation et entreposage dans les exploitations d’aliments pour animaux destinés à être utilisés pour l’alimentation d’animaux d’élevage non ruminants
CHAPITRE IV Conditions particulières d’application de certaines dérogations prévues au chapitre II SECTION A Conditions particulières applicables à la production et à l’utilisation de farines de poisson et d’aliments composés pour animaux contenant des farines de poisson, destinés à être utilisés dans l’alimentation d’animaux d’élevage non ruminants autres que les animaux à fourrure Les conditions particulières suivantes s’appliquent à la production et à l’utilisation de farines de poisson et d’aliments composés pour animaux contenant des farines de poisson destinés à être utilisés dans l’alimentation d’animaux d’élevage non ruminants autres que les animaux à fourrure:
SECTION B Conditions particulières applicables à l’utilisation de phosphate dicalcique et de phosphate tricalcique d’origine animale et d’aliments composés pour animaux contenant ces phosphates, destinés à être utilisés dans l’alimentation d’animaux d’élevage non ruminants autres que les animaux à fourrure Le document commercial ou le certificat sanitaire, selon le cas, qui accompagne le phosphate dicalcique ou le phosphate tricalcique d’origine animale, les aliments composés pour animaux contenant de tels phosphates et tout emballage renfermant ces produits doivent porter clairement la mention “Contient du phosphate dicalcique ou tricalcique d’origine animale — Ne pas utiliser dans l’alimentation des ruminants”. SECTION C Conditions particulières applicables à la production et à l’utilisation de produits sanguins dérivés de non-ruminants et d’aliments composés pour animaux contenant de tels produits, destinés à être utilisés dans l’alimentation d’animaux d’élevage non ruminants autres que les animaux à fourrure Les conditions particulières suivantes s’appliquent à la production et à l’utilisation de produits sanguins dérivés de non-ruminants et d’aliments composés pour animaux contenant de tels produits sanguins qui sont destinés à être utilisés dans l’alimentation d’animaux d’élevage non ruminants autres que les animaux à fourrure:
SECTION D Conditions particulières applicables à la production et à l’utilisation de protéines animales transformées dérivées de non-ruminants, autres que des farines de poisson, et d’aliments composés pour animaux contenant de telles protéines animales transformées, destinés à être utilisés pour l’alimentation d’animaux d’aquaculture Les conditions particulières suivantes s’appliquent à la production et à l’utilisation de protéines animales transformées dérivées de non-ruminants, autres que des farines de poisson, et d’aliments composés pour animaux contenant de telles protéines animales transformées, qui sont destinés à être utilisés pour l’alimentation d’animaux d’aquaculture:
SECTION E Conditions particulières applicables à la production, à la mise sur le marché et à l’utilisation d’aliments d’allaitement contenant des farines de poisson destinés à l’alimentation de ruminants non sevrés Les conditions particulières suivantes s’appliquent à la production, à la mise sur le marché et à l’utilisation d’aliments d’allaitement contenant des farines de poisson dans l’alimentation de ruminants d’élevage non sevrés:
CHAPITRE V Conditions générales SECTION A Listes Les États membres tiennent à jour et à la disposition du public:
SECTION B Transport des matières premières pour aliments des animaux et des aliments composés pour animaux contenant des produits dérivés de ruminants
SECTION C Production d’aliments composés pour animaux contenant des produits dérivés de ruminants Les aliments composés pour animaux contenant des produits dérivés de ruminants autres que ceux énumérés aux points a), b) et c) ne sont pas produits dans des établissements qui produisent des aliments pour animaux d’élevage autres que les animaux à fourrure:
SECTION D Utilisation et entreposage, dans les exploitations, de matières premières pour aliments des animaux et d’aliments composés pour animaux d’élevage contenant des produits dérivés de ruminants L’utilisation et l’entreposage de matières premières pour aliments des animaux et d’aliments composés pour animaux d’élevage contenant des produits dérivés de ruminants autres que ceux énumérés aux points a), b) et c) sont interdits dans les exploitations détenant des animaux d’élevage autres que les animaux à fourrure:
SECTION E Exportation de protéines animales transformées et de produits contenant de telles protéines
SECTION F Contrôles officiels
|
(1) JO L 300 du 14.11.2009, p. 1.
(2) JO L 54 du 26.2.2011, p. 1.
(3) JO L 31 du 1.2.2002, p. 1.
(4) JO L 229 du 1.9.2009, p. 1.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/17 |
RÈGLEMENT (UE) N o 57/2013 DE LA COMMISSION
du 23 janvier 2013
modifiant le règlement (CE) no 1418/2007 concernant l’exportation de certains déchets destinés à être valorisés vers certains pays n’appartenant pas à l’OCDE
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CE) no 1013/2006 du Parlement européen et du Conseil du 14 juin 2006 concernant les transferts de déchets (1), et notamment son article 37, paragraphe 2, troisième alinéa,
considérant ce qui suit:
|
(1) |
L’annexe du règlement (CE) no 1418/2007 de la Commission du 29 novembre 2007 concernant l’exportation de certains déchets destinés à être valorisés, énumérés à l’annexe III ou IIIA du règlement (CE) no 1013/2006 du Parlement européen et du Conseil, vers certains pays auxquels la décision de l’OCDE sur le contrôle des mouvements transfrontières de déchets ne s’applique pas (2) a été modifiée par le règlement (UE) no 674/2012 (3). |
|
(2) |
Conformément à l’article 37, paragraphes 1 et 2, du règlement (CE) no 1013/2006, la Commission a tenu compte de la réponse que la Malaisie a transmise à sa demande écrite. Par la suite, la Malaisie a indiqué par écrit que les informations qu’elle avait fournies dans sa réponse concernant la sous-entrée B1100 (mattes de galvanisation) ainsi que les entrées B3010 et GH013 ne reflétaient pas la législation et les procédures en vigueur, qui n’interdisaient pas les importations de ces déchets. Elle demandait donc que la procédure soit modifiée et que l’option c) remplace l’option a) pour la sous-entrée B1100 – mattes de galvanisation – et que l’option d) remplace l’option a) pour les entrées B3010 et GH013. |
|
(3) |
Afin de rectifier cette erreur et étant donné l’incidence sur les opérateurs économiques, l’annexe du règlement (CE) no 1418/2007 doit être modifiée en conséquence, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
L’annexe du règlement (CE) no 1418/2007 est modifiée conformément à l’annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le quatorzième jour suivant celui de sa publication au Journal officiel de l’Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 190 du 12.7.2006, p. 1.
(2) JO L 316 du 4.12.2007, p. 6.
(3) JO L 196 du 24.7.2012, p. 12.
ANNEXE
L’annexe du règlement (CE) no 1418/2007 est modifiée comme suit:
|
1) |
l’entrée suivante relative à la Malaisie:
est remplacée par les entrées suivantes:
|
|
2) |
l’entrée suivante relative à la Malaisie:
est remplacée par l’entrée suivante:
|
|
3) |
l’entrée suivante relative à la Malaisie:
est remplacée par les entrées suivantes:
|
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/19 |
RÈGLEMENT D’EXÉCUTION (UE) N o 58/2013 DE LA COMMISSION
du 23 janvier 2013
modifiant le règlement (CEE) no 2454/93 fixant certaines dispositions d’application du règlement (CEE) no 2913/92 du Conseil établissant le code des douanes communautaire
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CEE) no 2913/92 du Conseil du 12 octobre 1992 établissant le code des douanes communautaire (1), et notamment son article 247,
considérant ce qui suit:
|
(1) |
Le règlement (CE) no 1875/2006 de la Commission du 18 décembre 2006 modifiant le règlement (CEE) no 2454/93 fixant certaines dispositions d’application du règlement (CEE) no 2913/92 du Conseil établissant le code des douanes communautaire (2) a introduit la notion d’opérateurs économiques agréés (AEO, authorised economic operators). Il convient que les opérateurs économiques qui remplissent les conditions d’obtention du statut complet d’opérateur économique agréé ou du statut d’opérateur économique agréé «Sécurité et sûreté» soient considérés comme des partenaires fiables dans la chaîne d’approvisionnement et bénéficient donc de facilités en ce qui concerne les contrôles douaniers en matière de sécurité et de sûreté. |
|
(2) |
L’Union reconnaît les programmes de partenariat dans le domaine commercial de certains pays tiers qui ont été élaborés conformément au cadre de normes visant à sécuriser et à faciliter le commerce mondial de l’Organisation mondiale des douanes. Par conséquent, l’Union accorde des facilités aux opérateurs économiques d’un pays tiers qui bénéficient du statut de membre dans le cadre du programme de l’autorité douanière de ce pays tiers. Il est donc nécessaire d’introduire des moyens d’identifier, dans les déclarations sommaires d’entrée, les opérateurs économiques qui bénéficient du statut de membre en vertu des programmes de partenariat dans le domaine commercial des pays tiers. Les facilités considérées ne seront pas accordées sans une identification appropriée de ces opérateurs économiques dans les déclarations sommaires d’entrée. |
|
(3) |
Par conséquent, il convient d’adapter l’annexe 30 bis du règlement (CEE) no 2454/93 de la Commission (3) afin de permettre l’indication du numéro d’identification unique des opérateurs économiques des pays tiers. |
|
(4) |
Il convient dès lors de modifier le règlement (CEE) no 2454/93 en conséquence. |
|
(5) |
Les mesures prévues au présent règlement sont conformes à l’avis du comité du code des douanes, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
L’annexe 30 bis du règlement (CEE) no 2454/93 est modifiée conformément à l’annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le 31 janvier 2013.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 302 du 19.10.1992, p. 1.
(2) JO L 360 du 19.12.2006, p. 64.
(3) JO L 253 du 11.10.1993, p. 1.
ANNEXE
À l’annexe 30 bis du règlement (CEE) no 2454/93, section 4 «Notes explicatives sur les données», le troisième alinéa de la note explicative sur la donnée «Expéditeur» relative à la déclaration sommaire d’entrée est remplacé par le texte suivant:
«Déclaration sommaire d’entrée
Cette information prend la forme du numéro EORI de l’expéditeur lorsque la personne déposant la déclaration sommaire dispose de ce numéro.
Lorsque des facilités sont accordées dans le cadre d’un programme de partenariat dans le domaine commercial élaboré par un pays tiers et reconnu par l’Union, cette information peut prendre la forme d’un numéro d’identification unique délivré dans le pays tiers qui a été communiqué à l’Union par le pays tiers concerné. Ce numéro peut être utilisé lorsque la personne déposant la déclaration sommaire en dispose.
La structure du numéro est la suivante:
|
Champ |
Contenu |
Type de champ |
Format |
Exemples |
|
1 |
Identifiant du pays tiers (code pays ISO alpha-2) |
Alphabétique 2 |
a2 |
US JP |
|
2 |
Numéro d’identification unique délivré dans un pays tiers |
Alphanumérique maximum 15 |
an..15 |
1234567890ABCDE AbCd9875F pt20130101aa |
Exemples: “US1234567890ABCDE” pour un expéditeur des États-Unis (code pays: US) dont le numéro d’identification unique est “1234567890ABCDE”; “JPAbCd9875F” pour un expéditeur du Japon (code pays: JP) dont le numéro d’identification unique est “AbCd9875F”; “USpt20130101aa” pour un expéditeur des États-Unis (code pays: US) dont le numéro d’identification unique est “pt20130101aa”.
Identifiant du pays tiers: la codification alphabétique de l’Union pour les pays et territoires est fondée sur la norme ISO codes alpha 2 (a2) en vigueur pour autant qu’elle soit compatible avec les codes pays établis conformément à l’article 5, paragraphe 2, du règlement (CE) no 471/2009 du Parlement européen et du Conseil du 6 mai 2009 concernant les statistiques communautaires relatives au commerce extérieur avec les pays tiers et abrogeant le règlement (CE) no 1172/95 du Conseil (1).
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/21 |
RÈGLEMENT D’EXÉCUTION (UE) N o 59/2013 DE LA COMMISSION
du 23 janvier 2013
modifiant l’annexe du règlement (UE) no 37/2010 relatif aux substances pharmacologiquement actives et à leur classification en ce qui concerne les limites maximales de résidus dans les aliments d’origine animale, concernant la substance monensin
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CE) no 470/2009 du Parlement européen et du Conseil du 6 mai 2009 établissant des procédures communautaires pour la fixation des limites de résidus des substances pharmacologiquement actives dans les aliments d’origine animale, abrogeant le règlement (CEE) no 2377/90 du Conseil et modifiant la directive 2001/82/CE du Parlement européen et du Conseil et le règlement (CE) no 726/2004 du Parlement européen et du Conseil (1), et notamment son article 14, en liaison avec son article 17,
vu l’avis de l’Agence européenne des médicaments formulé par le comité des médicaments à usage vétérinaire,
considérant ce qui suit:
|
(1) |
Les limites maximales de résidus (ci-après «LMR») des substances pharmacologiquement actives destinées à être utilisées dans l’Union européenne dans des médicaments vétérinaires pour les animaux producteurs d’aliments ou dans des produits biocides utilisés dans l’élevage devraient être fixées conformément au règlement (CE) no 470/2009. |
|
(2) |
Les substances pharmacologiquement actives et leur classification en ce qui concerne les limites maximales de résidus dans les aliments d’origine animale figurent à l’annexe du règlement (UE) no 37/2010 de la Commission du 22 décembre 2009 relatif aux substances pharmacologiquement actives et à leur classification en ce qui concerne les limites maximales de résidus dans les aliments d’origine animale (2). |
|
(3) |
Le monensin figure actuellement dans le tableau 1 de l’annexe du règlement (UE) no 37/2010 en tant que substance autorisée, pour le muscle, la graisse, le foie, les reins et le lait des bovins. |
|
(4) |
Une demande de modification de l’entrée pour le monensin a été soumise à l’Agence européenne des médicaments. |
|
(5) |
Des données supplémentaires ont été fournies par le demandeur et évaluées par le comité des médicaments à usage vétérinaire. Il s’ensuit que ledit comité recommande la modification des LMR actuelles pour le monensin. |
|
(6) |
Il convient dès lors de modifier en conséquence les mentions relatives au monensin figurant dans le tableau 1 de l’annexe du règlement (UE) n 37/2010. |
|
(7) |
Il y a lieu de prévoir un délai raisonnable afin de permettre aux parties concernées de procéder à toute adaptation nécessaire pour se conformer à la nouvelle LMR. |
|
(8) |
Les mesures prévues par le présent règlement sont conformes à l’avis du comité permanent des médicaments vétérinaires, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
L’annexe du règlement (UE) no 37/2010 est modifiée conformément aux indications figurant à l’annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l'Union européenne.
Il s’applique à compter du 25 mars 2013.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 152 du 16.6.2009, p. 11.
(2) JO L 15 du 20.1.2010, p. 1.
ANNEXE
Dans le tableau 1 de l’annexe du règlement (UE) no 37/2010, l’entrée relative à la substance monensin est remplacée par la suivante:
|
Substance pharmacologiquement active |
Résidu marqueur |
Espèce animale |
LMR |
Denrées cibles |
Autres dispositions [conformément à l’article 14, paragraphe 7, du règlement (CE) no 470/2009] |
Classification thérapeutique |
|
«Monensin |
Monensin A |
Bovins |
2 μg/kg |
Muscle |
NÉANT |
Agents anti-infectieux/antibiotiques» |
|
10 μg/kg |
Graisse |
|||||
|
50 μg/kg |
Foie |
|||||
|
10 μg/kg |
Reins |
|||||
|
2 μg/kg |
Lait |
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/23 |
RÈGLEMENT D’EXÉCUTION (UE) N o 60/2013 DE LA COMMISSION
du 23 janvier 2013
modifiant pour la cent quatre-vingt-cinquième fois le règlement (CE) no 881/2002 du Conseil instituant certaines mesures restrictives spécifiques à l’encontre de certaines personnes et entités liées au réseau Al-Qaida
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CE) no 881/2002 du Conseil du 27 mai 2002 instituant certaines mesures restrictives spécifiques à l’encontre de certaines personnes et entités liées au réseau Al-Qaida (1), et notamment son article 7, paragraphe 1, point a), et son article 7 bis, paragraphe 5,
considérant ce qui suit:
|
(1) |
L’annexe I du règlement (CE) no 881/2002 énumère les personnes, groupes et entités auxquels s’applique le gel des fonds et des ressources économiques ordonné par ce règlement. |
|
(2) |
Le 14 janvier 2013, le Comité des sanctions du Conseil de sécurité des Nations unies a décidé de radier une personne physique de la liste des personnes, groupes et entités auxquels s’applique le gel des fonds et des ressources économiques après avoir examiné la demande de radiation présentée par cette personne, ainsi que le rapport d’ensemble du Médiateur institué conformément à la résolution 1904 (2009) du Conseil de sécurité des Nations unies. |
|
(3) |
Il convient donc de mettre à jour l’annexe I du règlement (CE) no 881/2002 en conséquence, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
L’annexe I du règlement (CE) no 881/2002 est modifiée conformément à l’annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le jour suivant celui de sa publication au Journal officiel de l’Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission, au nom du président,
Chef du service des instruments de politique étrangère
(1) JO L 139 du 29.5.2002, p. 9.
ANNEXE
L’annexe I du règlement (CE) no 881/2002 est modifiée comme suit:
La mention suivante, qui figure dans la rubrique «Personnes physiques», est supprimée:
«Adel Abdul Jalil Ibrahim Batterjee [alias a) ‘Adil Al-Battarjee, b) Adel Batterjee, c) ‘Adil ‘Abd al Jalil Batarji, d) Adel AbdulJaleel I. Batterjee]. Adresse: 2 Helmi Kutbi Street, Jeddah, Arabie saoudite. Né le a) 1.7.1946, b) 1.6.1946, à Jeddah, Arabie Saoudite. Nationalité: saoudienne. Passeport no: 572010 (délivré le 22.12.2004, expire le 28.10.2009).»
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/25 |
RÈGLEMENT D'EXÉCUTION (UE) N o 61/2013 DE LA COMMISSION
du 23 janvier 2013
établissant les valeurs forfaitaires à l'importation pour la détermination du prix d'entrée de certains fruits et légumes
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l'Union européenne,
vu le règlement (CE) no 1234/2007 du Conseil du 22 octobre 2007 portant organisation commune des marchés dans le secteur agricole et dispositions spécifiques en ce qui concerne certains produits de ce secteur (règlement «OCM unique») (1),
vu le règlement d'exécution (UE) no 543/2011 de la Commission du 7 juin 2011 portant modalités d’application du règlement (CE) no 1234/2007 du Conseil en ce qui concerne les secteurs des fruits et légumes et des fruits et légumes transformés (2), et notamment son article 136, paragraphe 1,
considérant ce qui suit:
|
(1) |
Le règlement d’exécution (UE) no 543/2011 prévoit, en application des résultats des négociations commerciales multilatérales du cycle d'Uruguay, les critères pour la fixation par la Commission des valeurs forfaitaires à l'importation des pays tiers, pour les produits et les périodes figurant à l'annexe XVI, partie A, dudit règlement. |
|
(2) |
La valeur forfaitaire à l'importation est calculée chaque jour ouvrable, conformément à l'article 136, paragraphe 1, du règlement d'exécution (UE) no 543/2011, en tenant compte des données journalières variables. Il importe, par conséquent, que le présent règlement entre en vigueur le jour de sa publication au Journal officiel de l’Union européenne, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
Les valeurs forfaitaires à l'importation visées à l'article 136 du règlement d’exécution (UE) no 543/2011 sont fixées à l'annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le jour de sa publication au Journal officiel de l'Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission, au nom du président,
José Manuel SILVA RODRÍGUEZ
Directeur général de l'agriculture et du développement rural
(1) JO L 299 du 16.11.2007, p. 1.
(2) JO L 157 du 15.6.2011, p. 1.
ANNEXE
Valeurs forfaitaires à l'importation pour la détermination du prix d'entrée de certains fruits et légumes
|
(EUR/100 kg) |
||
|
Code NC |
Code des pays tiers (1) |
Valeur forfaitaire à l'importation |
|
0702 00 00 |
MA |
65,3 |
|
TN |
84,9 |
|
|
TR |
103,3 |
|
|
ZZ |
84,5 |
|
|
0707 00 05 |
EG |
200,0 |
|
JO |
182,1 |
|
|
MA |
158,2 |
|
|
TR |
166,4 |
|
|
ZZ |
176,7 |
|
|
0709 91 00 |
EG |
128,6 |
|
ZZ |
128,6 |
|
|
0709 93 10 |
EG |
105,4 |
|
MA |
92,6 |
|
|
TR |
138,3 |
|
|
ZZ |
112,1 |
|
|
0805 10 20 |
EG |
54,1 |
|
MA |
56,8 |
|
|
TN |
54,0 |
|
|
TR |
63,8 |
|
|
ZA |
46,1 |
|
|
ZZ |
55,0 |
|
|
0805 20 10 |
MA |
89,0 |
|
ZZ |
89,0 |
|
|
0805 20 30, 0805 20 50, 0805 20 70, 0805 20 90 |
IL |
180,3 |
|
KR |
138,2 |
|
|
MA |
158,2 |
|
|
TR |
84,6 |
|
|
ZZ |
140,3 |
|
|
0805 50 10 |
EG |
56,9 |
|
TR |
74,0 |
|
|
ZZ |
65,5 |
|
|
0808 10 80 |
CN |
100,8 |
|
MK |
35,9 |
|
|
US |
176,0 |
|
|
ZZ |
104,2 |
|
|
0808 30 90 |
CN |
51,8 |
|
US |
132,9 |
|
|
ZZ |
92,4 |
|
(1) Nomenclature des pays fixée par le règlement (CE) no 1833/2006 de la Commission (JO L 354 du 14.12.2006, p. 19). Le code «ZZ» représente «autres origines».
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/27 |
RÈGLEMENT D'EXÉCUTION (UE) N o 62/2013 DE LA COMMISSION
du 23 janvier 2013
portant fixation d'un pourcentage d'acceptation pour la délivrance des certificats d'exportation, rejet des demandes de certificats d'exportation et suspension du dépôt de demandes de certificats d'exportation pour le sucre hors quota
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l'Union européenne,
vu le règlement (CE) no 1234/2007 du Conseil du 22 octobre 2007 portant organisation commune des marchés dans le secteur agricole et dispositions spécifiques en ce qui concerne certains produits de ce secteur (règlement «OCM unique») (1),
vu le règlement (CE) no 951/2006 de la Commission du 30 juin 2006 portant modalités d'application du règlement (CE) no 318/2006 du Conseil en ce qui concerne les échanges avec les pays tiers dans le secteur du sucre (2), et notamment son article 7 sexies en liaison avec son article 9, paragraphe 1,
considérant ce qui suit:
|
(1) |
Aux termes de l'article 61, premier alinéa, point d), du règlement (CE) no 1234/2007, le sucre produit pendant la campagne de commercialisation en sus du quota visé à l'article 56 dudit règlement ne peut être exporté que dans la limite des quantités fixées par la Commission. |
|
(2) |
Le règlement d'exécution (UE) no 394/2012 de la Commission du 8 mai 2012 fixant la limite quantitative applicable aux exportations de sucre et d'isoglucose hors quota jusqu'à la fin de la campagne de commercialisation 2012/2013 (3) établit les limites mentionnées ci-dessus. |
|
(3) |
Les quantités de sucre couvertes par les demandes de certificats d'exportation excèdent la limite quantitative fixée par le règlement d'exécution (UE) no 394/2012. Il y a donc lieu d'établir un pourcentage d’acceptation pour les quantités faisant l'objet des demandes présentées du 14 au 18 janvier 2013. Il convient dès lors de rejeter toutes les demandes de certificats d'exportation pour le sucre introduites après le 18 janvier 2013 et de suspendre le dépôt de demandes de certificats d'exportation, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
1. Les certificats d'exportation concernant le sucre hors quota pour lesquels des demandes ont été présentées du 14 au 18 janvier 2013 sont délivrés pour les quantités demandées, affectées d'un pourcentage d'acceptation de 40,367343 %.
2. Les demandes de certificats d'exportation pour le sucre hors quota présentées les 21, 22, 23, 24 et 25 janvier 2013 sont rejetées.
3. Le dépôt de demandes de certificats d'exportation pour le sucre hors quota est suspendu pour la période comprise entre le 28 janvier 2013 et le 30 septembre 2013.
Article 2
Le présent règlement entre en vigueur le jour suivant celui de sa publication au Journal officiel de l’Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission, au nom du président,
José Manuel SILVA RODRÍGUEZ
Directeur général de l'agriculture et du développement rural
(1) JO L 299 du 16.11.2007, p. 1.
(2) JO L 178 du 1.7.2006, p. 24.
(3) JO L 123 du 9.5.2012, p. 30.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/28 |
RÈGLEMENT D'EXÉCUTION (UE) N o 63/2013 DE LA COMMISSION
du 23 janvier 2013
modifiant les prix représentatifs et les montants des droits additionnels à l'importation pour certains produits du secteur du sucre, fixés par le règlement d'exécution (UE) no 892/2012 pour la campagne 2012/2013
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l'Union européenne,
vu le règlement (CE) no 1234/2007 du Conseil du 22 octobre 2007 portant organisation commune des marchés dans le secteur agricole et dispositions spécifiques en ce qui concerne certains produits de ce secteur (règlement «OCM unique») (1),
vu le règlement (CE) no 951/2006 de la Commission du 30 juin 2006 portant modalités d'application du règlement (CE) no 318/2006 du Conseil en ce qui concerne les échanges avec les pays tiers dans le secteur du sucre (2), et notamment son article 36, paragraphe 2, deuxième alinéa, deuxième phrase,
considérant ce qui suit:
|
(1) |
Les montants des prix représentatifs et des droits additionnels applicables à l'importation de sucre blanc, de sucre brut et de certains sirops pour la campagne 2012/2013 ont été fixés par le règlement d'exécution (UE) no 892/2012 de la Commission (3). Ces prix et droits ont été modifiés en dernier lieu par le règlement d'exécution (UE) no 48/2013 de la Commission (4). |
|
(2) |
Les données dont la Commission dispose actuellement conduisent à modifier lesdits montants, conformément à l'article 36 du règlement (CE) no 951/2006. |
|
(3) |
En raison de la nécessité d'assurer que cette mesure s'applique le plus rapidement possible après la mise à disposition des données actualisées, il convient que le présent règlement entre en vigueur le jour de sa publication, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
Les prix représentatifs et les droits additionnels applicables à l'importation des produits visés à l'article 36 du règlement (CE) no 951/2006, fixés par le règlement d'exécution (UE) no 892/2012 pour la campagne 2012/2013, sont modifiés et figurent à l’annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le jour de sa publication au Journal officiel de l’Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission, au nom du président,
José Manuel SILVA RODRÍGUEZ
Directeur général de l'agriculture et du développement rural
(1) JO L 299 du 16.11.2007, p. 1.
(2) JO L 178 du 1.7.2006, p. 24.
(3) JO L 263 du 28.9.2012, p. 37.
(4) JO L 18 du 22.1.2013, p. 15.
ANNEXE
Montants modifiés des prix représentatifs et des droits additionnels à l'importation du sucre blanc, du sucre brut et des produits du code NC 1702 90 95 applicables à partir du 24 janvier 2013
|
(en EUR) |
||
|
Code NC |
Montant du prix représentatif par 100 kg net du produit en cause |
Montant du droit additionnel par 100 kg net du produit en cause |
|
1701 12 10 (1) |
31,88 |
1,59 |
|
1701 12 90 (1) |
31,88 |
5,16 |
|
1701 13 10 (1) |
31,88 |
1,72 |
|
1701 13 90 (1) |
31,88 |
5,59 |
|
1701 14 10 (1) |
31,88 |
1,72 |
|
1701 14 90 (1) |
31,88 |
5,59 |
|
1701 91 00 (2) |
36,96 |
6,75 |
|
1701 99 10 (2) |
36,96 |
3,25 |
|
1701 99 90 (2) |
36,96 |
3,25 |
|
1702 90 95 (3) |
0,37 |
0,30 |
(1) Fixation pour la qualité type telle que définie à l'annexe IV, point III, du règlement (CE) no 1234/2007.
(2) Fixation pour la qualité type telle que définie à l'annexe IV, point II, du règlement (CE) no 1234/2007.
(3) Fixation par 1 % de teneur en saccharose.
DÉCISIONS
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/30 |
DÉCISION D’EXÉCUTION DU CONSEIL
du 22 janvier 2013
modifiant la décision d’exécution 2011/77/UE sur l’octroi d’une assistance financière de l’Union à l’Irlande
(2013/48/UE)
LE CONSEIL DE L’UNION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (UE) no 407/2010 du Conseil du 11 mai 2010 établissant un mécanisme européen de stabilisation financière (1), et notamment son article 3, paragraphe 2,
vu la proposition de la Commission européenne,
considérant ce qui suit:
|
(1) |
Le Conseil a octroyé à l’Irlande, à sa demande, une assistance financière par décision d’exécution 2011/77/UE (2) afin de soutenir un ambitieux programme de réformes économiques et financières destiné à rétablir la confiance, à permettre à l’économie de renouer avec une croissance durable et à préserver la stabilité financière de l’Irlande, de la zone euro et de l’Union. |
|
(2) |
Conformément à l’article 3, paragraphe 9, de la décision d’exécution 2011/77/UE, la Commission européenne, en collaboration avec le FMI et en liaison avec la BCE, a procédé à la huitième évaluation de la mise en œuvre, de l’effectivité et de l’incidence économique et sociale des mesures convenues. |
|
(3) |
Des progrès significatifs ont été accomplis en vue d’atteindre les objectifs de désendettement des banques fixés dans le programme. Plus particulièrement, deux banques nationales ont déjà atteint ou sont en passe d’atteindre l’objectif d’un ratio prêts/dépôts de 122,5 %, qui devait initialement être atteint à la fin de l’année 2013 au plus tard. La banque nationale restante a déjà procédé à des cessions d’actifs non stratégiques et ses exigences de désendettement en vertu du programme seront réévaluées en tenant compte de la future décision de la Commission européenne sur son plan de restructuration. |
|
(4) |
Compte tenu de ces progrès significatifs, une modification du cadre de surveillance fixé dans le programme pour assurer un désendettement des banques compatible avec les objectifs nominaux de cession d’actifs non stratégiques et du cadre de surveillance renforcée conçu pour que les banques améliorent leur ratio de liquidité à court et à long terme contribuerait à prévenir toute distorsion indue dans la rémunération des dépôts bancaires et à préparer les banques à se conformer aux exigences de Bâle III en matière de liquidité. |
|
(5) |
Eu égard à ces évolutions et considérations, il convient de modifier la décision d’exécution 2011/77/UE, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
L’article 3 de la décision d’exécution 2011/77/UE est modifié comme suit:
|
1) |
Au paragraphe 8, le point c) est remplacé par le texte suivant:
|
|
2) |
Le paragraphe 10 est remplacé par le texte suivant: «10. En 2013, l’Irlande, conformément aux stipulations du protocole d’accord:
|
Article 2
L’Irlande est destinataire de la présente décision.
Fait à Bruxelles, le 22 janvier 2013.
Par le Conseil
Le président
M. NOONAN
(1) JO L 118 du 12.5.2010, p. 1.
(2) JO L 30 du 4.2.2011, p. 34.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/32 |
DÉCISION D’EXÉCUTION DE LA COMMISSION
du 22 janvier 2013
autorisant la mise sur le marché de la zéaxanthine de synthèse en tant que nouvel ingrédient alimentaire en application du règlement (CE) no 258/97 du Parlement européen et du Conseil
[notifiée sous le numéro C(2013) 110]
(Le texte en langue néerlandaise est le seul faisant foi.)
(2013/49/UE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CE) no 258/97 du Parlement européen et du Conseil du 27 janvier 1997 relatif aux nouveaux aliments et aux nouveaux ingrédients alimentaires (1), et notamment son article 7,
considérant ce qui suit:
|
(1) |
Le 1er juin 2004, la société DSM Nutritional Products VML a introduit auprès des autorités compétentes néerlandaises une demande de mise sur le marché de la zéaxanthine de synthèse en tant que nouvel ingrédient alimentaire. |
|
(2) |
Le 16 juin 2005, l’organisme néerlandais compétent en matière d’évaluation des denrées alimentaires a rendu son rapport d’évaluation initiale. Il concluait dans celui-ci que l’utilisation de la zéaxanthine de synthèse à une dose maximale de 20 mg par personne et par jour n’était pas susceptible de présenter un risque significatif pour la santé humaine. Il estimait cependant que les données présentées n’étaient pas suffisantes pour mener à terme l’évaluation de l’innocuité de cette substance. |
|
(3) |
Une évaluation supplémentaire était donc jugée nécessaire. |
|
(4) |
Le 1er août 2005, la Commission a transmis le rapport d’évaluation initiale à tous les États membres pour recueillir leurs observations. |
|
(5) |
Le 2 février 2007, le demandeur a informé la Commission que l’autorisation de la zéaxanthine devrait ne porter que sur son utilisation comme ingrédient dans les compléments alimentaires. |
|
(6) |
La Commission a consulté l’Autorité européenne de sécurité des aliments (EFSA) le 20 mars 2007. |
|
(7) |
Le 24 avril 2008, l’EFSA a adopté un avis scientifique sur l’innocuité de la zéaxanthine de synthèse utilisée comme ingrédient dans les compléments alimentaires (2) dans lequel elle concluait que les données existantes ne permettaient pas d’établir l’innocuité de la zéaxanthine de synthèse utilisée comme ingrédient dans les compléments alimentaires au niveau proposé de 20 mg par personne et par jour. |
|
(8) |
Le 25 janvier 2012, le demandeur a fourni des informations complémentaires et proposé de limiter la dose de zéaxanthine de synthèse en tant qu’ingrédient dans les compléments alimentaires à 2 mg par personne et par jour. |
|
(9) |
À la demande de la Commission, l’EFSA a été invitée à revoir son avis sur l’innocuité de la zéaxanthine de synthèse en tant que nouvel ingrédient alimentaire dans les compléments alimentaires à la lumière des informations complémentaires. Le 13 septembre 2012, l’EFSA a adopté une déclaration sur l’innocuité de la zéaxanthine de synthèse en tant qu’ingrédient dans les compléments alimentaires (3) dans laquelle elle a conclu que le niveau d’utilisation proposé par le demandeur ne pose pas de problèmes de sécurité. |
|
(10) |
Il ressort de l’évaluation scientifique que la zéaxanthine de synthèse satisfait aux critères prévus à l’article 3, paragraphe 1, du règlement (CE) no 258/97. |
|
(11) |
L’adjonction intentionnelle de zéaxanthine de synthèse aux denrées alimentaires pour colorer celles-ci relève du règlement (CE) no 1333/2008 du Parlement européen et du Conseil du 16 décembre 2008 sur les additifs alimentaires (4) et devrait être autorisée conformément audit règlement. |
|
(12) |
Les mesures prévues à la présente décision sont conformes à l’avis du comité permanent de la chaîne alimentaire et de la santé animale, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
La zéaxanthine de synthèse telle que spécifiée en annexe peut être mise sur le marché dans l’Union en tant que nouvel ingrédient alimentaire dans les compléments alimentaires à une dose maximale recommandée par le producteur de 2 mg par jour.
Article 2
La zéaxanthine de synthèse autorisée par la présente décision fait l’objet de la mention «zéaxanthine de synthèse» sur l’étiquette des denrées alimentaires qui en contiennent.
Article 3
La société DSM Nutritional Products, Alexander Fleminglaan 1, 2613 AX Delft, Pays-Bas, est destinataire de la présente décision.
Fait à Bruxelles, le 22 janvier 2013.
Par la Commission
Tonio BORG
Membre de la Commission
(1) JO L 43 du 14.2.1997, p. 1.
(2) EFSA Journal (2008) 728, p. 1 à 27.
(3) EFSA Journal 2012; 10(10):2891.
(4) JO L 354 du 31.12.2008, p. 16.
ANNEXE
SPÉCIFICATIONS DE LA ZÉAXANTHINE DE SYNTHÈSE
Définition La zéaxanthine est un pigment xanthophylle présent dans la nature; c’est un caroténoïde oxygéné. La zéaxanthine de synthèse est produite par une transformation chimique en plusieurs étapes à partir de molécules plus petites.
La zéaxanthine de synthèse se présente sous la forme d’une poudre à base de gélatine ou d’amidon («granules») desséchée par pulvérisation, avec ajout d’α-tocophérol et de palmitate d’ascorbyle, ou d’une suspension d’huile de maïs, avec ajout d’α-tocophérol.
Description: Poudre cristalline rouge orangé inodore ou quasiment inodore
Formule chimique: C40H56O2
Formule développée:
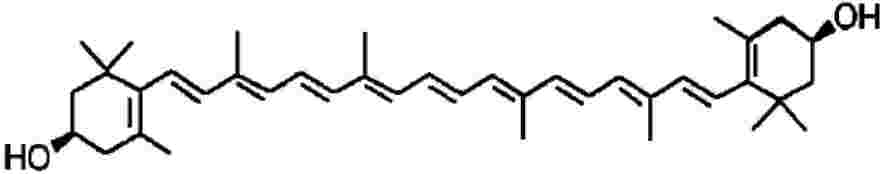
Numéro CAS: 144-68-3
Masse moléculaire: 568,9 daltons
Propriétés physico-chimiques de la zéaxanthine de synthèse
|
Perte à la dessiccation |
moins de 0,2 % |
|
Tous isomères trans-zéaxanthine |
plus de 96 % |
|
Isomères cis-zéaxanthine |
moins de 2 % |
|
Autres caroténoïdes |
moins de 1,5 % |
|
Oxyde de triphénylphosphine (no CAS: 791-28-6) |
moins de 50 mg/kg |
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/34 |
DÉCISION D’EXÉCUTION DE LA COMMISSION
du 22 janvier 2013
autorisant une extension de l’utilisation des graines de chia (Salvia hispanica) en tant que nouvel ingrédient alimentaire en application du règlement (CE) no 258/97 du Parlement européen et du Conseil
[notifiée sous le numéro C(2013) 123]
(Le texte en langue anglaise est le seul faisant foi.)
(2013/50/UE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu le règlement (CE) no 258/97 du Parlement européen et du Conseil du 27 janvier 1997 relatif aux nouveaux aliments et aux nouveaux ingrédients alimentaires (1), et notamment son article 7,
considérant ce qui suit:
|
(1) |
La décision 2009/827/CE de la Commission (2) a autorisé, conformément au règlement (CE) no 258/97, la mise sur le marché de graines de chia (Salvia hispanica) en tant que nouvel ingrédient alimentaire à utiliser dans les produits de panification, à raison d’une teneur maximale de 5 % de graines de chia (Salvia hispanica). |
|
(2) |
Le 14 avril 2011, The Chia Company a présenté aux autorités compétentes du Royaume-Uni une demande d’extension de l’utilisation des graines de chia en tant que nouvel ingrédient alimentaire sur le marché. La société demandait, en particulier, à pouvoir utiliser jusqu’à 10 % de graines de chia dans certaines catégories de denrées alimentaires et à pouvoir vendre des graines de chia préemballées, en recommandant un apport journalier de 15 g maximum. |
|
(3) |
Le 16 mars 2012, l’organisme britannique compétent en matière d’évaluation des denrées alimentaires a rendu son rapport d’évaluation initiale, dans lequel il concluait que l’extension de l’utilisation des graines de chia pour les catégories de denrées alimentaires proposées remplissait les critères énoncés à l’article 3, paragraphe 1, du règlement (CE) no 258/97. |
|
(4) |
Le 26 mars 2012, la Commission a transmis le rapport d’évaluation initiale à tous les États membres. |
|
(5) |
Des objections motivées ont été formulées dans le délai de 60 jours prévu au deuxième alinéa de l’article 6, paragraphe 4, du règlement (CE) no 258/97, notamment en ce qui concerne l’éventuelle absence de données toxicologiques. Les explications supplémentaires fournies par le demandeur ont permis de répondre à ces préoccupations de façon satisfaisante pour les États membres et la Commission. Par conséquent, il a été confirmé que les critères établis à l’article 3, paragraphe 1, du règlement (CE) no 258/97 étaient remplis. |
|
(6) |
Conformément à l’article 7, paragraphe 1, du règlement (CE) no 258/97, il convient d’adopter une décision d’exécution afin d’autoriser une extension de l’utilisation des graines de chia en tant que nouvel ingrédient alimentaire. |
|
(7) |
Les mesures prévues à la présente décision sont conformes à l’avis du comité permanent de la chaîne alimentaire et de la santé animale, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
La mise sur le marché dans l’Union de graines de chia (Salvia hispanica) conformes aux spécifications de l’annexe I, en tant que nouvel ingrédient alimentaire pour les utilisations visées à l’annexe II, est autorisée.
Les graines de chia (Salvia hispanica) en tant que telles ne peuvent être vendues au consommateur final que sous une forme préemballée.
Article 2
Les graines de chia (Salvia hispanica) autorisées par la présente décision sont dénommées «graines de chia (Salvia hispanica)» sur l’étiquette des denrées alimentaires qui en contiennent.
Il est nécessaire de prévoir un étiquetage supplémentaire des graines de chia (Salvia hispanica) préemballées pour informer le consommateur que l’apport journalier est limité à 15 g.
Article 3
The Chia Company, 262-276 Lorimer Street, Port Melbourne, Victoria 3207, Australie, est destinataire de la présente décision.
Fait à Bruxelles, le 22 janvier 2013.
Par la Commission
Tonio BORG
Membre de la Commission
(1) JO L 43 du 14.2.1997, p. 1.
(2) JO L 294 du 11.11.2009, p. 14.
ANNEXE I
CARACTÉRISTIQUES DES GRAINES DE CHIA (SALVIA HISPANICA)
Description
Le chia (Salvia hispanica) est une plante herbacée annuelle d’été appartenant à la famille des Lamiacées.
Après la récolte, les graines sont nettoyées mécaniquement. Les fleurs, les feuilles et les autres parties de la plante sont retirées.
Composition type des graines de chia
|
Matières sèches |
91-96 % |
|
Protéines |
20-22 % |
|
Graisses |
30-35 % |
|
Glucides |
25-41 % |
|
Fibres alimentaires [cellulose brute (1)] |
18-30 % |
|
Cendres |
4-6 % |
(1) La cellulose brute correspond à la partie de la cellulose qui est principalement constituée de cellulose, de pentosanes et de lignine non digestibles.
ANNEXE II
UTILISATIONS DES GRAINES DE CHIA (SALVIA HISPANICA)
|
Produits cuits au four |
pas plus de 10 % |
|
Céréales pour petit-déjeuner |
pas plus de 10 % |
|
Mélanges de fruits, de fruits à coque et de graines |
pas plus de 10 % |
|
Graines préemballées en tant que telles |
pas plus de 15 g par jour |
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/36 |
DÉCISION D’EXÉCUTION DE LA COMMISSION
du 23 janvier 2013
relative à l’évaluation du cadre réglementaire de pays tiers applicable aux substances actives de médicaments à usage humain et des activités respectives de contrôle et d’exécution, conformément à l’article 111 ter de la directive 2001/83/CE du Parlement européen et du Conseil
(Texte présentant de l'intérêt pour l'EEE)
(2013/51/UE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu la directive 2001/83/CE du Parlement européen et du Conseil du 6 novembre 2001 instituant un code communautaire relatif aux médicaments à usage humain (1), et notamment son article 111 ter, paragraphe 2,
considérant ce qui suit:
|
(1) |
L’article 111 ter, paragraphe 1, de la directive 2001/83/CE précise les aspects dont la Commission doit tenir particulièrement compte lors de l’évaluation du cadre réglementaire d’un pays tiers applicable aux substances actives exportées vers l’Union et de la capacité des activités respectives de contrôle et d’exécution à garantir un niveau de protection de la santé publique équivalent à celui de l’Union. |
|
(2) |
Il convient de décrire avec plus de précision les aspects et les documents utiles de l’Union européenne qui sont pris en considération lors de l’évaluation de ladite équivalence au sens de l’article 111 ter, paragraphe 1, de la directive 2001/83/CE. |
|
(3) |
Les mesures prévues à la présente décision sont conformes à l’avis du comité permanent des médicaments à usage humain, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
La présente décision précise la manière dont les aspects visés aux points a) à d) de l’article 111 ter, paragraphe 1, de la directive 2001/83/CE doivent être évalués afin de déterminer si le cadre réglementaire d’un pays tiers applicable aux substances actives exportées vers l’Union et les activités respectives de contrôle et d’exécution garantissent un niveau de protection de la santé publique équivalent à celui de l’Union.
Article 2
Aux fins de l’évaluation de l’équivalence du niveau de protection de la santé publique assurée par le cadre réglementaire d’un pays tiers applicable aux substances actives exportées vers l’Union et par les activités respectives de contrôle et d’exécution, conformément à l’article 111 ter de la directive 2001/83/CE, les exigences énoncées aux points a) à d) de l’article 111 ter, paragraphe 1, s’appliquent de la manière suivante:
|
a) |
Dans l’application du point a) de l’article 111 ter, paragraphe 1, la Commission prend en compte les lignes directrices applicables visées dans le deuxième alinéa de l’article 47 de la directive 2001/83/CE. |
|
b) |
Dans l’application du point b) de l’article 111 ter, paragraphe 1, la Commission prend en compte les lignes directrices applicables visées à l’article 3, paragraphe 1, de la directive 2003/94/CE de la Commission du 8 octobre 2003 établissant les principes et lignes directrices de bonnes pratiques de fabrication concernant les médicaments à usage humain et les médicaments expérimentaux à usage humain (2). |
|
c) |
Dans l’application du point c) de l’article 111 ter, paragraphe 1, la Commission évalue les ressources d’inspection, la qualification et la formation des inspecteurs, les procédures et stratégies d’inspection, les mécanismes de résolution des conflits d’intérêt, les normes de performance en matière d’inspections, les pouvoirs d’exécution, les mécanismes d’alerte et de crise, et la capacité d’analyse, compte tenu des lignes directrices applicables visées à l’article 3, paragraphe 1, de la directive 2003/94/CE. |
|
d) |
Dans l’application du point d) de l’article 111 ter, paragraphe 1, la Commission évalue les dispositions prises dans le pays tiers pour assurer une information régulière et rapide de l’Union européenne sur les producteurs de substances actives qui ne satisfont pas aux exigences. |
Article 3
La présente décision entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l’Union européenne.
Fait à Bruxelles, le 23 janvier 2013.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 311 du 28.11.2001, p. 67.
(2) JO L 262 du 14.10.2003, p. 22.
III Autres actes
ESPACE ÉCONOMIQUE EUROPÉEN
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/37 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 191/2012
du 26 octobre 2012
modifiant l'annexe I (questions vétérinaires et phytosanitaires) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Le règlement d'exécution (UE) no 176/2012 de la Commission du 1er mars 2012 modifiant les annexes B, C et D de la directive 90/429/CEE du Conseil en ce qui concerne les exigences de police sanitaire relatives à la brucellose et à la maladie d'Aujeszky (1) doit être intégré dans l'accord EEE. |
|
(2) |
La décision d'exécution 2011/396/UE de la Commission du 4 juillet 2011 autorisant un laboratoire situé au Japon à effectuer des tests sérologiques de contrôle de l'efficacité des vaccins antirabiques (2) doit être intégrée dans l'accord EEE. |
|
(3) |
La présente décision concerne la législation relative aux animaux vivants autres que les poissons et les animaux d'aquaculture. La législation relative à ces questions ne s'applique pas à l'Islande, comme cela est précisé au paragraphe 2 de la partie introductive du chapitre I de l'annexe I de l'accord EEE. La présente décision ne s'applique donc pas à l'Islande. |
|
(4) |
La présente décision concerne la législation relative aux questions vétérinaires. Cette législation ne s'applique pas au Liechtenstein aussi longtemps que l'application de l'accord entre la Communauté européenne et la Confédération suisse relatif aux échanges de produits agricoles est étendue au Liechtenstein, comme cela est précisé dans les adaptations sectorielles de l'annexe I de l'accord EEE. La présente décision ne s'applique donc pas au Liechtenstein. |
|
(5) |
Il convient dès lors de modifier l'annexe I de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le chapitre I de l'annexe I de l'accord EEE est modifié comme suit:
|
1) |
Le tiret suivant est ajouté au point 8 (directive 90/429/CEE du Conseil) de la partie 4.1 et au point 7 (directive 90/429/CEE du Conseil) de la partie 8.1:
|
|
2) |
Le point suivant est inséré après le point 96 (décision 2011/91/UE de la Commission) de la partie 4.2:
|
Article 2
Les textes du règlement d'exécution (UE) no 176/2012 et de la décision d'exécution 2011/396/UE en langue norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (3).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 61 du 2.3.2012, p. 1.
(2) JO L 176 du 5.7.2011, p. 51.
(3) Pas d'obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/39 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 192/2012
du 26 octobre 2012
modifiant l'annexe I (Questions vétérinaires et phytosanitaires) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «l'accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Le règlement (UE) no 200/2012 de la Commission du 8 mars 2012 concernant un objectif de l'Union pour la réduction de la prévalence de Salmonella enteritidis et de Salmonella typhimurium dans les cheptels de poulets de chair, dont la fixation est prévue au règlement (CE) no 2160/2003 du Parlement européen et du Conseil (1) doit être intégré dans l'accord EEE. |
|
(2) |
Le règlement d'exécution (UE) no 233/2012 de la Commission du 16 mars 2012 portant application du règlement (CE) no 999/2001 du Parlement européen et du Conseil en ce qui concerne l'approbation de la version modifiée du programme national de lutte contre la tremblante du Danemark (2) doit être intégré dans l'accord EEE. |
|
(3) |
La décision d'exécution 2011/825/UE de la Commission du 8 décembre 2011 modifiant la décision 2010/221/UE en ce qui concerne les mesures nationales visant à prévenir l'introduction de certaines maladies des animaux aquatiques dans certaines régions d'Irlande, de Finlande et de Suède (3) doit être intégrée dans l'accord EEE. |
|
(4) |
La décision d'exécution 2012/111/UE de la Commission du 10 février 2012 modifiant la décision 2007/453/CE en ce qui concerne le statut du Danemark et du Panama au regard de l'ESB (4) doit être intégrée dans l'accord EEE. |
|
(5) |
Le règlement (UE) no 200/2012 abroge le règlement (CE) no 646/2007 de la Commission (5), qui est intégré dans l'accord (EEE) et doit donc en être supprimé. |
|
(6) |
La présente décision concerne la législation relative aux questions vétérinaires. Cette législation ne s'applique pas au Liechtenstein aussi longtemps que l'application de l'accord entre la Communauté européenne et la Confédération suisse relatif aux échanges de produits agricoles est étendue au Liechtenstein, comme cela est précisé dans les adaptations sectorielles de l'annexe I de l'accord EEE. La présente décision ne s'applique donc pas au Liechtenstein. |
|
(7) |
Il convient dès lors de modifier l'annexe I de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le chapitre I de l'annexe I de l'accord EEE est modifié comme suit:
|
1) |
Le tiret suivant est ajouté au point 94 (décision 2010/221/UE de la Commission) de la partie 4.2:
|
|
2) |
Le texte du point 47 (règlement (CE) no 646/2007 de la Commission) de la partie 7.2 est supprimé. |
|
3) |
Le tiret suivant est ajouté au point 49 (décision 2007/453/CE de la Commission) de la partie 7.2:
|
|
4) |
Les points suivants sont insérés après le point 56 [règlement d'exécution (UE) no 931/2011 de la Commission] de la partie 7.2:
|
Article 2
Les textes du règlement (UE) no 200/2012, du règlement d’exécution (UE) no 233/2012 et des décisions d’exécution 2011/825/UE et 2012/111/UE en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (6).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 71 du 9.3.2012, p. 31.
(2) JO L 78 du 17.3.2012, p. 13.
(3) JO L 328 du 10.12.2011, p. 53.
(4) JO L 50 du 23.2.2012, p. 49.
(5) JO L 151 du 13.6.2007, p. 21.
(6) Pas d'obligations constitutionnelles signalées.] [Obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/41 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 193/2012
du 26 octobre 2012
modifiant l'annexe I (Questions vétérinaires et phytosanitaires) et l'annexe II (Réglementations techniques, normes, essais et certification) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Le règlement (UE) no 277/2012 de la Commission du 28 mars 2012 modifiant les annexes I et II de la directive 2002/32/CE du Parlement européen et du Conseil en ce qui concerne les teneurs maximales et les seuils d'intervention relatifs aux dioxines et aux polychlorobiphényles (1) doit être intégré dans l'accord EEE. |
|
(2) |
La recommandation 2012/154/UE de la Commission du 15 mars 2012 sur la surveillance de la présence d'alcaloïdes de l'ergot dans les aliments pour animaux et les denrées alimentaires (2) doit être intégrée dans l'accord EEE. |
|
(3) |
La présente décision concerne la législation relative aux aliments pour animaux et aux denrées alimentaires. Cette législation ne s'applique pas au Liechtenstein aussi longtemps que l'application de l'accord entre la Communauté européenne et la Confédération suisse relatif aux échanges de produits agricoles est étendue au Liechtenstein, comme cela est précisé dans les adaptations sectorielles de l'annexe I de l'accord EEE et dans la partie introductive du chapitre XII de l'annexe II de l'accord EEE. La présente décision ne s'applique donc pas au Liechtenstein. |
|
(4) |
Il convient dès lors de modifier les annexes I et II de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le chapitre II de l'annexe I de l'accord EEE est modifié comme suit:
|
1) |
le tiret suivant est ajouté au point 33 (directive 2002/32/CE du Parlement européen et du Conseil):
|
|
2) |
le point suivant est inséré après le point 40 [règlement (CE) no 396/2005 du Parlement européen et du Conseil]:
|
Article 2
À la rubrique «ACTES DONT LES PARTIES CONTRACTANTES PRENNENT ACTE», le point suivant est inséré après le point 13 (recommandation 2010/161/UE de la Commission) du chapitre XII de l'annexe II de l'accord EEE:
|
«14. |
32012 H 0154: recommandation 2012/154/UE de la Commission du 15 mars 2012 sur la surveillance de la présence d'alcaloïdes de l'ergot dans les aliments pour animaux et les denrées alimentaires (JO L 77 du 16.3.2012, p. 20).» |
Article 3
Les textes du règlement (UE) no 277/2012 et de la recommandation 2012/154/UE en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l’Union européenne, font foi.
Article 4
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (3).
Article 5
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l'EEE
Le président
Atle LEIKVOLL
(1) JO L 91 du 29.3.2012, p. 1.
(2) JO L 77 du 16.3.2012, p. 20.
(3) Pas d'obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/42 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 194/2012
du 26 octobre 2012
modifiant l'annexe II (réglementations techniques, normes, essais et certification) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Il convient d'intégrer dans l'accord EEE le règlement (UE) no 347/2012 de la Commission du 16 avril 2012 portant application du règlement (CE) no 661/2009 du Parlement européen et du Conseil en ce qui concerne les prescriptions pour la réception par type de certaines catégories de véhicules à moteur en matière de systèmes avancés de freinage d'urgence (1). |
|
(2) |
Il convient d'intégrer dans l'accord EEE le règlement (UE) no 351/2012 de la Commission du 23 avril 2012 mettant en œuvre le règlement (CE) no 661/2009 du Parlement européen et du Conseil en ce qui concerne les prescriptions pour la réception par type relatives au montage de systèmes d'avertissement de franchissement de ligne sur les véhicules à moteur (2), rectifié au JO L 121 du 8.5.2012, p. 44. |
|
(3) |
Il convient dès lors de modifier l'annexe II de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Les points suivants sont insérés après le point 45zzo [règlement (UE) no 65/2012 de la Commission] du chapitre I de l'annexe II de l'accord EEE:
|
«45zzp. |
32012 R 0347: règlement (UE) no 347/2012 de la Commission du 16 avril 2012 portant application du règlement (CE) no 661/2009 du Parlement européen et du Conseil en ce qui concerne les prescriptions pour la réception par type de certaines catégories de véhicules à moteur en matière de systèmes avancés de freinage d'urgence (JO L 109 du 21.4.2012, p. 1). |
|
45zzq. |
32012 R 0351: règlement (UE) no 351/2012 de la Commission du 23 avril 2012 mettant en œuvre le règlement (CE) no 661/2009 du Parlement européen et du Conseil en ce qui concerne les prescriptions pour la réception par type relatives au montage de systèmes d'avertissement de franchissement de ligne sur les véhicules à moteur (JO L 110 du 24.4.2012, p. 18), rectifié au JO L 121 du 8.5.2012, p. 44.» |
Article 2
Les textes des règlements (UE) no 347/2012 et (UE) no 351/2012, rectifié au JO L 121 du 8.5.2012, p. 44, en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (3).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 109 du 21.4.2012, p. 1.
(2) JO L 110 du 24.4.2012, p. 18.
(3) Pas d'obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/43 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 195/2012
du 26 octobre 2012
modifiant l'annexe II (réglementations techniques, normes, essais et certification) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Il convient d'intégrer dans l'accord EEE le règlement (UE) no 412/2012 de la Commission du 15 mai 2012 modifiant l'annexe XVII du règlement (CE) no 1907/2006 du Parlement européen et du Conseil concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances («REACH») (1). |
|
(2) |
Il convient dès lors de modifier en conséquence l'annexe II de l'accord EEE, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le tiret suivant est ajouté au point 12zc [règlement (CE) no 1907/2006 du Parlement européen et du Conseil] du chapitre XV de l'annexe II de l'accord EEE:
|
«— |
32012 R 0412: règlement (UE) no 412/2012 de la Commission du 15 mai 2012 (JO L 128 du 16.5.2012, p. 1).» |
Article 2
Les textes du règlement (UE) no 412/2012 en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (2).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 128 du 16.5.2012, p. 1.
(2) Pas d'obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/44 |
DÉCISION DU COMITÉ MIXTE DE L’EEE
N o 196/2012
du 26 octobre 2012
modifiant l’annexe II (Réglementations techniques, normes, essais et certification) de l’accord EEE
LE COMITÉ MIXTE DE L’EEE,
vu l’accord sur l’Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Il convient d’intégrer dans l’accord EEE la décision 2010/11/UE de la Commission du 7 janvier 2010 concernant les exigences de sécurité que doivent comporter les normes européennes relatives aux dispositifs de blocage des fenêtres et des portes de balcon à l’épreuve des enfants, à monter soi-même, en application de la directive 2001/95/CE du Parlement européen et du Conseil (1). |
|
(2) |
Il convient d’intégrer dans l’accord EEE la décision 2010/376/UE de la Commission du 2 juillet 2010 concernant les exigences de sécurité que doivent comporter les normes européennes relatives à certains produits utilisés dans l’environnement de sommeil des enfants, en application de la directive 2001/95/CE du Parlement européen et du Conseil (2). |
|
(3) |
Il convient d’intégrer dans l’accord EEE la décision d’exécution 2012/48/UE de la Commission du 26 janvier 2012 prorogeant la validité de la décision 2009/251/CE exigeant des États membres qu’ils veillent à ce que les produits contenant du fumarate de diméthyle (produit biocide) ne soient pas commercialisés ou mis à disposition sur le marché (3). |
|
(4) |
Il convient dès lors de modifier en conséquence l’annexe II de l’accord EEE, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le chapitre XIX de l’annexe II de l’accord EEE est modifié comme suit:
|
1) |
le tiret suivant est ajouté au point 3n (décision 2009/251/CE de la Commission):
|
|
2) |
les points suivants sont insérés après le point 3n (décision 2009/251/CE de la Commission):
|
Article 2
Les textes des décisions 2010/11/UE et 2010/376/UE et de la décision d'exécution 2012/48/UE en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l’Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l’article 103, paragraphe 1, de l’accord EEE aient été faites au Comité mixte de l’EEE (4).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l’Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 4 du 8.1.2010, p. 91.
(2) JO L 170 du 6.7.2010, p. 39.
(3) JO L 26 du 28.1.2012, p. 35.
(4) Pas d’obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/45 |
DÉCISION DU COMITÉ MIXTE DE L’EEE
N o 197/2012
du 26 octobre 2012
modifiant l’annexe II (réglementations techniques, normes, essais et certification) de l’accord EEE
LE COMITÉ MIXTE DE L’EEE,
vu l’accord sur l’Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Il convient d’intégrer dans l’accord EEE la décision 2010/81/UE de la Commission du 9 février 2010 établissant les classes de caractéristiques de réaction au feu pour certains produits de construction en ce qui concerne les adhésifs pour carrelages en céramique (1). |
|
(2) |
Il convient d’intégrer dans l’accord EEE la décision 2010/82/UE de la Commission du 9 février 2010 établissant les classes de caractéristiques de réaction au feu pour certains produits de construction en ce qui concerne les revêtements muraux décoratifs sous forme de rouleaux et de panneaux (2). |
|
(3) |
Il convient d’intégrer dans l’accord EEE la décision 2010/83/UE de la Commission du 9 février 2010 établissant les classes de caractéristiques de réaction au feu pour certains produits de construction en ce qui concerne les mastics de jointoiement séchant à l’air (3). |
|
(4) |
Il convient d’intégrer dans l’accord EEE la décision 2010/85/UE de la Commission du 9 février 2010 établissant les classes de caractéristiques de réaction au feu pour certains produits de construction en ce qui concerne les chapes cimentaires, les chapes à base de sulfate de calcium et les chapes de sols en résine synthétique (4). |
|
(5) |
Il convient d’intégrer dans l’accord EEE la décision 2010/679/UE de la Commission du 8 novembre 2010 modifiant la décision 95/467/CE portant application de l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil sur les produits de construction (5). |
|
(6) |
Il convient d’intégrer dans l’accord EEE la décision 2010/683/UE de la Commission du 9 novembre 2010 modifiant la décision 97/555/CE relative à la procédure d’attestation de conformité des produits de construction conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil, en ce qui concerne les ciments, chaux de construction et autres liants hydrauliques (6). |
|
(7) |
Il convient d’intégrer dans l’accord EEE la décision 2010/737/UE de la Commission du 2 décembre 2010 établissant la classification des caractéristiques de réaction au feu de certains produits de construction en ce qui concerne les tôles en acier revêtues de polyester ou de plastisol (7); |
|
(8) |
Il convient d’intégrer dans l’accord EEE la décision 2010/738/UE de la Commission du 2 décembre 2010 établissant les classes de caractéristiques de réaction au feu pour certains produits de construction en ce qui concerne les moulages en staff (8); |
|
(9) |
Il convient d’intégrer dans l’accord EEE la décision 2011/14/UE de la Commission du 13 janvier 2011 portant modification de la décision 97/556/CE relative à la procédure d’attestation de conformité de produits de construction conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil, en ce qui concerne les systèmes/kits mixtes pour l’isolation thermique externe avec enduit (ETICS) (9). |
|
(10) |
Il convient d’intégrer dans l’accord EEE la décision 2011/19/UE de la Commission du 14 janvier 2011 relative à la procédure d’attestation de conformité des produits de construction conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil, en ce qui concerne les mastics pour joints pour des usages non structuraux dans les constructions immobilières et pour chemins piétonniers (10). |
|
(11) |
Il convient d’intégrer dans l’accord EEE la décision 2011/232/UE de la Commission du 11 avril 2011 modifiant la décision 2000/367/CE établissant un système de classification des caractéristiques de résistance au feu des produits de construction, des ouvrages de construction ou de parties de ceux-ci (11). |
|
(12) |
Il convient d’intégrer dans l’accord EEE la décision 2011/246/UE de la Commission du 18 avril 2011 modifiant la décision 1999/93/CE relative à la procédure d’attestation de conformité des produits de construction conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil en ce qui concerne les portes, fenêtres, volets, stores, portails et quincailleries associées (12). |
|
(13) |
Il convient d’intégrer dans l’accord EEE la décision 2011/284/UE de la Commission du 12 mai 2011 relative à la procédure d’attestation de conformité des produits de construction, conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil, en ce qui concerne les câbles d’alimentation, de commande et de communication (13). |
|
(14) |
Il convient d’intégrer dans l’accord EEE la décision d’exécution 2012/201/UE de la Commission du 26 mars 2012 modifiant la décision 98/213/CE relative à la procédure d’attestation de conformité des produits de construction, conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil, en ce qui concerne les kits de cloisons (14). |
|
(15) |
Il convient d’intégrer dans l’accord EEE la décision d’exécution 2012/202/UE de la Commission du 29 mars 2012 modifiant la décision 1999/94/CE relative à la procédure d’attestation de conformité des produits de construction conformément à l’article 20, paragraphe 2, de la directive 89/106/CEE du Conseil en ce qui concerne les produits préfabriqués en béton de granulats courants, en béton de granulats légers ou en béton cellulaire autoclavé aéré (15). |
|
(16) |
Il convient dès lors de modifier en conséquence l’annexe II de l’accord EEE, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le chapitre XXI de l’annexe II de l’accord EEE est modifié comme suit:
|
1) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 10e tiret (décision 95/467/CE de la Commission): «, modifiée par:
|
|
2) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 18e tiret (décision 97/555/CE de la Commission): «, modifiée par:
|
|
3) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 19e tiret (décision 97/556/CE de la Commission): «, modifiée par:
|
|
4) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 25e tiret (décision 98/213/CE de la Commission): «, modifiée par:
|
|
5) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 40e tiret (décision 1999/93/CE de la Commission): «, modifiée par:
|
|
6) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 41e tiret (décision 1999/94/CE de la Commission): «, modifiée par:
|
|
7) |
Le texte suivant est ajouté au point 1 (directive 89/106/CEE du Conseil), 49e tiret (décision 2000/367/CE de la Commission): «, modifiée par:
|
|
8) |
Les points suivants sont insérés après le point 2g (décision 2006/600/CE de la Commission):
|
Article 2
Les textes des décisions 2010/81/UE, 2010/82/UE, 2010/83/UE, 2010/85/UE, 2010/679/UE, 2010/683/UE, 2010/737/UE, 2010/738/UE, 2011/14/UE, 2011/19/UE, 2011/232/UE, 2011/246/UE et 2011/284/UE et des décisions d'exécution 2012/201/UE et 2012/202/UE, en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l’Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l’article 103, paragraphe 1, de l’accord EEE aient été faites au Comité mixte de l’EEE (16).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l’Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 38 du 11.2.2010, p. 9.
(2) JO L 38 du 11.2.2010, p. 11.
(3) JO L 38 du 11.2.2010, p. 13.
(4) JO L 38 du 11.2.2010, p. 17.
(5) JO L 292 du 10.11.2010, p. 55.
(6) JO L 293 du 11.11.2010, p. 60.
(7) JO L 317 du 3.12.2010, p. 39.
(8) JO L 317 du 3.12.2010, p. 42.
(9) JO L 10 du 14.1.2011, p. 5.
(10) JO L 11 du 15.1.2011, p. 49.
(11) JO L 97 du 12.4.2011, p. 49.
(12) JO L 103 du 19.4.2011, p. 114.
(13) JO L 131 du 18.5.2011, p. 22.
(14) JO L 109 du 21.4.2012, p. 20.
(15) JO L 109 du 21.4.2012, p. 22.
(16) Pas d’obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/48 |
DÉCISION DU COMITÉ MIXTE DE L’EEE
N o 198/2012
du 26 octobre 2012
modifiant l'annexe II (Réglementations techniques, normes, essais et certification) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Il convient d'intégrer dans l'accord EEE le règlement (UE) no 207/2012 de la Commission du 9 mars 2012 relatif aux instructions d'emploi électroniques des dispositifs médicaux (1). |
|
(2) |
Il convient dès lors de modifier en conséquence l'annexe II de l'accord EEE, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le point suivant est ajouté après le point 8 (décision 2010/227/UE de la Commission) du chapitre XXX de l'annexe II de l'accord EEE:
|
«9. |
32012 R 0207: Règlement (UE) no 207/2012 de la Commission du 9 mars 2012 relatif aux instructions d'emploi électroniques des dispositifs médicaux (JO L 72 du 10.3.2012, p. 28).» |
Article 2
Les textes du règlement (UE) no 207/2012 en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (2).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 72 du 10.3.2012, p. 28.
(2) Pas d'obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/49 |
DÉCISION DU COMITÉ MIXTE DE L’EEE
N o 199/2012
du 26 octobre 2012
modifiant l’annexe XIII (Transports) de l’accord EEE
LE COMITÉ MIXTE DE L’EEE,
vu l’accord sur l’Espace économique européen, modifié par le protocole portant adaptation de cet accord, ci-après dénommé l’«accord», et notamment son article 98,
considérant ce qui suit:
|
(1) |
L’annexe XIII de l’accord a été modifiée par la décision du Comité mixte de l’EEE no 180/2012 du 28 septembre 2012 (1). |
|
(2) |
Le règlement (UE) no 1286/2011 de la Commission du 9 décembre 2011 portant adoption d’une méthodologie commune pour enquêter sur les accidents et incidents de mer conformément à l’article 5, paragraphe 4, de la directive 2009/18/CE du Parlement européen et du Conseil (2) doit être intégré dans l’accord, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le point suivant est inséré après le point 55ca [règlement d’exécution (UE) no 651/2011 de la Commission] de l’annexe XIII de l’accord:
|
«55cb. |
32011 R 1286: règlement (UE) no 1286/2011 de la Commission du 9 décembre 2011 portant adoption d’une méthodologie commune pour enquêter sur les accidents et incidents de mer conformément à l’article 5, paragraphe 4, de la directive 2009/18/CE du Parlement européen et du Conseil (JO L 328 du 10.12.2011, p. 36).» |
Article 2
Les textes du règlement (UE) no 1286/2011 en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l’Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l’article 103, paragraphe 1, de l’accord aient été faites au Comité mixte de l’EEE (3), ou le jour de l’entrée en vigueur de la décision du Comité mixte de l’EEE no 62/2012 du 30 mars 2012 (4), si cette date est ultérieure.
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l’Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 341 du 13.12.2012, p. 34.
(2) JO L 328 du 10.12.2011, p. 36.
(3) Pas d’obligations constitutionnelles signalées.
(4) JO L 207 du 2.8.2012, p. 42.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/50 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 200/2012
du 26 octobre 2012
modifiant l'annexe XX (Environnement) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Le règlement (CE) no 66/2010 du Parlement européen et du Conseil du 25 novembre 2009 établissant le label écologique de l'UE (1), rectifié dans le JO L 108 du 29.4.2010, p. 355, doit être intégré dans l'accord EEE. |
|
(2) |
Le règlement (CE) no 66/2010 abroge le règlement (CE) no 1980/2000 du Parlement européen et du Conseil (2), qui est intégré dans l’accord EEE et doit dès lors en être supprimé. |
|
(3) |
Il convient, dès lors, de modifier l'annexe XX de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le point 2a [règlement (CE) no 1980/2000 du Parlement européen et du Conseil] de l'annexe XX de l'accord EEE est remplacé par le texte suivant:
«32010 R 0066: règlement (CE) no 66/2010 du Parlement européen et du Conseil du 25 novembre 2009 établissant le label écologique de l'UE (JO L 27 du 30.1.2010, p. 1), rectifié dans le JO L 108 du 29.4.2010, p. 355.»
Article 2
Les textes du règlement (CE) no 66/2010, rectifié dans le JO L 108 du 29.4.2010, p. 355, en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (3).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 27 du 30.1.2010, p. 1.
(2) JO L 237 du 21.9.2000, p. 1.
(3) Obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/51 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 201/2012
du 26 octobre 2012
modifiant l'annexe XX (Environnement) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
La décision 2010/709/UE de la Commission du 22 novembre 2010 instituant le comité de l'Union européenne pour le label écologique (1) doit être intégrée dans l'accord EEE. |
|
(2) |
La décision 2011/263/UE de la Commission du 28 avril 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux détergents pour lave-vaisselle (2) doit être intégrée dans l'accord EEE. |
|
(3) |
La décision 2011/264/UE de la Commission du 28 avril 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux détergents textiles (3) doit être intégrée dans l'accord EEE. |
|
(4) |
La décision 2011/330/UE de la Commission du 6 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux ordinateurs portables (4) doit être intégrée dans l'accord EEE. |
|
(5) |
La décision 2011/331/UE de la Commission du 6 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux sources lumineuses (5) doit être intégrée dans l'accord EEE. |
|
(6) |
La décision 2011/333/UE de la Commission du 7 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne au papier à copier et au papier graphique (6), rectifiée dans le JO L 161 du 21.6.2011, p. 34, doit être intégrée dans l'accord EEE. |
|
(7) |
La décision 2011/337/UE de la Commission du 9 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux ordinateurs personnels (7) doit être intégrée dans l'accord EEE. |
|
(8) |
La décision 2011/381/UE de la Commission du 24 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux lubrifiants (8) doit être intégrée dans l'accord EEE. |
|
(9) |
La décision 2011/382/UE de la Commission du 24 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux détergents pour vaisselle à la main (9) doit être intégrée dans l'accord EEE. |
|
(10) |
La décision 2011/383/UE de la Commission du 28 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux nettoyants universels et aux nettoyants pour sanitaires (10), rectifiée dans le JO L 110 du 24.4.2012, p. 44, doit être intégrée dans l'accord EEE. |
|
(11) |
La décision 2010/709/UE abroge la décision 2000/730/CE de la Commission (11), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(12) |
La décision 2011/263/UE abroge la décision 2003/31/CE de la Commission (12), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(13) |
La décision 2011/264/UE abroge la décision 2003/200/CE de la Commission (13), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(14) |
La décision 2011/330/UE abroge la décision 2005/343/CE de la Commission (14), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(15) |
La décision 2011/331/UE abroge la décision 2002/747/CE de la Commission (15), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(16) |
La décision 2011/333/UE abroge la décision 2002/741/CE de la Commission (16), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(17) |
La décision 2011/337/UE abroge la décision 2005/341/CE de la Commission (17), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(18) |
La décision 2011/381/UE abroge la décision 2005/360/CE de la Commission (18), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(19) |
La décision 2011/382/UE abroge la décision 2005/342/CE de la Commission (19), qui est intégrée dans l'accord EEE et doit dès lors en être supprimée. |
|
(20) |
La décision 2011/383/UE abroge la décision 2005/344/CE de la Commission (20) qui est intégrée à l'accord EEE et est donc abrogée de l'accord EEE. |
|
(21) |
Il convient, dès lors, de modifier l'annexe XX de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
L'annexe XX de l'accord EEE est modifiée comme suit:
|
1) |
Le texte du point 2ad (décision 2000/730/CE de la Commission) est remplacé par le texte suivant: «32010 D 0709: décision 2010/709/UE de la Commission du 22 novembre 2010 instituant le comité de l'Union européenne pour le label écologique (JO L 308 du 24.11.2010, p. 53).» |
|
2) |
Le texte du point 2e (décision 2003/200/CE de la Commission) est remplacé par le texte suivant: «32011 D 0264: décision 2011/264/UE de la Commission du 28 avril 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux détergents textiles (JO L 111 du 30.4.2011, p. 34).» |
|
3) |
Le texte du point 2h (décision 2003/31/CE de la Commission) est remplacé par le texte suivant: «32011 D 0263: décision 2011/263/UE de la Commission du 28 avril 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux détergents pour lave-vaisselle (JO L 111 du 30.4.2011, p. 22).» |
|
4) |
Le texte du point 2o (décision 2002/747/CE de la Commission) est remplacé par le texte suivant: «32011 D 0331: décision 2011/331/UE de la Commission du 6 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux sources lumineuses (JO L 148 du 7.6.2011, p. 13).» |
|
5) |
Le texte du point 2q (décision 2005/341/CE de la Commission) est remplacé par le texte suivant: «32011 D 0337: décision 2011/337/UE de la Commission du 9 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux ordinateurs personnels (JO L 151 du 10.6.2011, p. 5).» |
|
6) |
Le texte du point 2r (décision 2005/342/CE de la Commission) est remplacé par le texte suivant: «32011 D 0382: décision 2011/382/UE de la Commission du 24 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux détergents pour vaisselle à la main (JO L 169 du 29.6.2011, p. 40).» |
|
7) |
Le texte du point 2s (décision 2005/343/CE de la Commission) est remplacé par le texte suivant: «32011 D 0330: décision 2011/330/UE de la Commission du 6 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux ordinateurs portables (JO L 148 du 7.6.2011, p. 5).» |
|
8) |
Le texte du point 2t (décision 2005/344/CE de la Commission) est remplacé par le texte suivant: «32011 D 0383: décision 2011/383/UE de la Commission du 28 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux nettoyants universels et aux nettoyants pour sanitaires (JO L 169 du 29.6.2011, p. 52), rectifiée dans le JO L 110 du 24.4.2012, p. 44.» |
|
9) |
Le texte du point 2u (décision 2005/360/CE de la Commission) est remplacé par le texte suivant: «32011 D 0381: décision 2011/381/UE de la Commission du 24 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne aux lubrifiants (JO L 169 du 29.6.2011, p. 28).» |
|
10) |
Le texte du point 2x (décision 2002/741/CE de la Commission) est remplacé par le texte suivant: «32011 D 0333: décision 2011/333/UE de la Commission du 7 juin 2011 établissant les critères écologiques pour l'attribution du label écologique de l'Union européenne au papier à copier et au papier graphique (JO L 149 du 8.6.2011, p. 12), rectifiée dans le JO L 161 du 21.6.2011, p. 34).» |
Article 2
Les textes des décisions 2010/709/UE, 2011/263/UE, 2011/264/UE, 2011/330/UE, 2011/331/UE, 2011/333/UE, rectifiée dans le JO L 161 du 21.6.2011, p. 34, 2011/337/UE, 2011/381/UE, 2011/382/UE et 2011/383/UE, rectifiée dans le JO L 110 du 24.4.2012, p. 44, en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (21), ou le jour de l'entrée en vigueur de la décision du Comité mixte de l'EEE no 200/2012 du 26 octobre 2012 (22), si cette date est ultérieure.
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 308 du 24.11.2010, p. 53.
(2) JO L 111 du 30.4.2011, p. 22.
(3) JO L 111 du 30.4.2011, p. 34.
(4) JO L 148 du 7.6.2011, p. 5.
(5) JO L 148 du 7.6.2011, p. 13.
(6) JO L 149 du 8.6.2011, p. 12.
(7) JO L 151 du 10.6.2011, p. 5.
(8) JO L 169 du 29.6.2011, p. 28.
(9) JO L 169 du 29.6.2011, p. 40.
(10) JO L 169 du 29.6.2011, p. 52.
(11) JO L 293 du 22.11.2000, p. 24
(12) JO L 9 du 15.1.2003, p. 11.
(13) JO L 76 du 22.3.2003, p. 25.
(14) JO L 115 du 4.5.2005, p. 35.
(15) JO L 242 du 10.9.2002, p. 44.
(16) JO L 237 du 5.9.2002, p. 6.
(17) JO L 115 du 4.5.2005, p. 1.
(18) JO L 118 du 5.5.2005, p. 26.
(19) JO L 115 du 4.5.2005, p. 9.
(20) JO L 115 du 4.5.2005, p. 42.
(21) Pas d'obligations constitutionnelles signalées.
(22) Voir page 50 du présent Journal officiel.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/54 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 202/2012
du 26 octobre 2012
modifiant l'annexe XX (Environnement) de l'accord EEE
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Le règlement (CE) no 1005/2009 du Parlement européen et du Conseil du 16 septembre 2009 relatif à des substances qui appauvrissent la couche d'ozone (1) doit être intégré dans l'accord EEE. |
|
(2) |
Le règlement (UE) no 744/2010 de la Commission du 18 août 2010 modifiant le règlement (CE) no 1005/2009 du Parlement européen et du Conseil relatif à des substances qui appauvrissent la couche d'ozone pour ce qui concerne les utilisations critiques des halons (2) doit être intégré dans l'accord EEE. |
|
(3) |
Le règlement (UE) no 291/2011 de la Commission du 24 mars 2011 concernant les utilisations essentielles en laboratoire et à des fins d'analyse, dans l'Union européenne, des substances réglementées autres que les hydrochlorofluorocarbones conformément au règlement (CE) no 1005/2009 du Parlement européen et du Conseil relatif à des substances qui appauvrissent la couche d'ozone (3) doit être intégré dans l'accord EEE. |
|
(4) |
Le règlement (CE) no 1005/2009 abroge le règlement (CE) no 2037/2000 du Parlement européen et du Conseil (4), qui est intégré dans l'accord EEE et doit dès lors en être supprimé. |
|
(5) |
Sans préjudice des décisions futures susceptibles d'être adoptées par le Comité mixte de l'EEE, il convient de noter que le règlement (CE) no 450/2008 du Parlement européen et du Conseil du 23 avril 2008 établissant le code des douanes communautaire (code des douanes modernisé) (5) n'est pas intégré dans l'accord EEE. Les références à ce règlement ne devraient donc pas s'appliquer. |
|
(6) |
Il convient, dès lors, de modifier l'annexe XX de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
L'annexe XX de l'accord EEE est modifiée comme suit:
|
1) |
le point 21aa [règlement (CE) no 2037/2000 du Parlement européen et du Conseil] est remplacé par le texte suivant: «32009 R 1005: règlement (CE) no 1005/2009 du Parlement européen et du Conseil du 16 septembre 2009 relatif à des substances qui appauvrissent la couche d'ozone (JO L 286 du 31.10.2009, p. 1), modifié par:
Aux fins du présent accord, les dispositions du règlement sont adaptées comme suit:
Les États de l'AELE mettent en vigueur, au niveau national, les mesures nécessaires pour se conformer aux dispositions correspondantes du protocole de Montréal et aux mesures correspondantes prévues dans le règlement (CE) no 1005/2009 du Parlement européen et du Conseil.» |
|
2) |
le point suivant est inséré après le point 21aa [règlement (CE) no 1005/2009 du Parlement européen et du Conseil]:
|
Article 2
Les textes des règlements (CE) no 1005/2009, (UE) no 744/2010 et (UE) no 291/2011, en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l'Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (6).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 286 du 31.10.2009, p. 1.
(2) JO L 218 du 19.8.2010, p. 2.
(3) JO L 79 du 25.3.2011, p. 4.
(4) JO L 244 du 29.9.2000, p. 1.
(5) JO L 145 du 4.6.2008, p. 1.
(6) Pas d'obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/56 |
DÉCISION DU COMITÉ MIXTE DE L’EEE
N o 203/2012
du 26 octobre 2012
modifiant l’annexe XX (Environnement) de l’accord EEE
LE COMITÉ MIXTE DE L’EEE,
vu l’accord sur l’Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
La décision 2009/10/CE de la Commission du 2 décembre 2008 établissant un formulaire relatif aux accidents majeurs conformément à la directive 96/82/CE du Conseil concernant la maîtrise des dangers liés aux accidents majeurs impliquant des substances dangereuses (1) doit être intégrée dans l’accord EEE. |
|
(2) |
Il convient, dès lors, de modifier l’annexe XX de l’accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
Le point suivant est inséré après le point 23aa (décision 2002/605/CE de la Commission) de l’annexe XX de l’accord EEE:
|
«23ab. |
32009 D 0010: décision 2009/10/CE de la Commission du 2 décembre 2008 établissant un formulaire relatif aux accidents majeurs conformément à la directive 96/82/CE du Conseil concernant la maîtrise des dangers liés aux accidents majeurs impliquant des substances dangereuses (JO L 6 du 10.1.2009, p. 64).» |
Article 2
Les textes de la décision 2009/10/CE en langues islandaise et norvégienne, à publier dans le supplément EEE du Journal officiel de l’Union européenne, font foi.
Article 3
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l’article 103, paragraphe 1, de l’accord EEE aient été faites au Comité mixte de l’EEE (2).
Article 4
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l’Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 6 du 10.1.2009, p. 64.
(2) Pas d’obligations constitutionnelles signalées.
|
24.1.2013 |
FR |
Journal officiel de l'Union européenne |
L 21/57 |
DÉCISION DU COMITÉ MIXTE DE L'EEE
N o 204/2012
du 26 octobre 2012
modifiant le protocole 10 de l'accord EEE concernant la simplification des contrôles et des formalités lors du transport de marchandises
LE COMITÉ MIXTE DE L'EEE,
vu l'accord sur l'Espace économique européen (ci-après dénommé «accord EEE»), et notamment son article 98,
considérant ce qui suit:
|
(1) |
Le chapitre II bis, article 9 ter, paragraphe 1, du protocole 10 de l'accord EEE prévoit que les parties contractantes mettent en place et appliquent aux marchandises qui entrent sur leur territoire douanier ou en sortent les mesures douanières de sécurité définies au chapitre II bis, garantissant ainsi un niveau de sécurité équivalent à leurs frontières externes. |
|
(2) |
Le chapitre II bis, article 9 nonies, du protocole 10 de l'accord EEE prévoit une procédure pour introduire les modifications nécessaires afin de tenir compte de l'évolution de la législation de l'Union européenne relative aux questions couvertes par le chapitre II bis. |
|
(3) |
La législation de l'Union européenne sur les mesures douanières de sécurité a été modifiée, en particulier par le règlement (CE) no 312/2009 de la Commission (1), le règlement (UE) no 169/2010 de la Commission (2) et le règlement (UE) no 430/2010 de la Commission (3). |
|
(4) |
Les dispositions du protocole 10 de l'accord EEE sont alignées sur les modifications de la législation de l'Union européenne, afin de garantir un niveau de sécurité équivalent. |
|
(5) |
La présente décision ne s'applique pas à l'Islande et au Liechtenstein. Toutefois, sous réserve d'une nouvelle décision, elle pourrait être ouverte à ces pays. |
|
(6) |
Il convient, dès lors, de modifier le protocole 10 de l'accord EEE en conséquence, |
A ADOPTÉ LA PRÉSENTE DÉCISION:
Article premier
L'annexe I du protocole 10 de l'accord EEE est modifiée comme suit:
|
1) |
l'article 2, paragraphe 1, point e), est remplacé par le texte suivant:
|
|
2) |
l'article 2, paragraphe 1, point j), est remplacé par le texte suivant:
|
|
3) |
les points suivants sont ajoutés après l'article 2, paragraphe 1, point l):
|
|
4) |
l'article 2, paragraphe 3, est remplacé par le texte suivant: «3. Une déclaration sommaire de sortie n'est pas requise dans les cas suivants:
|
Article 2
La présente décision entre en vigueur le 1er novembre 2012, pour autant que toutes les notifications prévues à l'article 103, paragraphe 1, de l'accord EEE aient été faites au Comité mixte de l'EEE (4).
Article 3
La présente décision est publiée dans la partie EEE et dans le supplément EEE du Journal officiel de l'Union européenne.
Fait à Bruxelles, le 26 octobre 2012.
Par le Comité mixte de l’EEE
Le président
Atle LEIKVOLL
(1) JO L 98 du 17.4.2009, p. 3.
(2) JO L 51 du 2.3.2010, p. 2.
(3) JO L 125 du 21.5.2010, p. 10.
(4) Pas d'obligations constitutionnelles signalées.
Déclaration conjointe des parties contractantes à la décision du Comité mixte de l'EEE no 204/2012 du 26 octobre 2012 modifiant le protocole 10, concernant le protocole 10, annexe I, article 1er, paragraphe 2
En ce qui concerne les données requises pour la déclaration sommaire d'entrée ou de sortie, les parties contractantes confirment que:
|
— |
les dispositions concernant les numéros EORI, |
|
— |
les dispositions concernant les exigences relatives aux demandes de détournement prévues au point 2.6 – tableau 6 de l'annexe 30 bis, |
introduites par le règlement (CE) no 312/2009 de la Commission du 16 avril 2009 ne s'appliquent pas aux déclarations déposées dans un État de l'AELE.