EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32010R1152
Commission Regulation (EU) No 1152/2010 of 8 December 2010 amending, for the purpose of its adaptation to technical progress, Regulation (EC) No 440/2008 laying down test methods pursuant to Regulation (EC) No 1907/2006 of the European Parliament and of the Council on the Registration, Evaluation, Authorisation and Restriction of Chemicals (REACH) Text with EEA relevance
Règlement (UE) n ° 1152/2010 de la Commission du 8 décembre 2010 modifiant, aux fins de son adaptation au progrès technique, le règlement (CE) n ° 440/2008 établissant des méthodes d'essai conformément au règlement (CE) n ° 1907/2006 du Parlement européen et du Conseil concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH) Texte présentant de l'intérêt pour l'EEE
Règlement (UE) n ° 1152/2010 de la Commission du 8 décembre 2010 modifiant, aux fins de son adaptation au progrès technique, le règlement (CE) n ° 440/2008 établissant des méthodes d'essai conformément au règlement (CE) n ° 1907/2006 du Parlement européen et du Conseil concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH) Texte présentant de l'intérêt pour l'EEE
OJ L 324, 9.12.2010, p. 13–38
(BG, ES, CS, DA, DE, ET, EL, EN, FR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
Special edition in Croatian: Chapter 15 Volume 009 P. 246 - 271
 In force
In force
|
9.12.2010 |
FR |
Journal officiel de l'Union européenne |
L 324/13 |
RÈGLEMENT (UE) No 1152/2010 DE LA COMMISSION
du 8 décembre 2010
modifiant, aux fins de son adaptation au progrès technique, le règlement (CE) no 440/2008 établissant des méthodes d'essai conformément au règlement (CE) no 1907/2006 du Parlement européen et du Conseil concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH)
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l'Union européenne,
vu le règlement (CE) no 1907/2006 du Parlement européen et du Conseil du 18 décembre 2006 concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH), instituant une agence européenne des produits chimiques, modifiant la directive 1999/45/CE et abrogeant le règlement (CEE) no 793/93 du Conseil et le règlement (CE) no 1488/94 de la Commission ainsi que la directive 76/769/CEE du Conseil et les directives 91/155/CEE, 93/67/CEE, 93/105/CE et 2000/21/CE de la Commission (1), et notamment son article 13, paragraphe 3,
considérant ce qui suit:
|
(1) |
Le règlement (CE) no 440/2008 de la Commission (2) définit les méthodes d'essai à appliquer pour déterminer les propriétés physico-chimiques ainsi que la toxicité et l'écotoxicité des substances, aux fins du règlement (CE) no 1907/2006. |
|
(2) |
Il est nécessaire de mettre à jour le règlement (CE) no 440/2008 afin d'y inclure en priorité deux nouvelles méthodes d'essai in vitro pour l'irritation oculaire, récemment adoptées par l'OCDE, en vue de réduire le nombre d'animaux utilisés à des fins expérimentales, conformément à la directive 86/609/CEE du Conseil du 24 novembre 1986 concernant le rapprochement des dispositions législatives, réglementaires et administratives des États membres relatives à la protection des animaux utilisés à des fins expérimentales ou à d'autres fins scientifiques (3). Les parties concernées ont été consultées sur le présent projet. |
|
(3) |
Il convient dès lors de modifier le règlement (CE) no 440/2008 en conséquence. |
|
(4) |
Les mesures prévues au présent règlement sont conformes à l’avis du comité institué par l’article 133 du règlement (CE) no 1907/2006, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
Les chapitres B.47 et B.48 qui figurent en annexe du présent règlement sont ajoutés dans la partie B de l'annexe du règlement (CE) no 440/2008.
Article 2
Le présent règlement entre en vigueur le troisième jour suivant celui de sa publication au Journal officiel de l'Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 8 décembre 2010.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 396 du 30.12.2006, p. 1.
(2) JO L 142 du 31.5.2008, p. 1.
(3) JO L 358 du 18.12.1986, p. 1.
ANNEXE
«B. 47 MÉTHODE D'ESSAI D'OPACITÉ ET DE PERMÉABILITÉ DE LA CORNÉE BOVINE POUR LA MISE EN ÉVIDENCE DES SUBSTANCES CORROSIVES ET FORTEMENT IRRITANTES POUR L'ŒIL
INTRODUCTION
|
1. |
La méthode d'essai d'opacité et de perméabilité de la cornée bovine (OPCB) est une méthode d'essai in vitro pouvant être utilisée, dans certaines circonstances, compte tenu de ses limites particulières, pour classer des substances et des mélanges dans la catégorie des produits “corrosifs et fortement irritants pour l’œil” (1) (2) (3). Aux fins de la présente méthode d'essai, les substances et mélanges fortement irritants sont définis comme ceux qui provoquent des lésions cutanées persistant, chez le lapin, au moins 21 jours après administration. Bien qu’elle n’ait pas été validée en tant que méthode remplaçant totalement l’essai oculaire in vivo chez le lapin, la méthode OPCB est néanmoins recommandée dans le cadre d’une stratégie d’essai séquentielle visant à établir une classification et un étiquetage réglementaires dans un champ spécifique d’application (4) (5). Les substances et mélanges d’essai (6) peuvent être classés corrosifs ou fortement irritants pour l’œil sans qu’il soit nécessaire de procéder à des essais supplémentaires chez le lapin. En revanche, une substance révélant un résultat négatif à l’issue de l’essai a besoin d’être testée sur des lapins selon une démarche expérimentale de type séquentiel, telle que celle décrite dans la ligne directrice de l’OCDE no 405 (7) (chapitre B.5 de la présente annexe). |
|
2. |
L'objet de la présente méthode d'essai est de décrire les procédures utilisées pour évaluer l'effet potentiel corrosif ou fortement irritant pour l'œil d'une substance d'essai. Cet effet est mesuré par la capacité de la substance à provoquer une opacité et une perméabilité cornéennes accrues sur une cornée bovine isolée. Les effets toxiques pour la cornée sont mesurés par: i) la diminution de la capacité de transmission de la lumière (opacité), et ii) l'augmentation du passage de la fluorescéine sodique (perméabilité). Les mesures de l'opacité et de la perméabilité de la cornée après exposition à la substance d'essai sont ensuite combinées pour établir le score d'irritation in vitro (SIIV), utilisé pour classer la substance d'essai en fonction de son pouvoir irritant. |
|
3. |
Des substances irritantes pour l’œil qui provoquent des lésions se résorbant en moins de 21 jours et des substances non irritantes ont également été testées par la méthode OPCB. Toutefois, pour les substances entrant dans ces catégories, la précision et la fiabilité de cette méthode n'ont pas été évaluées de façon formelle. |
|
4. |
Des définitions sont fournies dans l'appendice 1. |
REMARQUES PRÉLIMINAIRES ET LIMITES DE LA MÉTHODE
|
5. |
La présente méthode d'essai est fondée sur le protocole expérimental de la méthode OPCB (8) du Comité de coordination interagences pour la validation des méthodes alternatives (ICCVAM), élaboré à la suite d’une étude de validation internationale (4)(5)(9) à laquelle ont participé le Centre européen pour la validation de méthodes alternatives (ECVAM) et le Centre japonais pour la validation de méthodes alternatives (JaCVAM). Ce protocole s’appuie sur des informations provenant de l’Institute for In Vitro Sciences (IIVS) et sur le protocole INVITTOX no124 (10), qui a été utilisé lors de l’étude de prévalidation de l’essai OPCB conduite en 1997-1998 sous l’égide de la Communauté Européenne. Ces protocoles se fondent tous deux sur la méthode d’essai OPCB décrite pour la première fois par Gautheron et al. (11). |
|
6. |
Les limites connues de cette méthode d’essai concernent le taux élevé de faux positifs pour les alcools et les cétones, et le taux élevé de faux négatifs pour les substances solides, relevés dans la base de données de validation (voir paragraphe 44) (5). Si l’on exclut de la base de données les substances relevant de ces classes chimiques et physiques, la précision de la méthode OPCB au regard des systèmes de classifications de l’UE, de l’EPA et du SGH se trouve considérablement améliorée (5). Compte tenu de la finalité de cet essai (qui vise exclusivement à détecter les substances corrosives et fortement irritantes pour l’œil), les taux de faux négatifs ne sont pas préoccupants car les substances concernées feront ensuite l’objet d’essais chez le lapin ou d’autres essais in vitro dûment validés, conformément aux exigences de la réglementation, selon une démarche expérimentale séquentielle fondée sur la force probante des données. De surcroît, l’actuelle base de données de validation n’a pas permis de procéder à l’évaluation adéquate de certaines classes de substances chimiques ou de produits (par exemple, les mélanges). Les investigateurs peuvent néanmoins envisager d’avoir recours à cette méthode d’essai pour tous les types de matériel d’essai (y compris les mélanges), auquel cas un résultat positif pourrait être interprété comme révélateur d'un effet corrosif ou fortement irritant pour l’œil. Il convient toutefois d’interpréter avec prudence les résultats positifs obtenus avec des alcools ou des cétones en raison du risque de surestimation. |
|
7. |
Tous les modes opératoires faisant intervenir des yeux et des cornées de bovins doivent être conformes aux réglementations et procédures applicables à l’installation d’essai en matière de manipulation des produits dérivés d’animaux qui englobent, sans s’y limiter, les tissus et fluides tissulaires. Le respect des précautions universelles de laboratoire est recommandé (12). |
|
8. |
Bien qu’elle prenne en compte certains des effets oculaires évalués par la méthode d’essai d’irritation oculaire chez le lapin, et dans une certaine mesure leur degré de gravité, cette méthode d’essai présente toutefois l’inconvénient de ne pas prendre en considération les lésions de la conjonctive et de l’iris. De surcroît, même si la méthode OPCB ne permet pas en soi d'évaluer la réversibilité des lésions cornéennes, il a été proposé, sur la base d’études menées sur l’œil de lapin, d'utiliser une évaluation de la profondeur initiale de la lésion cornéenne pour distinguer les effets réversibles des effets irréversibles (13). Enfin, la méthode OPCB ne permet pas d'évaluer la toxicité systémique potentielle associée à l'exposition oculaire. |
|
9. |
Les travaux visant à mieux caractériser l’utilité et les limites de la méthode OPCB pour la mise en évidence des substances faiblement irritantes ou non irritantes se poursuivent (voir également le paragraphe 45). Les utilisateurs sont également incités à fournir des spécimens et/ou des données aux organismes de validation à des fins d’évaluation formelle des utilisations futures possibles de la méthode d’essai OPCB, notamment pour la mise en évidence des substances faiblement irritantes ou non irritantes. |
|
10. |
Tout laboratoire conduisant cet essai pour la première fois doit utiliser les substances chimiques d'épreuve de compétence mentionnées à l'appendice 2. Un laboratoire pourra faire valoir l’utilisation de ces substances pour démontrer sa compétence technique à conduire un essai selon la méthode OPCB avant de proposer les données issues de l’essai OPCB à des fins de classification réglementaire des dangers. |
PRINCIPE DE L'ESSAI
|
11. |
La méthode d'essai OPCB est un modèle organotypique qui permet de maintenir in vitro les fonctions physiologiques et biochimiques normales de la cornée bovine pendant une courte période. Selon cette méthode, les dommages causés par la substance d’essai sont évalués par des mesures quantitatives des modifications de l’opacité et de la perméabilité de la cornée réalisées, respectivement, à l’aide d’un opacitomètre et d’un spectrophotomètre visible. Ces deux mesures entrent dans le calcul du SIIV, utilisé pour assigner une catégorie de classification de danger d’irritation in vitro permettant d’estimer le potentiel d’irritation oculaire in vivo d’une substance d’essai (voir “Critères de décision”). |
|
12. |
La méthode d’essai OPCB utilise des cornées isolées provenant d’yeux de bovins récemment abattus. L’opacité cornéenne est mesurée par la quantité de lumière traversant la cornée. La perméabilité est mesurée par la quantité de fluorescéine sodique traversant toute l’épaisseur de la cornée, et détectée dans le milieu de la chambre postérieure. Les substances d’essai, introduites dans la chambre antérieure du porte-cornée, sont appliquées sur la surface épithéliale de la cornée. L’appendice 3 présente une description et un schéma de porte-cornée utilisé dans la méthode OPCB. Ces appareils sont disponibles dans le commerce auprès de différents fabricants, ou peuvent être construits. |
Provenance et âge des yeux de bovins et sélection des espèces animales
|
13. |
Les bovins envoyés à l’abattoir sont généralement destinés à la consommation humaine ou à d’autres usages commerciaux. Seules les cornées de bêtes en bonne santé, considérées comme propres à intégrer la chaîne alimentaire humaine, sont prélevées pour la méthode OPCB. Le poids des bovins variant considérablement en fonction de la race, de l'âge et du sexe, il n’existe aucune recommandation spécifique en la matière au moment de l’abattage. |
|
14. |
L’utilisation d’yeux provenant d’animaux d’âges différents peut entraîner des variations de dimension des cornées. Les cornées dont le diamètre horizontal est supérieur à 30,5 mm et l’épaisseur cornéenne centrale (ECC) supérieure ou égale à 1 100 μm ont généralement été prélevées sur des bovins de plus de huit ans, tandis que les cornées ayant un diamètre horizontal inférieur à 28,5 mm et une ECC inférieure à 900 μm proviennent plutôt de bêtes de moins de cinq ans (14). En conséquence, les yeux des bovins âgés de plus de 60 mois ne sont généralement pas utilisés. En général, les yeux des bovins de moins de 12 mois ne sont pas non plus utilisés, car leur développement n’est pas terminé et l'épaisseur ainsi que le diamètre de la cornée sont nettement inférieurs à ceux des yeux provenant de bovins adultes. Toutefois, les cornées issues d’animaux jeunes (entre 6 et 12 mois) sont acceptables car elles présentent certains avantages, tels qu’une plus grande disponibilité, une fourchette d’âge plus restreinte, et des risques moins importants d'exposition potentielle à l'encéphalopathie spongiforme bovine (15) pour le personnel. Une évaluation plus poussée des effets de la taille ou de l’épaisseur cornéenne sur la sensibilité aux substances corrosives et irritantes serait d’une grande utilité, aussi les utilisateurs sont-ils encouragés à consigner l’âge et/ou le poids estimés des animaux ayant fourni les cornées utilisées dans l’étude. |
Collecte et transport des yeux au laboratoire
|
15. |
Les yeux sont prélevés par les employés des abattoirs. Afin de minimiser tout endommagement, mécanique ou autre, des yeux, ceux-ci sont énucléés dès que possible après la mort de l’animal. Pour éviter d’exposer les yeux à des substances potentiellement irritantes, les employés de l’abattoir n’utilisent pas de détergent lors du rinçage de la tête de l’animal. |
|
16. |
Les yeux sont totalement immergés dans une solution saline équilibrée de Hank (HBSS), dans un récipient de taille adaptée, et transportés jusqu’au laboratoire en ayant soin de limiter le plus possible tout endommagement et/ou toute contamination bactérienne. Les yeux étant prélevés au cours de l'abattage, ils risquent d’entrer en contact avec du sang ou d’autres substances biologiques, notamment des bactéries et autres microorganismes. Il importe donc de réduire au minimum le risque de contamination (par exemple en plaçant le récipient contenant les yeux sur de la glace mouillée, et en ajoutant des antibiotiques à la HBSS utilisée pour le transport [100 UI/ml de pénicilline et 100 μg/ml de streptomycine, par exemple]). |
|
17. |
Il faut limiter au maximum l’intervalle de temps entre le prélèvement des yeux et l’utilisation des cornées dans le cadre de l’essai OPCB (l'utilisation a en général lieu le jour même du prélèvement) et démontrer qu’il ne compromet pas les résultats de l’essai. Ces résultats dépendent des critères de sélection des yeux, ainsi que des réponses des témoins positifs et négatifs. Tous les yeux utilisés dans l'essai proviennent d'un lot d'yeux collectés le même jour. |
Critères de sélection des yeux utilisés dans la méthode OPCB
|
18. |
Une fois parvenus au laboratoire, les yeux sont examinés avec soin pour déceler d’éventuels défauts, tels qu'une opacité avancée, des éraflures ou une néovascularisation. Seules les cornées d’yeux exempts de tout défaut seront utilisées. |
|
19. |
La qualité de chaque cornée est également évaluée à des stades ultérieurs de l’essai. Les cornées présentant une opacité supérieure à sept unités d’opacité (NB: l’opacitomètre est étalonné en fonction des normes d’opacité utilisées pour définir les unités d’opacité, voir appendice 3) après une période initiale d’équilibrage d’une heure sont écartées. |
|
20. |
Chaque lot de traitement (substance d’essai et témoins négatifs et positifs) est composé de trois yeux au minimum. L’essai OPCB nécessite trois cornées servant de témoins négatifs. Toutes les cornées étant prélevées sur le globe oculaire entier puis placées dans les chambres du porte-cornée, les manipulations peuvent entraîner d’éventuels artefacts sur les valeurs de l'opacité et de la perméabilité cornéennes de chaque élément (y compris le témoin négatif). Aussi, les valeurs d’opacité et de perméabilité mesurées sur les cornées témoins négatives servent-elles à corriger les valeurs d’opacité et de perméabilité cornéennes des spécimens et des témoins traités positifs lors du calcul du score d’irritation in vitro. |
MODE OPÉRATOIRE
Préparation des yeux
|
21. |
Des cornées exemptes de tout défaut sont découpées en conservant un bord de 2 à 3 mm de sclérotique destiné à faciliter les manipulations ultérieures, et en prenant soin de ne pas endommager l’épithélium et l’endothélium cornéens. Les cornées isolées sont placées dans des porte-cornées spécialement conçus à cet effet, qui se composent de deux compartiments, antérieur et postérieur, respectivement en contact avec les faces épithéliale et endothéliale de la cornée. Il convient de remplir jusqu’à débordement ces deux chambres d’un milieu essentiel minimum de Eagle (MEM) préalablement chauffé (en commençant par la chambre postérieure), en évitant toute formation de bulles d’air. L’appareil est ensuite équilibré à une température de 32 ± 1 °C pendant une heure au moins, afin que les cornées s’équilibrent avec le milieu et atteignent une activité métabolique aussi proche de la normale que possible (la température de la surface cornéenne in vivo est d’environ 32 °C). |
|
22. |
Après la période d’équilibrage, un nouveau MEM préalablement chauffé est ajouté dans les deux chambres, et une première mesure d’opacité est effectuée pour chaque cornée. Les cornées présentant une altération macroscopique des tissus (éraflures, pigmentation ou néovascularisation, par exemple) ou une opacité supérieure à 7 unités d'opacité sont écartées. L’opacité moyenne de toutes les cornées équilibrées est calculée. Au moins trois cornées présentant des valeurs d’opacité proches de la valeur médiane de toutes les cornées sont sélectionnées pour servir de témoins négatifs (ou témoins de solvant). Les cornées restantes sont ensuite réparties entre le lot de traitement et celui des témoins positifs. |
|
23. |
La capacité calorifique de l’eau étant supérieure à celle de l’air, l’eau procure des conditions de température plus stables pour l’incubation. Aussi est-il recommandé de plonger le porte-cornée dans un bain d’eau pour maintenir son contenu à 32 ± 1°C. Toutefois, il est également possible d’utiliser des incubateurs à air, à condition d’assurer la stabilité de la température (en chauffant au préalable les porte-cornées et le milieu, par exemple). |
Application de la substance d'essai
|
24. |
Deux protocoles d’application différents sont utilisés, l’un pour les liquides et les tensioactifs (solides ou liquides), et l’autre pour les solides non tensioactifs. |
|
25. |
Les liquides sont testés non dilués, tandis que les tensioactifs le sont à une concentration de 10 % en masse volumique dans une solution de chlorure de sodium à 0,9 %, d’eau distillée ou d’un autre solvant dont l’absence d’effets indésirables sur le système d’essai a été démontrée. Les semi-solides, crèmes et cires sont généralement testés en tant que liquides. Il conviendra de justifier de façon appropriée l’utilisation de tout autre taux de dilution. Les cornées sont ensuite exposées aux liquides ou tensioactifs pendant 10 minutes. L’utilisation d’une autre durée d’exposition devra être scientifiquement justifiée. |
|
26. |
Les solides non tensioactifs sont généralement testés sous forme de solutions ou de suspensions à une concentration de 20 % dans une solution de chlorure de sodium à 0,9 %, d’eau distillée ou d’un autre solvant dont l’absence d’effets indésirables sur le système d’essai a été démontrée. Dans certaines circonstances et uniquement si cela est justifié scientifiquement, les solides peuvent aussi être testés purs par application directe sur la surface cornéenne, selon la méthode en chambre ouverte (voir paragraphe 29). Les cornées sont exposées aux solides pendant quatre heures, mais comme pour les liquides et les tensioactifs, des durées d’exposition différentes sont possibles moyennant une justification scientifique appropriée. |
|
27. |
Différentes méthodes d’application peuvent être utilisées, en fonction de la nature physique et des caractéristiques chimiques des substances d’essai (solides, liquides, liquides visqueux ou non visqueux, par exemple). Il est très important que la substance d’essai recouvre convenablement la surface épithéliale puis soit correctement retirée durant les étapes de rinçage. Il conviendra généralement d’utiliser la méthode en chambre fermée pour les substances d’essai liquides non visqueuses ou légèrement visqueuses, tandis que la méthode en chambre ouverte sera privilégiée pour les substances d’essai semi-visqueuses et visqueuses et pour les solides purs. |
|
28. |
Dans la méthode en chambre fermée, une quantité de substance d’essai suffisante pour recouvrir la face épithéliale de la cornée (750 μl) est introduite dans la chambre antérieure par les trous de dosage situés sur la face supérieure de celle-ci. Les trous sont ensuite occultés à l’aide de capuchons durant la durée d’exposition. Il importe de s’assurer que chaque cornée est exposée à la substance d’essai pendant la durée qui convient. |
|
29. |
Dans la méthode en chambre ouverte, la goupille de fermeture et la fenêtre en verre de la chambre antérieure sont retirées avant l’application. La substance d’essai ou témoin (750 μl, ou une quantité suffisante pour recouvrir entièrement la cornée) est directement appliquée sur la surface épithéliale cornéenne à l’aide d’une micropipette. Si la substance d’essai est difficile à pipetter, il est possible d’utiliser une pipette à déplacement positif qui permet un dosage plus précis. L’embout de la pipette à déplacement positif est inséré dans l’embout distributeur de la seringue, de manière à ce que la substance puisse être chargée dans la pipette sous pression. Il convient ensuite de pousser le piston de la seringue tout en tirant simultanément celui de la pipette. Si des bulles d’air se forment dans l’embout de la pipette, il faut alors retirer la substance d’essai (en l’expulsant) et répéter le processus jusqu’à ce qu’aucune bulle d’air n’apparaisse au moment du remplissage de la pipette. Il est possible d’utiliser si nécessaire une seringue normale (sans aiguille), ce qui permet de mesurer un volume précis de substance d’essai et de l’appliquer plus facilement sur la surface épithéliale de la cornée. Après le dosage, la fenêtre en verre est replacée sur l’ouverture de la chambre antérieure afin de recréer un système fermé. |
Incubation post-exposition
|
30. |
Après la période d’exposition, la substance d’essai, ou la substance témoin négative ou positive, est retirée de la chambre antérieure et l’épithélium est rincé au moins trois fois (ou jusqu’à ce qu’aucune trace de la substance d’essai ne soit plus visible) au moyen d’un MEM contenant du rouge de phénol. Le rinçage est effectué à l’aide d’un milieu contenant du rouge de phénol, dont le changement de couleur permet de déterminer l’efficacité du rinçage des substances acides ou alcalines. Il convient de laver à nouveau les cornées si, après trois rinçages, le rouge de phénol est encore altéré (jaune ou violet) ou si la substance d’essai est toujours visible. Une fois le milieu débarrassé de la substance, les cornées subissent un dernier rinçage avec un MEM sans rouge de phénol, ce qui permet de s’assurer que la chambre antérieure est débarrassée de tout rouge de phénol avant la mesure d’opacité. La chambre antérieure est ensuite à nouveau remplie d’un MEM neuf sans rouge de phénol. |
|
31. |
Pour les liquides et les tensioactifs, les cornées sont incubées après rinçage pendant deux heures supplémentaires à 32 ± 1 °C. Il peut être utile, dans certaines circonstances (déterminées au cas par cas), de prévoir une durée d’incubation post-exposition plus longue. Les cornées sur lesquelles des solides ont été appliqués sont soigneusement rincées après la période d’exposition de quatre heures, et ne requièrent pas d’incubation supplémentaire. |
|
32. |
Au terme de la période d’incubation post-exposition pour les liquides et les tensioactifs, et au terme de la période d’exposition de quatre heures pour les solides non tensioactifs, les degrés d’opacité et de perméabilité de chaque cornée sont enregistrés. En outre, chaque cornée fait l'objet d'un examen visuel et les observations pertinentes sont consignées (exfoliation des tissus, résidus de substance d’essai ou opacité non uniforme, par exemple). Ces observations peuvent s’avérer importantes car elles peuvent se traduire par des variations de lecture de l’opacitomètre. |
Substances témoins
|
33. |
Des témoins négatifs ou des témoins de solvant/véhicule ainsi que des témoins positifs sont inclus en parallèle dans chaque expérience. |
|
34. |
Lorsqu’une substance liquide non diluée est soumise à l’essai, il convient d’inclure dans la méthode d’essai OPCB une substance témoin négatif concurrente (solution de chlorure de sodium à 0,9 % ou eau distillée, par exemple) afin de détecter des changements non intrinsèques au système d’essai et de fournir un point de référence pour les critères d’évaluation de l’essai. Cette méthode permet également de garantir que les conditions de l’essai n’entraînent aucune réaction d’irritation indésirable. |
|
35. |
Lorsqu’un liquide dilué, un tensioactif ou un solide est soumis à l’essai, il convient d’inclure dans la méthode d’essai OPCB un lot témoin de solvant/véhicule concurrent afin de détecter des changements non intrinsèques au système d’essai et de fournir un point de référence pour les critères d’évaluation de l’essai. On utilisera uniquement des solvants/véhicules dont l’absence d’effets indésirables sur le système d’essai a été démontrée. |
|
36. |
Chaque expérience comprend une substance irritante pour les yeux connue en tant que témoin positif, afin de vérifier l'induction d'une réponse appropriée. La méthode d’essai OPCB étant utilisée ici pour mettre en évidence des substances corrosives ou fortement irritantes, le témoin positif servant de référence est idéalement une substance entraînant une réaction d’irritation importante dans le cadre de cette méthode. Cependant, afin de pouvoir évaluer la variabilité des réponses du témoin positif dans le temps, l’ampleur des effets irritants ne devra pas être excessive. |
|
37. |
Pour les substances d’essai liquides, les témoins positifs peuvent être composés de diméthylformamide ou d’hydroxyde de sodium à 1 %, par exemple. Pour les substances d’essai solides, les témoins positifs peuvent être composés d’imidazole à 20 % (en masse volumique) dans une solution de chlorure de sodium à 0,9 %, par exemple. |
|
38. |
Les substances étalons sont utiles pour évaluer le potentiel d'irritation oculaire de produits chimiques inconnus d'une classe chimique ou d'une catégorie de produits spécifique, ou pour évaluer le potentiel d'irritation relatif d'une substance irritante pour les yeux au sein d'une plage spécifique de réponses. |
Effets mesurés
|
39. |
L’opacité est déterminée par la quantité de lumière traversant la cornée. L’opacité de la cornée est mesurée de manière quantitative à l’aide d’un opacitomètre, qui donne des valeurs d’opacité situées sur une échelle continue. |
|
40. |
La perméabilité est déterminée par la quantité de fluorescéine sodique pénétrant la totalité des couches cellulaires de la cornée (de l’épithélium sur la face externe de la cornée à l’endothélium sur sa face interne). Un volume de 1 ml de solution de fluorescéine sodique (respectivement 4 ou 5 mg/ml lors d’essais portant sur des liquides et des tensioactifs ou sur des solides non tensioactifs) est introduit dans la chambre antérieure du porte-cornée, en contact avec la face épithéliale de la cornée, tandis que la chambre postérieure, en contact avec la face endothéliale, est remplie d’un nouveau MEM. Le porte-cornée est ensuite incubé en position horizontale pendant 90 ± 5 min à une température de 32 ± 1 °C. La quantité de fluorescéine sodique passant dans la chambre postérieure est mesurée quantitativement par spectrophotométrie UV-visible. Les mesures spectrophotométriques évaluées à 490 nm sont enregistrées en tant que valeurs de densité optique (DO490) ou d’absorbance, mesurées sur une échelle continue. La perméabilité à la fluorescéine est déterminée à l’aide des valeurs de DO490 données par un spectrophotomètre visible utilisant un trajet optique standard de 1 cm. |
|
41. |
Il est également possible d’utiliser un lecteur de plaques de microtitration à 96 puits, à condition: i) de pouvoir définir l’intervalle linéaire du lecteur de plaque servant à déterminer les valeurs de la DO490 de la fluorescéine; et ii) d’utiliser le bon volume d’échantillons de fluorescéine sur la plaque à 96 puits afin d’obtenir des valeurs de la DO490 équivalentes au trajet optique standard de 1 cm (ce qui peut nécessiter de remplir entièrement les puits [généralement 360 μl]). |
RÉSULTATS ET RAPPORT
Évaluation des données
|
42. |
Une fois que les valeurs d’opacité et de perméabilité moyenne (DO490) ont été corrigées de l’opacité de fond et des valeurs DO490 de perméabilité des témoins négatifs, l’opacité moyenne et les valeurs DO490 de perméabilité moyenne pour chaque lot de traitement sont combinées dans une formule établie empiriquement pour calculer, comme suit, le score d’irritation in vitro (SIIV) de chaque lot de traitement: SIIV = valeur moyenne d’opacité + (15 × valeur DO490 de perméabilité moyenne) D’après Sina et al. (16), cette formule a été établie au cours d'études intra et interlaboratoires. Les données générées pour une série de 36 composés dans le cadre d’une étude interlaboratoires ont été soumises à une analyse à variables multiples afin de déterminer l'équation du meilleur ajustement entre les données in vivo et in vitro. Cette analyse a été réalisée par des scientifiques travaillant dans deux entreprises distinctes, qui ont obtenu des équations pratiquement identiques. |
|
43. |
Les valeurs d’opacité et de perméabilité sont également évaluées de manière indépendante afin de déterminer si une substance d'essai a provoqué une corrosion ou une forte irritation pour un seul des deux critères (voir «Critères de décision»). |
Critères de décision
|
44. |
Une substance induisant un SIIV ≥ 55,1 est définie comme corrosive ou fortement irritante. Comme indiqué au paragraphe 1, s'il n'est pas démontré que la substance d'essai est corrosive ou fortement irritante pour l'œil, il convient de mener des essais complémentaires à des fins de classification et d'étiquetage. La méthode d’essai OPCB présente une précision d’ensemble comprise entre 79 % (113/143) et 81 % (119/147), un taux de faux positifs allant de 19 % (20/103) à 21 % (22/103) et un taux de faux négatifs allant de 16 % (7/43) à 25 % (10/40), en comparaison avec les données de la méthode d’essai in vivo sur les yeux de lapin classées selon les systèmes de classification de l’EPA (1), de l’UE (2) ou du SGH (3). Si l’on exclut de la base de données les substances relevant de certaines classes chimiques (alcools, cétones) ou physiques (substances solides), la précision de la méthode OPCB au regard des systèmes de classification de l’UE, de l’EPA et du SGH va de 87 % (72/83) à 92 % (78/85), le taux de faux positifs de 12 % (7/58) à 16 % (9/56), et le taux de faux négatifs de 0 % (0/27) à 12 % (3/26). |
|
45. |
Même si une substance d’essai n’est pas classée comme corrosive ou fortement irritante pour l'œil, les données de la méthode d'essai OPCB peuvent servir, en association avec des résultats d’essais in vivo sur des yeux de lapin ou d’un autre test in vitro dûment validé, à évaluer plus en profondeur l’utilité et les limites de la méthode OPCB pour la détection des substances faiblement irritantes ou non irritantes (un document d'orientation sur l’utilisation de méthodes d’essai de toxicité oculaire in vitro est en cours d'élaboration). |
Critères d'acceptation de l'étude
|
46. |
Un essai est considéré comme acceptable si le témoin positif présente un SIIV compris dans un intervalle de deux écarts-types autour de la moyenne historique actuelle, qui est mise à jour au moins tous les trois mois, ou chaque fois qu’un essai acceptable est mené dans des laboratoires conduisant peu fréquemment (c'est-à-dire moins d'une fois par mois) ce type d’étude. Les réponses du témoin négatif ou du témoin de solvant/véhicule doivent donner des valeurs d’opacité et de perméabilité situées en deçà des limites maximales établies pour les valeurs d’opacité et de perméabilité de fond des cornées bovines traitées avec les témoins négatifs ou les témoins de solvant/véhicule correspondants. |
Rapport d'essai
|
47. |
Le rapport d’essai contient les renseignements suivants, pour autant qu'ils présentent un intérêt pour l'étude: Substances d’essai et témoins
Renseignements relatifs au commanditaire et à l’installation d’essai:
Justification du choix de la méthode d'essai et du mode opératoire Intégrité de la méthode d'essai Mode opératoire utilisé pour assurer l'intégrité (précision et fiabilité) de la méthode d'essai au cours du temps (par exemple essai périodique des substances d’épreuve de compétence, utilisation de données antérieures de témoins positifs et négatifs). Critères d'acceptabilité de l’essai
Conditions de l'essai
Résultats
Discussion des résultats Conclusion |
BIBLIOGRAPHIE
|
(1) |
U.S. EPA (1996). Label Review Manual: 2nd Edition. EPA737-B-96-001. Washington, DC: U.S. Environmental Protection Agency. |
|
(2) |
Règlement (CE) no 1272/2008 du Parlement européen et du Conseil du 16 décembre 2008 relatif à la classification, à l'étiquetage et à l'emballage des substances et des mélanges, modifiant et abrogeant les directives 67/548/CEE et 1999/45/CE et modifiant le règlement (CE) no 1907/2006. JO L 353 du 31.12.2008, p. 1. |
|
(3) |
Nations Unies (ONU) (2007). Système général harmonisé de classification et d'étiquetage des produits chimiques (SGH), deuxième édition révisée, Nations unies, New York et Genève, 2007. Disponible à l'adresse suivante: [http://www.unece.org/trans/danger/publi/ghs/ghs_rev02/02files_f.html] |
|
(4) |
ESAC (2007). Statement on the conclusion of the ICCVAM retrospective study on organotypic in vitro assays as screening tests to identify potential ocular corrosives and severe eye irritants. Disponible à l'adresse suivante: [http://ecvam.jrc.it/index.htm] |
|
(5) |
ICCVAM (2007). Test Method Evaluation Report - In Vitro Ocular Toxicity Test Methods for Identifying Ocular Severe Irritants and Corrosives. Interagency Coordinating Committee on the Validation of Alternative Methods (ICCVAM) and the National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). NIH Publication No.: 07-4517. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm] |
|
(6) |
Règlement (CE) no 1907/2006 du Parlement européen et du Conseil du 18 décembre 2006 concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH), instituant une agence européenne des produits chimiques, modifiant la directive 1999/45/CE et abrogeant le règlement (CEE) no 793/93 du Conseil et le règlement (CE) no 1488/94 de la Commission ainsi que la directive 76/769/CEE du Conseil et les directives 91/155/CEE, 93/67/CEE, 93/105/CE et 2000/21/CE de la Commission. JO L 396 du 30.12.2006, p. 1. |
|
(7) |
OCDE (2002). Ligne directrice 405. Ligne directrice de l'OCDE pour les essais de produits chimiques. Effet irritant/corrosif aigu sur les yeux. Disponible à l'adresse suivante: [http://www.oecd.org/document/40/0,2340,en_2649_34377_37051368_1_1_1_1,00.html] |
|
(8) |
ICCVAM (2007). ICCVAM Recommended BCOP Test Method Protocol. In: ICCVAM Test Method Evaluation Report - In Vitro Ocular Toxicity Test Methods for Identifying Ocular Severe Irritants and Corrosives. Interagency Coordinating Committee on the Validation of Alternative Methods (ICCVAM) and the National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). NIH Publication No.: 07-4517. Disponible à l'adresse suivante: http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm] |
|
(9) |
ICCVAM. (2006). Current Status of In Vitro Test Methods for Identifying Ocular Corrosives and Severe Irritants: Bovine Corneal Opacity and Permeability Test Method. NIH Publication No.: 06-4512. Research Triangle Park: National Toxicology Program. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_ice.htm] |
|
(10) |
INVITTOX (1999). Protocol 124: Bovine Corneal Opacity and Permeability Assay – SOP of Microbiological Associates Ltd. Ispra, Italy: Centre européen pour la validation des méthodes alternatives (ECVAM) |
|
(11) |
Gautheron, P., Dukic, M., Alix, D. and Sina, J.F. (1992). Bovine corneal opacity and permeability test: An in vitro assay of ocular irritancy. Fundam. Appl. Toxicol. 18:442-449. |
|
(12) |
Siegel, J.D., Rhinehart, E., Jackson, M., Chiarello, L., and the Healthcare Infection Control Practices Advisory Committee (2007). Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in Healthcare Settings. Disponible à l'adresse suivante: [http://www.cdc.gov/ncidod/dhqp/pdf]. |
|
(13) |
Maurer, J.K., Parker, R.D. and Jester, J.V. (2002). Extent of corneal injury as the mechanistic basis for ocular irritation: key findings and recommendations for the development of alternative assays. Reg. Tox. Pharmacol. 36:106-117. |
|
(14) |
Doughty, M.J., Petrou, S. and Macmillan, H. (1995). Anatomy and morphology of the cornea of bovine eyes from a slaughterhouse. Can. J. Zool. 73:2159-2165. |
|
(15) |
Collee, J. and Bradley, R. (1997). BSE: A decade on - Part I. The Lancet 349: 636-641. |
|
(16) |
Sina, J.F., Galer, D.M., Sussman, R.S., Gautheron, P.D., Sargent, E.V., Leong, B., Shah, P.V., Curren, R.D., and Miller, K. (1995). A collaborative evaluation of seven alternatives to the Draize eye irritation test using pharmaceutical intermediates. Fundam Appl Toxicol 26:20-31. |
|
(17) |
ICCVAM (2006). Background review document, Current Status of In Vitro Test Methods for Identifying Ocular Corrosives and Severe Irritants: Bovine Corneal Opacity and Permeability (BCOP) Test Method. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm] |
|
(18) |
ICCVAM (2006). Background review document, Current Status of In Vitro Test Methods for Identifying Ocular Corrosives and Severe Irritants: Isolated Chicken Eye (ICE) Test Method. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm] |
Appendice 1
DÉFINITIONS
Précision: degré de concordance entre les résultats de la méthode d'essai et les valeurs de référence acceptées. La précision constitue une mesure de la performance de la méthode d'essai et un aspect de sa «pertinence». Ce terme est souvent utilisé de façon interchangeable avec «concordance» pour désigner la proportion de résultats corrects d'une méthode d'essai.
Substance étalon: substance utilisée en tant que référence, pour la comparaison avec une substance d'essai. Une substance étalon présente les propriétés suivantes: i) provient d'une ou de plusieurs sources constantes et fiables; ii) présente une similitude structurale et fonctionnelle avec la classe des substances soumises à l'essai; iii) possède des caractéristiques physiques/chimiques connues; iv) est accompagnée de données confirmant ses effets connus, et v) a une puissance connue dans la fourchette de réponses désirées.
Cornée: partie transparente située à l’avant du globe oculaire, recouvrant l’iris et la pupille et laissant pénétrer la lumière vers l’intérieur de l’œil.
Opacité cornéenne: mesure de l’étendue du caractère opaque de la cornée suite à son exposition à une substance d’essai. Une augmentation de l'opacité cornéenne indique un endommagement de la cornée. L’opacité peut être évaluée de manière subjective, par exemple lors du test de Draize réalisé sur les yeux de lapin, ou de manière objective à l'aide d'un instrument de mesure tel qu'un «opacitomètre».
Perméabilité cornéenne: Mesure quantitative de l’endommagement de l’épithélium cornéen via la détermination de la quantité de fluorescéine sodique traversant toutes les couches cellulaires de la cornée.
Catégorie 1 de l'EPA: effet corrosif (destruction irréversible du tissu oculaire) ou complication cornéenne ou irritation persistant plus de 21 jours (1).
Catégorie R41 de l'UE: lésion des tissus oculaires ou dégradation sévère de la vue, provoquée par l'application d'une substance d'essai sur la face antérieure de l'œil, et qui n'est pas totalement réversible dans les 21 jours suivant l'application (2).
Taux de faux négatifs: proportion de substances positives faussement déclarées négatives par une méthode d'essai. C'est un indicateur de la performance de la méthode d'essai.
Taux de faux positifs: proportion des substances négatives faussement déclarées positives par une méthode d'essai. C'est un indicateur de la performance de la méthode d'essai.
SGH (Système général harmonisé de classification et d'étiquetage des produits chimiques): système proposant la classification des produits chimiques (substances et mélanges) conformément à des types et des niveaux normalisés de dangers physiques, sanitaires et environnementaux, ainsi que la communication des éléments d'information correspondants, notamment par des pictogrammes, mentions d’avertissement, mentions de danger, conseils de prudence et fiches de données de sécurité, afin de diffuser des informations sur leurs effets indésirables dans l'objectif de protéger les personnes (en particulier les employeurs, employés, transporteurs, consommateurs et personnels des services d'urgence) et l'environnement (3).
Catégorie 1 du SGH: lésion des tissus oculaires ou dégradation sévère de la vue, provoquée par l'application d'une substance d'essai sur la face antérieure de l'œil, et qui n'est pas totalement réversible dans les 21 jours suivant l'application (3).
Danger: propriété intrinsèque d'un agent ou situation susceptible de provoquer des effets néfastes lorsqu'un organisme, un système ou une (sous-)population est exposé(e) à cet agent.
Score d'irritation in vitro (SIIV): formule établie empiriquement et utilisée dans les essais OPCB, dans laquelle les valeurs d'opacité moyenne et de perméabilité moyenne pour chaque lot de traitement sont combinées pour obtenir le score in vitro unique de chaque lot de traitement. SIIV = valeur moyenne d’opacité + (15 x valeur moyenne de perméabilité).
Témoin négatif: réplicat non traité contenant tous les composants d’un système d’essai. Cet échantillon subit les mêmes procédures que les échantillons traités avec la substance d'essai et les autres échantillons témoins afin de déterminer si le solvant interagit avec le système d’essai.
Substance non irritante: substance qui n'est pas classée comme irritant oculaire dans la catégorie I, II ou III de l'EPA, la catégorie R41 ou R36 de l'UE, ou la catégorie 1, 2A ou 2B du SGH.
Substance corrosive pour l'œil: a) substance provoquant des lésions irréversibles des tissus oculaires; b) substance classée comme irritant oculaire dans la catégorie 1 du SGH, la catégorie 1 de l’EPA ou la catégorie R41 de l’UE (1) (2) (3).
Substance irritante pour l'œil: a) substance provoquant une modification réversible de l’œil suite à une application sur la face antérieure de l’œil; b) substance classée comme irritant oculaire dans la catégorie II ou III de l'EPA, la catégorie R36 de l'UE ou la catégorie 2A ou 2B du SGH (1) (2) (3).
Substance fortement irritante pour l'œil: a) substance provoquant des lésions des tissus oculaires suite à une application sur la face antérieure de l’œil, qui ne sont pas résorbées dans les 21 jours suivant le traitement ou entraînent une dégradation sévère de la vue; b) substance classée comme irritant oculaire dans la catégorie 1 du SGH, la catégorie 1 de l’EPA ou la catégorie R41 de l’UE (1) (2) (3).
Opacitomètre: Instrument servant à mesurer l’«opacité cornéenne» en évaluant la quantité de lumière transmise à travers la cornée. En général, cet instrument est composé de deux compartiments, chacun disposant de sa propre source lumineuse et d'une cellule photoélectrique. L’un des compartiments est utilisé pour la cornée traitée tandis que l'autre sert à étalonner l’instrument et à le mettre à zéro. La lumière d’une lampe halogène est dirigée à travers un compartiment témoin (chambre vide, sans vitre ni liquide) vers une cellule photoélectrique, et comparée à la lumière envoyée à travers le compartiment expérimental, qui abrite la chambre contenant la cornée, jusqu'à une cellule photoélectrique. La lumière transmise par les deux cellules photoélectriques est ensuite comparée, et une valeur chiffrée d'opacité s’affiche sur un écran numérique.
Témoin positif: réplicat contenant tous les composants d’un système d’essai, et traité avec une substance induisant notoirement une réponse positive. Afin de pouvoir évaluer la variabilité des réponses du témoin positif dans le temps, la sévérité de la réponse ne devra pas être excessive.
Fiabilité: mesure de la reproductibilité de l'essai mis en œuvre, au sein d'un laboratoire et entre des laboratoires, au cours du temps, en utilisant le même mode opératoire. Elle est évaluée par calcul de la reproductibilité intralaboratoire et interlaboratoires et de la répétabilité intralaboratoire.
Témoin de solvant/véhicule: échantillon non traité contenant tous les composants d’un système d’essai, y compris le solvant ou véhicule utilisé pour tester les échantillons témoins traités ou non avec la substance d’essai afin de déterminer une réponse de référence pour les échantillons traités avec la substance d’essai dissoute dans le même solvant ou véhicule. Testé avec un témoin négatif concurrent, cet échantillon indique également si le solvant ou véhicule interagit avec le système d'essai.
Stratégie d'essai séquentielle: démarche expérimentale séquentielle consistant à examiner toutes les informations existantes sur une substance d'essai dans un ordre déterminé, en ayant recours à chaque étape à une procédure fondée sur la force probante des données pour déterminer si les informations disponibles sont suffisantes pour décider d'une classification des dangers, avant de passer à l'étape suivante. Si le potentiel d’irritation d’une substance d’essai peut être déterminé sur la base des informations existantes, aucun essai supplémentaire n’est nécessaire. Dans le cas contraire, une procédure expérimentale progressive de type séquentiel sur des animaux est alors lancée jusqu’à ce qu’une classification sans équivoque puisse être effectuée.
Méthode d'essai validée: méthode d'essai ayant fait l'objet d'études de validation visant à déterminer sa pertinence (notamment sa précision) et sa fiabilité à des fins spécifiques. Il importe de noter que les performances d'une méthode d'essai validée peuvent être insuffisantes en termes de précision et de fiabilité pour qu'elle soit jugée acceptable pour les besoins envisagés.
Force probante des données: prise en compte des forces et des faiblesses de divers éléments d’information en vue d'aboutir à une conclusion concernant le danger potentiel d’une substance et d’étayer cette conclusion.
Appendice 2
Substances d’épreuve de compétence pour la méthode d’essai OPCB
Avant l'utilisation en routine d'une méthode d'essai conforme à la présente méthode, les laboratoires peuvent souhaiter faire la preuve de leurs compétences techniques en déterminant correctement la catégorie de corrosivité oculaire des 10 substances recommandées dans le tableau 1. Ces substances ont été sélectionnées de façon à représenter la gamme des réactions locales d'irritation/de corrosion oculaire, sur la base des résultats de l’essai in vivo sur œil de lapin (LD 405) [c’est-à-dire les catégories 1, 2A, 2B ou Non classé du SGH des Nations Unies (3) (7)]. Toutefois, compte tenu de l’utilité validée de ces essais (uniquement mise en évidence des substances corrosives/fortement irritantes pour l'œil), seuls deux résultats expérimentaux obtenus à des fins de classification (substance corrosive/fortement irritante ou substance non corrosive/faiblement irritante) permettent de démontrer les compétences des laboratoires. Les autres critères de sélection retenus ont trait à la disponibilité des substances dans le commerce, à la disponibilité de données de référence in vivo de bonne qualité, et à l’existence de données de bonne qualité issues des deux méthodes d’essai in vitro qui font l’objet de lignes directrices. Pour cette raison, les substances irritantes ont été sélectionnées dans la liste recommandée par l'ICCVAM de 122 substances de référence pour la validation de méthodes d'essai de toxicité oculaire in vitro [voir appendice H: Substances de référence recommandées par l'ICCVAM (5)]. Les données de référence sont disponibles dans les documents de l’ICCVAM (Background Review Documents) pour les méthodes OPCB et OPI (œil de poulet isolé) (17) (18).
Tableau 1
Substances recommandées pour la démonstration des compétences techniques des laboratoires au regard de la méthode d'essai OPCB
|
Substance |
No CAS |
Classe chimique (1) |
Forme physique |
Classification in vivo (2) |
Classification in vitro (3) |
|
Chlorure de benzalconium (5 %) |
8001-54-5 |
Composé d'onium |
Liquide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Chlorhexidine |
55-56-1 |
Amine, Amidine |
Solide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Acide dibenzoyl-L-tartrique |
2743-38-6 |
Acide carboxylique, ester |
Solide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Imidazole |
288-32-4 |
Hétérocycle |
Solide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Acide trichloroacétique (30 %) |
76-03-9 |
Acide carboxylique |
Liquide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Chlorure de 2,6-dichlorobenzoyle |
4659-45-4 |
Halogénure d'acyle |
Liquide |
Catégorie 2A |
Non corrosif/Faiblement irritant |
|
2-méthylacéto-acétate d'éthyle |
609-14-3 |
Cétone, Ester |
Liquide |
Catégorie 2B |
Non corrosif/Faiblement irritant |
|
Nitrate d'ammonium |
6484-52-2 |
Sel inorganique |
Solide |
Catégorie 2A |
Non corrosif/Faiblement irritant |
|
Glycérol |
56-81-5 |
Alcool |
Liquide |
Non étiqueté |
Non corrosif/Faiblement irritant |
|
n-Hexane |
110-54-3 |
Hydrocarbure (acyclique) |
Liquide |
Non étiqueté |
Non corrosif/Faiblement irritant |
|
Abréviations: No CAS = Numéro d'enregistrement au Chemical Abstract Service |
|||||
Appendice 3
PORTE-CORNÉE POUR LA MÉTHODE OPCB
|
1. |
Les porte-cornées pour la méthode OPCB sont fabriqués à partir d’un matériau inerte (polypropylène par exemple). Ils se composent de deux parties (une chambre antérieure et une chambre postérieure) et possèdent deux chambres internes cylindriques identiques. Chaque chambre a une contenance de 5 ml et est fermée par une vitre, à travers laquelle les mesures d’opacité sont lues. Chacune des chambres internes mesure 1,7 cm de diamètre et 2,2 cm de profondeur (4). Un joint torique situé au niveau de la chambre postérieure empêche toute fuite. La cornée est placée face endothéliale dessous, sur le joint torique de la chambre postérieure, et la chambre antérieure est placée du côté épithélial de la cornée. Les chambres sont maintenues en place par trois vis en acier inoxydable situées sur les bordures extérieures du porte-cornée. Chaque chambre comporte à son extrémité une vitre amovible permettant d’accéder facilement à la cornée. Un joint torique placé entre la vitre et la chambre empêche toute fuite. L’introduction et le vidage du milieu et des composés d’essai se font par deux trous situés sur la face supérieure de chaque chambre. Pendant le traitement et les périodes d’incubation, ces trous sont obturés par des capuchons en caoutchouc.
|
L'OPACITOMÈTRE
|
2. |
L’opacitomètre est un appareil permettant de mesurer la transmission de la lumière. La lumière d’une lampe halogène est dirigée à travers un compartiment témoin (chambre vide, sans vitre ni liquide) vers une cellule photoélectrique, et comparée à la lumière envoyée à travers le compartiment expérimental, qui abrite la chambre contenant la cornée, jusqu'à une cellule photoélectrique. La lumière transmise par les deux cellules photoélectriques est ensuite comparée, et une valeur chiffrée d'opacité s’affiche sur un écran numérique. Les unités d’opacité sont alors définies. |
|
3. |
L’opacitomètre fournit une réponse linéaire sous la forme d'une plage de mesures d’opacité couvrant les seuils utilisés pour les différentes classifications décrites par le modèle de prévision (c’est-à-dire, jusqu’aux seuils déterminant le caractère corrosif/fortement irritant). Afin de garantir des mesures linéaires et précises jusqu’à 75-80 unités d’opacité, il est nécessaire d’étalonner l’opacitomètre à l’aide d’une série de calibreurs. Les calibreurs (plaques opaques de polyester) sont placés à l’intérieur de la chambre d’étalonnage (une chambre de porte-cornée destinée à contenir les calibreurs) et une mesure des calibreurs est réalisée sur l'opacitomètre. La chambre d’étalonnage est conçue pour maintenir les calibreurs approximativement à la même distance de la source lumineuse et de la cellule photoélectrique que celle où se trouveront les cornées lors des mesures d'opacité. L'opacitomètre est tout d'abord étalonné à 0 unité d'opacité en utilisant la chambre d’étalonnage sans calibreur. Trois calibreurs différents sont ensuite placés l’un après l’autre à l’intérieur de la chambre d’étalonnage, et l’opacité est mesurée. Les calibreurs 1, 2 et 3 présentent des mesures d’opacité égales à leur valeur de consigne, soit respectivement 75, 150 et 225 unités d’opacité, ± 5 %. |
B. 48 MÉTHODE D'ESSAI SUR ŒIL DE POULET ISOLÉ POUR LA MISE EN ÉVIDENCE DES SUBSTANCES CORROSIVES ET FORTEMENT IRRITANTES POUR L'ŒIL
INTRODUCTION
|
1. |
La méthode d'essai sur œil de poulet isolé (OPI) est une méthode d'essai in vitro pouvant être utilisée, dans certaines circonstances et compte tenu de ses limites particulières, pour classer des substances et des mélanges dans la catégorie des produits “corrosifs et fortement irritants pour l’œil” (1) (2) (3). Aux fins de la présente méthode d'essai, les substances et mélanges fortement irritants sont ceux qui induisent des lésions oculaires qui persistent pendant au moins 21 jours après administration chez le lapin. Le remplacement intégral par l'OPI de la méthode de l'essai sur œil de lapin in vivo n'a pas été validé, mais l’utilisation de l’OPI est recommandée dans le cadre d'une stratégie d'essai séquentielle visant à établir une classification et un étiquetage réglementaires dans un domaine d'application défini (4) (5). Les substances et mélanges d’essai (6) qui répondent positivement dans cet essai peuvent être classés dans la catégorie des produits corrosifs et fortement irritants pour l'œil sans qu'il soit nécessaire de procéder à des essais supplémentaires chez le lapin. En revanche, une substance révélant un résultat négatif à l’issue de l’essai a besoin d’être testée sur des lapins selon une démarche expérimentale de type séquentiel, telle que celle décrite dans la ligne directrice de l’OCDE no 405 (7) (chapitre B.5 de la présente annexe). |
|
2. |
L'objectif de la présente méthode d'essai est de décrire les modes opératoires utilisés pour évaluer l'effet potentiel corrosif ou fortement irritant pour l'œil d'une substance d'essai. Cet effet est mesuré par la capacité du produit à induire une toxicité dans un œil de poulet énucléé. Les effets toxiques pour la cornée sont mesurés par i) une estimation qualitative de l'opacité, ii) une estimation qualitative des dommages subis par l'épithélium, fondée sur l'application de fluorescéine sur l'œil (rétention de fluorescéine), iii) une mesure quantitative de l'augmentation d'épaisseur (gonflement), et iv) une évaluation qualitative des dommages morphologiques macroscopiques infligés en surface. L'opacité cornéenne, le gonflement et l'estimation des dommages après exposition à une substance d'essai sont évalués individuellement, puis combinés pour établir une classification d'effet irritant pour l'œil. |
|
3. |
La méthode OPI a également été utilisée pour tester des substances irritantes pour l'œil qui induisent des lésions guéries en moins de 21 jours, ainsi que des substances non irritantes. Toutefois, la précision et la fiabilité de cette méthode n'ont pas été évaluées de façon formelle pour les substances entrant dans ces catégories. |
|
4. |
Des définitions sont fournies dans l'appendice 1. |
REMARQUES PRÉLIMINAIRES ET LIMITES DE LA MÉTHODE
|
5. |
La présente méthode d'essai est fondée sur le protocole expérimental de la méthode OPI du Comité de coordination inter-agences sur la validation des méthodes alternatives (ICCVAM) (8), élaboré à la suite d'une étude de validation internationale (4) (5) (9) à laquelle ont participé le Centre européen pour la validation de méthodes alternatives (ECVAM), le Centre japonais pour la validation de méthodes alternatives, et le département de toxicologie et pharmacologie appliquée de TNO Quality of Life (Pays-Bas). Le protocole s'appuie sur des informations dérivées de protocoles publiés et de celui qui est actuellement employé par TNO (10) (11) (12) (13) (14). |
|
6. |
Les limites connues de cette méthode d'essai concernent le taux de faux positifs obtenu pour les alcools, et les taux de faux négatifs obtenus pour les matières solides et les tensioactifs (voir paragraphe 47) (4). Si l’on exclut de la base de données les substances relevant de ces classes chimiques et physiques, la précision de la méthode OPI au regard des systèmes de classifications de l’UE, de l’EPA et du SGH se trouve considérablement améliorée (4). Compte tenu de la finalité de cet essai (qui vise exclusivement à détecter les substances corrosives et fortement irritantes pour l’œil), les taux de faux négatifs ne sont pas préoccupants car les substances concernées feront ensuite l’objet d’essais chez le lapin ou d’autres essais in vitro dûment validés, conformément aux exigences de la réglementation, selon une démarche expérimentale séquentielle fondée sur la force probante des données. De surcroît, l’actuelle base de données de validation n’a pas permis de procéder à l’évaluation adéquate de certaines classes de substances chimiques ou de produits (par exemple, les mélanges). Les chercheurs peuvent cependant envisager l'utilisation de cette méthode d'essai pour tous les types de matériel d’essai (y compris les mélanges), auquel cas un résultat positif pourrait être interprété comme révélateur d'un effet corrosif ou fortement irritant pour l'œil. Toutefois, il convient d'interpréter avec précaution les résultats positifs obtenus avec des alcools, compte tenu du risque de surévaluation. |
|
7. |
Tous les modes opératoires sur l'œil de poulet doivent respecter les réglementations applicables aux installations d'essai et les protocoles de manipulation de matériaux issus de l'homme et de l'animal, comprenant notamment, sans s'y limiter, les tissus et les fluides tissulaires. Le respect des précautions universelles de laboratoire est recommandé (15). |
|
8. |
Bien qu’elle prenne en compte certains des effets oculaires évalués par la méthode d’essai d’irritation oculaire chez le lapin, et dans une certaine mesure leur degré de gravité, cette méthode d’essai présente toutefois l’inconvénient de ne pas prendre en considération les lésions de la conjonctive et de l’iris. De plus, même si la méthode OPI ne permet pas en soi d'évaluer la réversibilité des lésions cornéennes, il a été proposé, sur la base d’études menées sur l’œil de lapin, d'utiliser une évaluation de la profondeur initiale de la lésion cornéenne pour distinguer les effets réversibles des effets irréversibles (16). Enfin, la méthode d’essai OPI ne permet pas d'évaluer la toxicité systémique potentielle associée à l'exposition oculaire. |
|
9. |
Les travaux visant à mieux caractériser l'utilité et les limites de la méthode d'essai OPI pour la mise en évidence des substances faiblement irritantes ou non irritantes se poursuivent (voir également paragraphe 48). Les utilisateurs sont également incités à fournir des spécimens et/ou des données aux organismes de validation à des fins d'évaluation formelle des utilisations futures possibles de la méthode d'essai OPI, notamment pour la mise en évidence des substances faiblement irritantes ou non irritantes. |
|
10. |
Tout laboratoire conduisant cet essai pour la première fois doit utiliser les substances chimiques d'épreuve de compétence mentionnées à l'appendice 2. Il peut utiliser ces substances pour démontrer sa compétence technique en matière d'application de la méthode d'essai OPI préalablement à la soumission des données obtenues avec cet essai à des fins de classification réglementaire des dangers. |
PRINCIPE DE L'ESSAI
|
11. |
La méthode d'essai OPI est un modèle organotypique qui permet de maintenir à court terme des yeux de poulet in vitro. Dans cette méthode, les dommages provoqués par la substance d'essai sont évalués par détermination du gonflement cornéen, de l'opacité de la cornée et de sa rétention de fluorescéine. L'observation des deux derniers paramètres est qualitative, alors que l'analyse du gonflement cornéen est quantitative. Chaque mesure est convertie en un score quantitatif qui est utilisé pour calculer un indice d'irritation général, ou fait l'objet d'une catégorisation qualitative qui sert à assigner une classification de substance corrosive et fortement irritante pour l'œil in vitro. L'un ou l'autre de ces résultats peut ensuite être utilisé pour prédire le potentiel d'effet corrosif et fortement irritant pour l'œil d'une substance d'essai in vivo (voir “Critères de décision”). |
Provenance et âge des yeux de poulet
|
12. |
Habituellement, on utilise pour cet essai des yeux prélevés sur des poulets d'abattoir destinés à la consommation humaine, et les animaux de laboratoire sont de ce fait inutiles. Seuls sont utilisés les yeux d'animaux sains, considérés comme propres à intégrer la chaîne alimentaire humaine. |
|
13. |
Aucune étude contrôlée visant à évaluer l'âge optimal des poulets n'a encore été menée, mais l'âge et le poids des poulets habituellement utilisés dans cette méthode d'essai sont ceux des petits poulets couramment traités dans un abattoir de volailles (à savoir, environ 7 semaines et 1,5 – 2,5 kg). |
Collecte et transport des yeux au laboratoire
|
14. |
Les têtes sont coupées immédiatement après sédation des poulets, généralement par choc électrique, et incision des cous pour la saignée. Il conviendra de repérer une source locale de poulets proche du laboratoire, afin que le transfert des têtes entre l'abattoir et le laboratoire soit suffisamment rapide pour limiter autant que possible la détérioration et/ou la contamination bactérienne. Il faut réduire au minimum l'intervalle de temps qui sépare la collecte des têtes de poulets et l'utilisation des yeux dans la méthode d'essai OPI (généralement deux heures) et démontrer qu'il ne compromet pas les résultats de l'essai. Ces résultats dépendent des critères de sélection des yeux, ainsi que des réponses des témoins positifs et négatifs. Tous les yeux utilisés dans l'essai proviennent d'un lot d'yeux collectés le même jour. |
|
15. |
Les yeux étant disséqués au laboratoire, les têtes sont transportées intactes depuis l'abattoir, à température ambiante, dans des boîtes en plastique humidifiées à l'aide de serviettes mouillées d'une solution saline isotonique. |
Critères de sélection des yeux utilisés dans la méthode OPI
|
16. |
Les yeux dont la coloration initiale par la fluorescéine ou le score d'opacité cornéenne sont élevés après énucléation (> 0,5 dans les deux cas) sont rejetés. |
|
17. |
Chaque lot de traitement et chaque lot témoin positif parallèle comprend au moins trois yeux. Le lot témoin négatif ou le témoin de solvant (si on utilise un solvant qui n'est pas une solution saline) comprend au moins un œil. |
MODE OPÉRATOIRE
Préparation des yeux
|
18. |
Les paupières sont soigneusement excisées en veillant à ne pas endommager la cornée. Pour évaluer rapidement l'intégrité de celle-ci, on applique une goutte de fluorescéine sodique à 2 % (p/v) sur la surface cornéenne pendant quelques secondes, puis on rince avec une solution saline isotonique. Les yeux traités à la fluorescéine sont ensuite examinés au biomicroscope pour vérifier que la cornée n'est pas endommagée (les scores de rétention de fluorescéine et d'opacité cornéenne doivent être ≤ 0,5). |
|
19. |
S'il n'est pas endommagé, l'œil est ensuite énucléé, en veillant à ne pas léser la cornée. Le globe oculaire est tiré hors de l'orbite en maintenant fermement la membrane nictitante à l'aide de pinces chirurgicales, et les muscles de l'œil sont coupés avec des ciseaux courbes à pointes émoussées. Il est important d'éviter d'endommager la cornée par une pression excessive (artéfacts de compression). |
|
20. |
Lorsque l'œil est retiré de l'orbite, une portion visible du nerf optique doit rester attachée. Une fois retiré de l'orbite, l'œil est placé sur un tampon absorbant et la membrane nictitante et le reste des tissus conjonctifs sont disséqués. |
|
21. |
L'œil énucléé est monté dans un clamp en acier inoxydable, en plaçant la cornée verticalement. Le clamp est ensuite transféré dans une chambre de l'appareil de surfusion (16). Dans l'appareil de surfusion, les clamps sont placés de telle sorte que la totalité de la cornée soit alimentée par le goutte-à-goutte de solution saline isotonique. La température dans les chambres de l'appareil de surfusion est régulée à 32 ± 1,5 °C. L'appendice 3 propose un schéma d'un appareil de surfusion classique et des clamps pour œil, disponibles dans le commerce ou à construire. L'appareil peut être modifié en fonction des besoins du laboratoire (par exemple, pour contenir un nombre d'yeux différent). |
|
22. |
Une fois placés dans l'appareil de surfusion, les yeux sont à nouveau examinés au biomicroscope afin de s'assurer qu'ils n'ont pas été endommagés lors de la dissection. Il est utile à ce stade de mesurer l'épaisseur de la cornée à son apex, au moyen du dispositif de mesure dont est muni le biomicroscope. Les yeux i) dont la rétention de fluorescéine est > 0,5, ii) dont l'opacité cornéenne est > 0,5 ou iii) qui présentent tout autre signe de lésion doivent être remplacés. Les yeux qui ne sont pas rejetés sur la base de ces critères, mais dont l'épaisseur cornéenne s'écarte de plus de 10 % de la valeur moyenne calculée pour l'ensemble des yeux doivent également être rejetés. La mesure de l'épaisseur cornéenne peut varier en fonction du réglage de la largeur de la fente du biomicroscope, et les examinateurs tiennent compte de cette contrainte en ajustant cette largeur à 0,095 mm. |
|
23. |
Une fois tous les yeux examinés et admis dans l'étude, ils sont incubés pendant environ 45 à 60 minutes pour leur permettre de s'équilibrer dans le système d'essai avant administration de la substance d'essai. Cette période est suivie des mesures de l'épaisseur et de l'opacité cornéennes au temps zéro (t = 0), qui serviront de mesures de référence. Le score de rétention de la fluorescéine déterminé lors de la dissection sert de mesure de référence pour ce critère d'évaluation. |
Application de la substance d'essai
|
24. |
Immédiatement après les mesures de référence au temps zéro, l'œil (dans son support) est retiré de l'appareil de surfusion, placé en position horizontale et la substance d'essai est appliquée sur la cornée. |
|
25. |
Les substances d'essai liquides sont généralement testées sans dilution, mais elles peuvent au besoin être diluées (par exemple, lors d'une étape prévue dans la conception de l'étude). Il est préférable d'utiliser une solution physiologique pour diluer les substances. Il est toutefois possible d'utiliser d'autres solvants en conditions contrôlées, sous réserve de démontrer le bien-fondé de leur utilisation au lieu de la solution physiologique saline. |
|
26. |
Les substances d'essai liquides sont appliquées sur la cornée de façon à couvrir uniformément la totalité de la surface; le volume habituel est de 0,03 ml. |
|
27. |
De préférence, les substances solides sont broyées aussi finement que possible au moyen d'un mortier et d'un pilon, ou d'un outil de broyage comparable. La poudre est appliquée sur la cornée de façon à couvrir uniformément la totalité de la surface; la quantité habituelle est de 0,03 g. |
|
28. |
La substance d'essai (liquide ou solide) est appliquée pendant 10 secondes, puis éliminée par rinçage de l'œil avec une solution saline isotonique (environ 20 ml) à température ambiante. L'œil (dans son support) est ensuite remis dans l'appareil de surfusion dans la position verticale initiale. |
Substances témoins
|
29. |
Il convient d'inclure des témoins négatifs ou de solvant/véhicule et des témoins positifs en parallèle dans chaque expérience. |
|
30. |
Dans le cas d'essais de liquides purs ou de solides, on utilise une solution saline physiologique comme témoin négatif parallèle dans la méthode d'essai OPI pour détecter des changements non spécifiques dans le système d'essai, et pour vérifier que les conditions de l'essai ne provoquent pas de réponse irritante indésirable. |
|
31. |
Dans le cas d'essais de liquides dilués, un lot témoin parallèle de solvant/véhicule est inclus dans la méthode d'essai pour détecter des changements non spécifiques dans le système d'essai, et pour vérifier que les conditions de l'essai ne provoquent pas de réponse irritante inappropriée. Comme le mentionne le paragraphe 25, il ne faut utiliser que des solvants ou des véhicules dont l'absence d'effet néfaste sur le système d'essai a été démontrée. |
|
32. |
Chaque expérience comprend une substance irritante pour les yeux connue en tant que témoin positif permettant de vérifier l'induction d'une réponse appropriée. La méthode d’essai OPI étant utilisée ici pour mettre en évidence des substances corrosives ou fortement irritantes, il convient que le témoin positif soit une substance de référence qui induit une réponse forte dans le cadre de cette méthode. Toutefois, pour pouvoir évaluer la variabilité de la réponse du témoin positif dans le temps, il ne faut pas que l'ampleur de cette réponse soit excessive. La quantité de données in vitro obtenues pour le témoin positif doit être suffisante pour permettre le calcul d'un intervalle acceptable défini statistiquement. En l'absence de données antérieures adéquates issues de la méthode d'essai OPI pour un témoin positif donné, il peut être nécessaire de mener des études pour obtenir ces informations. |
|
33. |
L'acide acétique à 10 % ou le chlorure de benzalconium à 5 % sont des exemples de témoins positifs dans les essais de substances d'essai liquides, et l'hydroxyde de sodium ou l'imidazole peuvent jouer ce rôle pour les substances d'essai solides. |
|
34. |
Les substances étalons sont utiles pour évaluer le potentiel d'irritation oculaire de produits chimiques inconnus d'une classe chimique ou d'une catégorie de produits spécifique, ou pour évaluer le potentiel d'irritation relatif d'une substance irritante pour les yeux au sein d'une plage spécifique de réponses. |
Effets mesurés
|
35. |
Les cornées traitées sont évaluées avant le traitement et 30, 75, 120, 180, et 240 minutes (± 5 minutes) après le rinçage suivant le traitement. Ces temps d'observation sont en nombre suffisant sur la période de traitement de 4 heures et les intervalles entre les mesures permettent d'effectuer les observations requises sur tous les yeux. |
|
36. |
Les effets évalués sont l'opacité cornéenne, le gonflement de la cornée et la rétention de fluorescéine, ainsi que les effets morphologiques (par exemple, piqûres ou relâchement de l'épithélium). Tous les effets, à l'exception de la rétention de fluorescéine (qui n'est mesurée que lors du prétraitement et 30 minutes après l'exposition à la substance d'essai), sont mesurés à chacun des temps d'observation indiqués ci-dessus. |
|
37. |
Il est conseillé de prendre des photographies pour attester l'opacité cornéenne, la rétention de fluorescéine, les effets morphologiques, et, le cas échéant, les observations histopathologiques. |
|
38. |
Après l'examen final à quatre heures, il est recommandé de conserver les yeux dans un fixateur approprié (par exemple, formol tamponné à pH neutre) en vue d'un éventuel examen histopathologique. |
|
39. |
Le gonflement cornéen est déterminé par des mesures d'épaisseur de la cornée réalisées au moyen d'un pachymètre optique monté sur un biomicroscope. Il est exprimé en pourcentage et calculé à partir des mesures d'épaisseur de la cornée, selon la formule suivante:
|
|
40. |
Le pourcentage moyen de gonflement cornéen pour tous les yeux est calculé à chaque temps d'observation. À partir du score moyen de gonflement cornéen le plus élevé obtenu sur l'ensemble des temps d'observation, un score général de catégorie est attribué à chaque substance d'essai. |
|
41. |
Le score d'opacité cornéenne est calculé sur la surface de cornée qui est la plus fortement opacifiée. La valeur moyenne d'opacité cornéenne pour tous les yeux est calculée à chaque temps d'observation. À partir du score moyen d'opacité cornéenne le plus élevé obtenu sur l'ensemble des temps d'observation, un score général de catégorie est attribué à chaque substance d'essai (Tableau 1). Tableau 1 Scores d'opacité cornéenne
|
|
42. |
Pour tous les yeux examinés, la valeur moyenne de rétention de la fluorescéine n'est calculée qu'au temps d'observation de 30 minutes, qui est utilisé pour déterminer le score général de catégorie attribué à chaque substance d'essai (Tableau 2). Tableau 2 Scores de rétention de fluorescéine
|
|
43. |
Les effets morphologiques comprennent le phénomène de “piqûre” des cellules épithéliales cornéennes, le “relâchement” de l'épithélium, la “rugosité” de la surface cornéenne et “l'adhérence” de la substance d'essai sur la cornée. La gravité de ces effets est variable et ils peuvent être observés simultanément. Leur classification est subjective et dépend de l'interprétation de l'observateur. |
RÉSULTATS ET RAPPORT
Évaluation des données
|
44. |
Les résultats d'opacité cornéenne, de gonflement de la cornée et de rétention de fluorescéine sont évalués séparément et aboutissent à la détermination d'une catégorie OPI par effet mesuré. Ces catégories sont ensuite combinées en une classification de l'effet irritant pour chaque substance d'essai. |
Critères de décision
|
45. |
Après évaluation de chacun des effets, des catégories OPI peuvent être assignées à la substance selon un barème prédéterminé. L'interprétation de l'épaisseur cornéenne (Tableau 3), de l'opacité de la cornée (Tableau 4) et de la rétention de fluorescéine (Tableau 5) au moyen de 4 catégories OPI, suit la progression suivante: Tableau 3 Critères de classification OPI pour l'épaisseur cornéenne
Tableau 4 Critères de classification OPI pour l'opacité.
Tableau 5 Critères de classification OPI pour la rétention moyenne de fluorescéine
|
|
46. |
La classification générale des effets irritants in vitro d'une substance d'essai est déterminée par la catégorie d'effet irritant qui correspond à la combinaison des catégories obtenues pour le gonflement cornéen, l'opacité cornéenne et la rétention de fluorescéine, et par application du schéma présenté dans le tableau 6. Tableau 6 Classification générale des effets irritants in vitro
|
|
47. |
Comme indiqué au paragraphe 1, s'il n'est pas démontré que la substance d'essai est corrosive ou fortement irritante pour l'œil, il convient de mener des essais complémentaires à des fins de classification et d'étiquetage. Pour la mise en évidence des substances corrosives ou fortement irritantes pour l'œil, la méthode d'essai OPI présente une précision globale comprise entre 83 % (120/144) et 87 % (134/154), un taux de faux positifs allant de 6 % (7/122) à 8 % (9/116), et un taux de faux négatifs allant de 41 % (13/32) à 50 % (15/30), en comparaison avec les résultats de la méthode d'essai sur œil de lapin in vivo, classés selon les systèmes de classification de l'EPA (1), de l'UE (2), ou du SGH (3). Lorsqu'on exclut de la base de données les substances de certaines catégories chimiques (à savoir, les alcools et les tensioactifs) et physiques (à savoir, les solides), la précision de l'OPI dans les systèmes de classification de l'EPA, de l'UE ou du SGH se situe entre 91 % (75/82) et 92 % (69/75), les taux de faux positifs entre 5 % (4/73) et 6 % (4/70), et les taux de faux négatifs entre 29 % (2/7) et 33 % (3/9) (4). |
|
48. |
Même si une substance d’essai n’est pas classée comme corrosive ou fortement irritante pour l'œil, les données de la méthode d'essai OPI peuvent servir, en association avec des résultats d’essais in vivo sur œil de lapin ou d’un autre test in vitro dûment validé, à évaluer plus en profondeur l’utilité et les limites de la méthode OPI pour la détection des substances faiblement irritantes ou non irritantes (un document d'orientation sur l’utilisation de méthodes d’essai de toxicité oculaire in vitro est en cours d'élaboration). |
Critères d'acceptation de l'étude
|
49. |
Un essai est considéré comme acceptable lorsque la classification de l'irritation obtenue pour les témoins négatifs et de véhicule/solvant parallèles, d'une part, et pour les témoins positifs parallèles, d'autre part, situe les substances correspondantes respectivement dans les catégories “substances non irritantes” et “substances fortement irritantes/corrosives”. |
Rapport d'essai
|
50. |
Le rapport d’essai contient les renseignements suivants, dès lors qu'ils s'appliquent à l'étude: Substances d’essai et témoins
Renseignements relatifs au commanditaire et à l’installation d’essai:
Justification du choix de la méthode d'essai et du mode opératoire Intégrité de la méthode d'essai Mode opératoire utilisé pour assurer l'intégrité (précision et fiabilité) de la méthode d'essai au cours du temps (par exemple essai périodique des substances d’épreuve de compétence, utilisation de données antérieures de témoins positifs et négatifs). Critères d'acceptabilité de l’essai Le cas échéant, gamme de témoins de référence parallèles acceptables selon des données antérieures; Conditions de l'essai
Résultats
Discussion des résultats Conclusion |
BIBLIOGRAPHIE
|
(1) |
U.S. EPA (1996). Label Review Manual: 2nd Edition. EPA737-B-96-001. Washington, DC: U.S. Environmental Protection Agency. |
|
(2) |
Règlement (CE) no 1272/2008 du Parlement européen et du Conseil du 16 décembre 2008 relatif à la classification, à l'étiquetage et à l'emballage des substances et des mélanges, modifiant et abrogeant les directives 67/548/CEE et 1999/45/CE et modifiant le règlement (CE) no 1907/2006. JO L 353 du 31.12.2008, p. 1. |
|
(3) |
Nations unies (NU) (2007). Système général harmonisé de classification et d'étiquetage des produits chimiques (SGH), deuxième édition révisée, Nations unies, New York et Genève, 2007. Disponible à l'adresse suivante: [http://www.unece.org/trans/danger/publi/ghs/ghs_rev02/02files_e.html] |
|
(4) |
ICCVAM (2007). Test Method Evaluation Report - In Vitro Ocular Toxicity Test Methods for Identifying Ocular Severe Irritants and Corrosives. Interagency Coordinating Committee on the Validation of Alternative Methods (ICCVAM) and the National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). NIH Publication No.: 07-4517. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm] |
|
(5) |
ESAC (2007). Statement on the conclusion of the ICCVAM retrospective study on organotypic in vitro assays as screening tests to identify potential ocular corrosives and severe eye irritants. Disponible à l'adresse suivante: [http://ecvam.jrc.it/index.htm]. |
|
(6) |
Règlement (CE) no 1907/2006 du Parlement européen et du Conseil du 18 décembre 2006 concernant l'enregistrement, l'évaluation et l'autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH), instituant une agence européenne des produits chimiques, modifiant la directive 1999/45/CE et abrogeant le règlement (CEE) no 793/93 du Conseil et le règlement (CE) no 1488/94 de la Commission ainsi que la directive 76/769/CEE du Conseil et les directives 91/155/CEE, 93/67/CEE, 93/105/CE et 2000/21/CE de la Commission. JO L 396 du 30.12.2006, p. 1. |
|
(7) |
OCDE (2002). Ligne directrice 405. Ligne directrice de l'OCDE pour les essais de produits chimiques. Effet irritant/corrosif aigu sur les yeux. Disponible à l'adresse suivante: [http://www.oecd.org/document/40/0, 2340, en_2649_34377_37051368_1_1_1_1,00.html] |
|
(8) |
ICCVAM (2007). ICCVAM Recommended ICE Test Method Protocol. In: ICCVAM Test Method Evaluation Report - In Vitro Ocular Toxicity Test Methods for Identifying Ocular Severe Irritants and Corrosives. Interagency Coordinating Committee on the Validation of Alternative Methods (ICCVAM) and the National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). NIH Publication No.: 07-4517. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm] |
|
(9) |
ICCVAM. (2006). Current Status of In Vitro Test Methods for Identifying Ocular Corrosives and Severe Irritants: Isolated Chicken Eye Test Method. NIH Publication No.: 06-4513. Research Triangle Park: National Toxicology Program. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_ice.htm] |
|
(10) |
Prinsen, M.K. and Koëter, B.W.M. (1993). Justification of the enucleated eye test with eyes of slaughterhouse animals as an alternative to the Draize eye irritation test with rabbits. Fd. Chem. Toxicol. 31:69-76. |
|
(11) |
INVITTOX (1994). Protocol 80: Chicken enucleated eye test (CEET). Disponible à l'adresse suivante: [http://ecvam.jrc.it/index.htm]. |
|
(12) |
Balls, M., Botham, P.A., Bruner, L.H. and Spielmann H. (1995). The EC/HO international validation study on alternatives to the Draize eye irritation test. Toxicol. In Vitro 9:871-929. |
|
(13) |
Prinsen, M.K. (1996). The chicken enucleated eye test (CEET): A practical (pre)screen for the assessment of eye irritation/corrosion potential of test materials. Food Chem. Toxicol. 34:291-296. |
|
(14) |
Chamberlain, M., Gad, S.C., Gautheron, P. and Prinsen, M.K. (1997). IRAG Working Group I: Organotypic models for the assessment/prediction of ocular irritation. Food Chem. Toxicol. 35:23-37. |
|
(15) |
Siegel, J.D., Rhinehart, E., Jackson, M., Chiarello, L., and the Healthcare Infection Control Practices Advisory Committee (2007). Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in Healthcare Settings. Disponible à l'adresse suivante: [http://www.cdc.gov/ncidod/dhqp/pdf/isolation2007.pdf]. |
|
(16) |
Maurer, J.K., Parker, R.D. and Jester J.V. (2002). Extent of corneal injury as the mechanistic basis for ocular irritation: key findings and recommendations for the development of alternative assays. Reg. Tox. Pharmacol. 36:106-117. |
|
(17) |
Burton, A.B.G., M. York and R.S. Lawrence (1981). The in vitro assessment of severe irritants. Fd. Cosmet.- Toxicol.- 19, 471-480. |
|
(18) |
ICCVAM (2006). Background review document, Current Status of In Vitro Test Methods for Identifying Ocular Corrosives and Severe Irritants: Bovine Corneal Opacity and Permeability (BCOP) Test Method. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm] |
|
(19) |
ICCVAM (2006). Background review document, Current Status of In Vitro Test Methods for Identifying Ocular Corrosives and Severe IrritantsIsolated Chicken Eye (ICE) Test Method. Disponible à l'adresse suivante: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm] |
Appendice 1
DÉFINITIONS
Précision: degré de concordance entre les résultats de la méthode d'essai et les valeurs de référence acceptées. La précision constitue une mesure de la performance de la méthode d'essai et un aspect de sa «pertinence». Ce terme est souvent utilisé de façon interchangeable avec «concordance» pour désigner la proportion de résultats corrects d'une méthode d'essai.
Substance étalon: substance utilisée en tant que référence, pour la comparaison avec une substance d'essai. Une substance étalon présente les propriétés suivantes: i) provient d'une ou de plusieurs sources constantes et fiables; ii) présente une similitude structurale et fonctionnelle avec la classe des substances soumises à l'essai; iii) possède des caractéristiques physiques/chimiques connues; iv) est accompagnée de données confirmant ses effets connus, et v) a une puissance connue dans la fourchette de réponses désirées.
Cornée: partie transparente située à l’avant du globe oculaire, recouvrant l’iris et la pupille et laissant pénétrer la lumière vers l’intérieur de l’œil.
Opacité cornéenne: mesure de l’étendue du caractère opaque de la cornée suite à son exposition à une substance d’essai. Une augmentation de l'opacité cornéenne indique un endommagement de la cornée.
Gonflement cornéen: mesure objective dans l'essai OPI de l'ampleur de la distension de la cornée après exposition à une substance d'essai. Elle est exprimée en pourcentage et est calculée au moyen des mesures initiales (avant administration de la dose) d'épaisseur cornéenne, et des mesures d'épaisseur relevées à intervalles réguliers après exposition à la substance d'essai dans l'essai OPI. Le degré de gonflement cornéen est un indicateur d'endommagement de la cornée.
Catégorie 1 de l'EPA: effet corrosif (destruction irréversible du tissu oculaire) ou complication cornéenne ou irritation persistant plus de 21 jours (1).
Catégorie R41 de l'UE: lésion des tissus oculaires ou dégradation sévère de la vue, provoquée par l'application d'une substance d'essai sur la face antérieure de l'œil, et qui n'est pas totalement réversible dans les 21 jours suivant l'application (2).
Taux de faux négatifs: proportion de substances positives faussement déclarées négatives par une méthode d'essai. C'est un indicateur de la performance de la méthode d'essai.
Taux de faux positifs: proportion des substances négatives faussement déclarées positives par une méthode d'essai. C'est un indicateur de la performance de la méthode d'essai.
Rétention de fluorescéine: mesure subjective, dans l'essai OPI, de la quantité de fluorescéine sodique qui est retenue par les cellules épithéliales de la cornée après exposition à une substance d'essai. Le degré de rétention de fluorescéine est un indicateur d'endommagement de la cornée.
SGH (Système général harmonisé de classification et d'étiquetage des produits chimiques): système proposant la classification des produits chimiques (substances et mélanges) conformément à des types et des niveaux normalisés de dangers physiques, sanitaires et environnementaux, ainsi que la communication des éléments d'information correspondants, notamment par des pictogrammes, mentions d’avertissement, mentions de danger, conseils de prudence et fiches de données de sécurité, afin de diffuser des informations sur leurs effets indésirables dans l'objectif de protéger les personnes (en particulier les employeurs, employés, transporteurs, consommateurs et personnels des services d'urgence) et l'environnement (3).
Catégorie 1 du SGH: lésion des tissus oculaires ou dégradation sévère de la vue, provoquée par l'application d'une substance d'essai sur la face antérieure de l'œil, et qui n'est pas totalement réversible dans les 21 jours suivant l'application (3).
Danger: propriété intrinsèque d'un agent ou situation susceptible de provoquer des effets néfastes lorsqu'un organisme, un système ou une (sous-)population est exposé(e) à cet agent.
Témoin négatif: réplicat non traité contenant tous les composants d’un système d’essai. Cet échantillon subit les mêmes procédures que les échantillons traités avec la substance d'essai et les autres échantillons témoins afin de déterminer si le solvant interagit avec le système d’essai.
Substance non irritante: substance qui n'est pas classée comme irritant oculaire dans la catégorie I, II ou III de l'EPA, la catégorie R41 ou R36 de l'UE, ou la catégorie 1, 2A ou 2B du SGH (1) (2) (3).
Substance corrosive pour l'œil: a) substance provoquant des lésions irréversibles des tissus oculaires; b) substance classée comme irritant oculaire dans la catégorie 1 du SGH, la catégorie 1 de l’EPA ou la catégorie R41 de l’UE (1) (2) (3).
Substance irritante pour l'œil: a) substance provoquant une modification réversible de l’œil suite à une application sur la face antérieure de l’œil; b) substance classée comme irritant oculaire dans la catégorie II ou III de l'EPA, la catégorie R36 de l'UE ou la catégorie 2A ou 2B du SGH (1) (2) (3).
Substance fortement irritante pour l'œil: a) substance provoquant des lésions des tissus oculaires suite à une application sur la face antérieure de l’œil, qui ne sont pas réversibles dans les 21 jours suivant l'application ou entraînent une dégradation sévère de la vue; b) substance classée comme irritant oculaire dans la catégorie 1 du SGH, la catégorie 1 de l’EPA ou la catégorie R41 de l’UE (1) (2) (3).
Témoin positif: réplicat contenant tous les composants d’un système d’essai, et traité avec une substance induisant notoirement une réponse positive. Afin de pouvoir évaluer la variabilité des réponses du témoin positif dans le temps, la sévérité de la réponse ne devra pas être excessive.
Fiabilité: mesure de la reproductibilité de l'essai mis en œuvre, au sein d'un laboratoire et entre des laboratoires, au cours du temps, en utilisant le même mode opératoire. Elle est évaluée par calcul de la reproductibilité intralaboratoire et interlaboratoires et de la répétabilité intralaboratoire.
Biomicroscope (lampe à fente): instrument utilisé pour examiner directement l'œil sous le grossissement d'un microscope binoculaire en créant une image stéréoscopique droite. Dans la méthode d’essai OPI, cet instrument est utilisé pour visualiser les structures antérieures de l’œil de poulet et également pour mesurer objectivement l’épaisseur de la cornée au moyen d’un dispositif adjoint de mesure de la profondeur.
Témoin de solvant/véhicule: échantillon non traité contenant tous les composants d’un système d’essai, y compris le solvant ou véhicule utilisé pour tester les échantillons témoins traités ou non avec la substance d’essai afin de déterminer une réponse de référence pour les échantillons traités avec la substance d’essai dissoute dans le même solvant ou véhicule. Testé avec un témoin négatif concurrent, cet échantillon indique également si le solvant ou véhicule interagit avec le système d'essai.
Stratégie d'essai séquentielle: démarche expérimentale séquentielle consistant à examiner toutes les informations existantes sur une substance d'essai dans un ordre déterminé, en ayant recours à chaque étape à une procédure fondée sur la force probante des données pour déterminer si les informations disponibles sont suffisantes pour décider d'une classification des dangers, avant de passer à l'étape suivante. Si le potentiel d’irritation d’une substance d’essai peut être déterminé sur la base des informations existantes, aucun essai supplémentaire n’est nécessaire. Dans le cas contraire, une procédure expérimentale progressive de type séquentiel sur des animaux est alors lancée jusqu’à ce qu’une classification sans équivoque puisse être effectuée.
Méthode d'essai validée: méthode d'essai ayant fait l'objet d'études de validation visant à déterminer sa pertinence (notamment sa précision) et sa fiabilité à des fins spécifiques. Il importe de noter que les performances d'une méthode d'essai validée peuvent être insuffisantes en termes de précision et de fiabilité pour qu'elle soit jugée acceptable pour les besoins envisagés.
Force probante des données: prise en compte des forces et des faiblesses de divers éléments d’information en vue d'aboutir à une conclusion concernant le danger potentiel d’une substance et d’étayer cette conclusion.
Appendice 2
SUBSTANCES D’ÉPREUVE DE COMPÉTENCE POUR LA MÉTHODE D'ESSAI OPI
Avant d'utiliser en routine une méthode conforme à cette méthode d'essai, certains laboratoires peuvent estimer souhaitable de démontrer leurs compétences techniques en identifiant correctement la catégorie de corrosivité oculaire des 10 substances recommandées dans le tableau 1. Ces substances ont été sélectionnées de façon à représenter la gamme des réactions locales d'irritation/corrosion oculaire, sur la base des résultats de l'essai sur œil de lapin in vivo (TG 405) (à savoir, les catégories 1, 2A, 2B, ou non classées ou non étiquetées selon le SGH des Nations unies) (3) (7). Toutefois, compte tenu de l’utilité validée de ces essais (uniquement mise en évidence des substances corrosives/fortement irritantes pour l'œil), seuls deux résultats expérimentaux obtenus à des fins de classification (substance corrosive/fortement irritante ou substance non corrosive/faiblement irritante) permettent de démontrer les compétences des laboratoires. Les autres critères de sélection retenus ont trait à la disponibilité des substances dans le commerce, à la disponibilité de données de référence in vivo de bonne qualité, et à l’existence de données de bonne qualité issues des deux méthodes d’essai in vitro qui font l’objet de lignes directrices. Pour cette raison, les substances irritantes ont été sélectionnées dans la liste recommandée par l'ICCVAM de 122 substances de référence pour la validation de méthodes d'essai de toxicité oculaire in vitro (voir appendice H, ICCVAM Recommended Reference Substances List)(4). Les données de référence sont disponibles dans les documents de l'ICCVAM (Background Review Documents) pour la méthode d’essai d’opacité et de perméabilité de la cornée bovine (OPCB) et la méthode OPI (18) (19).
Tableau 1
Substances recommandées pour la démonstration des compétences techniques relatives à la méthode OPI
|
Substance chimique |
No CAS |
Classe chimique (9) |
Forme physique |
Classification in vivo (10) |
Classification in vitro (11) |
|
Chlorure de benzalconium (5 %) |
8001-54-5 |
Composé d'onium |
Liquide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Chlorhexidine |
55-56-1 |
Amine, Amidine |
Solide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Acide dibenzoyl-L-tartrique |
2743-38-6 |
Acide carboxylique, ester |
Solide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Imidazole |
288-32-4 |
Hétérocycle |
Solide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Acide trichloroacétique (30 %) |
76-03-9 |
Acide carboxylique |
Liquide |
Catégorie 1 |
Corrosif/fortement irritant |
|
Chlorure de 2,6-dichlorobenzoyle |
4659-45-4 |
Halogénure d'acyle |
Liquide |
Catégorie 2A |
Non corrosif/Faiblement irritant |
|
2-méthylacéto-acétate d'éthyle |
609-14-3 |
Cétone, Ester |
Liquide |
Catégorie 2B |
Non corrosif/Faiblement irritant |
|
Nitrate d'ammonium |
6484-52-2 |
Sel inorganique |
Solide |
Catégorie 2A |
Non corrosif/Faiblement irritant |
|
Glycérol |
56-81-5 |
Alcool |
Liquide |
Non étiqueté |
Non corrosif/Faiblement irritant |
|
n-Hexane |
110-54-3 |
Hydrocarbure (acyclique) |
Liquide |
Non étiqueté |
Non corrosif/Faiblement irritant |
|
Abréviations: No CAS = Numéro d'enregistrement au Chemical Abstract Service |
|||||
Appendice 3
Schémas de l'appareil de surfusion et des clamps pour œil (méthode OPI)
[Voir Burton et al. (17) pour d'autres descriptions génériques de l'appareil de surfusion et du clamp pour œil]
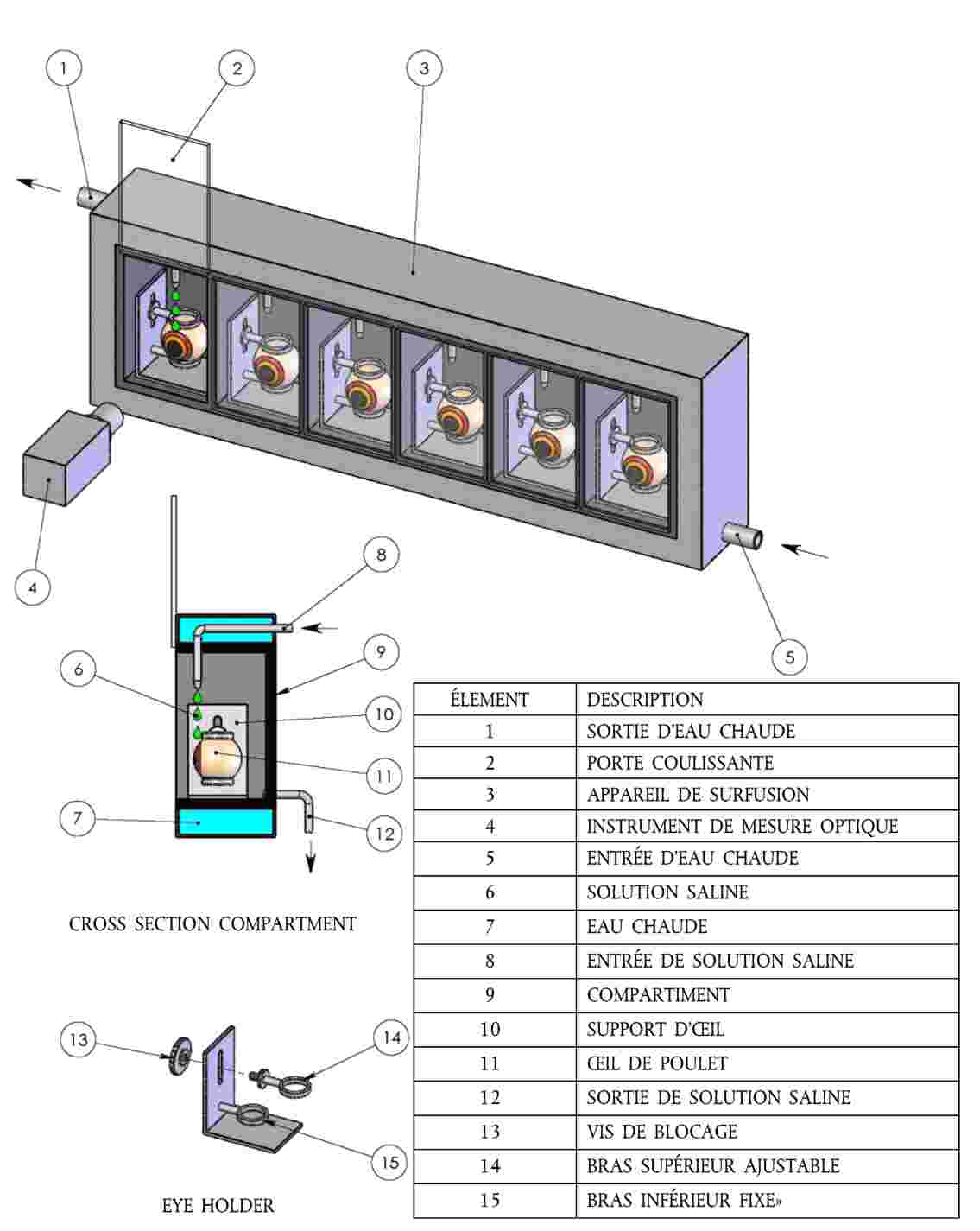
(1) Les classes de produits chimiques ont été attribuées à chaque substance testée à l'aide d'un système de classification normalisé, fondé sur le système de classification du Medical Subject Headings (MeSH) de la Bibliothèque nationale de médecine des États-Unis d'Amérique (disponible sur http//www.nlm.nih.gov/mesh).
(2) D'après les résultats de l'essai in vivo sur œil de lapin (Ligne directrice de l'OCDE no 405) et en utilisant le SGH des NU (3)(7).
(3) D'après les résultats des méthodes OPCB et OPI.
(4) Les dimensions indiquées ici sont celles d’un porte-cornée utilisé pour des bovins âgés de 12 à 60 mois. Pour des animaux âgés de 6 à 12 mois, le porte-cornée est conçu de telle sorte que chaque chambre ait une contenance de 4 ml et que chacune des chambres internes mesure 1,5 cm de diamètre et 2,2 cm de profondeur. Pour tout porte-cornée nouvellement conçu, il est essentiel que le rapport entre la surface cornéenne exposée et le volume de la chambre postérieure soit le même que celui du porte-cornée classique. Cette condition est indispensable pour garantir que les valeurs de perméabilité sont correctement déterminées pour le calcul du SIIV par la formule donnée.
(5) Les scores de gonflement cornéen ne sont applicables que si l'épaisseur est mesurée au moyen d'un biomicroscope Haag-Streit BP900 équipé d'un dispositif de mesure de profondeur no I avec un réglage de largeur de fente à 9½, soit 0,095 mm. Les utilisateurs tiennent compte du fait que les mesures d'épaisseur de cornée par un biomicroscope varient en fonction du réglage de la largeur de fente.
(6) Voir tableau 1
(7) Voir tableau 2.
(8) Combinaisons moins probables.
(9) Les classes de produits chimiques ont été attribuées à chaque substance testée à l'aide d'un système de classification normalisé, fondé sur le système de classification du Medical Subject Headings (MeSH) de la Bibliothèque nationale de médecine des États-Unis d'Amérique (disponible sur http//www.nlm.nih.gov/mesh).
(10) D'après les résultats de l'essai in vivo sur œil de lapin (Ligne directrice de l'OCDE no 405) et en utilisant le SGH des NU (3)(7).
(11) D'après les résultats des méthodes OPCB et OPI.



