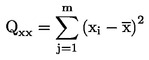EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32014R0709
Commission Regulation (EU) No 709/2014 of 20 June 2014 amending Regulation (EC) No 152/2009 as regards the determination of the levels of dioxins and polychlorinated biphenyls Text with EEA relevance
Règlement (UE) n ° 709/2014 de la Commission du 20 juin 2014 portant modification du règlement (CE) n ° 152/2009 en ce qui concerne la détermination des teneurs en dioxines et en polychlorobiphényles Texte présentant de l'intérêt pour l'EEE
Règlement (UE) n ° 709/2014 de la Commission du 20 juin 2014 portant modification du règlement (CE) n ° 152/2009 en ce qui concerne la détermination des teneurs en dioxines et en polychlorobiphényles Texte présentant de l'intérêt pour l'EEE
OJ L 188, 27.6.2014, p. 1–18
(BG, ES, CS, DA, DE, ET, EL, EN, FR, HR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
 In force
In force
- Date of document:
- 20/06/2014
- Date of effect:
- 17/07/2014; entrée en vigueur date de publication + 20 voir art. 2
- Date of end of validity:
- No end date
- Author:
- Commission européenne
- Form:
- Règlement
- Additional information:
- intérêt pour l'EEE
- Treaty:
- Traité sur le fonctionnement de l’Union européenne
- Legal basis:
-
- 32004R0882 - A11P4
- Link
- Link
- Link
- Select all documents mentioning this document No data available in the table
- Modifies:
-
Relation Act Comment Subdivision concerned From To Modifies 32009R0152 remplacement annexe V B 17/07/2014 - Link
- EUROVOC descriptor:
- Subject matter:
- Directory code:
|
27.6.2014 |
FR |
Journal officiel de l'Union européenne |
L 188/1 |
RÈGLEMENT (UE) No 709/2014 DE LA COMMISSION
du 20 juin 2014
portant modification du règlement (CE) no 152/2009 en ce qui concerne la détermination des teneurs en dioxines et en polychlorobiphényles
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l'Union européenne,
vu le règlement (CE) no 882/2004 du Parlement européen et du Conseil du 29 avril 2004 relatif aux contrôles officiels effectués pour s'assurer de la conformité avec la législation sur les aliments pour animaux et les denrées alimentaires et avec les dispositions relatives à la santé animale et au bien-être des animaux (1), et notamment son article 11, paragraphe 4,
considérant ce qui suit:
|
(1) |
Le règlement (CE) no 152/2009 de la Commission (2) énonce les méthodes de détermination des teneurs en dibenzo-p-dioxines polychlorées (PCDD), en dibenzofuranes polychlorés (PCDF) et en polychlorobiphényles (PCB) de type dioxine des aliments pour animaux. |
|
(2) |
Il convient de définir les exigences applicables aux méthodes de dépistage qui servent à détecter les échantillons présentant des teneurs significatives en PCDD/F et en PCB de type dioxine (permettant de sélectionner de préférence les échantillons dépassant les seuils d'intervention et garantissant la sélection des échantillons dépassant les teneurs maximales) et qui ont une grande capacité. En ce qui concerne les teneurs maximales, le taux de faux conformes de ces méthodes de dépistage devrait être inférieur à 5 %. |
|
(3) |
Lorsque la méthode de dépistage appliquée donne des résultats qui dépassent la valeur seuil, il convient d'analyser l'échantillon original au moyen d'une méthode permettant d'identifier et de quantifier les PCDD/F et les PCB de type dioxine contenus dans l'échantillon. Les méthodes d'identification et de quantification sont dénommées «méthodes de confirmation». Sur la base de l'évolution et des progrès techniques, la chromatographie en phase gazeuse couplée à la spectrométrie de masse en tandem (CG-SM/SM) devrait être autorisée en tant que méthode de confirmation servant à contrôler le respect de la teneur maximale, en plus de la chromatographie en phase gazeuse couplée à la spectrométrie de masse haute résolution (CG/SMHR). |
|
(4) |
L'expérience acquise à la faveur de l'application des règles en vigueur montre qu'il convient de modifier les dispositions actuelles en ce qui concerne la nécessité d'effectuer une double analyse, l'appréciation de la conformité en cas de double analyse et l'exigence relative à l'acceptabilité de l'écart entre l'estimation supérieure et l'estimation inférieure. |
|
(5) |
Il convient dès lors de modifier le règlement (CE) no 152/2009 en conséquence. |
|
(6) |
Les mesures prévues au présent règlement sont conformes à l'avis du comité permanent de la chaîne alimentaire et de la santé animale, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
L'annexe V, partie B, du règlement (CE) no 152/2009 est modifiée conformément à l'annexe du présent règlement.
Article 2
Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l'Union européenne.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 20 juin 2014.
Par la Commission
Le président
José Manuel BARROSO
(1) JO L 165 du 30.4.2004, p. 1.
(2) Règlement (CE) no 152/2009 de la Commission du 27 janvier 2009 portant fixation des méthodes d'échantillonnage et d'analyse destinées au contrôle officiel des aliments pour animaux (JO L 54 du 26.2.2009, p. 1).
ANNEXE
À l'annexe V du règlement (CE) no 152/2009, la partie B, intitulée «DÉTERMINATION DES TENEURS EN DIOXINES (PCDD/PCDF) ET EN PCB», est remplacée par le texte suivant.
«B. DÉTERMINATION DES TENEURS EN DIOXINES (PCDD/PCDF) ET EN PCB
CHAPITRE I
Méthodes de prélèvement d'échantillons et interprétation des résultats d'analyse
1. Objet et champ d'application
Les échantillons destinés au contrôle officiel des teneurs en dibenzo-p-dioxines polychlorées (PCDD), en dibenzofuranes polychlorés (PCDF), en polychlorobiphényles (PCB) (1) de type dioxine et en PCB autres que ceux de type dioxine des aliments pour animaux sont prélevés conformément aux dispositions de l'annexe I. Les exigences quantitatives concernant le contrôle des substances ou des produits répartis uniformément dans les aliments pour animaux prévues au point 5.1 de l'annexe I sont appliquées. Les échantillons globaux ainsi obtenus sont considérés comme représentatifs des lots ou sous-lots sur lesquels ils sont prélevés. Le respect des teneurs maximales fixées dans la directive 2002/32/CE est établi sur la base des teneurs déterminées dans les échantillons de laboratoire.
Aux fins de la présente partie B, les définitions figurant à l'annexe I de la décision 2002/657/CE de la Commission (2) s'appliquent.
Outre ces définitions, les définitions suivantes s'appliquent aux fins de la présente partie B:
|
|
“méthodes de dépistage”: méthodes servant à sélectionner les échantillons dont les teneurs en PCDD, PCDF et PCB de type dioxine dépassent les teneurs maximales ou les seuils d'intervention. Elles offrent une grande capacité de traitement d'échantillons à la fois efficace et économique et augmentent la probabilité de découvrir de nouveaux cas d'exposition élevée des consommateurs et de risques pour leur santé. Les méthodes de dépistage sont fondées sur des méthodes de bioanalyse ou sur des méthodes CG-SM. Les résultats des échantillons dépassant la valeur seuil, obtenus aux fins du contrôle du respect de la teneur maximale, sont vérifiés; à cette fin, l'échantillon initial est soumis à une nouvelle analyse complète, réalisée au moyen d'une méthode de confirmation; |
|
|
“méthodes de confirmation”: méthodes qui fournissent des informations complètes ou complémentaires permettant l'identification et la quantification univoque des PCDD, PCDF et des PCB de type dioxine à la teneur maximale ou, en cas de besoin, au seuil d'intervention. Ces méthodes recourent à la chromatographie en phase gazeuse couplée à la spectrométrie de masse haute résolution (CG-SMHR) ou à la chromatographie en phase gazeuse couplée à la spectrométrie de masse en tandem (CG-SM/SM). |
2. Respect de la teneur maximale
2.1. Spécification relative aux PCB autres que ceux de type dioxine
Le lot est conforme à la teneur maximale si le résultat d'analyse ne dépasse pas la teneur maximale en PCB autres que ceux de type dioxine fixée dans la directive 2002/32/CE, compte tenu de l'incertitude de mesure.
Le lot n'est pas conforme à la teneur maximale si le résultat d'analyse supérieur (3), confirmé par une double analyse (4), dépasse la teneur maximale fixée dans la directive 2002/32/CE, compte tenu de l'incertitude de mesure. La moyenne des deux dosages, compte tenu de l'incertitude de mesure, sert à vérifier la conformité.
L'incertitude de mesure est prise en compte de l'une des manières suivantes:
|
— |
en calculant l'incertitude étendue au moyen d'un facteur de couverture 2 qui donne un niveau de confiance d'environ 95 %. Un lot ou sous-lot est non conforme si la valeur mesurée moins U dépasse la teneur maximale, |
|
— |
en établissant la limite de décision (CCα) conformément à l'annexe I, point 3.1.2.5, de la décision 2002/657/CE. Un lot ou sous-lot est non conforme si la valeur mesurée est égale ou supérieure à la CCα. |
Les trois premiers alinéas s'appliquent au résultat d'analyse de l'échantillon destiné au contrôle officiel. En cas d'analyse à des fins de recours ou d'arbitrage, les règles nationales s'appliquent.
2.2. Spécification relative aux PCDD/F et aux PCB de type dioxine
Le lot est conforme aux teneurs maximales si le résultat d'une seule analyse,
|
— |
effectuée selon une méthode de dépistage avec un taux de faux conformes inférieur à 5 %, indique que la teneur ne dépasse pas les limites maximales respectives fixées pour les PCDD/PCDF et la somme des PCDD/PCDF et des PCB de type dioxine dans la directive 2002/32/CE, |
|
— |
effectuée selon une méthode de confirmation, ne dépasse pas les teneurs maximales respectives fixées pour les PCDD/PCDF et la somme des PCDD/PCDF et des PCB de type dioxine dans la directive 2002/32/CE, compte tenu de l'incertitude de mesure. |
Pour les analyses de dépistage, une valeur seuil doit être établie pour déterminer la conformité aux teneurs maximales respectives fixées pour les PCDD/PCDF ou pour la somme des PCDD/PCDF et des PCB de type dioxine.
Le lot n'est pas conforme à la teneur maximale si le résultat d'analyse supérieur (5), obtenu à l'aide d'une méthode de confirmation et confirmé par une double analyse, dépasse la teneur maximale fixée dans la directive 2002/32/CE, compte tenu de l'incertitude de mesure (6). La moyenne des deux déterminations, compte tenu de l'incertitude de mesure, sert à vérifier la conformité.
L'incertitude de mesure est prise en compte de l'une des manières suivantes:
|
— |
en calculant l'incertitude étendue au moyen d'un facteur de couverture 2 qui donne un niveau de confiance d'environ 95 %. Un lot ou sous-lot est non conforme si la valeur mesurée moins U dépasse la teneur maximale. En cas de détermination distincte des PCDD/PCDF et des PCB de type dioxine, la somme des estimations de l'incertitude élargie des résultats d'analyse distincts concernant les PCDD/PCDF et les PCB de type dioxine doit être utilisée pour la somme des PCDD/PCDF et des PCB de type dioxine, |
|
— |
en établissant la limite de décision (CCα) conformément au point 3.1.2.5 de l'annexe I de la décision 2002/657/CE. Un lot ou sous-lot est non conforme si la valeur mesurée est égale ou supérieure à la CCα. |
Les quatre premiers alinéas s'appliquent au résultat d'analyse de l'échantillon destiné au contrôle officiel. En cas d'analyse à des fins de recours ou d'arbitrage, les règles nationales s'appliquent.
3. Résultats dépassant les seuils d'intervention prévus à l'annexe II de la directive 2002/32/CE
Les seuils d'intervention sont utilisés aux fins de la sélection d'échantillons dans les cas où il est nécessaire de déterminer une source de contamination et de prendre des mesures de réduction ou d'élimination de celle-ci. Les méthodes de dépistage établissent des valeurs seuil appropriées aux fins de la sélection de ces échantillons. S'il est nécessaire d'accomplir des efforts considérables pour déterminer une source et pour réduire ou éliminer la contamination, il peut être approprié de confirmer le dépassement du seuil d'intervention en réalisant une double analyse au moyen d'une méthode de confirmation et en tenant compte de l'incertitude de mesure (7).
CHAPITRE II
Préparation des échantillons et prescriptions applicables aux méthodes d'analyse à utiliser pour le contrôle officiel des teneurs en dioxines (PCDD/PCDF) et en PCB de type dioxine des aliments pour animaux
1. Champ d'application
Les prescriptions du présent chapitre s'appliquent aux analyses d'aliments pour animaux effectuées aux fins du contrôle officiel des teneurs en dibenzo-p-dioxines polychlorées et dibenzofuranes polychlorés (PCDD/F) substitués en 2,3,7,8 et en polychlorobiphényles de type dioxine (PCB de type dioxine), ainsi qu'à d'autres fins réglementaires.
La présence de PCDD/F et de PCB de type dioxine dans les aliments pour animaux peut être contrôlée au moyen des deux types de méthodes d'analyse décrites ci-après.
|
a) |
Méthodes de dépistage Les méthodes de dépistage servent à sélectionner les échantillons dont les teneurs en PCDD/F et en PCB de type dioxine dépassent les teneurs maximales ou les seuils d'intervention. Elles devraient offrir une grande capacité de traitement d'échantillons à la fois efficace et économique et augmenter la probabilité de découvrir de nouveaux cas d'exposition élevée des consommateurs et de risques pour leur santé. Leur application doit permettre d'éviter les faux conformes. Elles peuvent comprendre des méthodes de bioanalyse et des méthodes de CG-SM. Elles permettent de comparer le résultat d'une analyse avec une valeur seuil et de confirmer ou d'infirmer (réponse positive ou négative) l'éventuel dépassement de la teneur maximale ou du seuil d'intervention. La concentration de PCDD/F et la somme des PCDD/F et des PCB de type dioxine dans les échantillons suspectés de non-conformité à la teneur maximale doivent être déterminées/confirmées au moyen d'une méthode de confirmation. En outre, les méthodes de dépistage peuvent donner une indication des teneurs en PCDD/F et en PCB de type dioxine des échantillons. En cas d'application de méthodes bioanalytiques de dépistage, le résultat est exprimé en équivalents de bioanalyse (BEQ), alors qu'en cas d'application de méthodes CG-SM physico-chimiques, il est exprimé en équivalents toxiques (TEQ). Les résultats numériques obtenus au moyen de méthodes de dépistage permettent de démontrer la conformité, la suspicion de non-conformité ou le dépassement des seuils d'intervention et donnent une indication sur la plage des teneurs en cas de suivi au moyen de méthodes de confirmation. Ils ne permettent pas, par exemple, d'évaluer les niveaux de bruit de fond, d'estimer l'ingestion, de suivre l'évolution chronologique des teneurs ou de réévaluer les seuils d'intervention et les teneurs maximales. |
|
b) |
Méthodes de confirmation Les méthodes de confirmation permettent l'identification et la quantification univoques des PCDD/F et des PCB de type dioxine présents dans un échantillon et de fournir des informations complètes à l'échelle du congénère. Par conséquent, ces méthodes permettent de contrôler les teneurs maximales et les seuils d'intervention et de confirmer les résultats obtenus au moyen des méthodes de dépistage. En outre, les résultats peuvent servir à d'autres fins, telles que la détermination des faibles niveaux de bruit de fond dans le contrôle des aliments pour animaux, le suivi de l'évolution chronologique, l'évaluation de l'exposition et la création d'une base de données en vue de la réévaluation éventuelle des seuils d'intervention et des teneurs maximales. Ils sont aussi importants pour établir les profils de congénères aux fins de la détermination de la source d'une contamination éventuelle. Ces méthodes reposent sur la chromatographie en phase gazeuse couplée à la spectrométrie de masse haute résolution (CG-SMHR). La chromatographie en phase gazeuse couplée à la spectrométrie de masse en tandem (CG-SM/SM) peut également être utilisée pour confirmer la conformité ou la non-conformité à la teneur maximale. |
2. Contexte
Pour le calcul des concentrations d'équivalents toxiques (TEQ), les concentrations des différentes substances dans un échantillon donné sont multipliées par leurs facteurs d'équivalence toxique (TEF) respectifs [voir note (1)* de bas de page au chapitre I], puis elles sont additionnées de façon à donner la concentration totale de composés de type dioxine, exprimée en TEQ.
Aux fins de la présente partie B, la limite de quantification spécifique acceptée d'un congénère est la teneur minimale en analyte mesurable avec une certitude statistique raisonnable, satisfaisant aux critères d'identification décrits dans des normes internationalement reconnues, telles que la norme EN 16215:2012 (Aliments des animaux — Dosage des dioxines et des PCB de type dioxine par CG-SMHR et des PCB indicateurs par CG-SMHR) et/ou les méthodes EPA 1613 et 1668 révisées.
La limite de quantification d'un congénère peut être:
|
a) |
la concentration d'un analyte dans l'extrait d'un échantillon qui produit une réponse instrumentale à deux ions suivis avec un rapport S/B (signal/bruit) de 3:1 pour le signal de données brut le moins intense; ou |
|
b) |
si, pour des raisons techniques, le calcul du rapport signal/bruit ne donne pas des résultats fiables, le point de concentration minimal sur une courbe d'étalonnage qui donne un écart acceptable (≤ 30 %) et cohérent (mesuré au moins au début et à la fin d'une série analytique d'échantillons) par rapport au facteur de réponse relatif moyen calculé pour tous les points de la courbe d'étalonnage de chaque série d'échantillons. La limite de quantification est calculée à partir du point de concentration le plus bas, compte tenu du taux de récupération des étalons internes et du prélèvement d'échantillons. |
Les méthodes bioanalytiques de dépistage ne donnent pas de résultats à l'échelle du congénère mais une simple indication (8) de la valeur TEQ, exprimée en équivalents de bioanalyse (BEQ) compte tenu du fait qu'il est possible que tous les composés présents dans un extrait d'échantillon produisant une réponse lors de l'essai ne remplissent pas l'ensemble des conditions du principe du TEQ.
Les méthodes de dépistage et de confirmation ne peuvent être appliquées aux fins du contrôle d'une matrice donnée que si les méthodes sont suffisamment sensibles pour déceler les teneurs de manière fiable au niveau du seuil d'intervention ou de la teneur maximale.
3. Prescriptions d'assurance qualité
3.1. Des mesures doivent être prises pour que soit évitée toute contamination croisée à chaque étape de la procédure d'échantillonnage et d'analyse.
3.2. Les échantillons doivent être conservés et transportés dans des récipients en verre, en aluminium, en polypropylène ou en polyéthylène adaptés à la conservation, préservant les teneurs en PCDD/PCDF et en PCB de type dioxine dans les échantillons de la moindre influence. Toute trace de poussière de papier doit être enlevée du contenant de l'échantillon.
3.3. La conservation et le transport de l'échantillon doivent être effectués d'une façon telle que l'intégrité de l'échantillon d'aliment pour animaux est préservée.
3.4. Si nécessaire, chaque échantillon pour laboratoire doit être broyé finement et soigneusement mélangé, selon une méthode garantissant une homogénéisation complète (par exemple de façon à pouvoir passer au travers d'un tamis à mailles de 1 mm). Les échantillons doivent être séchés avant le broyage si leur teneur en humidité est trop élevée.
3.5. Il y a lieu de contrôler les réactifs, la verrerie et l'équipement en vue de déceler toute influence des résultats exprimés en TEQ ou en BEQ.
3.6. Un essai à blanc est réalisé, en suivant tout le procédé d'analyse, mais sans l'échantillon.
3.7. Pour les méthodes de bioanalyse, l'ensemble de la verrerie et des solvants utilisés dans l'analyse doivent faire l'objet d'un dépistage de composés interférant avec la détection des composés cibles dans la plage de travail. La verrerie est rincée à l'aide de solvants ou chauffée à des températures permettant d'éliminer de sa surface les traces de PCDD/PCDF, de composés de type dioxine et de composés interférents.
3.8. La quantité de l'extrait doit être suffisamment élevée, de façon à répondre aux prescriptions en ce qui concerne une plage de travail suffisamment basse comprenant les concentrations des teneurs maximales ou du seuil d'intervention.
3.9. Les procédures spécifiques de préparation des échantillons utilisées pour les produits considérés doivent être conformes aux lignes directrices internationalement acceptées.
4. Prescriptions applicables aux laboratoires
4.1. Conformément aux dispositions du règlement (CE) no 882/2004, les laboratoires doivent être accrédités par un organisme habilité qui se conforme au guide ISO 58, de manière à garantir qu'ils appliquent les procédures d'assurance qualité à leurs analyses. Les laboratoires doivent être accrédités selon la norme EN ISO/CEI 17025.
4.2. L'aptitude des laboratoires doit être prouvée par la participation continue et réussie à des études interlaboratoires sur le dosage des PCDD/PCDF et des PCB de type dioxine dans les matrices d'aliments pour animaux et les plages de concentration correspondantes.
4.3. Les laboratoires appliquant les méthodes de dépistage pour les contrôles de routine des échantillons coopèrent étroitement avec les laboratoires appliquant la méthode de confirmation, tant pour le contrôle qualité que pour la confirmation du résultat de l'analyse des échantillons suspects.
5. Prescriptions fondamentales applicables aux procédés d'analyse relatifs aux dioxines (PCDD/PCDF) et aux PCB de type dioxine
5.1. Sensibilité élevée et limite de quantification basse
En ce qui concerne les PCDD/PCDF, étant donné la toxicité extrêmement élevée de certains de ces composés, les seuils de détection doivent être de l'ordre de quelques femtogrammes (10-15 g). Pour la plupart des congénères PCB, une limite de quantification de l'ordre du nanogramme (10–9 g) est déjà suffisante. Pour la mesure des congénères PCB de type dioxine plus toxiques (en particulier les congénères non ortho substitués), la limite inférieure de la plage de travail doit être sous le picogramme (10-12 g). Pour tous les autres congénères PCB, une limite de quantification de l'ordre du nanogramme (10-9 g) est suffisante.
5.2. Grande sélectivité (spécificité)
5.2.1. Il est nécessaire de distinguer les PCDD/PCDF et les PCB de type dioxine d'une multitude d'autres composés extraits simultanément de l'échantillon qui sont susceptibles d'interférer et peuvent être présents à des concentrations supérieures, jusqu'à plusieurs ordres de grandeur, à celles des analytes à doser. Pour les méthodes de CG-SM, il est nécessaire d'établir une distinction entre les congénères, notamment entre les congénères toxiques (par exemple, les dix-sept PCDD/PCDF substitués en 2,3,7,8 et les douze PCB de type dioxine) et les autres congénères.
5.2.2. Les méthodes de bioanalyse doivent permettre la détection des composés cibles en tant que somme des PCDD/PCDF et/ou des PCB de type dioxine. La purification des échantillons est destinée à éliminer les composés à l'origine de faux non conformes ou les composés susceptibles d'atténuer la réponse et de donner des faux conformes.
5.3. Grande exactitude (justesse et fidélité, taux de récupération apparent du bioessai)
5.3.1. Pour les méthodes de CG-SM, le dosage doit fournir une estimation juste de la concentration réelle dans un échantillon. Une grande exactitude est nécessaire pour empêcher que le résultat d'une analyse d'échantillon ne soit écarté en raison du manque de fiabilité de la valeur TEQ déterminée. L'exactitude est une expression de la justesse (la différence entre la valeur moyenne mesurée pour un analyte dans un matériau certifié et sa valeur certifiée, exprimée en pourcentage de cette valeur) et de la fidélité (RSDR est l'écart type relatif calculé à partir des résultats obtenus dans des conditions de reproductibilité).
5.3.2. Pour les méthodes de bioanalyse, le taux de récupération apparent du bioessai doit être déterminé. Le taux de récupération apparent du bioessai désigne la valeur BEQ calculée à partir de la courbe d'étalonnage de la TCDD ou du PCB 126 corrigée du blanc, puis divisée par la valeur TEQ déterminée par la méthode de confirmation. Elle vise à corriger des facteurs tels que la perte de PCDD/PCDF et de composés de type dioxine durant les phases d'extraction et de purification, la coextraction de composés qui augmentent ou atténuent la réponse (effets agonistes et antagonistes), la qualité de l'ajustement de la courbe ou les différences entre les valeurs TEF (facteur d'équivalence toxique) et REP (potentiel relatif). Le taux de récupération apparent du bioessai est calculé à partir d'échantillons de référence appropriés avec des profils de congénères représentatifs proches du niveau considéré.
5.4. Validation dans la plage de la teneur maximale et mesures générales de contrôle qualité
5.4.1. Les laboratoires doivent démontrer la validité de la méthode dans une certaine plage proche de la teneur maximale, par exemple à des niveaux correspondant à 0,5 fois, 1 fois et 2 fois la teneur maximale, avec un coefficient de variation acceptable pour les analyses répétées, durant la procédure de validation et l'analyse de routine.
5.4.2. Des essais à blanc et des expériences avec enrichissement ou des analyses sur des échantillons témoins (si possible, des matériaux de référence certifiés) sont effectués régulièrement dans le cadre des mesures internes de contrôle qualité. Il est nécessaire de réaliser et de vérifier des cartes de contrôle qualité pour les essais à blanc, les expériences avec enrichissement ou l'analyse des échantillons témoins afin de garantir que les performances analytiques sont conformes aux prescriptions.
5.5. Limite de quantification
5.5.1. Pour une méthode bioanalytique de dépistage, l'établissement de la limite de quantification n'est pas indispensable, mais il doit être démontré que la méthode permet de distinguer la valeur de blanc de la valeur seuil. En cas de transmission d'une valeur BEQ, il est nécessaire d'établir un seuil d'inscription permettant de savoir que faire des échantillons produisant une réponse au-dessous de ce seuil. Le seuil d'inscription doit présenter une différence avérée d'un facteur de trois au moins par rapport aux échantillons du blanc de procédure produisant une réponse au-dessous de la plage de travail. Il est donc calculé à partir d'échantillons contenant les composés cibles proches de la teneur minimale requise et non à partir d'un rapport S/B ou d'un blanc d'essai.
5.5.2. La limite de quantification pour une méthode de confirmation est de l'ordre d'un cinquième de la teneur maximale.
5.6. Critères d'analyse
La fiabilité des résultats des méthodes de confirmation ou de dépistage impose le respect des critères ci-après dans la plage de la teneur maximale ou du seuil d'intervention pour la valeur TEQ ou la valeur BEQ, qu'elle soit exprimée en TEQ totaux (somme des PCDD/F et des PCB de type dioxine) ou séparément pour les PCDD/F et les PCB de type dioxine.
|
|
Dépistage au moyen de méthodes de bioanalyse ou de méthodes physico-chimiques |
Méthodes de confirmation |
|
Taux de faux conformes (9) |
< 5 % |
|
|
Justesse |
|
De – 20 % à + 20 % |
|
Répétabilité (RSDr) |
< 20 % |
|
|
Reproductibilité intralaboratoire (RSDR) |
< 25 % |
< 15 % |
5.7. Prescriptions spécifiques applicables aux méthodes de dépistage
5.7.1. Le dépistage peut être effectué au moyen de méthodes de CG-SM et de méthodes de bioanalyse. Pour les méthodes de CG-SM, les prescriptions établies au point 6 doivent être appliquées. Pour les méthodes de bioanalyse cellulaire, des prescriptions spécifiques sont établies au point 7.
5.7.2. Les laboratoires appliquant les méthodes de dépistage pour les contrôles de routine d'échantillons coopèrent étroitement avec les laboratoires appliquant la méthode de confirmation.
5.7.3. Les performances de la méthode de dépistage doivent être vérifiées durant l'analyse de routine par un contrôle qualité des analyses et par la validation continue de la méthode. Il doit exister un programme continu de contrôle des résultats conformes.
5.7.4. Contrôle de l'atténuation éventuelle de la réponse cellulaire et cytotoxicité:
vingt pour cent des extraits d'échantillons doivent être mesurés par dépistage de routine sans et avec ajout de la 2,3,7,8-TCDD à la teneur maximale ou au seuil d'intervention, pour vérifier si la réponse est éventuellement atténuée par des substances interférentes présentes dans l'extrait d'échantillon. La concentration mesurée dans l'échantillon enrichi doit être comparée à la somme de la concentration de l'extrait non enrichi et de la concentration de l'enrichissement. Si cette concentration mesurée est inférieure de plus de 25 % à la concentration (somme) calculée, cela indique la possibilité d'atténuation du signal et l'échantillon en question doit faire l'objet de l'analyse de confirmation par CG-SMHR. Les résultats doivent être contrôlés à l'aide de cartes de contrôle qualité.
5.7.5. Contrôle qualité sur des échantillons conformes:
environ 2 à 10 % des échantillons conformes, en fonction de la matrice et de l'expérience du laboratoire, doivent être confirmés par CG-SMHR.
5.7.6. Détermination des taux de faux conformes à partir des données du contrôle qualité:
le taux de faux conformes résultant du dépistage des échantillons au-dessous et au-dessus de la teneur maximale ou du seuil d'intervention doit être déterminé. Les taux réels de faux conformes doivent être inférieurs à 5 %. Dès lors que le contrôle qualité des échantillons conformes fait apparaître au moins vingt résultats confirmés par matrice/groupe de matrices, des conclusions sur le taux de faux conformes doivent être tirées à partir de cette base de données. Les résultats des échantillons analysés au moyen d'essais interlaboratoires ou durant des cas de contamination, jusqu'à concurrence d'une concentration de deux fois la teneur maximale, par exemple, peuvent figurer parmi les vingt résultats à atteindre pour déterminer le taux de faux conformes. Les échantillons doivent couvrir les profils de congénères les plus fréquents et provenir de diverses sources.
Bien que les bioanalyses de dépistage servent avant tout à révéler les échantillons dépassant le seuil d'intervention, le critère appliqué pour la détermination des taux de faux conformes est la teneur maximale, compte tenu de l'incertitude de mesure de la méthode de confirmation.
5.7.7. Les résultats du dépistage indiquant que des échantillons pourraient être non conformes doivent toujours être vérifiés; à cette fin, l'échantillon initial est soumis à une nouvelle analyse complète, réalisée au moyen d'une méthode de confirmation. Ces échantillons peuvent également servir à l'évaluation du taux de faux non conformes. Pour les méthodes de dépistage, le taux de faux non conformes est la fraction des résultats dont la conformité est confirmée par une analyse de confirmation, alors que lors du dépistage précédent, les échantillons avaient été déclarés potentiellement non conformes. L'évaluation du caractère avantageux de la méthode de dépistage doit se fonder sur la comparaison du nombre d'échantillons faussement non conformes et du nombre total d'échantillons contrôlés. Ce taux doit être suffisamment bas pour rendre l'utilisation de la méthode de dépistage avantageuse.
5.7.8. Les méthodes de bioanalyse doivent fournir une indication juste de la valeur TEQ, calculée et exprimée en BEQ, au moins dans des conditions de validation.
De plus, pour les méthodes de bioanalyse appliquées dans des conditions de répétabilité, le RSDr intralaboratoire sera généralement inférieur au RSDR (reproductibilité).
6. Prescriptions spécifiques applicables aux méthodes de CG-SM à respecter à des fins de dépistage ou de confirmation
6.1. Écarts acceptables entre l'estimation supérieure et l'estimation inférieure des OMS-TEQ
L'écart entre l'estimation supérieure et l'estimation inférieure ne peut dépasser 20 % pour la confirmation du dépassement des teneurs maximales ou, en cas de besoin, des seuils d'intervention.
6.2. Mesure des taux de récupération
6.2.1. Des étalons internes de PCDD/PCDF substitués en 2,3,7,8 marqués au 13C et des étalons internes de PCB de type dioxine marqués au 13C doivent être ajoutés au tout début de la méthode d'analyse, par exemple avant la phase d'extraction, afin de valider le procédé d'analyse. Il est nécessaire d'ajouter au moins un congénère pour chacun des groupes d'isomères tétrachlorés à octachlorés des PCDD/PCDF et au moins un congénère pour chaque groupe d'isomères des PCB de type dioxine (une autre méthode consiste à ajouter au moins un congénère pour chaque fenêtre d'acquisition spectrométrique utilisée pour le contrôle des PCDD/PCDF et des PCB de type dioxine). Pour les méthodes de confirmation, il y a lieu d'utiliser la totalité des dix-sept étalons internes de PCDD/PCDF substitués en 2,3,7,8 marqués au 13C ainsi que la totalité des douze étalons internes de PCB de type dioxine marqués au 13C.
6.2.2. Des facteurs de réponse relatifs doivent également être déterminés dans le cas des congénères pour lesquels aucun analogue marqué au 13C n'est ajouté, en utilisant des solutions d'étalonnage appropriées.
6.2.3. Pour les aliments pour animaux d'origine végétale et les aliments pour animaux d'origine animale contenant moins de 10 % de graisses, il est obligatoire d'ajouter les étalons internes avant la phase d'extraction. Pour les aliments pour animaux d'origine animale contenant plus de 10 % de graisses, les étalons internes sont ajoutés soit avant soit après l'extraction des graisses. L'efficacité de l'extraction doit faire l'objet d'une validation appropriée, eu égard à la phase au cours de laquelle les étalons internes sont introduits et à la façon dont les résultats sont consignés (sur la base du produit ou des graisses).
6.2.4. Avant l'analyse CG-SM, un ou deux étalons de récupération (substitution) doivent être ajoutés.
6.2.5. Le taux de récupération doit être mesuré. Dans le cas des méthodes de confirmation, les taux de récupération des étalons internes doivent se situer dans une plage comprise entre 60 et 120 %. Pour des congénères individuels, en particulier pour certains dibenzo-p-dioxines et dibenzofuranes heptachlorés et octachlorés, des taux de récupération inférieurs ou supérieurs sont acceptables, à condition que leur contribution à la valeur TEQ ne dépasse pas 10 % de la valeur TEQ totale (sur la base de la somme des PCDD/PCDF et des PCB de type dioxine). Dans le cas des méthodes de dépistage par CG-SM, les taux de récupération doivent se situer dans une plage comprise entre 30 et 140 %.
6.3. Élimination des substances interférentes
|
— |
Les PCDD/PCDF sont séparés des composés chlorés interférents, tels que les PCB autres que ceux de type dioxine et les diphényléthers chlorés, au moyen de techniques chromatographiques appropriées (de préférence au moyen d'une colonne de florisil, d'alumine et/ou de charbon). |
|
— |
La séparation des isomères par chromatographie en phase gazeuse doit être < 25 % de pic à pic entre 1,2,3,4,7,8-HxCDF et 1,2,3,6,7,8-HxCDF. |
6.4. Étalonnage avec courbe étalon
La plage de la courbe d'étalonnage doit couvrir la plage correspondante des teneurs maximales ou des seuils d'intervention.
6.5. Critères spécifiques applicables aux méthodes de confirmation
|
— |
CG-SMHR:
|
|
— |
CG-SM/SM:
|
7. Prescriptions spécifiques applicables aux méthodes de bioanalyse
Les méthodes de bioanalyse sont des méthodes fondées sur le recours aux principes biologiques tels que les bioessais cellulaires, les tests d'interaction récepteurs ou les immuno-essais. Le présent point 7 énonce les prescriptions applicables aux méthodes de bioanalyse en général.
Dans une méthode de dépistage, l'échantillon est en principe déclaré conforme ou est déclaré suspecté d'être non conforme. À cette fin, la valeur BEQ calculée est comparée à la valeur seuil (voir point 7.3). Les échantillons au-dessous de la valeur seuil sont déclarés conformes, et ceux à la valeur seuil ou au-dessus de celle-ci sont déclarés suspectés d'être non conformes et nécessitent une analyse au moyen d'une méthode de confirmation. Dans la pratique, une valeur BEQ équivalant aux deux tiers de la teneur maximale peut servir de valeur seuil, à condition qu'un taux de faux conformes inférieur à 5 % et un taux acceptable de faux non conformes soient garantis. Avec des teneurs maximales distinctes pour les PCDD/F et pour la somme des PCDD/F et des PCB de type dioxine, le contrôle de la conformité des échantillons sans fractionnement requiert des valeurs seuil de bioessai appropriées pour les PCDD/F. Pour la vérification des échantillons dépassant les seuils d'intervention, la valeur seuil pourrait être un pourcentage approprié des seuils d'intervention respectifs.
En outre, dans le cas de certaines méthodes de bioanalyse, une valeur indicative exprimée en BEQ peut être donnée pour les échantillons situés dans la plage de travail et dépassant le seuil d'inscription (voir points 7.1.1 et 7.1.6).
7.1. Évaluation de la réponse à l'essai
7.1.1. Prescriptions générales
|
— |
Le calcul des concentrations à partir d'une courbe d'étalonnage de la TCDD fera apparaître une variation importante (coefficient de variation élevé — CV) des valeurs aux extrémités inférieure et supérieure de la courbe. La plage de travail est la zone où ce CV est inférieur à 15 %. L'extrémité inférieure de la plage de travail (seuil d'inscription) doit par ailleurs être établie à un niveau supérieur d'un facteur de trois au moins aux blancs de procédure. L'extrémité supérieure de la plage de travail est habituellement représentée par la valeur EC70 (70 % de la concentration effective maximale), mais elle se situe à un niveau inférieur si le CV est supérieur à 15 % dans cette plage. La plage de travail est établie pendant la validation. Les valeurs seuil (point 7.3) doivent se situer dans la plage de travail. |
|
— |
Les solutions étalon et les extraits d'échantillon doivent être analysés au moins en double. En cas d'utilisation de doubles, une solution étalon ou un extrait témoin analysé dans quatre à six puits répartis sur la plaque doivent produire une réponse ou une concentration (possible uniquement dans la plage de travail) sur la base d'un CV inférieur à 15 %. |
7.1.2. Étalonnage
7.1.2.1. Étalonnage avec courbe étalon
|
— |
Les teneurs dans les échantillons doivent être estimées par comparaison de la réponse à l'essai avec une courbe d'étalonnage de la TCDD (ou du PCB 126 ou d'un mélange type de PCDD/PCDF/PCB de type dioxine) pour calculer la valeur BEQ dans l'extrait et, par la suite, dans l'échantillon. |
|
— |
Les courbes d'étalonnage doivent contenir de huit à douze concentrations (au moins en double), la concentration dans la partie inférieure de la courbe (plage de travail) devant être suffisante. Une attention particulière doit être accordée à la qualité de l'ajustement de la courbe dans la plage de travail. La valeur R2 a peu ou n'a pas de valeur en tant que telle pour l'appréciation de la justesse de l'ajustement en régression non linéaire. La réduction de l'écart entre les valeurs calculées et les valeurs observées dans la plage de travail de la courbe améliorera l'ajustement (la réduction de la somme des résidus au carré, par exemple). |
|
— |
Le niveau estimatif dans l'extrait d'échantillon doit ensuite être corrigé de la valeur BEQ calculée pour un échantillon blanc de matrice/de solvant (pour tenir compte des impuretés provenant des solvants et substances chimiques utilisés) et du taux de récupération apparent (calculé à partir de la valeur BEQ d'échantillons de référence adéquats avec des profils de congénères représentatifs proches de la teneur maximale ou du seuil d'intervention). Pour la correction par le taux de récupération, le taux de récupération apparent doit se situer dans les limites de la plage requise (voir point 7.1.4). Les échantillons de référence utilisés pour corriger du taux de récupération doivent respecter les prescriptions énoncées au point 7.2. |
7.1.2.2. Étalonnage avec des échantillons de référence
Une autre solution consiste à utiliser une courbe d'étalonnage élaborée à partir d'au moins quatre échantillons de référence (voir point 7.2.4: une matrice blanche et trois échantillons de référence à 0,5 fois, 1,0 fois et 2,0 fois la teneur maximale ou le seuil d'intervention), ce qui permet de se passer de la correction par le blanc et le taux de récupération. Dans ce cas, la réponse à l'essai correspondant aux deux tiers de la teneur maximale (voir point 7.3) peut être calculée directement à partir de ces échantillons et servir de valeur seuil. Pour la vérification des échantillons dépassant les seuils d'intervention, la valeur seuil pourrait être un pourcentage approprié de ces seuils d'intervention.
7.1.3. Dosage distinct des PCDD/PCDF et des PCB de type dioxine
Les extraits peuvent être séparés en fractions contenant des PCDD/PCDF et des PCB de type dioxine, permettant une indication distincte des teneurs en PCDD/PCDF et en PCB de type dioxine (en BEQ). Il convient d'utiliser de préférence une courbe d'étalonnage du PCB 126 pour évaluer les résultats de la fraction contenant les PCB de type dioxine.
7.1.4. Taux de récupération apparents du bioessai
Le “taux de récupération apparent du bioessai” doit être calculé à partir d'échantillons de référence appropriés avec des profils de congénères représentatifs qui sont proches de la teneur maximale ou du seuil d'intervention et être exprimé en pourcentage de la valeur BEQ par rapport à la valeur TEQ. En fonction du type de bioessai et des TEF (10) utilisés, les écarts entre les facteurs TEF et REP pour les PCB de type dioxine peuvent entraîner des taux de récupération apparents faibles pour les PCB de type dioxine par rapport aux PCDD/PCDF. Par conséquent, en cas de dosage distinct des PCDD/PCDF et des PCB de type dioxine, les taux de récupération apparents du bioessai doivent être de 20 à 60 % pour les PCB de type dioxine et de 50 à 130 % pour les PCDD/PCDF (les plages s'appliquent pour la courbe d'étalonnage de la TCDD). Comme la contribution des PCB de type dioxine à la somme des PCDD/PCDF et des PCB de type dioxine peut varier en fonction des matrices et des échantillons, les taux de récupération apparents du bioessai pour la somme des PCDD/PCDF et des PCB de type dioxine reflètent ces plages et doivent se situer entre 30 et 130 %. Toute modification substantielle des valeurs TEF aux fins de la législation de l'Union relative aux PCDD/PCDF et aux PCB de type dioxine requiert la révision de ces plages.
7.1.5. Contrôle des taux de récupération de la purification
La perte de composés durant la purification doit être vérifiée pendant la validation. Un échantillon blanc enrichi d'un mélange des différents congénères doit faire l'objet d'une purification (n = 3 au moins) et la récupération et la variabilité doivent être vérifiées au moyen d'une méthode de confirmation. Le taux de récupération doit se situer entre 60 et 120 %, surtout pour les congénères contribuant à hauteur de plus de 10 % à la valeur TEQ dans différents mélanges.
7.1.6. Seuil d'inscription
S'agissant de l'inscription des valeurs BEQ dans un rapport, un seuil d'inscription est déterminé à partir des échantillons de matrice considérés associant des profils de congénères types, mais pas à partir de la courbe d'étalonnage des étalons, la précision de la plage inférieure de la courbe n'étant pas suffisante. Les effets de l'extraction et de la purification doivent être pris en compte. Le seuil d'inscription doit être établi à un niveau supérieur d'un facteur de trois au moins aux blancs de procédure.
7.2. Utilisation d'échantillons de référence
7.2.1. Les échantillons de référence représentent la matrice de prélèvement, les profils de congénères et les plages de concentration des PCDD/PCDF et des PCB de type dioxine proches de la teneur maximale ou du seuil d'intervention.
7.2.2. Chaque série d'essais doit comporter une matrice blanche ou, à défaut, un blanc de procédure et un échantillon de référence à la teneur maximale ou au seuil d'intervention. Ces échantillons doivent être extraits et analysés au même moment et dans les mêmes conditions. La réponse de l'échantillon de référence doit être nettement plus élevée que celle de l'échantillon blanc, garantissant ainsi la validité de l'essai. Ces échantillons peuvent être utilisés pour corriger du blanc et du taux de récupération.
7.2.3. Les échantillons de référence choisis pour corriger du taux de récupération doivent être représentatifs des échantillons de l'essai, ce qui signifie que les profils de congénères ne peuvent pas conduire à une surestimation des teneurs.
7.2.4. Des échantillons de référence supplémentaires, d'une concentration égale à 0,5 fois et 2 fois la teneur maximale ou le seuil d'intervention, par exemple, peuvent être inclus pour démontrer l'efficacité de l'essai dans la plage pertinente pour le contrôle de la teneur maximale ou du seuil d'intervention. Agrégés, ces échantillons peuvent servir au calcul des valeurs BEQ dans les échantillons d'essai (voir point 7.1.2.2).
7.3. Détermination de valeurs seuil
Le lien entre les résultats de bioanalyse en BEQ et les résultats des méthodes de confirmation en TEQ doit être établi, par exemple par des expériences d'étalonnage avec adaptation matricielle, à l'aide d'échantillons de référence enrichis pour atteindre 0, 0,5 fois, 1 fois et 2 fois la teneur maximale, avec six répétitions sur chaque teneur (n = 24). Les facteurs de correction (blanc et taux de récupération) peuvent être estimés à partir de ce lien mais doivent être contrôlés conformément au point 7.2.2.
Des valeurs seuil sont établies pour déterminer la conformité de l'échantillon avec les teneurs maximales ou pour vérifier que les seuils d'intervention, s'ils sont considérés, sont conformes aux teneurs maximales ou seuils d'intervention respectifs établis pour les PCDD/PCDF et pour les PCB de type dioxine pris isolément, ou pour la somme des PCDD/PCDF et des PCB de type dioxine. Elles sont représentées par l'extrémité inférieure de la répartition des résultats de bioanalyse (corrigés du blanc et du taux de récupération) correspondant à la limite de décision de la méthode de confirmation fondée sur un niveau de confiance de 95 %, soit un taux de faux conformes inférieur à 5 %, et sur un RSDR inférieur à 25 %. La limite de décision de la méthode de confirmation est la teneur maximale, compte tenu de l'incertitude de mesure.
La valeur seuil (en BEQ) peut être calculée selon l'une des formules énoncées aux points 7.3.1, 7.3.2 et 7.3.3 (voir graphique 1).
7.3.1. Utilisation de la plage inférieure de l'intervalle de prédiction de 95 % à la limite de décision de la méthode de confirmation:

où
|
BEQDL |
BEQ correspondant à la limite de décision de la méthode de confirmation, soit la teneur maximale compte tenu de l'incertitude de mesure |
|
sy,x |
Écart type résiduel |
|
t α,f = m-2 |
Facteur de Student (α = 5 %, f = degrés de liberté, unilatéral) |
|
m |
Nombre total de points d'étalonnage (indice j) |
|
n |
Nombre de répétitions à chaque niveau |
|
xi |
Concentration dans l'échantillon (en TEQ) du point d'étalonnage i, déterminée par une méthode de confirmation |
|
|
Concentration moyenne (en TEQ) de tous les échantillons d'étalonnage |
|
|
Qxx = Paramètre de la somme des carrés, i = indice pour le point d'étalonnage i |
7.3.2. Calcul à partir des résultats de bioanalyse (corrigés du blanc et du taux de récupération) de multiples analyses d'échantillons (n ≥ 6) contaminés à hauteur de la limite de décision de la méthode de confirmation, en tant qu'extrémité inférieure de la répartition des données à la valeur BEQ moyenne correspondante:
Valeur seuil = BEQDL — 1,64 x SDR
Où:
|
SDR |
Écart type des résultats de bioanalyse à la BEQDL, mesuré dans des conditions de reproductibilité intralaboratoire |
7.3.3. Mesure en tant que valeur moyenne des résultats de bioanalyse (en BEQ, corrigée du blanc et du taux de récupération) à partir de l'analyse multiple d'échantillons (n ≥ 6) contaminés aux deux tiers de la teneur maximale ou du seuil d'intervention, sachant que ce niveau sera proche de la valeur seuil déterminée conformément au point 7.3.1 ou 7.3.2:
Graphique 1
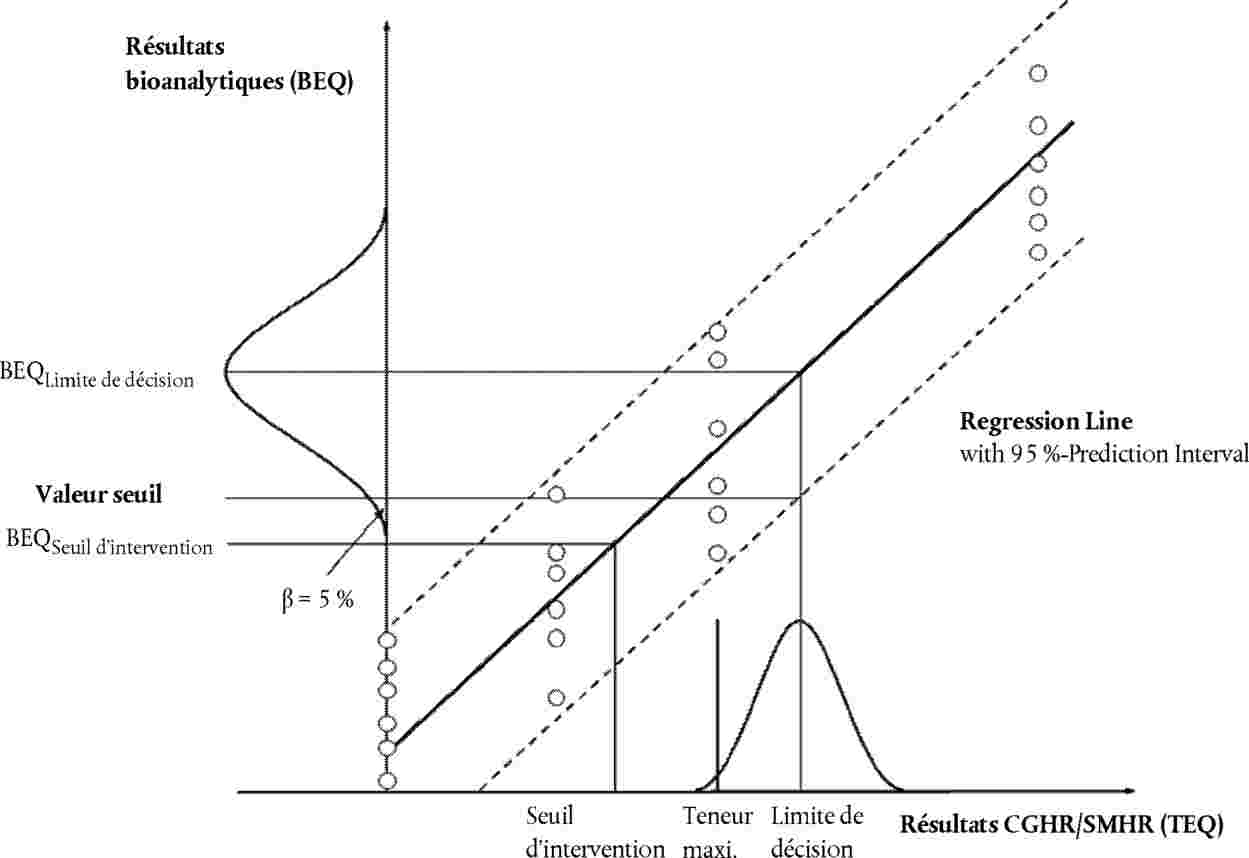
Graphique 1. Calcul des valeurs seuil sur la base d'un niveau de confiance de 95 %, soit un taux de faux conformes inférieur à 5 %, et d'un RSDR inférieur à 25 %:
|
1. |
à partir de la plage inférieure de l'intervalle de prédiction de 95 % à la limite de décision de la méthode de confirmation, |
|
2. |
à partir de l'analyse multiple d'échantillons (n ≥ 6) contaminés à hauteur de la limite de décision de la méthode de confirmation en tant qu'extrémité inférieure de la répartition des données (représentée dans le graphique par une courbe en cloche) à la valeur BEQ moyenne correspondante. |
7.3.4. Restriction aux valeurs seuil
Les valeurs seuil fondées sur la valeur BEQ calculées à partir du RSDR atteint durant la validation à l'aide d'un nombre limité d'échantillons de matrices/profils de congénères différents peuvent être supérieures aux teneurs maximales ou aux seuils d'intervention fondés sur la valeur TEQ en raison d'une plus grande fiabilité que celle qu'il est possible d'atteindre dans les analyses de routine lorsqu'un spectre inconnu de profils de congénères possibles doit être contrôlé. Dans de tels cas, les valeurs seuil sont calculées à partir d'un RSDR égal à 25 %, ou, de préférence, aux deux tiers de la teneur maximale ou du seuil d'intervention.
7.4. Caractéristiques de performances
7.4.1. Étant donné qu'aucun étalon interne ne peut être utilisé dans les méthodes de bioanalyse, des tests de répétabilité de ces méthodes doivent être effectués pour obtenir des données sur l'écart type au sein des séries d'essais et entre elles. La répétabilité doit être inférieure à 20 % et la reproductibilité intralaboratoire inférieure à 25 %. Ce calcul doit être fondé sur les valeurs calculées en BEQ après correction par le blanc et le taux de récupération.
7.4.2. Dans le cadre de la procédure de validation, l'essai doit permettre de distinguer un échantillon blanc d'une teneur à la valeur seuil, permettant ainsi l'identification des échantillons au-dessus de la valeur seuil correspondante (voir point 7.1.2).
7.4.3. Les composés cibles, les interférences potentielles et les valeurs maximales tolérées pour le blanc doivent être définis.
7.4.4. L'écart type relatif de la concentration calculée à partir des réponses (possible uniquement dans la plage de travail) d'un triple dosage d'un extrait d'échantillon ne peut être supérieur à 15 %.
7.4.5. Les résultats non corrigés du ou des échantillons de référence exprimés en BEQ (blanc et teneur maximale ou seuil d'intervention) doivent être utilisés pour évaluer les performances de la méthode de bioanalyse dans un intervalle de temps constant.
7.4.6. Il convient de réaliser et de vérifier des cartes de contrôle qualité pour les blancs de procédure et chaque type d'échantillon de référence afin de s'assurer que la performance analytique est conforme aux prescriptions, notamment pour les blancs de procédure en ce qui concerne la différence minimale requise par rapport à l'extrémité inférieure de la plage de travail et pour les échantillons de référence en ce qui concerne la reproductibilité intralaboratoire. Les blancs de procédure doivent être bien contrôlés en vue d'éviter les faux conformes lorsqu'ils sont retranchés.
7.4.7. Les résultats des échantillons suspects obtenus au moyen des méthodes de confirmation et 2 à 10 % des échantillons conformes (au minimum vingt échantillons par matrice) sont collectés et utilisés pour l'évaluation des performances de la méthode de dépistage et du lien entre les valeurs BEQ et TEQ. Cette base de données peut être utilisée aux fins de la réévaluation des valeurs seuil applicables aux échantillons de routine pour les matrices validées.
7.4.8. Les bonnes performances des méthodes peuvent également être démontrées à l'aide d'essais interlaboratoires. Les résultats des échantillons analysés dans des essais interlaboratoires, couvrant une concentration atteignant, par exemple, jusqu'à deux fois la teneur maximale, peuvent également faire partie de l'évaluation du taux de faux conformes, si un laboratoire est en mesure de démontrer ses bonnes performances. Les échantillons doivent couvrir les profils de congénères les plus fréquents et provenir de diverses sources.
7.4.9. En cas de crise, les valeurs seuil peuvent être réévaluées, reflétant mieux la matrice et les profils de congénères particuliers de ce cas précis.
8. Inscription des résultats dans un rapport
8.1. Méthodes de confirmation
8.1.1. Dans la mesure où le procédé d'analyse utilisé le permet, les résultats d'analyse comprennent les teneurs en congénères individuels des PCDD/PCDF et des PCB de type dioxine et sont indiqués en estimation inférieure, estimation supérieure et estimation intermédiaire, afin que soit consigné un maximum de données, ce qui permet une interprétation des résultats en fonction de prescriptions spécifiques.
8.1.2. Le rapport doit mentionner la méthode utilisée pour extraire les PCDD/PCDF et les PCB de type dioxine.
8.1.3. Les taux de récupération des étalons internes individuels doivent être mentionnés s'ils se situent en dehors de la plage mentionnée au point 6.2.5 ou si la teneur maximale est dépassée (dans ce cas, les taux de récupération doivent être fournis pour l'une des deux analyses faites en double). Dans tous les autres cas, ils doivent être communiqués sur demande.
8.1.4. L'incertitude de mesure doit également être mentionnée, car ce paramètre est pris en compte lorsqu'il s'agit de déterminer la conformité d'un échantillon. Par conséquent, les résultats de l'analyse sont consignés sous la forme x ± U, où x est le résultat de l'analyse et U l'incertitude de mesure élargie calculée au moyen d'un facteur d'élargissement de 2 qui donne un niveau de confiance d'environ 95 %. En cas de dosage distinct des PCDD/PCDF et des PCB de type dioxine, la somme des estimations de l'incertitude élargie des résultats d'analyse distincts concernant les PCDD/PCDF et les PCB de type dioxine doit être utilisée pour la somme des PCDD/PCDF et des PCB de type dioxine.
8.1.5. Si l'incertitude de mesure est prise en considération au moyen de la CCα (conformément au chapitre I, point 2.2, de la présente partie), ce paramètre doit figurer dans le rapport.
8.1.6. Les résultats doivent être exprimés dans les mêmes unités et par au moins le même nombre de chiffres significatifs que les teneurs maximales établies dans la directive 2002/32/CE.
8.2. Méthodes bioanalytiques de dépistage
8.2.1. Le dépistage donne un résultat qui doit être énoncé comme étant “conforme” ou “suspecté d'être non conforme” (“suspect”) dans le rapport.
8.2.2. Le dépistage peut aussi donner, pour les PCDD/PCDF et/ou les PCB de type dioxine, un résultat exprimé en BEQ, et non en TEQ.
8.2.3. Les échantillons dont la réponse est au-dessous du seuil d'inscription doivent être énoncés comme étant “sous le seuil d'inscription”.
8.2.4. Pour chaque type de matrice de prélèvement, le rapport doit mentionner la teneur maximale ou le seuil d'intervention sur lequel repose l'évaluation.
8.2.5. Le rapport doit mentionner le type d'essai appliqué, le principe de base de l'essai et le type d'étalonnage.
8.2.6. Le rapport doit mentionner la méthode utilisée pour extraire les PCDD/PCDF et les PCB de type dioxine.
8.2.7. Dans le cas d'échantillons suspectés d'être non conformes, le rapport doit comprendre une note sur les mesures à prendre. La concentration de PCDD/PCDF et la somme des PCDD/PCDF et des PCB de type dioxine dans ces échantillons présentant des teneurs élevées doivent être déterminées/confirmées au moyen d'une méthode de confirmation.
CHAPITRE III
Préparation des échantillons et prescriptions applicables aux méthodes d'analyse à utiliser pour le contrôle officiel des teneurs en PCB autres que ceux de type dioxine (PCB # 28, 52, 101, 138, 153 et 180)
1. Champ d'application
Les prescriptions du présent chapitre s'appliquent aux analyses d'aliments pour animaux effectuées aux fins du contrôle officiel des teneurs en biphényles polychlorés autres que ceux de type dioxine (PCB autres que ceux de type dioxine) et à d'autres fins réglementaires.
2. Méthodes de détection applicables
Chromatographie en phase gazeuse/détection à capture d'électrons (CG-DCE), CG-SMBR, CG-SM/SM, CG-SMHR ou méthodes équivalentes.
3. Identification et confirmation des analytes considérés
3.1. Temps de rétention relatif par rapport aux étalons internes ou aux étalons de référence (écart admissible de ± 0,25 %).
3.2. Séparation par chromatographie en phase gazeuse des six PCB indicateurs (PCB 28, PCB 52, PCB 101, PCB 138, PCB 153 et PCB 180) des substances interférentes, surtout les PCB coélués, notamment si les teneurs des échantillons sont dans les limites légales et si la non-conformité doit être confirmée.
[Les congénères qui coéluent souvent sont, par exemple, les PCB 28/31, les PCB 52/69 et les PCB 138/163/164. Pour la CG/SM, il convient de tenir compte aussi des interférences possibles de fragments de congénères plus fortement chlorés.]
3.3. Prescriptions applicables aux techniques de CG-SM:
Mesure d'au moins:
|
a) |
deux ions spécifiques pour la SMHR; |
|
b) |
deux ions spécifiques d'un m/z > 200 ou trois ions spécifiques d'un m/z > 100 pour la SMBR; |
|
c) |
d'un précurseur et de deux ions produits pour la SM-SM. |
Tolérances maximales admises applicables aux rapports isotopiques des fragments de masse sélectionnés:
Écart relatif entre le rapport de l'ion cible (l'ion recherché le plus abondant) et du ou des ions qualificateurs et le rapport théorique de ces ions ou celui déterminé grâce à un standard d'étalonnage:
|
Intensité relative du ou des ions qualificateurs par rapport à l'ion cible |
CG-IE-SM (écart relatif) |
CG-IC-SS, CG-SMn (écart relatif) |
|
> 50 % |
± 10 % |
± 20 % |
|
De > 20 % à 50 % |
± 15 % |
± 25 % |
|
De > 10 % à 20 % |
± 20 % |
± 30 % |
|
≤ 10 % |
± 50 % (11) |
± 50 % (11) |
3.4. Prescriptions applicables aux techniques de CG-DCE
Les résultats dépassant la tolérance doivent être confirmés avec deux colonnes de CG présentant des phases stationnaires de polarité différente.
4. Démonstration des performances de la méthode
Les performances de la méthode doivent être validées dans la plage autour de la teneur maximale (0,5 à 2 fois la teneur maximale) avec un coefficient de variation acceptable pour les analyses répétées (voir prescriptions relatives à la fidélité intermédiaire au point 9).
5. Limite de quantification
Les valeurs de blanc ne peuvent être supérieures à 30 % du niveau de contamination correspondant à la teneur maximale (12).
6. Contrôle qualité
Essais à blanc, analyse d'échantillons enrichis, échantillons servant au contrôle qualité, participation à des études interlaboratoires sur les matrices pertinentes à intervalles réguliers.
7. Mesure des taux de récupération
7.1. Des étalons internes appropriés présentant des propriétés physico-chimiques comparables à celles des analytes considérés doivent être utilisés.
7.2. Ajout d'étalons internes:
ajout dans les échantillons (avant l'extraction et la purification),
7.3. Prescriptions applicables aux méthodes recourant aux six congénères indicateurs des PCB marqués d'un isotope:
|
a) |
les résultats doivent être corrigés des taux de récupération des étalons internes; |
|
b) |
les taux de récupération des étalons internes marqués d'un isotope doivent se situer entre 50 et 120 %; |
|
c) |
les taux de récupération inférieurs ou supérieurs pour les congénères individuels avec une contribution à la somme des six PCB indicateurs inférieure à 10 % sont acceptables. |
7.4. Prescriptions applicables aux méthodes ne recourant pas à l'ensemble des six étalons internes marqués d'un isotope ou recourant à d'autres étalons internes:
|
a) |
le taux de récupération du ou des étalons internes doit être mesuré pour chaque échantillon; |
|
b) |
les taux de récupération du ou des étalons internes doivent se situer entre 60 et 120 %; |
|
c) |
les résultats doivent être corrigés des taux de récupération des étalons internes. |
7.5. Les taux de récupération des congénères non marqués doivent être vérifiés à l'aide d'échantillons enrichis ou d'échantillons de contrôle qualité présentant des concentrations de l'ordre de la teneur maximale. Les taux de récupération pour ces congénères sont réputés acceptables s'ils se situent entre 70 et 120 %.
8. Prescriptions applicables aux laboratoires
Conformément aux dispositions du règlement (CE) no 882/2004, les laboratoires doivent être accrédités par un organisme habilité qui se conforme au guide ISO 58, de manière à garantir qu'ils appliquent les procédures d'assurance qualité à leurs analyses. Les laboratoires doivent être accrédités selon la norme EN ISO/CEI 17025.
9. Caractéristiques de performances: critères afférents à la somme des six PCB indicateurs à la teneur maximale
|
Justesse |
De – 30 % à + 30 % |
|
Fidélité intermédiaire (RSD %) |
≤ 20 % |
|
Différence entre l'estimation supérieure et l'estimation inférieure |
≤ 20 % |
10. Inscription des résultats dans un rapport
10.1. Dans la mesure où le procédé d'analyse utilisé le permet, les résultats d'analyse comprennent les teneurs en congénères individuels des PCB et sont indiqués en estimation inférieure, estimation supérieure et estimation intermédiaire, afin que soit consigné un maximum de données, ce qui permet une interprétation des résultats en fonction de prescriptions spécifiques.
10.2. Le rapport mentionne également la méthode utilisée pour extraire les PCB et les graisses.
10.3. Les taux de récupération des étalons internes individuels doivent être fournis s'ils se situent en dehors de la plage mentionnée au point 7 ou si la teneur maximale est dépassée. Dans tous les autres cas, ils doivent être fournis sur demande.
10.4. L'incertitude de mesure doit également être inscrite dans le rapport, car ce paramètre est pris en compte lorsqu'il s'agit de déterminer la conformité d'un échantillon. Par conséquent, les résultats de l'analyse sont consignés sous la forme x +/- U, où x est le résultat de l'analyse et U l'incertitude de mesure élargie calculée au moyen d'un facteur d'élargissement de 2 qui donne un niveau de confiance d'environ 95 %.
10.5. Si l'incertitude de mesure est prise en considération au moyen de la CCα (conformément au chapitre I, point 2.1), ce paramètre doit être inscrit dans le rapport.
10.6. Les résultats doivent être exprimés dans les mêmes unités et par au moins le même nombre de chiffres significatifs que les teneurs maximales établies dans la directive 2002/32/CE.
(9) Au regard des teneurs maximales.
(11) Le nombre de fragments de masse dont l'intensité relative est supérieure à 10 % étant suffisant, il est préférable de ne pas utiliser d'ion(s) qualificateur(s) d'une intensité relative inférieure à 10 % par rapport à l'ion cible.