ISSN 1977-0898
Euroopa Liidu
Teataja
C 305

Eestikeelne väljaanne
Teave ja teatised
61. aastakäik
30. august 2018
|
ISSN 1977-0898 |
||
|
Euroopa Liidu Teataja |
C 305 |
|

|
||
|
Eestikeelne väljaanne |
Teave ja teatised |
61. aastakäik |
|
Sisukord |
Lehekülg |
|
|
|
II Teatised |
|
|
|
EUROOPA LIIDU INSTITUTSIOONIDE, ORGANITE JA ASUTUSTE TEATISED |
|
|
|
Euroopa Komisjon |
|
|
2018/C 305/01 |
Vastuväidete esitamisest loobumine teatatud koondumise kohta (juhtum M.8970 – Sumitomo/Parkwind/Northwester2) ( 1 ) |
|
|
V Teated |
|
|
|
HALDUSMENETLUSED |
|
|
|
Euroopa Personalivaliku Amet (EPSO) |
|
|
2018/C 305/13 |
||
|
|
KONKURENTSIPOLIITIKA RAKENDAMISEGA SEOTUD MENETLUSED |
|
|
|
Euroopa Komisjon |
|
|
2018/C 305/14 |
Eelteatis koondumise kohta (juhtum M.9072 – KKR / Altice / SFR Filiale) — Võimalik lihtsustatud korras menetlemine ( 1 ) |
|
|
|
|
|
(1) EMPs kohaldatav tekst |
|
ET |
|
II Teatised
EUROOPA LIIDU INSTITUTSIOONIDE, ORGANITE JA ASUTUSTE TEATISED
Euroopa Komisjon
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/1 |
Vastuväidete esitamisest loobumine teatatud koondumise kohta
(juhtum M.8970 – Sumitomo/Parkwind/Northwester2)
(EMPs kohaldatav tekst)
(2018/C 305/01)
30. juulil 2018 otsustas komisjon loobuda vastuväidete esitamisest eespool nimetatud teatatud koondumise kohta ning kuulutada koondumine siseturuga kokkusobivaks. Otsuse aluseks on nõukogu määruse (EÜ) nr 139/2004 (1) artikli 6 lõike 1 punkt b. Otsuse täielik tekst on kättesaadav ainult inglise keeles ning see avaldatakse pärast seda, kui sellest on kustutatud võimalikud ärisaladused. Otsus on kättesaadav:
|
— |
Euroopa konkurentsialasel veebisaidil (http://ec.europa.eu/competition/mergers/cases/). Veebisaidil pakutakse mitut võimalust otsida konkreetset ühinemisotsust, sealhulgas ettevõtja nime, juhtumi numbri ja kuupäeva järgi ning tegevusalade registri kaudu; |
|
— |
elektroonilises vormis EUR-Lex’i veebisaidil (http://eur-lex.europa.eu/homepage.html?locale=et) dokumendinumbri 32018M8970 all. EUR-Lex pakub on-line-juurdepääsu Euroopa õigusele. |
IV Teave
TEAVE EUROOPA LIIDU INSTITUTSIOONIDELT, ORGANITELT JA ASUTUSTELT
Euroopa Komisjon
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/2 |
Euro vahetuskurss (1)
29. august 2018
(2018/C 305/03)
1 euro =
|
|
Valuuta |
Kurss |
|
USD |
USA dollar |
1,1660 |
|
JPY |
Jaapani jeen |
129,73 |
|
DKK |
Taani kroon |
7,4571 |
|
GBP |
Inglise nael |
0,90500 |
|
SEK |
Rootsi kroon |
10,6923 |
|
CHF |
Šveitsi frank |
1,1385 |
|
ISK |
Islandi kroon |
124,90 |
|
NOK |
Norra kroon |
9,7475 |
|
BGN |
Bulgaaria leev |
1,9558 |
|
CZK |
Tšehhi kroon |
25,745 |
|
HUF |
Ungari forint |
324,63 |
|
PLN |
Poola zlott |
4,2838 |
|
RON |
Rumeenia leu |
4,6417 |
|
TRY |
Türgi liir |
7,5236 |
|
AUD |
Austraalia dollar |
1,5989 |
|
CAD |
Kanada dollar |
1,5093 |
|
HKD |
Hongkongi dollar |
9,1524 |
|
NZD |
Uus-Meremaa dollar |
1,7413 |
|
SGD |
Singapuri dollar |
1,5941 |
|
KRW |
Korea vonn |
1 299,27 |
|
ZAR |
Lõuna-Aafrika rand |
16,8176 |
|
CNY |
Hiina jüaan |
7,9626 |
|
HRK |
Horvaatia kuna |
7,4370 |
|
IDR |
Indoneesia ruupia |
17 087,73 |
|
MYR |
Malaisia ringit |
4,8076 |
|
PHP |
Filipiini peeso |
62,375 |
|
RUB |
Vene rubla |
79,4075 |
|
THB |
Tai baat |
38,140 |
|
BRL |
Brasiilia reaal |
4,8451 |
|
MXN |
Mehhiko peeso |
22,3252 |
|
INR |
India ruupia |
82,3405 |
(1) Allikas: EKP avaldatud viitekurss.
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/3 |
Euroopa Liidu kombineeritud nomenklatuuri selgitavad märkused
(2018/C 305/04)
Vastavalt nõukogu määruse (EMÜ) nr 2658/87 (1) artikli 9 lõike 1 punktile a muudetakse Euroopa Liidu kombineeritud nomenklatuuri selgitavaid märkusi (2) järgmiselt:
Leheküljel 379
|
9401 |
Istmed (v.a rubriigis 9402 nimetatud), voodiks teisendatavad või mitte, ja nende osad |
lisatakse olemasoleva teksti järele järgmine tekst:
„Selle rubriigi tähenduses kehtib mis tahes viide bambusele ainult rubriigi 1401 taimsete materjalide kohta. Teiselt poolt kehtib selle rubriigi mis tahes viide puidule ka rubriigi 4412 bambusplaatide kohta. (Vt ka grupi 44 märkusi 1 b ja 6.)“
|
9403 |
Muu mööbel ja selle osad |
lisatakse olemasoleva teksti järele järgmine tekst:
„Rubriigi 9401 selgitavat märkust bambust või puitu käsitlevate viidete kohta kohaldatakse mutatis mutandis.“
(1) Nõukogu 23. juuli 1987. aasta määrus (EMÜ) nr 2658/87 tariifi- ja statistikanomenklatuuri ning ühise tollitariifistiku kohta (EÜT L 256, 7.9.1987, lk 1).
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/4 |
Euroopa Liidu kombineeritud nomenklatuuri selgitavad märkused
(2018/C 305/05)
Vastavalt nõukogu määruse (EMÜ) nr 2658/87 (1) artikli 9 lõike 1 punktile a muudetakse Euroopa Liidu kombineeritud nomenklatuuri selgitavaid märkusi (2) järgmiselt:
Leheküljel 379
|
9403 |
Muu mööbel ja selle osad |
lisatakse olemasoleva teksti järele järgmine tekst:
„Sellesse rubriiki ei kuulu infotablood, näiteks reklaamtahvlid ja rullplakatid.
Need tuleb klassifitseerida muudesse nomenklatuuri rubriikidesse, kus neid täpsemalt kirjeldatakse (näiteks reklaamtahvlid kirjutamiseks või joonistamiseks, mis vastavad rubriigi 9610 toodetele), või nende koostismaterjali järgi:
|
a) |
rubriiki, kuhu need tooted otseselt kuuluvad (näiteks rubriigi 8310 toodetele vastavad mitteväärismetallist plaadid klassifitseeritakse sellesse rubriiki), või |
|
b) |
rubriiki, kuhu kuulub mitmesuguseid sellest materjalist tooteid (näiteks rubriik 3926 või rubriik 7616). |
Näide rubriiki 9610 klassifitseeritava reklaamtahvli kohta:

Tahvelpinnaga reklaamtahvel.
Näide rubriiki 8310 klassifitseeritava reklaamtahvli kohta:
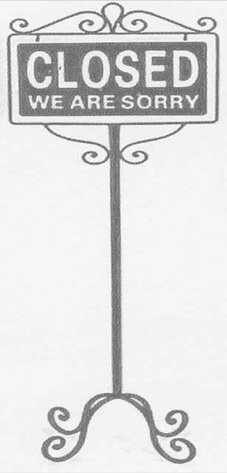
Üksnes mitteväärismetallist valmistatud reklaamtahvel.
Näiteid infotabloodest, mis tuleb klassifitseerida koostismaterjali järgi rubriiki, kuhu kuulub mitmesuguseid sellest materjalist tooteid:
|
|
|
|
Kõvaplastist alus ja alumiiniumraamist pealis plastplaadiga keskel, mis on mõlemalt poolt kaetud läbipaistva PVC-kilega. |
Alumiiniumalus ja -raam kummist kinnitusdetailidega ning paberipoogen, mida katab läbipaistev PVC-kile. |
|
Rubriik 7616 (põhiomaduse annab alumiiniumraam). |
Rubriik 7616 (põhiomaduse annab alumiiniumraam). |
|
|
|
|
Plastplaat, mis kinnitub viie peaaegu võrdse pikkusega plastvarda külge, millest igaüht saab eri suunda kallutada. Nelja varda otsas on plastkonks ja viienda otsa on paigaldatud plastotsak. |
|
|
Rubriik 3926 (toode on valmistatud üksnes plastist).“ |
|
(1) Nõukogu 23. juuli 1987. aasta määrus (EMÜ) nr 2658/87 tariifi- ja statistikanomenklatuuri ning ühise tollitariifistiku kohta (EÜT L 256, 7.9.1987, lk 1).
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/6 |
Euro käibemüntide uus liikmesriiki tähistav külg
(2018/C 305/06)

Luksemburgi käibele lastava uue 2-eurose mälestusmündi liikmesriiki tähistav külg
Euro käibemündid on seadusliku maksevahendina kasutusel kogu euroalal. Müntidega ametialaselt tegelevate isikute ja laiema avalikkuse teavitamiseks avaldab komisjon kõikide uute euromüntide kujunduse kirjelduse (1). Vastavalt nõukogu 10. veebruari 2009. aasta järeldustele (2) võivad euroala liikmesriigid ja riigid, kes on Euroopa Liiduga sõlminud euro käibemüntide käibelelaskmist käsitleva rahanduskokkuleppe, lasta käibele euro mälestusmünte. Selleks peavad olema täidetud teatavad tingimused, millest peamine on nõue, et mälestusmündina kasutataks üksnes 2-eurost münti. Mälestusmüntide tehnilised näitajad vastavad tavaliste 2-euroste käibemüntide näitajatele, kuid nende liikmesriiki tähistaval küljel on mälestust jäädvustav motiiv, mis on riigi või Euroopa tasandil sümboolne.
Käibele laskev riik : Luksemburg
Motiiv : suurhertsog Guillaume I 175. surma-aastapäev
Kujunduse kirjeldus : mündi paremal poolel on kujutatud Tema Kuninglik Kõrgus suurhertsog Henri, kes vaatab vasakule, ja vasakul poolel on kujutatud Tema Kuninglik Kõrgus suurhertsog Guillaume I. Kujutiste vahel on vertikaalselt aastaarvud 1772-1843 ja nimi „Guillaume Ier“. All on kiri „LUXEMBOURG“ ja aastaarv 2018.
Mündi välisringil on kujutatud Euroopa Liidu lipu 12 tähte.
Käibele lastavate müntide hinnanguline arv :
500 000Käibelelaskmise aeg : september 2018
(1) EÜT C 373, 28.12.2001, lk 1, kus on esitatud teave kõikide 2002. aastal käibele lastud müntide liikmesriiki tähistava külje kohta.
(2) Vt majandus- ja rahandusküsimuste nõukogu 10. veebruari 2009. aasta järeldused ning komisjoni 19. detsembri 2008. aasta soovitus, mis käsitleb ühiseid suuniseid euro käibemüntide liikmesriike tähistavate külgede ja kõnealuste müntide emiteerimise kohta (ELT L 9, 14.1.2009, lk 52).
Euroopa Andmekaitseinspektor
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/7 |
Arvamuse kokkuvõte, mis käsitleb ettepanekut sõnastada uuesti direktiiv avaliku sektori valduses oleva teabe taaskasutamise kohta
(Arvamuse täistekst (inglise, prantsuse ja saksa keeles) on Euroopa Andmekaitseinspektori veebilehel www.edps.europa.eu)
(2018/C 305/07)
Avaliku sektori teabe direktiivi eesmärk on lihtsustada avaliku sektori teabe taaskasutamist kogu Euroopa Liidus, ühtlustades põhitingimused, mis teevad avaliku sektori teabe direktiivi taaskasutajatele kättesaadavaks, et edendada avaliku sektori teabe direktiivil põhinevate liidu toodete ja teenuste arendamist ning vältida konkurentsimoonutusi.
Uute sätetega laiendatakse direktiivi rakendusala dokumentidele, mida valdavad avalik-õiguslikud ettevõtjad, kes tegutsevad sellistes riigihanke valdkondades nagu veemajandus, energia, transport ja postiteenused. Lisaks kohaldatakse sätteid dokumentide suhtes, mida valdavad avalikke teenuseid osutavad avalik-õiguslikud ettevõtjad, kui neid dokumente koostatakse seoses üldhuviteenuste osutamisega. Peale selle laieneb ettepaneku rakendusala teatud uuringuandmetele, näiteks teaduslike andmekogumisprotsesside tulemustele.
Arvamus keskendub konkreetsetele soovitustele, kuidas paremini selgitada avaliku sektori teabe direktiivi seost ja sidusust isikuandmete kaitse üldmääruse eranditega ning võrdlusele kohaldatava andmekaitseõigusega. Lisaks pakub see lisasoovitusi anonüümimise ja seoste kohta kulude ja andmekaitsega, juhtides tähelepanu ka andmekaitse mõju hindamisele, ühtlasi arvestades vastuvõetava taaskasutamise poliitikat.
Euroopa Andmekaitseinspektor toetub avaliku sektori teabe taaskasutamise direktiivi käsitleva käesoleva arvamuse koostamisel senisele tööle seoses n-ö „heade suurandmetega“ (Euroopa Liidu väärtuspõhine andmete ühiskasutus) ning eelkõige Euroopa Andmekaitseinspektori varem avaldatud arvamustele ja ametlikele märkustele, kooskõlas meie järelevalvejuhtumite tavaga. Juhime tähelepanu ka teemadele, mis vajavad ühtlustamist Euroopa Liidu tasandil, et avaliku sektori teabe direktiivi uuesti sõnastamisel oleks eeldatav kasulikkus.
Seoses ettepaneku artikli 1 lõike 2 punktiga g soovitab Euroopa Andmekaitseinspektor paremini selgitada avaliku sektori teabe direktiivi seoseid ja sidusust isikuandmete kaitse üldmäärusega, esitades sõnastusettepaneku.
Lisaks teeb Euroopa Andmekaitseinspektor ettepaneku viia praegu direktiivi 2013/37/EL artikli 1 lõikes 4 kehtestatud erisäte uuesti sisse direktiivi põhisätetesse ja ettepanekus selgesti märkida, et kohaldatakse isikuandmete kaitse üldmääruse artikli 4 lõikes 1 sätestatud isikuandmete määratlust. Samuti soovitab Euroopa Andmekaitseinspektor mainida isikuandmete kaitse üldmääruse artiklis 51 sätestatud järelevalveasutust ettepaneku artikli 4 lõikes 4.
Euroopa Andmekaitseinspektor soovitab samuti toetada anonüümimist, mainides anonüümset teavet õigustekstis ja laiendades reguleerimisalasse kuuluvate üksuste ulatust, kellel on õigus arvata anonüümimise kulud selliste kulude hulka, mille tasumist võib nõuda taaskasutajatelt.
Viimasena soovitab Euroopa Andmekaitseinspektor sätestada andmekaitse mõju hindamist tundlikke andmeid käsitlevate sektorite korral, näiteks tervishoiusektoris, millele litsentsiandja saaks otsustamisel tugineda ja selle alusel arvestada taaskasutamise tingimusi.
1. SISSEJUHATUS JA TAUST
|
1. |
Komisjon võttis 25. aprillil 2018 vastu ettepaneku muuta direktiivi 2013/37/EL (direktiivi 2003/98/EÜ läbivaatamise järel) avaliku sektori teabe taaskasutamise kohta (edaspidi „ettepanek“). Ettepanek kuulub 2018. aasta andmepaketi hulka, mis sisaldab ka teisi tähtsaid dokumente: i) komisjoni teatis „Euroopa ühtse andmeruumi loomine“ (edaspidi „teatis“); ii) erasektori andmete jagamise suunised talituste töödokumendina (edaspidi „suunised“); ja iii) avaliku sektori teabe direktiivi hinnang. |
|
2. |
Ettepaneku eesmärk on ajakohastada ja muuta direktiive 2013/37/EL ja 2003/98/EÜ (avaliku sektori teabe taaskasutamise kohta) olemasolevat teksti (avaliku sektori teabe direktiiv). |
|
3. |
Direktiivi läbivaatamine on üks kolmest meetmest, mida komisjon pakkus Euroopa Liidus ühtse andmeruumi loomiseks (vt komisjoni koondteatis COM (2018) 232, edaspidi „teatis“), koos erasektori andmete ühiskasutuse suunistega […] ning teadusinfo kättesaadavust ja säilitamist käsitleva soovituse ajakohastamisega […]. |
|
4. |
Euroopa Komisjoni eesmärk on toetada avaliku sektori teabe direktiivi muudatusettepanekuga avaliku sektori teabe, näiteks õigus-, liiklus-, ilma-, majandus- ja finantsandmete taaskasutamist, ühtlustades kogu Euroopa Liidus avaliku sektori teabe taaskasutajatele kättesaadavaks tegemise põhitingimused, et tõhustada liidu toodete ja teenuste arendamist, mis põhinevad avaliku sektori teabe direktiivil, ja vältida konkurentsimoonutusi. |
|
5. |
Ettepaneku üldeesmärk on saavutada kooskõla digitaalse ühtse turu strateegia eesmärkidega. Ettepanekuga soovitakse võimendada direktiivi mõju, tugevdades konkreetseid sätteid ja muutes neid asjakohaselt, et suurendada avaliku sektori taaskasutuseks kättesaadavate andmete hulka. Algatuse konkreetne eesmärk on ka väikeste ja keskmise suurusega ettevõtjate seisundi tugevdamine andmeturul, tagades õiglasema konkurentsi ja lihtsama juurdepääsu turgudele, koos piiriülese innovatsiooni tõhustamisega. |
|
6. |
Direktiivi asjaomaste uute sätetega muu hulgas laiendatakse rakendusala selliste avalik-õiguslike ettevõtjate valduses olevatele dokumentidele, kelle üksused tegutsevad aktiivselt sellistes riigihanke valdkondades nagu veemajandus, energia, transport ja postiteenused. Lisaks kohaldatakse sätteid dokumentide suhtes, mida valdavad avalikke teenuseid osutavad avalik-õiguslikud ettevõtjad, kui neid dokumente koostatakse seoses üldhuviteenuste osutamisega. Ettepaneku rakendusala laiendatakse ka teatud teadusuuringuandmetele, näiteks teaduslike andmekogumisprotsesside tulemustele (st katse- ja uuringutulemustele). Ettepanekuga sätestatakse praktiline „(…) horisontaalne raamistik, mis tagab taaskasutustingimuste minimaalse ühtlustamise kõikides valdkondades ja sektorites“ (1). |
|
7. |
Euroopa Andmekaitseinspektor märgib positiivse asjaoluna, et Euroopa Komisjoni andmetel on avaliku sektori teabe direktiivi uuesti sõnastamise eesmärk edendada avaliku sektori teabe taaskasutust, nagu rõhutatakse teatises: „vähendada eelkõige väikeste ja keskmise suurusega ettevõtjate turulepääsu takistavaid tõkkeid; minimeerida riski, et esimesena tegutsejal on ülemäära suur eelis, mis on kasulik suurtele ettevõtetele ja piirab seega kõnealuste andmete potentsiaalsete taaskasutajate arvu; suurendada ettevõtlusvõimalusi, kutsudes üles avaldama dünaamilisi andmeid ja kasutama rakendusliideseid“ (2). |
|
8. |
Avaliku sektori teabe direktiiv on osa Euroopa Liidu n-ö „heade suurandmete“ toetamise visioonist. Avaliku sektori teave on digitaalse ühtse turu suurandmete põhiallikas. Andmete arukal kasutamisel, sealhulgas töötlemisel tehisintellekti abil, võib olla pöördeline mõju kõigile majandussektoreile. |
|
9. |
Euroopa Andmekaitseinspektor esitas juba septembris 2016 koos arvamusega põhiõiguste sidusa jõustamise kohta suurandmete ajastul (3) Euroopa Liidu väärtustel põhineva Euroopa Liidu küberruumi kujundamise strateegia, juhtides tähelepanu sellistele probleemidele nagu turukontsentratsioon ja teabepõhine võim ning eraelu puutumatust suurendavate tehnoloogiate kui toote või teenuse funktsionaalsust kaotamata isikuandmete töötlemist minimeerivate meetmete nõrk turg (ajendatud privaatsuslõime (4) ja vaikeprivaatsuse põhimõttest). |
|
10. |
Peale selle soovib Euroopa Andmekaitseinspektor meenutada andmekaitse seisukohalt olulisi aluspõhimõtteid, mida Euroopa Komisjoni arvamuse kohaselt tuleb järgida andmete taaskasutamise kontekstis, nimelt i) andmete võimalikult vähene kinnistamine ja moonutamata konkurentsi tagamine; ii) läbipaistvus ja ühiskonna osalemine taaskasutuse eesmärgil, seoses kodanike ja/või andmesubjektidega, samuti läbipaistvus ja konkreetse eesmärgi määratlemine litsentsiandjate ja litsentsisaajate vahel; iii) andmekaitse mõju hindamine ja asjakohased andmekaitsetagatised taaskasutamisel (vastavalt mittekahjustamise põhimõttele – andmekaitse seisukohast). |
|
11. |
Kuigi Euroopa Komisjon küsis Euroopa Andmekaitseinspektorilt mitteametlikult nõu, ei ole määruse (EÜ) nr 45/2001 artikli 28 lõikega 2 nõutavat konsultatsiooni toimunud. Seetõttu põhineb arvamus sama määruse artikli 41 lõikel 2. Euroopa Andmekaitseinspektor soovitab vastuvõetud õigusakti preambulis viidata käesolevale arvamusele. |
7. KOKKUVÕTE
Euroopa Andmekaitseinspektor soovitab
|
— |
muuta ettepaneku artikli 1 lõike 2 punkti g ja konkreetselt sõnastada, kuidas erinevad „dokumendid“ ja „dokumentide osad“, mille suhtes avaliku sektori teabe direktiivi ei kohaldata andmekaitse põhjustel. |
|
— |
Lisada viide isikuandmete kaitse üldmääruse artiklis 51 sätestatud järelevalveasutusele ettepaneku artikli 4 lõikes 4, et veel rohkem tugevdada avaliku sektori teabe taaskasutamise ja isikuandmete kaitse seost. |
|
— |
Uuesti lisada ettepaneku põhiteksti andmekaitseõiguse kohaldatavuse erisäte, mis on praegu sätestatud direktiivi 2013/37/EL artikli 1 lõikes 4 (koos praegu kehtivate õigusaktide viidete vajaliku ajakohastamisega). |
|
— |
Rõhutada anonüümimist avaliku sektori teabe taaskasutuse kontekstis koos „anonüümse teabe“ mainimisega õigustekstis ja laiendada reguleerimisalasse kuuluvate üksuste ulatust, kellel on õigus arvata anonüümimise kulud selliste kulude hulka, mille tasumist võib nõuda taaskasutajatelt. |
|
— |
Selgesti sätestada ettepanekus, et kohaldatakse isikuandmete kaitse üldmääruse artikli 4 lõike 1 kohast isikuandmete mõistet. |
|
— |
Sätestada andmekaitse mõju hindamise nõue tundlikke andmeid käsitlevate sektorite korral, näiteks tervishoiusektoris, millele litsentsiandja saaks otsustamisel tugineda ja selle alusel arvestada taaskasutamise tingimusi. |
|
— |
Viimasena rõhutab Euroopa Andmekaitseinspektor neid soovitusi edastades järgmiste aluspõhimõtete asjakohasust andmekaitse jaoks, mida komisjoni arvamuse kohaselt tuleb järgida andmete taaskasutamise kontekstis, nimelt:
|
Brüssel, 10. juuli 2018
Euroopa Andmekaitseinspektor
Giovanni BUTTARELLI
(1) Seletuskiri ettepaneku kohta, mis käsitleb Euroopa Parlamendi ja nõukogu avaliku sektori valduses oleva teabe taaskasutamise direktiivi (uuesti sõnastatud), lk 3.
(2) Komisjoni teatis Euroopa Parlamendile, nõukogule, Euroopa Majandus- ja Sotsiaalkomiteele ning Regioonide Komiteele „Ühtse Euroopa andmeruumi loomine“, lk 5.
(3) https://edps.europa.eu/sites/edp/files/publication/16-09-23_bigdata_opinion_en.pdf, taaskasutamise kohta, lk 9.
(4) Euroopa Andmekaitseinspektori arvamus 05/2018 (esialgne arvamus privaatsuslõime kohta).
TEAVE LIIKMESRIIKIDELT
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/10 |
Komisjoni teadaanne vastavalt Euroopa Parlamendi ja nõukogu määruse (EÜ) nr 1008/2008 (ühenduses lennuteenuste osutamist käsitlevate ühiseeskirjade kohta) artikli 16 lõikele 4
Avaliku teenindamise kohustuste kehtestamine regulaarlennuliinidel
(EMPs kohaldatav tekst)
(2018/C 305/08)
|
Liikmesriik |
Portugal |
||||||
|
Lennuliin |
Bragança – Vila Real – Viseu – Cascais – Portimão – Cascais – Viseu – Vila Real – Bragança |
||||||
|
Avaliku teenindamise kohustuste jõustumise kuupäev |
23. detsember 2018 |
||||||
|
Aadress, millelt on võimalik saada avaliku teenindamise kohustuste teksti ning mis tahes asjakohast teavet ja/või dokumente |
Kõik dokumendid on kättesaadavad järgmisel aadressil: http://www.saphety.com Lisateave:
|
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/11 |
Komisjoni teadaanne vastavalt Euroopa Parlamendi ja nõukogu määruse (EÜ) nr 1008/2008 (ühenduses lennuteenuste osutamist käsitlevate ühiseeskirjade kohta) artikli 16 lõikele 4
Avaliku teenindamise kohustuste muutmine regulaarlennuliinidel
(EMPs kohaldatav tekst)
(2018/C 305/09)
|
Liikmesriik |
Ühendkuningriik |
|||||||||||
|
Lennuliin |
Oban – Coll Oban – Colonsay Oban – Tiree Coll – Tiree |
|||||||||||
|
Avaliku teenindamise kohustuste jõustumise esialgne kuupäev |
2. märts 2007 |
|||||||||||
|
Muudatuste jõustumise kuupäev |
16. mai 2019 |
|||||||||||
|
Aadress, millelt on võimalik saada avaliku teenindamise kohustuse teksti ning mis tahes asjakohast teavet ja/või dokumente |
Kõik dokumendid on kättesaadavad aadressil: http://www.publiccontractsscotland.gov.uk Lisateave:
|
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/12 |
Komisjoni teadaanne vastavalt Euroopa Parlamendi ja nõukogu määruse (EÜ) nr 1008/2008 (ühenduses lennuteenuste osutamist käsitlevate ühiseeskirjade kohta) artikli 17 lõikele 5
Hanketeade seoses regulaarlennuteenuste osutamisega avaliku teenindamise kohustuste alusel
(EMPs kohaldatav tekst)
(2018/C 305/10)
|
Liikmesriik |
Ühendkuningriik |
|||||||||||
|
Lennuliin |
Oban – Coll Oban – Colonsay Oban – Tiree Coll – Tiree |
|||||||||||
|
Lepingu kehtivusaeg |
16. mai 2019 – 15. mai 2022 |
|||||||||||
|
Taotluste ja pakkumuste esitamise tähtaeg |
19. november 2018 |
|||||||||||
|
Aadress, millelt on võimalik saada hanketeate teksti ning avaliku hankemenetluse ja avaliku teenindamise kohustusega seotud mis tahes asjakohast teavet ja/või dokumente |
Kõik dokumendid on kättesaadavad aadressil: http://www.publiccontractsscotland.gov.uk Lisateave:
|
EUROOPA MAJANDUSPIIRKONDA KÄSITLEV TEAVE
EFTA riikide alaline komitee
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/13 |
Ohtlikud ained — EMP EFTA riikide 2017. aasta teisel poolaastal tehtud autoriseerimisotsuste nimekiri vastavalt määruse (EÜ) nr 1907/2006 (REACH) artikli 64 lõikele 8
(2018/C 305/11)
Kaupade vaba liikumise I allkomitee
Teadmiseks EMP ühiskomiteele
Vastavalt EMP ühiskomitee 14. märtsi 2008. aasta otsusele nr 25/2008 kutsutakse EMP ühiskomiteed 27. aprilli 2018. aasta koosolekul arvesse võtma järgmist ajavahemikul 1. juuli – 31. detsember 2017 määruse (EÜ) nr 1907/2006 (REACH) artikli 64 lõike 8 alusel tehtud autoriseerimisotsuste nimekirja:
LISA
Autoriseerimisotsuste nimekiri
Ajavahemikus 1. juulist kuni 31. detsembrini 2017 tehti EMP EFTA riikides vastavalt määruse (EÜ) nr 1907/2006 (REACH) artikli 64 lõikele 8 järgmised autoriseerimisotsused:
|
Aine nimetus |
Komisjoni otsus vastavalt määruse (EÜ) nr 1907/2006 artikli 64 lõikele 8 |
Riik |
Otsuse kuupäev |
|
Ammooniumdikromaat |
C(2017) 3237 |
Island |
7.7.2017 |
|
Naatriumdikromaat |
C(2017) 3453 |
Island |
7.7.2017 |
|
Naatriumdikromaat |
C(2017) 3764 |
Island |
7.7.2017 |
|
Naatriumdikromaat |
C(2017) 3765 |
Island |
7.7.2017 |
|
Naatriumdikromaat |
C(2017) 3801 |
Island |
7.7.2017 |
|
Naatriumdikromaat |
C(2017) 3806 |
Island |
7.7.2017 |
|
Naatriumdikromaat |
C(2017) 3816 |
Island |
7.7.2017 |
|
1,2-dikloroetaan |
C(2017) 3821 |
Island |
7.7.2017 |
|
Kaaliumdikromaat |
C(2017) 3910 |
Island |
7.7.2017 |
|
Kroomtrioksiid ja dikroomtris(kromaat) |
C(2017) 5001 |
Island |
5.10.2017 |
|
Kroomtrioksiid ja dikroomtris(kromaat) |
C(2017) 5001 |
Liechtenstein |
4.9.2017 |
|
Kroomtrioksiid ja dikroomtris(kromaat) |
C(2017) 5001 |
Norra |
18.8.2017 |
|
Bis(2-metoksüetüül)eeter (diglüüm) |
C(2017) 5025 |
Island |
5.10.2017 |
|
Bis(2-metoksüetüül)eeter (diglüüm) |
C(2017) 5025 |
Liechtenstein |
4.9.2017 |
|
Bis(2-metoksüetüül)eeter (diglüüm) |
C(2017) 5025 |
Norra |
18.8.2017 |
|
Pliikromaat |
C(2017) 5012 |
Island |
5.10.2017 |
|
Pliikromaat |
C(2017) 5012 |
Liechtenstein |
4.9.2017 |
|
Pliikromaat |
C(2017) 5012 |
Norra |
18.8.2017 |
|
Kroomtrioksiid |
C(2017) 5880 |
Island |
5.10.2017 |
|
Kroomtrioksiid |
C(2017) 5880 |
Liechtenstein |
20.9.2017 |
|
Kroomtrioksiid |
C(2017) 5880 |
Norra |
25.9.2017 |
|
Kroomtrioksiid |
C(2017) 6727 |
Island |
9.11.2017 |
|
Kroomtrioksiid |
C(2017) 6727 |
Liechtenstein |
25.10.2017 |
|
Kroomtrioksiid |
C(2017) 6727 |
Norra |
8.11.2017 |
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/15 |
Ravimid — EMP EFTA riikide poolt 2017. aasta teisel poolaastal antud müügilubade nimekiri
(2018/C 305/12)
Kaupade vaba liikumise I allkomitee
Teadmiseks EMP ühiskomiteele
Vastavalt EMP ühiskomitee 28. mai 1999. aasta otsusele nr 74/1999 kutsutakse EMP ühiskomiteed 23. märtsil 2018 toimuval koosolekul arvesse võtma järgmisi ajavahemiku 1. juuli – 31. detsember 2017 ravimite müügilubade nimekirju:
|
I lisa |
Uute müügilubade nimekiri |
|
II lisa |
Uuendatud müügilubade nimekiri |
|
III lisa |
Pikendatud müügilubade nimekiri |
|
IV lisa |
Tagasivõetud müügilubade nimekiri |
|
V lisa |
Peatatud müügilubade nimekiri |
I LISA
Uute müügilubade nimekiri
Ajavahemikul 1. juuli – 31. detsember 2017 anti EMP EFTA riikides välja järgmised müügiload:
|
ELi number |
Toode |
Riik |
Väljaandmise kuupäev |
|
EU/1/02/226 |
InductOs |
Island |
18.8.2017 |
|
EU/1/15/999 |
Zykadia (tingimusteta loaks muutmine) |
Liechtenstein |
31.8.2017 |
|
EU/1/16/1138 |
Venclyxto |
Liechtenstein |
31.12.2017 |
|
EU/1/16/1155 |
Kyntheum |
Island |
16.8.2017 |
|
EU/1/16/1155 |
Kyntheum |
Liechtenstein |
31.8.2017 |
|
EU/1/16/1155 |
Kyntheum |
Norra |
14.8.2017 |
|
EU/1/17/1179 |
Veltassa |
Island |
11.8.2017 |
|
EU/1/17/1179 |
Veltassa |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1179 |
Veltassa |
Norra |
9.8.2017 |
|
EU/1/17/1181 |
Spherox |
Island |
24.7.2017 |
|
EU/1/17/1181 |
Spherox |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1181 |
Spherox |
Norra |
13.9.2017 |
|
EU/1/17/1184 |
Riximyo |
Island |
11.7.2017 |
|
EU/1/17/1185 |
Rixathon |
Island |
11.7.2017 |
|
EU/1/17/1191 |
Dinutuximab beta Apeiron |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1194 |
Febuxostat Mylan |
Island |
11.7.2017 |
|
EU/1/17/1195 |
Erelzi |
Island |
14.7.2017 |
|
EU/1/17/1195 |
Erelzi |
Norra |
7.7.2017 |
|
EU/1/17/1196 |
Kevzara |
Island |
14.7.2017 |
|
EU/1/17/1196 |
Kevzara |
Norra |
5.7.2017 |
|
EU/1/17/1197 |
Oxervate |
Island |
24.7.2017 |
|
EU/1/17/1197 |
OXERVATE |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1197 |
OXERVATE |
Norra |
17.7.2017 |
|
EU/1/17/1199 |
Cuprior |
Island |
13.9.2017 |
|
EU/1/17/1199 |
Cuprior |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1199 |
Cuprior |
Norra |
13.9.2017 |
|
EU/1/17/1200 |
Besponsa |
Island |
24.7.2017 |
|
EU/1/17/1200 |
Besponsa |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1200 |
Besponsa |
Norra |
13.7.2017 |
|
EU/1/17/1201 |
Skilarence |
Island |
14.7.2017 |
|
EU/1/17/1201 |
Skilarence |
Norra |
7.7.2017 |
|
EU/1/17/1202 |
Ucedane |
Island |
12.7.2017 |
|
EU/1/17/1202 |
Ucedane |
Norra |
5.7.2017 |
|
EU/1/17/1203 |
Insulin lispro Sanofi |
Island |
11.8.2017 |
|
EU/1/17/1203 |
Insulin Lispro Sanofi |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1203 |
Insulin lispro Sanofi |
Norra |
18.8.2017 |
|
EU/1/17/1205 |
Blitzima |
Island |
9.8.2017 |
|
EU/1/17/1205 |
Blitzima |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1205 |
Blitzima |
Norra |
1.8.2017 |
|
EU/1/17/1206 |
Tuxella |
Island |
9.8.2017 |
|
EU/1/17/1206 |
Tuxella |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1206 |
Tuxella |
Norra |
1.8.2017 |
|
EU/1/17/1207 |
Ritemvia |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1207 |
Ritemvia |
Island |
10.8.2017 |
|
EU/1/17/1207 |
Ritemvia |
Norra |
1.8.2017 |
|
EU/1/17/1208 |
Trimbow |
Island |
11.8.2017 |
|
EU/1/17/1208 |
Trimbow |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1208 |
Trimbow |
Norra |
9.8.2017 |
|
EU/1/17/1209 |
Reagila |
Island |
9.8.2017 |
|
EU/1/17/1209 |
Reagila |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1209 |
Reaglia |
Norra |
9.8.2017 |
|
EU/1/17/1210 |
Efavirenz/Emtricitabin/Tenofovirdisproksil Zentiva |
Norra |
8.8.2017 |
|
EU/1/17/1210 |
Efavirenz/Emtricitabine/Tenofovir disoproxil Zentiva |
Island |
10.8.2017 |
|
EU/1/17/1210 |
Efavirenz/Emtricitabine/Tenofovir disoproxil Zentiva |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1211 |
Entecavir Accord |
Island |
5.10.2017 |
|
EU/1/17/1211 |
Entecavir Accord |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1211 |
Entecavir Accord |
Norra |
20.10.2017 |
|
EU/1/17/1212 |
Mavenclad |
Island |
13.9.2017 |
|
EU/1/17/1212 |
MAVENCLAD |
Norra |
30.8.2017 |
|
EU/1/17/1212 |
MAVENCLAD |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1213 |
Maviret |
Island |
17.8.2017 |
|
EU/1/17/1213 |
Maviret |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1213 |
Maviret |
Norra |
7.8.2017 |
|
EU/1/17/1214 |
Bavencio |
Island |
4.10.2017 |
|
EU/1/17/1214 |
Bavencio |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1214 |
Bavencio |
Norra |
25.9.2017 |
|
EU/1/17/1215 |
Fotivda |
Island |
13.9.2017 |
|
EU/1/17/1215 |
Fotivda |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1215 |
Fotivda |
Norra |
31.8.2017 |
|
EU/1/17/1216 |
Imraldi |
Island |
12.9.2017 |
|
EU/1/17/1216 |
Imraldi |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1216 |
Imraldi |
Norra |
11.9.2017 |
|
EU/1/17/1217 |
Nitisinone MendeliKABS |
Island |
19.9.2017 |
|
EU/1/17/1217 |
Nitisinone MendeliKABS |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1217 |
Nitisinone MendeliKABS |
Norra |
1.9.2017 |
|
EU/1/17/1218 |
Rydapt |
Island |
4.10.2017 |
|
EU/1/17/1218 |
Rydapt |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1218 |
Rydapt |
Norra |
25.9.2017 |
|
EU/1/17/1220 |
Tecentriq |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1220 |
Tecentriq |
Norra |
27.9.2017 |
|
EU/1/17/1220 |
Tecentriq |
Island |
5.10.2017 |
|
EU/1/17/1221 |
Kisqali |
Island |
12.9.2017 |
|
EU/1/17/1221 |
Kisqali |
Norra |
30.8.2017 |
|
EU/1/17/1221 |
Kisqali |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1222 |
Efavirenz/Emtricitabine/Tenofovir disoproxil Mylan |
Island |
8.11.2017 |
|
EU/1/17/1222 |
Efavirenz/Emtricitabine/Tenofovir disoproxil Mylan |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1222 |
Efavirenz/Emtricitabine/Tenofovir disoproxil Mylan |
Norra |
27.9.2017 |
|
EU/1/17/1223 |
Vosevi |
Island |
16.8.2017 |
|
EU/1/17/1223 |
Vosevi |
Liechtenstein |
31.8.2017 |
|
EU/1/17/1223 |
Vosevi |
Norra |
8.8.2017 |
|
EU/1/17/1224 |
Xermelo |
Island |
4.10.2017 |
|
EU/1/17/1224 |
Xermelo |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1224 |
Xermelo |
Norra |
3.10.2017 |
|
EU/1/17/1225 |
Symtuza |
Island |
5.10.2017 |
|
EU/1/17/1225 |
Symtuza |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1225 |
Symtuza |
Norra |
11.10.2017 |
|
EU/1/17/1226 |
Lutathera |
Island |
10.10.2017 |
|
EU/1/17/1226 |
Lutathera |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1226 |
Lutathera |
Norra |
3.10.2017 |
|
EU/1/17/1227 |
Entecavir Mylan |
Island |
4.10.2017 |
|
EU/1/17/1227 |
Entecavir Mylan |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1227 |
Entecavir Mylan |
Norra |
27.9.2017 |
|
EU/1/17/1228 |
Tookad |
Island |
29.11.2017 |
|
EU/1/17/1228 |
TOOKAD |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1228 |
TOOKAD |
Norra |
22.11.2017 |
|
EU/1/17/1229 |
Dupixent |
Island |
10.10.2017 |
|
EU/1/17/1229 |
Dupixent |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1229 |
Dupixent |
Norra |
10.10.2017 |
|
EU/1/17/1230 |
Lacosamide Accord |
Island |
5.10.2017 |
|
EU/1/17/1230 |
Lacosamide Accord |
Liechtenstein |
31.10.2017 |
|
EU/1/17/1230 |
Lacosamide Accord |
Norra |
27.9.2017 |
|
EU/1/17/1232 |
Miglustat Gen.Orph |
Island |
30.11.2017 |
|
EU/1/17/1232 |
Miglustat Gen.Orph |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1232 |
Miglustat Gen.Orph |
Norra |
27.11.2017 |
|
EU/1/17/1233 |
Zubsolv |
Island |
29.11.2017 |
|
EU/1/17/1233 |
Zubsolv |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1233 |
Zubsolv |
Norra |
22.11.2017 |
|
EU/1/17/1234 |
Tremfya |
Island |
4.12.2017 |
|
EU/1/17/1235 |
Zejula |
Island |
4.12.2017 |
|
EU/1/17/1235 |
Zejula |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1235 |
Zejula |
Norra |
27.11.2017 |
|
EU/1/17/1236 |
Trelegy Ellipta |
Island |
30.11.2017 |
|
EU/1/17/1236 |
Trelegy Ellipta |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1236 |
Trelegy Ellipta |
Norra |
22.11.2017 |
|
EU/1/17/1237 |
Elebrato Ellipta |
Island |
30.11.2017 |
|
EU/1/17/1237 |
Elebrato Ellipta |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1237 |
Elebrato Ellipta |
Norra |
27.11.2017 |
|
EU/1/17/1238 |
Nyxoid |
Island |
29.11.2017 |
|
EU/1/17/1238 |
Nyxoid |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1238 |
Nyxoid |
Norra |
27.11.2017 |
|
EU/1/17/1239 |
VeraSeal |
Island |
30.11.2017 |
|
EU/1/17/1239 |
VeraSeal |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1239 |
VeraSeal |
Norra |
1.12.2017 |
|
EU/1/17/1240 |
Cyltezo |
Island |
29.11.2017 |
|
EU/1/17/1240 |
Cyltezo |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1240 |
Cyltezo |
Norra |
1.12.2017 |
|
EU/1/17/1241 |
Ontruzant |
Island |
30.11.2017 |
|
EU/1/17/1241 |
Ontruzant |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1241 |
Ontruzant |
Norra |
27.11.2017 |
|
EU/1/17/1242 |
Ritonavir Mylan |
Island |
29.11.2017 |
|
EU/1/17/1242 |
Ritonavir Mylan |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1242 |
Ritonavir Mylan |
Norra |
22.11.2017 |
|
EU/1/17/1243 |
Imatinib Teva B.V. |
Island |
30.11.2017 |
|
EU/1/17/1243 |
Imatinib Teva B.V. |
Liechtenstein |
31.12.2017 |
|
EU/1/17/1243 |
Imatinib Teva B.V. |
Norra |
22.11.2017 |
|
EU/1/17/1244 |
Tacforius |
Liechtenstein |
31.12.2017 |
|
EU/2/16/197 |
CLYNAV |
Island |
13.7.2017 |
|
EU/2/16/197 |
CLYNAV |
Liechtenstein |
31.8.2017 |
|
EU/2/16/197 |
CLYNAV |
Norra |
18.7.2017 |
|
EU/2/17/211 |
Prevomax |
Island |
13.7.2017 |
|
EU/2/17/211 |
Prevomax |
Norra |
6.7.2017 |
|
EU/2/17/212 |
Exzolt |
Island |
30.8.2017 |
|
EU/2/17/212 |
Exzolt |
Liechtenstein |
31.10.2017 |
|
EU/2/17/212 |
Exzolt |
Norra |
15.9.2017 |
|
EU/2/17/213 |
Innovax-ND-IBD |
Island |
11.9.2017 |
|
EU/2/17/213 |
Innovax-ND-IBD |
Norra |
18.9.2017 |
|
EU/2/17/214 |
VEPURED |
Island |
12.9.2017 |
|
EU/2/17/214 |
VEPURED |
Norra |
15.9.2017 |
|
EU/2/17/215 |
Suvaxyn PRRS MLV |
Island |
11.9.2017 |
|
EU/2/17/215 |
Suvaxyn PRRS MLV |
Liechtenstein |
31.10.2017 |
|
EU/2/17/215 |
Suvaxyn PRRS MLV |
Norra |
18.9.2017 |
|
EU/2/17/217 |
Nobivac LeuFel |
Island |
9.11.2017 |
|
EU/2/17/217 |
Nobivac LeuFel |
Liechtenstein |
31.12.2017 |
|
EU/2/17/217 |
Nobivac LeuFel |
Norra |
14.11.2017 |
|
EU/2/17/218 |
Bovilis Blue-8 |
Island |
1.12.2017 |
|
EU/2/17/218 |
Bovilis Blue-8 |
Liechtenstein |
31.12.2017 |
|
EU/2/17/218 |
Bovilis Blue-8 |
Norra |
19.12.2017 |
II LISA
Uuendatud müügilubade nimekiri
Ajavahemikul 1. juuli – 31. detsember 2017 uuendati EMP EFTA riikides järgmisi müügilube:
|
ELi number |
Toode |
Riik |
Väljaandmise kuupäev |
|
EU/1/07/401 |
alli |
Island |
14.7.2017 |
|
EU/1/07/401 |
alli |
Liechtenstein |
31.8.2017 |
|
EU/1/07/401 |
alli |
Norra |
5.7.2017 |
|
EU/1/07/402 |
Increlex |
Island |
12.7.2017 |
|
EU/1/07/402 |
INCRELEX |
Norra |
5.7.2017 |
|
EU/1/07/403 |
Atriance |
Island |
11.7.2017 |
|
EU/1/07/416 |
Ecalta |
Island |
13.9.2017 |
|
EU/1/07/416 |
Ecalta |
Liechtenstein |
31.10.2017 |
|
EU/1/07/416 |
Ecalta |
Norra |
22.9.2017 |
|
EU/1/07/421 |
Glubrava |
Island |
30.11.2017 |
|
EU/1/07/421 |
Glubrava |
Liechtenstein |
31.12.2017 |
|
EU/1/07/421 |
Glubrava |
Norra |
22.11.2017 |
|
EU/1/07/424 |
Torisel |
Island |
24.7.2017 |
|
EU/1/07/424 |
Torisel |
Liechtenstein |
31.8.2017 |
|
EU/1/07/424 |
Torisel |
Norra |
1.8.2017 |
|
EU/1/08/446 |
Privigen |
Island |
4.12.2017 |
|
EU/1/08/446 |
Privigen |
Liechtenstein |
31.12.2017 |
|
EU/1/08/446 |
Privigen |
Norra |
5.12.2017 |
|
EU/1/08/453 |
Prepandrix |
Island |
4.12.2017 |
|
EU/1/08/453 |
Prepandrix |
Liechtenstein |
31.12.2017 |
|
EU/1/08/453 |
Prepandrix |
Norra |
5.12.2017 |
|
EU/1/12/784 |
Cuprymina |
Island |
11.8.2017 |
|
EU/1/12/784 |
Cuprymina |
Liechtenstein |
31.8.2017 |
|
EU/1/12/784 |
Cuprymina |
Norra |
9.8.2017 |
|
EU/1/12/787 |
Revestive |
Island |
13.7.2017 |
|
EU/1/12/787 |
Revestive |
Norra |
5.7.2017 |
|
EU/1/12/788 |
Seebri Breezhaler |
Island |
11.8.2017 |
|
EU/1/12/788 |
Seebri Breezhaler |
Liechtenstein |
31.8.2017 |
|
EU/1/12/788 |
Seebri Breezhaler |
Norra |
9.8.2017 |
|
EU/1/12/789 |
Enurev Breezhaler |
Island |
24.7.2017 |
|
EU/1/12/789 |
Enurev Breezhaler |
Liechtenstein |
31.8.2017 |
|
EU/1/12/789 |
Enurev Breezhaler |
Norra |
9.8.2017 |
|
EU/1/12/790 |
Tovanor Breezhaler |
Island |
14.8.2017 |
|
EU/1/12/790 |
Tovanor Breezhaler |
Liechtenstein |
31.8.2017 |
|
EU/1/12/790 |
Tovanor Breezhaler |
Norra |
9.8.2017 |
|
EU/1/12/794 |
Adcetris |
Island |
4.12.2017 |
|
EU/1/12/794 |
ADCETRIS |
Liechtenstein |
31.12.2017 |
|
EU/1/12/794 |
ADCETRIS |
Norra |
27.11.2017 |
|
EU/1/12/795 |
Forxiga |
Island |
13.9.2017 |
|
EU/1/12/795 |
Forxiga |
Liechtenstein |
31.10.2017 |
|
EU/1/12/795 |
Forxiga |
Norra |
27.9.2017 |
|
EU/1/12/796 |
Picato |
Island |
24.7.2017 |
|
EU/1/12/796 |
Picato |
Liechtenstein |
31.8.2017 |
|
EU/1/12/796 |
Picato |
Norra |
8.8.2017 |
|
EU/1/12/797 |
Eylea |
Island |
10.8.2017 |
|
EU/1/12/797 |
Eylea |
Liechtenstein |
31.8.2017 |
|
EU/1/12/797 |
Eylea |
Norra |
18.8.2017 |
|
EU/1/12/798 |
Ibandronic acid Accord |
Island |
6.10.2017 |
|
EU/1/12/798 |
Ibandronic acid Accord |
Liechtenstein |
31.10.2017 |
|
EU/1/12/798 |
Ibandronic acid Accord |
Norra |
27.9.2017 |
|
EU/1/12/799 |
Memantine Merz |
Island |
24.7.2017 |
|
EU/1/12/799 |
Memantine Merz |
Liechtenstein |
31.8.2017 |
|
EU/1/12/799 |
Memantine Merz |
Norra |
9.8.2017 |
|
EU/1/12/800 |
Zoledronic Acid Hospira |
Island |
11.9.2017 |
|
EU/1/12/800 |
Zoledronic acid Hospira |
Liechtenstein |
31.8.2017 |
|
EU/1/12/800 |
Zoledronsyre Hospira |
Norra |
4.9.2017 |
|
EU/1/12/801 |
Constella |
Island |
14.9.2017 |
|
EU/1/12/801 |
Constella |
Liechtenstein |
31.10.2017 |
|
EU/1/12/801 |
Constella |
Norra |
22.9.2017 |
|
EU/1/12/802 |
Capecitabine medac |
Island |
12.7.2017 |
|
EU/1/12/803 |
NexoBrid |
Island |
30.11.2017 |
|
EU/1/12/803 |
NexoBrid |
Liechtenstein |
31.12.2017 |
|
EU/1/12/803 |
NexoBrid |
Norra |
11.12.2017 |
|
EU/1/12/805 |
AMYViD |
Island |
9.10.2017 |
|
EU/1/12/805 |
Amyvid |
Liechtenstein |
31.10.2017 |
|
EU/1/12/805 |
Amyvid |
Norra |
3.10.2017 |
|
EU/1/12/806 |
Ryzodeg |
Island |
4.10.2017 |
|
EU/1/12/806 |
Ryzodeg |
Liechtenstein |
31.10.2017 |
|
EU/1/12/806 |
Ryzodeg |
Norra |
10.10.2017 |
|
EU/1/12/807 |
Tresiba |
Island |
9.10.2017 |
|
EU/1/12/807 |
Tresiba |
Liechtenstein |
31.10.2017 |
|
EU/1/12/807 |
Tresiba |
Norra |
10.10.2017 |
|
EU/1/12/808 |
Imatinib Teva |
Island |
9.10.2017 |
|
EU/1/12/808 |
Imatinib Teva |
Liechtenstein |
31.10.2017 |
|
EU/1/12/808 |
Imatinib Teva |
Norra |
27.9.2017 |
|
EU/1/12/809 |
Betmiga |
Island |
6.10.2017 |
|
EU/1/12/809 |
Betmiga |
Liechtenstein |
31.10.2017 |
|
EU/1/12/809 |
Betmiga |
Norra |
3.10.2017 |
|
EU/1/12/811 |
Lyxumia |
Island |
6.10.2017 |
|
EU/1/12/811 |
Lyxumia |
Liechtenstein |
31.10.2017 |
|
EU/1/12/811 |
Lyxumia |
Norra |
9.10.2017 |
|
EU/1/12/812 |
Bexsero |
Island |
9.10.2017 |
|
EU/1/12/812 |
Bexsero |
Liechtenstein |
31.10.2017 |
|
EU/1/12/812 |
Bexsero |
Norra |
3.10.2017 |
|
EU/1/12/814 |
Zaltrap |
Island |
9.10.2017 |
|
EU/1/12/814 |
ZALTRAP |
Liechtenstein |
31.10.2017 |
|
EU/1/12/814 |
ZALTRAP |
Norra |
27.9.2017 |
|
EU/1/12/815 |
Selincro |
Island |
30.11.2017 |
|
EU/1/12/815 |
Selincro |
Liechtenstein |
31.12.2017 |
|
EU/1/12/815 |
Selincro |
Norra |
1.12.2017 |
|
EU/1/13/813 |
Perjeta |
Island |
19.12.2017 |
|
EU/1/13/813 |
Perjeta |
Liechtenstein |
31.12.2017 |
|
EU/1/13/817 |
Actelsar HCT |
Liechtenstein |
31.12.2017 |
|
EU/1/13/819 |
JETREA |
Island |
15.12.2017 |
|
EU/1/13/819 |
JETREA |
Liechtenstein |
31.12.2017 |
|
EU/1/13/819 |
JETREA |
Norra |
19.12.2017 |
|
EU/1/13/902 |
Translarna |
Island |
12.7.2017 |
|
EU/1/13/902 |
Translarna |
Norra |
5.7.2017 |
|
EU/1/14/987 |
Holoclar |
Island |
19.12.2017 |
|
EU/1/16/1094 |
Ninlaro |
Island |
6.10.2017 |
|
EU/1/16/1094 |
Ninlaro |
Liechtenstein |
31.10.2017 |
|
EU/1/16/1094 |
Ninlaro |
Norra |
26.9.2017 |
|
EU/1/16/1121 |
Zalmoxis |
Island |
24.7.2017 |
|
EU/1/16/1121 |
Zalmoxis |
Liechtenstein |
31.8.2017 |
|
EU/1/16/1121 |
Zalmoxis |
Norra |
4.8.2017 |
|
EU/1/16/1138 |
Venclyxto |
Island |
6.11.2017 |
|
EU/1/16/1138 |
Venclyxto |
Norra |
14.11.2017 |
|
EU/1/16/1139 |
Ocaliva |
Island |
8.12.2017 |
|
EU/1/16/1139 |
OCALIVA |
Liechtenstein |
31.12.2017 |
|
EU/1/16/1139 |
OCALIVA |
Norra |
18.12.2017 |
|
EU/1/16/1143 |
Lartruvo |
Island |
6.10.2017 |
|
EU/1/16/1143 |
Lartruvo |
Liechtenstein |
31.10.2017 |
|
EU/1/16/1143 |
Lartruvo |
Norra |
27.9.2017 |
|
EU/1/16/1169 |
Alecensa |
Island |
8.12.2017 |
|
EU/1/16/1169 |
Alecensa |
Liechtenstein |
31.12.2017 |
|
EU/1/16/1169 |
Alecensa |
Norra |
15.12.2017 |
|
EU/1/43/890 |
Cometriq |
Norra |
3.8.2017 |
|
EU/2/12/142 |
Cardalis |
Island |
4.7.2017 |
|
EU/2/12/144 |
Contacera |
Island |
5.12.2017 |
|
EU/2/12/144 |
Contacera |
Liechtenstein |
31.12.2017 |
|
EU/2/12/144 |
Contacera |
Norra |
15.12.2017 |
|
EU/2/12/145 |
Kexxtone |
Liechtenstein |
31.12.2017 |
|
EU/2/12/145 |
Kexxtone |
Norra |
28.12.2017 |
|
EU/2/12/147 |
Pexion |
Island |
5.12.2017 |
|
EU/2/12/147 |
Pexion |
Liechtenstein |
31.12.2017 |
|
EU/2/12/147 |
Pexion |
Norra |
6.12.2017 |
III LISA
Pikendatud müügilubade nimekiri
Ajavahemikul 1. juuli – 31. detsember 2017 pikendati EMP EFTA riikides järgmisi müügilube:
|
ELi number |
Toode |
Riik |
Väljaandmise kuupäev |
|
EU/1/01/177/002 |
SonoVue |
Norra |
4.9.2017 |
|
EU/1/03/256/022 |
Humira |
Island |
19.12.2017 |
|
EU/1/03/256/022 |
Humira |
Norra |
10.11.2017 |
|
EU/1/04/292/013-015 |
Mimpara |
Island |
15.9.2017 |
|
EU/1/04/292/013-015 |
Mimpara |
Norra |
28.8.2017 |
|
EU/1/06/356/020-022 |
Exjade |
Norra |
28.11.2017 |
|
EU/1/06/356/020-022 |
Exjade |
Island |
1.12.2017 |
|
EU/1/07/418/011-013 |
Celsentri |
Norra |
3.8.2017 |
|
EU/1/07/418/011-013 |
Celsentri |
Island |
13.7.2017 |
|
EU/1/07/422/015 |
Tasigna |
Island |
4.12.2017 |
|
EU/1/07/422/015 |
Tasigna |
Norra |
28.11.2017 |
|
EU/1/07/436/006 |
Isentress |
Island |
9.8.2017 |
|
EU/1/07/436/006 |
Isentress |
Norra |
7.8.2017 |
|
EU/1/08/481/004-005 |
Kuvan |
Island |
10.8.2017 |
|
EU/1/08/481/004-005 |
Kuvan |
Norra |
13.7.2017 |
|
EU/1/09/522/003 |
ellaOne |
Island |
1.12.2017 |
|
EU/1/09/522/003 |
ellaOne |
Norra |
10.11.2017 |
|
EU/1/09/531/022-033 |
Instanyl |
Island |
6.11.2017 |
|
EU/1/09/539/005-006 |
Samsca |
Island |
5.10.2017 |
|
EU/1/09/539/005-006 |
Samsca |
Norra |
18.9.2017 |
|
EU/1/10/618 |
Prolia |
Norra |
27.9.2017 |
|
EU/1/11/703 |
Xgeva |
Norra |
27.9.2017 |
|
EU/1/12/753/018-019 |
Signifor |
Island |
4.10.2017 |
|
EU/1/12/753/018-019 |
Signifor |
Norra |
18.9.2017 |
|
EU/1/12/787/003 |
Revestive |
Norra |
5.7.2017 |
|
EU/1/12/787/003 |
Revestive |
Island |
13.7.2017 |
|
EU/1/13/846/002-003 |
Xtandi |
Norra |
3.10.2017 |
|
EU/1/13/846/002-003 |
Xtandi |
Island |
6.10.2017 |
|
EU/1/13/860/003 |
Nexium Control |
Island |
11.7.2017 |
|
EU/1/13/860/003 |
Nexium Control |
Norra |
5.7.2017 |
|
EU/1/15/1070/002 |
Oncaspar |
Island |
19.12.2017 |
IV LISA
Tagasivõetud müügilubade nimekiri
Ajavahemikul 1. juuli – 31. detsember 2017 võeti EMP EFTA riikides tagasi järgmised müügiload:
|
ELi number |
Toode |
Riik |
Tagasivõtmise kuupäev |
|
EU/1/00/167 |
Prevenar |
Liechtenstein |
31.12.2017 |
|
EU/1/00/167 |
Prevenar |
Norra |
11.12.2017 |
|
EU/1/00/167 |
Prevenar |
Island |
1.12.2017 |
|
EU/1/07/394 |
Optaflu |
Norra |
18.10.2017 |
|
EU/1/07/398 |
Optimark |
Island |
10.10.2017 |
|
EU/1/09/561 |
Clopidogrel Teva Pharma |
Island |
11.7.2017 |
|
EU/1/11/674 |
Repso |
Liechtenstein |
31.8.2017 |
|
EU/1/11/674 |
Repso |
Norra |
8.8.2017 |
|
EU/1/11/674 |
Repso |
Island |
10.8.2017 |
|
EU/1/13/868 |
EVARREST |
Liechtenstein |
31.12.2017 |
|
EU/1/13/868 |
EVARREST |
Norra |
28.11.2017 |
|
EU/1/13/868 |
EVARREST |
Island |
4.12.2017 |
|
EU/1/14/976 |
Zontivity |
Liechtenstein |
31.8.2017 |
|
EU/1/15/996 |
Ristempa |
Liechtenstein |
31.10.2017 |
|
EU/1/15/996 |
Ristempa |
Norra |
9.10.2017 |
|
EU/1/15/996 |
Ristempa |
Island |
9.10.2017 |
|
EU/1/16/1113 |
Enzepi |
Island |
11.8.2017 |
|
EU/1/16/1113 |
Enzepi |
Liechtenstein |
31.8.2017 |
|
EU/1/16/1113 |
Enzepi |
Norra |
8.8.2017 |
V LISA
Peatatud müügilubade nimekiri
Ajavahemikul 1. juuli – 31. detsember 2017 peatati EMP EFTA riikides järgmised müügiload:
|
ELi number |
Toode |
Riik |
Peatamise kuupäev |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V Teated
HALDUSMENETLUSED
Euroopa Personalivaliku Amet (EPSO)
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/34 |
TEADE AVALIKU KONKURSI KORRALDAMISE KOHTA
(2018/C 305/13)
Euroopa Personalivaliku Amet (EPSO) korraldab järgmise avaliku konkursi:
|
|
EPSO/AST-SC/07/18 – RELVASTATUD TURVA- JA KAITSETÖÖTAJAD (SC 1 / SC 2) |
Konkursiteade avaldatakse Euroopa Liidu Teataja 30. augusti 2018. aasta väljaandes C 305 A 24 keeles.
Lisateave on esitatud EPSO veebisaidil https://epso.europa.eu/
KONKURENTSIPOLIITIKA RAKENDAMISEGA SEOTUD MENETLUSED
Euroopa Komisjon
|
30.8.2018 |
ET |
Euroopa Liidu Teataja |
C 305/35 |
Eelteatis koondumise kohta
(juhtum M.9072 – KKR / Altice / SFR Filiale)
Võimalik lihtsustatud korras menetlemine
(EMPs kohaldatav tekst)
(2018/C 305/14)
1.
24. augustil 2018 sai Euroopa Komisjon nõukogu määruse (EÜ) nr 139/2004 (1) artiklile 4 vastava teatise kavandatava koondumise kohta.Teatis puudutab järgmisi ettevõtjaid:
|
— |
KKR & Co. Inc („KKR“) (Ameerika Ühendriigid), |
|
— |
Altice France S.A. („Altice“) (Prantsusmaa), mis kuulub gruppi Altice, |
|
— |
SFR Filiale SAS („SFR Filiale“), mille üle on valitsev mõju ettevõtjal Altice. |
KKR ja Altice omandavad SFR Filiale üle täieliku ühiskontrolli ühinemismääruse artikli 3 lõike 1 punkti b tähenduses.
Koondumine toimub aktsiate või osade ostu teel.
2.
Asjaomaste ettevõtjate majandustegevus hõlmab järgmist:— KKR: investeerimisühing, kes pakub varahaldusteenuseid ja finantsturulahendusi,
— Altice: telekommunikatsiooni-, sisu-, meedia-, meelelahutus- ja reklaamiteenused,
— SFR Filiale: Altice’i Prantsusmaal asuva tütarettevõtja SFR S.A. telekommunikatsioonimastidega seotud äritegevus.
3.
Komisjon leiab pärast teatise esialgset läbivaatamist, et tehing, millest teatatakse, võib kuuluda ühinemismääruse kohaldamisalasse, kuid lõplikku otsust selle kohta ei ole veel tehtud.Tuleb märkida, et käesoleva juhtumi puhul võib olla võimalik kasutada korda, mis on esitatud komisjoni teatises lihtsustatud korra kohta teatavate koondumiste menetlemiseks vastavalt nõukogu määrusele (EÜ) nr 139/2004 (2).
4.
Komisjon kutsub huvitatud kolmandaid isikuid esitama oma võimalikke märkusi kavandatava toimingu kohta.Komisjon peab märkused kätte saama kümne päeva jooksul pärast käesoleva dokumendi avaldamist. Märkuste juures tuleks alati kasutada järgmist viidet:
M.9072 – KKR / Altice / SFR Filiale
Märkusi võib saata komisjonile elektronposti, faksi või postiga. Kontaktandmed:
|
e-post: COMP-MERGER-REGISTRY@ec.europa.eu |
|
faks +32 22964301 |
|
postiaadress: |
|
European Commission |
|
Directorate-General for Competition |
|
Merger Registry |
|
1049 Bruxelles/Brussel |
|
BELGIQUE/BELGIË |
(1) ELT L 24, 29.1.2004, lk 1 („ühinemismäärus“).