ISSN 1977-0642
Amtsblatt
der Europäischen Union
L 379

Ausgabe in deutscher Sprache
Rechtsvorschriften
63. Jahrgang
13. November 2020
|
ISSN 1977-0642 |
||
|
Amtsblatt der Europäischen Union |
L 379 |
|

|
||
|
Ausgabe in deutscher Sprache |
Rechtsvorschriften |
63. Jahrgang |
|
|
|
|
|
(1) Text von Bedeutung für den EWR. |
|
DE |
Bei Rechtsakten, deren Titel in magerer Schrift gedruckt sind, handelt es sich um Rechtsakte der laufenden Verwaltung im Bereich der Agrarpolitik, die normalerweise nur eine begrenzte Geltungsdauer haben. Rechtsakte, deren Titel in fetter Schrift gedruckt sind und denen ein Sternchen vorangestellt ist, sind sonstige Rechtsakte. |
II Rechtsakte ohne Gesetzescharakter
VERORDNUNGEN
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/1 |
DELEGIERTE VERORDNUNG (EU) 2020/1676 DER KOMMISSION
vom 31. August 2020
zur Änderung von Artikel 25 der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen in Bezug auf nach Wunsch formulierte Anstrichfarbe
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen, zur Änderung und Aufhebung der Richtlinien 67/548/EWG und 1999/45/EG und zur Änderung der Verordnung (EG) Nr. 1907/2006 (1), insbesondere auf Artikel 53 Absatz 1,
in Erwägung nachstehender Gründe:
|
(1) |
Die Verordnung (EG) Nr. 1272/2008 wurde durch die Verordnung (EU) 2017/542 der Kommission (2) dahin gehend geändert, dass bestimmte Vorschriften zur Übermittlung von Informationen für die gesundheitliche Notversorgung und zur Aufnahme eines „eindeutigen Rezepturidentifikators“ (unique formula identifier — UFI) in die ergänzenden Informationen, die auf dem Kennzeichnungsetikett eines gefährlichen Gemischs angegeben sind, hinzugefügt wurden. Importeure und nachgeschaltete Anwender müssen die Anforderungen aber erst nach und nach erfüllen und dabei je nach Verwendungszweck, für den ein Gemisch in Verkehr gebracht wird, die jeweils geltenden Mitteilungstermine beachten. |
|
(2) |
Die Farbenbranche hat konkrete Bedenken hinsichtlich der Durchführbarkeit der Anforderungen geäußert, die hinsichtlich der gesundheitlichen Notversorgung im Falle von Farben gelten, deren Formulierung in begrenzten Mengen auf individuellen Wunsch für einen einzelnen Verbraucher oder gewerblichen Anwender in der Verkaufsstelle zusammengestellt wurde. Zur Deckung der Nachfrage von Kunden nach sehr spezifischen Farbtönen können Formulierer beauftragt werden, Farben mit einer nahezu unbegrenzten Anzahl unterschiedlicher Zusammensetzungen zu formulieren und zu liefern. Die Einhaltung der Anforderungen bezüglich der gesundheitlichen Notversorgung würde es somit erforderlich machen, dass die Formulierer entweder im Voraus Informationen übermitteln und UFI für eine extrem hohe Zahl von Farben unterschiedlichster Farbkombinationen erstellen, von denen viele möglicherweise in Wirklichkeit nie geliefert werden, oder ansonsten jede Lieferung in der Verkaufsstelle aufschieben, bis die Informationen vorgelegt und die UFI erstellt worden sind. Beide Ansätze würden für die Hersteller von nach Wunsch formulierter Anstrichfarbe einen unverhältnismäßigen Aufwand bedeuten. |
|
(3) |
Um insbesondere für kleine und mittlere Unternehmen unverhältnismäßigen Verwaltungsaufwand in Bezug auf nach Wunsch formulierten Anstrichfarbe zu vermeiden, müssen die Anforderungen durch die Delegierte Verordnung (EU) 2020/1677 der Kommission (3) geändert werden, damit für nach Wunsch formulierte Anstrichfarbe die Möglichkeit einer Ausnahme von den Mitteilungspflichten gemäß Anhang VIII der Verordnung (EG) Nr. 1272/2008 und der Pflicht zur Erstellung eines UFI gemäß diesem Anhang vorgesehen wird. Damit jedoch in einem solchen Fall Giftnotrufzentralen eine geeignete gesundheitliche Notversorgung vornehmen können, müssen für die in nach Wunsch formulierter Anstrichfarbe enthaltenen einzelnen Gemische weiterhin alle Anforderungen des Anhangs VIII gelten. |
|
(4) |
In Anbetracht dessen ist es angezeigt, Artikel 25 der Verordnung (EG) Nr. 1272/2008 dahin gehend zu ändern, dass für nach Wunsch formulierte Anstrichfarbe, für die keine Informationen übermittelt werden und kein entsprechender UFI erstellt wird, eine Vorschrift festgelegt wird, wonach die UFI aller in der nach Wunsch formulierten Anstrichfarbe enthaltenen Gemische auf dem Etikett der nach Wunsch formulierten Anstrichfarbe anzugeben sind. Beträgt die Konzentration eines Gemisches mit einem UFI in der nach Wunsch formulierten Anstrichfarbe mehr als 5 %, sollte zudem die Konzentration in die ergänzenden Informationen auf dem Etikett der nach Wunsch formulierten Anstrichfarbe aufgenommen werden, da Gemische in nach Wunsch formulierter Anstrichfarbe mit einer solchen Konzentration eher für die gesundheitliche Notversorgung relevant sind. |
|
(5) |
In Anbetracht der Tatsache, dass das in Anhang VIII der Verordnung (EG) Nr. 1272/2008 für Gemische zur Verwendung durch Verbraucher und zur gewerblichen Verwendung auf den 1. Januar 2021 festgesetzte Einhaltungsdatum näher rückt und dass alle Sektoren durch die vorliegende Verordnung in die Lage versetzt werden, die Bestimmungen jenes Anhangs einzuhalten, sollte Letztere so früh wie möglich in Kraft treten. |
|
(6) |
Die Verordnung (EG) Nr. 1272/2008 sollte daher entsprechend geändert werden — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
In Artikel 25 der Verordnung (EG) Nr. 1272/2008 wird folgender Absatz angefügt:
„(8) Im Fall einer nach Wunsch formulierten Anstrichfarbe, für die keine Vorlage gemäß Anhang VIII erfolgt ist und kein entsprechender eindeutiger Rezepturidentifikator erstellt wurde, werden die eindeutigen Rezepturidentifikatoren aller in der nach Wunsch formulierten Anstrichfarbe enthaltenen Gemische mit einer Konzentration von mehr als 0,1 %, für die ihrerseits eine Mitteilung gemäß Artikel 45 einzureichen ist, in die ergänzenden Informationen auf dem Etikett der nach Wunsch formulierten Anstrichfarbe aufgenommen, die zusammen in absteigender Reihenfolge der Konzentration der Gemische in der nach Wunsch formulierten Anstrichfarbe gemäß Anhang VIII Teil A Abschnitt 5 aufgeführt sind.
Sofern in einem von Unterabsatz 1 erfassten Fall die Konzentration eines Gemisches mit einem eindeutigen Rezepturidentifikator in der nach Wunsch formulierten Anstrichfarbe mehr als 5 % beträgt, wird die Konzentration dieses Gemisches auch in die ergänzenden Informationen auf dem Etikett der nach Wunsch formulierten Anstrichfarbe neben ihrem eindeutigen Rezepturidentifikator gemäß Anhang VIII Teil B Abschnitt 3.4 aufgenommen.
Für die Zwecke dieses Absatzes bezeichnet ‚auf Wunsch formulierte Anstrichfarbe‘ eine Farbe, die in begrenzten Mengen auf individuellen Wunsch für einen einzelnen Verbraucher oder gewerblichen Anwender in der Verkaufsstelle durch Abtönen oder Farbmischen formuliert wird.“
Artikel 2
Diese Verordnung tritt am Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in allen Mitgliedstaaten.
Brüssel, den 31. August 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 353 vom 31.12.2008, S. 1.
(2) Verordnung (EU) 2017/542 der Kommission vom 22. März 2017 zur Änderung der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen durch Hinzufügung eines Anhangs über die harmonisierten Informationen für die gesundheitliche Notversorgung (ABl. L 78 vom 23.3.2017, S. 1).
(3) Delegierte Verordnung (EU) 2020/1677 der Kommission vom 31. August 2020 zur Änderung der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen zwecks Verbesserung der Praktikabilität der Informationsanforderungen im Zusammenhang mit der gesundheitlichen Notversorgung (siehe Seite 3 dieses Amtsblatts).
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/3 |
DELEGIERTE VERORDNUNG (EU) 2020/1677 DER KOMMISSION
vom 31. August 2020
zur Änderung der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen zwecks Verbesserung der Praktikabilität der Informationsanforderungen im Zusammenhang mit der gesundheitlichen Notversorgung
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen, zur Änderung und Aufhebung der Richtlinien 67/548/EWG und 1999/45/EG und zur Änderung der Verordnung (EG) Nr. 1907/2006 (1), insbesondere auf Artikel 45 Absatz 4,
in Erwägung nachstehender Gründe:
|
(1) |
Die Verordnung (EG) Nr. 1272/2008 wurde durch die Verordnung (EU) 2017/542 der Kommission (2) dahin gehend geändert, dass bestimmte Vorschriften über die Übermittlung von Informationen für die gesundheitliche Notversorgung und über die Aufnahme eines „eindeutigen Rezepturidentifikators“ in die ergänzenden Informationen, die auf dem Kennzeichnungsetikett eines gefährlichen Gemischs angegeben sind, hinzugefügt wurden. Diese Anforderungen wurden durch die Delegierte Verordnung (EU) 2020/11 der Kommission (3) geändert. Importeure und nachgeschaltete Anwender müssen die neuen Vorschriften nach und nach erfüllen und dabei je nach Verwendungszweck, für den ein Gemisch in Verkehr gebracht wird, die jeweils geltenden Mitteilungstermine beachten. |
|
(2) |
Verschiedene Industriesektoren haben Bedenken hinsichtlich der Praktikabilität der Informationsanforderungen im Zusammenhang mit der gesundheitlichen Notversorgung in bestimmten Fällen geäußert, insbesondere im Hinblick auf die Schwierigkeit, die genaue Zusammensetzung von Gemischen zu kennen, wenn Rohstoffe mit sehr variabler oder unbekannter Zusammensetzung bei der Herstellung des Gemischs verwendet werden, wenn von mehreren verschiedenen Lieferanten gelieferte, toxikologisch sehr ähnliche Bestandteile zusammen in derselben Produktionslinie verwendet werden oder wenn komplexe Lieferketten beteiligt sind. Im Falle nach Wunsch gefertigter Gemische wurden auch Bedenken geäußert, dass es nicht möglich sei, im Voraus die genaue Zusammensetzung der einzelnen nach Wunsch gefertigten, in Verkehr gebrachten Gemische zu kennen. |
|
(3) |
Es muss auf die Fälle eingegangen werden, in denen unterschiedliche, aber toxikologisch sehr ähnliche Bestandteile in einem Gemisch verwendet werden und nicht bekannt ist, welcher Bestandteil in einem gegebenen, zu einem bestimmten Zeitpunkt in Verkehr gebrachten Gemisch vorhanden ist. Um sicherzustellen, dass die Anforderungen an die gesundheitliche Notversorgung in der Praxis ordnungsgemäß erfüllt werden können, sollte es Importeuren und nachgeschalteten Anwendern gestattet sein, toxikologisch ähnliche Bestandteile eines Gemisches in einer Gruppe austauschbarer Bestandteile zusammenzufassen und Informationen über die Gesamtkonzentration dieser Bestandteile in dem Gemisch vorzulegen, ohne dass ihre Konzentrationen im Einzelnen angegeben werden müssen. Damit Giftnotrufzentralen eine geeignete gesundheitliche Notfallreaktion formulieren können, sollten Bestandteile nur dann in einer Gruppe austauschbarer Bestandteile zusammengefasst werden, wenn ihre Einstufung in Bezug auf gesundheitliche und physikalische Wirkungen identisch ist und wenn die Gefahrenidentifizierung und die zusätzlichen Gefahreninformationen für alle möglichen Kombinationen des endgültigen Gemisches, das diese Bestandteile enthält, identisch sind. Bei Bestandteilen, die in bestimmte Gefahrenklassen eingestuft sind, sollten sie dieselbe technische Funktion und dieselben toxikologischen Eigenschaften aufweisen, um in einer Gruppe zusammengefasst werden zu können. |
|
(4) |
Um besonderen Schwierigkeiten in den Sektoren Gips, Fertigbeton und Zement Rechnung zu tragen und die Einhaltung der Anforderungen zu ermöglichen, ohne das Sicherheitsniveau zu mindern, sollte es möglich sein, dass Informationen im Zusammenhang mit der gesundheitlichen Notversorgung, die sich auf bestimmte standardisierte Gemische in diesen drei Sektoren beziehen, durch einen Verweis auf eine Standardzusammensetzung übermittelt werden. Damit Giftnotrufzentralen jedoch geeignete Maßnahmen der gesundheitlichen Notversorgung festlegen können, sollte diese Option nur in den Fällen zur Verfügung stehen, in denen sich die Einstufung des Gemisches in Abhängigkeit von der Zusammensetzung des Gemisches innerhalb der in der Standardrezeptur angegebenen Konzentrationsbereiche nicht ändert und die Angaben zur Zusammensetzung mindestens so detailliert sind wie die Angaben in dem gemäß Artikel 31 der Verordnung (EG) Nr. 1907/2006 des Europäischen Parlaments und des Rates (4) erstellten Sicherheitsdatenblatt für das Gemisch (im Folgenden „Sicherheitsdatenblatt“). Für den Fall, dass die Angaben im Sicherheitsdatenblatt detaillierter sind als die Angaben zur Zusammensetzung in der Standardrezeptur, sollten Importeure und nachgeschaltete Anwender verpflichtet werden, die Informationen stattdessen im Sicherheitsdatenblatt mitzuteilen. |
|
(5) |
Um besonderen Schwierigkeiten Rechnung zu tragen, die bei bestimmten Kraftstoffen zu erwarten sind, und angesichts der Tatsache, dass die in Verkehr gebrachten Kraftstoffe in der Regel einer technischen Norm entsprechen und Giftnotrufzentralen eine geringe Zahl von Vergiftungsfällen im Zusammenhang mit Kraftstoffen gemeldet haben, sollte es möglich sein, bis eine geeignetere Lösung gefunden ist, Informationen zur gesundheitlichen Notversorgung unter Bezugnahme auf die im Sicherheitsdatenblatt enthaltenen Informationen sowie alle anderen bekannten Informationen über die chemische Zusammensetzung der Produkte vorzulegen. |
|
(6) |
Um die Nachfrage der Kunden nach sehr spezifischen Farbtönungen zu befriedigen, werden die Formulierer manchmal aufgefordert, am Verkaufsort nach Wunsch formulierte Anstrichfarbe zu formulieren und bereitzustellen. Diese nach Wunsch formulierte Anstrichfarbe kann möglicherweise eine nahezu unbegrenzte Anzahl unterschiedlicher Zusammensetzungen aufweisen. Daher würde die Einhaltung der Anforderungen an gesundheitliche Notversorgung gemäß Anhang VIII der Verordnung (EG) Nr. 1272/2008 ohne Abhilfemaßnahmen erfordern, dass die Formulierer nach Wunsch formulierter Anstrichfarbe entweder im Voraus Informationen übermitteln und eindeutige Rezepturidentifikatoren (Unique Formula Identifiers — UFI) für eine extrem große Anzahl von Anstrichfarben aller möglichen Farbkombinationen erstellen, von denen viele möglicherweise nie tatsächlich geliefert werden, oder jede Lieferung aufschieben müssten, bis die Informationen vorgelegt und die UFI generiert worden sind. Beide Ansätze würden die Branche der nach Wunsch formulierten Anstrichfarbe, insbesondere kleine und mittlere Unternehmen, unverhältnismäßig belasten, ohne das Sicherheitsniveau erheblich zu verbessern. |
|
(7) |
Giftnotrufzentralen haben keine signifikante Zahl von Unfällen im Zusammenhang mit Anstrichmitteln gemeldet. Angesichts der im Vergleich zu anderen Gemischen scheinbar geringeren Risiken ist es gerechtfertigt, hier einen flexibleren Ansatz zuzulassen, da dadurch das derzeitige Sicherheitsniveau nicht gesenkt würde. |
|
(8) |
Es ist daher angemessen, eine Möglichkeit vorzusehen, nach Wunsch formulierte Anstrichfarbe von den Mitteilungspflichten in Anhang VIII und von der Pflicht zur Erstellung eines UFI auszunehmen. In diesem Fall sollten jedoch die einzelnen in der nach Wunsch formulierter Anstrichfarbe enthaltenen Gemische weiterhin allen Anforderungen dieses Anhangs unterliegen, damit die Giftnotrufzentralen geeignete Maßnahmen der gesundheitlichen Notversorgung einleiten können. Über die vorliegende Verordnung hinaus wird mit der Delegierten Verordnung (EU) 2020/1676 der Kommission (5) auch Artikel 25 der Verordnung (EG) Nr. 1272/2008 dahin gehend geändert, dass eine neue Vorschrift für nach Wunsch formulierte Anstrichfarbe hinzugefügt wird, für die keine Mitteilung gemäß Anhang VIII erfolgt und kein entsprechender UFI erstellt wurde, wonach die UFI aller in der nach Wunsch formulierten Anstrichfarbe enthaltenen einzelnen Gemische anzugeben sind, einschließlich der Angaben zur spezifischen Konzentration der einzelnen Gemische bei einem UFI in einer Konzentration von mehr als 5 %. |
|
(9) |
Angesichts der Anzahl der Änderungen des Anhangs VIII der Verordnung (EG) Nr. 1272/2008 ist es aus Gründen der Rechtsklarheit angezeigt, den gesamten Anhang zu ersetzen. |
|
(10) |
In Anbetracht der Tatsache, dass das in Anhang VIII der Verordnung (EG) Nr. 1272/2008 für Gemische zur Verwendung durch Verbraucher und zur gewerblichen Verwendung auf den 1. Januar 2021 festgesetzte Einhaltungsdatum näher rückt und dass alle Sektoren durch die vorliegende Verordnung in die Lage versetzt werden, die Bestimmungen jenes Anhangs einzuhalten, sollte letztere so früh wie möglich in Kraft treten. |
|
(11) |
Die Verordnung (EG) Nr. 1272/2008 sollte daher entsprechend geändert werden — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Anhang VIII der Verordnung (EG) Nr. 1272/2008 erhält die Fassung des Anhangs der vorliegenden Verordnung.
Artikel 2
Diese Verordnung tritt am Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 31. August 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 353 vom 31.12.2008, S. 1.
(2) Verordnung (EU) 2017/542 der Kommission vom 22. März 2017 zur Änderung der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen durch Hinzufügung eines Anhangs über die harmonisierten Informationen für die gesundheitliche Notversorgung (ABl. L 78 vom 23.3.2017, S. 1).
(3) Delegierte Verordnung (EU) 2020/11 der Kommission vom 29. Oktober 2019 zur Änderung der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen in Bezug auf Informationen für die gesundheitliche Notversorgung (ABl. L 6 vom 10.1.2020, S. 8).
(4) Verordnung (EG) Nr. 1907/2006 des Europäischen Parlaments und des Rates vom 18. Dezember 2006 zur Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe (REACH), zur Schaffung einer Europäischen Agentur für chemische Stoffe, zur Änderung der Richtlinie 1999/45/EG und zur Aufhebung der Verordnung (EWG) Nr. 793/93 des Rates, der Verordnung (EG) Nr. 1488/94 der Kommission, der Richtlinie 76/769/EWG des Rates sowie der Richtlinien 91/155/EWG, 93/67/EWG, 93/105/EG und 2000/21/EG der Kommission (ABl. L 396 vom 30.12.2006, S. 1).
(5) Delegierte Verordnung (EU) 2020/1676 der Kommission vom 31. August 2020 zur Änderung von Artikel 25 der Verordnung (EG) Nr. 1272/2008 des Europäischen Parlaments und des Rates über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen in Bezug auf nach Wunsch formulierte Anstrichfarbe (siehe Seite 1 dieses Amtsblatts).
ANHANG
„ANHANG VIII
HARMONISIERTE INFORMATIONEN FÜR DIE GESUNDHEITLICHE NOTVERSORGUNG UND FÜR VORBEUGENDE MAßNAHMEN
TEIL A
ALLGEMEINE ANFORDERUNGEN
1. ANWENDUNG
|
1.1. |
Importeure und nachgeschaltete Anwender, die Gemische zur Verwendung durch Verbraucher im Sinne des Teils A Abschnitt 2.4 dieses Anhangs in Verkehr bringen, sind ab dem 1. Januar 2021 zur Einhaltung dieses Anhangs verpflichtet. |
|
1.2. |
Importeure und nachgeschaltete Anwender, die Gemische zur gewerblichen Verwendung im Sinne des Teils A Abschnitt 2.4 dieses Anhangs in Verkehr bringen, sind ab dem 1. Januar 2021 zur Einhaltung dieses Anhangs verpflichtet. |
|
1.3. |
Importeure und nachgeschaltete Anwender, die Gemische zur industriellen Verwendung oder Gemische, deren endgültige Verwendung nicht der Mitteilungspflicht im Sinne des Teils A Abschnitt 2.4 dieses Anhangs unterliegen, in Verkehr bringen, sind ab dem 1. Januar 2024 zur Einhaltung dieses Anhangs verpflichtet. |
|
1.4. |
Importeure und nachgeschaltete Anwender, die vor den in den Abschnitten 1.1, 1.2 und 1.3 genannten Anwendbarkeitsterminen einer nach Artikel 45 Absatz 1 benannten Stelle Informationen über gefährliche Gemische übermittelt haben, welche diesem Anhang nicht entsprechen, sind für diese Gemische bis zum 1. Januar 2025 nicht zur Einhaltung dieses Anhangs verpflichtet. |
|
1.5. |
Abweichend von Abschnitt 1.4 müssen Importeure und nachgeschaltete Anwender diesen Anhang einhalten, falls vor dem 1. Januar 2025 eine der in Teil B Abschnitt 4.1 dieses Anhangs beschriebenen Veränderungen eintritt, bevor sie dieses veränderte Gemisch in Verkehr bringen. |
2. ZWECK, GELTUNGSBEREICH UND BEGRIFFSBESTIMMUNGEN
|
2.1. |
Dieser Anhang umfasst die Anforderungen, die Importeure und nachgeschaltete Anwender, die Gemische in Verkehr bringen (im Folgenden ‚Mitteilungspflichtige“) in Bezug auf die Übermittlung von Informationen erfüllen müssen, sodass den benannten Stellen sämtliche Informationen vorliegen, die sie zur Erfüllung der Aufgaben benötigen, für die sie gemäß Artikel 45 zuständig sind. |
|
2.2. |
Dieser Anhang gilt nicht für Gemische für die wissenschaftliche Forschung und Entwicklung und für Gemische für produkt- und verfahrensorientierte Forschung und Entwicklung im Sinne des Artikels 3 Absatz 22 der Verordnung (EG) Nr. 1907/2006.
Dieser Anhang gilt nicht für Gemische, die nur in eine oder mehrere der folgenden Gefahrenkategorien eingestuft sind:
|
|
2.2a. |
Bei nach Wunsch formulierter Anstrichfarbe können sich die Mitteilungspflichtigen unbeschadet des Artikels 25 Absatz 8 dafür entscheiden, keine Informationen vorzulegen und keinen eindeutigen Rezepturidentifikator gemäß diesem Anhang zu erstellen. |
|
2.3. |
Im Fall von Gemischen, deren endgültige Verwendung nicht der Mitteilungspflicht unterliegt, bzw. von Gemischen, die nur zur industriellen Verwendung in Verkehr gebracht werden, können sich die Mitteilungspflichtigen — als Alternative zu den allgemeinen Anforderungen an eine Mitteilung — gemäß Teil B Abschnitt 3.1 für eine verkürzte Mitteilung entscheiden, sofern ein schneller Zugriff auf zusätzliche detaillierte Produktinformationen gemäß Abschnitt 1.3 dieses Teils gewährleistet ist. |
|
2.4. |
Für die Zwecke dieses Anhangs bezeichnet der Begriff:
|
3. ANFORDERUNGEN AN DIE MITTEILUNG
|
3.1. |
Vor dem Inverkehrbringen legen die Mitteilungspflichtigen in dem Mitgliedstaat oder den Mitgliedstaaten, in denen das Gemisch in Verkehr gebracht wird, den Stellen, die gemäß Artikel 45 Absatz 1 benannt wurden (im Folgenden „benannte Stellen“), Informationen zu jenen Gemischen vor, die aufgrund ihrer gesundheitlichen oder physikalischen Wirkungen als gefährlich eingestuft wurden.
Die Mitteilung enthält die nach Teil B verlangten Informationen. Sie wird elektronisch in dem von der Agentur kostenlos bereitgestellten XML-Format übermittelt. |
|
3.2. |
Fordert nach Eingang einer Mitteilung gemäß Abschnitt 3.1 eine benannte Stelle den Mitteilungspflichtigen unter Angabe der Gründe zur Übermittlung zusätzlicher Informationen oder zur Klärung auf, damit die benannte Stelle die Aufgaben wahrnehmen kann, für die sie gemäß Artikel 45 zuständig ist, hat der Mitteilungspflichtige diese angeforderten erforderlichen Informationen oder Klärungen unverzüglich zu liefern. |
|
3.3. |
Die Mitteilung erfolgt in den Amtssprachen der Mitgliedstaaten, in denen das Gemisch in Verkehr gebracht wird, sofern die betroffenen Mitgliedstaaten nicht etwas anderes bestimmen. |
|
3.4. |
Die bestimmungsgemäße Verwendung des Gemischs wird gemäß einem von der Agentur zur Verfügung gestellten einheitlichen Produktkategorisierungssystem beschrieben. |
|
3.5. |
Treten die Bedingungen nach Teil B Abschnitt 4.1 ein, ist unverzüglich eine Aktualisierung der Mitteilung einzureichen. |
4. GRUPPENMITTEILUNG
|
4.1. |
Für mehr als ein Gemisch kann eine einzige Mitteilung (im Folgenden „Gruppenmitteilung“) eingereicht werden, wenn alle Gemische einer Gruppe im Hinblick auf Gesundheitsgefahren und physikalische Gefahren dieselbe Einstufung aufweisen. |
|
4.2. |
Eine Gruppenmitteilung ist nur unter den folgenden Voraussetzungen zulässig: Alle Gemische der Gruppe enthalten die gleichen (nach Teil B Abschnitt 3.2 identifizierten) Bestandteile, und der mitgeteilte Konzentrationsbereich (nach Teil B Abschnitt 3.4) jedes Bestandteils ist für alle Gemische gleich. |
|
4.3. |
Abweichend von Abschnitt 4.2 ist eine Gruppenmitteilung auch dann zulässig, wenn die Unterschiede in der Zusammensetzung zwischen den verschiedenen Gemischen in der Gruppe nur Parfümstoffe betreffen, wobei jedoch der Gesamtanteil der sich unterscheidenden Parfümstoffe in jedem Gemisch nicht mehr als 5 % betragen darf. |
|
4.4. |
Im Falle einer Gruppenmitteilung müssen die in Teil B verlangten Informationen gegebenenfalls für jedes in der Gruppenmitteilung enthaltene Gemisch vorgelegt werden. |
5. EINDEUTIGER REZEPTURIDENTIFIKATOR (UNIQUE FORMULA IDENTIFIER — UFI)
|
5.1. |
Der Mitteilungspflichtige erstellt mit den von der Agentur zur Verfügung gestellten elektronischen Mitteln einen eindeutigen Rezepturidentifikator (Unique Formula Identifier, im Folgenden „UFI“). Bei dem UFI handelt es sich um einen eindeutigen alphanumerischen Code, der die eingereichten Informationen über die Zusammensetzung des Gemischs oder einer Gruppe von Gemischen zweifelsfrei einem spezifischen Gemisch oder einer spezifischen Gruppe von Gemischen zuordnet. Die Zuteilung eines UFI ist unentgeltlich.
Erfüllt eine Veränderung der Zusammensetzung des Gemischs oder der Gruppe von Gemischen eine oder mehrere der Bedingungen nach Teil B Abschnitt 4.1 vierter Gedankenstrich Buchstaben a, b und c, oder gegebenenfalls einer der Bedingungen gemäß dem zweiten Unterabsatz dieses Abschnitts, muss ein neuer UFI erstellt werden. Abweichend von Unterabsatz 2 dieses Abschnitts ist für Gemische in einer Gruppenmitteilung, die Parfümstoffe enthalten, kein neuer UFI erforderlich, sofern die Veränderung der Zusammensetzung lediglich diese Parfümstoffe oder die Zugabe neuer Parfümstoffe betrifft. Abweichend von Unterabsatz 2 dieses Abschnitts ist kein neuer UFI erforderlich, sofern die Veränderung, die die Bedingung nach Teil B Abschnitt 4.1 vierter Gedankenstrich Buchstabe a erfüllt, lediglich einen oder mehrere Bestandteile betrifft, der (die) bereits in einer Gruppe austauschbarer Bestandteile enthalten ist (sind), sofern die Gruppe austauschbarer Bestandteile bereits gemäß Teil B Abschnitt 3.5 in der Mitteilung angegeben ist. |
|
5.2. |
Dem UFI geht das Akronym „UFI“ in Großbuchstaben voraus, gefolgt von einem Doppelpunkt („UFI:“), und er ist deutlich sichtbar, lesbar und unverwischbar angebracht. |
|
5.3. |
Der Mitteilungspflichtige kann sich dafür entscheiden, den UFI nicht in die ergänzenden Informationen auf dem Kennzeichnungsetikett aufzunehmen, sondern ihn stattdessen auf der inneren Verpackung zusammen mit den anderen Kennzeichnungselementen aufzudrucken oder anzubringen.
Der Mitteilungspflichtige kann in Fällen, in denen die innere Verpackung entweder so beschaffen oder derart klein ist, dass der UFI darauf nicht angebracht werden kann, ihn zusammen mit den anderen Kennzeichnungselementen auf einer äußeren Verpackung aufdrucken oder anbringen. Im Fall von Gemischen, die nicht verpackt werden, wird der UFI im Sicherheitsdatenblatt angegeben oder gegebenenfalls in die Kopie der Kennzeichnungselemente gemäß Artikel 29 Absatz 3 aufgenommen. Bei den zur Verwendung in industriellen Anlagen gelieferten Gemischen kann sich der Mitteilungspflichtige dafür entscheiden, den UFI anstatt auf dem Kennzeichnungsetikett oder auf der Verpackung im Sicherheitsdatenblatt anzugeben. |
6. FORMATE UND TECHNISCHE UNTERSTÜTZUNG FÜR DIE ÜBERMITTLUNG DER INFORMATIONEN
|
6.1. |
Die Agentur spezifiziert, pflegt und aktualisiert den UFI-Generator, die XML-Formate für die Mitteilungen und ein einheitliches Produktkategorisierungssystem und stellt diese auf ihrer Website unentgeltlich zur Verfügung. |
|
6.2. |
Die Agentur stellt technische und wissenschaftliche Anleitung, technische Unterstützung und Instrumente zur Verfügung, um die Übermittlung der Informationen zu ermöglichen. |
TEIL B
IN EINER MITTEILUNG ENTHALTENE INFORMATIONEN
1. IDENTIFIZIERUNG DES GEMISCHS UND DES MITTEILUNGSPFLICHTIGEN
1.1. Produktidentifikator des Gemischs
Der Produktidentifikator wird gemäß Artikel 18 Absatz 3 Buchstabe a angegeben.
Der vollständige Handelsname bzw. die vollständigen Handelsnamen des Gemischs werden angegeben, einschließlich — falls relevant — des Markennamens/der Markennamen, des Namens des Produkts und abweichender Namen, die auf dem Kennzeichnungsetikett erscheinen, ohne Abkürzungen und in einer Form, die eine konkrete Identifizierung ermöglicht.
Des Weiteren enthält die Mitteilung die UFI(s).
1.2. Informationen des Mitteilungspflichtigen und der Kontaktstelle
Name, vollständige Anschrift, Telefonnummer und E-Mail-Adresse des Mitteilungspflichtigen werden angegeben, sowie — falls davon abweichend — Name, vollständige Anschrift, Telefonnummer und E-Mail-Adresse der Kontaktstelle, über die weitere Informationen, die für die Zwecke der gesundheitlichen Notversorgung relevant sind, zu beschaffen sind.
1.3. Name, Telefonnummer und E-Mail-Adresse für schnellen Zugriff auf zusätzliche Produktinformationen
Im Falle einer verkürzten Mitteilung gemäß Teil A Abschnitt 2.3 werden ein Name, eine Telefonnummer und eine E-Mail-Adresse angegeben, über die ein schneller Zugriff auf detaillierte zusätzliche Produktinformationen, die für die Zwecke der gesundheitlichen Notversorgung relevant sind, in der in Teil A Abschnitt 3.3 genannten Sprache verfügbar ist. Die Telefonnummer muss 24 Stunden täglich und sieben Tage in der Woche erreichbar sein.
2. GEFAHRENBEZEICHNUNG UND ZUSÄTZLICHE INFORMATIONEN
Dieser Abschnitt enthält die Informationsanforderungen zu den Gesundheitsgefahren und physikalischen Gefahren des Gemischs sowie die geeigneten Warninformationen für diese Gefahren sowie die zusätzlichen Informationen, die in der Mitteilung enthalten sein müssen.
2.1. Einstufung des Gemischs
Die Einstufung des Gemischs aufgrund der Gesundheitsgefahren und der physikalischen Gefahren (Gefahrenklasse und -kategorie) wird gemäß den Einstufungsvorschriften in Anhang I angegeben.
2.2. Kennzeichnungselemente
Sofern vorhanden sind die folgenden der nach Artikel 17 vorgeschriebenen Kennzeichnungselemente anzugeben:
|
— |
Gefahrenpiktogramm-Codes (Anhang V); |
|
— |
Signalwort; |
|
— |
Gefahrenhinweis-Codes (Anhang III, einschließlich ergänzender Gefahrenmerkmale); |
|
— |
Sicherheitshinweis-Codes (Anhang IV). |
2.3. Toxikologische Angaben
Die Mitteilung umfasst jene Informationen zu den toxikologischen Wirkungen des Gemischs oder seiner Bestandteile, die in Abschnitt 11 des Sicherheitsdatenblatts des Gemischs im Einklang mit Anhang II der Verordnung (EG) Nr. 1907/2006 vorgeschrieben sind.
2.4. Zusätzliche Informationen
Die folgenden zusätzlichen Informationen werden angegeben:
|
— |
Art(en) und Größe(n) der Verpackung, in der das Gemisch für die Verwendung durch Verbraucher oder die gewerbliche Verwendung in Verkehr gebracht wird; |
|
— |
Farbe(n) und physikalische Beschaffenheit(en) des Gemischs in der gelieferten Form; |
|
— |
falls vorhanden, pH-Wert des Gemischs in der gelieferten Form oder, falls es sich um ein festes Gemisch handelt, pH-Wert einer wässrigen Flüssigkeit oder Lösung in einer bestimmten Konzentration. Die Konzentration des Prüfgemischs im Wasser wird angegeben. Falls der pH-Wert nicht vorhanden ist, so ist dies zu begründen; |
|
— |
Produktkategorie (siehe Teil A Abschnitt 3.4); |
|
— |
Verwendung (Verwendung durch Verbraucher, gewerbliche Verwendung, industrielle Verwendung oder eine beliebige Kombination dieser drei Verwendungsformen). |
3. INFORMATIONEN ZU DEN GEMISCH-BESTANDTEILEN
3.1. Allgemeine Anforderungen
Gemäß den Abschnitten 3.2, 3.3 und 3.4 werden die chemische Identität und die Konzentrationen der Gemisch-Bestandteile in der Mitteilung angegeben.
Im Fall einer verkürzten Mitteilung gemäß Teil A Abschnitt 2.3 dürfen sich, abweichend vom Unterabsatz 1, die einzureichenden Informationen zur Zusammensetzung eines Gemischs für die industrielle Verwendung oder eines Gemischs, dessen endgültige Verwendung nicht der Mitteilungspflicht unterliegt, auf die gemäß Anhang II der Verordnung (EG) Nr. 1907/2006 im Sicherheitsdatenblatt enthaltenen Informationen beschränken, sofern gemäß Abschnitt 1.3 bei Notfällen ein schneller Zugriff auf zusätzliche Informationen zu den Bestandteilen gewährleistet ist.
Bestandteile, die nicht im Gemisch vorkommen, werden nicht angegeben. Wenn sie jedoch als Teil einer Gruppe austauschbarer Bestandteile gemäß Abschnitt 3.5 angegeben werden, bzw. wenn Angaben zu ihrer Konzentration als Konzentrationsbereich gemäß den Abschnitten 3.6 oder 3.7 erfolgen, können sie angegeben werden, wenn es sicher ist, dass sie zu irgendeinem Zeitpunkt im Gemisch vorkommen werden.
Abweichend von Unterabsatz 3 kommen bei einer Gruppenmitteilung Parfümstoffbestandteile in den Gemischen mindestens in einem der Gemische vor.
Wenn bei einer Gruppenmitteilung die Parfümstoffe zwischen den in der Gruppe enthaltenen Gemischen variieren, wird eine Liste der Gemische und der darin enthaltenen Parfümstoffe, einschließlich ihrer Einstufung, vorgelegt.
3.2. Identifizierung von Gemisch-Bestandteilen
Ein Gemisch-Bestandteil ist entweder ein Stoff oder ein Gemisch im Gemisch.
3.2.1. Stoffe
Der Produktidentifikator für die nach Abschnitt 3.3 identifizierten Stoffe wird gemäß Artikel 18 Absatz 2 angegeben. Allerdings darf auch eine INCI-Bezeichnung, eine Colour-Index-Bezeichnung oder eine andere internationale chemische Bezeichnung verwendet werden, sofern die chemische Bezeichnung bekannt ist und die Identität des Stoffs eindeutig definiert. Die chemische Bezeichnung der Stoffe, für die gemäß Artikel 24 eine alternative chemische Bezeichnung genehmigt wurde, muss ebenfalls angegeben werden.
3.2.2. Gemisch im Gemisch
Wenn ein Gemisch in der Zusammensetzung eines zweiten Gemischs, das in Verkehr gebracht wird, verwendet wird, dann wird das erste Gemisch als „Gemisch im Gemisch“ (im Folgenden „MIM“) bezeichnet.
Informationen zu den in einem MIM enthaltenen Stoffen werden gemäß den Kriterien in Abschnitt 3.2.1 angegeben, es sei denn, der Mitteilungspflichtige hat keinen Zugriff auf die Informationen über die vollständige Zusammensetzung des MIM. Ist Letzteres der Fall, gilt Folgendes:
|
a) |
Das MIM wird durch seinen Produktidentifikator gemäß Artikel 18 Absatz 3 Buchstabe a, zusammen mit seiner Konzentration und dem UFI identifiziert, falls dieser verfügbar ist und die benannte Stelle die Informationen über das MIM in einer früheren Mitteilung erhalten hat. |
|
b) |
Falls ein UFI für das MIM zwar erstellt wurde, die benannte Stelle jedoch die Informationen über das MIM nicht in einer vorherigen Mitteilung erhalten hat, wird das MIM durch seinen Produktidentifikator gemäß Artikel 18 Absatz 3 Buchstabe a, zusammen mit seiner Konzentration, dem UFI, und den gemäß Anhang II der Verordnung (EG) Nr. 1907/2006 im Sicherheitsdatenblatt des MIM enthaltenen Informationen zur Zusammensetzung und alle anderen bekannten Bestandteile sowie Name, E-Mail-Adresse und Telefonnummer des MIM-Lieferanten identifiziert. |
|
c) |
Falls kein UFI vorliegt, so wird das MIM durch seinen Produktidentifikator gemäß Artikel 18 Absatz 3 Buchstabe a zusammen mit seiner Konzentration und den im Sicherheitsdatenblatt gemäß Anhang II der Verordnung (EG) Nr. 1907/2006 enthaltenen Angaben zur Zusammensetzung des MIM und alle anderen bekannten Bestandteile sowie Name, E-Mail-Adresse und Telefonnummer des MIM-Lieferanten identifiziert. |
3.2.3. Identifizierung durch generische Bestandteilidentifikatoren
Abweichend von den Abschnitten 3.2.1 und 3.2.2 dürfen die generischen Bestandteilidentifikatoren „Parfümstoff“ oder „Farbstoff“ für Gemisch-Bestandteile, die ausschließlich dazu verwendet werden, dem Gemisch ein Parfüm oder eine Farbe hinzuzufügen, verwendet werden, wenn die folgenden Bedingungen erfüllt sind:
|
— |
die Gemisch-Bestandteile sind nicht als gesundheitsgefährdend eingestuft; |
|
— |
die Konzentration der Gemisch-Bestandteile, die mit einem generischen Bestandteilidentifikator gekennzeichnet sind, überschreitet nicht die folgenden Konzentrationen:
|
3.3. Mitteilungsanforderungen unterliegende Gemisch-Bestandteile
Die folgenden Gemisch-Bestandteile sind anzugeben:
|
(1) |
Gemisch-Bestandteile, die aufgrund ihrer Wirkungen auf die Gesundheit oder aufgrund ihrer physikalischen Wirkungen als ‚gefährlich‘ eingestuft sind und die
|
|
(2) |
Gemisch-Bestandteile, die aufgrund ihrer Wirkungen auf die Gesundheit oder aufgrund ihrer physikalischen Wirkungen nicht als ‚gefährlich‘ eingestuft sind, die identifiziert sind und die in einer Konzentration von 1 % oder höher vorkommen. |
3.4. Konzentration und Konzentrationsbereiche der Gemisch-Bestandteile
Die Mitteilungspflichtigen stellen die Informationen zur Verfügung, die in den Abschnitten 3.4.1 und 3.4.2 in Bezug auf die Konzentration der gemäß Abschnitt 3.3 identifizierten Gemisch-Bestandteile festgelegt sind.
3.4.1. Gefährliche Bestandteile, die für die gesundheitliche Notversorgung und vorbeugende Maßnahmen von besonderer Bedeutung sind
Wenn Gemisch-Bestandteile gemäß dieser Verordnung in mindestens eine der nachfolgend aufgeführten Gefahrenkategorien eingestuft sind, ist ihre Konzentration in einem Gemisch als genauer Prozentsatz auszudrücken, und zwar absteigend nach Masse oder Volumen:
|
— |
akute Toxizität, Kategorie 1, 2 oder 3; |
|
— |
spezifische Zielorgan-Toxizität — einmalige Exposition, Kategorie 1 oder 2; |
|
— |
spezifische Zielorgan-Toxizität — wiederholte Exposition, Kategorie 1 oder 2; |
|
— |
Ätzwirkung auf die Haut, Kategorie 1, 1A, 1B oder 1C; |
|
— |
schwere Augenschädigung, Kategorie 1. |
Alternativ zur Angabe der Konzentration in Form genauer Prozentsätze kann ein Konzentrationsbereich gemäß Tabelle 1 angegeben werden.
Tabelle 1
Konzentrationsbereiche der gefährlichen Bestandteile, die für die gesundheitliche Notversorgung von besonderer Bedeutung sind
|
Konzentrationsbereich des im Gemisch enthaltenen gefährlichen Bestandteils (%) |
Maximale Spanne des Konzentrationsbereichs, der in der Mitteilung zu verwenden ist |
|
≥ 25 — < 100 |
5 % (Prozentpunkte) |
|
≥ 10 — < 25 |
3 % (Prozentpunkte) |
|
≥ 1 — < 10 |
1 % (Prozentpunkte) |
|
≥ 0,1 — < 1 |
0,3 % (Prozentpunkte) |
|
> 0 — < 0,1 |
0,1 % (Prozentpunkte) |
3.4.2. Andere gefährliche Bestandteile und Bestandteile, die nicht als gefährlich eingestuft sind
Die Konzentrationen der gefährlichen Bestandteile im Gemisch, die nicht in eine der im Abschnitt 3.4.1 angeführten Gefahrenkategorien eingestuft sind, und der identifizierten Bestandteile, die nicht als gefährlich eingestuft sind, werden gemäß Tabelle 2 als Prozentbereiche ausgedrückt, und zwar absteigend nach Masse oder Volumen. Alternativ können auch genaue Prozentsätze angegeben werden.
Tabelle 2
Konzentrationsbereiche für andere gefährliche Bestandteile und für Bestandteile, die nicht als gefährlich eingestuft sind
|
Konzentrationsbereich des im Gemisch enthaltenen Bestandteils (%) |
Maximale Spanne des Konzentrationsbereichs, der in der Mitteilung zu verwenden ist |
|
≥ 25 — < 100 |
20 % (Prozentpunkte) |
|
≥ 10 — < 25 |
10 % (Prozentpunkte) |
|
≥ 1 — < 10 |
3 % (Prozentpunkte) |
|
> 0 — < 1 |
1 % (Prozentpunkte) |
Abweichend vom Unterabsatz 1 sind die Mitteilungspflichtigen im Rahmen einer Gruppenmitteilung über Parfümbestandteile, die keine Einstufung aufweisen oder die lediglich aufgrund ihrer Sensibilisierung der Haut (Kategorie 1, 1A oder 1B) oder aufgrund ihrer Aspirationsgefahr als gefährlich eingestuft sind, nicht verpflichtet, Informationen zur Konzentration anzugeben.
3.5. Zusammenfassen von Bestandteilen in einer Gruppe austauschbarer Bestandteile
Bestandteile können im Rahmen einer Mitteilung in einer Gruppe austauschbarer Bestandteile zusammengefasst werden, sofern
|
a) |
für alle Bestandteile in einer Gruppe austauschbarer Bestandteile gilt, dass
|
|
b) |
für alle möglichen Kombinationen des resultierenden endgültigen Gemischs auf der Grundlage der Bestandteile der Gruppe austauschbarer Bestandteile die Gefahrenbezeichnung und die zusätzlichen Informationen gemäß Teil B Abschnitt 2 identisch sind. |
Alternativ können Bestandteile, die nur aufgrund ihrer Ätzwirkung auf die Haut, ihrer Eigenschaften in Bezug auf Hautreizung, Augenschädigung, Augenreizung, Aspirationstoxizität, Atemwegs- oder Hautsensibilisierung oder einer Kombination davon als gefährlich eingestuft sind, auch in einer Gruppe austauschbarer Bestandteile zusammengefasst werden, sofern
|
a) |
die Einstufung im Hinblick auf die Gesundheitsgefahren und physikalischen Gefahren (Gefahrenklasse und -kategorie) für alle Bestandteile identisch ist und |
|
b) |
gegebenenfalls der pH-Wert aller wegen ihrer Ätzwirkung auf die Haut, bzw. ihrer Eigenschaften in Bezug auf Hautreizung, Augenschädigung oder Augenreizung als gefährlich eingestuften Bestandteile sauer, neutral oder alkalisch ist und |
|
c) |
die Gruppe austauschbarer Bestandteile nicht mehr als fünf Bestandteile enthält und |
|
d) |
für alle möglichen Kombinationen des resultierenden endgültigen Gemischs auf der Grundlage der in einer Gruppe austauschbarer Bestandteile zusammengefassten Bestandteile die Gefahrenbezeichnung und die zusätzlichen Informationen gemäß Teil B Abschnitt 2 identisch sind. |
3.5.1. Name der Gruppe austauschbarer Bestandteile und Identifizierung der in einer Gruppe zusammengefassten Bestandteile
Einer Gruppe austauschbarer Bestandteile wird ein Name zugewiesen, der der(den) technischen Funktion(en) der zusammengefassten Bestandteile entspricht, aufgrund deren ihre Aufnahme in das Gemisch erfolgt ist.
Jeder Bestandteil einer Gruppe austauschbarer Bestandteile ist gemäß Abschnitt 3.2.1 bzw. 3.2.2 anzugeben.
3.5.2. Konzentration und Konzentrationsbereiche der in einer Gruppe zusammengefassten Bestandteile
Abweichend von Abschnitt 3.4 Unterabsatz 1 übermitteln die Mitteilungspflichtigen bei Bestandteilen, die zu einer Gruppe austauschbarer Bestandteile zusammengefasst sind, die in den Abschnitten 3.4.1 und 3.4.2 festgelegten Angaben über die Gesamtkonzentration aller im Gemisch vorhandenen und im Rahmen der Gruppe austauschbarer Bestandteile zusammengefassten Bestandteile.
Wenn die in einer Gruppe austauschbarer Bestandteile zusammengefassten Gemischbestandteile gemäß dieser Verordnung in mindestens eine der im Abschnitt 3.4.1 angeführten Gefahrenkategorien eingestuft sind, ist die Gesamtkonzentration der im Gemisch vorkommenden und in der Gruppe austauschbarer Bestandteile zusammengefassten Bestandteile als genauer Prozentsatz auszudrücken, und zwar absteigend nach Masse oder Volumen. Alternativ kann ein Konzentrationsbereich gemäß Tabelle 1 des betreffenden Abschnitts angegeben werden.
Die Gesamtkonzentrationen der im Gemisch vorhandenen und in einer Gruppe austauschbarer Bestandteile zusammengefassten Bestandteile, die nicht in eine der im Abschnitt 3.4.1 angeführten Gefahrenkategorien eingestuft sind, und die Gesamtkonzentration der identifizierten, im Gemisch vorkommenden und in einer Gruppe austauschbarer Bestandteile zusammengefassten Bestandteile, die nicht als gefährlich eingestuft sind, werden gemäß Tabelle 2 in Abschnitt 3.4.2 als Prozentbereiche ausgedrückt, und zwar absteigend nach Masse oder Volumen. Alternativ können auch genaue Prozentsätze angegeben werden.
3.6. Gemische, die den Standardrezepturen entsprechen
Abweichend von den Abschnitten 3.2, 3.3 und 3.4 gilt für ein Gemisch mit einer Zusammensetzung, die einer in Teil D festgelegten Standardrezeptur entspricht, wenn sich die Einstufung des Gemisches in Abhängigkeit von der Konzentration der Bestandteile innerhalb der in der entsprechenden Standardrezeptur angegebenen Prozentbereiche nicht ändert, Folgendes:
|
— |
Wenn die Angaben zur Zusammensetzung in der Standardrezeptur zusammen mit den Angaben gemäß den Abschnitten 3.2 bis 3.4 über Identität und Konzentration der Bestandteile, die nicht in der Standardrezeptur angegeben sind, nicht weniger detailliert sind als die Angaben im Sicherheitsdatenblatt gemäß Anhang II der Verordnung (EG) Nr. 1907/2006, so können Angaben zur Identität und Konzentration eines oder mehrerer Bestandteile des Gemisches gemäß der Standardrezeptur für die in dieser Formel genannten Bestandteile und gemäß den Abschnitten 3.2 bis 3.4 für die anderen Bestandteile vorgelegt werden; |
|
— |
wenn die unter vorstehendem Gedankenstrich genannten Angaben weniger detailliert sind, als die Angaben im Sicherheitsdatenblatt gemäß Anhang II der Verordnung (EG) Nr. 1907/2006, so sind Angaben zur Identität und Konzentration aller Bestandteile des Gemisches im Sicherheitsdatenblatt gemäß Anhang II der Verordnung (EG) Nr. 1907/2006 zu machen. |
3.7. Kraft- und Brennstoffe
Abweichend von den Abschnitten 3.2, 3.3 und 3.4 können für die in Tabelle 3 aufgeführten Kraft- und Brennstoffe die Angaben zur Identität und Konzentration der im Sicherheitsdatenblatt gemäß Anhang II der Verordnung (EG) Nr. 1907/2006 aufgeführten Bestandteile des Gemisches übermittelt werden. Die Identität und Konzentration jedes anderen bekannten Bestandteils ist ebenfalls anzugeben.
Tabelle 3
Liste der Kraft- und Brennstoffe
|
Kraft- und Brennstoff |
Produktbeschreibung |
|
Benzin EN228 |
Kraftstoffe für Kraftfahrzeuge — unverbleites Benzin |
|
Benzin E85 |
Kraftstoffe für Kraftfahrzeuge — Ethanol (E85) — Kraftstoff für die Automobilindustrie |
|
Benzinalkylat |
Kraftstoffe — Spezialbenzin für Geräte mit Antrieb |
|
LPG |
Als Kraft- oder Brennstoff verwendetes Flüssiggas |
|
LNG |
Als Kraft- oder Brennstoff verwendetes Flüssigerdgas |
|
Dieselkraftstoff |
Kraftstoffe für Kraftfahrzeuge — Kraftstoffe für Dieselmotoren mit/ohne Biokraftstoff |
|
Paraffinhaltige Dieselkraftstoffe (z. B. GTL (Gas to Liquid), HVO (Hydriertes Pflanzenöl) und BTL (Biomass to Liquid)) |
Kraftstoffe für Kraftfahrzeuge — paraffinischer Dieselkraftstoff aus Synthese oder Hydrotreatment |
|
Heizöl |
Flüssige mineralische Brennstoffe mit den Eigenschaften von Heizöl für Privathaushalte |
|
MK 1-Dieselkraftstoff |
Kraftstoffe für Kraftfahrzeuge — Dieselkraftstoff der Umweltklasse 1 und 2 für Hochgeschwindigkeitsdieselmotoren |
|
Flugkraftstoffe |
Flugkraftstoffe für Turbinentriebwerke und Kolbenverbrennungsmotoren |
|
Kerosin — Leuchtpetroleum |
Paraffinische Lampenöle, Typ B und C |
|
Schweröl |
Alle Arten von Schweröl (heavy fuel oil) |
|
Schiffskraftstoff |
Schiffskraftstoffe, mit oder ohne Biodiesel |
|
Fettsäuremethylester (FAME) —Diesel B100 |
Fettsäuremethylester (FAME) für Dieselmotoren und Heizzwecke |
3.8. Einstufung der Gemisch-Bestandteile
Die Einstufung der in dem Gemisch gemäß Abschnitt 3.3 ermittelten Stoffe nach ihren gesundheitlichen und physikalischen Wirkungen (Gefahrenklassen, Gefahrenkategorien und Gefahrenhinweise) ist anzugeben. Dies schließt die Einstufung mindestens für alle Stoffe ein, die gemäß Anhang II Nummer 3.2.1 der Verordnung (EG) Nr. 1907/2006 im Sicherheitsdatenblatt des Gemisches und im Sicherheitsdatenblatt für alle in dem Gemisch enthaltenen MIM angegeben sind. Für diejenigen gemäß Abschnitt 3.3 identifizierten MIM, bei denen der Mitteilungspflichtige keinen Zugang zur vollständigen Zusammensetzung des MIM hat, ist zusätzlich die Einstufung des MIM in Bezug auf seine gesundheitlichen und physikalischen Auswirkungen anzugeben.
4. AKTUALISIERUNG DER MITTEILUNG
4.1. Bedingungen für die Aktualisierung der Mitteilung
In Fällen, in denen eine der folgenden Änderungen auf ein Gemisch in einer einzelnen oder einer Gruppenmitteilung zutrifft, reichen die Mitteilungspflichtigen eine aktualisierte Mitteilung ein, bevor sie dieses veränderte Gemisch in Verkehr bringen, und zwar:
|
— |
wenn sich der Produktidentifikator (oder der UFI) des Gemischs ändert; |
|
— |
wenn sich die Einstufung des Gemischs im Hinblick auf Gesundheitsgefahren oder physikalische Gefahren ändert; |
|
— |
wenn für die gefährlichen Eigenschaften des Gemischs oder seiner Bestandteile relevante neue toxikologische Informationen bekannt werden, die in Abschnitt 11 des Sicherheitsdatenblatts verlangt werden; |
|
— |
wenn eine Änderung in der Zusammensetzung des Gemischs eine der folgenden Bedingungen erfüllt:
|
Abweichend von Unterabsatz 1 vierter Gedankenstrich gilt Folgendes:
|
a) |
eine Aktualisierung der Mitteilung für Gemische mit einer Zusammensetzung, die einer der in Teil D genannten Standardrezepturen entspricht, ist nur erforderlich, wenn sich die Zusammensetzung des Gemisches so ändert, dass die Zusammensetzung des Gemisches nicht mehr der Standardrezeptur entspricht; |
|
b) |
bei Gemischen, für die Angaben zur Zusammensetzung auf der Grundlage des Sicherheitsdatenblatts gemäß Abschnitt 3.6 oder 3.7 gemacht werden, ist eine Aktualisierung der Mitteilung erforderlich, wenn Abschnitt 3 des Sicherheitsdatenblatts aktualisiert wird. Tabelle 4 Abweichungen bei der Bestandteil-Konzentration, die eine Aktualisierung der Mitteilung erfordern
|
Wenn sich die Parfümstoffe in einer Gruppenmitteilung ändern, wird die Liste der Gemische und der darin enthaltenen Parfümstoffe gemäß Abschnitt 3.1 aktualisiert.
4.2. Inhalt der Aktualisierung der Mitteilung
Die Aktualisierung der Mitteilung umfasst eine überarbeitete Version der vorhergehenden Mitteilung, die die neu verfügbaren Informationen gemäß Abschnitt 4.1 enthält.
TEIL C
FORMAT DER MITTEILUNG
1. FORMAT DER MITTEILUNG
1.1. Format der Mitteilung
Die Mitteilung der Informationen bei nach Artikel 45 benannten Stellen erfolgt in dem von der Agentur zur Verfügung gestellten Format. Das Mitteilungsformat enthält die folgenden Elemente:
1.2. Identifizierung des Gemischs, des Mitteilungspflichtigen und der Kontaktstelle
Produktidentifikator
|
— |
Vollständige(r) Handelsname(n) des Produkts (im Falle einer Gruppenmitteilung sind alle Produktidentifikatoren aufzuführen) |
|
— |
Andere Namen, Synonyme |
|
— |
Eindeutige(r) Rezepturidentifikator(en) (Unique Formula Identifier — UFI) |
|
— |
Andere Identifikatoren (Zulassungsnummer, Produktcodes der Unternehmen) |
Kontaktdaten des Mitteilungspflichtigen und der Kontaktstelle
|
— |
Name |
|
— |
Vollständige Anschrift |
|
— |
Telefonnummer |
|
— |
E-Mail-Adresse |
Kontaktinformationen für schnellen Zugriff auf zusätzliche Produktinformationen (24 Stunden/sieben Tage). Nur für verkürzte Mitteilung.
|
— |
Name |
|
— |
Telefonnummer (24 Stunden täglich, sieben Tage pro Woche erreichbar) |
|
— |
E-Mail-Adresse |
1.3. Einstufung des Gemischs, Kennzeichnungselemente und Toxikologie
Einstufung des Gemischs und Kennzeichnungselemente
|
— |
Gefahrenklasse und -kategorie |
|
— |
Gefahrenpiktogramm-Codes (Anhang V) |
|
— |
Signalwort |
|
— |
Gefahrenhinweis-Codes, einschließlich ergänzender Gefahrenmerkmale (Anhang III) |
|
— |
Sicherheitshinweis-Codes (Anhang IV) |
Toxikologische Angaben
|
— |
Beschreibung der Toxizität des Gemischs oder seiner Bestandteile (gemäß den Anforderungen in Abschnitt 11 des Sicherheitsdatenblatts im Einklang mit Anhang II der Verordnung (EG) Nr. 1907/2006) |
Zusätzliche Informationen zum Gemisch
|
— |
Farbe(n) |
|
— |
falls vorhanden, pH-Wert des Gemischs in der gelieferten Form oder, falls es sich um ein festes Gemisch handelt, pH-Wert einer wässrigen Flüssigkeit oder Lösung in einer bestimmten Konzentration. Die Konzentration des Prüfgemischs im Wasser wird angegeben. Falls der pH-Wert nicht vorhanden ist, so ist dies zu begründen; |
|
— |
physikalische Beschaffenheit(en) |
|
— |
Verpackung (Art(en) und Größe(n)) |
|
— |
beabsichtigte Verwendung (Produktkategorie) |
|
— |
Verwendungen (Verbraucher, gewerblich, industriell) |
1.4. Informationen zu den Gemisch-Bestandteilen und den Gruppen austauschbarer Bestandteile
Identifizierung von Gemisch-Bestandteilen
|
— |
Chemische Bezeichnung/Handelsname der Bestandteile |
|
— |
CAS-Nummer (falls zutreffend) |
|
— |
EG-Nummer (falls zutreffend) |
|
— |
UFI (falls zutreffend) |
Name der Gruppe austauschbarer Bestandteile (falls zutreffend)
Konzentration und Konzentrationsbereiche der Gemisch-Bestandteile
|
— |
Genaue Konzentration oder Konzentrationsbereich |
Einstufung der Gemisch-Bestandteile
|
— |
Gefahreneinstufung (falls zutreffend) |
|
— |
Zusätzliche Identifikatoren (falls zutreffend und falls relevant für gesundheitliche Notversorgung) |
Liste gemäß Teil B Abschnitt 3.1 Unterabsatz 5 (falls zutreffend)
TEIL D
STANDARDREZEPTUREN
Für die Standardrezepturen 1-17 gelten die nachfolgend aufgeführten Bedingungen:
|
— |
Schwermetalle, Spurenelemente: As, Ba, Cd, Cr, Co, Cu, Hg, Mo, Ni, Pb, Sb, Sn, Te, Tl, V unterhalb 0,1 Gewichtsprozent und Mn, Sr, Zn unterhalb 1 Gewichtsprozent |
|
— |
Polyzyklische aromatische Kohlenwasserstoffe (PAK) sind nicht vorhanden. |
Bemerkung zu den Standardrezepturen 1-17:
|
— |
(1) UVCB-Stoffe enthalten unterschiedliche Mengen von Calcit, Tricalciumsilikat, Dicalciumsilikat, Calciumoxid, Quarz, Kaliumchlorid, Kaliumsulfat, Calciumsulfat, Natriumaluminiumsilicat, Magnesiumaluminiumsilicat, Muskovit … |
1. ZEMENT
|
Zementstandardrezeptur — 1 |
||
|
Produktbeschreibung |
Portlandzement Mit einem Hauptbestandteil: Klinker |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
86,5-100 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 2 |
||
|
Produktbeschreibung |
Portland-Hüttenzement und Hochofenzement Mit zwei Hauptbestandteilen: Klinker und Schlacke |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
4,6-94 |
|
Hüttensand |
266-002-0 |
5,5-95 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 3 |
||
|
Produktbeschreibung |
Portland-Silicastaubzement Portlandzemente mit zwei Hauptbestandteilen: Klinker und Silicastaub |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
82-94 |
|
Silicastaub |
273-761-1 |
5,5-10 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 4 |
||
|
Produktbeschreibung |
Portland-Puzzolanzement, Puzzolanzement Portlandzemente mit zwei Hauptbestandteilen: Klinker und Puzzolan (natürliches Puzzolan oder natürliches Puzzolan, gebrannt) |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
41-94 |
|
Natürliches Puzzolan (gebrannt) |
310-127-6 |
5,5-55 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-303-2 |
0-0,1 |
|
Zementstandardrezeptur — 5 |
||
|
Produktbeschreibung |
Portland-Flugaschezement, Puzzolanzement Portlandzemente mit zwei Hauptbestandteilen: Klinker und Flugasche (kieselsäurereiche und kalkreiche Flugasche) |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
41-94 |
|
Flugasche |
931-322-8 |
5,5-55 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 6 |
||
|
Produktbeschreibung |
Portland-Schieferzement Portlandzemente mit zwei Hauptbestandteilen: Klinker und gebrannter Schiefer |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
59-94 |
|
Gebrannter Schiefer |
297-648-1 |
5,5-35 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 7 |
||
|
Produktbeschreibung |
Portland-Kalksteinzement Portlandzemente mit zwei Hauptbestandteilen: Klinker und Kalkstein |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
59-94 |
|
Kalkstein |
215-279-6 |
5,5-35 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 8 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Kompositzement (Schlacke — Kalkstein) Portlandzemente mit drei Hauptbestandteilen: Klinker, Schlacke und Kalkstein |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
31,9-88 |
|
Hüttensand |
266-002-0 |
5,5-59 |
|
Kalkstein |
215-279-6 |
5,5-29 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 9 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Kompositzement (Schlacke — Flugasche) Portlandzemente mit drei Hauptbestandteilen: Klinker, Hochofenschlacke, kieselsäurereiche und kalkreiche Flugasche |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
18,2-88 |
|
Hüttensand |
266-002-0 |
5,5-59 |
|
Flugasche |
931-322-8 |
5,5-49 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 10 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Kompositzement (Schlacke — Puzzolan) Portlandzemente mit drei Hauptbestandteilen: Klinker, Hochofenschlacke, natürliches Puzzolan oder natürliches Puzzolan, gebrannt |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
18,2-88 |
|
Hüttensand |
266-002-0 |
5,5-49 |
|
Natürliches Puzzolan (gebrannt) |
310-127-6 |
5,5-49 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 11 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Kompositzement (Schlacke — gebrannter Schiefer) Portlandzemente mit drei Hauptbestandteilen: Klinker, Hochofenschlacke, gebrannter Schiefer |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
59-94 |
|
Hüttensand |
266-002-0 |
5,5-29 |
|
Gebrannter Schiefer |
297-648-1 |
5,5-29 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 12 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Kompositzement (Kalkstein — Flugasche) Portlandzemente mit drei Hauptbestandteilen: Klinker, Kalkstein, kieselsäurereiche und kalkreiche Flugasche |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
46-94 |
|
Kalkstein |
215-279-6 |
5,5-29 |
|
Flugasche |
931-322-8 |
5,5-44 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 13 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Kompositzement (Kalkstein — Puzzolan) Portlandzemente mit drei Hauptbestandteilen: Klinker, Kalkstein, natürliches Puzzolan oder natürliches Puzzolan, gebrannt |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
46-94 |
|
Kalkstein |
215-279-6 |
5,5-29 |
|
Natürliches Puzzolan (gebrannt) |
310-127-6 |
5,5-44 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 14 |
||
|
Produktbeschreibung |
Portland-Kompositzement (Kalkstein — gebrannter Schiefer) Portlandzemente mit drei Hauptbestandteilen: Klinker, Kalkstein und gebrannter Schiefer |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
59-94 |
|
Kalkstein |
215-279-6 |
5,5-29 |
|
Gebrannter Schiefer |
297-648-1 |
5,5-29 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 15 |
||
|
Produktbeschreibung |
Portland-Kompositzement, Puzzolanzement (Flugasche — Puzzolan) Portlandzemente mit drei Hauptbestandteilen: Klinker, kieselsäurereiche und kalkreiche Flugasche, natürliches Puzzolan oder natürliches Puzzolan, gebrannt |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
41-94 |
|
Natürliches Puzzolan (gebrannt) |
310-127-6 |
5,5-55 |
|
Flugasche |
931-322-8 |
5,5-55 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 16 |
||
|
Produktbeschreibung |
Portland-Kompositzement Portlandzemente mit vier Hauptbestandteilen: Klinker und drei der nachfolgenden Bestandteile: Hochofenschlacke, Silicastaub, Flugasche, Puzzolan, gebrannter Schiefer, Kalkstein |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
59-94 |
|
Hüttensand Natürliches Puzzolan (gebrannt) Flugasche Gebrannter Schiefer Kalkstein Silicastaub |
266-002-0 310-127-6 931-322-8 297-648-1 215-279-6 273-761-1 |
5,5-23 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 17 |
||
|
Produktbeschreibung |
Kompositzement Portlandzemente mit vier Hauptbestandteilen: Klinker, Schlacke, kieselsäurereiche Flugasche und natürliches Puzzolan oder natürliches Puzzolan, gebrannt |
|
|
Bestandteil |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
18,3-64 |
|
Hüttensand |
266-002-0 |
16,5-49 |
|
Natürliches Puzzolan (gebrannt) |
310-127-6 |
5,5-43 |
|
Flugasche |
931-322-8 |
5,5-43 |
|
Calciumsulfat |
231-900-3 |
0-8 |
|
Zementofenstaub (1) |
270-659-9 |
0-5 |
|
Anorganische natürliche mineralische Stoffe |
310-127-6 |
|
|
Eisen(II)sulfat |
231-753-5 |
0-1 |
|
Zinn(II)sulfat |
231-302-2 |
0-0,1 |
|
Zementstandardrezeptur — 18 |
||
|
Produktbeschreibung |
Calciumaluminatzement |
|
|
Bestandteil |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Calciumaluminat-Zementklinker |
266-045-5 |
86,5-100 |
|
Schleifmittel |
- |
0-0,2 |
|
Zementstandardrezeptur — 19 |
||
|
Produktbeschreibung |
Mauerwerks-Zemente — mit Klinker und Kalkstein — MC 5, MC 12,5, MC 22,5 |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
25-60 |
|
Baukalk |
215-138-9 |
1-75 |
|
Kalkhydrat gemäß EN 459 |
215-137-3 |
|
|
Andere, nicht gefährliche anorganische Bestandteile |
310-127-6 |
0-74 |
|
Anorganische Pigmente gemäß EN 12878 |
- |
0-1 |
|
Zementstandardrezeptur — 20 |
||
|
Produktbeschreibung |
Mauerwerks-Zemente — mit Klinker und ohne Kalkstein — MC 5, MC 12,5, MC 22,5 |
|
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Portlandzementklinker |
266-043-4 |
25-60 |
|
Andere, nicht gefährliche anorganische Bestandteile |
310-127-6 |
40-75 |
|
Anorganische Pigmente gemäß EN 12878 |
|
0-1 |
2. GIPSBINDER
|
Gipsbinder-Standardrezeptur |
||
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Calciumsulfat |
231-900-3 |
≥ 50 — < 100 |
|
Calciumdihydroxid |
215-137-3 |
> 0 und ≤ 5 |
3. FERTIGBETON
|
Fertigbeton-Standardrezeptur 1 Betonfestigkeitsklassen C8/10, C12/15, C16/20, C20/25, C25/30, C28/35, C32/40, C35/45, C40/50, C45/55, C50/60 LC8/9, LC12/13, LC16/18, LC20/22, LC25/28, LC30/33, LC35/38, LC40/44, LC45/50, LC50/55, LC55/60 |
||
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Zement |
270-659-9 |
3-18 |
|
Wasser |
231-791-2 |
5-8 |
|
Zuschlagstoffe |
273-727-6 |
70-80 |
|
Betonbelüfter (Beimischung) |
- |
0-0,08 |
|
Betonverflüssiger/Hochleistungsbetonverflüssiger (Beimischung) |
- |
0-0,15 |
|
Betonverzögerer (Beimischung) |
- |
0-0,4 |
|
Betonbeschleuniger (Beimischung) |
- |
0-0,2 |
|
Wasserbeständigkeit (Beimischung) |
- |
0-0,25 |
|
Flugasche |
931-322-8 |
0-8 |
|
Silicastaub |
273-761-1 |
0-3 |
|
Hüttensand |
266-002-0 |
0-6 |
|
Fertigbeton-Standardrezeptur 2 Betonfestigkeitsklassen C55/67, C60/75, C70/85, C80/95, C90/105, C100/105 LC 60/66, LC70/77, LC80/88 |
||
|
Bezeichnung des Bestandteils |
EG-Nr. |
Konzentration (Gewichtsprozent) |
|
Zement |
270-659-9 |
12-25 |
|
Wasser |
231-791-2 |
5-8 |
|
Zuschlagstoffe |
273-727-6 |
70-80 |
|
Betonbelüfter (Beimischung) |
- |
0,04-0,08 |
|
Betonverflüssiger/Hochleistungsbetonverflüssiger (Beimischung) |
- |
0-0,15 |
|
Betonverzögerer (Beimischung) |
- |
0-0,4 |
|
Betonbeschleuniger (Beimischung) |
- |
0-0,2 |
|
Wasserbeständigkeit (Beimischung) |
- |
0-0,25 |
|
Flugasche |
931-322-8 |
0-8 |
|
Silicastaub |
273-761-1 |
0-3 |
|
Hüttensand |
266-002-0 |
0-6 |
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/24 |
DURCHFÜHRUNGSVERORDNUNG (EU) 2020/1678 DER KOMMISSION
vom 6. November 2020
zur Genehmigung einer Änderung der Spezifikation einer geschützten Ursprungsbezeichnung oder einer geschützten geografischen Angabe („Rioja“ (g. U.))
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) Nr. 1308/2013 des Europäischen Parlaments und des Rates vom 17. Dezember 2013 über eine gemeinsame Marktorganisation für landwirtschaftliche Erzeugnisse und zur Aufhebung der Verordnungen (EWG) Nr. 922/72, (EWG) Nr. 234/79, (EG) Nr. 1037/2001 und (EG) Nr. 1234/2007 des Rates (1), insbesondere auf Artikel 99,
in Erwägung nachstehender Gründe:
|
(1) |
Die Kommission hat den Antrag auf Genehmigung der Änderung der Spezifikation der geschützten Ursprungsbezeichnung „Rioja“ geprüft, den Spanien gemäß Artikel 105 der Verordnung (EU) Nr. 1308/2013 gestellt hat. |
|
(2) |
Die Kommission hat den Antrag auf Genehmigung der Änderung der Spezifikation gemäß Artikel 97 Absatz 3 der Verordnung (EU) Nr. 1308/2013 im Amtsblatt der Europäischen Union veröffentlicht (2). |
|
(3) |
Bei der Kommission ist kein Einspruch gemäß Artikel 98 der Verordnung (EU) Nr. 1308/2013 eingegangen. |
|
(4) |
Die Änderung der Spezifikation sollte daher gemäß Artikel 99 der Verordnung (EU) Nr. 1308/2013 genehmigt werden. |
|
(5) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ausschusses für die gemeinsame Organisation der Agrarmärkte — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Die im Amtsblatt der Europäischen Union veröffentlichte Änderung der Spezifikation für den Namen „Rioja“ (g. U.) wird genehmigt.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 6. November 2020
Für die Kommission,
im Namen der Präsidentin,
Janusz WOJCIECHOWSKI
Mitglied der Kommission
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/25 |
DURCHFÜHRUNGSVERORDNUNG (EU) 2020/1679 DER KOMMISSION
vom 6. November 2020
über die Gewährung des Schutzes gemäß Artikel 99 der Verordnung (EU) Nr. 1308/2013 des Europäischen Parlaments und des Rates für den Namen „Soltvadkerti“ (g. U.)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) Nr. 1308/2013 des Europäischen Parlaments und des Rates vom 17. Dezember 2013 über eine gemeinsame Marktorganisation für landwirtschaftliche Erzeugnisse und zur Aufhebung der Verordnungen (EWG) Nr. 922/72, (EWG) Nr. 234/79, (EG) Nr. 1037/2001 und (EG) Nr. 1234/2007 des Rates (1), insbesondere auf Artikel 99,
in Erwägung nachstehender Gründe:
|
(1) |
Die Kommission hat den von Ungarn eingereichten Antrag auf Eintragung des Namens „Soltvadkerti“ im Einklang mit Artikel 97 Absätze 2 und 3 der Verordnung (EU) Nr. 1308/2013 geprüft und im Amtsblatt der Europäischen Union (2) veröffentlicht. |
|
(2) |
Bei der Kommission ist kein Einspruch gemäß Artikel 98 der Verordnung (EU) Nr. 1308/2013 eingegangen. |
|
(3) |
Der Name „Soltvadkerti“ sollte im Einklang mit Artikel 99 der Verordnung (EU) Nr. 1308/2013 geschützt und in das Register gemäß Artikel 104 derselben Verordnung eingetragen werden. |
|
(4) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ausschusses für die gemeinsame Organisation der Agrarmärkte — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Der Name „Soltvadkerti“ (g. U.) wird hiermit geschützt.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 6. November 2020
Für die Kommission,
im Namen der Präsidentin,
Janusz WOJCIECHOWSKI
Mitglied der Kommission
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/26 |
DURCHFÜHRUNGSVERORDNUNG (EU) 2020/1680 DER KOMMISSION
vom 6. November 2020
über die Gewährung des Schutzes gemäß Artikel 99 der Verordnung (EU) Nr. 1308/2013 des Europäischen Parlaments und des Rates für den Namen „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ (g. U.)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) Nr. 1308/2013 des Europäischen Parlaments und des Rates vom 17. Dezember 2013 über eine gemeinsame Marktorganisation für landwirtschaftliche Erzeugnisse und zur Aufhebung der Verordnungen (EWG) Nr. 922/72, (EWG) Nr. 234/79, (EG) Nr. 1037/2001 und (EG) Nr. 1234/2007 des Rates (1), insbesondere auf Artikel 99,
in Erwägung nachstehender Gründe:
|
(1) |
Die Kommission hat den von Italien übermittelten Antrag auf Eintragung des Namens „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ gemäß Artikel 97 Absätze 2 und 3 der Verordnung (EU) Nr. 1308/2013 geprüft und im Amtsblatt der Europäischen Union (2) veröffentlicht. |
|
(2) |
Bei der Kommission ist kein Einspruch gemäß Artikel 98 der Verordnung (EU) Nr. 1308/2013 eingegangen. |
|
(3) |
Gemäß Artikel 99 der Verordnung (EU) Nr. 1308/2013 sollte der Name „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ geschützt und in das Register gemäß Artikel 104 der genannten Verordnung eingetragen werden. |
|
(4) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ausschusses für die gemeinsame Organisation der Agrarmärkte — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Der Name „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ (g. U.) wird geschützt.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 6. November 2020
Für die Kommission,
im Namen der Präsidentin,
Janusz WOJCIECHOWSKI
Mitglied der Kommission
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/27 |
VERORDNUNG (EU) 2020/1681 DER KOMMISSION
vom 12. November 2020
zur Änderung des Anhangs I der Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates hinsichtlich der Streichung bestimmter Aromastoffe aus der Unionsliste
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über Aromen und bestimmte Lebensmittelzutaten mit Aromaeigenschaften zur Verwendung in und auf Lebensmitteln sowie zur Änderung der Verordnung (EWG) Nr. 1601/91 des Rates, der Verordnungen (EG) Nr. 2232/96 und (EG) Nr. 110/2008 und der Richtlinie 2000/13/EG (1), insbesondere auf Artikel 11 Absatz 3,
gestützt auf die Verordnung (EG) Nr. 1331/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über ein einheitliches Zulassungsverfahren für Lebensmittelzusatzstoffe, -enzyme und -aromen (2), insbesondere auf Artikel 7 Absatz 4,
in Erwägung nachstehender Gründe:
|
(1) |
Anhang I der Verordnung (EG) Nr. 1334/2008 enthält eine Unionsliste der für die Verwendung in und auf Lebensmitteln zugelassenen Aromen und Ausgangsstoffe mit den Bedingungen für ihre Verwendung. |
|
(2) |
Mit der Durchführungsverordnung (EU) Nr. 872/2012 der Kommission (3) wurde die Liste der Aromastoffe festgelegt und in Anhang I Teil A der Verordnung (EG) Nr. 1334/2008 aufgenommen. |
|
(3) |
Anhang I der Verordnung (EG) Nr. 1334/2008 kann nach dem einheitlichen Verfahren gemäß Artikel 3 Absatz 1 der Verordnung (EG) Nr. 1331/2008 auf Initiative der Kommission oder auf Antrag eines Mitgliedstaats oder einer betroffenen Person aktualisiert werden. |
|
(4) |
Die Unionsliste der Aromen und Ausgangsstoffe in Anhang I der Verordnung (EG) Nr. 1334/2008 enthält unter anderem eine Reihe von Aromastoffen, für die die Europäische Behörde für Lebensmittelsicherheit (im Folgenden die „Behörde“) zum Zeitpunkt der Annahme der Liste durch die Verordnung (EU) Nr. 872/2012 auf der Grundlage der verfügbaren Daten ein etwaiges Sicherheitsrisiko für die Gesundheit der Verbraucher nicht ausschließen konnte und daher zusätzliche Daten für erforderlich hielt, um ihre Bewertung abzuschließen. Diese Stoffe wurden in die Unionsliste der Aromastoffe unter der Bedingung aufgenommen, dass die Sicherheitsdaten, welche die von der Behörde geäußerten Bedenken ausräumen, vor Ablauf der in Anhang I Teil A der Verordnung (EG) Nr. 1334/2008 festgelegten spezifischen Fristen vorgelegt werden. Diese Stoffe und ihre zugehörigen Fristen wurden in den Fußnoten 1 bis 4 aufgeführt. |
|
(5) |
Zu den in die Unionsliste der Aromen und Ausgangsstoffe aufgenommenen Stoffen, die mit dem Fußnotenhinweis gekennzeichnet wurden, dass zusätzliche wissenschaftliche Daten bis zum 31. Dezember 2012 vorzulegen sind, gehörten die folgenden fünf Stoffe: alpha-Damascon (FL-Nr. 07.134) (repräsentativer Stoff der Gruppe), delta-Damascon (FL-Nr. 07.130), cis-1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)but-2-en-1-on (FL-Nr. 07.225), trans-1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)but-2-en-1-on (FL-Nr. 07.226) und alpha-Damascenon (FL-Nr. 07.231) (im Folgenden die „betreffenden Stoffe“). Diese Stoffe gehören zur Untergruppe 2.4 von Stoffen der Aromastoffgruppe FGE.19 und wurden in die Aromastoffgruppe FGE 210 aufgenommen. In Bezug auf diese Stoffe hatte die Behörde in ihrem Gutachten von 2009 zur Bewertung der Aromastoffgruppe 210 (4) darauf hingewiesen, dass sie einen strukturellen Warnhinweis auf Genotoxizität in ihrer Molekularstruktur enthalten‚ da es sich um alpha, beta-ungesättigte Ketone handelt, und dass zusätzliche Genotoxizitätsdaten benötigt werden, um die Bedenken hinsichtlich ihrer Genotoxizität gemäß dem Papier der Behörde zur „Genotoxizitätsprüfungsstrategie für Stoffe, die zu Untergruppen der Aromastoffgruppe FGE.19 gehören“ (5) auszuräumen. |
|
(6) |
Am 28. Dezember 2012 wurden für die Untergruppe 2.4 von Stoffen der Aromastoffgruppe FGE.19 Daten übermittelt. |
|
(7) |
Die Behörde bewertete die vorgelegten Daten in ihrer am 19. Februar 2014 veröffentlichten Revision 1 des Gutachtens zum genotoxischen Potenzial der Stoffe der Aromastoffgruppe FGE 210 aus der chemischen Untergruppe 2.4 der Aromastoffgruppe FGE 19 (6). Nach Ansicht der Behörde reichten die vorgelegten Daten jedoch noch nicht aus, um das genotoxische Potenzial der betreffenden Stoffe auszuschließen, und sie forderte deshalb weitere Daten zur Genotoxizität der für diese Untergruppe repräsentativen Stoffe an. |
|
(8) |
Im Jahr 2014 wurden neue Daten übermittelt. Die Behörde bewertete die neuen Daten in der am 10. Juli 2015 veröffentlichten Revision 2 ihres Gutachtens (7). Nach Ansicht der Behörde reichten die neuen Daten jedoch noch immer nicht aus, um das genotoxische Potenzial der betreffenden Stoffe auszuschließen, und sie forderte noch einmal weitere wissenschaftliche Daten zur Genotoxizität der betreffenden Stoffe an. |
|
(9) |
Im Jahr 2016 wurden weitere Daten zu den betreffenden Stoffen übermittelt. Nach Eingang dieser Daten forderte die Behörde mit Schreiben vom 8. November 2016, 9. Februar 2017, 29. Juni 2017 und 8. Februar 2019 weitere Informationen und spezifische Untersuchungen an. Die übermittelten neuen Daten entsprachen jedoch nicht immer den von der Behörde angeforderten Untersuchungen und waren nicht geeignet, die Bedenken der Behörde angemessen auszuräumen. Unter Berücksichtigung all dieser zusätzlich übermittelten Daten nahm die Behörde in der am 22. Mai 2019 veröffentlichten Revision 3 ihres Gutachtens über die FGE.210 (8) eine erneute Bewertung des genotoxischen Potenzials der betreffenden Stoffe vor. Darin kam die Behörde zu dem Schluss, dass die Genotoxizitätsbedenken bei den fünf betreffenden Stoffen nicht ausgeräumt werden können. |
|
(10) |
Da weder die Daten, die innerhalb der ursprünglichen Frist übermittelt wurden, noch die Daten, die die Behörde nach Ablauf dieser Frist nacheinander angefordert hatte, es der Behörde im Jahr 2019 ermöglichten, die in ihrem Gutachten von 2009 geäußerten Bedenken auszuräumen, ist nach der Auffassung der Kommission nicht nachgewiesen worden, dass die betreffenden Stoffe kein Sicherheitsrisiko für die Gesundheit der Verbraucher darstellen. Auf der Grundlage der wissenschaftlichen Nachweise, die im Rahmen von Anhang I Teil A der Verordnung (EG) Nr. 1334/2008 für die Stoffe bis zum Abschluss ihrer Bewertung vorgelegt wurden, erfüllt die Verwendung der betreffenden Stoffe nicht die allgemeinen Bedingungen für die Verwendung von Aromen gemäß Artikel 4 der Verordnung (EG) Nr. 1334/2008. |
|
(11) |
Zum Schutz der menschlichen Gesundheit sollten die betreffenden Stoffe deshalb unverzüglich aus der Unionsliste gestrichen werden. |
|
(12) |
Anhang I Teil A der Verordnung (EG) Nr. 1334/2008 sollte daher entsprechend geändert werden. |
|
(13) |
Aus technischen Gründen sollten Übergangsfristen für Lebensmittel festgelegt werden, denen einer oder mehrere der fünf Aromastoffe zugesetzt wurden und die bereits vor Inkrafttreten dieser Verordnung in Verkehr gebracht oder aus Drittländern in die Union versandt wurden oder unterwegs waren. Die Übergangsfrist sollte nicht für Zubereitungen gelten, denen einer oder mehrere dieser fünf Aromastoffe zugesetzt wurden und die nicht als solche zum Verzehr bestimmt sind, da den Herstellern die Zusammensetzung dieser Zubereitungen bei ihrer Herstellung bekannt ist. |
|
(14) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für Pflanzen, Tiere, Lebensmittel und Futtermittel — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Anhang I Teil A der Verordnung (EG) Nr. 1334/2008 wird gemäß dem Anhang der vorliegenden Verordnung geändert.
Artikel 2
(1) Lebensmittel, denen einer der im Anhang dieser Verordnung aufgeführten Aromastoffe zugesetzt wurde und die vor dem Datum des Inkrafttretens dieser Verordnung rechtmäßig in Verkehr gebracht wurden, dürfen bis zu ihrem Mindesthaltbarkeits- oder Verbrauchsdatum weiterhin in Verkehr gebracht werden.
(2) Lebensmittel, die in die Union eingeführt werden und denen einer der im Anhang dieser Verordnung aufgeführten Aromastoffe zugesetzt wurde, dürfen bis zu ihrem Mindesthaltbarkeits- oder Verbrauchsdatum in Verkehr gebracht werden, wenn der Einführer dieser Lebensmittel nachweisen kann, dass sie aus dem betreffenden Drittland versandt wurden und sich auf dem Weg in die Union befanden, bevor diese Verordnung in Kraft trat.
(3) Die in den Absätzen 1 und 2 genannten Übergangsfristen gelten nicht für Zubereitungen, die nicht als solche zum Verzehr bestimmt sind und denen einer oder mehrere dieser fünf Aromastoffe zugesetzt wurden.
(4) Zubereitungen im Sinne dieser Verordnung sind Gemische aus einem oder mehreren Aromen, denen auch andere Lebensmittelzutaten wie Lebensmittelzusatzstoffe, Lebensmittelenzyme oder Trägerstoffe zugesetzt werden können, um ihre Lagerung, ihren Verkauf, ihre Standardisierung, ihre Verdünnung oder ihre Lösung zu erleichtern.
Artikel 3
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 12. November 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 354 vom 31.12.2008, S. 34.
(2) ABl. L 354 vom 31.12.2008, S. 1.
(3) Durchführungsverordnung (EU) Nr. 872/2012 der Kommission vom 1. Oktober 2012 zur Festlegung der Liste der Aromastoffe gemäß der Verordnung (EG) Nr. 2232/96 des Europäischen Parlaments und des Rates, zur Aufnahme dieser Liste in Anhang I der Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates sowie zur Aufhebung der Verordnung (EG) Nr. 1565/2000 der Kommission und der Entscheidung 1999/217/EG der Kommission (ABl. L 267 vom 2.10.2012, S. 1).
(4) Scientific Opinion on Flavouring Group Evaluation 210: alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19 (Wissenschaftliches Gutachten zur Bewertung der Aromastoffgruppe 210: alpha, beta-ungesättigte alizyklische Ketone und Vorstufen der chemischen Untergruppe 2.4 der FGE.19), EFSA Journal (2009) ON-1030, 1–18. https://efsa.onlinelibrary.wiley.com/doi/pdf/10.2903/j.efsa.2009.1030.
(5) Genotoxicity Test Strategy for Substances belonging to Subgroups of FGE.19 — Statement of the Panel on Food Contact Materials, Enzymes, Flavourings and Processing Aids (CEF) (Genotoxizitätsprüfungsstrategie für Stoffe, die zu Untergruppen der FGE.19 gehören — Erklärung des Gremiums für Materialien, die mit Lebensmitteln in Berührung kommen, Enzyme, Aromastoffe und Hilfsstoffe), EFSA Journal (2008) 854, 1–5. https://efsa.onlinelibrary.wiley.com/doi/pdf/10.2903/j.efsa.2008.854.
(6) Wissenschaftliches Gutachten zur Bewertung der Aromastoffgruppe 210, Revision 1 (FGE.210Rev1): Consideration of genotoxic potential for alpha,beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19 (Betrachtung des genotoxischen Potenzials alpha, beta-ungesättigter alizyklischer Ketone und Vorstufen der chemischen Untergruppe 2.4 der FGE.19), EFSA Journal 2014;12(2):3587, 35 ff. doi:10.2903/j.efsa.2014.3587.
(7) Wissenschaftliches Gutachten zur Bewertung der Aromastoffgruppe 210, Revision 2 (FGE.210Rev2): Consideration of genotoxic potential for alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19 (Betrachtung des genotoxischen Potenzials alpha, beta-ungesättigter alizyklischer Ketone und Vorstufen der chemischen Untergruppe 2.4 der FGE.19), 10. Juli 2015. EFSA Journal 2015;13(7):4172.doi:10.293/j.efsa.2015.4172.
(8) Wissenschaftliches Gutachten zur Bewertung der Aromastoffgruppe 210, Revision 3 (FGE.210Rev3): Consideration of genotoxic potential for alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19 (Betrachtung des genotoxischen Potenzials alpha, beta-ungesättigter alizyklischer Ketone und Vorstufen der chemischen Untergruppe 2.4 der FGE.19), EFSA Journal 2019; 17(5):5676.
ANHANG
In Anhang I Teil A Abschnitt 2 der Verordnung (EG) Nr. 1334/2008 werden folgende Einträge gestrichen:
|
„07.130 |
delta-Damascon |
57378-68-4 |
386 |
|
|
|
2 |
JECFA/EFSA |
|
07.134 |
alpha-Damascon |
43052-87-5 |
385 |
11053 |
|
|
2 |
JECFA/EFSA |
|
07.225 |
cis-1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)but-2-en-1-on |
23726-94-5 |
|
|
Mindestens 92 %; sekundäre Komponente 4 % trans-Isomer |
|
2 |
EFSA |
|
07.226 |
trans-1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)but-2-en-1-on |
24720-09-0 |
|
|
|
|
2 |
EFSA |
|
07.231 |
alpha-Damascenon |
35044-63-4 |
|
|
|
|
2 |
EFSA“ |
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/31 |
VERORDNUNG (EU) 2020/1682 DER KOMMISSION
vom 12. November 2020
zur Änderung von Anhang III der Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates über kosmetische Mittel
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates vom 30. November 2009 über kosmetische Mittel (1), insbesondere auf Artikel 31 Absatz 1,
in Erwägung nachstehender Gründe:
|
(1) |
Die Stoffe 2-Hydroxyethylmethacrylat (HEMA) und 11,14-Dioxa-2,9-diazaheptadec-16-ensäure, 4,4,6,16-Tetramethyl-10,15-dioxo, 2-[(2-methyl-1-oxo-2-propenyl)oxy]ethylester (Di-HEMA-Trimethylhexyldicarbamat oder Di-HEMA-TMHDC) unterliegen derzeit keinen Verboten oder Beschränkungen gemäß der Verordnung (EG) Nr. 1223/2009. |
|
(2) |
Am 2. Juli 2014 erließ die schwedische Agentur für Medizinprodukte, die für die Zwecke der Verordnung (EG) Nr. 1223/2009 zuständige schwedische Behörde, einen Beschluss gemäß Artikel 27 der Verordnung (EG) Nr. 1223/2009, mit dem vorläufige restriktive Maßnahmen für ein Nagelkosmetikum eingeführt wurden, das eine große Zahl unerwünschter Wirkungen verursacht hatte, und teilte diesen mit. Als Stoffe, die diese unerwünschten Wirkungen verursachen dürften, wurden HEMA und Di-HEMA-TMHDC ermittelt. |
|
(3) |
Die schwedische Agentur für Medizinprodukte unterrichtete unverzüglich nach Artikel 27 Absatz 2 der Verordnung (EG) Nr. 1223/2009 die Kommission und die zuständigen Behörden der anderen Mitgliedstaaten über die ergriffenen Maßnahmen und teilte ihnen alle sachdienlichen Daten mit. |
|
(4) |
Der Wissenschaftliche Ausschuss „Verbrauchersicherheit“ (SCCS) kam in seiner Stellungnahme vom 21./22. Juni 2018 (2) zu dem Schluss‚ dass „HEMA und Di-HEMA-TMHDC bei angemessener Anwendung auf die Nagelplatte (…) als Teil eines künstlichen Nagelmodellierungssystems kein Risiko einer Sensibilisierung darstellen dürften, sofern ihre Verwendung auf die Nagelplatte beschränkt ist und der Kontakt mit der angrenzenden Haut vermieden wird“. Der SCCS kam ferner zu dem Schluss, dass „sowohl HEMA als auch Di-HEMA-TMHDC leichte bis mittelgradige Sensibilisatoren sind und unter normalen und vernünftigerweise vorhersehbaren Verwendungsbedingungen das Risiko einer Sensibilisierung aufgrund einer missbräuchlichen Verwendung der Mittel, einer unsachgemäß durchgeführten Anwendung oder einer unbeabsichtigten Kontamination der an die Nägel angrenzenden Haut bergen“. |
|
(5) |
Nach Artikel 3 der Verordnung (EG) Nr. 1223/2009 müssen auf dem Markt bereitgestellte kosmetische Mittel bei normaler oder vernünftigerweise vorhersehbarer Verwendung für die menschliche Gesundheit sicher sein. |
|
(6) |
Bei der Beurteilung der „normalen oder vernünftigerweise vorhersehbaren Verwendung“ ist der möglichen missbräuchlichen, unsachgemäßen oder unbeabsichtigten Verwendung Rechnung zu tragen. Bei Mitteln, die einen hohen Genauigkeitsgrad erfordern, müssen Situationen berücksichtigt werden, in denen sie nicht ausreichend präzise angewendet werden. |
|
(7) |
Die in einigen Mitgliedstaaten gemeldeten Fälle von Sensibilisierung für Nagelmittel, die HEMA und Di-HEMA-TMHDC enthalten, führen die Kommission zu dem Schluss, dass die Gefahr besteht, dass solche Produkte mit unzureichender Genauigkeit angewendet werden, was zu einem Kontakt mit der Haut in der Nähe der Nagelplatte führt. |
|
(8) |
Es sollte zwischen der gewerblichen Verwendung und der Verwendung kosmetischer Mittel durch Verbraucher unterschieden werden. An gewerbliche Anwender werden höhere Sicherheitsanforderungen gestellt. Insbesondere wird von gewerblichen Anwendern erwartet, dass sie im Vergleich zu Verbrauchern über mehr Fähigkeiten, Erfahrungen und Kenntnisse in Bezug auf die Verwendung eines kosmetischen Mittels verfügen. |
|
(9) |
Mögliche Gesundheits- und Sicherheitsrisiken für Berufsangehörige sind in bestimmten Richtlinien der Union geregelt, in denen Mindestanforderungen festgelegt sind, insbesondere in den Richtlinien 89/391/EWG (3) und 98/24/EG (4) des Rates. Es können zusätzliche Vorschriften für die berufliche Sicherheit gelten. |
|
(10) |
Da in der Stellungnahme des SCCS die Stoffe HEMA und Di-HEMA-TMHDC in Nagelmitteln nur als sicher gelten, wenn sie auf der Nagelplatte aufgetragen werden, und da unter „normaler oder vernünftigerweise vorhersehbarer Verwendung“ die Möglichkeit der Anwendung auf der Haut neben der Nagelplatte berücksichtigt werden sollte, besteht ein potenzielles Risiko für die menschliche Gesundheit durch die Verwendung von HEMA und Di-HEMA-TMHDC in Nagelmitteln. |
|
(11) |
Da erwartet wird, dass die Verwendung von Nagelmitteln, die HEMA und Di-HEMA-TMHDC enthalten, durch gewerbliche Anwender sicherer ist, sollten solche Produkte nur von gewerblichen Anwendern verwendet werden, weshalb auf der Verpackung solcher Produkte der Hinweis „Nur für gewerbliche Verwendung“ angebracht werden sollte. |
|
(12) |
Um sowohl die gewerblichen Anwender als auch die Verbraucher auf das potenzielle Gesundheitsrisiko aufmerksam zu machen, sollte auf der Verpackung von Nagelmitteln, die HEMA und Di-HEMA-TMHDC enthalten, der Hinweis „Erzeugnis kann eine allergische Reaktion hervorrufen“ hinzugefügt werden. |
|
(13) |
Daher sollten die von Schweden ergriffenen Schutzmaßnahmen als gerechtfertigt angesehen werden. Folglich ist es erforderlich, die Verwendung von HEMA und Di-HEMA-TMHDC in Nagelmitteln zu beschränken. |
|
(14) |
Anhang III der Verordnung (EG) Nr. 1223/2009 sollte daher entsprechend geändert werden. |
|
(15) |
Es sollte ein angemessener Zeitraum vorgesehen werden, damit die Industrie den neuen Anforderungen Rechnung tragen kann. |
|
(16) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für kosmetische Mittel — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Anhang III der Verordnung (EG) Nr. 1223/2009 wird gemäß dem Anhang der vorliegenden Verordnung geändert.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 12. November 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 342 vom 22.12.2009, S. 59.
(2) SCCS/1592/17;
https://ec.europa.eu/health/sites/health/files/scientific_committees/consumer_safety/docs/sccs_o_214.pdf
(3) Richtlinie 89/391/EWG des Rates vom 12. Juni 1989 über die Durchführung von Maßnahmen zur Verbesserung der Sicherheit und des Gesundheitsschutzes der Arbeitnehmer bei der Arbeit (ABl. L 183 vom 29.6.1989, S. 1).
(4) Richtlinie 98/24/EG des Rates vom 7. April 1998 zum Schutz von Gesundheit und Sicherheit der Arbeitnehmer vor der Gefährdung durch chemische Arbeitsstoffe bei der Arbeit (vierzehnte Einzelrichtlinie im Sinne des Artikels 16 Absatz 1 der Richtlinie 89/391/EWG) (ABl. L 131 vom 5.5.1998, S. 11).
ANHANG
In Anhang III der Verordnung (EG) Nr. 1223/2009 werden in der Tabelle die folgenden Einträge eingefügt:
|
Laufende Nummer |
Bezeichnung der Stoffe |
Einschränkungen |
Wortlaut der Anwendungsbedingungen und Warnhinweise |
|||||
|
Chemische Bezeichnung/ INN |
Gemeinsame Bezeichnung im Glossar der Bestandteile |
CAS-Nummer |
EG-Nummer |
Art des Mittels, Körperteile |
Höchstkonzentration in der gebrauchsfertigen Zubereitung |
Sonstige |
|
|
|
a |
b |
c |
d |
e |
f |
g |
h |
i |
|
„313 |
2-Hydroxyethylmethacrylat (*1) |
HEMA |
868-77-9 |
212-782-2 |
Nagelmittel |
|
Nur gewerbliche Verwendung |
Nur für gewerbliche Verwendung Kann eine allergische Reaktion hervorrufen |
|
314 |
11,14-Dioxa-2,9-diazaheptadec-16-ensäure, 4,4,6,16-Tetramethyl-10,15-dioxo, 2-[(2-methyl-1-oxo-2-propenyl)oxy]ethylester (*2) |
DI-HEMA-TRIMETHYLHEXYLDICARBAMATE |
41137-60-4/72869-86-4 |
255-239-5/276-957-5 |
Nagelmittel |
|
Nur gewerbliche Verwendung |
Nur für gewerbliche Verwendung Kann eine allergische Reaktion hervorrufen |
(*1) Ab dem 3. Juni 2021 dürfen kosmetische Mittel, die diesen Stoff enthalten und diesen Bedingungen nicht entsprechen, auf dem Unionsmarkt nicht mehr in Verkehr gebracht werden. Ab dem 3. September 2021 dürfen kosmetische Mittel, die diesen Stoff enthalten und diesen Bedingungen nicht entsprechen, auf dem Unionsmarkt nicht mehr bereitgestellt werden.
(*2) Ab dem 3. Juni 2021 dürfen kosmetische Mittel, die diesen Stoff enthalten und diesen Bedingungen nicht entsprechen, auf dem Unionsmarkt nicht mehr in Verkehr gebracht werden. Ab dem 3. September 2021 dürfen kosmetische Mittel, die diesen Stoff enthalten und diesen Bedingungen nicht entsprechen, auf dem Unionsmarkt nicht mehr bereitgestellt werden.“
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/34 |
VERORDNUNG (EU) 2020/1683 DER KOMMISSION
vom 12. November 2020
zur Änderung der Anhänge II und III der Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates über kosmetische Mittel
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates vom 30. November 2009 über kosmetische Mittel (1), insbesondere auf Artikel 31 Absatz 1,
in Erwägung nachstehender Gründe:
|
(1) |
Im Anschluss an die Veröffentlichung einer wissenschaftlichen Studie über die Anwendung von permanenten Haarfärbemitteln und das Auftreten von Blasenkrebs („Use of permanent hair dyes and bladder cancer risk“) im Jahr 2001 kam der Wissenschaftliche Ausschuss „Kosmetische Mittel und für den Verbraucher bestimmte Non-Food-Erzeugnisse“, der später mit dem Beschluss 2004/210/EG der Kommission (2) durch den Wissenschaftlichen Ausschuss „Konsumgüter“ (SCCP) ersetzt wurde, zu dem Ergebnis, dass die möglichen gesundheitlichen Risiken der Anwendung von Haarfärbemitteln Anlass zur Besorgnis geben. |
|
(2) |
Der SCCP empfahl des Weiteren eine umfassende Sicherheitsbewertungsstrategie für Inhaltsstoffe von Haarfärbemitteln samt Vorschriften für die Prüfung dieser Stoffe auf ihre mögliche Genotoxizität und Karzinogenität. |
|
(3) |
Aufgrund der Gutachten des SCCP vereinbarte die Kommission mit den Mitgliedstaaten und Interessenträgern eine Gesamtstrategie zur Regulierung der in Haarfärbemitteln verwendeten Stoffe, der zufolge die Industrie Dossiers mit aktualisierten wissenschaftlichen Daten zur Sicherheit der Inhaltsstoffe vorzulegen hatte, auf deren Grundlage der SCCP eine Risikobewertung vornehmen konnte. |
|
(4) |
Der SCCP, der mit dem Beschluss 2008/721/EG der Kommission (3) durch den Wissenschaftlichen Ausschuss „Verbrauchersicherheit“ (SCCS) ersetzt wurde, hat die Sicherheit einzelner in Haarfärbemitteln verwendeter Stoffe bewertet, für die die Industrie aktualisierte Dossiers vorgelegt hatte. |
|
(5) |
Auf der Grundlage der Überprüfung durch den SCCS ist es erforderlich, zur Gewährleistung der Sicherheit von Haarfärbemitteln für die menschliche Gesundheit unter Berücksichtigung der abschließenden Gutachten des SCCS die Verwendung der folgenden drei Haarfärbestoffe zu verbieten: 1,2,4-Trihydroxybenzol (4), 2-((4-Amino-2-nitrophenyl)amino)-benzoesäure (5) und 4-Amino-3-hydroxytoluol (6). Darüber hinaus ist es unter Berücksichtigung der abschließenden Gutachten des SCCS bezüglich sechs weiterer Haarfärbestoffe, nämlich Dimethylpiperazinium Aminopyrazolopyridin HCl (7), Methylimidazoliumpropyl-p-Phenylendiamin HCl (8), HC Orange Nr. 6 (9), Acid Orange 7 (10), Tetrabromphenolblau (11) und Indigofera Tinctoria (12), angemessen, Höchstkonzentrationen für ihre Verwendung in Haarfärbemitteln festzulegen. |
|
(6) |
In der in Punkt 1 Buchstabe c der Präambel der Anhänge II bis VI der Verordnung (EG) Nr. 1223/2009 festgelegten Definition von Haarmitteln ist das Auftragen von Haarfärbestoffen auf Wimpern nicht eingeschlossen. Begründet wurde dies damit, dass das Risikoniveau bei einer Anwendung kosmetischer Mittel auf dem Kopfhaar und auf den Wimpern jeweils unterschiedlich ist. Daher war eine spezielle Risikobewertung für die Verwendung von Haarfärbestoffen auf den Wimpern erforderlich. |
|
(7) |
Der Stoff 2-Methoxymethyl-p-Phenylendiamin und sein Sulfat sind unter der Eintragsnummer 292 in Anhang III der Verordnung (EG) Nr. 1223/2009 aufgelistet. Unter Berücksichtigung der Schlussfolgerungen des aktuellen Gutachtens des SCCS (13) bezüglich der Verwendung dieser Stoffe für Wimpern, sollte der Geltungsumfang der für diese Stoffe geltenden Beschränkungen auf Wimpernfärbemittel ausgedehnt werden. |
|
(8) |
Um jedoch jegliches Risiko im Zusammenhang mit der Selbstanwendung von Wimpernfärbemitteln, die 2-Methoxymethyl-p-Phenylendiamin und sein Sulfat enthalten, durch Verbraucher zu vermeiden, sollten diese Stoffe nur für die gewerbliche Verwendung zulässig sein. |
|
(9) |
Damit Verbraucher und gewerbliche Verwender über mögliche Nebenwirkungen der Anwendung von Haarfärbemitteln und Wimpernfärbemitteln aufgeklärt werden und um das Risiko der Hautsensibilisierung durch diese Mittel zu verringern, sollten auf dem Etikett geeignete Warnhinweise angebracht werden. |
|
(10) |
Die Verordnung (EG) Nr. 1223/2009 sollte daher entsprechend geändert werden. |
|
(11) |
Es sollten angemessene Fristen gewährt werden, damit die Industrie Anpassungen an die neuen Anforderungen vornehmen und die betreffenden kosmetischen Mittel auslaufen lassen kann, welche diese Anforderungen nicht erfüllen. |
|
(12) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für kosmetische Mittel — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Die Verordnung (EG) Nr. 1223/2009 wird entsprechend dem Anhang der vorliegenden Verordnung geändert.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 12. November 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 342 vom 22.12.2009, S. 59.
(2) Beschluss 2004/210/EG der Kommission vom 3. März 2004 zur Einsetzung Wissenschaftlicher Ausschüsse im Bereich Verbrauchersicherheit, öffentliche Gesundheit und Umwelt (ABl. L 66 vom 4.3.2004, S. 45).
(3) Beschluss 2008/721/EG der Kommission vom 5. September 2008 zur Einrichtung einer Beratungsstruktur der Wissenschaftlichen Ausschüsse und Sachverständigen im Bereich Verbrauchersicherheit, öffentliche Gesundheit und Umwelt und zur Aufhebung des Beschlusses 2004/210/EG (ABl. L 241 vom 10.9.2008, S. 21).
(4) SCCS/1598/18
(5) SCCS/1497/12
(6) SCCS/1400/11
(7) SCCS/1584/17
(8) SCCS/1609/19
(9) SCCS/1579/16
(10) SCCS/1536/14
(11) SCCS/1610/19
(12) SCCS/1615/20
(13) SCCS/1603/18
ANHANG
Die Verordnung (EG) Nr. 1223/2009 wird wie folgt geändert:
|
1. |
In Anhang II werden in der Tabelle folgende Einträge angefügt:
|
|||||||||||||||||||
|
2. |
In Anhang III wird die Tabelle wie folgt geändert:
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(*1) Ab dem 3. September 2021 dürfen Haarfärbemittel und Mittel zum Färben von Wimpern, die diesen Stoff enthalten, auf dem Unionsmarkt nicht mehr in Verkehr gebracht werden.
Ab dem 3. Juni 2022 dürfen Haarfärbemittel und Mittel zum Färben von Wimpern, die diesen Stoff enthalten, auf dem Unionsmarkt nicht mehr bereitgestellt werden.“
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/42 |
VERORDNUNG (EU) 2020/1684 DER KOMMISSION
vom 12. November 2020
zur Änderung von Anhang VI der Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates über kosmetische Mittel
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates vom 30. November 2009 über kosmetische Mittel (1), insbesondere auf Artikel 31 Absatz 2,
in Erwägung nachstehender Gründe:
|
(1) |
Der Wissenschaftliche Ausschuss „Verbrauchersicherheit“ (SCCS) kam in seiner Stellungnahme vom 13. Dezember 2019 (2) (im Folgenden „Stellungnahme des SCCS“) zu dem Schluss, dass die Verwendung von Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetat als UV-Filter in einer Höchstkonzentration von 3 % in kosmetischen Mitteln unbedenklich ist. Da keine Daten zur Inhalationstoxizität vorlagen, wurde diese in der Stellungnahme des SCCS nicht bewertet. Die Stellungnahme des SCCS ist daher nicht auf sprühbare kosmetische Mittel anwendbar, die durch Inhalation zu einer Exposition der Lunge des Endnutzers führen könnten. |
|
(2) |
Der SCCS kam in seiner Stellungnahme außerdem zu dem Schluss, dass Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetat ein sekundäres Amin ist und daher stark zu Nitrosierung und zur Bildung von Nitrosamin neigt. Es sollte nicht in Kombination mit nitrosierenden Stoffen verwendet werden. Der Gehalt an Nitrosamin sollte weniger als 50 ppb betragen. |
|
(3) |
Angesichts der Stellungnahme des SCCS und zur Anpassung an den technischen und wissenschaftlichen Fortschritt sollte die Verwendung von Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetat als UV-Filter in kosmetischen Mitteln bis zu einer Höchstkonzentration von 3 % zugelassen werden, mit Ausnahme von Anwendungen, die durch Inhalation zur Exposition der Lunge des Endnutzers führen können. |
|
(4) |
Anhang VI der Verordnung (EG) Nr. 1223/2009 sollte daher entsprechend geändert werden. |
|
(5) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für kosmetische Mittel — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Anhang VI der Verordnung (EG) Nr. 1223/2009 wird gemäß dem Anhang der vorliegenden Verordnung geändert.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 12. November 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 342 vom 22.12.2009, S. 59.
(2) SCCS/1605/19.
ANHANG
In Anhang VI der Verordnung (EG) Nr. 1223/2009 wird der folgende Eintrag eingefügt:
|
Laufende Nummer |
Bezeichnung der Stoffe |
Bedingungen |
Wortlaut der Anwendungsbedingungen und Warnhinweise |
|||||||||||
|
Chemische Bezeichnung/INN/XAN |
Gemeinsame Bezeichnung im Glossar der Bestandteile |
CAS-Nummer |
EG-Nummer |
Art des Mittels, Körperteile |
Höchstkonzentration in der gebrauchsfertigen Zubereitung |
Sonstige |
||||||||
|
a |
b |
c |
d |
e |
f |
g |
h |
i |
||||||
|
„32 |
2-Ethoxyethyl (2Z)-2-cyano-2-[3-(3-methoxypropylamino) cyclohex-2-en-1-ylidene]acetat |
Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetate |
1419401-88-9 |
700-860-3 |
|
3 % |
|
|
||||||
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/44 |
DURCHFÜHRUNGSVERORDNUNG (EU) 2020/1685 DER KOMMISSION
vom 12. November 2020
zur Änderung der Verordnung (EU) Nr. 37/2010 in Bezug auf die Einstufung des Stoffs Bupivacain hinsichtlich der Rückstandshöchstmenge
(Text von Bedeutung für den EWR)
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EG) Nr. 470/2009 des Europäischen Parlaments und des Rates vom 6. Mai 2009 über die Schaffung eines Gemeinschaftsverfahrens für die Festsetzung von Höchstmengen für Rückstände pharmakologisch wirksamer Stoffe in Lebensmitteln tierischen Ursprungs, zur Aufhebung der Verordnung (EWG) Nr. 2377/90 des Rates und zur Änderung der Richtlinie 2001/82/EG des Europäischen Parlaments und des Rates und der Verordnung (EG) Nr. 726/2004 des Europäischen Parlaments und des Rates (1), insbesondere auf Artikel 14 in Verbindung mit Artikel 17,
gestützt auf die Stellungnahmen der Europäischen Arzneimittel-Agentur, die am 20. Februar 2020 und am 18. Juni 2020 vom Ausschuss für Tierarzneimittel abgegeben wurden,
in Erwägung nachstehender Gründe:
|
(1) |
Gemäß Artikel 17 der Verordnung (EG) Nr. 470/2009 werden die Höchstmengen an Rückständen pharmakologisch wirksamer Stoffe, die in der Union zur Verwendung in Arzneimitteln für Tiere, die der Lebensmittelgewinnung dienen, oder in Biozidprodukten, die in der Tierhaltung eingesetzt werden, bestimmt sind, in einer Verordnung festgelegt. |
|
(2) |
Tabelle 1 im Anhang der Verordnung (EU) Nr. 37/2010 der Kommission (2) enthält eine Liste pharmakologisch wirksamer Stoffe und deren Einstufung hinsichtlich der Rückstandshöchstmengen in Lebensmitteln tierischen Ursprungs. |
|
(3) |
Der Stoff Bupivacain ist in dieser Tabelle nicht aufgeführt. |
|
(4) |
Der Europäischen Arzneimittel-Agentur (im Folgenden „Agentur“) liegt ein Antrag auf Festsetzung von Rückstandshöchstmengen für Bupivacain zur Anwendung auf der Haut und zur epiläsionalen Anwendung nur bei Schweinen (bei bis zu 7 Tage alten Ferkeln) und bei Rindern (bei bis zu 2 Monate alten Kälbern) vor. |
|
(5) |
Die Agentur gelangte auf Grundlage der Stellungnahme des Ausschusses für Tierarzneimittel zu dem Schluss, dass die Festlegung einer Rückstandshöchstmenge für Bupivacain bei Schweinen und Rindern innerhalb dieser Altersgrenzen zum Schutz der menschlichen Gesundheit nicht erforderlich ist, und empfahl die Einstufung „keine Rückstandshöchstmenge(n) erforderlich“. |
|
(6) |
Gemäß Artikel 5 der Verordnung (EG) Nr. 470/2009 ist die Agentur verpflichtet, die Anwendung von Rückstandshöchstmengen, die für einen pharmakologisch wirksamen Stoff in einem bestimmten Lebensmittel bzw. in Bezug auf eine oder mehrere Tierarten festgesetzt wurden, auf ein anderes von derselben Tierart stammendes Lebensmittel bzw. auf andere Tierarten zu erwägen. |
|
(7) |
Nach Auffassung der Agentur ist es aufgrund unzureichender Daten derzeit nicht angezeigt, die Einstufung „keine Rückstandshöchstmenge(n) erforderlich“ für Bupivacain von Schweinen und Rindern auf andere, der Lebensmittelgewinnung dienende Tierarten zu extrapolieren. |
|
(8) |
Die Verordnung (EU) Nr. 37/2010 sollte daher entsprechend geändert werden. |
|
(9) |
Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für Tierarzneimittel — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
Der Anhang der Verordnung (EU) Nr. 37/2010 wird gemäß dem Anhang der vorliegenden Verordnung geändert.
Artikel 2
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 12. November 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 152 vom 16.6.2009, S. 11.
(2) Verordnung (EU) Nr. 37/2010 der Kommission vom 22. Dezember 2009 über pharmakologisch wirksame Stoffe und ihre Einstufung hinsichtlich der Rückstandshöchstmengen in Lebensmitteln tierischen Ursprungs (ABl. L 15 vom 20.1.2010, S. 1).
ANHANG
In Tabelle 1 des Anhangs der Verordnung (EU) Nr. 37/2010 wird an der alphabetisch richtigen Stelle ein Eintrag für folgenden Stoff eingefügt:
|
Pharmakologisch wirksame(r) Stoff(e) |
Markerrückstand |
Tierart(en) |
Rückstandshöchstmenge(n) |
Zielgewebe |
Sonstige Vorschriften (gemäß Artikel 14 Absatz 7 der Verordnung (EG) Nr. 470/2009) |
Therapeutische Einstufung |
|
„Bupivacain |
NICHT ZUTREFFEND |
Schweine |
Keine Rückstandshöchstmenge(n) erforderlich |
NICHT ZUTREFFEND |
Nur zur Verwendung bei bis zu 7 Tage alten Ferkeln. Nur zur Anwendung auf der Haut und zur epiläsionalen Anwendung. |
Lokalanästhetikum“ |
|
Rinder |
Nur zur Verwendung bei bis zu 2 Monate alten Kälbern. Nur zur Anwendung auf der Haut und zur epiläsionalen Anwendung. |
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/47 |
DURCHFÜHRUNGSVERORDNUNG (EU) 2020/1686 DER KOMMISSION
vom 12. November 2020
zur zollamtlichen Erfassung der Einfuhren bestimmter warmgewalzter Flacherzeugnisse aus Eisen, nicht legiertem Stahl oder anderem legiertem Stahl mit Ursprung in der Türkei
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) 2016/1036 des Europäischen Parlaments und des Rates vom 8. Juni 2016 über den Schutz gegen gedumpte Einfuhren aus nicht zur Europäischen Union gehörenden Ländern (1) (im Folgenden „Grundverordnung“), insbesondere auf Artikel 14 Absatz 5,
nach Unterrichtung der Mitgliedstaaten,
in Erwägung nachstehender Gründe:
|
(1) |
Am 14. Mai 2020 veröffentlichte die Europäische Kommission (im Folgenden „Kommission“) im Amtsblatt der Europäischen Union (2) eine Bekanntmachung (im Folgenden „Einleitungsbekanntmachung“) über die Einleitung eines Antidumpingverfahrens (im Folgenden „Antidumpingverfahren“) betreffend die Einfuhren bestimmter warmgewalzter Flacherzeugnisse aus Eisen, nicht legiertem oder anderem legiertem Stahl mit Ursprung in der Türkei in die Union; das Verfahren wurde auf einen Antrag hin eingeleitet, der am 31. März 2020 von Eurofer (im Folgenden „Antragsteller“) im Namen von Herstellern gestellt wurde, auf die mehr als 25 % der gesamten Unionsproduktion von bestimmten warmgewalzten Flacherzeugnissen aus Eisen, nicht legiertem oder anderem legiertem Stahl entfallen. |
1. ZOLLAMTLICH ZU ERFASSENDE WARE
|
(2) |
Bei der zollamtlich zu erfassenden Ware (im Folgenden „betroffene Ware“) handelt es sich um Flacherzeugnisse aus Eisen, nicht legiertem Stahl oder anderem legiertem Stahl, auch in Rollen (Coils) (auch zugeschnittene Waren und Schmalbanderzeugnisse („narrow strip“)), nur warmgewalzt, weder plattiert noch überzogen. Diese Waren werden derzeit unter den KN-Codes 7208 10 00, 7208 25 00, 7208 26 00, 7208 27 00, 7208 36 00, 7208 37 00, 7208 38 00, 7208 39 00, 7208 40 00, 7208 52 10, 7208 52 99, 7208 53 10, 7208 53 90, 7208 54 00, 7211 13 00, 7211 14 00, 7211 19 00, ex 7225 19 10 (TARIC-Code 7225191090), 7225 30 90, ex 7225 40 60 (TARIC-Code 7225406090), 7225 40 90, ex 7226 19 10 (TARIC-Code 7226191090), 7226 91 91 und 7226 91 99 eingereiht. Die KN- und TARIC-Codes werden nur informationshalber angegeben. |
|
(3) |
Nicht zollamtlich zu erfassen sind (i) Erzeugnisse aus nicht rostendem Stahl und kornorientiertem Siliciumelektrostahl; (ii) Erzeugnisse aus Werkzeugstahl und Schnellarbeitsstahl; (iii) Erzeugnisse, nicht in Rollen, ohne Oberflächenmuster, mit einer Dicke von mehr als 10 mm und einer Breite von 600 mm oder mehr; (iv) Erzeugnisse, nicht in Rollen, ohne Oberflächenmuster, mit einer Dicke von 4,75 mm bis 10 mm und einer Breite von 2 050 mm oder mehr. |
2. ANTRAG
|
(4) |
Am 17. September 2020 reichte der Antragsteller einen Antrag nach Artikel 14 Absatz 5 der Grundverordnung auf zollamtliche Erfassung ein. Der Antragsteller beantragte, dass die Einfuhren der betroffenen Ware zollamtlich erfasst werden, sodass Maßnahmen gegenüber diesen Einfuhren vom Zeitpunkt der zollamtlichen Erfassung an rückwirkend angewendet werden können. |
|
(5) |
Die folgenden interessierten Parteien haben zu dem Antrag Stellung genommen: die Regierung der Türkei, das Konsortium der Verwender, die Gruppen Colakoglu und Erdemir sowie Habas (ausführende Hersteller), der Verband der türkischen Stahlausführer (im Folgenden „ÇİB“) und der Verband der türkischen Stahlerzeuger (im Folgenden „TCUD“). |
3. GRÜNDE FÜR DIE ZOLLAMTLICHE ERFASSUNG
|
(6) |
Nach Artikel 14 Absatz 5 der Grundverordnung kann die Kommission die Zollbehörden anweisen, geeignete Schritte zur zollamtlichen Erfassung der Einfuhren zu unternehmen, sodass in der Folge Maßnahmen gegenüber diesen Einfuhren vom Zeitpunkt dieser zollamtlichen Erfassung an eingeführt werden können, sofern sämtliche Voraussetzungen der Grundverordnung erfüllt sind. Die zollamtliche Erfassung der Einfuhren kann auf einen Antrag des Wirtschaftszweigs der Union vorgenommen werden, wenn dieser Antrag ausreichende Beweise dafür enthält, dass die Maßnahme gerechtfertigt ist. |
|
(7) |
Der Antragsteller brachte vor, dass es ausgehend von den jüngsten zur Verfügung stehenden statistischen Daten nach der Einleitung der Untersuchung zu einem erheblichen Anstieg der Einfuhren gekommen sei, der die Abhilfewirkung der endgültigen Zölle wahrscheinlich ernsthaft beeinträchtigen würde. Seitens der Türkei habe es schon früher über einen längeren Zeitraum hinweg Dumpingfälle gegeben und die Einführer hätten Kenntnis von den Dumpingpraktiken in der Türkei gehabt oder haben müssen. |
|
(8) |
Die Kommission prüfte den Antrag im Lichte des Artikels 10 Absatz 4 der Grundverordnung. Die Kommission prüfte, ob die Einführer von dem Dumping, von seinem Ausmaß und von der mutmaßlichen oder festgestellten Schädigung Kenntnis hatten oder hätten haben müssen. Sie prüfte auch, ob ein weiterer erheblicher Anstieg der Einfuhren verzeichnet wurde, der mit Blick auf die zeitliche Komponente, die Menge und sonstige Umstände die Abhilfewirkung eines anzuwendenden endgültigen Antidumpingzolls wahrscheinlich ernsthaft untergraben würde. |
3.1. Kenntnis der Einführer von dem Dumping, dem Ausmaß des Dumpings und der mutmaßlichen Schädigung
|
(9) |
In diesem Stadium liegen der Kommission hinreichende Beweise dafür vor, dass die Einfuhren der betroffenen Ware aus der Türkei gedumpt sind. Der Antrag enthielt ausreichende Beweise für das Vorliegen von Dumping, die sich auf einen Vergleich des wie beschrieben ermittelten Normalwerts mit dem Preis der betroffenen Ware bei der Ausfuhr in die Union (auf der Stufe ab Werk) stützen. Insgesamt wurde angesichts der Höhe der mutmaßlichen Dumpingspannen von 4 % bis 8 % durch diese Beweise hinreichend belegt, dass die ausführenden Hersteller Dumping praktizieren. |
|
(10) |
Der Antrag enthielt auch ausreichende Beweise für eine mutmaßliche Schädigung des Wirtschaftszweigs der Union, einschließlich einer negativen Entwicklung der wichtigsten Leistungsindikatoren des Wirtschaftszweigs der Union. |
|
(11) |
Diese Informationen waren sowohl in der nichtvertraulichen Fassung des Antrags als auch in der am 14. Mai 2020 veröffentlichten Einleitungsbekanntmachung enthalten. Durch die Veröffentlichung im Amtsblatt der Europäischen Union ist die Einleitungsbekanntmachung ein öffentliches, allen Einführern zugängliches Dokument. Zudem haben Einführer als interessierte Parteien im Rahmen der Untersuchung Zugang zur nichtvertraulichen Fassung des Antrags und zum nichtvertraulichen Dossier. Auf dieser Grundlage war die Kommission daher der Ansicht, dass die Einführer Kenntnis von dem Dumping, seinem Ausmaß und der mutmaßlichen Schädigung hatten oder hätten haben müssen. (3) |
|
(12) |
Wie in Erwägungsgrund 5 ausgeführt, haben mehrere interessierte Parteien Stellungnahmen zu dem Antrag auf zollamtliche Erfassung eingereicht. In Bezug auf das erste Kriterium hoben die türkische Regierung, Habas, der ÇİB und die Gruppen Colakoglu und Erdemir hervor, dass die bloße Einleitung einer Antidumpinguntersuchung nicht automatisch bedeute, dass tatsächlich Dumping vorliege, da bestimmte Untersuchungen (einige davon die Türkei betreffend) schließlich ohne die Einführung von Zöllen eingestellt würden. Es handele sich vielmehr um einen „einseitigen Vorwurf“. Davon ausgehend könne ein Einführer nicht von einem Umstand (den Dumpingpraktiken) Kenntnis haben, der in der Untersuchung noch gar nicht festgestellt worden sei. Darüber hinaus beanstandeten die türkische Regierung, Habas und der ÇİB bestimmte zusätzliche Beweise, die von Eurofer in dem Antrag vorgelegt worden waren, darunter die Behauptung, der Geschäftsführer eines türkischen ausführenden Herstellers habe von der bevorstehenden Antidumpinguntersuchung gewusst, sowie die Information, dass Einfuhren der betroffenen Ware in Drittländern handelspolitischen Schutzmaßnahmen unterliegen würden. Schließlich merkte der TCUD an, dass einige der von Eurofer vorgebrachten Behauptungen bezüglich der Antidumpingmaßnahmen gegen türkische Einfuhren der betroffenen Ware in den eingereichten Unterlagen nicht wahrheitsgemäß dargelegt worden seien. In diesem Zusammenhang argumentierte der TCUD, dass ein Unternehmen nach einer Anfechtung vor den zuständigen Gerichten von den US-Maßnahmen befreit worden sei und dass ein anderes Drittland (Marokko) nach der Entscheidung eines WTO-Panels die Antidumpingzölle gegenüber der Türkei aufgehoben habe. |
|
(13) |
In Artikel 14 Absatz 5 der Grundverordnung ist vorgesehen, dass die Kommission ab Einleitung der Untersuchung und nach rechtzeitiger Unterrichtung der Mitgliedstaaten die Zollbehörden anweisen kann, geeignete Schritte zu unternehmen, um die Einfuhren zollamtlich zu erfassen, sodass in der Folge Maßnahmen gegenüber diesen Einfuhren vom Zeitpunkt dieser zollamtlichen Erfassung an eingeführt werden können. Das Hauptziel der zollamtlichen Erfassung besteht in diesem Fall darin, im Einklang mit Artikel 10 Absatz 4 der Grundverordnung die rückwirkende Einführung vorläufiger Maßnahmen bis zu 90 Tage vor ihrer Anwendung zu ermöglichen. Im Lichte dieser Bestimmung kann die Kommission die Einfuhren nicht zollamtlich erfassen, nachdem ein vorläufiger Zoll bereits eingeführt wurde. |
|
(14) |
Wenn, wie von einigen Parteien behauptet, eine zollamtliche Erfassung erst möglich ist, nachdem im Rahmen einer Untersuchung Dumping festgestellt wurde, dann kann sie per Definition niemals vor der Einführung vorläufiger Zölle erfolgen. Ein solcher Ansatz würde das Instrument der zollamtlichen Erfassung jedoch vollständig seiner rechtlichen Wirksamkeit („effet utile“) berauben. (4) Daher muss die Kommission schon vor der Einführung eines vorläufigen Zolls eine Entscheidung darüber treffen, ob die Einfuhren zollamtlich erfasst werden können. In diesem Zusammenhang stellte die Kommission fest, dass zu dem Zeitpunkt, als der Antragsteller den Antrag auf zollamtliche Erfassung stellte, die besten verfügbaren Informationen die im Antrag enthaltenen Angaben waren, die die Kommission, wie in der Einleitungsbekanntmachung angegeben, als Grundlage für die Einleitung der Antidumpinguntersuchung heranzog und aus denen hervorging, dass Beweise vorlagen, die tendenziell darauf hindeuten, dass schädigendes Dumping stattfand. Daher wies die Kommission diese Vorbringen als unbegründet zurück. Außerdem war es angesichts dieser Feststellung nicht erforderlich, dass die Kommission die genannten zusätzlichen Beweise zu Einfuhren der türkischen ausführenden Hersteller in Drittländer und die damit zusammenhängenden Argumente prüfte. |
|
(15) |
Die Kommission kam daher zu dem Schluss, dass das erste Kriterium für die zollamtliche Erfassung erfüllt war. |
3.2. Weiterer erheblicher Anstieg der Einfuhren
|
(16) |
Die Kommission analysierte dieses Kriterium auf der Grundlage der in der Datenbank Surveillance 2 enthaltenen statistischen Daten zu der betroffenen Ware. Um zu beurteilen, ob seit der Einleitung der Untersuchung ein weiterer erheblicher Anstieg stattgefunden hat, legte die Kommission zunächst die zu vergleichenden Zeiträume fest. Zum einen bewertete sie die Daten zu den Einfuhren aus der Türkei nach der Einleitung der Antidumpinguntersuchung (d. h. ab dem Zeitpunkt, als die Einführer Kenntnis von den Dumpingpraktiken hatten oder hätten haben müssen) bis zum jüngsten Zeitraum, d. h. von Juni bis Mitte Oktober 2020. Zum anderen ermittelte die Kommission die Einfuhrmengen aus der Türkei für den gleichen Zeitraum im Untersuchungszeitraum (5) (d. h. von Juni bis Mitte Oktober 2019) sowie die monatlichen durchschnittlichen Einfuhrmengen im gesamten Untersuchungszeitraum. |
|
(17) |
Die Kommission war der Auffassung, dass in diesem Fall ein Vergleich der durchschnittlichen monatlichen Einfuhrmengen nach der Einleitung mit den durchschnittlichen monatlichen Einfuhrmengen aus der Türkei im gesamten Untersuchungszeitraum angesichts der Marktentwicklungen und der Aufstockung der Lagerbestände, die sich aus den derzeitigen Schutzmaßnahmen für die betroffene Ware ergeben, nicht ausreichen würde, um zu beurteilen, ob ein erheblicher Anstieg der Einfuhren zu verzeichnen war. Daher hielt es die Kommission für angemessen, ihre Feststellungen auf den Vergleich der durchschnittlichen monatlichen Einfuhrmengen nach der Einleitung mit denjenigen aus dem gleichen Zeitraum im Untersuchungszeitraum zu stützen, um den potenziellen Einfluss der laufenden Schutzmaßnahmen auf das Verhalten der Einfuhrströme aus der Türkei im bewerteten Zeitraum besser widerzuspiegeln (6). Darüber hinaus hat ein Vergleich der Einfuhrmengen nach der Einleitung mit den Einfuhrmengen im gleichen Zeitraum des Vorjahres den Vorteil, dass etwaige saisonale Effekte gebührend berücksichtigt werden (7). |
|
(18) |
In Bezug auf den Einfluss der Schutzmaßnahmen auf die Einfuhrströme aus der Türkei stellte die Kommission fest, dass die Einfuhren der betroffenen Ware aus der Türkei während des gesamten Jahres 2019 (also während des Untersuchungszeitraums) durch zahlreiche Anpassungen der Funktionsweise der Schutzmaßnahmen beeinflusst wurden, die sich auf das Ausfuhrverhalten der türkischen Unternehmen auswirkten. |
|
(19) |
Erstens fiel Januar 2019, der Monat mit den weitaus meisten Einfuhren der betroffenen Ware aus der Türkei, mit dem letzten Monat der vorläufigen Schutzmaßnahmen zusammen. Diesbezüglich herrschte auf dem Markt Unsicherheit darüber, in welcher Form endgültige Maßnahmen ergriffen werden würden. Die Kommission wies darauf hin, dass der bis zum Ende des betreffenden Monats nicht verkaufte Anteil des zollfreien Zollkontingents nicht auf den nächsten Zeitraum übertragen worden wäre, d. h. dieser Anteil am zollfreien Zollkontingent wäre „verloren gegangen“. Eine ähnliche Situation, d. h. der/die letzte(n) Monat(e) vor einem neuen Maßnahmenzeitraum, trat im Quartal Februar-März 2019 ein. Zweitens wurden im Februar, April, Juli und Oktober des Jahres 2019 neue Tranchen zollfreier Zollkontingente freigegeben. Im Rahmen der Schutzmaßnahmen für bestimmte Stahlerzeugnisse hat jede Freigabe von Zollkontingenten in der Regel dazu geführt, dass immer zu Quartalsbeginn große Mengen eingeführt werden. Schließlich kündigte die Kommission im August 2019 im Rahmen der ersten Überprüfung der Schutzmaßnahmen für Stahlerzeugnisse an, dass sie für Einfuhren der betroffenen Ware aus der Türkei eine Obergrenze von 30 % des verfügbaren Zollkontingents für die entsprechende Warenkategorie anwenden werde, was im Vorfeld dieser Änderung der Zollkontingentverwaltung ebenfalls zu einem Anstieg der Einfuhren beigetragen hat. |
|
(20) |
Die Kommission hob ferner hervor, dass die genannten Ereignisse Auswirkungen auf die Einfuhrströme hatten, wie aus den Statistiken hervorgeht. Insbesondere die Monate Januar, März und September rangieren bei den monatlichen Ausfuhrmengen aus der Türkei im Jahr 2019 an erster, zweiter und vierter Stelle (teilweise mit deutlichem Abstand gegenüber jedem anderen Monat dieses Jahres) (8). Daher kam die Kommission zu dem Schluss, dass das Verhalten der Marktteilnehmer und die Entwicklung der Einfuhrströme das ganze Jahr über durch all diese Regulierungsmaßnahmen im Rahmen der Schutzmaßnahmen für Stahlerzeugnisse erheblich beeinflusst wurde. |
|
(21) |
Die Lage in einem wesentlich kürzeren Zeitraum (von Juni bis Mitte Oktober) wurde von den regulatorischen Änderungen bei der Verwaltung der Zollkontingente weniger stark beeinflusst. Daher verglich die Kommission die durchschnittliche monatliche Einfuhrmenge aus der Türkei im Zeitraum Juni bis Mitte Oktober 2020 mit der durchschnittlichen monatlichen Einfuhrmenge im gleichen Zeitraum des Vorjahres 2019. |
|
(22) |
Der Vergleich zeigt für diesen Zeitraum einen Anstieg der durchschnittlichen monatlichen Einfuhrmenge aus der Türkei um 6 %.
Quelle: Datenbank Surveillance 2 |
||||||||||||||
|
(23) |
Die Kommission prüfte die Einfuhrentwicklungen im ausgewählten Zeitraum und im entsprechenden Zeitraum des Untersuchungszeitraums noch eingehender, um festzustellen, ob dieser Anstieg um 6 % im vorliegenden Fall einen erheblichen Anstieg der Einfuhren darstellte. Insbesondere stellte die Kommission fest, dass die Einfuhrmengen aus der Türkei im September 2020 unerheblich waren. Diese außergewöhnlich niedrige Einfuhrmenge war weitgehend darauf zurückzuführen, dass die Türkei im Rahmen der Schutzmaßnahmen für Stahl in diesem Monat ihr länderspezifisches Zollkontingent für Warenkategorie 1 (zu der die betroffene Ware gehört) praktisch ausgeschöpft hatte und daher nur zu einem Zollsatz von 25 % noch nennenswerte Mengen der betroffenen Ware hätte ausführen können. (10) Aufgrund dieser außergewöhnlich niedrigen Einfuhrmengen im September 2020 verringerten sich die durchschnittlichen monatlichen Einfuhrmengen in dem maßgeblichen Zeitraum, den die Kommission für den Vergleich gewählt hatte (Juni bis Mitte Oktober 2020), erheblich. Gleichzeitig stellte die Kommission fest, dass gerade im selben Monat des Vorjahres, im September 2019, ein sehr hohes Einfuhrvolumen zu verzeichnen war, weil im Oktober 2019 die Anpassungen infolge der ersten Überprüfung der Schutzmaßnahmen wirksam werden sollten. Daher führten die türkischen Hersteller im Vorgriff auf dieses Ereignis im September 2019 sehr große Mengen aus. |
|
(24) |
Angesichts der Erwägungen im vorstehenden Erwägungsgrund war die Kommission der Auffassung, dass die Einfuhren der Monate September 2019 bzw. 2020 nicht repräsentativ waren, und bewertete auch die Einfuhrmengen, ohne diesen Monat in beiden Jahren einzubeziehen. Dieser Vergleich bestätigte, dass der Anstieg der Einfuhrmengen im Vergleich zu den gleichen Monaten im Untersuchungszeitraum sehr beträchtlich war. Vergleicht man beispielsweise den Zeitraum Juni-August im Jahr 2020 und den gleichen Zeitraum im Jahr 2019, so war ein Anstieg um + 44 % zu verzeichnen. Ein erheblicher Anstieg um + 49 % ergäbe sich auch beim Vergleich des Zeitraums Juni-Mitte Oktober 2020 mit dem gleichen Zeitraum im Jahr 2019 ohne den Monat September. In Anbetracht dieser Erwägungen kam die Kommission zu dem Schluss, dass der Anstieg der Einfuhren in diesem Fall erheblich ist. |
|
(25) |
Was dieses Kriterium anbelangt, so beanstandeten die türkische Regierung, Habas, der ÇİB, die Gruppen Colakoglu und Erdemir sowie das Konsortium der Verwender von warmgewalzten Flacherzeugnissen aus Stahl den vom Antragsteller vorgeschlagenen Zeitraum für die Beurteilung der Frage, ob ein erheblicher Anstieg der Einfuhren stattgefunden hat. Stattdessen schlugen diese Parteien andere Zeiträume für die Durchführung eines solchen Vergleichs vor, der ihrer Ansicht nach zeigen würde, dass dieses Kriterium nicht erfüllt sei. Habas und das Konsortium der Verwender von warmgewalzten Flacherzeugnissen aus Stahl gaben an, dass ein quartalsweiser Vergleich der jeweils ersten Hälfte (d. h. der ersten beiden Quartale) der Jahre 2019 und 2020 einen Rückgang der Einfuhren aufzeigen würde. Der ÇİB sowie die Gruppen Colakoglu und Erdemir brachten vor, dass der von Eurofer gewählte Zeitraum von Juni bis Juli 2020 zu kurz und daher nicht repräsentativ sei. Zudem behaupteten der ÇİB und das Konsortium der Verwender, dass sowieso jeglicher Anstieg der Einfuhren durch die Lockerung der Lockdown-Maßnahmen in der Union im Zusammenhang mit der COVID-19-Pandemie bedingt gewesen sei, die in der Zeit kurz nach der Einleitung der Untersuchung stattgefunden habe. Der ÇİB argumentierte, dass die Kommission die Menge der Einfuhren, die nach der Einleitung der Untersuchung erfolgten, mit der Einfuhrmenge im Untersuchungszeitraum vergleichen müsse. Die Einfuhren der Türkei hätten im Zeitraum Januar bis Mai 2020 einen stetigen Rückgang verzeichnet und seien in den Monaten Juni und Juli 2020 nur soweit wieder angestiegen, dass sie zu ihrem „normalen“ Niveau zurückgekehrt seien. Darüber hinaus solle die Kommission angesichts der Auswirkungen der angeblich besonderen Situation nach der Quarantäne die Daten nach der Einleitung der Untersuchung vom Juni 2020 unberücksichtigt lassen. In diesem Fall ergebe der Vergleich mit dem Monatsdurchschnitt im Untersuchungszeitraum einen Anstieg von 12 %, was nicht als weiterer wesentlicher Anstieg, sondern eher als sehr bescheidener Anstieg zu werten sei. Andere Parteien schlugen vor, die Einfuhrtrends in den jeweils ersten sieben Monaten (Januar-Juli) der Jahre 2017 bis 2020 und die Einfuhrtrends in den Jahren 2017 bis 2020 insgesamt (auf Jahresbasis) zu beurteilen (11) bzw. den Monatsdurchschnitt der Jahre 2018 und 2019 mit dem Monatsdurchschnitt im Zeitraum von Januar bis Juli 2020, den Monatsdurchschnitt im Zeitraum von Januar bis Juli der Jahre 2018 und 2019 mit dem gleichen Zeitraum im Jahr 2020 sowie den Monatsdurchschnitt im Untersuchungszeitraum mit der Einfuhrmenge im Juli 2020 zu vergleichen (12), was einen Rückgang der Einfuhren aufzeigen würde. Die Gruppen Colakoglu und Erdemir beanstandeten außerdem, dass der Antrag trotz der Zeitspanne, die zwischen dem Ende des Untersuchungszeitraums und der Einleitung der Untersuchung verstrichen sei, keine Angaben zu den Einfuhrmengen in dieser Zeit enthalte. |
|
(26) |
Darüber hinaus brachte das Konsortium der Verwender von warmgewalzten Flacherzeugnissen aus Stahl vor, dass die zollamtliche Erfassung die Einfuhrmengen verringern und zu einem Versorgungsengpass führen würde, der den Betrieb der Produktionsanlagen bestimmter Verwender in der Union gefährden würde. Dies würde angeblich den Markt stören und den unabhängigen Verwendern der betroffenen Ware irreparablen Schaden zufügen. |
|
(27) |
Alle interessierten Parteien, die auf den Antrag von Eurofer auf zollamtliche Erfassung reagierten, gaben übereinstimmend an, dass die Türkei aufgrund der Auswirkungen der Schutzmaßnahmen für Stahlerzeugnisse nicht in der Lage sei, ihre Ausfuhren in den kommenden Monaten (d. h. in den Monaten vor der Einführung vorläufiger Antidumpingmaßnahmen) weiter zu steigern, und dass die Kommission deshalb den Antrag auf zollamtliche Erfassung zurückweisen sollte. |
|
(28) |
Hinsichtlich der von den Parteien vorgeschlagenen alternativen Zeiträume verweist die Kommission auf ihre Argumentation und Erläuterungen in Abschnitt 3.2. Darüber hinaus wurden einige Einwände vorgebracht, die eine spezifische Gegenargumentation rechtfertigen. Erstens weist die Kommission darauf hin, dass sie in der Regel zwar auch die durchschnittlichen monatlichen Einfuhrmengen eines Zeitraums nach der Einleitung mit den durchschnittlichen Einfuhrmengen im Untersuchungszeitraum vergleicht, ein solcher Vergleich jedoch nicht immer angemessen ist. Im vorliegenden Fall hat die Kommission festgestellt und in den Erwägungsgründen 16 bis 20 erläutert, dass in Anbetracht der besonderen Marktbedingungen in Bezug auf die untersuchten Einfuhren die Verwendung der durchschnittlichen Einfuhren des Jahres 2019 nicht die geeignetste Vergleichsgrundlage ist. |
|
(29) |
Zweitens stellt die Kommission fest, dass sich einer der Vorschläge auf die Entwicklungen aus einer Zeit vor der Einleitung der Antidumpinguntersuchung bezog. Dies würde der Feststellung widersprechen, dass die Dumpingpraktiken in der Türkei erst durch die Veröffentlichung der Einleitungsbekanntmachung bekannt geworden sind. Daher sind die Einfuhrtrends vor dem Zeitpunkt, ab dem ein Einführer von dem Vorliegen von Dumping hätte Kenntnis haben können, bei der Beurteilung, ob ein Antrag auf zollamtliche Erfassung begründet ist, nicht zu berücksichtigen. |
|
(30) |
Drittens stellt die Kommission auch fest, dass der Antrag von Eurofer zwar den Ausgangspunkt für die Analyse darstellt, die Kommission jedoch auch eine umfassende eigene Analyse durchführen muss. In diesem Zusammenhang liegt der Kommission ein Datensatz vor, der sich auf einen kürzer zurückliegenden Zeitraum bezieht als die von Eurofer im Antrag angegebenen Daten (nämlich einer, der bis Mitte Oktober 2020 reicht). (13) Darüber hinaus hielt es die Kommission aus den vorstehend genannten Gründen auch für angemessener, diesen Datensatz mit dem gleichen Zeitraum im Untersuchungszeitraum zu vergleichen. |
|
(31) |
Deshalb ist die Kommission nicht der Ansicht, dass die alternativen Vorschläge zwingende Gründe aufgezeigt haben, aus denen sie für die Beurteilung der Einfuhrentwicklungen besser geeignet wären als der in Abschnitt 3.2 entwickelte Ansatz. Daher wies die Kommission diese Vorbringen zurück. |
|
(32) |
Den Behauptungen, dass aufgrund der bestehenden Schutzmaßnahmen keinerlei Risiko eines weiteren erheblichen Anstiegs der Einfuhren bestehe, widersprach die Kommission aus folgenden Gründen. |
|
(33) |
Erstens greift die zollamtliche Erfassung einer Entscheidung über die rückwirkende Erhebung vorläufiger Antidumpingzölle nicht vor. Ob Schutzmaßnahmen bis zur Einführung vorläufiger Maßnahmen einen Anstieg der Einfuhren verhindern werden, sollte im Zusammenhang mit einer möglichen rückwirkenden Erhebung der Zölle geprüft werden. (14) |
|
(34) |
In jedem Fall bestätigt die Kommission, dass die Türkei infolge der durch die Schutzmaßnahmen eingeführten Änderungen ab dem 1. Juli 2020 einem länderspezifischen Zollkontingent unterliegt, dessen vierteljährliche Mengen in Anhang II der Durchführungsverordnung (EU) 2020/894 der Kommission (15) festgelegt sind. Auch nach Ausschöpfung dieser Mengen darf die Türkei weiterhin in die Union ausführen (16). |
|
(35) |
Die Kommission ist jedoch nicht der Meinung, dass dieser Umstand allein automatisch verhindern würde, dass die Einfuhren aus der Türkei vor der etwaigen Einführung vorläufiger Antidumpingzölle erheblich ansteigen. Der Grund dafür ist, dass in dem Zeitraum, der für die mögliche Einführung vorläufiger Zölle noch verbleibt, d. h. bis Mitte Januar 2021, noch zwei Tranchen zollfreier länderspezifischer Zollkontingente für die Türkei freigegeben werden sollen. (17) Darüber hinaus könnte ein eventueller Vergleich zwischen den Einfuhrmengen zur Beurteilung der Frage, ob eine rückwirkende Erhebung von Zöllen gerechtfertigt ist, auch eine Zeitspanne vor dem Zeitpunkt abdecken, seit dem für die Türkei ein länderspezifisches Zollkontingent gilt (siehe Erwägungsgründe 18 und 19). Daher gibt es zum gegenwärtigen Zeitpunkt keine Beweise dafür, dass die Gesamtmengen, die die Türkei bis zu einer eventuellen Einführung vorläufiger Antidumpingmaßnahmen zollfrei (und zu dem Zollsatz von 25 %) ausführen könnte, keinen weiteren wesentlichen Anstieg darstellen würden. In jedem Fall wird die Kommission diesbezüglich nur dann zu einem Schluss gelangen können, wenn am Ende der laufenden Untersuchung endgültige Antidumpingzölle eingeführt werden. |
|
(36) |
Daher weist die Kommission die Behauptung zurück, dass aufgrund der geltenden Schutzmaßnahmen ein weiterer erheblicher Anstieg der Einfuhren ausgeschlossen werden sollte. |
|
(37) |
Schließlich stellt die Kommission fest, dass die Stellungnahme des Konsortiums der Verwender zu den Auswirkungen der zollamtlichen Erfassung auf die Verfügbarkeit der betroffenen Ware und auf unabhängige Verwender nicht unter die rechtlichen Anforderungen fällt, die bei der Entscheidung über die zollamtliche Erfassung von Einfuhren zu prüfen sind. Daher geht die Kommission in diesem Stadium des Verfahrens nicht darauf ein. |
|
(38) |
In Anbetracht der obigen Erwägungen kam die Kommission zu dem Schluss, dass das zweite Kriterium für die zollamtliche Erfassung ebenfalls erfüllt war. |
3.3. Beeinträchtigung der Abhilfewirkung des Zolls
|
(39) |
Der Kommission liegen hinreichende Nachweise dafür vor, dass ein weiterer Anstieg der Einfuhren aus der Türkei zu noch weiter sinkenden Preisen zu einer zusätzlichen Schädigung führen würde. |
|
(40) |
Wie in Abschnitt 3.2 dargelegt, gibt es hinreichende Nachweise für einen erheblichen Anstieg der Einfuhren der betroffenen Ware. |
|
(41) |
Zudem gibt es Belege für eine rückläufige Entwicklung bei den Einfuhrpreisen der betroffenen Ware. In diesem Zusammenhang sind die Preise der Einfuhren aus der Türkei in die Union im Zeitraum von Juni bis Mitte Oktober 2020 im Vergleich zum selben Zeitraum im Jahr 2019 um durchschnittlich 13 % und im Vergleich zum Monatsdurchschnitt im Untersuchungszeitraum um 14 % gesunken.
Quelle: Datenbank Surveillance 2 |
||||||||||||||
|
(42) |
Angesichts des Zeitaspekts, der Menge und sonstiger Umstände wie beispielsweise der Preispolitik der ausführenden Hersteller würde dieser weitere Anstieg der Einfuhren nach der Einleitung der Untersuchung demnach die Abhilfewirkung endgültiger Zölle wahrscheinlich ernsthaft untergraben, es sei denn solche Zölle würden rückwirkend angewandt. |
|
(43) |
Die Kommission kam daher zu dem Schluss, dass auch das dritte Kriterium für die zollamtliche Erfassung erfüllt war. |
4. VERFAHREN
|
(44) |
Die Kommission gelangte zu dem Schluss, dass genügend Beweise vorliegen, um die zollamtliche Erfassung der Einfuhren der betroffenen Ware nach Artikel 14 Absatz 5 der Antidumping-Grundverordnung zu rechtfertigen. |
|
(45) |
Alle interessierten Parteien sind gebeten, unter Vorlage sachdienlicher Beweise schriftlich Stellung zu nehmen. Die Kommission kann die interessierten Parteien anhören, sofern die Parteien dies schriftlich beantragen und nachweisen, dass besondere Gründe für ihre Anhörung sprechen. |
5. ZOLLAMTLICHE ERFASSUNG
|
(46) |
Nach Artikel 14 Absatz 5 der Grundverordnung sollten die Einfuhren der betroffenen Ware zollamtlich erfasst werden, damit, falls die Untersuchungsergebnisse zur Einführung von Antidumpingzöllen führen, diese Zölle bei Erfüllung der nötigen Voraussetzungen nach Maßgabe der geltenden Rechtsvorschriften rückwirkend auf die zollamtlich erfassten Einfuhren erhoben werden können. |
|
(47) |
Eine etwaige künftige Zollschuld ergäbe sich aus den Feststellungen der Antidumpinguntersuchung. |
|
(48) |
In dem Antrag, der zur Einleitung einer Antidumpinguntersuchung geführt hat, werden bei der betroffenen Ware die Dumpingspannen auf 4 % bis 8 % und die Schadensbeseitigungsschwelle auf einen Bereich zwischen 10 % und 25 % geschätzt. Der Betrag der möglichen künftigen Zollschuld kann auf die Höhe der höchsten Dumpingspanne geschätzt werden, die auf der Grundlage des Antrags veranschlagt wird, d. h. 8 % des CIF-Einfuhrwerts der betroffenen Ware. |
6. VERARBEITUNG PERSONENBEZOGENER DATEN
|
(49) |
Alle im Rahmen dieser zollamtlichen Erfassung erhobenen personenbezogenen Daten werden nach der Verordnung (EU) 2018/1725 des Europäischen Parlaments und des Rates (18) verarbeitet — |
HAT FOLGENDE VERORDNUNG ERLASSEN:
Artikel 1
(1) Die Zollbehörden werden nach Artikel 14 Absatz 5 der Verordnung (EU) 2016/1036 angewiesen, geeignete Schritte zu unternehmen, um die in die Union getätigten Einfuhren von Flacherzeugnissen aus Eisen, nicht legiertem Stahl oder anderem legiertem Stahl, auch in Rollen (Coils) (auch zugeschnittene Waren und Schmalbanderzeugnisse („narrow strip“)), nur warmgewalzt, weder plattiert noch überzogen, zollamtlich zu erfassen. Diese Waren werden derzeit unter den KN-Codes 7208 10 00, 7208 25 00, 7208 26 00, 7208 27 00, 7208 36 00, 7208 37 00, 7208 38 00, 7208 39 00, 7208 40 00, 7208 52 10, 7208 52 99, 7208 53 10, 7208 53 90, 7208 54 00, 7211 13 00, 7211 14 00, 7211 19 00, ex 7225 19 10 (TARIC-Code 7225191090), 7225 30 90, ex 7225 40 60 (TARIC-Code 7225406090), 7225 40 90, ex 7226 19 10 (TARIC-Code 7226191090), 7226 91 91 und 7226 91 99 eingereiht und haben ihren Ursprung in der Türkei.
(2) Die zollamtliche Erfassung endet neun Monate nach Inkrafttreten dieser Verordnung.
(3) Alle interessierten Parteien können innerhalb von 21 Tagen nach Veröffentlichung dieser Verordnung schriftlich Stellung nehmen, sachdienliche Beweise vorlegen oder eine Anhörung beantragen.
Artikel 2
Diese Verordnung tritt am Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 12. November 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 176 vom 30.6.2016, S. 21.
(2) ABl. C 166 vom 14.5.2020, S. 9.
(3) Siehe Urteil des Gerichts (Zweite Kammer) vom 8. Mai 2019 in der Rechtssache T-749/16, Stemcor/Europäische Kommission, Rn. 56.
(4) Siehe Urteil des Gerichts (Zweite Kammer) vom 8. Mai 2019 in der Rechtssache T-749/16‚ Stemcor/Europäische Kommission, Rn. 33.
(5) Der Untersuchungszeitraum (im Folgenden „UZ“) erstreckte sich vom 1. Januar 2019 bis zum 31. Dezember 2019.
(6) Die Einfuhren der betroffenen Ware aus der Türkei unterliegen seit Mitte Juli 2018 Schutzmaßnahmen (unter Warenkategorie 1). Die Zollkontingente im Rahmen der Schutzmaßnahmen werden quartalsweise verwaltet. Daher wird bei einem Vergleich derselben Zeiträume der Trend weniger stark durch die zahlreichen Änderungen in der Verwaltung der Zollkontingente beeinflusst, die während des Untersuchungszeitraums, der ein volles Jahr (2019) umfasst, stattfanden, da die Türkei im Laufe des Jahres 2019 drei verschiedenen Regelungen für die Verwaltung der Zollkontingente unterlag.
(7) Die Kommission stellte fest, dass bei der betroffenen Ware der Verbrauch im Sommerzeitraum gegenüber dem Zeitraum davor stets zurückgegangen ist. Mit den von der Kommission in diesem Fall verwendeten Zeiträumen würde somit jegliche Verzerrung durch etwaige saisonale Effekte vermieden werden.
(8) De facto sind die durchschnittlichen Einfuhrmengen in diesen Monaten mehr als doppelt so hoch wie in den anderen neun Monaten des Jahres 2019.
(9) Dieser Vergleich wird als angemessener erachtet, siehe Erwägungsgründe 17 bis 21.
(10) Bis die nächste Tranche des länderspezifischen Zollkontingents zur Verfügung gestanden hätte.
(11) Konsortium der Verwender von warmgewalzten Flacherzeugnissen aus Stahl.
(12) Gruppen Colakoglu und Erdemir.
(13) In dem Antrag von Eurofer auf zollamtliche Erfassung wurden nur Daten für die Monate Juni und Juli 2020 berücksichtigt.
(14) Das heißt, wenn die Einfuhrdaten für den Zeitraum vorliegen, der für die Entscheidung, ob eine rückwirkende Erhebung von Zöllen gerechtfertigt ist, maßgeblich ist.
(15) Durchführungsverordnung (EU) 2020/894 der Kommission vom 29. Juni 2020 zur Änderung der Durchführungsverordnung (EU) 2019/159 zur Einführung endgültiger Schutzmaßnahmen gegenüber den Einfuhren bestimmter Stahlerzeugnisse (ABl. L 206 vom 30.6.2020, S. 27).
(16) Zu einem Zollsatz von 25 % bis zur Freigabe der nächsten Tranche von Zollkontingenten im nächsten Quartal.
(17) Eine Tranche für das Quartal Oktober bis Dezember 2020 und eine weitere für Januar bis März 2021.
(18) Verordnung (EU) 2018/1725 des Europäischen Parlaments und des Rates vom 23. Oktober 2018 zum Schutz natürlicher Personen bei der Verarbeitung personenbezogener Daten durch die Organe, Einrichtungen und sonstigen Stellen der Union, zum freien Datenverkehr und zur Aufhebung der Verordnung (EG) Nr. 45/2001 und des Beschlusses Nr. 1247/2002/EG (ABl. L 295 vom 21.11.2018, S. 39).
RICHTLINIEN
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/55 |
DELEGIERTE RICHTLINIE (EU) 2020/1687 DER KOMMISSION
vom 2. September 2020
zur Änderung des Anhangs des Rahmenbeschlusses 2004/757/JI des Rates im Hinblick auf die Aufnahme der neuen psychoaktiven Substanz N, N-Diethyl-2-[[4-(1-methylethoxy)-phenyl]-methyl]-5-nitro-1H-benzimidazol-1-ethanamin (Isotonitazen) in die Definition von Drogen
DIE EUROPÄISCHE KOMMISSION —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf den Rahmenbeschluss 2004/757/JI des Rates vom 25. Oktober 2004 zur Festlegung von Mindestvorschriften über die Tatbestandsmerkmale strafbarer Handlungen und die Strafen im Bereich des illegalen Drogenhandels (1), insbesondere auf Artikel 1a und 8a,
in Erwägung nachstehender Gründe:
|
(1) |
Der gemäß Artikel 5c Absatz 4 der Verordnung (EG) Nr. 1920/2006 des Europäischen Parlaments und des Rates (2) erweiterte Wissenschaftliche Ausschuss der Europäischen Beobachtungsstelle für Drogen und Drogensucht (EMCDDA, im Folgenden „Beobachtungsstelle“) hat am 26. Mai 2020 gemäß Artikel 5c der genannten Verordnung einen Risikobewertungsbericht über die neue psychoaktive Substanz N, N–Diethyl-2-[[4-(1-methylethoxy)-phenyl]methyl]-5-nitro-1-H-benzimidazol-1-ethanamin (Isotonitazen) erstellt. Die Beobachtungsstelle legte den Risikobewertungsbericht der Kommission und den Mitgliedstaaten am 29. Mai 2020 vor. |
|
(2) |
Bei Isotonitazen handelt es sich um ein synthetisches Opioidanalgetikum, das eng mit den Substanzen Etonitazen und Clonitazen verwandt ist, die beide gemäß dem Einheits-Übereinkommen der Vereinten Nationen von 1961 über Suchtstoffe in der durch das Protokoll von 1972 geänderten Fassung internationaler Kontrolle unterliegen. |
|
(3) |
Isotonitazen ist mindestens seit April 2019 in der Union verfügbar und wurde in fünf Mitgliedstaaten sowie im Vereinigten Königreich festgestellt. Insgesamt wurden 24 Beschlagnahmen von vier Mitgliedstaaten gemeldet; darüber hinaus meldete ein Mitgliedstaat eine biologische Probe und das Vereinigte Königreich meldete bei der Obduktion festgestellte Proben. Da aufgrund der Neuartigkeit des Stoffes auf dem Markt keine routinemäßigen Kontrollen zu diesem Stoff erfolgen, ist generell von einer höheren Dunkelziffer auszugehen. In den meisten Fällen wurde der Stoff als Pulver beschlagnahmt, aber auch in flüssiger Form identifiziert. Die gefundenen Mengen sind relativ gering. Sie sollten jedoch vor dem Hintergrund der hohen Wirksamkeit von Isotonitazen bewertet werden. |
|
(4) |
Bisher wurden von Deutschland und dem Vereinigten Königreich zwei Todesfälle im Zusammenhang mit Isotonitazen gemeldet. Die Todesfälle ereigneten sich 2019. Für den Todesfall in Deutschland liegen keine detaillierten Informationen vor. In dem vom Vereinigten Königreich gemeldeten Fall wurden in den biologischen Proben der Obduktion (3) mehrere andere Stoffe identifiziert. Bisher wurden keine akuten Vergiftungen im Zusammenhang mit Isotonitazen gemeldet. Wie bei anderen synthetischen Opioiden dürfte Naloxon als Gegenmittel bei einer Vergiftung durch Isotonitazen wirken. Sowohl bei Vergiftungen als auch bei Todesfällen ist von einer hohen Dunkelziffer auszugehen, da in beiden Fällen keine routinemäßigen Kontrollen zu dem Stoff erfolgen und dieser erst kürzlich auf dem Unionsmarkt festgestellt wurde. |
|
(5) |
Es gibt keine direkten Hinweise auf die Beteiligung der organisierten Kriminalität an der Herstellung, dem Vertrieb, dem Handel und der Beschaffung von Isotonitazen in der Union. Die verfügbaren Informationen deuten darauf hin, dass Isotonitazen von chemischen Unternehmen mit Sitz außerhalb der Union hergestellt wird. |
|
(6) |
Isotonitazen wird anscheinend sowohl in Kleinhandels- als auch in Großhandelsmengen online vertrieben, hauptsächlich als Pulver, aber auch als gebrauchsfertige Nasensprays. Die Hinweise aufgrund von Sicherstellungen deuten darauf hin, dass Isotonitazen möglicherweise auch auf dem illegalen Markt für Opioide verkauft wurde. Daher wissen Nutzer möglicherweise nicht, dass sie Isotonitazen verwenden. |
|
(7) |
Es bestehen keine anerkannten Einsatzmöglichkeiten von Isotonitazen zu human- oder veterinärmedizinischen Zwecken in der Union und vermutlich auch nicht anderswo. Es gibt keine Anhaltspunkte dafür, dass die Substanz neben ihrem Einsatz als analytischer Referenzstandard und in der wissenschaftlichen Forschung zu anderen Zwecken genutzt werden könnte. |
|
(8) |
Der Risikobewertungsbericht zeigt, dass viele mit Isotonitazen im Zusammenhang stehende Fragen, die der Mangel an Informationen zu den Risiken für die Gesundheit von Einzelpersonen sowie die öffentliche Gesundheit und die Gesellschaft aufwirft, durch weitere Forschung geklärt werden könnten. Zu den sozialen Risiken im Zusammenhang mit Isotonitazen liegen keine spezifischen Informationen vor. Die verfügbaren Nachweise und Informationen über die von dem Stoff ausgehenden Gesundheitsrisiken, auch angesichts der Tatsache, dass der Stoff relativ unbekannt ist, bieten jedoch ausreichenden Grund für die Einbeziehung von Isotonitazen in die Definition von Drogen. |
|
(9) |
Isotonitazen ist nicht auf der Liste der Substanzen verzeichnet, die gemäß dem Einheits-Übereinkommen der Vereinten Nationen von 1961 über Suchtstoffe in der durch das Protokoll von 1972 geänderten Fassung oder dem Übereinkommen der Vereinten Nationen von 1971 über psychotrope Stoffe Kontrollmaßnahmen unterliegen. Isotonitazen wird derzeit keiner Bewertung im Rahmen des Systems der Vereinten Nationen unterzogen. |
|
(10) |
Vier Mitgliedstaaten haben Isotonitazen gesetzlichen Kontrollmaßnahmen im Rahmen ihrer nationalen Drogenkontrollgesetze unterworfen, und ein Mitgliedstaat sowie das Vereinigte Königreich und Norwegen kontrollieren Isotonitazen im Rahmen sonstiger legislativer Maßnahmen; die Aufnahme dieser Substanz in die Kategorie Drogen und somit ihre Erfassung vom Anwendungsbereich der gemäß der Definition des Rahmenbeschlusses 2004/757/JI festgelegten Bestimmungen in Bezug auf Straftatbestände und Sanktionen würde daher dazu beitragen, Probleme bei der grenzüberschreitenden Strafverfolgung und justiziellen Zusammenarbeit zu vermeiden und vor den mit der Verfügbarkeit und dem Konsum der Substanz verbundenen Risiken zu schützen. |
|
(11) |
Durch Artikel 1a des Rahmenbeschlusses 2004/757/JI wird der Kommission die Befugnis übertragen, delegierte Rechtsakte zu erlassen, damit auf Unionsebene zügig und fachkompetent auf von den Mitgliedstaaten ermittelte und gemeldete neue psychoaktive Substanzen reagiert werden kann, indem der Anhang des Rahmenbeschlusses dahin gehend geändert wird, dass die betreffenden Stoffe in die Definition von Drogen aufgenommen werden. |
|
(12) |
Die verfügbaren Informationen deuten darauf hin, dass der Konsum von Isotonitazen Gesundheitsschäden verursacht, die mit seiner akuten Toxizität und seinem Missbrauchs- und Abhängigkeitspotenzial zusammenhängen. Diese Gesundheitsschädigung gilt als lebensbedrohlich. Darüber hinaus besteht das Potenzial für schwere körperliche oder geistige Beeinträchtigung oder eine erhebliche Ausbreitung von Krankheiten einschließlich der Übertragung von Viren durch Blut. Diese Auswirkungen, einschließlich der Abhängigkeit, sind mit anderen Opioidanalgetika vergleichbar, die internationalen Kontrollmaßnahmen unterliegen. |
|
(13) |
Da die Bedingungen für die Ausübung der Befugnis zum Erlass eines delegierten Rechtsakts erfüllt sind und das Verfahren eingehalten wurde, sollte eine delegierte Richtlinie erlassen werden, um Isotonitazen in den Anhang des Rahmenbeschlusses 2004/757/JI aufzunehmen und diese Substanz folglich den strafrechtlichen Bestimmungen der Union über den illegalen Drogenhandel zu unterwerfen. |
|
(14) |
Irland ist durch den Rahmenbeschluss 2004/757/JI, geändert durch die Richtlinie (EU) 2017/2103 des Europäischen Parlaments und des Rates (4), gebunden und beteiligt sich daher an der Annahme und Anwendung des vorliegenden Beschlusses. |
|
(15) |
Dänemark ist durch den Rahmenbeschluss 2004/757/JI in der bis zum 21. November 2018 geltenden Fassung, nicht aber durch die Richtlinie (EU) 2017/2103 gebunden. Dänemark beteiligt sich daher nicht an der Annahme und Anwendung dieser Richtlinie und ist weder durch diese Richtlinie gebunden noch zu ihrer Anwendung verpflichtet. |
|
(16) |
Gemäß der Gemeinsamen Politischen Erklärung vom 28. September 2011 der Mitgliedstaaten und der Kommission zu erläuternden Dokumenten (5) haben sich die Mitgliedstaaten verpflichtet, in begründeten Fällen zusätzlich zur Mitteilung ihrer Umsetzungsmaßnahmen ein oder mehrere Dokumente zu übermitteln, in denen der Zusammenhang zwischen den Bestandteilen einer Richtlinie und den entsprechenden Teilen nationaler Umsetzungsinstrumente erläutert wird. |
|
(17) |
Der Rahmenbeschluss 2004/757/JI sollte daher entsprechend geändert werden — |
HAT FOLGENDE RICHTLINIE ERLASSEN:
Artikel 1
Änderung des Rahmenbeschlusses 2004/757/JI
Im Anhang des Rahmenbeschlusses 2004/757/JI wird folgende Nummer 17 angefügt:
|
„17. |
N,N-Diethyl-2-[[4-(1-methylethoxy)phenyl]methyl]-5-nitro-1H-benzimidazol-1-ethanamin (Isotonitazen). (*1) |
Artikel 2
Umsetzung
(1) Die Mitgliedstaaten erlassen die Rechts- und Verwaltungsvorschriften, um dieser Richtlinie spätestens bis zum/binnen 3. Juni 2021 nachzukommen. Sie teilen der Kommission unverzüglich den Wortlaut dieser Vorschriften mit.
Bei Erlass dieser Vorschriften nehmen die Mitgliedstaaten in den Vorschriften selbst oder durch einen Hinweis bei der amtlichen Veröffentlichung auf die vorliegende Richtlinie Bezug. Die Mitgliedstaaten regeln die Einzelheiten dieser Bezugnahme.
(2) Die Mitgliedstaaten teilen der Kommission den Wortlaut der wichtigsten nationalen Vorschriften mit, die sie auf dem unter diese Richtlinie fallenden Gebiet erlassen.
Artikel 3
Inkrafttreten
Diese Richtlinie tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Artikel 4
Diese Richtlinie ist gemäß den Verträgen an die Mitgliedstaaten gerichtet.
Brüssel, den 2. September 2020
Für die Kommission
Die Präsidentin
Ursula VON DER LEYEN
(1) ABl. L 335 vom 11.11.2004, S. 8.
(2) Verordnung (EG) Nr. 1920/2006 des Europäischen Parlaments und des Rates vom 12. Dezember 2006 über die Europäische Beobachtungsstelle für Drogen und Drogensucht (ABl. L 376 vom 27.12.2006, S. 1).
(3) Todesfälle wurden auch in Kanada (drei Fälle) und in den Vereinigten Staaten (18 Fälle) berichtet.
(4) Richtlinie (EU) 2017/2103 des Europäischen Parlaments und des Rates vom 15. November 2017 zur Änderung des Rahmenbeschlusses 2004/757/JI des Rates zur Aufnahme neuer psychoaktiver Substanzen in die Drogendefinition und zur Aufhebung des Beschlusses 2005/387/JI des Rates (ABl. L 305 vom 21.11.2017, S. 12).
BESCHLÜSSE
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/58 |
BESCHLUSS (EU) 2020/1688 DER EUROPÄISCHEN ZENTRALBANK
vom 25. September 2020
zur Änderung des Beschlusses (EU) 2020/187 über die Umsetzung des dritten Programms zum Ankauf gedeckter Schuldverschreibungen (EZB/2020/48)
DER EZB-RAT —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union, insbesondere auf Artikel 127 Absatz 2 erster Gedankenstrich,
gestützt auf die Satzung des Europäischen Systems der Zentralbanken und der Europäischen Zentralbank, insbesondere auf Artikel 12.1 zweiter Unterabsatz in Verbindung mit Artikel 3.1 erster Gedankenstrich und Artikel 18.1,
in Erwägung nachstehender Gründe:
|
(1) |
Durch den Beschluss EZB/2014/40 der Europäischen Zentralbank (1) wurde das dritte Programm zum Ankauf gedeckter Schuldverschreibungen (third covered bond purchase programme — CBPP3) eingeführt. Der Beschluss wurde mit dem Beschluss (EU) 2020/187 der Europäischen Zentralbank (EZB/2020/8) (2) neu gefasst. Neben dem Ankaufprogramm für Asset-Backed Securities, dem Programm zum Ankauf von Wertpapieren des öffentlichen Sektors an den Sekundärmärkten und dem Programm zum Ankauf von Wertpapieren des Unternehmenssektors ist das CBPP3 Teil des erweiterten Programms zum Ankauf von Vermögenswerten (asset purchase programme — APP) der Europäischen Zentralbank (EZB). Ziel des APP ist es, die Transmission der Geldpolitik weiter zu verbessern, die Kreditversorgung der Wirtschaft im Euro-Währungsgebiet zu vereinfachen, die Kreditbedingungen für private Haushalte und Unternehmen zu lockern und entsprechend dem vorrangigen Ziel der EZB, die Preisstabilität zu gewährleisten, dazu beizutragen, dass die Inflationsraten mittelfristig auf ein Niveau von unter, aber nahe 2 % zurückkehren. |
|
(2) |
Am 5. März 2020 hat der EZB-Rat grundsätzlich beschlossen, unter bestimmten vorher festgelegten Umständen eine automatische Zugangsbeschränkung zu geldpolitischen Geschäften des Eurosystems für zugelassene Geschäftspartner einzuführen. Infolgedessen hat der EZB-Rat außerdem beschlossen, wenn und solange eine solche automatische Beschränkung oder eine Aussetzung oder ein Ausschluss gemäß der Leitlinie (EU) 2015/510 der Europäischen Zentralbank (EZB/2014/60) (3) gilt, einen entsprechenden automatischen Ausschluss von Ankäufen gedeckter Schuldverschreibungen, die vom Geschäftspartner begeben wurden, im Rahmen des CBPP3 einzuführen. Der EZB-Rat hat ferner beschlossen, dass die Änderungen, die den Beschlüssen Rechnung tragen, ab dem Datum gelten sollten, ab dem die jährliche Änderung der Leitline (EU) 2015/510 (EZB/2014/60) gilt. |
|
(3) |
Der Beschluss (EU) 2020/187 (EZB/2020/8) sollte daher entsprechend geändert werden — |
HAT FOLGENDEN BESCHLUSS ERLASSEN:
Artikel 1
Änderung
Der Beschluss (EU) 2020/187 (EZB/2020/8) wird wie folgt geändert:
Artikel 3 Absatz 3 Buchstabe d erhält folgende Fassung:
|
„d) |
Schuldverschreibungen, die von Kreditinstituten begeben werden, deren Zugang zu geldpolitischen Geschäften des Eurosystems gemäß der Leitlinie (EU) 2015/510 (EZB/2014/60) beschränkt, ausgesetzt oder ausgeschlossen worden ist, sind für die Dauer der Beschränkung, der Aussetzung oder des Ausschlusses automatisch von Ankäufen im Rahmen des CBPP3 ausgeschlossen. Abweichend vom ersten Satz dieses Buchstaben d behält der EZB-Rat die Befugnis, nach einer Prüfung im jeweiligen Einzelfall den Ausschluss gedeckter Schuldverschreibungen, die von einem Kreditinstitut begeben wurden, dessen Zugang zu geldpolitischen Geschäften des Eurosystems gemäß der Leitlinie (EU) 2015/510 (EZB/2014/60) beschränkt, ausgesetzt oder ausgeschlossen worden ist, erneut zu prüfen und den Ausschluss zu widerrufen, wenn der EZB-Rat dies für angemessen hält“. |
Artikel 2
Inkrafttreten
Dieser Beschluss tritt am zwanzigsten Tag nach seiner Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Er gilt ab dem 1. Januar 2021.
Geschehen zu Frankfurt am Main am 25. September 2020.
Für den EZB-Rat
Die Präsidentin der EZB
Christine LAGARDE
(1) Beschluss EZB/2014/40 der Europäischen Zentralbank vom 15. Oktober 2014 über die Umsetzung des dritten Programms zum Ankauf gedeckter Schuldverschreibungen (ABl. L 335 vom 22.11.2014, S. 22).
(2) Beschluss (EU) 2020/187 der Europäischen Zentralbank vom 3. Februar 2020 über die Umsetzung des dritten Programms zum Ankauf gedeckter Schuldverschreibungen (EZB/2020/8) (ABl. L 39 vom 12.2.2020, S. 6).
(3) Leitlinie (EU) 2015/510 der Europäischen Zentralbank vom 19. Dezember 2014 über die Umsetzung des geldpolitischen Handlungsrahmens des Eurosystems (Leitlinie allgemeine Dokumentation) (EZB/2014/60) (ABl. L 91 vom 2.4.2015, S. 3).
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/60 |
BESCHLUSS (EU) 2020/1689 DER EUROPÄISCHEN WERTPAPIER- UND MARKTAUFSICHTSBEHÖRDE
vom 16. September 2020
zur Verlängerung der gemäß Artikel 28 Absatz 1 Buchstabe a der Verordnung (EU) Nr. 236/2012 des Europäischen Parlaments und des Rates angeordneten vorübergehenden Herabsetzung der für natürliche oder juristische Personen, die eine Netto-Leerverkaufsposition im ausgegebenen Aktienkapital eines Unternehmens, dessen Aktien zum Handel an einem geregelten Markt zugelassen sind, halten, geltenden Meldeschwellen für die Meldung von Netto-Leerverkaufspositionen an die zuständigen Behörden
DER RAT DER AUFSEHER DER EUROPÄISCHEN WERTPAPIER- UND MARKTAUFSICHTSBEHÖRDE —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf das Abkommen über den Europäischen Wirtschaftsraum, insbesondere auf Anhang IX,
gestützt auf die Verordnung (EU) Nr. 1095/2010 des Europäischen Parlaments und des Rates vom 24. November 2010 zur Errichtung einer Europäischen Aufsichtsbehörde (Europäische Wertpapier- und Marktaufsichtsbehörde), zur Änderung des Beschlusses Nr. 716/2009/EG und zur Aufhebung des Beschlusses 2009/77/EG der Kommission, insbesondere auf Artikel 9 Absatz 5, Artikel 43 Absatz 1 und Artikel 44 Absatz 1 (1),
gestützt auf die Verordnung (EU) Nr. 236/2012 des Europäischen Parlaments und des Rates vom 14. März 2012 über Leerverkäufe und bestimmte Aspekte von Credit Default Swaps (2), insbesondere auf Artikel 28 Absatz 1,
gestützt auf die Delegierte Verordnung (EU) Nr. 918/2012 der Kommission vom 5. Juli 2012 zur Ergänzung der Verordnung (EU) Nr. 236/2012 des Europäischen Parlaments und des Rates über Leerverkäufe und bestimmte Aspekte von Credit Default Swaps im Hinblick auf Begriffsbestimmungen, die Berechnung von Netto-Leerverkaufspositionen, gedeckte Credit Default Swaps auf öffentliche Schuldtitel, Meldeschwellen, Liquiditätsschwellen für die vorübergehende Aufhebung von Beschränkungen, signifikante Wertminderungen bei Finanzinstrumenten und ungünstige Ereignisse (3), insbesondere auf Artikel 24,
gestützt auf Beschluss (EU) 2020/525 der Europäischen Wertpapier- und Marktaufsichtsbehörde vom 16. März 2020 zur gemäß Artikel 28 Absatz 1 Buchstabe a der Verordnung (EU) Nr. 236/2012 ergehenden Aufforderung an natürliche oder juristische Personen, die eine Netto-Leerverkaufsposition halten, die Meldeschwellen für Netto-Leerverkaufspositionen im ausgegebenen Aktienkapital eines Unternehmens, dessen Aktien zum Handel an einem geregelten Markt zugelassen sind, vorübergehend zu senken, um die zuständigen Behörden beim Überschreiten einer bestimmten Schwelle zu benachrichtigen (4),
gestützt auf Beschluss (EU) 2020/1123 der Europäischen Wertpapier- und Marktaufsichtsbehörde vom 10. Juni 2020 zur Verlängerung der gemäß Artikel 28 Absatz 1 Buchstabe a der Verordnung (EU) Nr. 236/2012 des Europäischen Parlaments und des Rates angeordneten vorübergehenden Herabsetzung der Meldeschwellen für Netto-Leerverkaufspositionen, deren Überschreitung natürliche oder juristische Personen, die eine Netto-Leerverkaufsposition im ausgegebenen Aktienkapital eines Unternehmens, dessen Aktien zum Handel an einem geregelten Markt zugelassen sind, den zuständigen Behörden melden müssen (5),
in Erwägung nachstehender Gründe:
1. EINLEITUNG
|
(1) |
Mit dem Beschluss (EU) 2020/525 forderte die ESMA gemäß Artikel 28 Absatz 1 Buchstabe a der Verordnung (EU) Nr. 236/2012 natürliche oder juristische Personen, die Netto-Leerverkaufspositionen in Bezug auf das ausgegebene Aktienkapital eines Unternehmens halten, dessen Aktien zum Handel an einem geregelten Markt zugelassen sind, auf, einer zuständigen Behörde jede solche Position zu melden, wenn diese Position 0,1 % des ausgegebenen Aktienkapitals erreicht, überschreitet oder unterschreitet. |
|
(2) |
Die durch den Beschluss (EU) 2020/525 eingeführte Maßnahme trug der Notwendigkeit Rechnung, dass die zuständigen nationalen Behörden und angesichts der jüngsten außergewöhnlichen Entwicklungen auf den Finanzmärkten in der Lage sein müssen, die von Marktteilnehmern eingegangenen Netto-Leerverkaufspositionen in Aktien, die zum Handel an einem geregelten Markt zugelassen sind, zu überwachen. |
|
(3) |
Mit dem Beschluss (EU) 2020/1123 der ESMA wurde die vorübergehende Anordnung verlängert, ungeachtet der teilweisen Erholung der EU-Finanzmärkte von den seit Ausbruch der Pandemie verzeichneten Verlusten, da die Aussichten auf eine künftige Erholung jedoch nach wie vor ungewiss und die ordnungsgemäße Funktionsweise und Integrität der Finanzmärkte und die Stabilität des Finanzsystems weiterhin bedroht sind. |
|
(4) |
Gemäß Artikel 28 Absatz 10 der Verordnung (EU) Nr. 236/2012 muss die ESMA diese Maßnahme in geeigneten Zeitabständen, mindestens aber alle drei Monate, überprüfen. |
|
(5) |
Für die von der ESMA zum Zwecke dieser Überprüfung durchgeführte Indikatorenanalyse wurden u. a. Preise, Volatilität, Credit-Default-Swaps-Spread-Indizes sowie die Entwicklung von Netto-Leerverkaufspositionen berücksichtigt, insbesondere diejenigen zwischen 0,1 % und 0,2 %. Auf Grundlage der durchgeführten Analyse hat die ESMA beschlossen, dass sie die Maßnahme um zusätzliche drei Monate verlängern sollte. |
2. EIGNUNG DER MASSNAHME ZUR BEWÄLTIGUNG RELEVANTER BEDROHUNGEN UND GRENZÜBERGREIFENDER AUSWIRKUNGEN (ARTIKEL 28 ABSATZ 2 BUCHSTABE a DER VERORDNUNG (EU) Nr. 236/2012)
a) Bedrohung der ordnungsgemäßen Funktionsweise und Integrität der Finanzmärkte
|
(6) |
Die COVID-19-Pandemie hat weiterhin negative Auswirkungen auf die Realwirtschaft, und die Gesamtaussichten auf eine künftige Erholung sind nach wie vor ungewiss, insbesondere vor dem Hintergrund der jüngsten Entwicklungen in der EU und darüber hinaus. Die ESMA weist darauf hin, dass in mehreren Ländern die Anzahl der COVID-19-Fälle in den letzten Wochen erheblich gestiegen ist, was die Möglichkeit einer zweiten Welle von COVID-19-Infektionen und noch ungewissere Zukunftsaussichten befürchten lässt. |
|
(7) |
Die Aktienmärkte in der EU sind, gemessen am Euro Stoxx 50 Index, im Zeitraum zwischen dem 20. Februar und dem 3. September 2020 um 14 % zurückgegangen; im Vergleich dazu betrug der Wertverlust zwischen dem 20. Februar und dem 4. Juni 13 % (Abbildung 1). Gegenüber den im März verzeichneten Werten (als der Rückgang gegenüber Februar 2020 etwa 30 % betrug, vgl. Beschluss (EU) 2020/525) hat der EuroStoxx 50 Index erheblich zugelegt, ohne jedoch auf das vor COVID-19 erreichte Niveau zurückzukehren. |
|
(8) |
Gemessen am VSTOXX (6) ist auch die Volatilität, verglichen mit Februar 2020, immer noch relativ hoch. Im September wurde ein etwas höheres Niveau (+ 15 %) verzeichnet als im Juni (+ 13 %). Dies gilt auch, und sogar in höherem Maße, für den VIX (7) (+ 18 % im September im Vergleich zu + 9 % im Juni) (Abbildung 1 und Abbildung 2). |
|
(9) |
Bei den Credit Default Swaps (CDS) wurden im Zeitraum 4. Juni bis 3. September Rückgänge zwischen 17 % und 28 % verzeichnet (Abbildung 1). Die Aussagekraft der CDS lässt sich derzeit allerdings besser verstehen, wenn man die Daten im Zusammenhang mit dem von der Europäischen Zentralbank (EZB) beschlossenen Anleihekaufprogramm Pandemic Emergency Purchase Programme (PEPP) betrachtet. Anfang März begannen die CDS-Spreads hohe Volatilität zu zeigen, was auf ein hohes Ausfallrisiko hindeutet. Die von der ESMA auf Grundlage der Daten bis zum 4. Juni vorgenommene Verlängerung des Beschlusses (EU) 2020/525 wurde auch auf die seinerzeit hohen und volatilen CDS-Spreads gestützt, die als Anzeichen für die Risikoeinschätzung im Markt gewertet wurden. |
|
(10) |
Mit der am 4. Juni beschlossenen Erhöhung des PEPP um weitere 600 Mrd. EUR wurde der von der EZB angekündigte geldpolitische Stimulus auf insgesamt 1,35 Billionen EUR angehoben, wodurch die Aussagekraft der CDS-Spreads für die Risikowahrnehmung im Markt reduziert wurde. |
|
(11) |
Ähnliche Erwägungen lassen sich auch im Hinblick auf die Aussagekraft der Märkte für Staatsanleihen anstellen, die — wie die CDS-Spreads — durch die Geldpolitik der Zentralbanken beeinflusst werden. Aus Abbildung 1 geht hervor, dass die Renditen der zehnjährigen Staatsanleihen in Deutschland, Frankreich, Großbritannien und Italien gegenüber den Werten im Juni im Durchschnitt etwa 22 Basispunkte verloren haben. |
|
(12) |
Die ESMA ist daher der Ansicht, dass die Aktienmarktentwicklung, die wesentlich weniger durch die Geldpolitik der Zentralbanken beeinflusst ist, mehr Aufschluss über das derzeitige Risikoniveau der Finanzmärkte in der EU geben dürfte. |
|
(13) |
Ähnlich wie der Euro Stoxx 50 hat auch der STOXX EUROPE 800 Index (ohne die Schweiz) seit dem 20. Februar 2020 (bis September) etwa 17 % verloren, bis zum Juni betrug der Rückgang 16 %. Der STOXX Europe Total Market Banks Index (der europäische Banken erfasst) ist seit Februar (bis September) um 37 % zurückgegangen, bis zum Juni lag der Rückgang bei etwa 30 %. |
|
(14) |
Wie die ESMA in ihrem zweiten, im September 2020 veröffentlichten „Report on Trends, Risks and Vulnerabilities“ (TRV-Bericht) berichtet, gab es im 2. Quartal 2020 Anzeichen für eine unterschiedliche Sektorentwicklung, die vor allem Kreditinstitute betraf. Ende Juni lagen die EU-Sektorindizes für Fluggesellschaften und den Banksektor immer noch 36 % bzw. 30 % unter ihrem jeweiligen Niveau von Anfang Januar. Abbildung 3 ist zu entnehmen, dass sowohl der Bank- als auch der Versicherungssektor seit Juni recht stabil sind, die Entwicklung im Zeitraum 20. Februar bis 3. September jedoch schlechter war als im Zeitraum 20. Februar bis 4. Juni: – 38 % gegenüber – 33 % für den Banksektor und – 21 % gegenüber – 20 % für den Versicherungssektor. Dagegen hat sich die Entwicklung der Sektoren außerhalb des Finanzbereichs (8) leicht gebessert: auf jetzt – 9 % gegenüber zuvor – 11 %. |
|
(15) |
Die Preiserholung gewisser Sektoren erfolgte vor dem Hintergrund einer weiteren Verschlechterung des makroökonomischen Umfelds und einer tiefgreifenden und weltweit synchron verlaufenden Rezession. Laut dem TRV-Bericht stellt sich angesichts der derzeit erkennbaren Abkopplung der Finanzmarktentwicklung von der konjunkturellen Grunddynamik die Frage der Nachhaltigkeit der künftigen Markterholung. |
|
(16) |
Betrachtet man die Gesamtzahlen auf nationaler oder EU-Ebene, so ist keine Preiserholung zu erkennen: Abbildung 5 zeigt, dass die Preise unionsweit fielen, dass es von Juni bis September keine erheblichen Verbesserungen gab und dass die Aktienindexentwicklung für 22 EU-Märkte im Zeitraum 20. Februar bis 3. September noch stärker rückläufig war als im Zeitraum 20. Februar bis 4. Juni. Vergleicht man die Preise vom 3. September mit den Preisen vom 20. Februar 2020, haben die Aktienmärkte von 25 Ländern (im Juni: 24 Ländern) mindestens 10 % ihres Werts verloren. Im selben Zeitraum sind die Aktienkurse europäischer Kreditinstitute zwischen 10 % und 59 % gefallen, was im Vergleich zu Wertverlusten zwischen 9 % und 48 % im Zeitraum Februar bis Juni zu betrachten ist. |
|
(17) |
Der prozentuale Anteil von Aktien mit einer Netto-Leerverkaufsposition zwischen 0,1 % und 0,2 % ist im Zeitraum 16. März bis 11. Juni 2020 stetig gestiegen und hat dann bis zum 4. September 2020 (9) stabil bei im Durchschnitt etwa 13 % der Gesamt-Netto-Leerverkaufspositionen gelegen (Abbildung 6). Die niedrigere Meldeschwelle hat gezeigt, dass der prozentuale Anteil der Netto-Leerverkaufspositionen zwischen 0,1 % und 0,2 % in einigen Ländern bis zu etwa 50 % der insgesamt gemeldeten Positionen ausmachte. Abschließend ist festzustellen, dass der prozentuale Anteil der Netto-Leerverkaufspositionen zwischen 0,1 % und 0,2 %, die wegen der vorübergehend herabgesetzten Meldeschwelle gemeldet werden mussten, nach wie vor einen relevanten Teil der Gesamtmenge der Netto-Leerverkaufspositionen ausmacht und im derzeitigen Umfeld für die Regulierungsbehörden eine hohe Aussagekraft hat. |
|
(18) |
Insgesamt sind die erheblichen Preisrückgänge in Schlüsselsektoren, die relativ hohe Volatilität, die potenzielle Abkopplung der Finanzmarktentwicklung von der konjunkturellen Grunddynamik und der unverändert hohe Bestand an Netto-Leerverkaufspositionen im Zusammenspiel mit der Entwicklung der COVID-19-Pandemie und deren Auswirkungen auf die Realwirtschaft ein Signal dafür, dass der Zustand der Finanzmärkte in der EU nach wie vor fragil ist. Bei dieser Lage ist es umso wahrscheinlicher, dass der Druck durch Leerverkäufe in den kommenden Monaten negative Entwicklungen auslösen oder verstärken könnte, was wiederum negative Auswirkungen auf das Marktvertrauen oder die Integrität der Kursbildung haben kann. |
|
(19) |
Die ESMA ist deshalb der Ansicht, dass das Zusammenspiel der oben beschriebenen Umstände eine schwerwiegende Bedrohung für die ordnungsgemäße Funktionsweise und Integrität der Finanzmärkte darstellt. |
b) Bedrohung der Stabilität eines Teils oder des gesamten Finanzsystems der Union
|
(20) |
Wie die EZB in ihrem Finanzstabilitätsbericht erklärt (10), beschreibt der Begriff der Finanzstabilität einen Zustand, in dem das Finanzsystem — bestehend aus Finanzintermediären, Märkten und Marktinfrastrukturen — Schocks und dem Entstehen finanzieller Schieflagen standhalten kann. |
|
(21) |
Die COVID-19-Pandemie hat weiterhin schwerwiegende Auswirkungen auf die Realwirtschaft in der Union. Laut dem TRV-Bericht der ESMA ist das Marktumfeld trotz der Markterholung weiterhin fragil, sodass die ESMA eine „längere Risikophase für institutionelle Anleger und Kleinanleger, mit der Gefahr weiterer — möglicherweise erheblicher — Marktkorrekturen und (…) sehr hohen Risiken im gesamten Zuständigkeitsbereich der ESMA“ (11) erwartet. Diesbezüglich hat die ESMA die Öffentlichkeit vor der Möglichkeit einer Abkopplung der jüngsten Finanzmarktentwicklung von der konjunkturellen Grunddynamik gewarnt. |
|
(22) |
Der obige Abschnitt 2.a enthält nähere Angaben zur Entwicklung des Banksektors, der Versicherungssektoren und der Finanzmärkte. |
|
(23) |
Diese weitverbreiteten Kursrückgänge haben für die Mehrheit der EU-Aktien aus allen Sektoren eine Situation der Fragilität geschaffen, in der weitere, nicht durch zusätzliche Fundamentaldaten ausgelöste Kursrückgänge äußerst nachteilige Folgen haben könnten. |
|
(24) |
Im derzeitigen unsicheren Kontext könnten nach Einschätzung der ESMA verschiedene Faktoren — unter anderem ein Anstieg der Anzahl der Leerverkäufe eingehenden oder erhebliche Netto-Leerverkaufspositionen ausbauenden Marktteilnehmer — erheblichen Verkaufsdruck und außergewöhnliche Volatilität der Aktienkurse auslösen. |
|
(25) |
Insbesondere weist die ESMA darauf hin, dass hinsichtlich der allgemeinen Kursrückgänge bei Kreditinstituten, auf die die im Juni getroffene Verlängerungsentscheidung unter anderem gestützt wurde, keine Besserung eingetreten ist. Dies deutet darauf hin, dass Kreditinstitute, von denen einige systemrelevant sind, nach wie vor durch Leerverkaufsstrategien und den Aufbau erheblicher Netto-Leerverkaufspositionen gefährdet sein können, ganz unabhängig davon, ob diese Strategien und Positionen auf Fundamentaldaten beruhen. |
|
(26) |
Nach wie vor besteht die Gefahr, dass die Zunahme von Leerverkaufsstrategien und der Aufbau von erheblichen Netto-Leerverkaufspositionen für bestimmte Emittenten zu einer ungeordneten Abwärtsspirale der Kurse führen könnte, die auf Bereiche innerhalb desselben Mitgliedstaats oder anderswo in der Union übergreifen und letztendlich das Finanzsystem eines oder mehrerer Mitgliedstaaten gefährden könnte. |
|
(27) |
Trotz der beobachteten teilweisen Erholung in gewissen Bereichen der europäischen Finanzmärkte ist die ESMA der Ansicht, dass die derzeitigen Marktbedingungen eine schwerwiegende Bedrohung der Stabilität des Finanzsystems der Union darstellen. |
|
(28) |
Im Rahmen des Mandats der ESMA verpflichtet die beabsichtigte Verlängerung der Maßnahme natürliche oder juristische Personen, die eine Netto-Leerverkaufsposition in Aktien halten, die zum Handel auf einem geregelten Markt zugelassen sind, die Meldung an die zuständigen nationalen Behörden bei einer niedrigeren als der in Artikel 5 der Verordnung (EU) Nr. 236/2012 vorgesehenen Schwelle vorzunehmen. |
|
(29) |
Die verlängerte Maßnahme soll dafür sorgen, dass die zuständigen nationalen Behörden und die ESMA weiterhin besser in der Lage sind, die Situation angemessen zu bewerten; auf Fundamentaldaten reagierende Marktbewegungen von solchen zu unterscheiden, die durch Leerverkäufe ausgelöst oder verstärkt worden sein könnten; und zu reagieren, wenn im Hinblick auf die Integrität, ordnungsgemäße Funktionsweise und Stabilität der Märkte strengere Maßnahmen erforderlich sind. |
c) Grenzübergreifende Auswirkungen
|
(30) |
Eine weitere Voraussetzung dafür, dass die ESMA diese Maßnahme ergreifen kann, ist, dass die festgestellten Bedrohungen grenzübergreifende Auswirkungen haben. |
|
(31) |
Wie vorstehend beschrieben, haben sich die EU-Aktienmärkte, wenn man auf die nationalen und gesamteuropäischen Indizes abstellt, noch nicht voll von den im März gesehenen schweren Kurseinbrüchen erholt. |
|
(32) |
Angesichts des Umstands, dass die Finanzmärkte der meisten Mitgliedstaaten der EU, wenngleich in unterschiedlichem Maße, durch diese Bedrohungen gefährdet sind, sind die grenzübergreifenden Auswirkungen nach wie vor besonders ernst zu nehmen, da die Verbundenheit der EU-Finanzmärkte untereinander die Wahrscheinlichkeit, dass durch Leerverkaufsdruck ausgelöste Effekte auf andere Märkte übergreifen oder sie anstecken könnte, erhöht. |
|
(33) |
Die ESMA ist daher der Ansicht, dass die Bedrohungen für die Integrität und ordnungsgemäße Funktionsweise der Märkte sowie die Finanzstabilität grenzübergreifende Auswirkungen haben. Die COVID-19-Krise ist solcher Art, dass die Auswirkungen gesamteuropäischen und globalen Charakters sind. |
3. KEINE ZUSTÄNDIGE BEHÖRDE HAT MASSNAHMEN ERGRIFFEN, UM DER BEDROHUNG ZU BEGEGNEN, ODER EINE ODER MEHRERE DER ZUSTÄNDIGEN BEHÖRDEN HABEN MASSNAHMEN ERGRIFFEN, DIE DER BEDROHUNG NICHT IN ANGEMESSENER WEISE GERECHT WERDEN (ARTIKEL 28 ABSATZ 2 BUCHSTABE b DER VERORDNUNG (EU) Nr. 236/2012).
|
(34) |
Eine weitere Voraussetzungen dafür, dass die ESMA die im vorliegenden Beschluss genannte Maßnahme einführen kann, ist, dass nicht von einer oder mehreren zuständigen Behörden Maßnahmen ergriffen wurden, um der Bedrohung zu begegnen, oder dass die ergriffenen Maßnahmen der Bedrohung nicht in angemessener Weise gerecht werden. |
|
(35) |
Die im Beschluss (EU) 2020/525 beschriebenen Bedenken hinsichtlich der ordnungsgemäßen Funktionsweise und Integrität des Markts sowie der Finanzstabilität, die weiterhin auch für diesen Beschluss gelten, haben einige zuständige nationale Behörden dazu veranlasst, nationale Maßnahmen zur Einschränkung des Leerverkaufs von Aktien in Spanien, Frankreich, Österreich, Belgien, Griechenland und Italien (12) (am 18. Mai abgelaufen), zu ergreifen. |
|
(36) |
Nach Ablauf oder Aufhebung der vorübergehenden Maßnahmen wurden in der EU keine weiteren Maßnahmen auf der Grundlage der Verordnung (EU) Nr. 236/2012 ergriffen, und zum Zeitpunkt des vorliegenden Beschlusses sind keine derartigen Maßnahmen in Kraft. |
|
(37) |
Zum Zeitpunkt der Verabschiedung dieses Beschlusses hat keine der zuständigen Behörden Maßnahmen ergriffen, um die Entwicklung der Netto-Leerverkaufspositionen durch die Herabsetzung der Meldeschwellen besser sichtbar zu machen, weil sich die zuständigen Behörden auf den Beschluss (EU) 2020/1123 stützen können. |
|
(38) |
Die Notwendigkeit gesteigerter Sichtbarkeit von Netto-Leerverkaufspositionen ist insofern umso dringender erforderlich, als die oben genannten Beschränkungen, die aufgrund Artikel 20 der Verordnung (EU) Nr. 236/2012 verhängt wurden, nicht mehr gelten, die Unsicherheit wegen der sich hinziehenden Auswirkungen von COVID-19 jedoch fortbesteht. Da Leerverkäufe und Geschäfte mit entsprechender Wirkung keinen äußeren Beschränkungen mehr unterliegen, müssen die zuständigen nationalen Behörden unionsweit in der Lage sein, vorab zu erkennen, ob Netto-Leerverkaufspositionen in solchem Umfang aufgebaut werden, dass die oben beschriebenen Bedrohungen für die Finanzmärkte und die Finanzstabilität entstehen und durch Leerverkaufsdruck verstärkt werden könnten. |
|
(39) |
Vor dem Hintergrund der oben genannten unionsweiten Bedrohungen ist weiterhin deutlich, dass die Informationen, die bei Anwendung der ordentlichen Meldeschwelle in Artikel 5 Absatz 2 der Verordnung (EU) Nr. 236/2012 bei den zuständigen nationalen Behörden eingehen, unter den derzeitigen angespannten Marktbedingungen nicht ausreichen. Nach Auffassung der ESMA sollte die Herabsetzung der Meldeschwelle sicherstellen, dass alle zuständigen nationalen Behörden in der gesamten EU wie auch die ESMA über den bestmöglichen Datensatz verfügen, der für die Überwachung der Markttrends und erforderlichenfalls für die Vorbereitung weiterer eigener Maßnahmen und Maßnahmen der ESMA verfügbar ist. |
4. WIRKSAMKEIT DER MASSNAHME (ARTIKEL 28 ABSATZ 3 BUCHSTABE a DER VERORDNUNG (EU) Nr. 236/2012)
|
(40) |
Außerdem hat die ESMA berücksichtigt, inwieweit die verlängerte Maßnahme die erkannten Bedrohungen signifikant verringert. |
|
(41) |
Die ESMA ist der Ansicht, dass die Märkte trotz der außerordentlichen Verluste, die seit dem 20. Februar 2020 beim Handel mit Aktien an geregelten Märkten entstanden sind, ordnungsgemäß funktioniert haben und die Integrität der Märkte weitgehend gewahrt worden ist. |
|
(42) |
Die ESMA hat daher die aktuellen Bedingungen analysiert, insbesondere im Hinblick darauf, inwieweit sie die Integrität der Märkte und die Finanzstabilität in der Union gefährden und ob die verlängerte Maßnahme der ESMA einen zukunftsorientierten Ansatz darstellen würde, solchen Bedrohungen wirksam zu begegnen. |
a) Die Maßnahme bewirkt eine signifikante Verringerung der Bedrohung für die ordnungsgemäße Funktionsweise und Integrität der Finanzmärkte
|
(43) |
Unter den oben beschriebenen Bedingungen kann jede plötzliche Erhöhung des Verkaufsdrucks und der Marktvolatilität, die durch Leerverkäufe und den Aufbau von Leerverkaufspositionen ausgelöst wird, Abwärtstrends auf den Finanzmärkten verstärken. Zu anderen Zeiten können Leerverkäufe einen positiven Beitrag zur Ermittlung der richtigen Bewertung von Emittenten leisten, doch unter den aktuellen Marktbedingungen stellen sie eine zusätzliche Gefahr für die ordnungsgemäße Funktionsweise und Integrität der Märkte dar. |
|
(44) |
Angesichts der horizontalen Auswirkungen der anhaltenden Notsituation auf ein breites Spektrum von Aktien in der gesamten Union kann jeder plötzliche Kursverfall durch zusätzlichen Verkaufsdruck verstärkt werden, der durch Leerverkäufe und die Zunahme von Netto-Leerverkaufspositionen ausgelöst wird; solange diese unterhalb der in Artikel 5 der Verordnung (EU) Nr. 236/2012 festgelegten gewöhnlichen Meldeschwellen für die Meldung an die zuständigen nationalen Behörden liegen, würden sie, wenn es die verlängerte Maßnahme nicht gäbe, unentdeckt bleiben. |
|
(45) |
Aus den oben genannten Gründen müssen die zuständigen nationalen Behörden und die ESMA frühestmöglich erkennen, dass Marktteilnehmer Leerverkäufe eingehen und erhebliche Netto-Leerverkaufspositionen aufbauen, um erforderlichenfalls zu verhindern, dass von diesen Positionen das Signal zu einer Kaskade von Verkaufsaufträgen ausgeht, die einen weiteren signifikanten Kursverfall verursachen. |
|
(46) |
Ohne Verlängerung dieser Maßnahme um weitere drei Monate wäre es nach Ansicht der ESMA den zuständigen nationalen Behörden wie auch der ESMA im aktuellen unsicheren und fragilen Umfeld nicht möglich, den Markt angemessen zu überwachen. Dies gilt umso mehr im Hinblick auf die zu erkennende Abkopplung der Finanzmarktentwicklung von der konjunkturellen Grunddynamik im Zusammenspiel mit der Weiterentwicklung der COVID-19-Pandemie. Derartige Faktoren könnten plötzlichen und erheblichen Verkaufsdruck sowie ungewöhnliche Aktienkursschwankungen in der Union auslösen, die wiederum durch den Aufbau von Leerverkaufspositionen weiter verstärkt werden könnten. |
|
(47) |
Allerdings ist die ESMA der Ansicht, dass die Aufrechterhaltung der Offenlegungsschwelle, die in Artikel 6 der Verordnung (EU) Nr. 236/2012 festgelegt ist und bei einem Prozentsatz von 0,5 % des ausgegebenen Aktienkapitals des betreffenden Unternehmens liegt, ausreicht, da eine Herabsetzung dieser Schwelle zur Aufrechterhaltung geordneter Märkte und zur Eindämmung von Risiken für die Finanzstabilität nicht erforderlich erscheint. Die ESMA wird die Marktbedingungen weiter laufend überwachen und erforderlichenfalls weitere Maßnahmen ergreifen. |
b) Die Bedrohung der Stabilität eines Teils oder des gesamten Finanzsystems in der Union wird durch die Maßnahme signifikant verringert
|
(48) |
Wie oben beschrieben hat sich der Aktienmarkt in der EU im Zeitraum Juni bis September 2020, verglichen mit der Entwicklung seit dem 20. Februar, größtenteils verschlechtert. Der Aktienhandel ist seit dem 20. Februar 2020 von erheblichem Verkaufsdruck und relativ hoher Volatilität geprägt. Wie oben aufgezeigt, gibt es nach wie vor verschiedene Risikofaktoren, die sich auf viele Sektoren der Realwirtschaft wie auch auf die EU-Finanzmärkte auswirken. In diesem Umfeld können das Eingehen von Leerverkäufen und der Aufbau erheblicher Netto-Leerverkaufspositionen den Verkaufsdruck und die Abwärtstrends verstärken, wodurch wiederum die Bedrohung zunehmen kann, was sich äußerst nachteilig auf die Finanzstabilität von Finanzinstituten und Unternehmen aus anderen Sektoren auswirken kann. |
|
(49) |
In diesem Zusammenhang würde eine unzulängliche Datenlage die Fähigkeit der zuständigen nationalen Behörden und der ESMA, potenziell negativen Auswirkungen auf die Wirtschaft und letztlich die Finanzstabilität der gesamten Union entgegenzuwirken, beeinträchtigen. |
|
(50) |
Die verlängerte Maßnahme der ESMA, durch die die Schwellen für die Meldung von Netto-Leerverkaufspositionen an die zuständigen nationalen Behörden vorübergehend gesenkt werden, wirkt der Bedrohung für die Stabilität von Teilen oder letztlich des gesamten Finanzsystems der Union entgegen, da sie die Datenlage und die Fähigkeit der zuständigen nationalen Behörden, Bedrohungen frühzeitig entgegenzuwirken, verbessert. |
c) Verbesserung der Fähigkeit der zuständigen Behörden, die Bedrohung zu überwachen
|
(51) |
Unter normalen Marktbedingungen überwachen die zuständigen nationalen Behörden jede Bedrohung, die sich aus Leerverkäufen und dem Aufbau von Netto-Leerverkaufspositionen ergeben kann, mittels der im Unionsrecht vorgesehenen Aufsichtsinstrumente, insbesondere mittels der Meldepflichten für Netto-Leerverkaufspositionen, die in der Verordnung (EU) Nr. 236/2012 niedergelegt sind (13). |
|
(52) |
Wegen der jetzigen Marktbedingungen ist es jedoch erforderlich, die Überwachungstätigkeiten der zuständigen nationalen Behörden und der ESMA in Bezug auf aggregierte Netto-Leerverkaufspositionen in zum Handel an geregelten Märkten zugelassenen Aktien zu verstärken. Zu diesem Zweck ist es wegen der durch die COVID-19-Krise verursachten anhaltenden Unsicherheit wichtig, dass der Aufbau von Netto-Leerverkaufsposition den zuständigen nationalen Behörden weiterhin frühzeitig gemeldet wird, bevor diese die Meldeschwelle von 0,2 % des ausgegebenen Aktienkapitals erreichen, die in Artikel 5 Absatz 2 der Verordnung (EU) Nr. 236/2012 vorgesehen ist. |
|
(53) |
Dies wird daran deutlich, dass der prozentuale Anteil der Aktien mit einer Netto-Leerverkaufsposition zwischen 0,1 % und 0,2 %, der im Zeitraum 16. März bis 11. Juni 2020 stetig gestiegen und seither stabil geblieben ist, bis zum 4. September 2020 (14) über den gesamten Beobachtungszeitraum im Durchschnitt 13 % betragen hat. Daraus ist zu schließen, dass der prozentuale Anteil der Netto-Leerverkaufspositionen zwischen 0,1 % und 0,2 %, die wegen der von der ESMA angeordneten niedrigeren Meldeschwelle gemeldet werden mussten, weiterhin einen relevanten Teil der Gesamtmenge der Netto-Leerverkaufsposition ausmacht. |
|
(54) |
Durch die verlängerte Maßnahme der ESMA wird somit gewährleistet, dass die zuständigen nationalen Behörden weiterhin besser in der Lage sein werden, erkannten Bedrohungen frühzeitiger entgegenzuwirken, denn die Maßnahme ermöglicht es ihnen wie auch der ESMA, Gefahren für die ordnungsgemäße Funktionsweise der Märkte und die Finanzstabilität rechtzeitig entgegenzuwirken, falls sich Anzeichen für eine angespannte Marktlage zeigen sollten. |
5. DIESE MASSNAHMEN LASSEN KEINE GEFAHR EINER AUFSICHTSARBITRAGE ENTSTEHEN (ARTIKEL 28 ABSATZ 3 BUCHSTABE b DER VERORDNUNG (EU) Nr. 236/2012)
|
(55) |
Wenn die ESMA eine Maßnahme nach Artikel 28 der Verordnung (EU) Nr. 236/2012 ergreift oder verlängert, sollte sie berücksichtigen, ob durch die Maßnahme die Gefahr der Aufsichtsarbitrage entsteht. |
|
(56) |
Da die verlängerte Maßnahme der ESMA die Meldepflichten der Marktteilnehmer in Bezug auf alle Aktien betrifft, die zum Handel an geregelten Märkten in der Union zugelassen sind, schafft sie für alle zuständigen nationalen Behörden eine einheitliche Meldeschwelle und gewährleistet somit für die Marktteilnehmer innerhalb und außerhalb der Union gleiche Wettbewerbsbedingungen für den Handel mit den besagten Aktien. |
6. DIE MASSNAHME DER ESMA BEEINTRÄCHTIGT NICHT UNVERHÄLTNISMÄSSIG DIE EFFIZIENZ DER FINANZMÄRKTE, ETWA DURCH VERRINGERUNG DER LIQUIDITÄT DIESER MÄRKTE ODER SCHAFFUNG VON UNSICHERHEIT FÜR DIE MARKTTEILNEHMER (ARTIKEL 28 ABSATZ 3 BUCHSTABE c DER VERORDNUNG (EU) Nr. 236/2012)
|
(57) |
Die ESMA muss beurteilen, ob die Maßnahme nachteilige Auswirkungen hat, die im Vergleich zu ihren Vorteilen unverhältnismäßig wären. |
|
(58) |
Die ESMA erachtet es für geboten, dass die zuständigen nationalen Behörden die Entwicklung der Netto-Leerverkaufspositionen genau überwachen, bevor einschneidendere Maßnahmen in Erwägung gezogen werden. Die ESMA weist darauf hin, dass die gewöhnlichen Meldeschwellen (0,2 % des ausgegebenen Aktienkapitals) unter den nach wie vor außergewöhnlichen Marktbedingungen möglicherweise nicht ausreichen, Trends und eintretende Bedrohungen rechtzeitig zu erkennen. |
|
(59) |
Die Einführung der strengeren Meldepflicht mag zwar Mehrbelastungen für die meldenden Unternehmen mit sich gebracht haben, doch Letztere haben ihre internen Systeme bereits der Anwendung der Beschlüsse (EU) 2020/525 und (EU) 2020/1123 angepasst, sodass diese verlängerte Maßnahme voraussichtlich keine weiteren Compliance-Kosten für die meldenden Unternehmen zur Folge haben wird. Zudem hindert sie die Marktteilnehmer nicht daran, Leerverkaufspositionen in Aktien einzugehen oder ihre Leerverkaufspositionen auszubauen. Die Effizienz des Markts wird also nicht beeinträchtigt. |
|
(60) |
Verglichen mit anderen potenziellen und noch einschneidenderen Maßnahmen dürfte sich diese verlängerte Maßnahme nicht auf die dem Markt zur Verfügung stehende Liquidität auswirken, da die strengere Meldepflicht für eine begrenzte Anzahl von Marktteilnehmern diese wohl nicht veranlassen wird, ihre Handelsstrategien und damit ihre Marktbeteiligung zu ändern. Darüber hinaus ist für Market-Making-Tätigkeiten und Stabilisierungsprogramme eine Ausnahme vorgesehen, um zu vermeiden, dass für Unternehmen, die in Bezug auf die Bereitstellung von Liquidität und die Verringerung der Volatilität eine wichtige, in der aktuellen Situation besonders relevante Leistung anbieten, eine Mehrbelastung entsteht. |
|
(61) |
Was den Anwendungsbereich der verlängerten Maßnahme angeht, ist die ESMA der Ansicht, dass das angestrebte Ergebnis verfehlt werden könnte, wenn der Anwendungsbereich auf einen oder mehrere Sektoren oder auf eine Teilmenge von Emittenten beschränkt würde. Das Ausmaß des nach dem Ausbruch der COVID-19-Pandemie verzeichneten Kursverfalls, die große Bandbreite der betroffenen Aktien (und Sektoren) und die enge Verflechtung der Volkswirtschaften und Handelsplätze der EU lassen vermuten, dass eine unionsweite Maßnahme wahrscheinlich besser als sektorale Maßnahmen geeignet sein wird, um den zuständigen nationalen Behörden frühzeitig Marktinformationen zu liefern. |
|
(62) |
Da mit der Maßnahme keine neuen regulatorischen Auflagen eingeführt werden, sondern lediglich die relevante Schwelle für die normale, seit 2012 geltende Meldepflicht gesenkt wird, schafft sie keine Unsicherheit für die Marktteilnehmer. Außerdem betont die ESMA, dass mit der Beschränkung der verlängerten Maßnahme auf die Meldung von Aktien, die zum Handel an einem geregelten Markt in der Union zugelassen sind, genau die Positionen erfasst werden, bei denen zusätzliche Meldungen besonders relevant sein dürften. |
|
(63) |
Aus diesem Grund ist die ESMA der Ansicht, dass eine in dieser Weise erhöhte Transparenzverpflichtung keine unverhältnismäßige Beeinträchtigung der Effizienz der Finanzmärkte oder der Anleger und auch keine Unsicherheit in den Finanzmärkten bewirken dürfte. |
|
(64) |
Angesichts der derzeit verfügbaren Informationen und des nach wie vor insgesamt wegen der COVID-19-Pandemie unsicheren Ausblicks, hält die ESMA eine Verlängerung der Maßnahme um drei Monate für angemessen. Die ESMA beabsichtigt, zur regulären Meldepflicht zurückzukehren, sobald sich die Lage bessert, kann aber zugleich für den Fall, dass sich die Lage verschlechtert oder die Märkte weiter fragil bleiben, die Möglichkeit der Verlängerung der Maßnahme nicht ausschließen. |
|
(65) |
Auf dieser Grundlage und zum heutigen Datum hält die ESMA diesen Beschluss, die vorübergehende Maßnahme zur Verschärfung der Transparenzpflichten für Netto-Leerverkaufspositionen zu verlängern, angesichts der weiterhin widrigen Gegebenheiten für verhältnismäßig. |
7. KONSULTATION UND UNTERRICHTUNG (ARTIKEL 28 ABSÄTZE 4 UND 5 DER VERORDNUNG (EU) Nr. 236/2012)
|
(66) |
Die ESMA hat den Europäischen Ausschuss für Systemrisiken (ESRB) konsultiert. Der ESRB hat keine Einwände gegen die Verabschiedung des vorgeschlagenen Beschlusses erhoben. |
|
(67) |
Die ESMA hat den zuständigen nationalen Behörden den beabsichtigten Beschluss mitgeteilt. |
|
(68) |
Die verlängerte Maßnahme der ESMA tritt am 18. September 2020 in Kraft — |
HAT FOLGENDEN BESCHLUSS ERLASSEN:
Artikel 1
Begriffsbestimmung
Für die Zwecke dieses Beschlusses bezeichnet der Ausdruck „geregelter Markt“ einen geregelten Markt im Sinne von Artikel 4 Absatz 1 Ziffer 21 der Richtlinie 2014/65/EU des Europäischen Parlaments und des Rates (15).
Artikel 2
Vorübergehende zusätzliche Transparenzpflichten
(1) Natürliche oder juristische Personen, die eine Netto-Leerverkaufsposition in Bezug auf das ausgegebene Aktienkapital eines Unternehmens halten, dessen Aktien zum Handel an einem geregelten Markt zugelassen sind, müssen gemäß den Artikeln 5 und 9 der Verordnung (EU) Nr. 236/2012 der jeweils zuständigen Behörde melden, wenn die Position eine in Absatz 2 des vorliegenden Artikels genannte Meldeschwelle erreicht oder unterschreitet.
(2) Eine Meldeschwelle liegt bei 0,1 % und danach jeweils in Intervallen von 0,1 % des ausgegebenen Aktienkapitals des betreffenden Unternehmens.
Artikel 3
Ausnahmen
(1) Gemäß Artikel 16 der Verordnung (EU) Nr. 236/2012 gelten die in Artikel 2 genannten vorübergehenden zusätzlichen Transparenzpflichten nicht für Aktien, die zwar zum Handel an einem geregelten Markt zugelassen sind, deren Haupthandelsplatz sich aber in einem Drittland befindet.
(2) Gemäß Artikel 17 der Verordnung (EU) Nr. 236/2012 gelten die in Artikel 2 genannten vorübergehenden zusätzlichen Transparenzpflichten nicht für Geschäfte, die aufgrund von Market-Making-Tätigkeiten getätigt werden.
(3) Die in Artikel 2 genannten vorübergehenden zusätzlichen Transparenzpflichten gelten nicht für eine Netto-Leerverkaufsposition im Zusammenhang mit Stabilisierungsmaßnahmen gemäß Artikel 5 der Verordnung (EU) Nr. 596/2014 des Europäischen Parlaments und des Rates (16).
Artikel 4
Inkrafttreten und Geltungsbereich
Dieser Beschluss tritt am 18. September 2020 in Kraft. Er gilt ab dem Tag seines Inkrafttretens für einen Zeitraum von drei Monaten.
Geschehen zu Paris am 16. September 2020.
Für den Rat der Aufseher
Steven MAIJOOR
Vorsitzender
(1) ABl. L 331 vom 15.12.2010, S. 84.
(2) ABl. L 86 vom 24.3.2012, S. 1.
(3) ABl. L 274 vom 9.10.2012, S. 1.
(4) ABl. L 116 vom 15.4.2020, S. 5.
(5) ABl. L 245 vom 30.7.2020, S. 17.
(6) Der VSTOXX erfasst die implizite Volatilität auf Grundlage der Euro Stoxx 50 Optionspreise.
(7) Der VIX Index wird in Echtzeit auf Grundlage des Mittelwerts der Bid/Ask-Preise der Optionen auf den S&P 500 Index berechnet.
(8) Bei den Sektoren außerhalb des Finanzbereichs sind die folgenden Teilsektoren ausgenommen: Banken, Versicherungen und Finanzdienstleistungen.
(9) Wegen eines technischen Problems liegen Dänemarks Berichte über die täglichen Netto-Leerverkaufspositionen für den Zeitraum 31. August bis 4. September nicht vor.
(10) https://www.ecb.europa.eu/pub/financial-stability/fsr/html/ecb.fsr201911~facad0251f.en.html
(11) TRV-Bericht, Executive Summary, Seite 4.
(12) In Italien wurde die Maßnahme am 18. Mai aufgehoben.
(13) Siehe Artikel 5 der Verordnung (EU) Nr. 236/2012.
(14) Wegen eines technischen Problems liegen Dänemarks Berichte über die täglichen Netto-Leerverkaufspositionen für den Zeitraum 31. August bis 4. September nicht vor.
(15) Richtlinie 2014/65/EU des Europäischen Parlaments und des Rates vom 15. Mai 2014 über Märkte für Finanzinstrumente sowie zur Änderung der Richtlinien 2002/92/EG und 2011/61/EU (ABl. L 173 vom 12.6.2014, S. 349).
(16) Verordnung (EU) Nr. 596/2014 des Europäischen Parlaments und des Rates vom 16. April 2014 über Marktmissbrauch (Marktmissbrauchsverordnung) und zur Aufhebung der Richtlinie 2003/6/EG des Europäischen Parlaments und des Rates und der Richtlinien 2003/124/EG, 2003/125/EG und 2004/72/EG der Kommission (ABl. L 173 vom 12.6.2014, S. 1).
ANHANG
In diesem Anhang bezieht sich „ESMA-Beschluss“ auf den Beschluss (EU) 2020/525.
Abbildung 1
Finanzindikatoren
|
Aktienmarktentwicklung |
Veränderungen vom 20.2.2020 bis zum 3.9.2020 (in %) |
Indexstand zum 3.9.2020 |
Veränderungen vom 20.2.2020 bis zum 4.6.2020 (in %) |
Indexstand zum 4.6.2020 |
|
STOXX EUROPE 800 ex. Schweiz |
– 17 |
116 |
– 16 |
117 |
|
EURO STOXX INDEX |
– 13 |
362 |
– 13 |
364 |
|
EURO STOXX 50 |
– 14 |
3 304 |
– 13 |
3 323 |
|
US S&P 500 |
2 |
3 451 |
– 8 |
3 112 |
|
JP Nikkei |
0 |
23 466 |
– 3 |
22 864 |
|
Global |
– 1 |
228 |
– 9 |
211 |
|
Europäische Banken |
– 37 |
93 |
– 30 |
104 |
|
IT Finanzwerte |
– 30 |
27 |
– 29 |
28 |
|
ES Finanzwerte |
– 48 |
34 |
– 35 |
42 |
|
DE Finanzwerte |
– 13 |
123 |
– 11 |
126 |
|
FR Finanzwerte |
– 34 |
118 |
– 28 |
130 |
|
Volatilität |
Veränderungen vom 20.2.2020 bis zum 3.9.2020 (in %) |
Indexstand zum 3.9.2020 |
Veränderungen vom 20.2.2020 bis zum 4.6.2020 (in %) |
Indexstand zum 4.6.2020 |
|
VSTOXX |
15 |
29 |
13 |
28 |
|
VIX |
18 |
33 |
9 |
25 |
|
Credit Default Swap (Kreditausfallversicherung) |
Veränderungen in bp vom 20.2.2020 bis zum 3.9.2020 |
CDS-Spreads in bp zum 3.9.2020 |
Veränderungen in bp vom 20.2.2020 bis zum 4.6.2020 |
CDS-Spreads in bp zum 4.6.2020 |
|
Europa Corporate |
5 |
45 |
22 |
62 |
|
Europa High Yield |
92 |
290 |
157 |
355 |
|
Europa Finanzwerte |
15 |
59 |
29 |
73 |
|
Europa nachrangige Finanzwerte |
38 |
124 |
62 |
149 |
|
10-jähr. Staatsanleihen |
Veränderungen in bp vom 20.2.2020 bis zum 3.9.2020 |
Anleiherenditen in % zum 3.9.2020 |
Veränderungen in bp vom 20.2.2020 bis zum 4.6.2020 |
Anleiherenditen in % zum 4.6.2020 |
|
DE10Y |
– 5 |
– 0,49 |
15 |
– 0,29 |
|
ES10Y |
9 |
0,33 |
32 |
0,55 |
|
FR10Y |
2 |
– 0,19 |
23 |
0,01 |
|
IT10Y |
15 |
1,06 |
51 |
1,42 |
|
US10Y |
– 90 |
0,62 |
– 67 |
0,86 |
|
GB10Y |
– 34 |
0,24 |
– 24 |
0,34 |
|
JP10Y |
8 |
0,04 |
9 |
0,05 |
|
Anmerkung: Aktienmarktentwicklung in %, sonstige Änderungen in absoluten Zahlen. Quellen: Refinitiv EIKON, ESMA. |
||||

Anmerkung: Implizite Volatilität von EURO STOXX 50 (VSTOXX) und S&P 500 (VIX), in %.
Quellen: Refinitiv Datastream, ESMA.

Anmerkung: Aktienkurse. 20.2.2020 = 100.
Quellen: Refinitiv Datastream, ESMA.

Anmerkung: Aktienkurse. 20.2.2020 = 100.
Quellen: Refinitiv Datastream, ESMA.
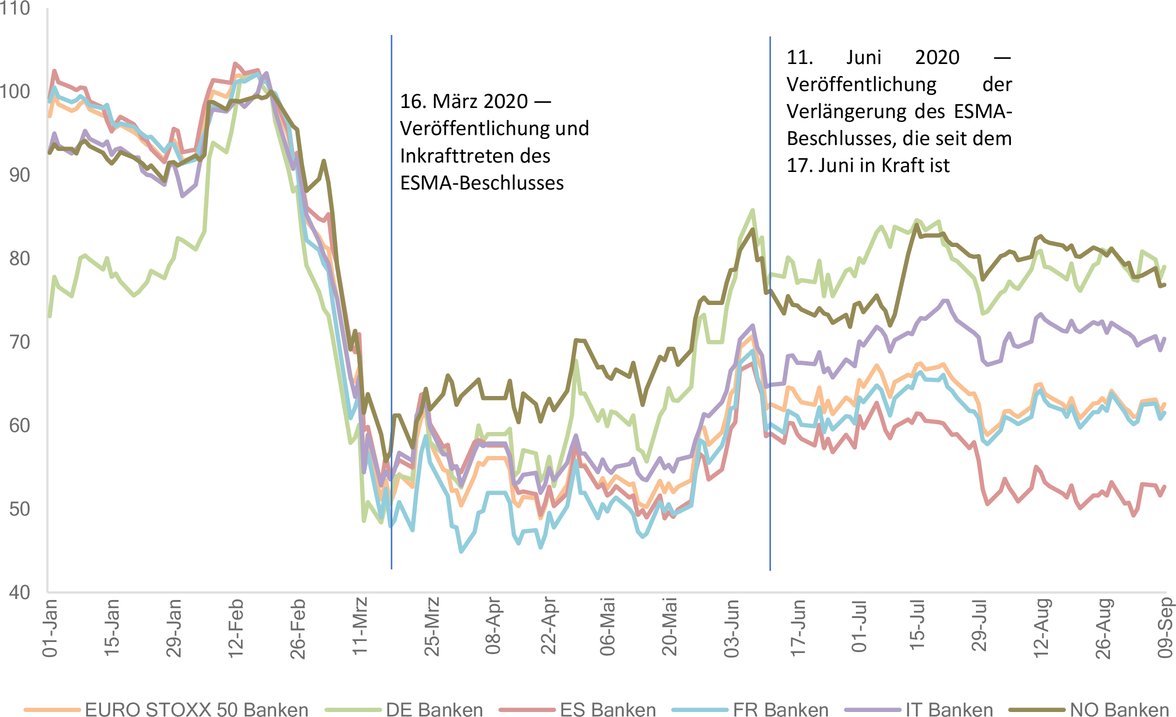
Anmerkung: Aktienkurse. 20.2.2020 = 100.
Quellen: Refinitiv Datastream, ESMA.
Abbildung 4
EU-CDS-Spread-Indizes
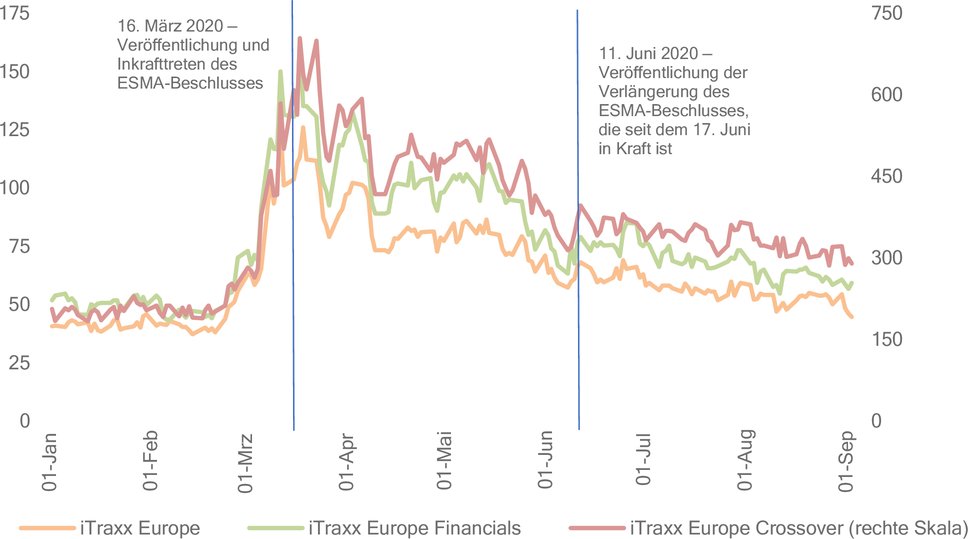
Anmerkung: CDS-Spreads auf europäische IG Corporates (iTraxx Europe), European High Yield Corporates (iTraxx Europe Crossover) und europäische Finanzwerte, in bp.
Quellen: Refinitiv EIKON; ESMA.
Abbildung 5
Europäische Aktienindexentwicklung, nach Ländern
|
|
Prozentuale Veränderung vom 20.2.2020 bis 3.9.2020 |
Prozentuale Veränderung vom 20.2.2020 bis 4.6.2020 |
|
STOXX EUROPE 800 ex. Schweiz |
– 16,67 |
– 15,78 |
|
EURO STOXX INDEX |
– 13,22 |
– 12,72 |
|
EURO STOXX 50 |
– 13,57 |
– 13,07 |
|
AT |
– 30,21 |
– 23,30 |
|
BE |
– 19,22 |
– 14,86 |
|
BG |
– 20,67 |
– 15,69 |
|
CY |
– 39,52 |
– 34,73 |
|
CZ |
– 17,81 |
– 13,94 |
|
DE |
– 4,44 |
– 7,32 |
|
DK |
4,24 |
– 2,48 |
|
EE |
– 13,55 |
– 13,16 |
|
ES |
– 29,45 |
– 21,88 |
|
FI |
– 5,35 |
– 8,66 |
|
FR |
– 17,37 |
– 15,91 |
|
GB |
– 21,32 |
– 13,93 |
|
GR |
– 29,24 |
– 26,64 |
|
HR |
– 19,61 |
– 17,16 |
|
HU |
– 24,05 |
– 17,83 |
|
IE |
– 13,00 |
– 12,90 |
|
IS |
– 1,50 |
– 4,44 |
|
IT |
– 22,04 |
– 20,01 |
|
LT |
5,06 |
– 1,98 |
|
LU |
– 25,92 |
– 21,60 |
|
LV |
5,53 |
– 1,81 |
|
MT |
– 20,80 |
– 12,92 |
|
NL |
– 11,66 |
– 9,17 |
|
NO |
– 11,80 |
– 10,22 |
|
PL |
– 15,75 |
– 13,47 |
|
PT |
– 20,09 |
– 13,64 |
|
RO |
– 10,73 |
– 11,45 |
|
SE |
– 7,28 |
– 9,47 |
|
SI |
– 13,01 |
– 10,83 |
|
SK |
– 7,05 |
0,07 |
|
Quellen: Refinitiv EIKON; ESMA. |
||
Abbildung 6
Netto-Leerverkaufsposition zwischen 0,1 % und 0,2 % über den Zeitraum 16. März bis 4. September 2020 (1)

LEITLINIEN
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/77 |
LEITLINIE (EU) 2020/1690 DER EUROPÄISCHEN ZENTRALBANK
vom 25. September 2020
zur Änderung der Leitlinie (EU) 2015/510 über die Umsetzung des geldpolitischen Handlungsrahmens des Eurosystems
(EZB/2020/45)
DER EZB-RAT —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union, insbesondere auf Artikel 127 Absatz 2 erster Gedankenstrich,
gestützt auf die Satzung des Europäischen Systems der Zentralbanken und der Europäischen Zentralbank, insbesondere auf Artikel 3.1 erster Gedankenstrich, Artikel 9.2, Artikel 12.1, Artikel 14.3, Artikel 18.2 und Artikel 20 Absatz 1,
in Erwägung nachstehender Gründe:
|
(1) |
Eine einheitliche Geldpolitik erfordert die Definition der Instrumente und Verfahren, die vom Eurosystem einzusetzen sind, damit eine solche Geldpolitik in den Mitgliedstaaten, deren Währung der Euro ist, einheitlich durchgeführt werden kann. |
|
(2) |
Die Leitlinie (EU) 2015/510 der Europäischen Zentralbank (EZB/2014/60) (1) sollte geändert werden, um notwendige technische und redaktionelle Anpassungen im Zusammenhang mit bestimmten Aspekten geldpolitischer Geschäfte zu berücksichtigen. |
|
(3) |
Zur Verringerung der Komplexität des Sicherheitenrahmens des Eurosystems insgesamt, der Risiken, denen das Eurosystem ausgesetzt ist, und der operationalen Belastung in Bezug auf die Beurteilung der Notenbankfähigkeit sollten nicht gesetzlich geregelte gedeckte Schuldverschreibungen (d. h. vertraglich geregelte gedeckte Schuldverschreibungen) nicht mehr als Sicherheiten des Eurosystems akzeptiert werden. Die Begriffsbestimmungen und Vorschriften in Bezug auf gedeckte Schuldverschreibungen im Sicherheitenrahmen des Eurosystems sollten daher geändert werden, um die Art der notenbankfähigen gedeckten Schuldverschreibungen auf gesetzlich geregelte gedeckte Schuldverschreibungen und Multi-cédulas zu beschränken. |
|
(4) |
Zur Berücksichtigung des gemäß dem Beschluss (EU) 2019/1743 der Europäischen Zentralbank (EZB/2019/31) (2) seit dem 30. Oktober 2019 geltenden zweistufigen Systems für die Verzinsung von Überschussreserven sollte klargestellt werden, welcher Rechtsrahmen für die Verzinsung von Mindestreserven und Überschussreserven gilt. |
|
(5) |
Zur weiteren Verringerung der Komplexität des Sicherheitenrahmens des Eurosystems und aufgrund der begrenzten Nutzung der von nichtfinanziellen Kapitalgesellschaften ausgegebenen oder garantierten marktfähigen Schuldtitel, für die keine angemessene Bonitätsbeurteilung zur Verfügung steht, sollten diese nach einem Übergangszeitraum nicht mehr als Sicherheiten des Eurosystems akzeptiert werden. |
|
(6) |
Im Hinblick auf die jüngsten Finanzinnovationen im Bereich Nachhaltigkeit im Finanzsystem (Sustainable Finance) beabsichtigt das Eurosystem, bestimmte marktfähige Schuldtitel mit Kuponstrukturen, die an die Erfüllung vordefinierter Nachhaltigkeitsziele durch den Emittenten gekoppelt sind, zu akzeptieren. |
|
(7) |
Es sollte klargestellt werden, dass Vermögenswerte mit Kupons, die an interpolierte Referenzsätze gekoppelt sind, nur unter bestimmten Bedingungen notenbankfähig sind, und diese Bedingungen sollten festgelegt werden. |
|
(8) |
Damit Kategorien besicherter marktfähiger Sicherheiten, die als Sicherheiten für Kreditgeschäfte des Eurosystems zugelassen sind, im Ansatz einheitlich und transparent behandelt werden, sollten außer Asset-Backed Securities und gedeckte Schuldverschreibungen keine besicherten marktfähigen Sicherheiten mehr als Sicherheiten des Eurosystems akzeptiert werden. |
|
(9) |
Die Anforderungen für Daten auf Einzelkreditebene für als Sicherheiten des Eurosystems zugelassene Asset-Backed Securities sollten für diejenigen Asset-Backed Securities angepasst werden, bei denen die Daten auf Einzelkreditebene gemäß Verordnung (EU) 2017/2402 (3) des Europäischen Parlaments und des Rates gemeldet werden. |
|
(10) |
Bestimmte Vorschriften in Bezug auf die Zulässigkeit von Kreditforderungen als Sicherheiten des Eurosystems und die Meldung von Daten zu Kreditforderungen sollten geändert werden, um die Verfügbarkeit von Informationen über Kreditforderungen innerhalb des Sicherheitenrahmens zu verbessern, mehr Klarheit in Bezug auf die Regeln zur Bestimmung der Zulässigkeit von Kreditforderungen als Sicherheiten zu schaffen und die Prüfverfahren für Sicherheiten dieser Art klarzustellen. |
|
(11) |
Zur Sicherstellung einer größeren Transparenz, Konsistenz und Rechtssicherheit sollten die allgemeinen Zulassungskriterien für externe Ratingagenturen (external credit assessment institutions — ECAIs) im Rahmenwerk für Bonitätsbeurteilungen im Eurosystem (Eurosystem credit assessment frame work — ECAF) klargestellt werden. |
|
(12) |
Die Regeln in Bezug auf die Verwendung unbesicherter Schuldtitel, die von einem Geschäftspartner oder mit diesem eng verbundenen Stellen begeben werden, sollten vereinfacht werden. |
|
(13) |
Zur Erhöhung der Transparenz des Geschäftspartner-Rahmenwerks des Eurosystems sollten die geltenden Fristen für Geschäftspartner, welche die Mindestanforderungen an das Eigenkapital nicht erfüllen, klargestellt werden. |
|
(14) |
Die finanzielle Sanktion für Verstöße im Zusammenhang mit der Nutzung notenbankfähiger Sicherheiten als Sicherheiten des Eurosystems sollte angepasst werden, um den Geschäftspartnern Anreize zur aktiven Meldung solcher Verstöße zu geben. |
|
(15) |
Die Leitlinie (EU) 2015/510 (EZB/2014/60) sollte daher entsprechend geändert werden — |
HAT FOLGENDE LEITLINIE ERLASSEN:
Artikel 1
Änderungen
Die Leitlinie (EU) 2015/510 (EZB/2014/60) wird wie folgt geändert:
|
1. |
Artikel 2 wird wie folgt geändert:
|
|
2. |
Artikel 54 wird wie folgt geändert:
|
|
3. |
In Artikel 61 Absatz 1 wird folgender Satz angefügt: „Diese Sicherheiten sind nur bis zu dem Datum notenbankfähig, an dem das Sicherheitenmanagementsystem des Eurosystems (Eurosystem Collateral Management System — ECMS) in Betrieb geht (‚Tag der Inbetriebnahme‘).“ |
|
4. |
Artikel 63 Absatz 1 wird wie folgt geändert:
|
|
5. |
Der folgende Artikel 64a wird eingefügt: „Artikel 64a Marktfähige Sicherheiten außer Asset-Backed Securities und gedeckte Schuldverschreibungen 1. Um notenbankfähig zu sein, müssen marktfähige Sicherheiten — außer Asset-Backed Securities, gesetzlich geregelte gedeckte Schuldverschreibungen und Multi-cédulas — unbesicherte Verpflichtungen sowohl des Emittenten als auch des Garanten sein. Bei marktfähigen Sicherheiten mit mehr als einem Emittenten oder mit mehr als einem Garanten gilt die Anforderung dieses Absatzes für jeden Emittenten und jeden Garanten. 2. Marktfähige Sicherheiten, die besichert sind und vor dem 1. Januar 2021 notenbankfähig waren, aber die Anforderungen an die Notenbankfähigkeit gemäß diesem Artikel nicht erfüllen, bleiben bis zum 1. Januar 2026 notenbankfähig, wenn sie alle anderen Kriterien für die Notenbankfähigkeit marktfähiger Sicherheiten erfüllen. Abweichend von Satz 1 dieses Absatzes sind gedeckte Schuldverschreibungen, die weder gesetzlich geregelte gedeckte Schuldverschreibungen noch Multi-cédulas sind, ab dem 1. Januar 2021 nicht mehr notenbankfähig.“ |
|
6. |
Artikel 78 wird wie folgt geändert:
|
|
7. |
Artikel 80 erhält folgende Fassung: „Artikel 80 Zulassungskriterien für gedeckte Schuldverschreibungen, die durch Asset-Backed Securities besichert sind 1. Unbeschadet der Notenbankfähigkeit gesetzlich geregelter gedeckter Schuldverschreibungen gemäß Artikel 64a gilt für die Notenbankfähigkeit von nach dem Recht eines EWR-Mitgliedstaats gesetzlich geregelten gedeckten Schuldverschreibungen, die durch Asset-Backed Securities besichert sind, dass der Deckungspool dieser Schuldverschreibungen (im Sinne der Absätze 1 bis 4 „der Deckungspool“) nur Asset-Backed Securities enthalten darf, die sämtliche der nachstehenden Kriterien erfüllen.
2. Vorbehaltlich Absatz 4 überprüfen die NZBen anhand folgender Maßnahmen, dass im Deckungspool nur Asset-Backed Securities enthalten sind, welche die Anforderungen von Absatz 1 erfüllen.
3. Kommt der Emittent einer konkreten Anfrage nicht nach oder erachtet das Eurosystem die Bescheinigung inhaltlich für unrichtig oder unzulänglich, sodass nicht überprüft werden kann, ob der Deckungspool den Kriterien von Absatz 1 genügt, lehnt das Eurosystem die Hereinnahme der nach dem Recht eines EWR-Mitgliedstaats gesetzlich geregelten gedeckten Schuldverschreibungen als notenbankfähige Sicherheiten ab oder setzt ihre Notenbankfähigkeit aus. 4. Ist nach den einschlägigen Rechtsvorschriften oder nach dem Prospekt die Hereinnahme von Asset-Backed Securities, die den Anforderungen von Absatz 1 nicht genügen, als Vermögenswerte des Deckungspools ausgeschlossen, ist eine Überprüfung nach Absatz 2 nicht erforderlich. 5. Die enge Verbindung im Sinne von Absatz 1 Buchstabe b ist zu dem Zeitpunkt festzustellen, zu dem die Anteile der Seniortranchen der Asset-Backed Securities in den Deckungspool der nach dem Recht eines EWR-Mitgliedstaats gesetzlich geregelten gedeckten Schuldverschreibung übertragen werden. 6. Der Deckungspool der nach dem Recht eines nicht dem EWR angehörenden G-10-Landes gesetzlich geregelten gedeckten Schuldverschreibungen darf keine Asset-Backed Securities enthalten.“ |
|
8. |
Artikel 87 wird wie folgt geändert:
|
|
9. |
Artikel 90 wird wie folgt geändert:
|
|
10. |
Artikel 100 erhält folgende Fassung: „Artikel 100 Prüfung der Verfahren und Systeme zur Einreichung von Kreditforderungen Die NZBen, Aufsichtsbehörden oder externen Rechnungsprüfer führen vor der ersten Nutzung von Kreditforderungen als Sicherheiten durch den Geschäftspartner eine Prüfung zur Bestätigung der Angemessenheit der Verfahren und Systeme durch, die der Geschäftspartner zur Bereitstellung von Informationen über die Kreditforderungen beim Eurosystem verwendet. Danach ist die Prüfung der Verfahren und Systeme mindestens alle fünf Jahre durchzuführen. Im Fall von wesentlichen Änderungen dieser Verfahren oder Systeme kann eine erneute Prüfung durchgeführt werden.“ |
|
11. |
In Artikel 101 wird nach Buchstabe a der folgende neue Buchstabe aa eingefügt:
(*5) Verordnung (EU) 2016/867 der Europäischen Zentralbank vom 18. Mai 2016 über die Erhebung granularer Kreditdaten und Kreditrisikodaten (EZB/2016/13) (ABl. L 144 vom 1.6.2016, S. 44).“" |
|
12. |
Artikel 102 Satz 2 erhält folgende Fassung: (betrifft nicht die deutsche Fassung) |
|
13. |
Artikel 120 Absätze 2 und 2a erhalten folgende Fassung: „2. Im Anschluss an das in Anhang IXc beschriebene Antragsverfahren behält sich das Eurosystem das Recht vor, zu entscheiden, ob ein ECAF-Zulassungsverfahren auf Anfrage einer Ratingagentur zu eröffnen ist. Bei seiner Entscheidung hat das Eurosystem unter anderem zu berücksichtigen, ob die Ratingagentur entsprechende Abdeckungsgrade für die effiziente Umsetzung des ECAF im Einklang mit den Anforderungen von Anhang IXa aufweist. 2a. Nach Einleitung eines ECAF-Zulassungsverfahrens untersucht das Eurosystem sämtliche zusätzliche als relevant erachtete Informationen, um die effiziente Umsetzung des ECAF sicherzustellen, einschließlich der Fähigkeit der ECAIs, i) Kriterien und Regeln des ECAF-Leistungüberwachungsverfahrens im Einklang mit den Vorgaben in Anhang IX und den spezifischen Kriterien in Anhang IXb (soweit maßgeblich) zu erfüllen und ii) die in Anhang IXc festgelegten Zulassungskriterien einzuhalten. Das Eurosystem behält sich das Recht vor, über die Zulassung einer ECAI für ECAF-Zwecke auf der Grundlage der vorgelegten Informationen und seiner eigenen sorgfältigen Prüfung und Beurteilung zu entscheiden.“ |
|
14. |
Artikel 138 wird wie folgt geändert:
|
|
15. |
Artikel 139 wird wie folgt geändert:
|
|
16. |
Artikel 148 Absatz 2 erhält folgende Fassung: „2. Geschäftspartner können notenbankfähige Sicherheiten, die keine Termineinlagen sind, grenzüberschreitend wie folgt als Sicherheit nutzen:
|
|
17. |
Artikel 155 erhält folgende Fassung: „Artikel 155 Finanzielle Sanktionen bei Verstößen gegen bestimmte operationale Regeln 1. Verstößt ein Geschäftspartner gegen eine in Artikel 154 Absatz 1 genannte Verpflichtung, verhängt das Eurosystem für jeden Verstoß eine finanzielle Sanktion. Die anzuwendende Sanktion wird gemäß Anhang VII berechnet. 2. Behebt ein Geschäftspartner einen Verstoß gegen eine in Artikel 154 Absatz 1 Buchstabe c genannte Verpflichtung und teilt der Geschäftspartner dies der NZB mit, bevor die NZB, die EZB oder ein externer Rechnungsprüfer dem Geschäftspartner den Verstoß mitteilt (‚Selbstanzeige eines Verstoßes‘), so verringert sich die entsprechende gemäß Anhang VII berechnete finanzielle Sanktion um 50 %. Die finanzielle Sanktion verringert sich auch bei Verstößen, die der Geschäftspartner der NZB mitteilt, die aber nicht von der EZB oder NZB festgestellt worden sind, sowie im Zusammenhang mit Vermögenswerten, die bereits zurückgenommen wurden. Die finanzielle Sanktion verringert sich nicht bei Vermögenswerten, die vom Anwendungsbereich eines laufenden Prüfverfahrens erfasst sind und von welchem der Geschäftspartner aufgrund einer Mitteilung der NZB, der EZB oder eines externen Rechnungsprüfers Kenntnis hat.“ |
|
18. |
Artikel 156 Absatz 4 Buchstabe a erhält folgende Fassung: (betrifft nicht die deutsche Fassung) |
|
19. |
Artikel 158 wird wie folgt geändert:
|
|
20. |
Artikel 159 Absatz 4 Buchstabe b erhält folgende Fassung:
|
|
21. |
Die Anhänge I, VIII, IXa und XII werden gemäß Anhang I dieser Leitlinie geändert. |
|
22. |
Der in Anhang II dieser Leitlinie enthaltene Text wird als neuer Anhang IXc angefügt. |
Artikel 2
Wirksamwerden und Umsetzung
1. Diese Leitlinie wird am Tag ihrer Bekanntgabe an die nationalen Zentralbanken der Mitgliedstaaten, deren Währung der Euro ist, wirksam.
2. Die nationalen Zentralbanken der Mitgliedstaaten, deren Währung der Euro ist, treffen die erforderlichen Maßnahmen zur Erfüllung dieser Leitlinie, und wenden diese ab dem 1. Januar 2021 an. Sie teilen der Europäischen Zentralbank die Rechtstexte und Umsetzungsmaßnahmen in Bezug auf diese Maßnahmen spätestens bis zum 6. November 2020 mit.
Artikel 3
Adressaten
Diese Leitlinie ist an alle Zentralbanken des Eurosystems gerichtet.
Geschehen zu Frankfurt am Main am 25. September 2020.
Die Präsidentin der EZB
Für den EZB-Rat
Christine LAGARDE
(1) Leitlinie (EU) 2015/510 der Europäischen Zentralbank vom 19. Dezember 2014 über die Umsetzung des geldpolitischen Handlungsrahmens des Eurosystems (Leitlinie allgemeine Dokumentation) (EZB/2014/60) (ABl. L 91 vom 2.4.2015, S. 3).
(2) Beschluss (EU) 2019/1743 der Europäischen Zentralbank vom 15. Oktober 2019 über die Verzinsung von Überschussreserven und bestimmten Einlagen (EZB/2019/31) (ABl. L 267 vom 21.10.2019, S. 12).
(3) Verordnung (EU) 2017/2402 des Europäischen Parlaments und des Rates vom 12. Dezember 2017 zur Festlegung eines allgemeinen Rahmens für Verbriefungen und zur Schaffung eines spezifischen Rahmens für einfache, transparente und standardisierte Verbriefung und zur Änderung der Richtlinien 2009/65/EG, 2009/138/EG, 2011/61/EU und der Verordnungen (EG) Nr. 1060/2009 und (EU) Nr. 648/2012 (ABl. L 347 vom 28.12.2017, S. 35).
ANHANG I
Die Anhänge I, VIII, IXa und XII der Leitlinie (EU) 2015/510 (EZB/2014/60) werden wie folgt geändert:
|
1. |
In Anhang I erhält der zweite Satz von Absatz 5 folgende Fassung: „Hierzu zählen u. a. Institute, die Sanierungsmaßnahmen unterworfen sind, sowie Institute, die dem Einfrieren ihres Vermögens bzw. sonstigen von der Union gemäß Artikel 75 des Vertrags oder einem Mitgliedstaat verhängten Maßnahmen, durch die die Verfügung über das Vermögen des Instituts eingeschränkt wird, oder einer Entscheidung des Eurosystems unterliegen, durch die der Zugang des Instituts zu den Offenmarktgeschäften oder zu den ständigen Fazilitäten des Eurosystems ausgesetzt oder ausgeschlossen wird.“ |
|
2. |
Anhang VIII wird wie folgt geändert:
|
|
3. |
Anhang IXa Abschnitt 2 Absatz 1 erhält folgende Fassung:
|
|
4. |
In Anhang XII wird der Begriff „OGAW-konformer Jumbo-Pfandbrief“ durch den Begriff „Jumbo-Pfandbrief“ ersetzt. |
ANHANG II
Der folgende neue Anhang IXc wird angefügt:
„ANHANG IXc
ZULASSUNGSKRITERIEN UND ANTRAGSVERFAHREN FÜR EXTERNE RATINGAGENTUREN (ECAI)
Dieser Anhang legt im Einzelnen die Zulassungskriterien für externe Ratingagenturen (external credit assessment institutions — ECAI) fest sowie das Verfahren, mit dem eine Ratingagentur einen Antrag stellen kann, um als ECAI für die Zwecke des Rahmenwerks für Bonitätsbeurteilungen im Eurosystem (Eurosystem credit assessment framework — ECAF) gemäß Artikel 120 dieser Leitlinie zugelassen zu werden.
I. ANTRAGSVERFAHREN FÜR DIE ZULASSUNG ALS ECAI IM RAHMEN DES ECAF
|
1. |
Ein Antrag einer externen Ratingagentur auf Zulassung als ECAI im Rahmen des ECAF ist bei der Direktion Risikomanagement der EZB (DRMSecretariat@ecb.europa.eu) zu stellen. Der Antrag hat geeignete Gründe und Begleitdokumente gemäß Abschnitt II zu enthalten, die zeigen, dass der Antragsteller die in dieser Leitlinie aufgeführten Anforderungen an ECAI erfüllt. Antrag, Gründe und Begleitdokumente sind in schriftlicher Form in englischer Sprache, unter Verwendung der jeweils einschlägigen Formulare, in elektronischer Form vorzulegen. |
|
2. |
Als erste Stufe des Antragsverfahrens hat die Ratingagentur die Einhaltung der jeweiligen, in Artikel 120 und Anhang IXa dieser Leitlinie sowie im vorliegenden Anhang aufgeführten Abdeckungserfordernisse nachzuweisen. Wurde ein Antrag der Ratingagentur auf ECAF-Zulassung bereits vom Eurosystem abgelehnt, hat die Ratingagentur außerdem darzulegen, wie sie ihre vorherige Nichteinhaltung behoben hat. Die einzelnen Schritte dieser ersten Stufe sind wie folgt:
|
|
3. |
Kommt die EZB zu dem Schluss, dass die Ratingagentur die jeweiligen Abdeckungserfordernisse einhält und gegebenenfalls ihre vorherige Nichteinhaltung behoben hat, und wenn die die EZB beschließt, das ECAF-Zulassungsverfahrens zu eröffnen, kann die Ratingagentur mit der zweiten Stufe des Antragsverfahrens fortfahren. Als zweite Stufe hat die Ratingagentur die Einhaltung aller sonstigen jeweiligen, in dieser Leitlinie aufgeführten Anforderungen nachzuweisen. Die einzelnen Schritte der zweiten Stufe sind wie folgt:
|
II. FÜR DEN ANTRAG AUF ECAF-ZULASSUNG UND DESSEN VOLLSTÄNDIGKEIT ERFORDERLICHE INFORMATIONEN
|
1. |
Im Rahmen der ersten Stufe des Antragsverfahrens hat eine Ratingagentur die folgenden Informationen zur Verfügung zu stellen:
|
|
2. |
Die EZB kann ergänzende Informationen anfordern, beispielsweise als Nachweis der Stabilität der Abdeckung einer Ratingagentur im Zeitverlauf, der Verfahren für die Ratingvergabe der Ratingagentur sowie der Qualität der Ratings der Ratingagentur im jeweiligen Abdeckungszeitraum. |
|
3. |
Im Rahmen der zweiten Stufe des Antragsverfahrens hat eine Ratingagentur die folgende Dokumentation und Informationen zur Verfügung zu stellen:
|
|
4. |
Die EZB kann von der Ratingagentur relevante ergänzende Informationen anfordern, beispielsweise über von der Ratingagentur abgegebene Asset-, Emittenten- und Garantenratings, die beispielsweise aufgrund geografischer Beschränkungen für ECAF-Zwecke nicht zugelassen sind. |
III. ECAF-ZULASSUNGSKRITERIEN
|
1. |
Voraussetzung für eine ECAF-Zulassung ist, dass die Ratingagentur die jeweiligen Anforderungen dieser Leitlinie erfüllt. Hierzu gehören die Gewährleistung entsprechender Abdeckungsgrade für die effiziente Umsetzung des ECAF, die Erfüllung operationaler Kriterien, die Bereitstellung von Informationen über ECAI-Bonitätsbeurteilungen und für die Zwecke des Leistungsüberwachungsverfahrens sowie die Fähigkeit, die Kriterien und Regeln des ECAF-Leistungüberwachungsverfahrens zu erfüllen. |
|
2. |
Im Hinblick auf die Anforderung, entsprechende Abdeckungsgrade aufzuweisen, gilt Folgendes:
|
|
3. |
Im Hinblick auf die Verfügbarkeit von Informationen über ECAI-Bonitätsbeurteilungen und für die Zwecke des Leistungsüberwachungsverfahrens gilt Folgendes:
|
|
4. |
Im Hinblick auf die Fähigkeit einer Ratingagentur, die Kriterien und Regeln des ECAF-Leistungsüberwachungsverfahrens zu erfüllen, müssen die Durchführung der Ratings der Ratingagentur sowie deren Zuweisung von Ausfällen im Zeitverlauf konsistent sein, um a) eine angemessene Einordnung der durch die Bonitätsbeurteilung gewonnenen Werte in die harmonisierte Ratingskala des Eurosystems und b) die Vergleichbarkeit der Ergebnisse der Bonitätsbeurteilungen der Ratingagentur über die verschiedenen Systeme und Quellen des ECAF hinweg zu gewährleisten. Die von der Ratingagentur herangezogenen Ratingübergangstabellen und Ausfallstatistiken sollten mit den gemäß den eigenen Ratingskalas der Ratingagentur erwarteten Werten übereinstimmen, da gemäß Anhang IX dieser Leitlinie Abweichungen der beobachteten Ausfallraten von den zugewiesenen Ausfallraten die Qualität der Bonitätsbeurteilungen in Frage stellen können, was wiederum eine effiziente Umsetzung des ECAF verhindern würde. |
|
5. |
Im Hinblick auf die operationalen Kriterien gilt Folgendes:
|
|
6. |
Sämtliche ECAF-Zulassungskriterien müssen erfüllt werden, damit eine Ratingagentur für die Zwecke des ECAF zugelassen werden kann. Da der Antrag auf ECAF-Zulassung eine technisch sehr anspruchsvolle qualitative und quantitative Bewertung erfordert, kann das Eurosystem erforderlichenfalls weitere relevante Faktoren im Zusammenhang mit den Anforderungen dieser Leitlinie an das ECAF bewerten. |
IV. ECAF-ZULASSUNGSKRITERIEN FÜR EXTERNE RATINGAGENTUREN UND DEREN EINHALTUNG IM ZEITVERLAUF
|
1. |
Ratingagenturen haben die Zulassungskriterien für Ratingagenturen sowohl zum Zeitpunkt ihres Antrags auf ECAF-Zulassung als auch jederzeit nach ihrer Zulassung zu erfüllen. |
|
2. |
Nach Artikel 126 dieser Leitlinie kann das Eurosystem Maßnahmen gegenüber jeder Ratingagentur ergreifen, die
Gibt das Eurosystem der Ratingagentur seinen Beschluss bekannt, Maßnahmen nach Artikel 126 zu ergreifen, nennt es Gründe für den Beschluss. |
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/92 |
LEITLINIE (EU) 2020/1691 DER EUROPÄISCHEN ZENTRALBANK
vom 25. September 2020
zur Änderung der Leitlinie EZB/2014/31 über zusätzliche zeitlich befristete Maßnahmen hinsichtlich der Refinanzierungsgeschäfte des Eurosystems und der Notenbankfähigkeit von Sicherheiten
(EZB/2020/47)
DER EZB-RAT —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union, insbesondere auf Artikel 127 Absatz 2 erster Gedankenstrich,
gestützt auf die Satzung des Europäischen Systems der Zentralbanken und der Europäischen Zentralbank, insbesondere auf Artikel 3.1 erster Gedankenstrich und die Artikel 5.1, 12.1, 14.3 und 18.2,
in Erwägung nachstehender Gründe:
|
(1) |
Asset-Backed Securities, deren zugrunde liegenden Sicherheiten Wohnungsbauhypotheken oder Kredite an kleine und mittlere Unternehmen oder beides darstellen und die bestimmte Voraussetzungen von Artikel 3 Absatz 5 der Leitlinie EZB/2014/31 (1) nicht erfüllen, sollten angesichts der Tatsache, dass von dieser Anlagenklasse noch nie Gebrauch gemacht worden ist, nicht mehr als Sicherheiten für die Kreditgeschäfte des Eurosystems zugelassen sein. |
|
(2) |
Sind Kreditforderungen, die den Regeln nach Artikel 154 Absatz 1 Buchstabe c der Leitlinie (EU) 2015/510 der Europäischen Zentralbank (EZB/2014/60) (2) nicht entsprechen, in einem Pool zusätzlicher Kreditforderungen gemäß Artikel 4 der Leitlinie ECB/2014/31 enthalten, sollte die Methode zur Berechnung finanzieller Sanktionen geändert werden, um unverhältnismäßige finanzielle Sanktionen zu vermeiden. |
|
(3) |
Die Leitlinie EZB/2014/31 sollte daher entsprechend geändert werden — |
HAT FOLGENDE LEITLINIE ERLASSEN:
Artikel 1
Änderungen
Die Leitlinie EZB/2014/31 wird wie folgt geändert:
|
1. |
Artikel 3 Absatz 5 wird gestrichen. |
|
2. |
Artikel 4 wird wie folgt geändert:
|
Artikel 2
Wirksamwerden und Umsetzung
(1) Diese Leitlinie wird am Tag ihrer Bekanntgabe an die nationalen Zentralbanken der Mitgliedstaaten, deren Währung der Euro ist, wirksam.
(2) Die nationalen Zentralbanken der Mitgliedstaaten, deren Währung der Euro ist, treffen die erforderlichen Maßnahmen zur Erfüllung der vorliegenden Leitlinie und wenden diese Maßnahmen ab dem 1. Januar 2021 an. Sie teilen der Europäischen Zentralbank die Rechtstexte und Umsetzungsmaßnahmen in Bezug auf diese Maßnahmen spätestens bis zum 6. November 2020 mit.
Artikel 3
Adressaten
Diese Leitlinie ist an alle Zentralbanken des Eurosystems gerichtet.
Geschehen zu Frankfurt am Main am 25. September 2020.
Für den EZB-Rat
Die Präsidentin der EZB
Christine LAGARDE
(1) Leitlinie EZB/2014/31 der Europäischen Zentralbank vom 9. Juli 2014 über zusätzliche zeitlich befristete Maßnahmen hinsichtlich der Refinanzierungsgeschäfte des Eurosystems und der Notenbankfähigkeit von Sicherheiten und zur Änderung der Leitlinie EZB/2007/9 (ABl. L 240 vom 13.8.2014, S. 28).
(2) Leitlinie (EU) 2015/510 der Europäischen Zentralbank vom 19. Dezember 2014 über die Umsetzung des geldpolitischen Handlungsrahmens des Eurosystems (Leitlinie allgemeine Dokumentation) (EZB/2014/60) (ABl. L 91 vom 2.4.2015, S. 3).
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/94 |
LEITLINIE (EU) 2020/1692 DER EUROPÄISCHEN ZENTRALBANK
vom 25. September 2020
zur Änderung der Leitlinie (EU) 2016/65 über die bei der Umsetzung des geldpolitischen Handlungsrahmens des Eurosystems anzuwendenden Bewertungsabschläge
(EZB/2020/46)
DER EZB-RAT —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union, insbesondere auf Artikel 127 Absatz 2 erster Gedankenstrich,
gestützt auf die Satzung des Europäischen Systems der Zentralbanken und der Europäischen Zentralbank, insbesondere auf Artikel 3.1 erster Gedankenstrich, Artikel 9.2, Artikel 12.1, Artikel 14.3, Artikel 18.2 und Artikel 20 Absatz 1,
in Erwägung nachstehender Gründe:
|
(1) |
Der Risikokontroll- und Bewertungsrahmen des Eurosystems muss angepasst werden, um dem Umstand Rechnung zu tragen, dass nicht gesetzlich geregelte gedeckte Schuldverschreibungen (d. h. vertragliche gedeckte Schuldverschreibungen) nicht mehr als Sicherheiten des Eurosystems akzeptiert werden sollten. |
|
(2) |
Die Leitlinie (EU) 2016/65 der Europäischen Zentralbank (EZB/2015/35) (1) sollte daher entsprechend geändert werden — |
HAT FOLGENDE LEITLINIE ERLASSEN:
Artikel 1
Änderungen
Die Leitlinie (EU) 2016/65 (EZB/2015/35) wird wie folgt geändert:
|
(1) |
Artikel 2 wird wie folgt geändert:
|
|
(2) |
Im Anhang erhält Tabelle 1 folgende Fassung: „Tabelle 1 Haircutkategorien für notenbankfähige marktfähige Sicherheiten auf der Grundlage der Art des Emittenten und/oder der Art der Sicherheit
|
Artikel 2
Wirksamwerden und Umsetzung
(1) Diese Leitlinie wird am Tag ihrer Bekanntgabe an die nationalen Zentralbanken der Mitgliedstaaten, deren Währung der Euro ist, wirksam.
(2) Die nationalen Zentralbanken der Mitgliedstaaten, deren Währung der Euro ist, treffen die zur Erfüllung dieser Leitlinie erforderlichen Maßnahmen und wenden diese ab dem 1. Januar 2021 an. Sie teilen der Europäischen Zentralbank die entsprechenden Rechtstexte und Umsetzungsmaßnahmen bis spätestens 6. November 2020 mit.
Artikel 3
Adressaten
Diese Leitlinie ist an die nationalen Zentralbanken der Mitgliedstaaten gerichtet, deren Währung der Euro ist.
Geschehen zu Frankfurt am Main am 25. September 2020.
Für den EZB-Rat
Die Präsidentin der EZB
Christine LAGARDE
(1) Leitlinie (EU) 2016/65 der Europäischen Zentralbank vom 18. November 2015 über die bei der Umsetzung des geldpolitischen Handlungsrahmens des Eurosystems anzuwendenden Bewertungsabschläge (EZB/2015/35) (ABl. L 14 vom 21.1.2016, S. 30).
GESCHÄFTS- UND VERFAHRENSORDNUNGEN
|
13.11.2020 |
DE |
Amtsblatt der Europäischen Union |
L 379/96 |
BESCHLUSS DES VERWALTUNGSRATS DES GEMEINSAMEN UNTERNEHMENS FÜR BIOBASIERTE INDUSTRIEZWEIGE
vom 26. März 2020
zur Festlegung interner Vorschriften zur Beschränkung bestimmter Rechte von betroffenen Personen bei der Verarbeitung personenbezogener Daten im Rahmen der Tätigkeit des Gemeinsamen Unternehmens für biobasierte Industriezweige (GUBBI)
DER VERWALTUNGSRAT DES GEMEINSAMEN UNTERNEHMENS FÜR BIOBASIERTE INDUSTRIEZWEIGE (im Folgenden „GUBBI“) —
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) 2018/1725 des Europäischen Parlaments und des Rates vom 23. Oktober 2018 zum Schutz natürlicher Personen bei der Verarbeitung personenbezogener Daten durch die Organe, Einrichtungen und sonstigen Stellen der Union, zum freien Datenverkehr und zur Aufhebung der Verordnung (EG) Nr. 45/2001 und des Beschlusses Nr. 1247/2002/EG (1), insbesondere auf Artikel 25,
gestützt auf die Verordnung (EU) Nr. 560/2014 des Rates vom 6. Mai 2014 zur Gründung des Gemeinsamen Unternehmens für biobasierte Industriezweige (2), insbesondere auf Artikel 7 Absatz 3 Buchstabe s,
gestützt auf die Leitlinien des Europäischen Datenschutzbeauftragten zu Artikel 25 der neuen Verordnung und die internen Vorschriften,
nach Konsultation des EDSB gemäß Artikel 41 Absatz 2 der Verordnung (EU) 2018/1725,
in Erwägung nachstehender Gründe:
|
(1) |
Das GUBBI übt seine Tätigkeiten in Übereinstimmung mit der Verordnung (EU) Nr. 560/2014 aus. |
|
(2) |
Nach Artikel 25 Absatz 1 der Verordnung (EU) 2018/1725 müssen Beschränkungen der Anwendung der Artikel 14 bis 22, 35 und 36 sowie des Artikels 4 dieser Verordnung, insofern dessen Bestimmungen den in den Artikeln 14 bis 22 vorgesehenen Rechten und Pflichten entsprechen, auf vom GUBBI zu erlassenden internen Vorschriften beruhen, wenn sie nicht auf Rechtsakten basieren, die auf der Grundlage der Verträge erlassen wurden. |
|
(3) |
Diese internen Vorschriften (einschließlich ihrer Bestimmungen über die Beurteilung der Notwendigkeit und Verhältnismäßigkeit einer Beschränkung) finden keine Anwendung, wenn ein aufgrund der Verträge erlassener Rechtsakt die Beschränkung von Rechten betroffener Personen vorsieht. |
|
(4) |
Wenn das GUBBI seine Pflichten bezüglich Rechten betroffener Personen gemäß der Verordnung (EU) 2018/1725 erfüllt, ist zu berücksichtigen, ob eine der in dieser Verordnung vorgesehenen Ausnahmen Anwendung findet. |
|
(5) |
Im Rahmen seiner Verwaltungstätigkeit ist das GUBBI befugt, Verwaltungsuntersuchungen, Disziplinarverfahren und erste Maßnahmen im Zusammenhang mit dem OLAF gemeldeten Fällen möglicher Unregelmäßigkeiten durchzuführen, Meldungen von Missständen (Whistleblowing) zu bearbeiten, (formelle und informelle) Verfahren in Bezug auf Mobbing zu bearbeiten, interne und externe Beschwerden zu bearbeiten, interne Prüfungen durchzuführen, Untersuchungen durch den Datenschutzbeauftragten in Übereinstimmung mit Artikel 45 Absatz 2 der Verordnung (EU) 2018/1725 sowie interne (IT)-Sicherheitsuntersuchungen durchzuführen. |
|
(6) |
Das GUBBI verarbeitet mehrere Kategorien personenbezogener Daten, einschließlich harter Daten („objektive“ Daten wie Identifikationsdaten, Kontaktdaten, berufsbezogene Daten, Verwaltungsdaten, Daten aus bestimmten Quellen, elektronische Kommunikations- und Verkehrsdaten) und weicher Daten („subjektive“ fallbezogene Daten wie Begründungen, verhaltensbezogene Daten, Bewertungen, Leistungs- und Verhaltensdaten und Daten, die sich auf den Gegenstand des Verfahrens oder der Tätigkeit beziehen oder im Zusammenhang damit vorgebracht werden) (3). |
|
(7) |
Das GUBBI, vertreten durch seinen Exekutivdirektor, ist der für die Verarbeitung Verantwortliche; dies gilt auch, wenn Befugnisse des Verantwortlichen innerhalb des GUBBI weiter delegiert werden, um den operativen Verantwortlichkeiten für bestimmte Vorgänge der Verarbeitung personenbezogener Daten Rechnung zu tragen. |
|
(8) |
Die personenbezogenen Daten werden in einer elektronischen Umgebung oder auf Papier sicher gespeichert, wodurch unrechtmäßiger Zugang oder unrechtmäßige Übermittlung von Daten an Personen, die keine Kenntnis dieser Daten haben müssen, verhindert wird. Die verarbeiteten personenbezogenen Daten werden nicht länger aufbewahrt, als es für die Zwecke, für die sie verarbeitet werden, notwendig und angemessen ist; der Aufbewahrungszeitraum ist in den Datenschutzhinweisen, Datenschutzerklärungen oder Verzeichnissen des GUBBI angegeben. |
|
(9) |
Die internen Vorschriften sollten für sämtliche Verarbeitungsvorgänge gelten, die vom GUBBI zur Durchführung von Verwaltungsuntersuchungen, Disziplinarverfahren, ersten Maßnahmen im Zusammenhang mit dem OLAF gemeldeten Fällen möglicher Unregelmäßigkeiten, Meldungen von Missständen (Whistleblowing), (formellen und informellen) Verfahren in Bezug auf Mobbing, zur Bearbeitung von internen und externen Beschwerden, zur Durchführung von internen Prüfungen, Untersuchungen durch den Datenschutzbeauftragten gemäß Artikel 45 Absatz 2 der Verordnung (EU) 2018/1725 und intern oder extern abgewickelten (z. B. durch das CERT-EU) (IT-)Sicherheitsüberprüfungen ausgeführt werden. |
|
(10) |
Sie sollten auch für Verarbeitungsvorgänge gelten, die vor der Einleitung der vorstehend genannten Verfahren, während dieser Verfahren und bei der Überwachung der aufgrund des Ergebnisses dieser Verfahren getroffenen Folgemaßnahmen vorgenommen werden. Unterstützung und Zusammenarbeit, die das GUBBI nationalen Behörden und internationalen Organisationen außerhalb ihrer Verwaltungsuntersuchungen gewährt, sollten ebenfalls eingeschlossen sein. |
|
(11) |
In Fällen, in denen diese internen Vorschriften Anwendung finden, muss das GUBBI die Gründe dafür darlegen, dass die Beschränkungen in einer demokratischen Gesellschaft unbedingt notwendig und verhältnismäßig sind und den Wesensgehalt der Grundrechte und Grundfreiheiten achten. |
|
(12) |
Innerhalb dieses Rahmens ist das GUBBI verpflichtet, die Grundrechte der betroffenen Personen, insbesondere jene bezüglich des Rechts auf Unterrichtung, Auskunft zu und Berichtigung von personenbezogenen Daten, des Rechts auf Löschung, Einschränkung der Verarbeitung, des Rechts zu Mitteilungen über eine Verletzung des Schutzes personenbezogener Daten an den Betroffenen oder Vertraulichkeit von Kommunikationen, wie in Verordnung (EU) 2018/1725 verankert, während der obigen Vorgänge soweit wie möglich zu respektieren. |
|
(13) |
Das GUBBI kann jedoch verpflichtet sein, die Informationen über die Rechte der betroffenen Person und anderer betroffener Personen zu beschränken, um insbesondere ihre eigenen Ermittlungen, die Ermittlungen und Verfahren anderer Behörden sowie die Rechte Dritter, mit denen ihre Ermittlungen oder andere Verfahren in Beziehung stehen, zu schützen. |
|
(14) |
Das GUBBI kann daher die Unterrichtung zum Zweck des Schutzes der Untersuchung sowie der Grundrechte und Grundfreiheiten anderer betroffener Personen beschränken. |
|
(15) |
Das GUBBI sollte in regelmäßigen Abständen prüfen, ob die Bedingungen, auf denen die Beschränkung beruht, noch gelten, und die Beschränkung aufheben, falls sie nicht mehr gelten. |
|
(16) |
Der Verantwortliche muss den Datenschutzbeauftragten zum Zeitpunkt einer Zurückstellung und während der Überprüfungen unterrichten — |
HAT FOLGENDEN BESCHLUSS ERLASSEN:
Artikel 1
Gegenstand und Anwendungsbereich
(1) Mit diesem Beschluss werden Vorschriften in Bezug auf die Bedingungen festgelegt, unter denen das GUBBI im Rahmen seiner unter Absatz 2 aufgeführten Verfahren gemäß Artikel 25 der Verordnung (EU) 2018/1725 befugt ist, die Anwendung der in den Artikeln 14 bis 21, 35 und 36 sowie in Artikel 4 der Verordnung verankerten Rechte zu beschränken.
(2) Im Rahmen der Verwaltungstätigkeit des GUBBI findet dieser Beschluss Anwendung, soweit das Programmbüro personenbezogene Daten verarbeitet, um Verwaltungsuntersuchungen, Disziplinarverfahren und erste Maßnahmen im Zusammenhang mit dem OLAF gemeldeten Fällen möglicher Unregelmäßigkeiten durchzuführen, die Meldung von Missständen (Whistleblowing) zu bearbeiten, (formelle sowie informelle) Verfahren in Bezug auf Mobbing durchzuführen, interne und externe Beschwerden zu bearbeiten, interne Prüfungen durchzuführen, Untersuchungen durch den Datenschutzbeauftragten gemäß Artikel 45 Absatz 2 der Verordnung (EU) 2018/1725 sowie (IT-)Sicherheitsuntersuchungen intern oder unter externer Mitwirkung (z. B. von CERT-EU) durchzuführen.
(3) Die entsprechenden Kategorien personenbezogener Daten umfassen harte Daten („objektive“ Daten wie Identifikationsdaten, Kontaktdaten, berufsbezogene Daten, Verwaltungsdaten, Daten aus bestimmten Quellen, elektronische Kommunikations- und Verkehrsdaten) und weiche Daten („subjektive“ fallbezogene Daten wie Begründungen, verhaltensbezogene Daten, Bewertungen, Leistungs- und Verhaltensdaten sowie Daten, die sich auf den Gegenstand des Verfahrens oder der Tätigkeit beziehen oder im Zusammenhang damit vorgebracht werden).
(4) Wenn das GUBBI seine Pflichten bezüglich Rechten betroffener Personen gemäß der Verordnung (EU) 2018/1725 erfüllt, ist zu berücksichtigen, ob eine der in dieser Verordnung vorgesehenen Ausnahmen Anwendung findet.
(5) Vorbehaltlich der in diesem Beschluss festgelegten Voraussetzungen können die folgenden Rechte beschränkt werden: die Unterrichtung der betroffenen Personen, das Recht auf Auskunft, Berichtigung, Löschung, Einschränkung der Verarbeitung, Benachrichtigung der von einer Verletzung des Schutzes personenbezogener Daten betroffenen Personen sowie Vertraulichkeit der Kommunikation.
Artikel 2
Angabe des Verantwortlichen
Der für die Verarbeitungsvorgänge Verantwortliche ist das GUBBI, vertreten durch seinen Exekutivdirektor, der die Funktion des Verantwortlichen delegieren kann. Den betroffenen Personen wird in den Datenschutzhinweisen oder -aufzeichnungen, die auf der Website und/oder im Intranet des GUBBI veröffentlicht werden, mitgeteilt, an welche Person die Verantwortung delegiert wurde.
Artikel 3
Angabe der Garantien
(1) Das GUBBI richtet die folgenden Garantien zum Schutz gegen Missbrauch oder unrechtmäßigen Zugang oder unrechtmäßige Übermittlung von personenbezogenen Daten ein: (4)
|
a) |
Dokumente in Papierform werden in gesicherten Schränken aufbewahrt und ausschließlich befugtem Personal zugänglich gemacht. |
|
b) |
Alle elektronischen Daten werden in einer sicheren IT-Anwendung gemäß den Sicherheitsstandards des GUBBI sowie in speziellen elektronischen Verzeichnissen gespeichert, die ausschließlich befugtem Personal zugänglich sind. Angemessene Zugangsrechte werden individuell erteilt. |
|
c) |
Der Schutz der Datenbank erfolgt durch ein System mit einmaliger Anmeldung mit Kennwort und automatischer Verbindung mit Benutzerkennung und Kennwort (Single Sign-on-System). Die Ersetzung von Benutzern ist streng untersagt. Elektronische Aufzeichnungen werden sicher aufbewahrt, um die Vertraulichkeit und den Schutz der darin enthaltenen Daten zu garantieren. |
|
d) |
Alle Personen, die Zugang zu den Daten haben, sind zur Geheimhaltung verpflichtet. |
(2) Die Aufbewahrungsfrist für die in Artikel 1 Absatz 3 genannten personenbezogenen Daten ist nicht länger als für die Datenverarbeitungszwecke notwendig und angemessen. Sie darf keinesfalls länger sein als die Aufbewahrungsfrist, die in den Datenschutzhinweisen, Datenschutzerklärungen oder Verzeichnissen angegeben ist, auf die in Artikel 6 Bezug genommen wird.
(3) Wenn das GUBBI die Anwendung einer Beschränkung in Betracht zieht, sind die Risiken für die Rechte und Freiheiten der betroffenen Person abzuwägen, insbesondere gegenüber dem Risiko für die Rechte und Freiheiten anderer betroffener Personen sowie dem Risiko, dass die Wirksamkeit der von dem gemeinsamen Unternehmen durchgeführten Untersuchungen oder Verfahren zunichtegemacht wird, z. B. durch Vernichtung von Beweismaterial. Die Risiken für die Rechte und Freiheiten der betroffenen Personen betreffen in erster Linie (jedoch nicht nur) Reputationsrisiken sowie Risiken für das Recht auf Verteidigung und den Anspruch auf rechtliches Gehör.
Artikel 4
Beschränkungen
(1) Beschränkungen werden vom GUBBI nur vorgenommen, um Folgendes zu garantieren:
|
a) |
die nationale Sicherheit, die öffentliche Sicherheit oder die Landesverteidigung der Mitgliedstaaten; |
|
b) |
die Verhütung, Ermittlung, Aufdeckung und Verfolgung von Straftaten oder die Strafvollstreckung, einschließlich des Schutzes vor und der Abwehr von Gefahren für die öffentliche Sicherheit; |
|
c) |
sonstige wichtige Ziele des allgemeinen öffentlichen Interesses der Union oder eines Mitgliedstaats, insbesondere die Ziele der gemeinsamen Außen- und Sicherheitspolitik der Union oder ein wichtiges wirtschaftliches oder finanzielles Interesse der Union oder eines Mitgliedstaats, etwa im Währungs-, Haushalts- und Steuerbereich bzw. im Bereich der öffentlichen Gesundheit und der sozialen Sicherheit; |
|
d) |
die innere Sicherheit der Organe und Einrichtungen der Union, einschließlich ihrer elektronischen Kommunikationsnetze; |
|
e) |
die Verhütung, Ermittlung, Aufdeckung und Verfolgung von Verstößen gegen die berufsständischen Regeln reglementierter Berufe; |
|
f) |
Kontroll-, Überwachungs- und Ordnungsfunktionen, die dauernd oder zeitweise mit der Ausübung öffentlicher Gewalt in den unter den Buchstaben a bis c genannten Zwecke verbunden sind; |
|
g) |
der Schutz der betroffenen Person oder der Rechte und Freiheiten anderer Personen; |
|
h) |
die Durchsetzung zivilrechtlicher Ansprüche. |
(2) Im Rahmen der besonderen Anwendung zu den in Absatz 1 genannten Zwecken kann das GUBBI unter folgenden Umständen Beschränkungen anwenden:
|
a) |
in Bezug auf personenbezogene Daten, die mit Dienststellen der Kommission oder anderen Organen, Einrichtungen und sonstigen Stellen der Union ausgetauscht werden;
|
|
b) |
in Bezug auf personenbezogene Daten, die mit zuständigen Behörden der Mitgliedstaaten ausgetauscht werden;
|
|
c) |
in Bezug auf personenbezogene Daten, die mit Drittländern oder internationalen Organisationen ausgetauscht werden, wenn eindeutige Nachweise dafür vorliegen, dass die Ausübung dieser Rechte und Pflichten die Zusammenarbeit des GUBBI mit Drittländern oder internationalen Organisationen bei der Wahrnehmung ihrer Aufgaben wahrscheinlich gefährden würde. |
Vor der Anwendung von Beschränkungen unter den in Unterabsatz 1 Buchstaben a und b genannten Umständen konsultiert das GUBBI die zuständigen Dienststellen der Kommission, die Einrichtungen, Organe und sonstigen Stellen der Union oder die zuständigen Behörden der Mitgliedstaaten, es sei denn, für das GUBBI ist klar, dass die Anwendung einer Beschränkung in einem der in diesen Buchstaben genannten Rechtsakte vorgesehen ist.
Artikel 5
Beschränkungen der Rechte betroffener Personen
(1) In hinreichend begründeten Fällen und unter den in diesem Beschluss festgelegten Bedingungen können die folgenden Rechte durch den Verantwortlichen, sofern dies notwendig und verhältnismäßig ist, im Zusammenhang mit den unter Absatz 2 nachstehend aufgeführten Verarbeitungsvorgängen beschränkt werden:
|
a) |
das Recht auf Unterrichtung; |
|
b) |
das Auskunftsrecht; |
|
c) |
das Recht auf Berichtigung, Löschung und Einschränkung der Verarbeitung; |
|
d) |
das Recht auf Benachrichtigung der von einer Verletzung des Schutzes personenbezogener Daten betroffenen Personen; |
|
e) |
das Recht auf Vertraulichkeit der elektronischen Kommunikation. |
(2) Nach Artikel 25 Absatz 2 Buchstabe a der Verordnung (EU) 2018/1725 kann der Verantwortliche in hinreichend begründeten Fällen und unter den in diesem Beschluss festgelegten Bedingungen Beschränkungen im Zusammenhang mit den folgenden Verarbeitungsvorgängen anwenden:
|
a) |
Durchführung von Verwaltungsuntersuchungen und Disziplinarverfahren; |
|
b) |
erste Maßnahmen im Zusammenhang mit dem OLAF gemeldeten Fällen möglicher Unregelmäßigkeiten; |
|
c) |
Verfahren in Bezug auf gemeldete Missstände (Whistleblowing); |
|
d) |
(formelle und informelle) Verfahren in Bezug auf Mobbing (7); |
|
e) |
Bearbeitung interner und externer Beschwerden; |
|
f) |
interne Prüfungen; |
|
g) |
vom Datenschutzbeauftragten gemäß Artikel 45 Absatz 2 der Verordnung (EU) 2018/1725 durchgeführte Untersuchungen; |
|
h) |
intern oder unter externer Mitwirkung (z. B. durch die CERT-EU) durchgeführte (IT-) Sicherheitsüberprüfungen; |
|
i) |
im Rahmen der Verwaltung der Finanzhilfen oder des Vergabeverfahrens nach Ende der Frist für die Einreichung von Vorschlägen oder Angeboten. (8) |
Die Beschränkung gilt, solange die Gründe dafür weiterhin vorliegen.
(3) Wenn das GUBBI die in Absatz 1 vorgesehenen Rechte ganz oder teilweise beschränkt, ergreift es die in den Artikeln 6 und 7 dieses Beschlusses genannten Maßnahmen.
(4) Wenn betroffene Personen gemäß Artikel 17 der Verordnung (EU) 2018/1725 Auskunft über ihre personenbezogenen Daten, die im Zusammenhang mit einem oder mehreren spezifischen Fällen verarbeitet wurden, oder über einen spezifischen Datenverarbeitungsvorgang verlangen, beschränkt das GUBBI seine Antragsprüfung auf diese personenbezogenen Daten.
Artikel 6
Notwendigkeit und Verhältnismäßigkeit der Beschränkungen
(1) Jede in Artikel 5 dargelegte Beschränkung muss im Hinblick auf die Risiken für die Rechte und Freiheiten der betroffenen Personen notwendig und verhältnismäßig sein und den Wesensgehalt der Grundrechte und Grundfreiheiten in einer demokratischen Gesellschaft achten.
(2) Wird eine Beschränkung in Betracht gezogen, ist deren Notwendigkeit und Verhältnismäßigkeit auf Grundlage der vorliegenden Vorschriften zu prüfen. Diese Prüfung wird im Rahmen der regelmäßigen Überprüfung durchgeführt, nachdem beurteilt wurde, ob die sachlichen und rechtlichen Gründe für eine Beschränkung weiterhin gegeben sind. Zu Rechenschaftszwecken wird dies von Fall zu Fall mittels einer internen Beurteilungsmitteilung dokumentiert.
(3) Beschränkungen sind befristet und werden aufgehoben, sobald die Umstände, die sie rechtfertigen, nicht mehr vorliegen. Dies gilt insbesondere, wenn nicht mehr anzunehmen ist, dass die Ausübung des beschränkten Rechts die Wirkung der verhängten Beschränkung zunichtemachen oder die Rechte oder Freiheiten anderer betroffener Personen beeinträchtigen würde.
Die Beschränkung wird von dem GUBBI nach ihrer Anordnung alle sechs Monate sowie bei Abschluss der jeweiligen Ermittlungen, des relevanten Verfahrens oder der relevanten Untersuchungen überprüft. Danach überwacht der Verantwortliche alle sechs Monate, ob die Aufrechterhaltung der Beschränkung weiterhin notwendig ist.
(4) Wenn das GUBBI die in Absatz 5 dieses Beschlusses dargelegten Beschränkungen gänzlich oder teilweise anwendet, zeichnet es die Gründe für die Beschränkung und die Rechtsgrundlage gemäß Absatz 1 einschließlich einer Beurteilung der Notwendigkeit und Verhältnismäßigkeit der Beschränkung auf.
Der Vermerk sowie gegebenenfalls die Unterlagen, die die tatsächlichen und rechtlichen Grundlagen enthalten, werden registriert. Sie werden dem Europäischen Datenschutzbeauftragten auf Anfrage zur Verfügung gestellt.
Artikel 7
Unterrichtungspflicht
(1) Das GUBBI nimmt in die auf seiner Website veröffentlichten und/oder im Intranet verbreiteten Datenschutzhinweise, Datenschutzerklärungen oder Verzeichnisse im Sinne von Artikel 31 der Verordnung (EU) 2018/1725, in denen betroffene Personen über ihre Rechte im Rahmen eines gegebenen Verfahrens informiert werden, Informationen über die mögliche Beschränkung dieser Rechte auf. Darin ist darüber zu informieren, welche Rechte aus welchen Gründen und für welche Dauer eingeschränkt werden können.
Unbeschadet der Bestimmungen in Artikel 6 Absatz 4 informiert das GUBBI, sofern dies verhältnismäßig ist, auch alle betroffenen Personen, die als von den spezifischen Verarbeitungsvorgängen betroffene Personen gelten, unverzüglich einzeln schriftlich über ihre Rechte bezüglich gegenwärtiger oder künftiger Beschränkungen.
(2) Wenn das GUBBI die in Absatz 5 vorgesehenen Rechte ganz oder teilweise beschränkt, informiert es die betroffene Person über die auferlegte Beschränkung und über die Hauptgründe dafür sowie über die Möglichkeit des Einlegens einer Beschwerde beim Europäischen Datenschutzbeauftragten oder eines Rechtsbehelfs beim Gerichtshof der Europäischen Union.
Die Unterrichtung über Informationen im Sinne von Absatz 2 kann zurückgestellt, unterlassen oder abgelehnt werden, wenn sie die Wirkung der gemäß Artikel 25 Absatz 8 der Verordnung (EU) 2018/1725 angewandten Beschränkung zunichtemachen würde.
Artikel 8
Prüfung durch den Datenschutzbeauftragten
(1) Das GUBBI unterrichtet den eigenen Datenschutzbeauftragten („DSB“) unverzüglich, wenn der Verantwortliche gemäß diesem Beschluss die Rechte betroffener Personen beschränkt oder eine solche Beschränkung ausweitet. Der Verantwortliche gewährt dem DSB Zugang zu den Aufzeichnungen, die die Beurteilung der Notwendigkeit und Verhältnismäßigkeit der Beschränkung enthalten, und dokumentiert das Datum, an dem der DSB unterrichtet wird, in den Aufzeichnungen.
(2) Der DSB kann den Verantwortlichen schriftlich auffordern, die vorgenommenen Beschränkungen zu überprüfen. Der Verantwortliche informiert den DSB schriftlich über das Ergebnis der erbetenen Überprüfung.
(3) Der DSB wird über das gesamte Verfahren hindurch einbezogen. Der Verantwortliche informiert den DSB über die Aufhebung der Beschränkung.
Artikel 9
Inkrafttreten
Dieser Beschluss tritt am zwanzigsten Tag nach seiner Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Brüssel, den 26. März 2020
Für den Verwaltungsrat des GUBBI
Mat QUAEDVLIEG
Der Vorsitzende
(1) ABl. L 295 vom 21.11.2018, S. 39.
(2) ABl. L 169 vom 7.6.2014, S. 130.
(3) Im Fall gemeinsamer Verantwortlichkeit werden Daten entsprechend der Mittel und Zwecke verarbeitet, die in der jeweiligen Vereinbarung zwischen den gemeinsam Verantwortlichen nach Artikel 28 der Verordnung (EU) 2018/1725 festgelegt sind.
(4) Diese Aufzählung ist nicht erschöpfend.
(5) Verordnung (EU) 2016/679 des Europäischen Parlaments und des Rates vom 27. April 2016 zum Schutz natürlicher Personen bei der Verarbeitung personenbezogener Daten, zum freien Datenverkehr und zur Aufhebung der Richtlinie 95/46/EG (Datenschutz-Grundverordnung) (ABl. L 119 vom 4.5.2016, S. 1).
(6) Richtlinie (EU) 2016/680 des Europäischen Parlaments und des Rates vom 27. April 2016 zum Schutz natürlicher Personen bei der Verarbeitung personenbezogener Daten durch die zuständigen Behörden zum Zwecke der Verhütung, Ermittlung, Aufdeckung oder Verfolgung von Straftaten oder der Strafvollstreckung sowie zum freien Datenverkehr und zur Aufhebung des Rahmenbeschlusses 2008/977/JI des Rates (ABl. L 119 vom 4.5.2016, S. 89).
(7) Dieser Verarbeitungsvorgang gilt nicht für Artikel 5 Absatz 1 Buchstabe d.
(8) Dieser Verarbeitungsvorgang gilt nur für Artikel 5 Absatz 1 Buchstabe c.