ISSN 1977-0634
doi:10.3000/19770634.L_2013.279.dan
Den Europæiske Unions
Tidende
L 279

Dansk udgave
Retsforskrifter
56. årgang
19. oktober 2013
|
ISSN 1977-0634 doi:10.3000/19770634.L_2013.279.dan |
||
|
Den Europæiske Unions Tidende |
L 279 |
|

|
||
|
Dansk udgave |
Retsforskrifter |
56. årgang |
|
|
|
|
|
(1) EØS-relevant tekst |
|
DA |
De akter, hvis titel er trykt med magre typer, er løbende retsakter inden for rammerne af landbrugspolitikken og har normalt en begrænset gyldighedsperiode. Titlen på alle øvrige akter er trykt med fede typer efter en asterisk. |
II Ikke-lovgivningsmæssige retsakter
INTERNATIONALE AFTALER
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/1 |
Meddelelse om ikrafttrædelsen af fiskeripartnerskabsaftalen mellem Den Gabonesiske Republik og Det Europæiske Fællesskab
Den Europæiske Union og Den Gabonesiske Republik undertegnede den 6. juni 2007 i Bruxelles en fiskeripartnerskabsaftale mellem Den Gabonesiske Republik og Det Europæiske Fællesskab (1).
Det Europæiske Fællesskab meddelte samme dag, at det havde afsluttet de nødvendige interne procedurer for indgåelsen af aftalen. Den Gabonesiske Republik gav meddelelse herom den 11. juni 2007.
Protokollen trådte derfor i kraft den 11. juni 2007 i overensstemmelse med dens artikel 17.
(1) EUT L 109 af 26.4.2007, s. 3.
FORORDNINGER
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/2 |
KOMMISSIONENS DELEGEREDE FORORDNING (EU) Nr. 1002/2013
af 12. juli 2013
om ændring af Europa-Parlamentets og Rådets forordning (EU) nr. 648/2012 om OTC-derivater, centrale modparter og transaktionsregistre for så vidt angår oversigten over undtagne enheder
(EØS-relevant tekst)
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Europa-Parlamentets og Rådets forordning (EU) nr. 648/2012 af 4. juli 2012 om OTC-derivater, centrale modparter og transaktionsregistre (1), særlig artikel 1, stk. 6, og
ud fra følgende betragtninger:
|
(1) |
Kommissionen har vurderet den internationale behandling af offentlige organer, der har ansvar for forvaltningen af den offentlige gæld, eller som deltager heri, og centralbanker og forelagt sine konklusioner for Europa-Parlamentet og Rådet (2). Kommissionen har navnlig foretaget en sammenlignende analyse af behandlingen af disse offentlige organer og centralbanker inden for de retlige rammer i et betydeligt antal tredjelande samt af risikostyringsstandarderne for derivattransaktioner, der indgås af disse organer og centralbanker i disse jurisdiktioner. |
|
(2) |
På grundlag af analysen har Kommissionen konkluderet, at centralbanker og offentlige organer, der har ansvar for forvaltningen af den offentlige gæld, eller som deltager heri, bør undtages fra clearing- og indberetningsforpligtelsen vedrørende OTC-derivater som følge af de bestemmelser om OTC-derivater, der er indført i Japan og USA. |
|
(3) |
Tilføjelsen af centralbanker og offentlige organer, der har ansvar for forvaltningen af den offentlige gæld, eller som deltager heri, fra Japan og fra USA til oversigten over undtagne enheder som omhandlet i forordning (EU) nr. 648/2012 har til formål at fremme neutrale markedsvilkår ved gennemførelsen af OTC-derivatreformer med hensyn til transaktioner med centralbanker i disse jurisdiktioner og at bidrage til øget sammenhæng og konsekvens på internationalt plan. |
|
(4) |
Både varetagelsen af pengepolitiske forpligtelser og forvaltningen af statsgæld har konsekvenser for velfungerende rentemarkeder og bør koordineres for at sikre, at disse to funktioner udføres effektivt. Da anvendelsesområdet for forordning (EU) nr. 648/2012 ikke omfatter centralbanker og andre offentlige organer i Unionen, der forvalter den offentlige gæld, for at undgå at begrænse deres muligheder for at varetage deres opgaver af samfundsmæssig interesse, ville anvendelse af forskellige bestemmelser på sådanne funktioner, når de udføres af enheder fra tredjelande, skade deres effektivitet. For at sikre, at tredjelandes centralbanker og andre offentlige organer, der har ansvar for forvaltningen af den offentlige gæld, eller som deltager heri, fortsat kan varetage deres opgaver på passende vis, bør tredjelandes offentlige organer, der har ansvar for forvaltningen af den offentlige gæld, eller som deltager heri, også være undtaget fra forordning (EU) nr. 648/2012 — |
VEDTAGET DENNE FORORDNING:
Artikel 1
I artikel 1, stk. 4, i forordning (EU) nr. 648/2012 tilføjes som litra c):
|
»c) |
centralbanker og offentlige organer, der har ansvar for forvaltningen af den offentlige gæld, eller som deltager heri, i følgende lande:
|
Artikel 2
Denne forordning træder i kraft på tyvendedagen efter offentliggørelsen i Den Europæiske Unions Tidende.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 12. juli 2013.
På Kommissionens vegne
José Manuel BARROSO
Formand
(1) EUT L 201 af 27.7.2012, s. 1.
(2) COM(2013) 158 final.
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/4 |
KOMMISSIONENS DELEGEREDE FORORDNING (EU) Nr. 1003/2013
af 12. juli 2013
om supplerende regler til Europa-Parlamentets og Rådets forordning (EU) nr. 648/2012 for så vidt angår gebyrer, som Den Europæiske Værdipapir- og Markedstilsynsmyndighed (ESMA) pålægger transaktionsregistre
(EØS-relevant tekst)
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Europa-Parlamentets og Rådets forordning (EU) nr. 648/2012 af 4. juli 2012 om OTC-derivater, centrale modparter og transaktionsregistre (1), særlig artikel 72, stk. 3, og
ud fra følgende betragtninger:
|
(1) |
I henhold til artikel 62 i Europa-Parlamentets og Rådets forordning (EU) nr. 1095/2010 af 24. november 2010 om oprettelse af en europæisk tilsynsmyndighed (Den Europæiske Værdipapir- og Markedstilsynsmyndighed), om ændring af afgørelse nr. 716/2009/EF og om ophævelse af Kommissionens afgørelse 2009/77/EF (2) består Den Europæiske Værdipapir- og Markedstilsynsmyndigheds (ESMA) indtægter af gebyrer til ESMA i de tilfælde, der er nærmere omhandlet i EU-lovgivningen, samt bidrag fra de nationale offentlige myndigheder og et tilskud fra Unionen. |
|
(2) |
Transaktionsregistre, der er etaberet i Unionen, bør pålægges et registreringsgebyr for at afspejle ESMA's udgifter til behandlingen af registreringsansøgningen. Udgifterne i forbindelse med behandlingen af ansøgningen stiger, hvis et transaktionsregister har til hensigt at dække mindst tre derivatklasser eller at tilbyde accessoriske tjenester. Registreringsgebyret bør derfor beregnes under hensyn til disse to objektive kriterier. |
|
(3) |
Ydelse af accessoriske tjenester og indberetningstjenester for mere end tre derivatklasser forventes også at have en direkte indflydelse på transaktionsregistrets fremtidige omsætning. I forbindelse med opkrævning af registreringsgebyrer bør transaktionsregistre derfor inddeles i tre forskellige kategorier for forventet samlet omsætning (stor, mellemstor og lille forventet samlet omsætning), for hvilke der bør gælde forskellige registreringsgebyrer, afhængigt af om de har til hensigt at levere accessoriske tjenester eller indberetningstjenester i mere end tre derivatklasser eller begge dele. |
|
(4) |
Hvis et transaktionsregister efter at være blevet registreret begynder at tilbyde accessoriske tjenester eller at drive virksomhed for mere end tre derivatklasser og derved kommer op i en højere kategori hvad angår forventet samlet omsætning, bør transaktionsregistret betale forskellen mellem det registreringsgebyr, der oprindelig er betalt, og det registreringsgebyr, der svarer til den nye kategori af forventet samlet omsætning, som det er omfattet af. |
|
(5) |
For at modvirke ubegrundede ansøgninger bør registreringsgebyrer ikke tilbagebetales, hvis en ansøger trækker sin ansøgning tilbage under registreringsproceduren, eller hvis registrering nægtes. |
|
(6) |
For at sikre en effektiv anvendelse af ESMA's budget og samtidig lette den finansielle byrde for medlemsstaterne og Unionen er det nødvendigt at sikre, at transaktionsregistre som minimum betaler alle udgifterne i forbindelse med tilsynet med dem. Gebyrerne bør fastsættes på et niveau, der forhindrer, at der opstår en væsentlig akkumulering af underskud eller overskud i forbindelse med aktiviteter i tilknytning til transaktionsregistre. Hvis der opstår tilbagevendende underskud eller overskud, bør Kommissionen tage niveauet for gebyrerne op til revision. |
|
(7) |
For at sikre en rimelig og klar fordeling af gebyrerne, som samtidig afspejler den faktiske administrative indsats, der kræves for hver tilsynsunderlagt enhed, bør tilsynsgebyret beregnes på grundlag af den omsætning, som transaktionsregistrets hovedaktiviteter genererer. De tilsynsgebyrer, der pålægges et transaktionsregister, bør svare til det pågældende transaktionsregisters aktiviteter sammenlignet med alle registrerede og tilsynsunderlagte transaktionsregistres aktiviteter i et givet regnskabsår. Da der er en række faste administrative omkostninger forbundet med tilsynet med transaktionsregistre, bør der imidlertid fastsættes et minimumstilsynsgebyr. |
|
(8) |
Da der kun vil være begrænsede data til rådighed vedrørende et transaktionsregisters aktiviteter i det første år, det er registreret, bør det første årlige tilsynsgebyr beregnes på grundlag af registreringsgebyret og den tilsynsindsats, ESMA har lagt i tilsynet med transaktionsregistret det pågældende år. |
|
(9) |
Transaktionsregistre er relativt nye enheder, der tilbyder nye regulerede finansielle tjenester, og derfor findes der endnu ikke et pålideligt mål for deres omsætning. For at nå frem til et skøn over transaktionsregistrenes omsætning bør der dog tages hensyn til en række indikatorer, navnlig transaktionsregistrenes hovedindtægter ved centralt at indsamle og opbevare optegnelser over derivater, eksklusive eventuelle indtægter fra accessoriske tjenester, antallet af indberettede handler i en given periode og antallet af udestående handler ved udløbet af hver periode. I transaktionsregistrets første driftsår bør tilsynsgebyret svare til den indsats, ESMA har lagt i tilsynet fra datoen for registreringen og til årets udgang, på grundlag af de efter den forventede samlede omsætning fastsatte registreringsgebyrer. |
|
(10) |
Transaktionsregistre, der registreres i 2013, vil ikke begynde at levere tjenester før udgangen af 2013, og deres aktivitetsniveau i 2013 må forventes at være meget tæt på nul. Deres årlige tilsynsgebyr for 2014 bør derfor beregnes på grundlag af deres relevante omsætning i første halvdel af 2014. |
|
(11) |
Da transaktionsregisterbranchen endnu er i sin vorden, og da der må tages hensyn til mulige udviklingstendenser, bør metoden for beregning af transaktionsregistres omsætning tages op til revision, hvis det er nødvendigt. Kommissionen bør evaluere egnetheden af metoden for beregning af omsætningen som fastsat i denne forordning inden fire år efter forordningens ikrafttræden. |
|
(12) |
Der bør fastsættes bestemmelser om gebyrer, der skal pålægges transaktionsregistre fra tredjelande, når disse ansøger om anerkendelse i Unionen i henhold til de relevante bestemmelser i forordning (EU) nr. 648/2012, til dækning af udgifterne til anerkendelse og de årlige administrative tilsynsudgifter. I denne henseende baseres ESMA's udgifter på de nødvendige omkostninger ved anerkendelse af et sådant transaktionsregister fra et tredjeland, jf. artikel 77, stk. 2, i den nævnte forordning, indgåelsen af samarbejdsordninger med de kompetente myndigheder i det tredjeland, hvor det ansøgende transaktionsregister er registreret, i henhold til artikel 75, stk. 3, i den nævnte forordning, og tilsynet med anerkendte transaktionsregistre. Udgifterne i forbindelse med indgåelsen af samarbejdsordninger deles mellem de anerkendte transaktionsregistre fra samme tredjeland. |
|
(13) |
De tilsynsfunktioner, som ESMA udøver over for anerkendte transaktionsregistre fra tredjelande, vedrører hovedsagelig gennemførelsen af samarbejdsordninger, herunder effektiv udveksling af data mellem de relevante myndigheder. Udgifterne ved disse funktioner bør dækkes af de tilsynsgebyrer, der pålægges anerkendte transaktionsregistre. Da disse udgifter vil være meget mindre end de udgifter, som ESMA har i forbindelse med det direkte tilsyn med registrerede transaktionsregistre i Unionen, bør tilsynsgebyrerne for anerkendte transaktionsregistre være væsentligt lavere end det minimumstilsynsgebyr, der pålægges registrerede transaktionsregistre, som ESMA fører direkte tilsyn med. |
|
(14) |
Under hensyn til de mulige fremtidige udviklingstendenser bør metoden for beregning af den relevante omsætning samt niveauet for registrerings-, anerkendelses- og tilsynsgebyrer tages op til revision og ajourføres, når det er nødvendigt. |
|
(15) |
Der opstår udgifter for de nationale kompetente myndigheder, når de udfører opgaver i henhold til forordning (EU) nr. 648/2012, særlig i forbindelse med delegation af opgaver i henhold til artikel 74 i forordning (EU) nr. 648/2012. De gebyrer, som ESMA pålægger transaktionsregistre, bør også dække disse udgifter. For at undgå, at de kompetente myndigheder lider tab eller opnår overskud ved udførelse af delegerede opgaver, eller når de yder bistand til ESMA, bør ESMA kun refundere de faktiske omkostninger, som den nationale kompetente myndighed har afholdt. |
|
(16) |
Denne forordning bør danne grundlag for ESMA's ret til at opkræve gebyrer af transaktionsregistre. For straks at fremme effektive tilsyns- og håndhævelsesaktiviteter bør den træde i kraft på tredjedagen efter offentliggørelsen — |
VEDTAGET DENNE FORORDNING:
KAPITEL I
ALMINDELIGE BESTEMMELSER
Artikel 1
Genstand
Ved denne forordning fastsættes bestemmelser for de gebyrer, som Den Europæiske Værdipapir- og Markedstilsynsmyndighed (ESMA) skal pålægge transaktionsregistre i forbindelse med registrering, tilsyn og anerkendelse.
Artikel 2
Dækning af de fulde udgifter til tilsyn
De gebyrer, som transaktionsregistre pålægges, skal dække:
|
a) |
alle udgifter ved ESMA's registrering af og tilsyn med transaktionsregistre, jf. forordning (EU) nr. 648/2012, herunder udgifter i forbindelse med anerkendelse af transaktionsregistre |
|
b) |
alle udgifter i forbindelse med godtgørelse til de nationale kompetente myndigheder, der har udført opgaver i henhold til forordning (EU) nr. 648/2012, særlig i forbindelse med delegation af opgaver i henhold til artikel 74 i forordning (EU) nr. 648/2012. |
Artikel 3
Relevant omsætning
1. Et transaktionsregisters relevante omsætning i et givet regnskabsår (n) er summen af en tredjedel af hver af følgende:
|
a) |
indtægterne ved transaktionsregistrets hovedopgave bestående i centralt at indsamle og opbevare optegnelser over derivater beregnet på grundlag af de reviderede regnskaber for det foregående år (n–1) divideret med de samlede indtægter for alle registrerede transaktionsregistre ved udførelsen af deres hovedopgave bestående i centralt at indsamle og opbevare optegnelser over derivater i det foregående år (n–1) |
|
b) |
antallet af handler, der er indberettet til transaktionsregistret i det foregående år (n–1), divideret med det samlede antal handler, der er indberettet til alle registrerede transaktionsregistre i det foregående år (n–1) |
|
c) |
antallet af registrerede udestående handler pr. 31. december det foregående år (n–1) divideret med det samlede antal registrerede udestående handler pr. 31. december det foregående år (n–1) i alle registrerede transaktionsregistre. |
Den relevante omsætning for et givet transaktionsregister (TRi i nedenstående formel) som omhandlet i første afsnit beregnes som følger:
![]()
2. Hvis transaktionsregistret ikke har udøvet virksomhed i hele året (n–1), beregnes den relevante omsætning skønsmæssigt efter formlen i stk. 1 ved for transaktionsregistret og for hvert af elementerne i stk. 1, litra a), b) og c), at ekstrapolere værdierne beregnet for det antal måneder, i hvilket transaktionsregistret udøvede virksomhed i år (n–1), i forhold til hele året (n–1).
Artikel 4
Justering af gebyrer
1. De gebyrer, der pålægges transaktionsregistre, bør fastsættes på et niveau, der forhindrer, at der opstår en væsentlig akkumulering af underskud eller overskud.
Hvis der forekommer et tilbagevendende væsentligt overskud eller underskud, ændrer Kommissionen gebyrernes niveau.
2. Hvis de gebyrer, der pålægges transaktionsregistre, i år (n) er utilstrækkelige til at dække ESMA's samlede nødvendige udgifter til registrering af, tilsyn med og anerkendelse af transaktionsregistre, hæver ESMA i år (n+1) de tilsynsgebyrer, der skal pålægges de transaktionsregistre, der har været registreret i hele år (n), og som stadig er registreret i år (n+1), med det nødvendige beløb.
3. Justeringen af gebyrer for at tage hensyn til underskud, jf. stk. 2, skal beregnes for hvert enkelt transaktionsregister i forhold til dets relevante omsætning i år (n).
KAPITEL II
GEBYRER
Artikel 5
Typer af gebyrer
1. Transaktionsregistre, der er etableret i Unionen, og som ansøger om registrering i henhold til artikel 55, stk. 1, i forordning (EU) nr. 648/2012, pålægges følgende typer gebyrer:
|
a) |
registreringsgebyrer i henhold til artikel 6 |
|
b) |
årlige tilsynsgebyrer i henhold til artikel 7. |
2. Transaktionsregistre, der er etableret i tredjelande, og som ansøger om anerkendelse i henhold til artikel 77, stk. 1, i forordning (EU) nr. 648/2012, pålægges følgende typer gebyrer:
|
a) |
anerkendelsesgebyrer i henhold til artikel 8, stk. 1 |
|
b) |
årlige tilsynsgebyrer for anerkendte transaktionsregistre i henhold til artikel 8, stk. 2. |
Artikel 6
Registreringsgebyr
1. Det registreringsgebyr, der skal betales af ansøgende transaktionsregistre, beregnes afhængigt af den tilsynsindsats, der er nødvendig for at vurdere og behandle ansøgningen, samt transaktionsregistrenes forventede samlede omsætning, jf. stk. 2-6.
2. Ved beregningen af registreringsgebyret skal følgende aktiviteter tages i betragtning:
|
a) |
transaktionsregistrets ydelse af accessoriske tjenester som f.eks. handelsbekræftelse, »trade matching«, servicering af kredithændelser, porteføljebekræftelse eller porteføljekomprimering |
|
b) |
transaktionsregistrets ydelse af registertjenester for tre eller flere klasser af derivater. |
3. Med henblik på stk. 2 anses et transaktionsregister for at yde accessoriske tjenester i følgende tilfælde:
|
a) |
hvis det yder direkte accessoriske tjenester |
|
b) |
hvis en enhed, der tilhører samme gruppe som transaktionsregistret, yder indirekte accessoriske tjenester |
|
c) |
hvis en enhed, med hvilken transaktionsregistret har indgået en aftale om samarbejde om ydelse af tjenester som led i handels- eller efterhandelskæden eller på dette forretningsområde, yder de accessoriske tjenester. |
4. Hvis et transaktionsregister ikke udøver nogen af de aktiviteter, der er omhandlet i stk. 2, anses det pågældende transaktionsregister for at have en lille forventet samlet omsætning og skal betale et registreringsgebyr på 45 000 EUR.
5. Hvis et transaktionsregister udøver en af de to aktiviteter, der er omhandlet i stk. 2, anses det pågældende transaktionsregister for at have en mellemstor forventet samlet omsætning og skal betale et registreringsgebyr på 65 000 EUR.
6. Hvis et transaktionsregister udøver begge de to aktiviteter, der er omhandlet i stk. 2, anses det pågældende transaktionsregister for at have en stor forventet samlet omsætning og skal betale et registreringsgebyr på 100 000 EUR.
7. Hvis der sker en væsentlig ændring med hensyn til ydelse af tjenester, som har til følge, at transaktionsregistret i henhold til stk. 4, 5 og 6 skal betale et højere registreringsgebyr end det oprindelig betalte, pålægges transaktionsregistret at betale forskellen mellem det oprindelig betalte registreringsgebyr og det højere registreringsgebyr, som den væsentlige ændring medfører.
Artikel 7
Årligt tilsynsgebyr for registrerede transaktionsregistre
1. Et registreret transaktionsregister pålægges et årligt tilsynsgebyr.
2. Det samlede årlige tilsynsgebyr for et givet regnskabsår (n) beregnes som følger:
|
a) |
som grundlag for beregningen af det samlede årlige tilsynsgebyr for et givet regnskabsår (n) anvendes det overslag over udgifterne til tilsyn med transaktionsregistre, der fremgår af ESMA's i overensstemmelse med artikel 63 i forordning (EU) nr. 1095/2010 opstillede og godkendte budget for det pågældende år. |
|
b) |
det samlede årlige tilsynsgebyr for et givet regnskabsår (n) beregnes ved at fratrække følgende fra det i litra a) omhandlede overslag over udgifterne:
|
|
c) |
et registreret transaktionsregister skal betale et årligt tilsynsgebyr beregnet ved at fordele det samlede årlige tilsynsgebyr beregnet i henhold til litra b) på alle transaktionsregistre, der er registreret i år n–1, efter andelen af transaktionsregistrets relevante omsætning i forhold til den samlede relevante omsætning for alle registrerede transaktionsregistre beregnet efter artikel 3, stk. 1, og justeret efter artikel 4, stk. 2 og 3. |
3. Det årlige tilsynsgebyr, som transaktionsregistret skal betale, kan ikke være mindre end 30 000 EUR.
4. Uanset stk. 2 og 3 skal et registreret transaktionsregister det år, hvor det bliver registreret, betale et første tilsynsgebyr svarende til det mindste af følgende beløb:
|
a) |
det registreringsgebyr, der skal betales i henhold til artikel 6 |
|
b) |
det registreringsgebyr, der skal betales i henhold til artikel 6, multipliceret med forholdet mellem antal arbejdsdage fra dets registreringsdato til årets udgang og 60 arbejdsdage. |
Beregningen foretages efter følgende formel:

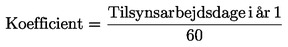
Artikel 8
Gebyr for anerkendelse af transaktionsregistre fra tredjelande
1. Et transaktionsregister, der ansøger om anerkendelse, betaler et ansøgningsgebyr, der beregnes som summen af følgende:
|
a) |
20 000 EUR |
|
b) |
det beløb, der fremkommer ved at fordele 35 000 EUR på det samlede antal transaktionsregistre fra det samme tredjeland, der enten er anerkendt af ESMA, eller som har ansøgt om anerkendelse, men som endnu ikke er blevet anerkendt. |
2. Et transaktionsregister, der er anerkendt i henhold til artikel 77, stk. 1, i forordning (EU) nr. 648/2012, betaler et årligt tilsynsgebyr på 5 000 EUR.
KAPITEL III
BETALINGS- OG GODTGØRELSESBESTEMMELSER
Artikel 9
Generelle betalingsbetingelser
1. Alle gebyrer betales i euro. Gebyrerne betales som anført i artikel 10, 11 og 12.
2. Forsinkede betalinger medfører krav om betaling af en tvangsbøde på 0,1 % af det skyldige beløb pr. dag.
Artikel 10
Betaling af registreringsgebyrer
1. Det i artikel 6 omhandlede registreringsgebyr betales fuldt ud, når transaktionsregistret ansøger om registrering.
2. Registreringsgebyrer godtgøres ikke, hvis et transaktionsregister trækker sin ansøgning om registrering tilbage, før ESMA har vedtaget en begrundet afgørelse om registrering eller om nægtelse af registrering, eller hvis registrering nægtes.
Artikel 11
Betaling af årlige tilsynsgebyrer
1. Det i artikel 7 omhandlede årlige tilsynsgebyr for et givet regnskabsår betales i to rater.
Første rate forfalder den 28. februar i samme år og fastsættes til to tredjedele af det skønsmæssigt beregnede årlige tilsynsgebyr. Hvis de relevante tal for omsætningen beregnet i henhold til artikel 3 endnu ikke foreligger, beregnes omsætningen på grundlag af den seneste relevante omsætning som beregnet efter artikel 3.
Anden rate forfalder den 31. august. Anden rate er det årlige tilsynsgebyr beregnet i henhold til artikel 7 minus første rate.
2. ESMA sender opkrævninger for raterne til transaktionsregistrene mindst 30 dage før den respektive betalingsdato.
Artikel 12
Betaling af anerkendelsesgebyrer
1. De i artikel 8, stk. 1, omhandlede anerkendelsesgebyrer betales fuldt ud, når transaktionsregistret ansøger om anerkendelse. De godtgøres ikke.
2. Hver gang der indgives en ny ansøgning om anerkendelse af et transaktionsregister fra et tredjeland, omberegner ESMA det i artikel 8, stk. 1, litra b), omhandlede beløb.
ESMA godtgør ligeligt blandt de transaktionsregistre fra det samme tredjeland, der allerede er anerkendt, forskellen mellem det beløb, der er pålagt i henhold til artikel 8, stk. 1, litra b), og det beløb, der fremkommer ved omberegningen. Forskellen godtgøres enten ved direkte betaling eller ved nedsættelse af de gebyrer, der pålægges det følgende år.
3. Det årlige tilsynsgebyr for et anerkendt transaktionsregister forfalder ved udgangen af februar. ESMA sender en opkrævning til et anerkendt transaktionsregister mindst 30 dage før denne dato.
Artikel 13
Godtgørelse til kompetente myndigheder
1. Kun ESMA kan pålægge transaktionsregistre gebyrer for registrering, tilsyn og anerkendelse.
2. ESMA godtgør en kompetent myndighed de faktiske omkostninger, myndigheden har pådraget sig i forbindelse med udførelse af arbejde i henhold til forordning (EU) nr. 648/2012, navnlig som følge af delegation af opgaver i henhold til artikel 74 i forordning (EU) nr. 648/2012.
KAPITEL IV
OVERGANGSBESTEMMELSER OG AFSLUTTENDE BESTEMMELSER
Artikel 14
Gebyrer i 2013
1. Transaktionsregistre, der ansøger om registrering i 2013, betaler det i artikel 6 omhandlede registreringsgebyr fuldt ud ved indgivelsen af ansøgningen om registrering, dog tidligst 30 dage efter denne forordnings ikrafttræden.
2. Transaktionsregistre, der registreres i 2013, betaler for 2013 et første årligt tilsynsgebyr beregnet i henhold til artikel 7, stk. 4, fuldt ud 30 dage efter at der er truffet afgørelse om registrering, dog tidligst 60 dage efter denne forordnings ikrafttræden.
3. Transaktionsregistre fra tredjelande, der ansøger om anerkendelse i 2013, betaler det i artikel 8, stk. 1, omhandlede anerkendelsesgebyr fuldt ud ved indgivelsen af ansøgningen om anerkendelse, dog tidligst 30 dage efter denne forordnings ikrafttræden.
4. Transaktionsregistre fra tredjelande, der anerkendes i 2013, betaler for 2013 et årligt tilsynsgebyr beregnet i henhold til artikel 8. stk. 3, fuldt ud 30 dage efter at der er truffet afgørelse om anerkendelse, dog tidligst 60 dage efter denne forordnings ikrafttræden.
Artikel 15
Årligt tilsynsgebyr for 2014 for transaktionsregistre, der registreres i 2013
1. Transaktionsregistre, der registreres i 2013, betaler et årligt tilsynsgebyr for 2014 beregnet i henhold til artikel 7 på grundlag af deres relevante omsætning i perioden fra den 1. januar 2014 til den 30. juni 2014, jf. stk. 2.
2. Med henblik på beregningen af tilsynsgebyrer for 2014 for transaktionsregistre, der registreres i 2013, jf. artikel 7, er et transaktionsregisters relevante omsætning summen af en tredjedel af hver af følgende:
|
a) |
indtægterne ved transaktionsregistrets hovedopgave bestående i centralt at indsamle og opbevare optegnelser over derivater i perioden fra den 1. januar 2014 til den 30. juni 2014 divideret med de samlede indtægter for alle registrerede transaktionsregistre ved udførelsen af deres hovedopgave bestående i centralt at indsamle og opbevare optegnelser over derivater i perioden fra den 1. januar 2014 til den 30. juni 2014 |
|
b) |
antallet af handler, der er indberettet til transaktionsregistret i perioden fra den 1. januar 2014 til den 30. juni 2014, divideret med det samlede antal handler, der er indberettet til alle registrerede transaktionsregistre i perioden fra den 1. januar 2014 til den 30. juni 2014 |
|
c) |
antallet af registrerede udestående handler pr. 30. juni 2014 divideret med det samlede antal registrerede udestående handler pr. 30. juni 2014 i alle registrerede transaktionsregistre. |
3. Det årlige tilsynsgebyr for 2014 for transaktionsregistre, der registreres i 2013, betales i to rater.
Den første rate forfalder den 28. februar 2014 og er af samme størrelse som det registreringsgebyr, som transaktionsregistret har betalt i 2013 i henhold til artikel 6.
Anden rate forfalder den 31. august. Anden rate er det årlige tilsynsgebyr beregnet i henhold til stk. 1 og 2 minus første rate.
Hvis det beløb, et transaktionsregister har betalt som første rate, er større end det årlige tilsynsgebyr beregnet i henhold til stk. 1 og 2, godtgør ESMA transaktionsregistret forskellen mellem det ved første rate betalte beløb og det årlige tilsynsgebyr beregnet i henhold til stk. 1 og 2.
4. ESMA sender opkrævninger for raterne vedrørende det årlige tilsynsgebyr for 2014 til transaktionsregistre, der registreres i 2013, senest 30 dage før betalingsdatoen.
5. Når de reviderede regnskaber for 2014 foreligger, indberetter transaktionsregistre, der registreres i 2013, til ESMA eventuelle ændringer i de i stk. 2, litra a), b) eller c), omhandlede indikatorer, der anvendes ved beregningen af den relevante omsætning i henhold til stk. 2, og som skyldes forskellen mellem de endelige data og de foreløbige data, der er anvendt ved beregningen.
Transaktionsregistre betaler forskellen mellem det faktisk betalte årlige tilsynsgebyr for 2014 og det årlige tilsynsgebyr for 2014, der skal betales som følge af ændringer af de indikatorer, der er omhandlet i stk. 2, litra a), b) eller c), og som anvendes til beregning af den relevante omsætning i henhold til stk. 2.
ESMA sender opkrævningen for en eventuel yderligere betaling, som et transaktionsregister skal foretage som følge af en ændring af en eller flere af de indikatorer, der er omhandlet i stk. 2, litra a), b) eller c), og som anvendes til beregning af den relevante omsætning i henhold til stk. 2, senest 30 dage før den respektive betalingsdato.
Artikel 16
Ikrafttræden
Denne forordning træder i kraft på tredjedagen efter offentliggørelsen i Den Europæiske Unions Tidende.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 12. juli 2013.
På Kommissionens vegne
José Manuel BARROSO
Formand
(1) EUT L 201 af 27.7.2012, s. 1.
(2) EUT L 331 af 15.12.2010, s. 84.
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/10 |
KOMMISSIONENS FORORDNING (EU) Nr. 1004/2013
af 15. oktober 2013
om ændring af bilag II og III til Europa-Parlamentets og Rådets forordning (EF) nr. 396/2005 for så vidt angår maksimalgrænseværdierne for restkoncentrationer af 8-hydroxyquinolin, cyproconazol, cyprodinil, fluopyram, nikotin, pendimethalin, penthiopyrad og trifloxystrobin i eller på visse produkter
(EØS-relevant tekst)
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Europa-Parlamentets og Rådets forordning (EF) nr. 396/2005 af 23. februar 2005 om maksimalgrænseværdier for pesticidrester i eller på vegetabilske og animalske fødevarer og foderstoffer og om ændring af Rådets direktiv 91/414/EØF (1), særlig artikel 14, stk. 1, litra a, og
ud fra følgende betragtninger:
|
(1) |
Der er i bilag II og i del B i bilag III til forordning (EF) nr. 396/2005 fastsat maksimalgrænseværdier for restkoncentrationer af pendimethalin og trifloxystrobin. Der er i del A i bilag III til forordning (EF) nr. 396/2005 fastsat maksimalgrænseværdier for restkoncentrationer af cyproconazol, cyprodinil, fluopyram, nikotin og penthiopyrad. Der er ikke fastsat specifikke maksimalgrænseværdier i bilag II og III for 8-hydroxyquinolin, og stoffet er heller ikke optaget i bilag IV til forordning (EF) nr. 396/2005, hvorfor en standardværdi på 0,01 mg/kg har fundet anvendelse. |
|
(2) |
Der er i forbindelse med en procedure for godkendelse af anvendelse af et plantebeskyttelsesmiddel, der indeholder aktivstoffet 8-hydroxyquinolin på tomater indgivet en ansøgning i henhold til artikel 6, stk. 1, i forordning (EF) nr. 396/2005 om ændring af de gældende maksimalgrænseværdier. |
|
(3) |
For så vidt angår cyproconazol er der indgivet en sådan ansøgning for sennepsfrø og sæddodder. For så vidt angår cyprodinil er der indgivet en sådan ansøgning for radiser og cucurbitae (ikke spiselig skræl). For så vidt angår pendimethalin er der indgivet en sådan ansøgning for skorzonerrod, knoldselleri, kålroer, majroer, bladselleri og urteudtræk (rødder). For så vidt angår trifloxystrobin er der indgivet en sådan ansøgning for bønner (med bælg). |
|
(4) |
I overensstemmelse med artikel 8 i forordning (EF) nr. 396/2005 har de berørte medlemsstater evalueret disse ansøgninger, og evalueringsrapporterne er sendt til Kommissionen. |
|
(5) |
Den Europæiske Fødevaresikkerhedsautoritet (i det følgende benævnt "autoriteten") har vurderet ansøgningerne og vurderingsrapporterne, idet den især undersøgte risiciene for forbrugerne og, hvor det var relevant, for dyr, og afgivet begrundede udtalelser om de foreslåede maksimalgrænseværdier (2). Autoriteten har sendt udtalelserne til Kommissionen og medlemsstaterne og offentliggjort dem. |
|
(6) |
Autoriteten konkluderede i sine begrundede udtalelser, at for så vidt angår anvendelse af cyproconazol på sennepsfrø og sæddodder, er de forelagte data kun tilstrækkelige til, at der kan fastsættes en ny maksimalgrænseværdi for brug i det nordlige EU. For så vidt angår anvendelsen af pendimethalin på knoldselleri, kålroer, majroer og bladselleri konkluderede autoriteten, at de forelagte data ikke er tilstrækkelige til at fastsætte en ny maksimalgrænseværdi. |
|
(7) |
For så vidt angår alle andre ansøgninger konkluderede autoriteten, at alle datakrav var opfyldt, og at de ændringer af maksimalgrænseværdierne, som ansøgerne havde anmodet om, var acceptable med hensyn til forbrugersikkerheden på grundlag af en vurdering af forbrugereksponeringen for 27 specifikke europæiske forbrugergrupper. Der blev taget hensyn til de nyeste oplysninger om stoffernes toksikologiske egenskaber. Der kunne ikke påvises nogen risiko for, at det acceptable daglige indtag (ADI) eller den akutte referencedosis (ARfD) overskrides, hverken ved livslang eksponering for disse stoffer gennem forbrug af alle fødevareprodukter, der kan indeholde stofferne, eller ved kortvarig eksponering gennem et højt forbrug af de pågældende afgrøder og produkter. |
|
(8) |
For så vidt angår penthiopyrad indsendte ansøgeren yderligere data, der bekræfter, at penthiopyrads metabolisme i genmodificerede afgrøder fungerer på samme måde som i konventionelle afgrøder. For at undgå handelsbarrierer for importen af solsikkefrø, rapsfrø, sojabønner og bomuldsfrø er det nødvendigt at fastsætte højere maksimalgrænseværdier for restkoncentrationer. Der bør derfor fastsættes nye maksimalgrænseværdier i del A i bilag III til forordning (EF) nr. 396/2005 for disse produkter. |
|
(9) |
For så vidt angår fluopyram blev der i forordning (EF) nr. 270/2012 (3) fastsat midlertidige maksimalgrænseværdier for adskillige produkter indtil den 31. december indtil der er indsendt yderligere restkoncentrationsdata. Sådanne data blev forelagt Tyskland, der er rapporterende medlemsstat for det stof, den 17. december 2012. For at give den rapporterende medlemsstat den nødvendige tid til at vurdere disse data og forberede en vurderingsrapport, autoriteten den nødvendige tid til at vurdere den rapport og Kommissionen den nødvendige tid til at træffe afgørelse er det hensigtsmæssigt at forlænge gyldigheden af disse maksimalgrænseværdier indtil to år efter offentliggørelsen af denne forordning. |
|
(10) |
For så vidt angår nikotin blev der i forordning (EF) nr. 812/20 (4) fastsat midlertidige maksimalgrænseværdier for te, urteudtræk, krydderier, hyben og friske urter indtil 14. august 2013, indtil der er indsendt og vurderet nye data og oplysninger om den naturlige forekomst eller dannelse af nikotin i de pågældende produkter. Kommissionen er informeret om et forskningsprojekt, som undersøger nikotinkilderne i disse afgrøder. I lyset af den forventede varighed af undersøgelsen og for at give Kommissionen den nødvendige tid til at træffe afgørelse er det hensigtsmæssigt at forlænge gyldigheden af disse maksimalgrænseværdier indtil tre år efter offentliggørelsen af denne forordning. |
|
(11) |
På baggrund af autoritetens begrundede udtalelser og under hensyntagen til alle relevante faktorer opfylder de ændringer af maksimalgrænseværdierne, som der er ansøgt om, de relevante krav i artikel 14, stk. 2, i forordning (EF) nr. 396/2005. |
|
(12) |
Forordning (EF) nr. 396/2005 bør ændres i overensstemmelse hermed. |
|
(13) |
Af hensyn til retssikkerheden bør ændringen vedrørende nikotin finde anvendelse fra 15. august 2013. |
|
(14) |
Foranstaltningerne i denne forordning er i overensstemmelse med udtalelse fra Den Stående Komité for Fødevarekæden og Dyresundhed — |
VEDTAGET DENNE FORORDNING:
Artikel 1
Bilag II og III til forordning (EF) nr. 396/2005 ændres som angivet i bilaget til nærværende forordning.
Artikel 2
Denne forordning træder i kraft dagen efter offentliggørelsen i Den Europæiske Unions Tidende.
Den anvendes dog fra den 15. august 2013 for nikotin i hyben med kodenummer 0154050, friske urter med kodenummer 0256000, te med kodenummer 0610000, urteudtræk med kodenummer 0630000 og krydderier med kodenummer 0800000.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 15. oktober 2013.
På Kommissionens vegne
José Manuel BARROSO
Formand
(1) EUT L 70 af 16.3.2005, s. 1.
(2) EFSA's videnskabelige rapporter foreligger online: http://www.efsa.europa.eu:
Reasoned opinion on the modification of the existing MRL for 8-hydroxyquinoline in tomatoes. EFSA Journal 2013; 11(5):3224 (20 pp.). doi:10.2903/j.efsa.2013.3224.
Reasoned opinion on the modification of the existing MRL for cyproconazole in mustard seed and gold of pleasure. EFSA Journal 2013; 11(4):3194 (26 pp.). doi:10.2903/j.efsa.2013.3194.
Reasoned opinion on the modification of the existing MRLs for cyprodinil in radishes and cucurbits inedible peel. EFSA Journal 2013; 11(4):3184 (24 pp.). doi:10.2903/j.efsa.2013.3184.
Reasoned opinion on the modification of the existing MRLs for pendimethalin in various crops. EFSA Journal 2013; 11(5):3217 (27 pp.). doi:10.2903/j.efsa.2013.3217.
Reasoned opinion on the modification of the existing MRL for trifloxystrobin in beans with pods. EFSA Journal 2013; 11(4):3199 (24 pp.). doi:10.2903/j.efsa.2013.3199.
(3) EUT L 89 af 27.3.2012, s. 5.
(4) EUT L 208 af 13.8.2011, s. 1.
BILAG
I bilag II og III til forordning (EF) nr. 396/2005 foretages følgende ændringer:
|
1) |
I bilag II affattes kolonnerne vedrørende pendimethalin og trifloxystrobin således: »Pesticidrester og maksimalgrænseværdier (mg/kg)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2) |
I del A i bilag III foretages følgende ændringer:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
3) |
I del B i bilag III affattes kolonnen vedrørende pendimethalin således: »Pesticidrester og maksimalgrænseværdier (mg/kg)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(1) Bilag I indeholder en fuldstændig liste over vegetabilske og animalske produkter, som der er fastsat maksimalgrænseværdier for.
(2) Angiver bestemmelsesgrænseværdien.
(3) Pesticid/kode-kombination, som maksimalgrænseværdierne i bilag III, del B, gælder for.
(F)= Fedtopløselig
Trifloxystrobin (F) (R)
|
(R) |
= |
Definitionen på restkoncentration er forskellig for følgende pesticid/kodenummer-kombinationer: Trifloxystrobin- kode 1000000: Summen af trifloxystrobin og metabolitten (E, E)-methoxyimino- {2-[1-(3-trifluormethyl-phenyl)-ethylideneamino-oxymethyl]-phenyl}-eddikesyre (CGA 321113)« |
(4) Bilag I indeholder en fuldstændig liste over vegetabilske og animalske produkter, som der er fastsat maksimalgrænseværdier for.
(5) Angiver bestemmelsesgrænseværdien.
(F)= Fedtopløselig
Cyprodinil (F) (R)
|
(R) |
= |
Definitionen på restkoncentration er forskellig for følgende pesticid/kodenummer-kombinationer: Cyprodinil - kode 1000000: Summen af cyprodinil og metabolit CGA 304075 |
Fluopyram (R)
Fluopyram - kode: 1000000: sum af fluopyram og fluopyram-benzamid (M25), udtrykt som fluopyram
|
(+) |
Den Europæiske Fødevaresikkerhedsautoritet har påpeget, at visse oplysninger om restkoncentrationstest ikke foreligger. Når Kommissionen tager maksimalgrænseværdien op til revision, vil den tage hensyn til de i første punktum omhandlede oplysninger, hvis de foreligger senest den 19. oktober 2015, eller den vil, hvis oplysningerne ikke foreligger på nævnte tidspunkt, tage hensyn til, at oplysningerne ikke foreligger.
|
Nikotin
|
(+) |
Den videnskabelige dokumentation giver ikke noget afgørende bevis, for at nikotin forekommer naturligt i den pågældende afgrøde, og for at belyse dens dannelsesmekanisme. Når maksimalgrænseværdien for restkoncentrationer revurderes vil Kommissionen tage hensyn til oplysningerne, hvis de indsendes inden den 19. oktober 2016, eller hvis oplysningerne ikke er indsendt inden den dato til fraværet af oplysninger.
|
|
(+) |
Følgende maksimalgrænseværdier for restkoncentrationer gælder for tørrede vilde svampe: 2,3 mg/kg for rørhatte, 1,2 mg/kg for andre tørrede vilde svampe end rørhatte. Maksimalgrænseværdierne tages op til fornyet overvejelse inden den 30. november 2014. Bekræftende data, herunder videnskabelig dokumentation om naturlig forekomst eller dannelse af nikotin i den pågældende afgrøde, vil blive evalueret. En ny vurdering af dataene kan medføre, at maksimalgrænseværdierne for restkoncentrationer ændres.
|
|
(+) |
Den videnskabelige dokumentation giver ikke noget afgørende bevis, for at nikotin forekommer naturligt i den pågældende afgrøde, og for at belyse dens dannelsesmekanisme. Når maksimalgrænseværdien for restkoncentrationer revurderes vil Kommissionen tage hensyn til oplysningerne, hvis de indsendes inden den 19. oktober 2016, eller hvis oplysningerne ikke er indsendt inden den dato til fraværet af oplysninger.
|
(6) Bilag I indeholder en fuldstændig liste over vegetabilske og animalske produkter, som der er fastsat maksimalgrænseværdier for.
(7) Angiver bestemmelsesgrænseværdien.«
(8) Bilag I indeholder en fuldstændig liste over vegetabilske og animalske produkter, som der er fastsat maksimalgrænseværdier for.
(9) Angiver bestemmelsesgrænseværdien.
(F)= Fedtopløselig«
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/57 |
KOMMISSIONENS GENNEMFØRELSESFORORDNING (EU) Nr. 1005/2013
af 17. oktober 2013
om godkendelse af en væsentlig ændring af varespecifikationen for en betegnelse, der er opført i registret over beskyttede oprindelsesbetegnelser og beskyttede geografiske betegnelser [Emmental français est-central (BGB)]
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Europa-Parlamentets og Rådets forordning (EU) nr. 1151/2012 af 21. november 2012 om kvalitetsordninger for landbrugsprodukter og fødevarer (1), særlig artikel 52, stk. 2, og
ud fra følgende betragtninger:
|
(1) |
Forordning (EU) nr. 1151/2012 har ophævet og erstattet Rådets forordning (EF) nr. 510/2006 af 20. marts 2006 om beskyttelse af geografiske betegnelser og oprindelsesbetegnelser for landbrugsprodukter og fødevarer (2). |
|
(2) |
Kommissionen har i overensstemmelse med artikel 9, stk. 1, første afsnit, i forordning (EF) nr.510/2006 behandlet Frankrigs ansøgning om godkendelse af en ændring af varespecifikationen for den beskyttede geografiske betegnelse "Emmental français est-central", der er registreret i henhold til Kommissionens forordning (EF) nr. 1107/1996 (3). |
|
(3) |
Eftersom den pågældende ændring er væsentlig, har Kommissionen i overensstemmelse med artikel 6, stk. 2, i forordning (EF) nr. 510/2006 offentliggjort ændringsansøgningen i Den Europæiske Unions Tidende (4). Da Kommissionen ikke har modtaget indsigelser, jf. artikel 7 i forordning (EF) nr. 510/2006, bør ændringen af varespecifikationen godkendes — |
VEDTAGET DENNE FORORDNING:
Artikel 1
Den ændring af varespecifikationen, der blev offentliggjort i Den Europæiske Unions Tidende, og som vedrører betegnelsen i bilaget til denne forordning, godkendes.
Artikel 2
Denne forordning træder i kraft på tyvendedagen efter offentliggørelsen i Den Europæiske Unions Tidende.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 17. oktober 2013.
På Kommissionens vegne For formanden
Dacian CIOLOȘ
Medlem af Kommissionen
(1) EUT L 343 af 14.12.2012, s. 1.
(2) EUT L 93 af 31.3.2006, s. 12.
(3) EFT L 148 af 21.6.1996, s. 1.
(4) EUT C 352 af 16.11.2012, s. 17.
BILAG
Landbrugsprodukter bestemt til konsum, som er opført i traktatens bilag I:
Kategori 1.3. Oste
FRANKRIG
Emmental français est-central (BGB)
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/59 |
KOMMISSIONENS GENNEMFØRELSESFORORDNING (EU) Nr. 1006/2013
af 18. oktober 2013
om godkendelse af L-cystin som tilsætningsstof til foder til alle dyrearter
(EØS-relevant tekst)
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om den Europæiske Unions funktionsmåde,
under henvisning til Europa-Parlamentets og Rådets forordning (EF) nr. 1831/2003 af 22. september 2003 om fodertilsætningsstoffer (1), særlig artikel 9, stk. 2, og
ud fra følgende betragtninger:
|
(1) |
Forordning (EF) nr. 1831/2003 indeholder bestemmelser om godkendelse af fodertilsætningsstoffer og om grundlaget og procedurerne for meddelelse af sådanne godkendelser. |
|
(2) |
Der er i overensstemmelse med artikel 7 i forordning (EF) nr. 1831/2003 indsendt en ansøgning om godkendelse af L-cystin som fodertilsætningsstof i den funktionelle gruppe »aminosyrer, deres salte og analoger«. Ansøgningen var vedlagt de oplysninger og dokumenter, der kræves i henhold til artikel 7, stk. 3, i forordning (EF) nr. 1831/2003. |
|
(3) |
Ansøgningen vedrører godkendelse i tilsætningsstofkategorien »tilsætningsstoffer med ernæringsmæssige egenskaber« af L-cystin som tilsætningsstof til foder til alle dyrearter. |
|
(4) |
Den Europæiske Fødevaresikkerhedsautoritet (»autoriteten«) konkluderede i sin udtalelse af 13. marts 2013 (2), at L-cystin under de foreslåede anvendelsesbetingelser ikke har skadelige virkninger på dyrs eller menneskers sundhed eller på miljøet, og at det kan betragtes som effektivt med hensyn til at bidrage til at dække behovet for svovlholdige aminosyrer hos alle dyrearter. Autoriteten mener ikke, at der er behov for særlige krav om overvågning efter markedsføringen. Autoriteten har ligeledes gennemgået den rapport om analysemetoden for fodertilsætningsstoffet i foder, der blev forelagt af det i henhold til forordning (EF) nr. 1831/2003 oprettede referencelaboratorium. |
|
(5) |
Vurderingen af stoffet viser, at betingelserne for godkendelse, jf. artikel 5 i forordning (EF) nr. 1831/2003, er opfyldt. Derfor bør anvendelsen af stoffet godkendes som anført i bilaget til nærværende forordning. |
|
(6) |
Foranstaltningerne i denne forordning er i overensstemmelse med udtalelse fra Den Stående Komité for Fødevarekæden og Dyresundhed — |
VEDTAGET DENNE FORORDNING:
Artikel 1
Det i bilaget opførte stof, der tilhører tilsætningsstofkategorien »tilsætningsstoffer med ernæringsmæssige egenskaber« og den funktionelle gruppe »aminosyrer, deres salte og analoger«, tillades anvendt som fodertilsætningsstof på de betingelser, der er fastsat i bilaget.
Artikel 2
Denne forordning træder i kraft på tyvendedagen efter offentliggørelsen i Den Europæiske Unions Tidende.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 18. oktober 2013.
På Kommissionens vegne
José Manuel BARROSO
Formand
(1) EUT L 268 af 18.10.2003, s. 29.
(2) EFSA Journal 2013; 11(4):3173.
BILAG
|
Tilsætningsstoffets identifikationsnummer |
Navn på indehaveren af godkendelsen |
Tilsætningsstof |
Sammensætning, kemisk betegnelse, beskrivelse og analysemetode |
Dyreart eller -kategori |
Maksimumsalder |
Minimumsindhold |
Maksimumsindhold |
Andre bestemmelser |
Godkendelse gyldig til |
||||||||||||||
|
mg/kg fuldfoder med et vandindhold på 12 % |
|||||||||||||||||||||||
|
Kategori: tilsætningsstoffer med ernæringsmæssige egenskaber. Funktionel gruppe: aminosyrer, deres salte og analoger |
|||||||||||||||||||||||
|
3c391 |
— |
L-cystin |
|
Alle dyrearter |
— |
— |
— |
|
8. november 2023 |
||||||||||||||
(1) Nærmere oplysninger om analysemetoderne findes på referencelaboratoriets hjemmeside: http://irmm.jrc.ec.europa.eu/EURLs/EURL_feed_additives/authorisation/evaluation_reports/Pages/index.aspx
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/61 |
KOMMISSIONENS GENNEMFØRELSESFORORDNING (EU) Nr. 1007/2013
af 18. oktober 2013
om tillæg til fangstkvoterne for ansjos i Biscayabugten for 2013/2014 af de mængder, som Frankrig og Spanien har tilbageholdt i fangstperioden 2012/2013 i medfør af artikel 4, stk. 2, i Rådets forordning (EF) nr. 847/96
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Rådets forordning (EF) nr. 847/96 af 6. maj 1996 om supplerende betingelser for forvaltningen af TAC'er og kvoter fra år til år (1), særlig artikel 4, stk. 2, og
ud fra følgende betragtninger:
|
(1) |
I henhold til artikel 4, stk. 2, i forordning (EF) nr. 847/96 kan medlemsstaterne inden den 31. oktober i det år, som fangstkvoten gælder for, anmode Kommissionen om at tilbageholde op til 10 % af denne kvote til overførsel til det følgende år. Kommissionen forhøjer den relevante kvote med den tilbageholdte mængde. |
|
(2) |
TAC'en og medlemsstaternes kvoter for ansjosbestanden i Biscayabugten (ICES-underområde VIII) fastsættes for en årlig forvaltningsperiode, der går fra den 1. juli til den 30. juni det følgende år. |
|
(3) |
Rådets forordning (EU) nr. 694/2012 af 27. juli 2012 om fastsættelse af fiskerimuligheder for ansjos i Biscayabugten for fangstperioden 2012/2013 (2), fastsætter fangstkvoterne for ansjos i Biscayabugten (ICES underområde VIII) for perioden som starter den 1. juli 2012 og slutter den 30. juni 2013. |
|
(4) |
Rådets forordning (EU) nr. 713/2013 af 23. juli 2013 om fastsættelse af fiskerimuligheder for ansjos i Biscayabugten for fangstperioden 2013/2014 (3), fastsætter fangstkvoterne for ansjos i Biscayabugten (ICES underområde VIII) for perioden som starter den 1. juli 2013 og slutter den 30. juni 2014. |
|
(5) |
I henhold til de relevante forordninger om fiskerimuligheder og efter at have taget hensyn til udvekslingen af fiskerimuligheder i henhold til artikel 20, stk. 5, i Rådets forordning (EF) nr. 2371/2002 af 20. december 2002 om bevarelse og bæredygtig udnyttelse af fiskeressourcerne som led i den fælles fiskeripolitik (4) og overførsel af kvoter i overensstemmelse med artikel 4, stk. 2, i Rådets forordning (EF) nr. 847/96 svarede de kvoter for ansjos i Biscayabugten, der var til rådighed for Frankrig og Spanien ved udgangen af fangstperioden 2012/2013, til henholdsvis 4 876 tons og 16 460 tons. |
|
(6) |
Ved udgangen af fangstperioden 2012/2013 indberettede Frankrig og Spanien fangster af ansjos i Biscayabugten på henholdsvis 4 805,1 tons og 11 275,2 tons. |
|
(7) |
I henhold til artikel 4, stk. 2, i forordning (EF) nr. 847/96 har både Frankrig og Spanien anmodet om, at en del af deres tildelte fangstkvote for ansjos i Biscayabugten for fangstperioden 2012/2013 blev tilbageholdt og overført til den følgende fangstperiode. De tilbageholdte mængder bør inden for de grænser, som er fastsat i den pågældende forordning, lægges til kvoten for fangstperioden 2013/2014. |
|
(8) |
Foranstaltningerne i denne forordning er i overensstemmelse med udtalelse fra Komitéen for Fiskeri og Akvakultur — |
VEDTAGET DENNE FORORDNING:
Artikel 1
1. Den fangstkvote for ansjos, der ved forordning (EU) nr. 713/2013 er fastsat for Frankrig i Biscayabugten, forhøjes med 70,9 tons.
2. Den fangstkvote for ansjos, der ved forordning (EU) nr. 713/2013 er fastsat for Spanien i Biscayabugten, forhøjes med 1 646 tons.
Artikel 2
Denne forordning træder i kraft dagen efter offentliggørelsen i Den Europæiske Unions Tidende.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 18. oktober 2013.
På Kommissionens vegne
José Manuel BARROSO
Formand
(1) EFT L 115 af 9.5.1996, s. 3.
(2) EUT L 203 af 31.7.2012, s. 26.
(3) EUT L 201 af 26.7.2013, s. 8.
(4) EFT L 358 af 31.12.2002, s. 59.
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/63 |
KOMMISSIONENS GENNEMFØRELSESFORORDNING (EU) Nr. 1008/2013
af 18. oktober 2013
om faste importværdier med henblik på fastsættelse af indgangsprisen for visse frugter og grøntsager
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Rådets forordning (EF) nr. 1234/2007 af 22. oktober 2007 om en fælles markedsordning for landbrugsprodukter og om særlige bestemmelser for visse landbrugsprodukter (fusionsmarkedsordningen) (1),
under henvisning til Kommissionens gennemførelsesforordning (EU) nr. 543/2011 af 7. juni 2011 om gennemførelsesbestemmelser til Rådets forordning (EF) nr. 1234/2007 for så vidt angår frugt og grøntsager og forarbejdede frugter og grøntsager (2), særlig artikel 136, stk. 1, og
ud fra følgende betragtninger:
|
(1) |
Ved gennemførelsesforordning (EU) nr. 543/2011 fastsættes der på basis af resultatet af de multilaterale handelsforhandlinger under Uruguay-runden kriterier for Kommissionens fastsættelse af faste importværdier for tredjelande for de produkter og perioder, der er anført i del A i bilag XVI til nævnte forordning. |
|
(2) |
Der beregnes hver arbejdsdag en fast importværdi i henhold til artikel 136, stk. 1, i gennemførelsesforordning (EU) nr. 543/2011 under hensyntagen til varierende daglige data. Derfor bør nærværende forordning træde i kraft på dagen for offentliggørelsen i Den Europæiske Unions Tidende — |
VEDTAGET DENNE FORORDNING:
Artikel 1
De faste importværdier som omhandlet i artikel 136 i gennemførelsesforordning (EU) nr. 543/2011 fastsættes i bilaget til nærværende forordning.
Artikel 2
Denne forordning træder i kraft på dagen for offentliggørelsen i Den Europæiske Unions Tidende.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 18. oktober 2013.
På Kommissionens vegne For formanden
Jerzy PLEWA
Generaldirektør for landbrug og udvikling af landdistrikter
(1) EUT L 299 af 16.11.2007, s. 1.
(2) EUT L 157 af 15.6.2011, s. 1.
BILAG
Faste importværdier med henblik på fastsættelse af indgangsprisen for visse frugter og grøntsager
|
(EUR/100 kg) |
||
|
KN-kode |
Tredjelandskode (1) |
Fast importværdi |
|
0702 00 00 |
MA |
53,1 |
|
MK |
47,7 |
|
|
ZZ |
50,4 |
|
|
0707 00 05 |
MK |
54,3 |
|
TR |
126,8 |
|
|
ZZ |
90,6 |
|
|
0709 93 10 |
TR |
144,2 |
|
ZZ |
144,2 |
|
|
0805 50 10 |
AR |
100,6 |
|
CL |
101,0 |
|
|
IL |
97,0 |
|
|
TR |
87,3 |
|
|
ZA |
102,0 |
|
|
ZZ |
97,6 |
|
|
0806 10 10 |
BR |
254,7 |
|
TR |
151,4 |
|
|
ZZ |
203,1 |
|
|
0808 10 80 |
CL |
154,8 |
|
NZ |
116,7 |
|
|
US |
156,2 |
|
|
ZA |
120,6 |
|
|
ZZ |
137,1 |
|
|
0808 30 90 |
TR |
126,8 |
|
ZZ |
126,8 |
|
(1) Landefortegnelse fastsat ved Kommissionens forordning (EF) nr. 1833/2006 (EUT L 354 af 14.12.2006, s. 19). Koden »ZZ« = »anden oprindelse«.
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/65 |
KOMMISSIONENS GENNEMFØRELSESFORORDNING (EU) Nr. 1009/2013
af 18. oktober 2013
om fastsættelse af den tildelingskoefficient, der skal anvendes på ansøgninger om importlicens for olivenolie, der er indgivet fra den 14. til den 15. oktober 2013 som led i toldkontingentet for Tunesien og om suspension af udstedelsen af importlicenser for oktober 2013
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Rådets forordning (EF) nr. 1234/2007 af 22. oktober 2007 om en fælles markedsordning for landbrugsprodukter og om særlige bestemmelser for visse landbrugsprodukter (fusionsmarkedsordningen) (1),
under henvisning til Kommissionens forordning (EF) nr. 1301/2006 af 31. august 2006 om fælles regler for administration af toldkontingenter for import af landbrugsprodukter på grundlag af en importlicensordning (2), særlig artikel 7, stk. 2, og
ud fra følgende betragtninger:
|
(1) |
Ved artikel 3, stk. 1 og 2, i protokol nr. 1 (3) til Euro-Middelhavsaftalen om oprettelse af en associering mellem Det Europæiske Fællesskab og dets medlemsstater på den ene side og Den Tunesiske Republik på den anden side (4) åbnes der et toldfrit toldkontingent for import af ubehandlet olivenolie henhørende under KN-kode 1509 10 10 og 1509 10 90, som er fuldstændigt fremstillet i Tunesien, og som transporteres direkte fra dette land til EU, inden for en mængde, der fastsættes hvert år. |
|
(2) |
I artikel 2, stk. 2, i Kommissionens forordning (EF) nr. 1918/2006 af 20. december 2006 om åbning og forvaltning af et toldkontingent for olivenolie med oprindelse i Tunesien (5), fastsættes der månedlige kvantitative begrænsninger for udstedelsen af importlicenser. |
|
(3) |
I henhold til artikel 3, stk. 1, i forordning (EF) nr. 1918/2006 er der til myndighederne blevet indsendt ansøgninger om udstedelse af importlicens for en samlet mængde, der overstiger den maksimumsmængde, der er fastsat for oktober måned, jf. forordningens artikel 2, stk. 2. |
|
(4) |
Derfor bør Kommissionen fastsætte en tildelingskoefficient, så der kan udstedes importlicenser i forhold til den disponible mængde. |
|
(5) |
Da maksimumsmængden for oktober måned er nået, kan der ikke udstedes nogen importlicenser for denne måned — |
VEDTAGET DENNE FORORDNING:
Artikel 1
De importlicensansøgninger, der blevet indsendt den 14. og den 15. oktober 2013 i henhold til artikel 3, stk. 1, i forordning (EF) nr. 1918/2006, multipliceres med en tildelingskoefficient på 39,536727 %.
Udstedelsen af importlicenser for de mængder, der er ansøgt om fra den 21. oktober 2013, suspenderes for oktober måned 2013.
Artikel 2
Denne forordning træder i kraft den 19. oktober 2013.
Denne forordning er bindende i alle enkeltheder og gælder umiddelbart i hver medlemsstat.
Udfærdiget i Bruxelles, den 18. oktober 2013.
På Kommissionens vegne For formanden
Jerzy PLEWA
Generaldirektør for landbrug og udvikling af landdistrikter
(1) EUT L 299 af 16.11.2007, s. 1.
(2) EUT L 238 af 1.9.2006, s. 13.
(3) EFT L 97 af 30.3.1998, s. 57.
(4) EFT L 97 af 30.3.1998, s. 2.
(5) EUT L 365 af 21.12.2006, s. 84.
AFGØRELSER
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/66 |
DEN UDENRIGS- OG SIKKERHEDSPOLITISKE KOMITÉS AFGØRELSE EUPOL RD CONGO/1/2013
af 8. oktober 2013
om forlængelse af mandatet for missionschefen for om Den Europæiske Unions politimission vedrørende reformen af sikkerhedssektoren og dens retlige grænseflade i Den Demokratiske Republik Congo (EUPOL RD Congo)
(2013/511/FUSP)
DEN UDENRIGS- OG SIKKERHEDSPOLITISKE KOMITÉ HAR —
under henvisning til traktaten om Den Europæiske Union, særlig artikel 38, stk. 3,
under henvisning til Rådets afgørelse 2010/576/FUSP af 23. september 2010 om Den Europæiske Unions politimission vedrørende reformen af sikkerhedssektoren og dens retlige grænseflade i Den Demokratiske Republik Congo (EUPOL RD Congo) (1), særlig artikel 10, stk. 1, og
ud fra følgende betragtninger:
|
(1) |
I henhold til artikel 10, stk. 1, i afgørelse 2010/576/FUSP bemyndiges Den Udenrigs- og Sikkerhedspolitiske Komité (PSC) til i overensstemmelse med traktatens artikel 38, stk. 3, at træffe de relevante afgørelser med henblik på at udøve politisk kontrol med og strategisk ledelse af EUPOL RD Congo. Denne bemyndigelse omfatter især at træffe afgørelse om udnævnelse af en missionschef på forslag fra Unionens højtstående repræsentant for udenrigsanliggender og sikkerhedspolitik (den højtstående repræsentant). |
|
(2) |
Den 8. oktober 2010 udpegede PSC, efter et forslag fra den højtstående repræsentant og i henhold til afgørelse EUPOL RD Congo/1/2010 (2), ledende inspektør Jean-Paul RIKIR til missionschef for EUPOL RD Congo med virkning fra den 1. oktober 2010. |
|
(3) |
Den 16. september 2011 forlængede PSC, efter et forslag fra den højtstående repræsentant og i henhold til afgørelse EUPOL RD Congo/1/2011 (3), ledende inspektør Jean-Paul RIKIRs mandat som missionschef for EUPOL RD Congo indtil den 30. september 2012. |
|
(4) |
Den 25. september 2012 forlængede PSC, efter et forslag fra den højtstående repræsentant og i henhold til afgørelse EUPOL RD Congo/1/2012 (4), ledende inspektør Jean-Paul RIKIRs mandat som missionschef for EUPOL RD Congo indtil den 30. september 2013. |
|
(5) |
Den 23. september 2013 vedtog Rådet afgørelse 2013/467/FUSP (5) om forlængelse af EUPOL RD Congo indtil den 30. september 2014. |
|
(6) |
Den 10. september 2013 foreslog den højtstående repræsentant, at ledende inspektør Jean-Paul RIKIRs mandat som missionschef for EUPOL RD Congo forlænges til den 30. september 2014. |
|
(7) |
Da ledende inspektør Jean-Paul RIKIRs indeværende mandat som missionschef for EUPOL RD Congo udløb den 30. september 2013, bør denne afgørelse anvendes fra den 1. oktober 2013 — |
VEDTAGET DENNE AFGØRELSE:
Artikel 1
Ledende inspektør Jean-Paul RIKIRs mandat som missionschef for Den Europæiske Unions politimission vedrørende reformen af sikkerhedssektoren og dens retlige grænseflade i Den Demokratiske Republik Congo (EUPOL RD Congo) forlænges herved til den 30. september 2014.
Artikel 2
Denne afgørelse træder i kraft på dagen for vedtagelsen.
Den anvendes fra den 1. oktober 2013.
Udfærdiget i Bruxelles, den 8. oktober 2013.
På Den Udenrigs- og Sikkerhedspolitiske Komités vegne
W. STEVENS
Formand
(1) EUT L 254 af 29.9.2010, s. 33.
(2) EUT L 266 af 9.10.2010, s. 60.
(3) EUT L 245 af 22.9.2011, s. 21.
(4) EUT L 264 af 29.9.2012, s. 13.
(5) EUT L 252 af 24.9.2013, s. 27.
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/67 |
KOMMISSIONENS GENNEMFØRELSESAFGØRELSE
af 17. oktober 2013
om EU-tilskud til visse medlemsstater med henblik på støtte til frivillige overvågningsundersøgelser af tab af honningbikolonier for sæsonen 2013/14
(meddelt under nummer C(2013) 6742)
(Kun den danske, den engelske, den estiske, den finske, den franske, den græske, den italienske, den lettiske, den litauiske, den nederlandske, den polske, den portugisiske, den slovakiske, den spanske, den svenske, den tyske og den ungarske udgave er autentiske)
(2013/512/EU)
EUROPA-KOMMISSIONEN HAR —
under henvisning til traktaten om Den Europæiske Unions funktionsmåde,
under henvisning til Rådets beslutning 2009/470/EF af 25. maj 2009 om visse udgifter på veterinærområdet (1), særlig artikel 23, og
ud fra følgende betragtninger:
|
(1) |
Meddelelsen fra Kommissionen til Europa-Parlamentet og Rådet om honningbiers sundhed (2) giver et overblik over de igangværende initiativer vedrørende honningbiers sundhed i EU, som Kommissionen allerede har iværksat. Hovedproblemet, der omhandles i meddelelsen, er den stigende dødelighed blandt bier på verdensplan. |
|
(2) |
I EFSA's projekt fra 2009 om biers dødelighed og tilsyn med bier i Europa (3) konkluderedes det, at overvågningssystemerne i EU generelt er svage, og at der mangler data på nationalt plan i medlemsstaterne og sammenlignelige data på EU-plan. |
|
(3) |
Med henblik på forbedring af adgangen til data om biers dødelighed besluttede Kommissionen at yde støtte til visse overvågningsundersøgelser i medlemsstaterne vedrørende tabene af honningbier. |
|
(4) |
Ved Kommissionens gennemførelsesafgørelse 2012/362/EU (4) blev der ydet tilskud til de programmer for frivillige overvågningsundersøgelser af tab af honningbikolonier, der gennemføres af Belgien, Danmark, Tyskland, Estland, Grækenland, Spanien, Frankrig, Italien, Letland, Litauen, Ungarn, Polen, Portugal, Slovakiet, Finland, Sverige og Det Forenede Kongerige for sæsonen 2012/13. |
|
(5) |
Der skal i henhold til undersøgelserne aflægges i alt tre besøg i bigårdene, dvs. inden vintersæsonen, efter vintersæsonen og i den produktive sæson. |
|
(6) |
I denne type undersøgelse er det vigtigt at have sammenlignelige data vedrørende tabene, som indsamles i forskellige år. Dette gælder især for overvågningsundersøgelser af tab af honningbikolonier, fordi de klimatiske forhold i væsentlig grad ændrer resultaterne. Hvis sådanne undersøgelser kun gennemføres i et enkelt år, giver de derfor kun delvise data, som ikke giver et tilstrækkeligt grundlag for at drage konklusioner eller aflæse tendenser vedrørende sådanne tab. |
|
(7) |
Af ovennævnte årsager er det hensigtsmæssigt at fortsætte de frivillige overvågningsundersøgelser af tab af honningbikolonier i den periode, der starter med kontrollen inden vintersæsonen i efteråret 2013, og som slutter med kontrollen efter vintersæsonen og kontrollen vedrørende hele den produktive sæson i 2014. |
|
(8) |
De undersøgelser, der skal gennemføres i sæsonen 2013/14, er baseret på dokumentet »Basis for a pilot surveillance project on honey bee colony losses« (5) fra EU-referencelaboratoriet for biers sundhed, jf. del II i bilag VII til Europa-Parlamentets og Rådets forordning (EF) nr. 882/2004 (6), som giver medlemsstaterne retningslinjer for udarbejdelse af deres respektive overvågningsundersøgelser. |
|
(9) |
De samme medlemsstater, som deltog i de første frivillige overvågningsundersøgelser af tab af honningbikolonier i 2012/13, blev opfordret til at forelægge Kommissionen deres programmer for sæsonen 2013/14 på grundlag af EU-referencelaboratoriets tekniske dokument om biers sundhed. |
|
(10) |
Belgien, Danmark, Tyskland, Estland, Grækenland, Spanien, Frankrig, Italien, Letland, Litauen, Ungarn, Polen, Portugal, Slovakiet, Finland, Sverige og Det Forenede Kongerige har udarbejdet programmer for frivillige overvågningsundersøgelser af tab af honningbikolonier i overensstemmelse med det tekniske dokument »Basis for a pilot surveillance project on honey bee colony losses« og har anmodet om EU-tilskud. |
|
(11) |
Der bør fra 1. juli 2013 ydes tilskud til de programmer for frivillige overvågningsundersøgelser af tab af honningbikolonier, der gennemføres af Belgien, Danmark, Tyskland, Estland, Grækenland, Spanien, Frankrig, Italien, Letland, Litauen, Ungarn, Polen, Portugal, Slovakiet, Finland, Sverige og Det Forenede Kongerige. |
|
(12) |
Ifølge Rådets forordning (EF) nr. 1290/2005 (7) skal veterinærforanstaltninger finansieres via den Europæiske Garantifond for Landbruget. Finanskontrollen af foranstaltningerne foretages i henhold til samme forordnings artikel 9, 36 og 37. |
|
(13) |
Udbetaling af tilskuddet bør gøres betinget af, at de påtænkte programmer for overvågningsundersøgelser rent faktisk er gennemført, og at myndighederne afgiver alle nødvendige oplysninger til Kommissionen og EU-referencelaboratoriet for biers sundhed. |
|
(14) |
Foranstaltningerne i denne afgørelse er i overensstemmelse med udtalelse fra Den Stående Komité for Fødevarekæden og Dyresundhed — |
VEDTAGET DENNE AFGØRELSE:
Artikel 1
1. Der ydes EU-tilskud til de programmer for overvågningsundersøgelser af tab af honningbikolonier, der gennemføres af Belgien, Danmark, Tyskland, Estland, Grækenland, Spanien, Frankrig, Italien, Letland, Litauen, Ungarn, Polen, Portugal, Slovakiet, Finland, Sverige og Det Forenede Kongerige.
2. EU-tilskuddet:
|
a) |
fastsættes til 70 % af hver enkelt af de i stk. 1 nævnte medlemsstaters støtteberettigede udgifter til de programmer for overvågningsundersøgelser af tab af honningbikolonier, der er anført i bilag I, i perioden 1. juli 2013 til 30. september 2014 |
|
b) |
må ikke overstige:
|
|
c) |
må ikke overstige 348 EUR pr. besøg på bigårde. |
Artikel 2
1. Det samlede tilskud, der ved denne afgørelse tillades ydet til udgifter i forbindelse med programmerne omhandlet i artikel 1, må højst udgøre 1 847 930 EUR, der finansieres over Den Europæiske Unions almindelige budget.
2. Udgifter til personale, der skal foretage laboratorieundersøgelser, prøveudtagning eller kontrol, udgifter til hjælpematerialer og generalomkostninger i forbindelse med overvågningsundersøgelserne er støtteberettigede i overensstemmelse med reglerne i bilag III.
3. EU-tilskuddet udbetales efter fremlæggelse og godkendelse af de(n) i artikel 3, stk. 2 og 3, omhandlede rapporter og dokumentation.
Artikel 3
1. Programmerne udføres i overensstemmelse med det tekniske dokument »Basis for a pilot surveillance project on honey bee colony losses« og i overensstemmelse med de programmer for overvågningsundersøgelser af tab af honningbikolonier, som medlemsstaterne har forelagt.
2. Belgien, Danmark, Tyskland, Estland, Grækenland, Spanien, Frankrig, Italien, Letland, Litauen, Ungarn, Polen, Portugal, Slovakiet, Finland, Sverige og Det Forenede Kongerige forelægger Kommissionen:
|
— |
en foreløbig teknisk rapport om det første besøg i forbindelse med programmet for overvågningsundersøgelsen senest den 1. marts 2014 |
|
— |
en endelig teknisk rapport om det andet og tredje besøg i forbindelse med programmet for overvågningsundersøgelsen senest den 31. oktober 2014 |
|
— |
den tekniske rapport skal være i overensstemmelse med en standardrapport, der udarbejdes af Kommissionen i samarbejde med EU-referencelaboratoriet for biers sundhed. |
3. Belgien, Danmark, Tyskland, Estland, Grækenland, Spanien, Frankrig, Italien, Letland, Litauen, Ungarn, Polen, Portugal, Slovakiet, Finland, Sverige og Det Forenede Kongerige forelægger Kommissionen:
|
— |
en papirudgave og en elektronisk udgave af deres økonomiske rapport, der udarbejdes i overensstemmelse med bilag II, senest den 31. december 2014 |
|
— |
på Kommissionens anmodning dokumentation for alle udgifter, der er angivet i betalingsanmodningen. |
4. Resultatet af undersøgelserne stilles til rådighed for Kommissionen og EU-referencelaboratoriet for biers sundhed.
Artikel 4
Denne afgørelse er rettet til Kongeriget Belgien, Kongeriget Danmark, Forbundsrepublikken Tyskland, Republikken Estland, Den Hellenske Republik, Kongeriget Spanien, Den Franske Republik, Den Italienske Republik, Republikken Letland, Republikken Litauen, Ungarn, Republikken Polen, Den Portugisiske Republik, Den Slovakiske Republik, Republikken Finland, Kongeriget Sverige og Det Forenede Kongerige Storbritannien og Nordirland.
Udfærdiget i Bruxelles, den 17. oktober 2013.
På Kommissionens vegne
Tonio BORG
Medlem af Kommissionen
(1) EUT L 155 af 18.6.2009, s. 30.
(2) KOM(2010) 714 endelig.
(3) Se følgende websted: http://www.efsa.europa.eu/en/efsajournal/doc/154r.pdf.
(4) Kommissionens gennemførelsesafgørelse 2012/362/EU af 4. juli 2012 om EU-tilskud til visse medlemsstater med henblik på støtte til frivillige overvågningsundersøgelser af tab af honningbikolonier (EUT L 176 af 6.7.2012, s. 65).
(5) Kan downloades fra http://ec.europa.eu/food/animal/liveanimals/bees/docs/annex_i_pilot_project_en.pdf.
(6) Europa-Parlamentets og Rådets forordning (EF) nr. 882/2004 af 29. april 2004 om offentlig kontrol med henblik på verifikation af, at foderstof- og fødevarelovgivningen samt dyresundheds- og dyrevelfærdsbestemmelserne overholdes (EUT L 165 af 30.4.2004, s. 1).
(7) Rådets forordning (EF) nr. 1290/2005 af 21. juni 2005 om finansiering af den fælles landbrugspolitik (EUT L 209 af 11.8.2005, s. 1).
BILAG I
|
Medlemsstat |
Antal bigårde |
Antal planlagte besøg pr. bigård, jf. overvågningsundersøgelsen |
Direkte omkostninger i alt (laboratorieundersøgelser + besøg med henblik på prøveudtagning og kontrol) |
Generalomkostninger (7 %) |
Samlede omkostninger |
EU-tilskud (70 %) |
|
BE |
150 |
3 |
35 830 |
2 508 |
38 338 |
26 837 |
|
DK |
200 |
3 |
155 430 |
10 880 |
166 310 |
116 417 |
|
DE |
220 |
3 |
214 212 |
14 995 |
229 207 |
160 445 |
|
EE |
196 |
3 |
86 606 |
6 062 |
92 668 |
64 868 |
|
EL |
200 |
3 |
104 701 |
7 329 |
112 030 |
78 421 |
|
ES |
203 |
3 |
197 659 |
13 836 |
211 495 |
148 047 |
|
FR |
396 |
3 |
385 581 |
26 991 |
412 572 |
288 801 |
|
IT |
195 |
3 |
189 870 |
13 291 |
203 161 |
142 212 |
|
LV |
193 |
3 |
115 234 |
8 066 |
123 300 |
86 310 |
|
LT |
193 |
3 |
93 822 |
6 568 |
100 390 |
70 273 |
|
HU |
196 |
3 |
152 483 |
10 674 |
163 157 |
114 209 |
|
PL |
190 |
3 |
170 915 |
11 964 |
182 879 |
128 015 |
|
PT |
145 |
3 |
38 930 |
2 725 |
41 655 |
29 159 |
|
SK |
200 |
3 |
123 151 |
8 621 |
131 772 |
92 240 |
|
FI |
161 |
3 |
156 764 |
10 973 |
167 737 |
117 416 |
|
SE |
150 |
3 |
99 318 |
6 952 |
106 270 |
74 389 |
|
UK |
200 |
3 |
146 691 |
10 268 |
156 959 |
109 871 |
|
I alt |
|
|
2 467 197 |
172 703 |
2 639 900 |
1 847 930 |
BILAG II
STANDARDFORMULAR TIL DEN ØKONOMISKE RAPPORT OM FRIVILLIGE OVERVÅGNINGSUNDERSØGELSER AF TAB AF HONNINGBIKOLONIER
|
Samlede projektomkostninger (faktiske udgifter, ekskl. moms) |
||
|
Medlemsstat: |
|
Antal bigårde, der er besøgt: |
|
|
|
Samlet antal kolonier, der er udtaget prøver af: |
|
Laboratorieudgifter |
|||
|
Personalekategori |
Antal arbejdsdage |
Løn pr. dag |
I alt |
|
… |
|
|
|
|
… |
|
|
|
|
|
|
|
|
|
Hjælpematerialer (beskrivelse) |
Mængde |
Pris pr. enhed |
I alt |
|
… |
|
|
|
|
… |
|
|
|
|
Udgifter til prøveudtagning og kontrol (besøg på bigårde) |
|||
|
Personalekategori |
Antal arbejdsdage |
Løn pr. dag |
I alt |
|
… |
|
|
|
|
… |
|
|
|
|
|
|
|
|
|
Hjælpematerialer (beskrivelse) |
Mængde |
Pris pr. enhed |
I alt |
|
… |
|
|
|
|
… |
|
|
|
Støttemodtagerens attestering
Vi attesterer, at:
|
— |
ovennævnte udgifter er påløbet under udførelsen af de opgaver, der er beskrevet i det tekniske dokument »Basis for a pilot surveillance project on honey bee colony losses« (1), og er direkte forbundet med gennemførelsen af det program for overvågningsundersøgelsen, som der er ydet tilskud til i henhold til Kommissionens gennemførelsesafgørelse 2013/512/EU |
|
— |
der er tale om faktisk afholdte udgifter, som er bogført korrekt og tilskudsberettigede i henhold til Kommissionens gennemførelsesafgørelse 2013/512/EU |
|
— |
alle bilag for udgifterne er til rådighed til revisionsformål |
|
— |
der ikke er anmodet om andre EU-tilskud til de projekter, der er anført i Kommissionens gennemførelsesafgørelse 2013/512/EU. |
Dato:
Den ansvarliges navn og underskrift:
(1) Kan downloades fra http://ec.europa.eu/food/animal/liveanimals/bees/docs/annex_i_pilot_project_en.pdf.
BILAG III
REGLER FOR STØTTEBERETTIGELSE
1. Laboratorieudgifter
|
— |
Personaleudgifterne må kun omfatte udgifter, der kan henføres direkte til arbejdskraften (grundløn, udgifter til social sikring og pensionsbidrag), og som er afholdt i forbindelse med gennemførelse af overvågningsundersøgelsen og laboratorieundersøgelserne. Der skal i denne forbindelse føres månedlige timesedler. |
|
— |
Lønudgifterne pr. dag beregnes på grundlag af 220 arbejdsdage pr. år. |
|
— |
Godtgørelse af udgifter til hjælpematerialer baseres på de faktiske udgifter, som medlemsstaterne har afholdt til laboratorieundersøgelserne. |
|
— |
Personaleudgifter til koordinering, planlægning og transport er ikke støtteberettigede. Udgifter til testkit, reagenser og alle hjælpematerialer godtgøres kun, hvis de er anvendt ved nedenstående undersøgelser. |
|
— |
Varroatælling (vaskning) skal gennemføres for alle kolonier, der besøges for første gang, og for symptomatiske kolonier ved de efterfølgende besøg. |
|
— |
Påvisning og karakterisering af lille stadebille (Aethina tumida) og tropilaelapsmide) — foretages i forbindelse med den kliniske undersøgelse. |
|
— |
Klinisk observation (herunder observation af symptomer på bipest, nosemasyge, virusser), sporetællinger vedrørende mikrosporidium-parasit (Nosema spp.), dyrkning, mikroskopundersøgelser og biokemiske undersøgelser med henblik på identifikation af de organismer, der forårsager europæisk bipest (Melissococcus plutonius) og amerikansk bipest (Paenibacillus larvae), på symptomatiske kolonier. |
|
— |
Amerikansk bipest — bekræftelse ved hjælp af polymerasekædereaktion (PCR) af identifikationen af de organismer, der forårsager amerikansk bipest og europæisk bipest, på symptomatiske kolonier. |
|
— |
CBPV-test (PCR) på symptomatiske kolonier. |
2. Udgifter til prøveudtagning og kontrol
|
— |
Udgifter til prøveudtagning og kontrol er kun støtteberettigede, hvis de er direkte forbundet med besøg på bigårde og er begrænset til den tid, der reelt er brugt på bigårdene. Personaleudgifterne må kun omfatte udgifter, der kan henføres direkte til arbejdskraften (grundløn, udgifter til social sikring og pensionsbidrag), og som er afholdt i forbindelse med gennemførelse af undersøgelsen. Der skal i denne forbindelse føres månedlige timesedler. |
|
— |
Personaleudgifter til koordinering, planlægning og transport er ikke støtteberettigede. |
|
— |
Lønudgifterne pr. dag beregnes på grundlag af 220 arbejdsdage pr. år. |
|
— |
Godtgørelse af udgifter til hjælpematerialer baseres på de faktiske udgifter, medlemsstaterne har afholdt, og godtgørelse finder kun sted, hvis hjælpematerialerne er blevet anvendt under besøg på bigårde. |
3. Generalomkostninger
Der kan ansøges om et engangstilskud på 7 % af alle direkte støtteberettigede udgifter.
4. De udgifter, medlemsstaterne forelægger med henblik på EU-tilskud, angives i euro eksklusive moms og andre skatter og afgifter.
RETSAKTER VEDTAGET AF ORGANER OPRETTET VED INTERNATIONALE AFTALER
|
19.10.2013 |
DA |
Den Europæiske Unions Tidende |
L 279/73 |
AFGØRELSE Nr. 1/2013 TRUFFET AF DET BLANDEDE UDVALG EU-MONACO NEDSAT VED AFTALEN MELLEM DET EUROPÆISKE FÆLLESSKAB OG FYRSTENDØMMET MONACO OM ANVENDELSE AF VISSE EF-RETSAKTER PÅ FYRSTENDØMMET MONACOS OMRÅDE
af 12. juli 2013
om ændring af bilaget til aftalen
(2013/513/EU)
DEN BLANDEDE UDVALG HAR —
under henvisning til aftalen mellem Det Europæiske Fællesskab og Fyrstendømmet Monaco om anvendelse af visse fællesskabsretsakter på Fyrstendømmet Monacos område (1) undertegnet i Bruxelles den 4. december 2003 (i det følgende »aftalen«), særlig artikel 1, stk. 1, og
ud fra følgende betragtninger:
|
(1) |
Unionen har siden aftalens ikrafttrædelse den 1. maj 2004 vedtaget en række retsakter, der hører under aftalens anvendelsesområde, og nogle retsakter, der står opført i bilaget, er ophævet. Det blandede udvalg bør derfor træffe en afgørelse for at ajourføre bilaget ved at tilføje de nye retsakter og fjerne de retsakter, som er ophævet. |
|
(2) |
Det skal erindres, at Europa-Kommissionens retsakter, som er vedtaget i henhold til de i aftalens bilag opførte retsakter, finder anvendelse på Monacos område, uden at en afgørelse fra det blandede udvalg er nødvendig, jf. aftalens artikel 1, stk. 2 — |
VEDTAGET DENNE AFGØRELSE:
Artikel 1
Teksten i bilaget til aftalen mellem Det Europæiske Fællesskab og Fyrstendømmet Monaco om anvendelse af visse fællesskabsretsakter på Fyrstendømmet Monacos område erstattes af teksten i bilaget til nærværende afgørelse.
Artikel 2
Denne afgørelse træder i kraft på dagen for vedtagelsen.
Udfærdiget i Monaco, den 12. juli 2013.
På Det Blandede Udvalgs vegne
Stéphane VALÉRI
Formand
(1) EUT L 332 af 19.12.2003, s. 42.
BILAG
»BILAG
I. LÆGEMIDLER
OMHANDLEDE RETSAKTER
|
1. |
Europa-Parlamentets og Rådets direktiv 2001/83/EF af 6. november 2001 om oprettelse af en fællesskabskodeks for humanmedicinske lægemidler, som ændret ved:
|
|
2. |
Europa-Parlamentets og Rådets forordning (EF) nr. 726/2004 af 31. marts 2004 om fastlæggelse af fællesskabsprocedurer for godkendelse og overvågning af human- og veterinærmedicinske lægemidler og om oprettelse af et europæisk lægemiddelagentur, som ændret ved:
|
|
3. |
Europa-Parlamentets og Rådets direktiv 2001/82/EF af 6. november 2001 om oprettelse af en fællesskabskodeks for veterinærlægemidler, som ændret ved:
|
|
4. |
Rådets forordning (EF) nr. 297/95 af 10. februar 1995 om fastsættelse af gebyrer til Det Europæiske Agentur for Lægemiddelvurdering, som ændret ved:
|
|
5. |
Europa-Parlamentets og Rådets forordning (EF) nr. 470/2009 af 6. maj 2009 om fællesskabsprocedurer for fastsættelse af grænseværdier for restkoncentrationer af farmakologisk virksomme stoffer i animalske fødevarer, om ophævelse af Rådets forordning (EØF) nr. 2377/90 og om ændring af Europa-Parlamentets og Rådets direktiv 2001/82/EF og Europa-Parlamentets og Rådets forordning (EF) nr. 726/2004 (EUT L 152 af 16.6.2009, s. 11). |
|
6. |
Kommissionens forordning (EF) nr. 668/2009 af 24. juli 2009 om gennemførelse af Europa-Parlamentets og Rådets forordning (EF) nr. 1394/2007 for så vidt angår vurdering og certificering af kvalitetsdata og ikke-kliniske data vedrørende lægemidler til avanceret terapi, der er udviklet af mikrovirksomheder, små og mellemstore virksomheder (EUT L 194 af 25.7.2009, s. 7). |
|
7. |
Kommissionens forordning (EU) nr. 37/2010 af 22. december 2009 om farmakologisk virksomme stoffer og disses klassifikation med hensyn til maksimalgrænseværdier for restkoncentrationer i animalske fødevarer, som ændret ved:
|
|
8. |
Kommissionens forordning (EU) nr. 488/2012 af 8. juni 2012 om ændring af Kommissionens forordning (EF) nr. 658/2007 om økonomiske sanktioner for tilsidesættelse af visse forpligtelser i forbindelse med markedsføringstilladelser udstedt i henhold til Europa-Parlamentets og Rådets forordning (EF) nr. 726/2004 (EUT L 150 af 9.6.2012, s. 68). |
|
9. |
Kommissionens forordning (EF) nr. 1234/2008 af 24. november 2008 om behandling af ændringer af betingelserne i markedsføringstilladelser for humanmedicinske lægemidler og veterinærlægemidler, som ændret ved Kommissionens forordning (EU) nr. 712/2012 af 3. august 2012 om ændring af forordning (EF) nr. 1234/2008 om behandling af ændringer af betingelserne i markedsføringstilladelser for humanmedicinske lægemidler og veterinærlægemidler (EUT L 209 af 4.8.2012, s. 4). |
|
10. |
Kommissionens gennemførelsesforordning (EU) nr. 198/2013 af 7. marts 2013 om valg af et symbol med henblik på at identificere humanmedicinske lægemidler, der er underlagt supplerende overvågning (EUT L 65 af 8.3.2013, s. 17). |
|
11. |
Europa-Parlamentets og Rådets forordning (EF) nr. 469/2009 af 6. maj 2009 om det supplerende beskyttelsescertifikat for lægemidler (EUT L 152 af 16.6.2009, s. 1). |
|
12. |
Europa-Parlamentets og Rådets direktiv 2009/35/EF af 23. april 2009 om stoffer, der må tilsættes lægemidler med henblik på farvning af disse (EUT L 109 af 30.4.2009, s. 10). |
|
13. |
Europa-Parlamentets og Rådets forordning (EF) nr. 1394/2007 af 13. november 2007 om lægemidler til avanceret terapi og om ændring af direktiv 2001/83/EF og forordning (EF) nr. 726/2004 (EUT L 324 af 10.12.2007, s. 121), som ændret ved Europa-Parlamentets og Rådets forordning (EU) nr. 1235/2010 af 15. december 2010 (EUT L 348 af 31.12.2010, s. 1). |
|
14. |
Kommissionens forordning (EF) nr. 658/2007 af 14. juni 2007 om økonomiske sanktioner for tilsidesættelse af visse forpligtelser i forbindelse med markedsføringstilladelser udstedt i henhold til Europa-Parlamentets og Rådets forordning (EF) nr. 726/2004 (EUT L 155 af 15.6.2007, s. 10). |
|
15. |
Europa-Parlamentets og Rådets forordning (EF) nr. 1901/2006 af 12. december 2006 om lægemidler til pædiatrisk brug og om ændring af forordning (EØF) nr. 1768/92, direktiv 2001/20/EF, direktiv 2001/83/EF og forordning (EF) nr. 726/2004 (EUT L 378 af 27.12.2006, s. 1), som ændret ved:
|
|
16. |
Kommissionens forordning (EF) nr. 507/2006 af 29. marts 2006 om tilladelse til markedsføring af humanmedicinske lægemidler omfattet af Europa-Parlamentets og Rådets forordning (EF) nr. 726/2004 på særlige vilkår (EUT L 92 af 30.3.2006, s. 6). |
|
17. |
Kommissionens forordning (EF) nr. 2049/2005 af 15. december 2005 om fastsættelse i henhold til Europa-Parlamentets og Rådets forordning (EF) nr. 726/2004 af regler om mikrovirksomheders og små og mellemstore virksomheders betaling af gebyrer til og modtagelse af administrativ bistand fra Det Europæiske Lægemiddelagentur (EUT L 329 af 16.12.2005, s. 4). |
|
18. |
Kommissionens direktiv 2005/28/EF af 8. april 2005 om principper og detaljerede retningslinjer for god klinisk praksis i forbindelse med testpræparater til human brug og om krav i forbindelse med tilladelse til fremstilling eller import af sådanne præparater (EUT L 91 af 9.4.2005, s. 13). |
|
19. |
Europa-Parlamentets og Rådets direktiv 2004/10/EF af 11. februar 2004 om indbyrdes tilnærmelse af lovgivning om anvendelsen af principper for god laboratoriepraksis og om kontrol med deres anvendelse ved forsøg med kemiske stoffer (EUT L 50 af 20.2.2004, s. 44), som ændret ved Europa-Parlamentets og Rådets forordning (EF) nr. 219/2009 af 11. marts 2009 (EUT L 87 af 31.3.2009, s. 109). |
|
20. |
Europa-Parlamentets og Rådets direktiv 2004/9/EF af 11. februar 2004 om inspektion og verifikation af god laboratoriepraksis (GLP) (EUT L 50 af 20.2.2004, s. 28), som ændret ved Europa-Parlamentets og Rådets forordning (EF) nr. 219/2009 af 11. marts 2009 (EUT L 87 af 31.3.2009, s. 109). |
|
21. |
Kommissionens direktiv 2003/94/EF af 8. oktober 2003 om principper og retningslinjer for god fremstillingspraksis for humanmedicinske lægemidler og testpræparater til human brug (EUT L 262 af 14.10.2003, s. 22). |
|
22. |
Rådets forordning (EF) nr. 953/2003 af 26. maj 2003 om hindring af omlægning til Den Europæiske Union af handelen med visse essentielle lægemidler (EUT L 135 af 3.6.2003, s. 5), som ændret ved:
|
|
23. |
Europa-Parlamentets og Rådets forordning (EF) nr. 141/2000 af 16. december 1999 om lægemidler til sjældne sygdomme (EFT L 18 af 22.1.2000, s. 1), som ændret ved Europa-Parlamentets og Rådets forordning (EF) nr. 596/2009 af 18. juni 2009 (EUT L 188 af 18.7.2009, s. 14). |
|
24. |
Kommissionens direktiv 91/412/EØF af 23. juli 1991 om principper og retningslinjer for god fremstillingspraksis for veterinærmedicinske præparater (EFT L 228 af 17.8.1991, s. 70). |
|
25. |
Rådets direktiv 89/105/EØF af 21. december 1988 om gennemsigtighed i prisbestemmelserne for lægemidler til mennesker og disse lægemidlers inddragelse under de nationale sygesikringsordninger (EFT L 40 af 11.2.1989, s. 8). |
|
26. |
Europa-Parlamentets og Rådets direktiv 2001/20/EF af 4. april 2001 om indbyrdes tilnærmelse af medlemsstaternes love og administrative bestemmelser om anvendelse af god klinisk praksis ved gennemførelse af kliniske forsøg med lægemidler til human brug (EUT L 121 af 1.5.2001, s. 34), som ændret ved:
|
|
27. |
Europa-Parlamentets og Rådets direktiv 2002/98/EF af 27. januar 2003 om fastsættelse af standarder for kvaliteten og sikkerheden ved tapning, testning, behandling, opbevaring og distribution af humant blod og blodkomponenter og om ændring af direktiv 2001/83/EF (EUT L 33 af 8.2.2003, s. 30) (udelukkende for så vidt angår tapning og testning af blod og blodkomponenter, der anvendes som udgangsmateriale ved fremstilling af lægemidler). |
|
28. |
Europa-Parlamentets og Rådets direktiv 2004/23/EF af 31. marts 2004 om fastsættelse af standarder for kvaliteten og sikkerheden ved donation, udtagning, testning, behandling, præservering, opbevaring og distribution af humane væv og celler (EUT L 102 af 7.4.2004, s. 48) (udelukkende for så vidt angår udtagning, donation, kodning og testning af væv og celler samt kodning af donationer og af deres emballage, der anvendes som udgangsmateriale ved fremstilling af lægemidler til avanceret terapi som omhandlet i Europa-Parlamentets og Rådets forordning (EF) nr. 1394/2007). |
II. KOSMETISKE PRODUKTER
OMHANDLEDE RETSAKTER
|
1. |
Rådets direktiv 76/768/EØF af 27. juli 1976 om indbyrdes tilnærmelse af medlemsstaternes lovgivning om kosmetiske midler (EFT L 262 af 27.9.1976, s. 169), som ændret ved:
Rådets direktiv 76/768/EØF ophæves med virkning fra den 11. juli 2013 og erstattes med: Europa-Parlamentets og Rådets forordning (EF) nr. 1223/2009 af 30. november 2009 om kosmetiske produkter (EUT L 342 af 22.12.2009, s. 59). |
|
2. |
Europa-Parlamentets og Rådets forordning (EF) nr. 1223/2009 af 30. november 2009 om kosmetiske produkter (EUT L 342 af 22.12.2009, s. 59), som ændret ved:
|
|
3. |
Kommissionens første direktiv 80/1335/EØF af 22. december 1980 om indbyrdes tilnærmelse af medlemsstaternes lovgivning om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 383 af 31.12.1980, s. 27), som ændret ved Kommissionens direktiv 87/143/EØF af 10. februar 1987 (EFT L 57 af 27.2.1987, s. 56). |
|
4. |
Kommissionens andet direktiv 82/434/EØF af 14. maj 1982 om indbyrdes tilnærmelse af medlemsstaternes lovgivning om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 185 af 30.6.1982, s. 1), som ændret ved Kommissionens direktiv 90/207/EØF af 4. april 1990 (EFT L 108 af 28.4.1990, s. 92). |
|
5. |
Kommissionens tredje direktiv 83/514/EØF af 27. september 1983 om indbyrdes tilnærmelse af medlemsstaternes lovgivning om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 291 af 24.10.1983, s. 9). |
|
6. |
Kommissionens fjerde direktiv 85/490/EØF af 11. oktober 1985 om indbyrdes tilnærmelse af medlemsstaternes lovgivning om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 295 af 7.11.1985, s. 30). |
|
7. |
Kommissionens femte direktiv 93/73/EØF af 9. september 1993 om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 231 af 14.9.1993, s. 34). |
|
8. |
Kommissionens direktiv 95/17/EF af 19. juni 1995 om gennemførelsesbestemmelser til Rådets direktiv 76/768/EØF for så vidt angår dispensation til at en eller flere bestanddele ikke opføres på den liste, der er fastsat for etikettering af kosmetiske midler (EFT L 140 af 23.6.1995, s. 26), som ændret ved:
Kommissionens direktiv 95/17/EF ophæves med virkning fra den 11. juli 2013. |
|
9. |
Kommissionens sjette direktiv 95/32/EF af 7. juli 1995 om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 178 af 28.7.1995, s. 20). |
|
10. |
Kommissionens syvende Direktiv 96/45/EF af 2. juli 1996 om analysemetoderne for kontrol af kosmetiske midlers sammensætning (EFT L 213 af 22.8.1996, s. 8). |
|
11. |
Kommissionens afgørelse af 8. maj 1996 om oprettelse af en fortegnelse og en fælles nomenklatur for bestanddele i kosmetiske produkter (EFT L 132 af 1.6.1996, s. 1), som ændret ved Kommissionens afgørelse 2006/257/EF (EUT L 97 af 5.4.2006, s. 1). |
III. MEDICINSK UDSTYR
OMHANDLEDE RETSAKTER
|
1. |
Rådets direktiv 90/385/EØF af 20. juni 1990 om indbyrdes tilnærmelse af medlemsstaternes lovgivning om aktive, implantable medicinske anordninger (EFT L 189 af 20.7.1990, s. 17), som ændret ved:
|
|
2. |
Rådets direktiv 93/42/EØF af 14. juni 1993 om medicinske anordninger (EFT L 169 af 12.7.1993, s. 1), som ændret ved:
|
|
3. |
Europa-Parlamentets og Rådets direktiv 98/79/EF af 27. oktober 1998 om medicinsk udstyr til in vitro-diagnostik (EFT L 331 af 7.12.1998, s. 1), som ændret ved:
|
|
4. |
Kommissionens beslutning 2002/364/EF af 7. maj 2002 om fælles tekniske specifikationer for medicinsk udstyr til in vitro-diagnostik (EFT L 131 af 16.5. 2002, s. 17), som ændret ved:
|
|
5. |
Kommissionens direktiv 2003/12/EF af 3. februar 2003 om omklassificering af brystimplantater i overensstemmelse med direktiv 93/42/EØF om medicinsk udstyr (EUT L 28 af 4.2.2003, s. 43). |
|
6. |
Kommissionens direktiv 2003/32/EF af 23. april 2003 om detaljerede specifikationer af kravene i Rådets direktiv 93/42/EØF med hensyn til medicinsk udstyr, der er fremstillet af animalsk væv (EUT L 105 af 26.4.2003, s. 18). |
|
7. |
Kommissionens direktiv 2005/50/EF af 11. august 2005 om omklassificering af hofte-, knæ- og skulderledsproteser i overensstemmelse med Rådets direktiv 93/42/EØF om medicinsk udstyr (EUT L 210 af 12.8.2005, s. 41). |
|
8. |
Kommissionens afgørelse 2010/227/EU af 19. april 2010 om den europæiske database for medicinsk udstyr (Eudamed) (EUT L 102 af 23.4.2010, s. 45). |
|
9. |
Kommissionens forordning (EU) nr. 207/2012 af 9. marts 2012 om elektroniske brugsanvisninger til medicinsk udstyr (EUT L 72 af 10.3.2012, s. 28). |
|
10. |
Kommissionens forordning (EU) nr. 722/2012 af 8. august 2012 om særlige krav for så vidt angår kravene i Rådets direktiv 90/385/EØF og 93/42/EØF med hensyn til aktivt, implantabelt medicinsk udstyr og medicinsk udstyr, der er fremstillet af animalsk væv (EUT L 212 af 9.8.2012, s. 3).« |