ISSN 1977-0626
Úřední věstník
Evropské unie
L 379

České vydání
Právní předpisy
Ročník 63
13. listopadu 2020
|
ISSN 1977-0626 |
||
|
Úřední věstník Evropské unie |
L 379 |
|

|
||
|
České vydání |
Právní předpisy |
Ročník 63 |
|
|
|
|
|
(1) Text s významem pro EHP. |
|
CS |
Akty, jejichž název není vyti_těn tučně, se vztahují ke každodennímu řízení záležitostí v zemědělství a obecně platí po omezenou dobu. Názvy všech ostatních aktů jsou vytištěny tučně a předchází jim hvězdička. |
II Nelegislativní akty
NAŘÍZENÍ
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/1 |
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2020/1676
ze dne 31. srpna 2020,
kterým se mění článek 25 nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí, pokud jde o barvy namíchané na přání zákazníka
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 ze dne 16. prosince 2008 o klasifikaci, označování a balení látek a směsí, o změně a zrušení směrnic 67/548/EHS a 1999/45/ES a o změně nařízení (ES) č. 1907/2006 (1), a zejména na čl. 53 odst. 1 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Nařízení (ES) č. 1272/2008 bylo změněno nařízením Komise (EU) 2017/542 (2) za účelem doplnění některých požadavků na předkládání informací týkajících se reakce na ohrožení zdraví a vložení „jednoznačného identifikátoru složení“ (UFI) do doplňujících informací uvedených na štítku nebezpečné směsi. Dovozci a následní uživatelé musí začít splňovat požadavky po etapách – podle jednotlivých dat pro dosažení souladu – v závislosti na tom, pro jaké použití je směs uváděna na trh. |
|
(2) |
Odvětví barev vyjádřilo konkrétní obavy týkající se praktického provádění požadavků na reakci na ohrožení zdraví v případě barev vyráběných v omezených množstvích na míru pro jednotlivého zákazníka nebo profesionálního uživatele v místě prodeje. Aby byla uspokojena poptávka zákazníků po velmi specifických odstínech, mohou být příslušní pracovníci požádáni, aby míchali a dodávali barvy s téměř neomezeným počtem různých složení. Dodržování požadavků na reakci na ohrožení zdraví by proto vyžadovalo, aby pracovníci buď předkládali informace a předem vytvořili identifikátory UFI pro obzvláště vysoký počet barev všech možných kombinací barev, z nichž mnohé ve skutečnosti nemusí být nikdy dodány, nebo aby odložili každou dodávku v místě prodeje až do okamžiku předložení informací a vytvoření identifikátoru UFI. Každý z těchto přístupů by nepřiměřeně zatížil odvětví barev namíchaných na přání zákazníka. |
|
(3) |
Aby se předešlo nepřiměřené administrativní zátěži, zejména pro malé a střední podniky, u barev namíchaných na přání zákazníka, je třeba požadavky změnit nařízením Komise v přenesené pravomoci (EU) 2020/1677 (3), a to s cílem umožnit u barev namíchaných na přání zákazníka výjimku z oznamovací povinnosti podle přílohy VIII nařízení (ES) č. 1272/2008 a z povinnosti vytvořit identifikátor UFI uvedené ve zmíněné příloze. Aby však toxikologická střediska mohla formulovat vhodnou reakci na ohrožení zdraví, musí jednotlivé směsi obsažené v barvách namíchaných na přání zákazníka nadále splňovat všechny požadavky přílohy VIII. |
|
(4) |
S ohledem na tuto skutečnost je vhodné změnit článek 25 nařízení (ES) č. 1272/2008 s cílem stanovit pravidlo pro barvy namíchané na přání zákazníka, u nichž se neoznamují žádné informace ani se nevytváří žádný odpovídající identifikátor UFI, což by vyžadovalo, aby se na štítku barvy namíchané na přání zákazníka uváděly identifikátory UFI všech směsí obsažených v barvě namíchané na přání zákazníka. Kromě toho, pokud je koncentrace směsi s identifikátorem UFI obsažené v barvě namíchané na přání zákazníka vyšší než 5 %, měla by být tato koncentrace zahrnuta v doplňujících informacích uvedených na štítku barvy namíchané na přání zákazníka, neboť směsi v těchto barvách o takové koncentraci jsou s větší pravděpodobností relevantní pro reakce na ohrožení zdraví. |
|
(5) |
Vzhledem k tomu, že datum, kdy musí být splněny požadavky u směsí pro spotřebitelské a profesionální použití, tj. 1. ledna 2021, stanovené v příloze VIII nařízení (ES) č. 1272/2008 se blíží a že toto nařízení umožňuje splňovat požadavky uvedené přílohy všem odvětvím, mělo by toto nařízení vstoupit v platnost co nejdříve. |
|
(6) |
Nařízení (ES) č. 1272/2008 by proto mělo být odpovídajícím způsobem změněno, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
V článku 25 nařízení (ES) č. 1272/2008 se doplňuje nový odstavec, který zní:
„8. V případě barvy namíchané na přání zákazníka, u níž nebylo předloženo žádné podání v souladu s přílohou VIII ani nebyl vytvořen žádný odpovídající jednoznačný identifikátor složení, musí být v doplňujících informacích uvedených na štítku barvy namíchané na přání zákazníka zahrnuty jednoznačné identifikátory složení všech směsí obsažených v barvě namíchané na přání zákazníka o koncentraci vyšší než 0,1 %, které samy podléhají oznamovací povinnosti podle článku 45, přičemž musí být uvedeny společně a v sestupném pořadí podle koncentrace směsí v barvě namíchané na přání zákazníka v souladu s ustanoveními přílohy VIII části A oddílu 5.
V případě, na který se vztahuje první pododstavec, pokud je koncentrace směsi s jednoznačným identifikátorem složení v barvě namíchané na přání zákazníka vyšší než 5 %, musí být v doplňujících informacích uvedených na štítku barvy namíchané na přání zákazníka rovněž zahrnuta koncentrace této směsi vedle jejího jednoznačného identifikátoru složení v souladu s přílohou VIII částí B oddílem 3.4.
Pro účely tohoto odstavce se „barvou namíchanou na přání zákazníka“ rozumí barva vyrobená v omezených množstvích na míru pro jednotlivého zákazníka nebo profesionálního uživatele v místě prodeje prostřednictvím tónování nebo mísení barev.“
Článek 2
Toto nařízení vstupuje v platnost prvním dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 31. srpna 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 353, 31.12.2008, s. 1.
(2) Nařízení Komise (EU) 2017/542 ze dne 22. března 2017, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí doplněním nové přílohy upravující harmonizované informace týkající se reakce na ohrožení zdraví (Úř. věst. L 78, 23.3.2017, s. 1).
(3) Nařízení Komise v přenesené pravomoci (EU) 2020/1677, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí v zájmu zlepšení praktického provádění požadavků na informace týkající se reakce na ohrožení zdraví (Viz strana 3 tohoto Úředního věstníku).
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/3 |
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2020/1677
ze dne 31. srpna 2020,
kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí v zájmu zlepšení praktického provádění požadavků na informace týkající se reakce na ohrožení zdraví
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 ze dne 16. prosince 2008 o klasifikaci, označování a balení látek a směsí, o změně a zrušení směrnic 67/548/EHS a 1999/45/ES a o změně nařízení (ES) č. 1907/2006 (1), a zejména na čl. 45 odst. 4 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Nařízení (ES) č. 1272/2008 bylo změněno nařízením Komise (EU) 2017/542 (2) za účelem doplnění některých požadavků na předkládání informací týkajících se reakce na ohrožení zdraví a vložení „jednoznačného identifikátoru složení“ do doplňujících informací uvedených na štítku nebezpečné směsi. Tyto požadavky byly změněny nařízením Komise v přenesené pravomoci (EU) 2020/11 (3). Dovozci a následní uživatelé musí začít splňovat požadavky po etapách – podle jednotlivých dat pro dosažení souladu – v závislosti na tom, pro jaké použití je směs uváděna na trh. |
|
(2) |
Různá průmyslová odvětví vyjádřila obavy týkající se praktického provádění požadavků na informace o reakci na ohrožení zdraví v některých případech, zejména pokud jde o obtížné zjišťování přesného složení směsí v případech, kdy jsou při výrobě směsi použity suroviny se značně variabilním nebo neznámým složením, v případech, kdy jsou toxikologicky velmi podobné složky dodávané několika různými dodavateli používány společně ve stejné výrobní lince, nebo v případech složitých dodavatelských řetězců. V případě namíchaných směsí byly rovněž vyjádřeny obavy ohledně toho, že není možné předem zjistit, jaké konkrétní namíchané směsi mají být uvedeny na trh. |
|
(3) |
Je nezbytné řešit situaci, kdy se ve směsi používají různé, avšak toxikologicky velmi podobné složky a kdy není známo, která složka je přítomna v konkrétní směsi uvedené na trh v daném okamžiku. Aby se zajistilo řádné dodržování požadavků na reakci na ohrožení zdraví v praxi, mělo by být dovozcům a následným uživatelům povoleno seskupit toxikologicky podobné složky směsi do skupiny zaměnitelných složek a poskytnout informace o celkové koncentraci těchto složek přítomných ve směsi, aniž by bylo nutné specifikovat jejich jednotlivé koncentrace. Aby mohla toxikologická střediska formulovat vhodnou reakci na ohrožení zdraví, měly by být složky seskupeny do skupiny zaměnitelných složek, pouze pokud je jejich klasifikace na základě jejich účinků na zdraví nebo fyzikálních účinků stejná a pokud jsou určení nebezpečnosti a doplňující informace o nebezpečnosti totožné pro všechny možné kombinace výsledné konečné směsi obsahující tyto složky. U složek klasifikovaných do určitých tříd nebezpečnosti by rovněž mělo být nezbytné, aby k seskupení měly stejnou technickou funkci a stejné toxikologické vlastnosti. |
|
(4) |
S cílem řešit specifické problémy týkající se odvětví sádrovce, betonu připraveného pro lití a cementu a umožnit jim splnit požadavky na reakci na ohrožení zdraví, aniž by došlo ke snížení úrovně bezpečnosti, by mělo být možné, aby informace o reakci na ohrožení zdraví týkající se některých standardizovaných směsí v rámci těchto tří odvětví byly předloženy s odkazem na standardní složení. Aby však mohla toxikologická střediska formulovat vhodnou reakci na ohrožení zdraví, měla by být tato možnost dostupná pouze v případech, kdy se klasifikace směsi nemění podle složení směsi v rozmezí koncentrací stanovených ve standardním složení a kdy jsou informace o složení alespoň stejně podrobné jako informace obsažené v bezpečnostním listu směsi sestaveném podle článku 31 nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 (4) (dále jen „bezpečnostní list“). V případě, že informace obsažené v bezpečnostním listu jsou podrobnější než informace o složení ve standardním vzorci, měli by být dovozci a následní uživatelé povinni místo toho oznámit informace v bezpečnostním listu. |
|
(5) |
V zájmu řešení konkrétních obtíží předpokládaných u některých paliv a s ohledem na skutečnost, že paliva uváděná na trh jsou obvykle v souladu s technickou normou a že toxikologická střediska oznámila nízký počet případů otravy palivy, by mělo být možné informace o reakci na ohrožení zdraví, jakož i jakékoli jiné známé informace o chemickém složení přípravků předkládat pomocí odkazu na informace obsažené v bezpečnostním listu, dokud nebude nalezeno vhodnější řešení. |
|
(6) |
Aby byla uspokojena poptávka zákazníků po velmi specifických odstínech, bývají příslušní pracovníci někdy požádáni, aby míchali a dodávali barvy na přání zákazníka v místě prodeje. Tyto barvy namíchané na přání zákazníka mohou mít téměř neomezený počet různých složení. V případě, že by nebyla přijata žádná zmírňující opatření, by dodržování požadavků na reakci na ohrožení zdraví podle přílohy VIII nařízení (ES) č. 1272/2008 tudíž vyžadovalo, aby pracovníci, kteří míchají barvy na přání zákazníka, buď předkládali informace a předem vytvořili jednoznačné identifikátory složení (UFI) pro obzvláště vysoký počet barev všech možných kombinací barev, z nichž mnohé ve skutečnosti nemusí být nikdy dodány, nebo aby odložili každou dodávku až do okamžiku předložení informací a vytvoření identifikátoru UFI. Každý z těchto přístupů by znamenal nepřiměřenou zátěž pro odvětví barev namíchaných na přání zákazníka, zejména pro malé a střední podniky, aniž by došlo ke značnému zvýšení úrovně bezpečnosti. |
|
(7) |
Toxikologická střediska neoznámila významný počet nehod souvisejících s barvami. Vzhledem k zjevně nižším rizikům ve srovnání s jinými směsmi je oprávněné umožnit pružnější přístup, neboť by to nesnížilo současnou úroveň bezpečnosti. |
|
(8) |
Je proto vhodné stanovit možnost vyjmout barvy namíchané na přání zákazníka z oznamovacích povinností podle přílohy VIII a z požadavku na vytvoření identifikátoru UFI. Aby však v takovém případě mohla toxikologická střediska formulovat vhodnou reakci na ohrožení zdraví, měly by jednotlivé směsi obsažené v barvách namíchaných na přání zákazníka nadále splňovat všechny požadavky uvedené přílohy. Vedle tohoto nařízení mění nařízení Komise v přenesené pravomoci (EU) 2020/1676 (5) článek 25 nařízení (ES) č. 1272/2008 s cílem doplnit nové pravidlo v případě barev namíchaných na přání zákazníka, u nichž nebylo předloženo žádné podání v souladu s přílohou VIII ani nebyl vytvořen žádný odpovídající identifikátor UFI, které vyžaduje, aby na štítku barvy namíchané na přání zákazníka byly uvedeny identifikátory UFI všech jednotlivých směsí obsažených v barvě namíchané na přání zákazníka, a to společně se specifickou koncentrací každé takové směsi s identifikátorem UFI obsažené v koncentraci vyšší než 5 %. |
|
(9) |
Vzhledem k počtu změn přílohy VIII nařízení (ES) č. 1272/2008 je vhodné v zájmu právní jasnosti nahradit celou přílohu. |
|
(10) |
Vzhledem k tomu, že datum, kdy musí být splněny požadavky u směsí pro spotřebitelské a profesionální použití, tj. 1. ledna 2021, stanovené v příloze VIII nařízení (ES) č. 1272/2008 se blíží a že toto nařízení umožňuje splňovat požadavky uvedené přílohy všem odvětvím, mělo by toto nařízení vstoupit v platnost co nejdříve. |
|
(11) |
Nařízení (ES) č. 1272/2008 by proto mělo být odpovídajícím způsobem změněno, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Příloha VIII nařízení (ES) č. 1272/2008 se nahrazuje zněním uvedeným v příloze tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost prvním dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 31. srpna 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 353, 31.12.2008, s. 1.
(2) Nařízení Komise (EU) 2017/542 ze dne 22. března 2017, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí doplněním nové přílohy upravující harmonizované informace týkající se reakce na ohrožení zdraví (Úř. věst. L 78, 23.3.2017, s. 1).
(3) Nařízení Komise v přenesené pravomoci (EU) 2020/11 ze dne 29. října 2019, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí, pokud jde o informace týkající se reakce na ohrožení zdraví (Úř. věst. L 6, 10.1.2020, s. 8).
(4) Nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006 o registraci, hodnocení, povolování a omezování chemických látek, o zřízení Evropské agentury pro chemické látky, o změně směrnice 1999/45/ES a o zrušení nařízení Rady (EHS) č. 793/93, nařízení Komise (ES) č. 1488/94, směrnice Rady 76/769/EHS a směrnic Komise 91/155/EHS, 93/67/EHS, 93/105/ES a 2000/21/ES (Úř. věst. L 396, 30.12.2006, s. 1).
(5) Nařízení Komise v přenesené pravomoci (EU) 2020/1676 ze dne 31. srpna 2020, kterým se mění článek 25 nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 o klasifikaci, označování a balení látek a směsí, pokud jde o barvy namíchané na přání zákazníka (viz strana 1 v tomto čísle Úředního věstníku).
PŘÍLOHA
„PŘÍLOHA VIII
HARMONIZOVANÉ INFORMACE TÝKAJÍCÍ SE REAKCE NA OHROŽENÍ ZDRAVÍ A PREVENTIVNÍCH OPATŘENÍ
ČÁST A
OBECNÉ POŽADAVKY
1. POUŽITÍ
|
1.1. |
Dovozci a následní uživatelé, kteří uvádějí na trh směsi pro spotřebitelské použití ve smyslu oddílu 2.4 části A této přílohy, musí splňovat požadavky této přílohy ode dne 1. ledna 2021. |
|
1.2. |
Dovozci a následní uživatelé, kteří uvádějí na trh směsi pro profesionální použití ve smyslu oddílu 2.4 části A této přílohy, musí splňovat požadavky této přílohy ode dne 1. ledna 2021. |
|
1.3. |
Dovozci a následní uživatelé, kteří uvádějí na trh směsi pro průmyslové použití nebo směsi, jejichž konečné použití nepodléhá oznamování ve smyslu oddílu 2.4 části A této přílohy, musí splňovat požadavky této přílohy ode dne 1. ledna 2024. |
|
1.4. |
Od dovozců a následných uživatelů, kteří předložili subjektu určenému podle čl. 45 odst. 1 informace týkající se nebezpečných směsí, jež nejsou v souladu s touto přílohou, před daty použitelnosti uvedenými v oddílech 1.1, 1.2 a 1.3, se do 1. ledna 2025 nepožaduje, aby dodržovali ustanovení této přílohy, pokud jde o tyto směsi. |
|
1.5. |
Odchylně od oddílu 1.4 platí, že pokud jedna ze změn popsaných v oddíle 4.1 části B této přílohy nastane před 1. lednem 2025, dovozci a následní uživatelé musí splnit požadavky této přílohy před uvedením dané směsi v pozměněné podobě na trh. |
2. ÚČEL, OBLAST PŮSOBNOSTI A DEFINICE
|
2.1. |
Tato příloha stanoví požadavky, jež musí dovozci a následní uživatelé, kteří uvádějí směsi na trh (dále jen „předkladatelé“), plnit, pokud jde o předkládání informací, aby měly určené subjekty k dispozici informace nezbytné k plnění úkolů, za které jsou odpovědné podle článku 45. |
|
2.2. |
Tato příloha se nevztahuje na směsi pro vědecký výzkum a vývoj a na směsi pro výzkum a vývoj zaměřený na výrobky a postupy vymezený v čl. 3 bodě 22 nařízení (ES) č. 1907/2006.
Tato příloha se nevztahuje na směsi klasifikované pouze pro jednu nebo více z těchto nebezpečností:
|
|
2.2a |
V případě barev namíchaných na přání zákazníka mohou předkladatelé, aniž je dotčen čl. 25 odst. 8, rozhodnout, že nepředloží informace a nevytvoří jednoznačný identifikátor složení podle této přílohy. |
|
2.3. |
V případě směsí, jejichž konečné použití nepodléhá oznamování, nebo směsí uváděných na trh pouze pro průmyslové použití mohou předkladatelé jako alternativu k obecným požadavkům na podání v souladu s druhým pododstavcem oddílu 3.1. části B zvolit omezené podání za předpokladu, že je zajištěn rychlý přístup k doplňujícím podrobným informacím o výrobku v souladu s oddílem 1.3 uvedené části. |
|
2.4. |
Pro účely této přílohy se použijí následující definice:
|
3. POŽADAVKY NA PODÁNÍ
|
3.1. |
Před uvedením směsí na trh musí předkladatelé poskytnout informace týkající se směsí klasifikovaných jako nebezpečné na základě jejich účinků na zdraví nebo fyzikálních účinků subjektům určeným podle čl. 45 odst. 1 (dále jen „určené subjekty“) v členském státě nebo členských státech, v nichž je směs uváděna na trh.
Podání musí obsahovat informace stanovené v části B. Musí být předloženo elektronicky ve formátu XML, který bezplatně poskytne agentura. |
|
3.2. |
Pokud po přijetí podání podle oddílu 3.1 určený subjekt vznese vůči předkladateli odůvodněný požadavek, že pro splnění úkolů, za které je určený subjekt odpovědný podle článku 45, potřebuje doplňující informace nebo vysvětlení, musí předkladatel tyto nezbytné informace nebo vysvětlení poskytnout bez zbytečného prodlení. |
|
3.3. |
Nestanoví-li dotčený členský stát nebo dotčené členské státy jinak, podání se předkládá v úředním jazyce nebo úředních jazycích členského státu či členských států, v nichž je směs uváděna na trh. |
|
3.4. |
Zamýšlené použití směsi musí být popsáno v souladu s harmonizovaným systémem kategorizace výrobků poskytnutým agenturou. |
|
3.5. |
Pokud jsou splněny podmínky stanovené v oddíle 4.1 části B, musí být bez zbytečného prodlení provedena aktualizace podání. |
4. SKUPINOVÉ PODÁNÍ
|
4.1. |
V případě, že všechny směsi v dané skupině mají tutéž klasifikaci nebezpečnosti pro zdraví a fyzikální nebezpečnosti, může být předloženo pro více než jednu směs jediné podání. Toto podání se označuje jako „skupinové podání“. |
|
4.2. |
Skupinové podání je přípustné, pouze pokud všechny směsi ve skupině obsahují stejné složky (jak je uvedeno v oddíle 3.2 části B) a u každé složky je uvedené rozmezí koncentrace stejné pro všechny směsi (jak je uvedeno v oddíle 3.4 části B). |
|
4.3. |
Odchylně od oddílu 4.2 je skupinové podání přípustné rovněž v případě, že se rozdílné složení různých směsí ve skupině týká pouze parfémů, a to za předpokladu, že celková koncentrace různých parfémů obsažených v každé směsi nepřekračuje 5 %. |
|
4.4. |
V případě skupinového podání se informace požadované v části B v příslušném případě poskytnou pro každou ze směsí zastoupených v dané skupině. |
5. JEDNOZNAČNÝ IDENTIFIKÁTOR SLOŽENÍ (UFI)
|
5.1. |
Předkladatel vytvoří jednoznačný identifikátor složení (dále jen „UFI“), a to elektronickými prostředky, které poskytne agentura. UFI je jedinečný alfanumerický kód, který předložené informace týkající se složení směsi nebo skupiny směsí jednoznačně přiřazuje ke konkrétní směsi nebo skupině směsí. Přidělení UFI je bezplatné.
Pokud změna ve složení směsi nebo skupiny směsí splňuje jednu nebo více podmínek uvedených v písmenech a), b) a c) čtvrté odrážky oddílu 4.1 části B, nebo případně jednu či více podmínek stanovených ve druhém pododstavci uvedeného oddílu, musí být vytvořen nový identifikátor UFI. Odchylně od druhého pododstavce tohoto oddílu se nový identifikátor UFI nevyžaduje u směsí uvedených ve skupinovém podání, které obsahují parfémy, a to za předpokladu, že se změna složení týká pouze těchto parfémů nebo přidání nových parfémů. Odchylně od druhého pododstavce tohoto oddílu se nový identifikátor UFI nevyžaduje, pokud se změna splňující podmínku uvedenou v písmeni a) čtvrté odrážky prvního pododstavce oddílu 4.1 části B týká výhradně jedné nebo více složek seskupených do skupiny zaměnitelných složek, které již byly zahrnuty do podání v souladu s oddílem 3.5 části B. |
|
5.2. |
Před identifikátorem UFI musí být velkými písmeny uvedena zkratka „UFI“ následovaná dvojtečkou („UFI:“) a identifikátor musí být jasně viditelný, čitelný a nesmazatelný. |
|
5.3. |
Předkladatel se může rozhodnout, že místo toho, aby identifikátor UFI zahrnul do doplňujících informací na štítku, natiskne nebo připevní identifikátor UFI na vnitřní obal umístěný u ostatních prvků označení.
Pokud má vnitřní obal takový tvar nebo je tak malý, že na něj identifikátor UFI nelze umístit, může předkladatel natisknout nebo připevnit identifikátor UFI umístěný u ostatních prvků označení na vnější obal. V případě směsí, které nejsou baleny, se identifikátor UFI uvede v bezpečnostním listu nebo se případně uvede v kopii prvků označení uvedených v čl. 29 odst. 3. V případě balených směsí dodávaných k použití v průmyslových areálech může předkladatel místo toho, aby identifikátor UFI zahrnul do informací na štítku nebo na obalu, rozhodnout o jeho uvedení v bezpečnostním listu. |
6. FORMÁTY A TECHNICKÁ PODPORA PRO PŘEDKLÁDÁNÍ INFORMACÍ
|
6.1. |
Agentura specifikuje, provozuje a aktualizuje generátor UFI, formáty XML pro podání a harmonizovaný systém kategorizace výrobků a bezplatně je zpřístupňuje na svých internetových stránkách. |
|
6.2. |
Agentura poskytuje vědecké a technické poradenství, technickou podporu a nástroje usnadňující předkládání informací. |
ČÁST B
INFORMACE OBSAŽENÉ V PODÁNÍ
1. IDENTIFIKACE SMĚSI A PŘEDKLADATELE
1.1. Identifikátor výrobku pro směs
Identifikátor výrobku se uvede v souladu s čl. 18 odst. 3 písm. a).
Uvede se úplný obchodní název směsi, včetně, v příslušném případě, obchodní značky (obchodních značek), názvu výrobku a alternativních názvů, jak jsou uvedeny na štítku, bez zkratek a tak, aby umožňovaly její konkrétní identifikaci.
Kromě toho musí podání obsahovat identifikátor či identifikátory UFI.
1.2. Údaje o předkladateli a kontaktním místě
Musí být uvedeno jméno/název, úplná adresa, telefonní číslo a e-mailová adresa předkladatele, a pokud se liší, jméno/název, úplná adresa, telefonní číslo a e-mailová adresa kontaktního místa, které se má použít pro získání dalších informací relevantních z hlediska reakce na ohrožení zdraví.
1.3. Jméno (název), telefonní číslo a e-mailová adresa pro rychlý přístup k doplňujícím informacím o výrobku
V případě omezeného podání podle oddílu 2.3 části A musí být uvedeno jméno/název, telefonní číslo a e-mailová adresa, kde je k dispozici rychlý přístup k podrobným doplňujícím informacím o výrobku relevantním z hlediska reakce na ohrožení zdraví v jazyce uvedeném v oddíle 3.3 části A. Uvedené telefonní číslo musí být dostupné 24 hodin denně, 7 dní v týdnu.
2. IDENTIFIKACE NEBEZPEČNOSTI A DOPLŇUJÍCÍ INFORMACE
V tomto oddíle jsou stanoveny požadavky na informace týkající se nebezpečnosti pro zdraví a fyzikální nebezpečnosti dané směsi a příslušné varovné informace související s touto nebezpečností, jakož i doplňující informace, které mají být obsaženy v podání.
2.1. Klasifikace směsi
Klasifikace směsi z hlediska nebezpečnosti pro zdraví a fyzikální nebezpečnosti (třída a kategorie nebezpečnosti a standardní věty o nebezpečnosti) musí být uvedena v souladu s klasifikačními pravidly stanovenými v příloze I.
2.2. Prvky označení
V příslušném případě se uvedou tyto prvky označení požadované v souladu s článkem 17:
|
— |
kódy výstražných symbolů nebezpečnosti (příloha V), |
|
— |
signální slovo, |
|
— |
kódy standardních vět o nebezpečnosti (příloha III, včetně doplňujících informací o nebezpečnosti), |
|
— |
kódy pokynů pro bezpečné zacházení (příloha IV). |
2.3. Toxikologické informace
Podání musí obsahovat informace o toxikologických účincích dané směsi nebo jejích složek, které jsou vyžadovány v oddíle 11 bezpečnostního listu směsi v souladu s přílohou II nařízení (ES) č. 1907/2006.
2.4. Doplňující informace
Musí být uvedeny tyto doplňující informace:
|
— |
druh(y) a velikost(i) obalů používaných k uvádění směsi na trh pro spotřebitelské nebo profesionální použití, |
|
— |
barva (barvy) a skupenství směsi ve stavu, ve kterém se dodává, |
|
— |
je-li k dispozici, hodnota pH směsi ve stavu, ve kterém se dodává, nebo, je-li výrobek v tuhém skupenství, hodnota pH vodné kapaliny nebo roztoku v dané koncentraci. Uvede se koncentrace zkušební směsi ve vodě. Není-li hodnota pH k dispozici, uvedou se důvody, |
|
— |
kategorie výrobku (viz oddíl 3.4 části A), |
|
— |
použití (spotřebitelské, profesionální, průmyslové nebo jejich libovolná kombinace). |
3. INFORMACE TÝKAJÍCÍ SE SLOŽEK SMĚSI
3.1. Obecné požadavky
V podání musí být uvedena chemická identifikace a koncentrace složek obsažených ve směsi v souladu s oddíly 3.2, 3.3 a 3.4.
Odchylně od prvního pododstavce mohou být v případě omezeného podání podle oddílu 2.3 části A informace, které mají být předloženy v souvislosti se složením směsi pro průmyslové použití nebo směsi, jejíž konečné použití nepodléhá oznamování, omezeny na informace obsažené v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006 za předpokladu, že jsou v případě ohrožení v souladu s oddílem 1.3 na vyžádání rychle dostupné doplňující informace týkající se složení.
Složky, které nejsou ve směsi přítomny, se neoznamují. Pokud jsou však oznámeny jako součást skupiny zaměnitelných složek podle oddílu 3.5 nebo pokud jejich koncentrace byla uvedena jako rozmezí procentních podílů v souladu s oddíly 3.6 nebo 3.7, mohou být oznámeny, jestliže budou v určitém okamžiku ve směsi jistě přítomny.
Odchylně od třetího pododstavce musí být v rámci skupinového podání v alespoň jedné ze směsí přítomny složky parfému.
V případě skupinových podání, v nichž se parfémy v jednotlivých směsích zastoupených v dané skupině liší, musí být předložen seznam těchto směsí a parfémů, které obsahují, včetně jejich klasifikace.
3.2. Identifikace složek směsi
Složka směsi je buď látka, nebo směs ve směsi.
3.2.1. Látky
Identifikátor výrobku musí být v případě látek identifikovaných podle oddílu 3.3 uveden v souladu s čl. 18 odst. 2. Lze nicméně použít název INCI, název podle colour index nebo jiný mezinárodní chemický název, pokud je příslušný chemický název dobře znám a jednoznačně definuje identitu látky. Musí být uveden rovněž chemický název látek, pro něž byl povolen alternativní chemický název podle článku 24.
3.2.2. Směs ve směsi
Pokud je směs použita ve složení jiné směsi uvedené na trh, označuje se první směs jako směs ve směsi (dále jen „MIM“).
Informace o látkách obsažených v MIM se poskytují v souladu s kritérii uvedenými v oddíle 3.2.1, kromě situace, kdy předkladatel nemá přístup k informacím ohledně úplného složení MIM. V takovém případě,
|
a) |
pokud byl pro MIM vytvořen identifikátor UFI a určený subjekt obdržel informace o MIM v předchozím podání, identifikuje se MIM pomocí jejího identifikátoru výrobku podle čl. 18 odst. 3 písm. a) a prostřednictvím její koncentrace a UFI; |
|
b) |
pokud byl pro MIM vytvořen identifikátor UFI, avšak určený subjekt neobdržel informace o MIM v předchozím podání, identifikuje se MIM pomocí jejího identifikátoru výrobku podle čl. 18 odst. 3 písm. a) a prostřednictvím její koncentrace a UFI a informací o složení MIM uvedených v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006 a všech dalších známých složkách, jakož i jména/názvu, e-mailové adresy a telefonního čísla dodavatele MIM; |
|
c) |
pokud není k dispozici identifikátor UFI, identifikuje se MIM pomocí jejího identifikátoru výrobku podle čl. 18 odst. 3 písm. a) a prostřednictvím její koncentrace a informací o složení MIM uvedených v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006 a všech dalších známých složkách, jakož i jména/názvu, e-mailové adresy a telefonního čísla dodavatele MIM. |
3.2.3. Identifikace pomocí obecných identifikátorů složky
Odchylně od oddílů 3.2.1 a 3.2.2 lze pro složky směsi používané výhradně k přidání parfémů nebo barviv použít obecné identifikátory složky „parfémy“ nebo „barviva“, jsou-li splněny tyto podmínky:
|
— |
složky směsi nejsou klasifikovány pro žádnou nebezpečnost pro zdraví, |
|
— |
koncentrace složek směsi identifikovaných daným obecným identifikátorem složky celkově nepřesahuje:
|
3.3. Složky směsi, na něž se vztahují požadavky na předkládání informací
Uvádějí se tyto složky směsi:
|
1) |
složky směsi klasifikované jako nebezpečné na základě svých účinků na zdraví nebo fyzikálních účinků, které:
|
|
2) |
složky směsi, které nejsou klasifikovány jako nebezpečné na základě svých účinků na zdraví nebo fyzikálních účinků a jsou identifikovány a přítomny v koncentracích rovnajících se nebo vyšších než 1 %. |
3.4. Koncentrace a rozmezí koncentrace složek směsi
Předkladatelé poskytnou informace stanovené v oddílech 3.4.1 a 3.4.2 týkající se koncentrace složek směsi identifikovaných v souladu s oddílem 3.3.
3.4.1. Nebezpečné složky se zásadním významem z hlediska reakce na ohrožení zdraví a preventivní opatření
Pokud jsou složky směsi klasifikovány v souladu s tímto nařízením v minimálně jedné z kategorií nebezpečnosti uvedených níže, jejich koncentrace ve směsi se vyjádří jako přesný procentní podíl, a to v sestupném pořadí podle hmotnosti nebo objemu:
|
— |
akutní toxicita, kategorie 1, 2 nebo 3, |
|
— |
toxicita pro specifické cílové orgány – jednorázová expozice kategorie 1 nebo 2, |
|
— |
toxicita pro specifické cílové orgány – opakovaná expozice kategorie 1 nebo 2, |
|
— |
žíravost pro kůži, kategorie 1, 1 A, 1 B nebo 1C, |
|
— |
vážné poškození očí, kategorie 1. |
Jako alternativa k uvedení přesných procentních podílů koncentrací může být uvedeno rozmezí procentních podílů v souladu s tabulkou 1.
Tabulka 1
Rozmezí koncentrací platná pro nebezpečné složky se zásadním významem z hlediska reakce na ohrožení zdraví
|
Rozmezí koncentrace nebezpečné složky obsažené ve směsi (%) |
Maximální rozsah rozmezí koncentrace, který může být použit v podání: |
|
≥ 25 – < 100 |
5 % jednotkových |
|
≥ 10 – < 25 |
3 % jednotkových |
|
≥ 1 – < 10 |
1 % jednotkových |
|
≥ 0,1 – < 1 |
0,3 % jednotkových |
|
> 0 – < 0,1 |
0,1 % jednotkových |
3.4.2. Jiné nebezpečné složky a složky, které nejsou klasifikovány jako nebezpečné
Koncentrace nebezpečných složek ve směsi, které nejsou klasifikovány v žádné z kategorií nebezpečnosti uvedených v oddíle 3.4.1, a identifikovaných složek, které nejsou klasifikovány jako nebezpečné, se vyjádří v souladu s tabulkou 2 jako rozmezí procentních podílů v sestupném pořadí podle hmotnosti nebo objemu. Alternativně lze uvést přesné procentní podíly.
Tabulka 2
Rozmezí koncentrací platná pro ostatní nebezpečné složky a složky, které nejsou klasifikovány jako nebezpečné
|
Rozmezí koncentrace složky obsažené ve směsi (%) |
Maximální rozsah rozmezí koncentrace, který může být použit v podání: |
|
≥ 25 – < 100 |
20 % jednotkových |
|
≥ 10 – < 25 |
10 % jednotkových |
|
≥ 1 – < 10 |
3 % jednotkových |
|
> 0 – < 1 |
1 % jednotkových |
Odchylně od prvního pododstavce se v případě složek parfémů v rámci skupinového podání, které nejsou klasifikovány nebo jsou klasifikovány jen pro senzibilizaci kůže kategorie 1, 1 A nebo 1B nebo pro toxicitu při vdechnutí, se od předkladatelů nevyžaduje poskytnutí informací o jejich koncentraci.
3.5. Seskupování složek do skupiny zaměnitelných složek
Složky mohou být v podání seskupeny do skupiny zaměnitelných složek, jestliže:
|
a) |
u všech složek ve skupině zaměnitelných složek
|
|
b) |
u všech možných kombinací výsledné konečné směsi na základě složek ve skupině zaměnitelných složek jsou identifikace nebezpečnosti a doplňující informace uvedené v oddíle 2 části B stejné. |
Alternativně mohou být složky, které jsou klasifikovány jen pro žíravost pro kůži, dráždivost pro kůži, poškození očí, podráždění očí, toxicitu při vdechnutí nebo senzibilizaci dýchacích cest nebo kůže nebo jejich kombinaci, seskupeny do skupiny zaměnitelných složek, jestliže:
|
a) |
klasifikace z hlediska nebezpečnosti pro zdraví a fyzikální nebezpečnosti (třída a kategorie nebezpečnosti) je stejná u všech složek a |
|
b) |
případně je pH všech složek klasifikovaných pro žíravost pro kůži, dráždivost pro kůži, poškození očí nebo podráždění očí buď kyselé, nebo neutrální, nebo zásadité a |
|
c) |
skupina zaměnitelných složek neobsahuje více než pět složek a |
|
d) |
u všech možných kombinací výsledné konečné směsi na základě složek seskupených do skupiny zaměnitelných složek jsou identifikace nebezpečnosti a doplňující informace uvedené v oddíle 2 části B stejné. |
3.5.1. Název skupiny zaměnitelných složek a identifikace seskupených složek
Skupina zaměnitelných složek se označení názvem, který odpovídá technické funkci (funkcím) seskupených složek, pro niž (něž) byly začleněny do směsi.
Každá složka ve skupině zaměnitelných složek je v příslušném případě identifikována v souladu s oddílem 3.2.1 nebo 3.2.2.
3.5.2. Koncentrace a rozmezí koncentrace seskupených složek
Odchylně od prvního pododstavce oddílu 3.4 u složek seskupených do skupiny zaměnitelných složek poskytnou předkladatelé informace stanovené v oddílech 3.4.1 a 3.4.2 týkající se celkové koncentrace všech složek přítomných ve směsi a seskupených do skupiny zaměnitelných složek.
Pokud jsou složky směsi seskupené do skupiny zaměnitelných složek klasifikovány v souladu s tímto nařízením pro alespoň jednu z kategorií nebezpečnosti uvedených v oddíle 3.4.1, vyjádří se celková koncentrace složek přítomných ve směsi a seskupených do skupiny zaměnitelných složek jako přesné procentní podíly, a to v sestupném pořadí podle hmotnosti nebo objemu. Jako alternativa může být uvedeno rozmezí procentních podílů v souladu s tabulkou 1 uvedeného oddílu.
Celková koncentrace nebezpečných složek přítomných ve směsi a seskupených do skupiny zaměnitelných složek, které nejsou klasifikovány pro žádnou z kategorií nebezpečnosti uvedených v oddíle 3.4.1, a celková koncentrace identifikovaných složek přítomných ve směsi a seskupených do skupiny zaměnitelných složek, které nejsou klasifikovány jako nebezpečné, se vyjádří v souladu s tabulkou 2 oddílu 3.4.2 jako rozmezí procentních podílů v sestupném pořadí podle hmotnosti nebo objemu. Alternativně lze uvést přesné procentní podíly.
3.6. Směsi splňující standardní vzorce
Odchylně od oddílů 3.2, 3.3 a 3.4 u směsi se složením, které je v souladu se standardním vzorcem uvedeným v části D, pokud se klasifikace směsi nemění v závislosti na koncentraci složek v rozmezí procentních podílů uvedených v odpovídajícím standardním vzorci:
|
— |
jestliže informace o složení ve standardním vzorci společně s informacemi uvedenými v oddílech 3.2 až 3.4 o identifikaci a koncentraci složek, které nejsou uvedeny ve standardním vzorci, nejsou méně podrobné než informace uvedené v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006, může být identifikace a koncentrace jedné nebo více složek směsi předložena podle standardního vzorce pro složky uvedené v tomto vzorci a podle oddílů 3.2 až 3.4 pro ostatní složky, |
|
— |
jestliže informace uvedené v předchozí odrážce jsou méně podrobné než informace uvedené v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006, uvedou se informace o identifikaci a koncentraci všech složek směsi uvedené v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006. |
3.7. Paliva
Odchylně od oddílů 3.2, 3.3 a 3.4 může být u paliv uvedených v tabulce 3 předložena identifikace a koncentrace složek směsi obsažené v bezpečnostním listu podle přílohy II nařízení (ES) č. 1907/2006. Předloží se rovněž identifikace a koncentrace všech dalších známých složek.
Tabulka 3
Seznam paliv
|
Palivo |
Popis výrobku |
|
Benzin EN228 |
Motorová paliva – bezolovnatý benzin |
|
Benzin E85 |
Motorová paliva – motorové palivo ethanol (E85) |
|
Alkylátový benzin |
Pohonné hmoty – zvláštní benzin pro pohonná zařízení |
|
Zkapalněný ropný plyn (LPG) |
Zkapalněný ropný plyn používaný jako palivo |
|
Zkapalněný zemní plyn (LNG) |
Zkapalněný zemní plyn používaný jako palivo |
|
Motorová nafta |
Motorová paliva – paliva pro naftové motory s biopalivem/bez biopaliva |
|
Parafinická naftová paliva (např. GTL, BTL nebo HVO) |
Motorová paliva – parafinické naftové palivo získané syntézou nebo hydrorafinací |
|
Topné oleje |
Kapalná nerostná paliva s vlastnostmi topného oleje pro použití v domácnosti |
|
Diesel MK 1 |
Motorová paliva – naftové palivo environmentální třídy 1 a 2 pro rychloběžné vznětové motory |
|
Letecká paliva |
Paliva pro letecké turbínové motory a pístové motory |
|
Petrolej – parafin ke svícení |
Parafin ke svícení olej do lamp typu B a C |
|
Těžký topný olej |
Všechny třídy těžkého topného oleje |
|
Lodní palivo |
Lodní paliva, též obsahující bionaftu |
|
Methylestery mastných kyselin (FAME) – Diesel B100 |
Methylestery mastných kyselin (FAME) pro použití ve vznětových motorech a v topení |
3.8. Klasifikace složek směsi
Uvede se klasifikace na základě zdravotních a fyzikálních účinků (třídy nebezpečnosti, kategorie nebezpečnosti a standardní věty o nebezpečnosti) látek identifikovaných v souladu s oddílem 3.3 a obsažených ve směsi. To zahrnuje klasifikaci minimálně všech látek uvedených podle oddílu 3.2.1 přílohy II nařízení (ES) č. 1907/2006 v bezpečnostním listu směsi a v bezpečnostním listu všech MIM obsažených ve směsi. U MIM identifikovaných v souladu s oddílem 3.3, u nichž předkladatel nemá přístup k úplnému složení MIM, se kromě toho uvede klasifikace na základě zdravotních a fyzikálních účinků MIM.
4. AKTUALIZACE PODÁNÍ
4.1. Podmínky aktualizace podání
Pokud dojde u směsi v rámci jednotlivého nebo skupinového podání k jedné z následujících změn, poskytnou předkladatelé před uvedením dané směsi v pozměněné podobě na trh aktualizaci podání:
|
— |
v případě změny identifikátoru výrobku pro směs nebo UFI, |
|
— |
v případě změny klasifikace směsi z hlediska nebezpečnosti pro zdraví a fyzikální nebezpečnosti, |
|
— |
v případě, že jsou k dispozici nové toxikologické informace o nebezpečných vlastnostech dané směsi nebo jejích složek, jež jsou požadovány v oddíle 11 bezpečnostního listu, |
|
— |
v případě, že změna složení směsi splňuje jednu z těchto podmínek:
|
Odchylně od čtvrté odrážky prvního pododstavce platí následující:
|
a) |
aktualizace podání u směsí se složením, které je v souladu s jakýmkoli standardním vzorcem uvedeným v části D, se vyžaduje, pouze pokud se složení směsi změní tak, že již není v souladu se standardním vzorcem; |
|
b) |
u směsí, u nichž jsou informace o složení poskytnuty na základě bezpečnostního listu v souladu s oddílem 3.6 nebo 3.7, se vyžaduje aktualizace podání v případě, že je aktualizován oddíl 3 bezpečnostního listu. Tabulka 4 Změny koncentrace složek, které vyžadují aktualizaci podání
|
Pokud dojde ve skupinovém podání ke změně, pokud jde o parfémy, musí být aktualizován seznam směsí a parfémů, které obsahují, jak je vyžadováno v oddíle 3.1.
4.2. Obsah aktualizace podání
Aktualizace podání musí obsahovat revidovanou verzi předchozího podání, v níž jsou uvedeny nové dostupné informace, jak je popsáno v oddíle 4.1.
ČÁST C
FORMÁT PRO PŘEDKLÁDÁNÍ INFORMACÍ
1. FORMÁT PRO PŘEDKLÁDÁNÍ INFORMACÍ
1.1. Formát pro předkládání informací
Předložení informací určeným subjektům v souladu s článkem 45 musí být ve formátu, který poskytne agentura. Formát pro předkládání informací musí obsahovat tyto prvky:
1.2. Identifikace směsi, předkladatele a kontaktního místa
Identifikátor výrobku
|
— |
úplný obchodní název výrobku (v případě skupinového podání musí být uvedeny všechny identifikátory výrobku), |
|
— |
jiné názvy, synonyma, |
|
— |
jednoznačný identifikátor/jednoznačné identifikátory složení (UFI), |
|
— |
jiné identifikátory (číslo povolení, kódy výrobku společnosti). |
Kontaktní údaje předkladatele a kontaktního místa
|
— |
jméno/název, |
|
— |
úplná adresa, |
|
— |
telefonní číslo, |
|
— |
e-mailová adresa. |
Kontaktní údaje pro rychlý přístup k doplňujícím informacím o výrobku (24 hodin denně, 7 dní v týdnu). Pouze pro omezené podání.
|
— |
jméno/název, |
|
— |
telefonní číslo (dostupné 24 hodin denně, 7 dní v týdnu), |
|
— |
e-mailová adresa. |
1.3. Klasifikace směsi, prvky označení a toxikologické informace
Klasifikace směsi a prvky označení
|
— |
třída a kategorie nebezpečnosti, |
|
— |
kódy výstražných symbolů nebezpečnosti (příloha V), |
|
— |
signální slovo, |
|
— |
kódy standardních vět o nebezpečnosti včetně doplňujících informací o nebezpečnosti (příloha III), |
|
— |
kódy pokynů pro bezpečné zacházení (příloha IV). |
Toxikologické informace
|
— |
popis toxicity dané směsi nebo jejích složek (jak je vyžadováno v oddíle 11 bezpečnostního listu v souladu s přílohou II nařízení č. 1907/2006). |
Doplňující informace o směsi
|
— |
barva (barvy), |
|
— |
je-li k dispozici, hodnota pH směsi ve stavu, ve kterém se dodává, nebo, je-li směs v tuhém skupenství, hodnota pH vodné kapaliny nebo roztoku v dané koncentraci. Uvede se koncentrace zkušební směsi ve vodě. Není-li hodnota pH k dispozici, uvedou se důvody, |
|
— |
skupenství, |
|
— |
obal (typ (typy) a velikost (velikosti)), |
|
— |
zamýšlené použití (kategorie výrobku), |
|
— |
použití (spotřebitelské, profesionální, průmyslové). |
1.4. Informace týkající se složek směsi a skupin zaměnitelných složek
Identifikace složek směsi
|
— |
chemický/obchodní název složek, |
|
— |
číslo CAS (v příslušném případě), |
|
— |
číslo ES (v příslušném případě), |
|
— |
UFI (v příslušném případě). |
Název skupin zaměnitelných složek (v příslušných případech)
Koncentrace a rozmezí koncentrace složek směsi
|
— |
přesné koncentrace nebo rozmezí koncentrace. |
Klasifikace složek směsi
|
— |
klasifikace nebezpečnosti (v příslušném případě), |
|
— |
další identifikátory (v příslušném případě, pokud jsou relevantní pro reakci v oblasti zdraví). |
Seznam podle pátého pododstavce oddílu 3.1 části B (v příslušném případě)
ČÁST D
STANDARDNÍ VZORCE
U standardních vzorců 1–17 se použijí tyto podmínky:
|
— |
Těžký kov, stopové prvky: As, Ba, Cd, Cr, Co, Cu, Hg, Mo, Ni, Pb, Sb, Sn, Te, Tl, V o obsahu menším než 0,1 % hmotnostních a Mn, Sr, Zn o obsahu menším než 1 % hmotnostních. |
|
— |
Polycyklické aromatické uhlovodíky (PAH) nejsou přítomny. |
Poznámka týkající se standardních vzorců 1–17:
|
— |
(1) Látka UVCB sestává z variabilního množství kalcitu, křemičitanu trojvápenatého, křemičitanu dvojvápenatého, oxidu vápenatého, křemene, chloridu draselného, síranu draselného, síranu vápenatého, hlinitokřemičitanu sodného, hlinitokřemičitanu hořečnatého, muskovitu, … |
1. CEMENT
|
Cement – standardní vzorec 1 |
||
|
Popis výrobku |
Portlandský cement s jednou hlavní složkou: slínkem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
86,5–100 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0–0,1 |
|
Cement – standardní vzorec 2 |
||
|
Popis výrobku |
Portlandský struskový cement a vysokopecní cement s dvěma hlavními složkami: slínkem a struskou |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
4,6–94 |
|
Granulovaná vysokopecní struska |
266-002-0 |
5,5–95 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 3 |
||
|
Popis výrobku |
Portlandský cement s křemičitým úletem Portlandské cementy s dvěma hlavními složkami: slínkem a křemičitým úletem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
82–94 |
|
Křemičitý úlet |
273-761-1 |
5,5–10 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 4 |
||
|
Popis výrobku |
Portlandský pucolánový cement, pucolánový cement Portlandské cementy s dvěma hlavními složkami: slínkem a pucolánem (přírodním nebo přírodním kalcinovaným pucolánem) |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
41–94 |
|
Přírodní (kalcinovaný) pucolán |
310-127-6 |
5,5–55 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-303-2 |
0 – 0,1 |
|
Cement – standardní vzorec 5 |
||
|
Popis výrobku |
Portlandský popílkový cement, pucolánový cement Portlandské cementy s dvěma hlavními složkami: slínkem a polétavým popílkem (křemičitým a vápenatým popílkem) |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
41–94 |
|
Polétavý popílek |
931-322-8 |
5,5–55 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 6 |
||
|
Popis výrobku |
Portlandský cement s páleným lupkem Portlandské cementy s dvěma hlavními složkami: slínkem a páleným lupkem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
59–94 |
|
Pálený lupek |
297-648-1 |
5,5–35 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 7 |
||
|
Popis výrobku |
Portlandský cement s vápencem Portlandské cementy s dvěma hlavními složkami: slínkem a vápencem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
59–94 |
|
Vápenec |
215-279-6 |
5,5–35 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 8 |
||
|
Popis výrobku |
Portlandský směsný cement, směsný cement (struska – vápenec) Portlandské cementy se třemi hlavními složkami: slínkem, struskou a vápencem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
31,9–88 |
|
Granulovaná vysokopecní struska |
266-002-0 |
5,5–59 |
|
Vápenec |
215-279-6 |
5,5–29 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 9 |
||
|
Popis výrobku |
Portlandský směsný cement, směsný cement (struska – polétavý popílek) Portlandské cementy se třemi hlavními složkami: slínkem, vysokopecní struskou, křemičitým a vápenatým polétavým popílkem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
18,2–88 |
|
Granulovaná vysokopecní struska |
266-002-0 |
5,5–59 |
|
Polétavý popílek |
931-322-8 |
5,5–49 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 10 |
||
|
Popis výrobku |
Portlandský směsný cement, směsný cement (struska – pucolán) Portlandské cementy se třemi hlavními složkami: slínkem, vysokopecní struskou, přírodním nebo přírodním kalcinovaným pucolánem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
18,2–88 |
|
Granulovaná vysokopecní struska |
266-002-0 |
5,5–49 |
|
Přírodní (kalcinovaný) pucolán |
310-127-6 |
5,5–49 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 11 |
||
|
Popis výrobku |
Portlandský směsný cement (struska – pálený lupek) Portlandské cementy se třemi hlavními složkami: slínkem, vysokopecní struskou, páleným lupkem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
59–94 |
|
Granulovaná vysokopecní struska |
266-002-0 |
5,5–29 |
|
Pálený lupek |
297-648-1 |
5,5–29 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 12 |
||
|
Popis výrobku |
Portlandský směsný cement (vápenec – polétavý popílek) Portlandské cementy se třemi hlavními složkami: slínkem, vápencem, křemičitým a vápenatým polétavým popílkem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
46–94 |
|
Vápenec |
215-279-6 |
5,5–29 |
|
Polétavý popílek |
931-322-8 |
5,5–44 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 13 |
||
|
Popis výrobku |
Portlandský směsný cement (vápenec – pucolán) Portlandské cementy se třemi hlavními složkami: slínkem, vápencem, přírodním nebo přírodním kalcinovaným pucolánem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
46–94 |
|
Vápenec |
215-279-6 |
5,5–29 |
|
Přírodní (kalcinovaný) pucolán |
310-127-6 |
5,5–44 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 14 |
||
|
Popis výrobku |
Portlandský směsný cement (vápenec – pálený lupek) Portlandské cementy se třemi hlavními složkami: slínkem, vápencem a páleným lupkem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
59–94 |
|
Vápenec |
215-279-6 |
5,5–29 |
|
Pálený lupek |
297-648-1 |
5,5–29 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0 – 0,1 |
|
Cement – standardní vzorec 15 |
||
|
Popis výrobku |
Portlandský směsný cement, pucolánový cement (polétavý popílek – pucolán) Portlandské cementy se třemi hlavními složkami: slínkem, křemičitým a vápenatým polétavým popílkem, přírodním nebo přírodním kalcinovaným pucolánem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
41–94 |
|
Přírodní (kalcinovaný) pucolán |
310-127-6 |
5,5–55 |
|
Polétavý popílek |
931-322-8 |
5,5–55 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0–0,1 |
|
Cement – standardní vzorec 16 |
||
|
Popis výrobku |
Portlandské směsné cementy Portlandské cementy se čtyřmi hlavními složkami: slínkem a třemi z těchto složek – vysokopecní struskou, křemičitým úletem, polétavým popílkem, pucolánem, páleným lupkem, vápencem |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
59–94 |
|
Granulovaná vysokopecní struska Přírodní (kalcinovaný) pucolán Polétavý popílek Pálený lupek Vápenec Křemičitý úlet |
266-002-0 310-127-6 931-322-8 297-648-1 215-279-6 273-761-1 |
5,5–23 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0 – 1 |
|
Síran cínatý |
231-302-2 |
0–0,1 |
|
Cement – standardní vzorec 17 |
||
|
Popis výrobku |
Směsný cement Portlandské cementy se čtyřmi hlavními složkami: slínkem, struskou, křemičitým polétavým popílkem a přírodním nebo přírodním kalcinovaným pucolánem |
|
|
Složka |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
18,3–64 |
|
Granulovaná vysokopecní struska |
266-002-0 |
16,5–49 |
|
Přírodní (kalcinovaný) pucolán |
310-127-6 |
5,5–43 |
|
Polétavý popílek |
931-322-8 |
5,5–43 |
|
Síran vápenatý |
231-900-3 |
0–8 |
|
Prach ze spalin (1) |
270-659-9 |
0–5 |
|
Anorganické přírodní nerostné materiály |
310-127-6 |
|
|
Síran železnatý |
231-753-5 |
0–1 |
|
Síran cínatý |
231-302-2 |
0–0,1 |
|
Cement – standardní vzorec 18 |
||
|
Popis výrobku |
Vápenohlinitanový cement |
|
|
Složka |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek vápenohlinitanového cementu |
266-045-5 |
86,5–100 |
|
Brusná přísada |
– |
0–0,2 |
|
Cement – standardní vzorec 19 |
||
|
Popis výrobku |
Cementy pro zdění – se slínkem a vápnem – MC 5, MC 12,5, MC 22,5 |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
25–60 |
|
Stavební vápno podle EN 459 |
215-138-9 |
1–75 |
|
Hašené vápno podle EN 459 |
215-137-3 |
|
|
Jiné, anorganické složky neklasifikované jako nebezpečné |
310-127-6 |
0–74 |
|
Anorganické pigmenty podle EN 12878 |
– |
0–1 |
|
Cement – standardní vzorec 20 |
||
|
Popis výrobku |
Cementy pro zdění – se slínkem bez vápna – MC 5, MC 12,5, MC 22,5 |
|
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Slínek portlandského cementu |
266-043-4 |
25–60 |
|
Jiné, anorganické složky neklasifikované jako nebezpečné |
310-127-6 |
40–75 |
|
Anorganické pigmenty podle EN 12878 |
|
0–1 |
2. SÁDROVCOVÉ POJIVO
|
Sádrovcové pojivo – standardní vzorec |
||
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Síran vápenatý |
231-900-3 |
≥ 50 a < 100 |
|
Hydroxid vápenatý |
215-137-3 |
> 0 a ≤ 5 |
3. BETON PŘIPRAVENÝ PRO LITÍ
|
Beton připravený pro lití – standardní vzorec 1 Třídy pevnosti betonu C8/10, C12/15, C16/20, C20/25, C25/30, C28/35, C32/40, C35/45, C40/50, C45/55, C50/60 LC8/9, LC12/13, LC16/18, LC20/22, LC25/28, LC30/33, LC35/38, LC40/44, LC45/50, LC50/55, LC55/60 |
||
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Cement |
270-659-9 |
3–18 |
|
Voda |
231-791-2 |
5–8 |
|
Plniva do betonu |
273-727-6 |
70–80 |
|
Provzdušňovače (příměs) |
– |
0 – 0,08 |
|
Plastifikátory/superplastifikátory (příměs) |
– |
0–0,15 |
|
Zpomalovače (příměs) |
– |
0 – 0,4 |
|
Urychlovače (příměs) |
– |
0 – 0,2 |
|
Odolné proti vodě (příměs) |
– |
0 – 0,25 |
|
Polétavý popílek |
931-322-8 |
0 – 8 |
|
Křemičitý úlet |
273-761-1 |
0–3 |
|
Granulovaná vysokopecní struska |
266-002-0 |
0–6 |
|
Beton připravený pro lití – standardní vzorec 2 Třídy pevnosti betonu C55/67, C60/75, C70/85, C80/95, C90/105, C100/105, LC 60/66, LC70/77, LC80/88 |
||
|
Název složky |
Číslo ES |
Koncentrace (hmotnostních %) |
|
Cement |
270-659-9 |
12–25 |
|
Voda |
231-791-2 |
5–8 |
|
Plniva do betonu |
273-727-6 |
70–80 |
|
Provzdušňovače (příměs) |
– |
0,04 – 0,08 |
|
Plastifikátory/superplastifikátory (příměs) |
– |
0–0,15 |
|
Zpomalovače (příměs) |
– |
0 – 0,4 |
|
Urychlovače (příměs) |
– |
0 – 0,2 |
|
Odolné proti vodě (příměs) |
– |
0 – 0,25 |
|
Polétavý popílek |
931-322-8 |
0 – 8 |
|
Křemičitý úlet |
273-761-1 |
0–3 |
|
Granulovaná vysokopecní struska |
266-002-0 |
0–6 |
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/24 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2020/1678
ze dne 6. listopadu 2020,
kterým se schvaluje změna specifikace chráněného označení původu nebo chráněného zeměpisného označení („Rioja“ (CHOP))
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 ze dne 17. prosince 2013, kterým se stanoví společná organizace trhů se zemědělskými produkty a zrušují nařízení Rady (EHS) č. 922/72, (EHS) č. 234/79, (ES) č. 1037/2001 a (ES) č. 1234/2007 (1), a zejména na článek 99 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Komise přezkoumala žádost o schválení změny specifikace chráněného označení původu „Rioja“, kterou podalo Španělsko v souladu s článkem 105 nařízení (EU) č. 1308/2013. |
|
(2) |
Komise v souladu s čl. 97 odst. 3 nařízení (EU) č. 1308/2013 (2) zveřejnila žádost o schválení změny specifikace v Úředním věstníku Evropské unie. |
|
(3) |
Komise neobdržela žádné námitky podle článku 98 nařízení (EU) č. 1308/2013. |
|
(4) |
Změna specifikace by proto měla být v souladu s článkem 99 nařízení (EU) č. 1308/2013 schválena. |
|
(5) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Výboru pro společnou organizaci zemědělských trhů, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Změna specifikace zveřejněná v Úředním věstníku Evropské unie týkající se názvu „Rioja“ (CHOP) se schvaluje.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 6. listopadu 2020.
Za Komisi,
jménem předsedkyně,
Janusz WOJCIECHOWSKI
člen Komise
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/25 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2020/1679
ze dne 6. listopadu 2020,
kterým se přiznává ochrana podle článku 99 nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 názvu „Soltvadkerti“ (CHOP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 ze dne 17. prosince 2013, kterým se stanoví společná organizace trhů se zemědělskými produkty a zrušují nařízení Rady (EHS) č. 922/72, (EHS) č. 234/79, (ES) č. 1037/2001 a (ES) č. 1234/2007 (1), a zejména na článek 99 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
V souladu s čl. 97 odst. 2 a 3 nařízení (EU) č. 1308/2013 byla žádost Maďarska o zápis názvu „Soltvadkerti“ do evidence posouzena Komisí a následně zveřejněna v Úředním věstníku Evropské unie (2). |
|
(2) |
Komise neobdržela žádné námitky podle článku 98 nařízení (EU) č. 1308/2013. |
|
(3) |
V souladu s článkem 99 nařízení (EU) č. 1308/2013 by měl být název „Soltvadkerti“ chráněn a zapsán do evidence uvedené v článku 104 zmíněného nařízení. |
|
(4) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Výboru pro společnou organizaci zemědělských trhů, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Název „Soltvadkerti“ (CHOP) je tímto chráněn.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 6. listopadu 2020.
Za Komisi,
jménem předsedkyně,
Janusz WOJCIECHOWSKI
člen Komise
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/26 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2020/1680
ze dne 6. listopadu 2020,
kterým se názvu „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ (CHOP) uděluje ochrana podle článku 99 nařízení Evropského parlamentu a Rady (EU) č. 1308/2013
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 ze dne 17. prosince 2013, kterým se stanoví společná organizace trhů se zemědělskými produkty a zrušují nařízení Rady (EHS) č. 922/72, (EHS) č. 234/79, (ES) č. 1037/2001 a (ES) č. 1234/2007 (1), a zejména na článek 99 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
V souladu s čl. 97 odst. 2 a 3 nařízení (EU) č. 1308/2013 byla žádost Itálie o zápis názvu „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ do evidence posouzena Komisí a následně zveřejněna v Úředním věstníku Evropské unie (2). |
|
(2) |
Komise neobdržela žádné námitky podle článku 98 nařízení (EU) č. 1308/2013. |
|
(3) |
V souladu s článkem 99 nařízení (EU) č. 1308/2013 by měl být název „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ chráněn a zapsán do evidence uvedené v článku 104 zmíněného nařízení. |
|
(4) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Výboru pro společnou organizaci zemědělských trhů, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Název „Friuli“/„Friuli Venezia Giulia“/„Furlanija“/„Furlanija Julijska krajina“ (CHOP) je tímto chráněn.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 6. listopadu 2020.
Za Komisi,
jménem předsedkyně,
Janusz WOJCIECHOWSKI
člen Komise
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/27 |
NAŘÍZENÍ KOMISE (EU) 2020/1681
ze dne 12. listopadu 2020,
kterým se mění příloha I nařízení Evropského parlamentu a Rady (ES) č. 1334/2008, pokud jde o odstranění některých aromatických látek ze seznamu Unie
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1334/2008 ze dne 16. prosince 2008 o aromatech a některých složkách potravin s aromatickými vlastnostmi pro použití v potravinách nebo na jejich povrchu a o změně nařízení Rady (EHS) č. 1601/91, nařízení (ES) č. 2232/96 a (ES) č. 110/2008 a směrnice 2000/13/ES (1), a zejména na čl. 11 odst. 3 uvedeného nařízení,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1331/2008 ze dne 16. prosince 2008, kterým se stanoví jednotné povolovací řízení pro potravinářské přídatné látky, potravinářské enzymy a potravinářská aromata (2), a zejména na čl. 7 odst. 4 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Příloha I nařízení (ES) č. 1334/2008 stanoví seznam aromat a výchozích materiálů Unie schválených pro použití v potravinách nebo na jejich povrchu a podmínky jejich použití. |
|
(2) |
Prováděcím nařízením Komise (EU) č. 872/2012 (3) byl přijat seznam aromatických látek, který byl vložen do části A přílohy I nařízení (ES) č. 1334/2008. |
|
(3) |
Přílohu I nařízení (ES) č. 1334/2008 lze aktualizovat jednotným postupem uvedeným v čl. 3 odst. 1 nařízení (ES) č. 1331/2008, a to buď z podnětu Komise, nebo na základě žádosti podané členským státem nebo zúčastněnou stranou. |
|
(4) |
Seznam aromat a výchozích materiálů Unie stanovený v příloze I nařízení (ES) č. 1334/2008 obsahuje mimo jiné řadu aromatických látek, u nichž v době přijetí seznamu nařízením (EU) č. 872/2012 nebyl Evropský úřad pro bezpečnost potravin (dále jen „úřad“) schopen na základě dostupných údajů vyloučit bezpečnostní riziko pro zdraví spotřebitele, a dospěl proto k závěru, že pro dokončení hodnocení těchto látek jsou zapotřebí doplňující údaje. Uvedené látky byly zařazeny na seznam aromatických látek Unie, avšak pod podmínkou, že před uplynutím konkrétních lhůt stanovených v části A přílohy I nařízení (ES) č. 1334/2008 budou předloženy bezpečnostní údaje týkající se obav vyjádřených úřadem. Tyto látky a jejich lhůty byly označeny poznámkami pod čarou č. 1 až 4. |
|
(5) |
Mezi látkami, které byly zařazeny na seznam aromat a výchozích materiálů Unie, ale byly označeny odkazem na poznámku pod čarou, jež vyžaduje, aby do 31. prosince 2012 byly předloženy doplňující vědecké údaje, bylo těchto pět látek: α-damaskon (číslo FL 07.134) (reprezentativní látka skupiny), δ-damaskon (číslo FL 07.130), cis-1-(2,6,6-trimethylcyklohex-2-en-1-yl)but-2-en-1-on (číslo FL 07.225), trans-1-(2,6,6-trimethylcyklohex-2-en-1-yl)but-2-en- 1-on (číslo FL 07.226) a α-damascenon (číslo FL 07.231) (dále jen „dotčené látky“). Tyto látky jsou součástí podskupiny 2.4 látek ze skupiny aromatických látek FGE.19 a byly zařazeny do skupiny aromatických látek FGE 210. Pokud jde o tyto látky, úřad ve svém stanovisku ohledně hodnocení skupiny aromatických látek 210 z roku 2009 (4) uvedl, že v jejich molekulární struktuře je obsaženo strukturální riziko genotoxicity, jelikož se jedná o alfa- a beta-nenasycené ketony, a že jsou zapotřebí doplňující údaje o genotoxicitě, aby bylo možné vyloučit obavy ohledně jejich genotoxicity v souladu s dokumentem úřadu s názvem „Genotoxicity test strategy for substances belonging to subgroups of the Flavouring Group FGE.19“ („Strategie testování genotoxicity pro látky patřící do podskupin skupiny aromatických látek FGE.19“) (5). |
|
(6) |
Dne 28. prosince 2012 byly předloženy údaje týkající se podskupiny 2.4 látek ze skupiny aromatických látek FGE.19. |
|
(7) |
Úřad předložené údaje vyhodnotil v rámci revize 1 stanoviska o genotoxickém potenciálu látek ze skupiny aromatických látek FGE 210 z chemické skupiny FGE 2.4 skupiny aromatických látek FGE 19, jež byla zveřejněna dne 19. února 2014 (6). Úřad však dospěl k závěru, že předložené údaje stále nepostačují k vyloučení genotoxického potenciálu dotčených látek, a požádal o další doplňující údaje o genotoxicitě u látek, které jsou pro tuto podskupinu reprezentativní. |
|
(8) |
Nové údaje byly předloženy v roce 2014. Úřad tyto nové údaje vyhodnotil v rámci revize 2 svého stanoviska, jež byla zveřejněna dne 10. července 2015 (7). Úřad však dospěl k závěru, že tyto nové údaje nepostačují k vyloučení genotoxického potenciálu dotčených látek, a znovu požádal, aby byly předloženy další vědecké údaje o genotoxicitě dotčených látek. |
|
(9) |
Další údaje o dotčených látkách byly předloženy v roce 2016. Po předložení těchto údajů si úřad prostřednictvím dopisů z 8. listopadu 2016, 9. února 2017, 29. června 2017 a 8. února 2019 vyžádal další informace a provedení specifických studií. Poskytnuté nové údaje však ne vždy odpovídaly studiím požadovaným úřadem a nebyly vhodné k řádnému vyřešení obav úřadu. S ohledem na veškeré uvedené doplňující údaje, jež byly předloženy, vyhodnotil úřad znovu genotoxický potenciál dotčených látek v rámci revize 3 stanoviska týkajícího se skupiny FGE.210 (8), jež byla zveřejněna dne 22. května 2019. Úřad dospěl k závěru, že obavy ohledně genotoxicity nelze u těchto pěti dotčených látek vyloučit. |
|
(10) |
Vzhledem k tomu, že ani údaje předložené v původní lhůtě, ani údaje předložené po následných žádostech úřadu po uvedené lhůtě neumožnily úřadu v roce 2019 vyloučit obavy vyjádřené v jeho stanovisku z roku 2009, má Komise za to, že není prokázáno, že dotčené látky nepředstavují bezpečnostní riziko pro zdraví spotřebitele. Na základě vědeckých důkazů předložených v rámci stanoveném v části A přílohy I nařízení (ES) č. 1334/2008 pro látky před dokončením jejich hodnocení proto použití dotčených látek nesplňuje obecné podmínky použití aromat uvedené v článku 4 nařízení (ES) č. 1334/2008. |
|
(11) |
V zájmu ochrany lidského zdraví by proto měly být dotčené látky odstraněny ze seznamu Unie. |
|
(12) |
Část A přílohy I nařízení (ES) č. 1334/2008 by proto měla být odpovídajícím způsobem změněna. |
|
(13) |
Z technických důvodů by se měla stanovit přechodná období pro dotčené potraviny, do nichž byla přidána některá z pěti uvedených aromatických látek a které byly uvedeny na trh nebo odeslány do Unie ze třetích zemí a byly na cestě přede dnem vstupu tohoto nařízení v platnost. Uvedené přechodné období by se nemělo vztahovat na přípravky, do nichž byla přidána některá z pěti uvedených aromatických látek a které nejsou určeny ke spotřebě jako takové, jelikož složení těchto přípravků znají jejich výrobci při jejich přípravě. |
|
(14) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro rostliny, zvířata, potraviny a krmiva, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Část A přílohy I nařízení (ES) č. 1334/2008 se mění v souladu s přílohou tohoto nařízení.
Článek 2
1. Potraviny, do nichž byla přidána některá z aromatických látek uvedených v příloze tohoto nařízení a které byly v souladu s právními předpisy uvedeny na trh přede dnem vstupu tohoto nařízení v platnost, smějí být nadále uváděny na trh do svého data minimální trvanlivosti nebo data spotřeby.
2. Potraviny dovezené do Unie, do nichž byla přidána některá z aromatických látek uvedených v příloze tohoto nařízení, smějí být uváděny na trh do svého data minimální trvanlivosti nebo data spotřeby, pokud může dovozce těchto potravin prokázat, že byly z dotčené třetí země odeslány a byly na cestě do Unie přede dnem vstupu tohoto nařízení v platnost.
3. Přechodná období stanovená v odstavcích 1 a 2 se nepoužijí na přípravky, do nichž byla přidána některá z těchto pěti aromatických látek a které nejsou určeny ke spotřebě jako takové.
4. Pro účely tohoto nařízení se přípravky rozumí směsi jednoho nebo několika aromat, do nichž mohou být zahrnuty i jiné složky potravin, jako jsou potravinářské přídatné látky, enzymy nebo nosiče, aby se usnadnilo jejich skladování, prodej, standardizace, ředění nebo rozpouštění.
Článek 3
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 12. listopadu 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 354, 31.12.2008, s. 34.
(2) Úř. věst. L 354, 31.12.2008, s. 1.
(3) Prováděcí nařízení Komise (EU) č. 872/2012 ze dne 1. října 2012, kterým se přijímá seznam aromatických látek, jak stanoví nařízení Evropského parlamentu a Rady (ES) č. 2232/96, a kterým se tento seznam vkládá do přílohy I nařízení Evropského parlamentu a Rady (ES) č. 1334/2008 a kterým se zrušuje nařízení Komise (ES) č. 1565/2000 a rozhodnutí Komise 1999/217/ES (Úř. věst. L 267, 2.10.2012, s. 1).
(4) Scientific Opinion on Flavouring Group Evaluation 210: alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19; EFSA Journal (2009) ON-1030, 1–18. https://efsa.onlinelibrary.wiley.com/doi/pdf/10.2903/j.efsa.2009.1030
(5) Genotoxicity Test Strategy for Substances belonging to Subgroups of FGE.19 - Statement of the Panel on Food Contact Materials, Enzymes, Flavourings and Processing AIDS (CEF); EFSA Journal (2008) 854, 1–5.https://efsa.onlinelibrary.wiley.com/doi/pdf/10.2903/j.efsa.2008.854.
(6) Scientific Opinion on Flavouring Group Evaluation 210, Revision 1 (FGE.210Rev1): Consideration of genotoxic potential for alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19. EFSA Journal 2014;12(2):3587, 35 s. doi:10.2903/j.efsa.2014.3587
(7) Scientific Opinion on Flavouring Group Evaluation 210 Revision 2 (FGE.210Rev2): Consideration of genotoxic potential for alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19. ze dne 10. července 2015, EFSA Journal 2015;13(7):4172.doi:10.293/j.efsa.2015.4172.
(8) Scientific Opinion on Flavouring Group Evaluation 210 Revision 3 (FGE.210Rev3): Consideration of genotoxic potential for alpha, beta-unsaturated alicyclic ketones and precursors from chemical subgroup 2.4 of FGE.19. EFSA Journal 2019; 17(5):5676.
PŘÍLOHA
V příloze I části A oddíle 2 nařízení (ES) č. 1334/2008 se zrušují tyto položky:
|
„07.130 |
δ-damaskon |
57378-68-4 |
386 |
|
|
|
2 |
JECFA/EFSA |
|
07.134 |
α-damaskon |
43052-87-5 |
385 |
11053 |
|
|
2 |
JECFA/EFSA |
|
07.225 |
cis-1-(2,6,6-trimethylcyklohex-2-en-1-yl)but-2-en-1-on |
23726-94-5 |
|
|
Nejméně 92 %; 4 % příměsi trans-isomeru |
|
2 |
EFSA |
|
07.226 |
trans-1-(2,6,6-trimethylcyklohex-2-en-1-yl)but-2-en-1-on |
24720-09-0 |
|
|
|
|
2 |
EFSA |
|
07.231 |
α-damascenon |
35044-63-4 |
|
|
|
|
2 |
EFSA“ |
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/31 |
NAŘÍZENÍ KOMISE (EU) 2020/1682
ze dne 12. listopadu 2020,
kterým se mění příloha III nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 o kosmetických přípravcích
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 ze dne 30. listopadu 2009 o kosmetických přípravcích (1), a zejména na čl. 31 odst. 1 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Látky 2-Hydroxyethyl-methakrylát (HEMA) a 11,14-Dioxa-2,9-diazaheptadec-16-enová kyselina, 4,4,6,16-tetramethyl-10,15-dioxo-, 2-[(2-methyl-1-oxo-2-propenyl)oxy]ethylester (Di-HEMA Trimethylhexyl Dicarbamate neboli Di-HEMA TMHDC) v současné době nepodléhají žádnému zákazu nebo omezení podle nařízení (ES) č. 1223/2009. |
|
(2) |
Švédská agentura pro léčivé přípravky, která je švédským příslušným orgánem pro účely nařízení (ES) č. 1223/2009, dne 2. července 2014 přijala a oznámila své rozhodnutí podle článku 27 nařízení (ES) č. 1223/2009, kterým se zavádí dočasná omezující opatření týkající se kosmetického přípravku na nehty, který způsobil vysoký počet nežádoucích účinků. Látkami, u nichž bylo zjištěno, že pravděpodobně způsobují uvedené nežádoucí účinky, jsou HEMA a Di-HEMA TMHDC. |
|
(3) |
V souladu s čl. 27 odst. 2 nařízení (ES) č. 1223/2009 švédská agentura pro léčivé přípravky neprodleně sdělila Komisi a příslušným orgánům ostatních členských států přijatá opatření a údaje, z nichž vycházela. |
|
(4) |
Vědecký výbor pro bezpečnost spotřebitele (VVBS) ve svém stanovisku z 21.–22. června 2018 (2) dospěl k závěru, že „pokud jsou látky HEMA a di-HEMA-TMHDC vhodně aplikovány na nehtovou ploténku (…) v rámci systému pro modeláž umělých nehtů, pravděpodobně nepředstavují riziko senzibilizace, za předpokladu, že je jejich použití omezeno pouze na nehtovou ploténku a je zabráněno styku s přiléhající kůží“. VVBS dále dospěl k závěru, že „látky HEMA i di-HEMA-TMHDC jsou slabé až mírné senzibilátory a za obvyklých a rozumně předvídatelných podmínek použití představují riziko senzibilizace v důsledku nesprávného použití přípravků nebo nevhodně prováděné aplikace nebo neúmyslné kontaminace kůže přiléhající k nehtům“. |
|
(5) |
Podle článku 3 nařízení (ES) č. 1223/2009 musí být kosmetické prostředky dodávané na trh bezpečné pro lidské zdraví, jsou-li používány za obvyklých nebo rozumně předvídatelných podmínek použití. |
|
(6) |
Při posuzování „obvyklých nebo rozumně předvídatelných podmínek použití“ je nutno vzít v úvahu možné nesprávné, nevhodné nebo neúmyslné použití. V případě přípravků vyžadujících vysokou úroveň přesnosti je nezbytné vzít v úvahu situace nedostatečné přesnosti jejich aplikace. |
|
(7) |
Případy senzibilizace na přípravky na nehty obsahující látky HEMA a Di-HEMA TMHDC, které byly hlášeny v některých členských státech, vedou Komisi k závěru, že existuje riziko, že tyto přípravky mohou být aplikovány s nedostatečnou přesností, což způsobí styk s kůží přiléhající k nehtové ploténce. |
|
(8) |
Mělo by se rozlišovat mezi profesionálním a spotřebitelským použitím kosmetických přípravků. U profesionálních uživatelů se předpokládají vyšší bezpečnostní standardy. Předpokládá se, že profesionální uživatel má více dovedností, zkušeností a znalostí týkajících se použití kosmetického přípravku než spotřebitel. |
|
(9) |
Možná zdravotní a bezpečnostní rizika pro profesionální uživatele upravují některé směrnice Unie, kterými se stanoví minimální požadavky, zejména směrnice Rady 89/391/EHS (3) a 98/24/ES (4). Mohou platit další bezpečnostní předpisy pro profesionální použití. |
|
(10) |
Jelikož výbor VVBS ve svém stanovisku považuje látky HEMA a Di-HEMA TMHDC v přípravcích na nehty za bezpečné pouze tehdy, jsou-li aplikovány na nehtovou ploténku, a jelikož by za „obvyklých nebo rozumně předvídatelných podmínek použití“ měla být vzata v úvahu možnost aplikace na kůži přiléhající k nehtové ploténce, existuje, pokud jde o spotřebitele, potenciální riziko pro lidské zdraví v důsledku použití látek HEMA a Di-HEMA TMHDC v přípravcích na nehty. |
|
(11) |
Jelikož se předpokládá, že použití přípravků na nehty obsahujících látky HEMA a Di-HEMA TMHDC profesionálními uživateli je pro spotřebitele bezpečnější, měly by tyto přípravky používat pouze profesionální uživatelé, a proto by na vnějším obalu uvedených přípravků mělo být uvedeno upozornění „Jen pro profesionální použití“. |
|
(12) |
Aby byli profesionální uživatelé i spotřebitelé upozorněni na potenciální zdravotní rizika, mělo by být na vnějším obalu přípravků na nehty obsahujících látky HEMA a Di-HEMA TMHDC uvedeno upozornění „Může způsobit alergickou reakci“. |
|
(13) |
Ochranné opatření přijaté Švédskem by proto mělo být považováno za odůvodněné. V důsledku toho je nezbytné omezit používání látek HEMA a Di-HEMA TMHDC v přípravcích na nehty. |
|
(14) |
Příloha III nařízení (ES) č. 1223/2009 by proto měla být odpovídajícím způsobem změněna. |
|
(15) |
Je vhodné stanovit přiměřenou lhůtu, aby se dané odvětví mohlo těmto novým požadavkům přizpůsobit. |
|
(16) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro kosmetické přípravky, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Příloha III nařízení (ES) č. 1223/2009 se mění v souladu s přílohou tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 12. listopadu 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 342, 22.12.2009, s. 59.
(2) SCCS/1592/17;
https://ec.europa.eu/health/sites/health/files/scientific_committees/consumer_safety/docs/sccs_o_214.pdf
(3) Směrnice Rady 89/391/EHS ze dne 12. června 1989 o zavádění opatření pro zlepšení bezpečnosti a ochrany zdraví zaměstnanců při práci (Úř. věst. L 183, 29.6.1989, s. 1).
(4) Směrnice Rady 98/24/ES ze dne 7. dubna 1998 o bezpečnosti a ochraně zdraví zaměstnanců před riziky spojenými s chemickými činiteli používanými při práci (čtrnáctá samostatná směrnice ve smyslu čl. 16 odst. 1 směrnice 89/391/EHS) (Úř. věst. L 131, 5.5.1998, s. 11).
PŘÍLOHA
V tabulce v příloze III nařízení (ES) č. 1223/2009 se doplňují následující položky:
|
Referenční číslo |
Identifikace látky |
Omezení |
Znění podmínek použití a upozornění |
|||||
|
Chemický název/ INN |
Název v seznamu přísad podle společné nomenklatury |
Číslo CAS |
Číslo ES |
Druh výrobku, části těla |
Nejvyšší koncentrace v přípravku připraveném k použití |
Jiné |
|
|
|
a |
b |
c |
d |
e |
f |
g |
h |
i |
|
„313 |
2-Hydroxyethyl-methakrylát (*1) |
HEMA |
868-77-9 |
212-782-2 |
Přípravky na nehty |
|
Jen profesionální použití |
Jen pro profesionální použití. Může způsobit alergickou reakci. |
|
314 |
11,14-Dioxa-2,9-diazaheptadec-16-enová kyselina, 4,4,6,16-tetramethyl-10,15-dioxo-, 2-[(2-methyl-1-oxo-2-propenyl)oxy]ethylester (*2) |
DI-HEMA TRIMETHYLHEXYL DICARBAMATE |
41137-60-4/72869-86-4 |
255-239-5/276-957-5 |
Přípravky na nehty |
|
Jen profesionální použití |
Jen pro profesionální použití. Může způsobit alergickou reakci. |
(*1) Ode dne 3. června 2021 nesmí být na trh Unie uváděny přípravky, které obsahují uvedenou látku a nejsou v souladu s uvedenými podmínkami. Ode dne 3. září 2021 nesmí být na trh Unie dodávány přípravky, které obsahují uvedenou látku a nejsou v souladu s uvedenými podmínkami.“
(*2) Ode dne 3. června 2021 nesmí být na trh Unie uváděny přípravky, které obsahují uvedenou látku a nejsou v souladu s uvedenými podmínkami. Ode dne 3. září 2021 nesmí být na trh Unie dodávány přípravky, které obsahují uvedenou látku a nejsou v souladu s uvedenými podmínkami.“
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/34 |
NAŘÍZENÍ KOMISE (EU) 2020/1683
ze dne 12. listopadu 2020,
kterým se mění přílohy II a III nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 o kosmetických přípravcích
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 ze dne 30. listopadu 2009 o kosmetických přípravcích (1), a zejména na čl. 31 odst. 1 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
V návaznosti na zveřejnění vědecké studie v roce 2001 nazvané „Use of permanent hair dyes and bladder cancer risk“ (Používání trvalých barev na vlasy a riziko rakoviny močového měchýře) došel Vědecký výbor pro kosmetické prostředky a nepotravinářské výrobky určené spotřebitelům, následně nahrazený podle rozhodnutí Komise 2004/210/ES (2) Vědeckým výborem pro spotřební zboží (dále jen „VVSZ“), k závěru, že možná zdravotní rizika používání barev na vlasy jsou znepokojující. |
|
(2) |
VVSZ dále doporučil vytvořit celkovou strategii posuzování bezpečnosti látek k barvení vlasů, včetně požadavků na zkoušky látek používaných v přípravcích k barvení vlasů s ohledem na jejich možnou genotoxicitu nebo karcinogenitu. |
|
(3) |
V návaznosti na stanoviska VVSZ se Komise s členskými státy a zúčastněnými stranami dohodla na celkové strategii regulace látek používaných v přípravcích k barvení vlasů, podle níž měly průmyslové subjekty předložit podklady s aktualizovanými vědeckými údaji o bezpečnosti látek k barvení vlasů, aby mohl VVSZ provést posouzení rizika. |
|
(4) |
Vědecký výbor pro bezpečnost spotřebitele (VVBS), který podle rozhodnutí Komise 2008/721/ES (3) nahradil VVSZ, posoudil bezpečnost jednotlivých látek k barvení vlasů, jichž se týkaly aktualizované podklady předložené průmyslovými subjekty. |
|
(5) |
V důsledku posouzení ze strany VVBS je za účelem zajištění bezpečnosti přípravků k barvení vlasů pro lidské zdraví nezbytné zakázat používání tří látek k barvení vlasů, a to 1,2,4-Trihydroxybenzenu (4), 2-(4-Amino-2-nitroanilino)benzoové kyseliny (5) a 4-Amino-3-hydroxytoluenu (6), na základě konečných stanovisek vydaných VVBS ohledně jejich bezpečnosti. S ohledem na konečná stanoviska VVBS ohledně dalších šesti látek k barvení vlasů, a to látek Dimethylpiperazinium Aminopyrazolopyridine HCl (7), Methylimidazoliumpropyl p-phenylenediamine HCl (8), HC Orange No. 6 (9), Acid Orange 7 (10), Tetrabromophenol Blue (11) a Indigofera Tinctoria (12), je navíc vhodné stanovit jejich nejvyšší koncentrace pro použití v přípravcích k barvení vlasů. |
|
(6) |
Definice přípravku na vlasy stanovená v bodě 1 písm. c) úvodu k přílohám II až VI nařízení (ES) č. 1223/2009 vylučuje použití přípravků k barvení vlasů na řasy, a to na základě odlišné úrovně rizika použití kosmetického přípravku na vlasy na hlavě ve srovnání s použitím téhož přípravku na řasy. V případě aplikace přípravků k barvení vlasů na řasy bylo tedy třeba provést zvláštní posouzení bezpečnosti. |
|
(7) |
Látka 2-Methoxymethyl-p-Phenylenediamine a její sulfát jsou již uvedeny v položce 292 v příloze III nařízení (ES) č. 1223/2009. S ohledem na závěry nejnovějšího stanoviska VVBS (13) ohledně používání uvedených látek na řasy by oblast použití omezení, které se na ně vztahuje, měla být rozšířena o přípravky určené k barvení řas. |
|
(8) |
Aby se zabránilo jakémukoli riziku spojenému s aplikací přípravků určených k barvení řas obsahujících látku 2-Methoxymethyl-p-Phenylenediamine a její sulfát samotnými spotřebiteli, měly by být uvedené přípravky povoleny pouze pro profesionální použití. |
|
(9) |
Aby byli spotřebitelé a profesionální uživatelé informováni o možných nežádoucích účincích použití barev na vlasy a přípravků určených k barvení řas, měla by být za účelem snížení rizika senzibilizace kůže u těchto přípravků na jejich etiketách vytištěna příslušná upozornění. |
|
(10) |
Nařízení (ES) č. 1223/2009 by proto mělo být odpovídajícím způsobem změněno. |
|
(11) |
Je vhodné poskytnout průmyslovým subjektům přiměřené lhůty, aby se mohly přizpůsobit novým požadavkům a postupně vyřadily kosmetické přípravky, které zmíněným požadavkům nevyhovují. |
|
(12) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro kosmetické přípravky, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Nařízení (ES) č. 1223/2009 se mění v souladu s přílohou tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 12. listopadu 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 342, 22.12.2009, s. 59.
(2) Rozhodnutí Komise 2004/210/ES ze dne 3. března 2004 o zřízení vědeckých výborů v oblasti bezpečnosti spotřebitele, veřejného zdraví a životního prostředí (Úř. věst. L 66, 4.3.2004, s. 45).
(3) Rozhodnutí Komise 2008/721/ES ze dne 5. září 2008 o zřízení poradní struktury vědeckých výborů a odborníků v oblasti bezpečnosti spotřebitele, veřejného zdraví a životního prostředí a o zrušení rozhodnutí 2004/210/ES (Úř. věst. L 241, 10.9.2008, s. 21).
(4) SCCS/1598/18
(5) SCCS/1497/12
(6) SCCS/1400/11
(7) SCCS/1584/17
(8) SCCS/1609/19
(9) SCCS/1579/16
(10) SCCS/1536/14
(11) SCCS/1610/19
(12) SCCS/1615/20
(13) SCCS/1603/18
PŘÍLOHA
Nařízení (ES) č. 1223/2009 se mění takto:
|
1) |
V tabulce v příloze II se doplňují nové položky, které znějí:
|
|||||||||||||||||||
|
2) |
Tabulka v příloze III se mění takto:
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(*1) Ode dne 3. září 2021 nesmí být na trh Unie uváděny přípravky k barvení vlasů a obočí, které obsahují uvedené látky.
Ode dne 3. června 2022 nesmí být na trh Unie dodávány přípravky k barvení vlasů a obočí, které obsahují uvedené látky.“
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/42 |
NAŘÍZENÍ KOMISE (EU) 2020/1684
ze dne 12. listopadu 2020,
kterým se mění příloha VI nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 o kosmetických přípravcích
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 ze dne 30. listopadu 2009 o kosmetických přípravcích (1), a zejména na čl. 31 odst. 2 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Vědecký výbor pro bezpečnost spotřebitele (VVBS) ve svém stanovisku ze dne 13. prosince 2019 (2) (dále jen „stanovisko VVBS“) dospěl k závěru, že použití látky Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetate jako a UV filtru v kosmetických přípravcích v koncentraci nejvýše 3 % je bezpečné. Inhalační toxicita nebyla ve stanovisku VVBS posouzena, jelikož nebyly poskytnuty žádné údaje. Stanovisko VVBS se nevztahuje na žádné kosmetické přípravky ve formě spreje, které by mohly vést k expozici plic konečného uživatele při vdechování. |
|
(2) |
VVBS ve svém stanovisku rovněž dospěl k závěru, že Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetate je sekundární amin, a je tedy náchylný k nitrosaci a tvorbě nitrosaminu. Neměl by být používán v kombinaci s nitrosačními látkami. Obsah nitrosaminů by měl být nižší než 50 ppb. |
|
(3) |
S ohledem na stanovisko VVBS a s cílem zohlednit technický a vědecký pokrok by použití látky Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetate jako filtru ultrafialového záření v kosmetických přípravcích mělo být povoleno v koncentraci nejvýše 3 % s výjimkou aplikací, které mohou vést k expozici plic konečného uživatele při vdechování. |
|
(4) |
Příloha VI nařízení (ES) č. 1223/2009 by proto měla být odpovídajícím způsobem změněna. |
|
(5) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro kosmetické přípravky, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Příloha VI nařízení (ES) č. 1223/2009 se mění v souladu s přílohou tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 12. listopadu 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 342, 22.12.2009, s. 59.
(2) SCCS/1605/19.
PŘÍLOHA
V příloze VI nařízení (ES) č. 1223/2009 se doplňuje nová položka, která zní:
|
Referenční číslo |
Identifikace látky |
Podmínky |
Znění podmínek použití a upozornění |
|||||||||||
|
Chemický název/INN/XAN |
Název v seznamu přísad podle společné nomenklatury |
Číslo CAS |
Číslo ES |
Druh výrobku, části těla |
Nejvyšší koncentrace v přípravku připraveném k použití |
Jiné |
||||||||
|
a |
b |
c |
d |
e |
f |
g |
h |
i |
||||||
|
„32 |
2-Ethoxyethyl-(2Z)-2-kyano-2-[3-(3-methoxypropylamino)cyklohex-2-en-1-yliden]acetát |
Methoxypropylamino Cyclohexenylidene Ethoxyethylcyanoacetate |
1419401-88-9 |
700-860-3 |
|
3 % |
|
|
||||||
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/44 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2020/1685
ze dne 12. listopadu 2020,
kterým se mění nařízení (EU) č. 37/2010 za účelem klasifikace látky bupivakain podle maximálního limitu reziduí
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 470/2009 ze dne 6. května 2009, kterým se stanoví postupy Společenství pro stanovení limitů reziduí farmakologicky účinných látek v potravinách živočišného původu, kterým se zrušuje nařízení Rady (EHS) č. 2377/90 a kterým se mění směrnice Evropského parlamentu a Rady 2001/82/ES a nařízení Evropského parlamentu a Rady (ES) č. 726/2004 (1), a zejména na článek 14 ve spojení s článkem 17 uvedeného nařízení,
s ohledem na stanoviska Evropské agentury pro léčivé přípravky vydaná ve dnech 20. února 2020 a 18. června 2020 Výborem pro veterinární léčivé přípravky,
vzhledem k těmto důvodům:
|
(1) |
Článek 17 nařízení (ES) č. 470/2009 požaduje, aby byl maximální limit reziduí (MLR) farmakologicky účinných látek určených k použití v Unii ve veterinárních léčivých přípravcích pro zvířata určená k produkci potravin nebo v biocidních přípravcích používaných v chovu zvířat stanoven nařízením. |
|
(2) |
Tabulka 1 přílohy nařízení Komise (EU) č. 37/2010 (2) stanoví farmakologicky účinné látky a jejich klasifikaci podle MLR v potravinách živočišného původu. |
|
(3) |
V uvedené tabulce látka bupivakain není zařazena. |
|
(4) |
Evropské agentuře pro léčivé přípravky (dále jen „agentura EMA“) byla předložena žádost o stanovení MLR pro látku bupivakain pouze pro kožní a epilezionální podání u prasat pro selata do věku 7 dnů a u skotu pro telata do věku 2 měsíců. |
|
(5) |
Agentura EMA na základě stanoviska Výboru pro veterinární léčivé přípravky dospěla k závěru, že pro bupivakain u prasat a skotu v tomto věkovém rozpětí není pro ochranu lidského zdraví nezbytné stanovit MLR, a doporučila klasifikaci „není nutné stanovit MLR“. |
|
(6) |
Podle článku 5 nařízení (ES) č. 470/2009 má agentura EMA zvážit, zda mají být MLR stanovené pro danou farmakologicky účinnou látku v určité potravině používány i pro jinou potravinu získanou ze stejného druhu nebo MLR stanovené u jednoho nebo více určitých druhů používány i u jiných druhů. |
|
(7) |
Agentura EMA usoudila, že rozšíření klasifikace bupivakainu „není nutné stanovit MLR“ z prasat a skotu na ostatní druhy zvířat určených k produkci potravin není v současné době z důvodu nedostatečných údajů vhodné. |
|
(8) |
Nařízení (EU) č. 37/2010 by proto mělo být odpovídajícím způsobem změněno. |
|
(9) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro veterinární léčivé přípravky, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Příloha nařízení (EU) č. 37/2010 se mění v souladu s přílohou tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 12. listopadu 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 152, 16.6.2009, s. 11.
(2) Nařízení Komise (EU) č. 37/2010 ze dne 22. prosince 2009 o farmakologicky účinných látkách a jejich klasifikaci podle maximálních limitů reziduí v potravinách živočišného původu (Úř. věst. L 15, 20.1.2010, s. 1).
PŘÍLOHA
V tabulce 1 přílohy nařízení (EU) č. 37/2010 se v abecedním pořadí vkládá položka pro následující látku:
|
Farmakologicky účinná(-é) látka(-y) |
Indikátorové reziduum |
Druh zvířat |
MLR |
Cílové tkáně |
Další ustanovení (podle čl. 14 odst. 7 nařízení (ES) č. 470/2009) |
Zařazení podle léčebného účelu |
|
„Bupivakain |
NETÝKÁ SE TÉTO POLOŽKY |
prasata |
není nutné stanovit MLR |
NETÝKÁ SE TÉTO POLOŽKY |
pouze pro použití u selat do 7 dnů věku pouze pro kožní a epilezionální podání |
lokální anestetikum“ |
|
skot |
pouze pro použití u telat do 2 měsíců věku pouze pro kožní a epilezionální podání |
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/47 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2020/1686
ze dne 12. listopadu 2020,
kterým se zavádí celní evidence dovozu určitých plochých za tepla válcovaných výrobků ze železa, nelegované nebo ostatní legované oceli pocházejících z Turecka
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) 2016/1036 ze dne 8. června 2016 o ochraně před dumpingovým dovozem ze zemí, které nejsou členy Evropské unie (1) (dále jen „základní nařízení“), a zejména na čl. 14 odst. 5 uvedeného nařízení,
po informování členských států,
vzhledem k těmto důvodům:
|
(1) |
Dne 14. května 2020 oznámila Evropská komise (dále jen „Komise“) prostřednictvím oznámení zveřejněného v Úředním věstníku Evropské unie (2) (dále jen „oznámení o zahájení“), že zahajuje antidumpingové řízení (dále jen „antidumpingové řízení“) týkající se dovozu určitých plochých za tepla válcovaných výrobků ze železa, nelegované nebo ostatní legované oceli pocházejících z Turecka do Unie na základě podnětu podaného dne 31. března 2020 Evropským ocelářským svazem (dále jen „žadatel“) jménem výrobců představujících více než 25 % celkové výroby určitých plochých za tepla válcovaných výrobků ze železa, nelegované nebo ostatní legované oceli v Unii. |
1. VÝROBEK, KTERÝ JE PŘEDMĚTEM CELNÍ EVIDENCE
|
(2) |
Výrobky, které jsou předmětem celní evidence (dále jen „dotčený výrobek“), jsou ploché válcované výrobky ze železa, nelegované oceli nebo ostatní legované oceli, též ve svitcích (včetně výrobků „zkracovaných na míru“ a „úzkých pásů“), po válcování za tepla již dále neopracované, neplátované, nepokovené ani nepotažené. Tyto výrobky mají v současnosti kódy KN 7208 10 00, 7208 25 00, 7208 26 00, 7208 27 00, 7208 36 00, 7208 37 00, 7208 38 00, 7208 39 00, 7208 40 00, 7208 52 10, 7208 52 99, 7208 53 10, 7208 53 90, 7208 54 00, 7211 13 00, 7211 14 00, 7211 19 00, ex 7225 19 10 (kód TARIC 7225191090), 7225 30 90, ex 7225 40 60 (kód TARIC 7225406090), 7225 40 90, ex 7226 19 10 (kód TARIC 7226191090), 7226 91 91 a 7226 91 99. Kódy KN a kódy TARIC se uvádějí pouze pro informaci. |
|
(3) |
Předmětem celní evidence nejsou: i) výrobky z korozivzdorné oceli a křemíkové elektrooceli s orientovanou strukturou; ii) výrobky z nástrojové oceli a rychlořezné oceli; iii) výrobky, které nejsou ve svitcích a nemají reliéfní vzor, o tloušťce převyšující 10 mm a o šířce 600 mm nebo větší, a iv) výrobky, které nejsou ve svitcích a nemají reliéfní vzor, o tloušťce 4,75 mm nebo větší, avšak nepřesahující 10 mm, a o šířce 2 050 mm nebo větší. |
2. ŽÁDOST
|
(4) |
Dne 17. září 2020 podal žadatel žádost o zavedení celní evidence podle čl. 14 odst. 5 základního nařízení. Žadatel požádal o zavedení celní evidence dovozu dotčeného výrobku, aby mohla být vůči dováženým výrobkům zavedena opatření se zpětnou působností ode dne uvedené celní evidence. |
|
(5) |
V reakci na žádost předložily připomínky tyto zúčastněné strany: vláda Turecka, konsorcium uživatelů (uživatelé), skupiny Colakoglu, Erdemir a Habas (vyvážející výrobci), Sdružení tureckých vývozců oceli (dále jen „ÇİB“) a Sdružení tureckých výrobců oceli (dále jen „TCUD“). |
3. DŮVODY PRO CELNÍ EVIDENCI
|
(6) |
Podle čl. 14 odst. 5 základního nařízení může Komise vyzvat celní orgány, aby přijaly vhodná opatření k zavedení takové celní evidence dovozu, aby následně mohla být vůči dováženým výrobkům, pokud jsou splněny všechny podmínky stanovené v základním nařízení, zavedena opatření ode dne dané celní evidence. Celní evidenci dovozu lze zavést na řádně odůvodněnou žádost výrobního odvětví Unie. |
|
(7) |
Žadatel uvedl, že podle posledních dostupných statistik došlo po zahájení šetření k podstatnému zvýšení dovozu, což pravděpodobně vážně ohrozilo nápravný účinek konečného cla. Dále žadatel namítl, že k dumpingu z Turecka docházelo po delší dobu a že dovozci si byli, nebo si měli být vědomi dumpingových praktik z Turecka. |
|
(8) |
Komise zkoumala žádost na základě čl. 10 odst. 4 základního nařízení. Komise ověřila, zda dovozci o dumpingu věděli nebo měli vědět, pokud jde o rozsah dumpingu a předpokládanou nebo skutečnou újmu. Rovněž analyzovala, zda došlo k dalšímu podstatnému zvýšení dovozu, které s ohledem na čas, jakož i objem a další okolnosti může vážně ohrozit nápravný účinek případného uloženého konečného antidumpingového cla. |
3.1. Povědomí dovozců o dumpingu, rozsahu dumpingu a údajné újmě
|
(9) |
V této fázi má Komise k dispozici dostatečné důkazy o tom, že dovoz dotčeného výrobku z Turecka je dumpingový. V podnětu byly předloženy dostatečné důkazy o dumpingu vycházející ze srovnání takto stanovené běžné hodnoty s vývozní cenou (na úrovni ceny ze závodu) dotčeného výrobku při jeho prodeji na vývoz do Unie. Tyto důkazy ve svém celku a s ohledem na rozsah údajných dumpingových rozpětí v rozmezí od 4 % do 8 % poskytují dostatečnou oporu pro tvrzení, že vyvážející výrobci provádějí dumping. |
|
(10) |
V podnětu byly rovněž předloženy dostatečné důkazy o údajné újmě výrobního odvětví Unie, včetně nepříznivého vývoje klíčových ukazatelů výkonnosti výrobního odvětví Unie. |
|
(11) |
Tyto informace byly uvedeny jak ve verzi podnětu, která nemá důvěrnou povahu, tak i v oznámení o zahájení zveřejněném dne 14. května 2020. Oznámení o zahájení řízení bylo zveřejněno v Úředním věstníku Evropské unie, a jedná se tudíž o veřejný dokument, který je přístupný všem dovozcům. Jako zúčastněné strany šetření mají dovozci navíc přístup k verzi podnětu, která nemá důvěrnou povahu, a ke spisu, který nemá důvěrnou povahu. Komise byla proto toho názoru, že na základě toho dovozci věděli nebo měli vědět o dumpingu, jeho rozsahu a údajné újmě (3). |
|
(12) |
Jak je uvedeno v 5. bodě odůvodnění, k žádosti o zavedení celní evidence předložilo připomínky několik zúčastněných stran. Pokud jde o první kritérium, vláda Turecka, společnosti Habas, ÇİB a skupiny Colakoglu a Erdemir zdůraznily, že pouhé zahájení antidumpingového šetření automaticky neznamená, že k dumpingu skutečně dochází, neboť některá šetření (z nichž některá se týkají Turecka) jsou ukončena bez uložení cel. Půjde spíše o „jednostranné tvrzení“. Dovozce si tedy nemůže být vědom něčeho („dumpingových praktik“), co ještě nebylo prokázáno šetřením. Vláda Turecka a společnosti Habas a ÇİB rovněž zpochybnily některé další důkazy uvedené v žádosti Evropským ocelářským svazem, včetně tvrzení, že ředitel tureckého vyvážejícího výrobce věděl o nadcházejícím antidumpingovém šetření, a informace, že dovoz dotčeného výrobku je ve třetích zemích předmětem opatření na ochranu obchodu. Konečně, sdružení TCUD uvedlo, že některá z tvrzení o antidumpingových opatřeních proti tureckému dovozu dotčeného výrobku, jež Evropský ocelářský svaz uvedl, nejsou v podání popsána pravdivě. V tomto smyslu sdružení TCUD namítlo, že z opatření USA byla po námitce před příslušnými soudy jedna společnost vyňata a že antidumpingová cla proti Turecku zrušila po rozhodnutí panelu WTO další třetí země (Maroko). |
|
(13) |
V čl. 14 odst. 5 základního nařízení je stanoveno, že od zahájení šetření a poté, co jsou včas informovány všechny členské státy, může Komise vyzvat celní orgány, aby přijaly vhodná opatření k zavedení celní evidence dovozu, aby následně mohla být vůči dováženým výrobkům zavedena opatření ode dne dané celní evidence. Hlavním cílem celní evidence dovozu je v tomto případě umožnit uložení prozatímních opatření se zpětnou účinností až 90 dnů před jejich uplatněním v souladu s čl. 10 odst. 4 základního nařízení. Vzhledem k tomuto ustanovení nemůže Komise evidovat dovozy poté, co již bylo uloženo prozatímní clo. |
|
(14) |
Pokud by byla celní evidence dovozu možná až poté, co byl dumping zjištěn vyšetřováním, jak navrhují některé strany, tak by z definice nikdy nemohla být prováděna před uložením prozatímních cel. Tento přístup by nástroj celní evidence zcela zbavil zamýšleného účinku (effet utile) (4). Komise proto musí rozhodnout, zda má, či nemá evidovat dovoz ještě před stanovením prozatímního cla. V této souvislosti Komise uvedla, že ve fázi, kdy žadatel podal žádost o zavedení celní evidence, byly údaje uvedené v žádosti, na jejichž základě, jak je uvedeno v oznámení o zahájení, Komise zahájila antidumpingové šetření, nejlepšími dostupnými informacemi, které uvedly existenci důkazů ukazujících, že dochází k dumpingu působícímu újmu. Komise proto tato tvrzení zamítla jako nedůvodná. Vzhledem k tomuto zjištění kromě toho nemusela Komise posuzovat další důkazy, které jsou zmiňovány výše a které se týkají dovozu tureckých vyvážejících výrobců do třetích zemí, ani související argumenty. |
|
(15) |
Komise tak dospěla k závěru, že první kritérium pro celní evidenci bylo splněno. |
3.2. Další podstatné zvýšení dovozu
|
(16) |
Komise analyzovala toto kritérium na základě statistických údajů o dotčeném výrobku, které jsou dostupné v databázi Surveillance 2. Při posuzování, zda od zahájení šetření došlo k dalšímu podstatnému zvýšení, Komise nejprve určila časová období, jež je třeba porovnat. Na jedné straně posoudila údaje o dovozu z Turecka po zahájení antidumpingového šetření (tj. od okamžiku, od kterého si dovozci byli nebo měli být vědomi dumpingových praktik) až do posledního období, tj. období od června do poloviny října 2020. Na druhé straně Komise vypočetla turecký dovoz za stejné období v průběhu šetření (5) (tj. od června do poloviny října 2019) a průměrné měsíční objemy dovozu za celé období šetření. |
|
(17) |
Komise dospěla k závěru, že v tomto případě by srovnání mezi průměrnými měsíčními objemy dovozu po zahájení šetření a průměrnými tureckými měsíčními objemy dovozu v celém období šetření s ohledem na vývoj trhu a výsledek hromadění zásob v důsledku probíhajících ochranných opatření postihujících dotčený výrobek nestačilo na posouzení, zda došlo k podstatnému nárůstu dovozu. Komise tedy usoudila, že je vhodné vycházet z porovnání průměrných měsíčních objemů dovozu po zahájení šetření se stejnou dobou v období šetření, aby to lépe odráželo potenciální vliv probíhajících ochranných opatření na průběh dovozních toků z Turecka v posuzovaném období (6). Srovnání objemů dovozu po zahájení šetření s objemy dovozů ve stejném období předchozího roku by navíc zohlednilo případné sezónní vlivy (7). |
|
(18) |
Pokud jde o vliv ochranných opatření na turecké dovozní toky, Komise uvedla, že po celý rok 2019 (období šetření) byl turecký dovoz dotčeného výrobku ovlivněn četnými úpravami fungování ochranných opatření, jež ovlivnily vývozní chování z Turecka. |
|
(19) |
Za prvé, leden 2019, zdaleka nejvýkonnější měsíc tureckého dovozu dotčeného výrobku, se časově shodoval s posledním měsícem prozatímních ochranných opatření. V tomto ohledu panovala na trhu nejistota, v jaké formě budou přijata konečná opatření. Komise uvedla, že objem bezcelní kvóty neprodaný do konce tohoto měsíce se do následujícího období nepřevádí, tj. objemy bezcelní kvóty budou „ztraceny“. K podobné situaci, tj. poslední měsíc (měsíce) před novým obdobím opatření, došlo ve čtvrtletí únor–březen 2019. Za druhé, v únoru, dubnu, červenci a říjnu roku 2019 byly otevřeny nové tranše kvót s bezcelní sazbou. Na základě ochranných opatření u některých výrobků z oceli každé otevření celní kvóty obvykle vedlo na začátku každého čtvrtletí k dovozu velkých objemů. Konečně, v srpnu 2019 Komise ohlásila v rámci prvního přezkumného šetření ochranných opatření v oblasti oceli, že pro dovoz dotčeného výrobku z Turecka stanoví 30 % strop nad celní kvótu dostupnou v rámci příslušné kategorie výrobků, což také vedlo k nárůstu dovozu před touto změnou správy celních kvót. |
|
(20) |
Komise dále zdůraznila, že výše uvedené události ovlivnil tok objemů dovozu, jak se ukázalo ve statistikách. Zejména na měsíce leden, březen a září připadá první, druhé a čtvrté místo z hlediska objemů, které Turecko v roce 2019 měsíčně vyvezlo (v některých případech šlo o významně vyšší objemy než v jakémkoli jiném měsíci tohoto roku) (8). Proto Komise dospěla k závěru, že všechna tato regulační opatření v rámci ochranných opatření v oblasti oceli významně ovlivnila chování účastníků trhu a trend toků dovozu v celém roce. |
|
(21) |
Situace v podstatně kratším období (od června do poloviny října) byla regulačními změnami správy celních kvót ovlivněna méně. Komise proto porovnala průměrný měsíční objem tureckého dovozu v období od června do poloviny října 2020 s průměrným měsíčním objemem dovozu ve stejném období předchozího roku – 2019. |
|
(22) |
Srovnání ukazuje, že průměrný měsíční objem dovozu z Turecka se v tomto období zvýšil o 6 %.
Zdroj: databáze Surveillance 2 |
||||||||||||||
|
(23) |
Komise dále zkoumala trendy dovozu ve zvoleném období a příslušné době v rámci období šetření, aby stanovila, zda uvedený 6 % nárůst v tomto případě představuje podstatné zvýšení dovozu. Komise zejména zjistila, že v měsíci září 2020 byly objemy dovozu z Turecka zanedbatelné. Tyto výjimečně nízké objemy dovozu byly do velké míry způsobeny skutečností, že na základě ochranných opatření v oblasti oceli Turecko v tomto měsíci v podstatě vyčerpalo svou celní kvótu u kategorie výrobků 1 (do níž patří dotčený výrobek), a proto by mohlo vyvážet významné množství dotčeného výrobku pouze s 25 % clem (10). Tento výjimečně nízký objem dovozu v září 2020 do velké míry snížil průměrné měsíční objemy dovozu v příslušném období zvoleném Komisí k provedení srovnání (od června do poloviny října 2020). Komise současně uvedla, že přesně ve stejném měsíci předchozího roku, v září 2019, byl objem dovozu velmi vysoký vzhledem ke skutečnosti, že v říjnu 2019 nabyly účinnosti úpravy po prvním přezkumném šetření ochranných opatření. V očekávání těchto událostí tak turečtí výrobci v průběhu měsíce září 2019 vyvezli velmi velká množství. |
|
(24) |
S ohledem na skutečnosti uvedené v předchozím bodě odůvodnění dospěla Komise k závěru, že dovoz v měsíci září roku 2019 a roku 2020 není reprezentativní, a posoudila také úrovně dovozu bez zahrnutí tohoto měsíce v obou letech. Toto porovnání potvrdilo, že nárůsty objemů dovozu byly v porovnání se stejnými měsíci v průběhu období šetření velmi významné. Například při porovnávání období od června do srpna v roce 2020 a stejného období v roce 2019 došlo k nárůstu o 44 %. Při porovnání období od června do poloviny října 2020 se stejným obdobím v roce 2019 by při vynechání měsíce září rovněž došlo k významnému nárůstu o 49 %. S ohledem na tyto skutečnosti dospěla Komise k závěru, že nárůst dovozu je v tomto případě podstatný. |
|
(25) |
Pokud jde o toto kritérium, vláda Turecka, společnosti Habas, ÇİB, skupiny Colakoglu a Erdemir a konsorcium uživatelů ploché za tepla válcované oceli zpochybnily období navržené žadatelem pro posouzení, zda došlo k podstatnému nárůstu dovozů. Místo toho tyto strany navrhly jiná období pro provedení těchto porovnání, která by podle jejich názoru ukázala, že toto kritérium nebylo splněno. Společnost Habas a konsorcium uživatelů ploché za tepla válcované oceli navrhly, že čtvrtletní porovnání stejných období roku 2019 a prvního pololetí roku 2020, tj. prvních dvou čtvrtletí každého roku, by ukázalo pokles dovozu. Společnosti ÇİB a skupiny Colakoglu a Erdemir namítly, že období zvolené Evropským ocelářským svazem, tedy od června do července 2020, je příliš krátké, a není tedy reprezentativní. Kromě toho společnost ÇİB a konsorcium uživatelů ploché za tepla válcované oceli uvedly, že důvody pro zvýšení dovozu byly stejně důsledkem uvolnění omezení volného pohybu osob v Unii souvisejícího s pandemií COVID-19, které se časově shodovalo s ranými fázemi období po zahájení šetření. Společnost ÇİB namítla, že Komise musí porovnávat objem dovozu, k němuž došlo po zahájení šetření, s objemem dovozu, který se uskutečnil v průběhu období šetření. Tato strana dále namítla, že turecké dovozy vykazovaly od ledna do května 2020 stabilní pokles a že se v měsíci červnu a červenci 2020 zvýšily a navrátily na „svou obvyklou úroveň“. Dále společnost ÇİB dospěla k závěru, že Komise by neměla brát v úvahu údaje po zahájení šetření za červen 2020 vzhledem k dopadu údajné zvláštní situace „po karanténě“. V tomto případě by srovnání s měsíčním průměrem v období šetření ukázalo nárůst ve výši 12 %, což nesplňuje podmínky „dalšího podstatného nárůstu“, ale jde spíše o „velmi mírný“ nárůst. Další strany navrhly posuzovat trendy dovozu v prvních sedmi měsících (od ledna do července) období od roku 2017 do roku 2020, trendy dovozu v letech 2017 až 2020 (roční vyjádření) (11), měsíční průměr v letech 2018 a 2019 s měsíčním průměrem v období od ledna do července 2020, měsíční průměr v období od ledna do července 2018 a 2019 se stejným obdobím v roce 2020 a měsíční průměr v období šetření s objemem dovozu v měsíci červenci 2020 (12), aby ukázaly, že došlo k poklesu v dovozu. Skupiny Colakoglu a Erdemir rovněž poukázaly na skutečnost, že v žádosti nebyly uvedeny žádné údaje o dovozu od konce období šetření do zahájení šetření, přestože mezi těmito dvěma okamžiky uplynula určitá doba. |
|
(26) |
Konsorcium uživatelů ploché za tepla válcované oceli kromě toho dále uvedlo, že celní evidence sníží úroveň dovozu a způsobí nedostatečnou nabídku, což ohrozí provoz některých výrobních zařízení uživatelů usazených v Unii. Údajně by to narušilo trh a způsobilo nenapravitelnou újmu nezávislým uživatelům dotčeného výrobku. |
|
(27) |
Všechny zúčastněné strany, které reagovaly na žádost o celní evidenci od Evropského ocelářského svazu, shodně tvrdily, že vzhledem k dopadům ochranných opatření v oblasti oceli na Turecko nebude Turecko moci v nadcházejících měsících (tj. v měsících před stanovením prozatímních antidumpingových opatření) dále zvyšovat svůj vývoz, a že by tedy Komise neměla žádosti o celní evidenci vyhovět. |
|
(28) |
Pokud jde o různá období navrhovaná stranami, Komise odkazuje na zdůvodnění a vysvětlení uvedená výše v oddílu 3.2. V této souvislosti je však třeba řadu tvrzení vyvrátit. Komise v první řadě uvádí, že i když obvykle srovnává také průměrný měsíční dovoz v období po zahájení šetření s průměrnými úrovněmi dovozu v období šetření, nemusí být toto srovnání vždy vhodné. V tomto případě Komise zjistila a ve výše uvedeném 16. až 20. bodě odůvodnění vysvětlila, že s ohledem na konkrétní tržní okolnosti, pokud jde o šetřený dovoz, není použití průměrného dovozu v roce 2019 nejvhodnějším východiskem pro srovnání. |
|
(29) |
Za druhé, Komise uvádí, že jeden z návrhů odkazoval na trendy z období před zahájením antidumpingového šetření. To by nebylo v souladu se zjištěním, že povědomí o dumpingových praktikách z Turecka vyplývá ze zveřejnění oznámení o zahájení šetření. Trend dovozu z období před okamžikem, kdy si dovozce mohl být vědom existence dumpingu, se při posuzování, zda je žádost o celní evidenci opodstatněná, tedy nebere v úvahu. |
|
(30) |
Za třetí, Komise dále uvádí, že i když výchozí bod pro analýzu představuje žádost Evropského ocelářského svazu, musí Komise přesto provést i svou vlastní komplexní analýzu. V tomto směru má Komise k dispozici soubor údajů za pozdější období, než je období uvedené v žádosti Evropského ocelářského svazu (a to do poloviny října 2020) (13). Komise kromě toho považovala za vhodnější porovnávat tento soubor údajů se stejnou dobou v období šetření, a to z výše uvedených důvodů. |
|
(31) |
Komise se tedy nedomnívá, že by odlišné návrhy ukázaly přesvědčivé důvody, díky nimž by byly k posouzení trendů dovozu vhodnější než návrh uvedený v oddíle 3.2. Komise proto tato tvrzení zamítla. |
|
(32) |
Pokud jde o tvrzení, že s ohledem na zavedená ochranná opatření stejně nehrozí žádné nebezpečí dalšího podstatného nárůstu dovozu, Komise s těmito tvrzeními z následujících důvodů nesouhlasila. |
|
(33) |
Za prvé, celní evidence nepředjímá rozhodnutí o vybírání prozatímních antidumpingových cel se zpětnou působností. Zda ochranná opatření zabrání nárůstu dovozu do uložení prozatímních opatření, by mělo být posuzováno v souvislosti s případným vybíráním cel se zpětnou působností (14). |
|
(34) |
Komise v každém případě uznává, že v důsledku změn zavedených ochrannými opatřeními od 1. července 2020 se na Turecko vztahuje celní kvóta pro Turecko, jejíž čtvrtletní objemy jsou stanoveny v příloze II prováděcího nařízení Komise (EU) 2020/894 (15). Pokud jsou tyto objemy vyčerpány, může Turecko stejně i nadále do Unie vyvážet (16). |
|
(35) |
Komise však nesouhlasí s tím, že by tato skutečnost sama o sobě automaticky bránila podstatnému nárůstu dovozu z Turecka před uložením případného prozatímního antidumpingového cla. Je tomu tak proto, že do doby, než mohou být nejpozději uložena prozatímní cla, tedy do poloviny ledna 2021, by pro Turecko byly uvolněny dvě tranše bezcelních kvót (17). Kromě toho by případné srovnání objemů dovozu za účelem posouzení, zda je vybírání cel se zpětnou působností opodstatněné, mohlo zahrnovat také období před okamžikem, kdy se na Turecko začala vztahovat celní kvóta, jak je vysvětleno výše ve 18. až 19. bodě odůvodnění. V této fázi proto neexistuje žádný důkaz, že by celkové objemy, které by Turecko mohlo vyvážet bezcelně (a s 25 % clem) až do případného uložení prozatímních antidumpingových opatření, nemohly představovat další podstatné zvýšení. V každém případě bude Komise moci učinit závěr k této záležitosti až v případě, že po ukončení probíhajícího šetření bude stanoveno konečné antidumpingové clo. |
|
(36) |
Komise proto zamítá tvrzení, že vzhledem k zavedeným ochranným opatřením je třeba další podstatný nárůst dovozu vyloučit. |
|
(37) |
Konečně, Komise uvádí, že připomínka vznesená konsorciem uživatelů týkající se dopadu celní evidence na nabídku dotčeného výrobku a na nezávislé uživatele nespadá pod právní požadavky, jež mají být při rozhodování o celní evidenci dovozu posuzovány. V této fázi řízení se jí proto Komise nezabývá. |
|
(38) |
Vzhledem k výše uvedeným skutečnostem Komise dospěla k závěru, že bylo splněno i druhé kritérium pro celní evidenci. |
3.3. Ohrožení vyrovnávacího účinku cla
|
(39) |
Komise má k dispozici dostatečné důkazy o tom, že pokračující nárůst dovozu z Turecka za stále nižší ceny by způsobil další újmu. |
|
(40) |
Jak je uvedeno v oddíle 3.2, existují dostatečné důkazy o podstatném zvýšení dovozu dotčeného výrobku. |
|
(41) |
Kromě toho existují důkazy o klesajícím trendu v dovozních cenách dotčeného výrobku. V tomto ohledu dovozní ceny z Turecka do Unie poklesly v období od června do poloviny října 2020 v průměru o 13 % při porovnání se stejným obdobím roku 2019 a o 14 % při porovnání s měsíčním průměrem v období šetření.
Zdroj: databáze Surveillance 2 |
||||||||||||||
|
(42) |
Je proto pravděpodobné, že další nárůst dovozu po zahájení řízení by s ohledem na jeho načasování, objem a jiné okolnosti, jako je chování vyvážejících výrobců v oblasti tvorby cen, mohl vážně ohrozit vyrovnávací účinek jakéhokoli konečného cla, pokud by toto clo nebylo uloženo se zpětnou působností. |
|
(43) |
Komise proto dospěla k závěru, že bylo splněno i třetí kritérium pro celní evidenci. |
4. POSTUP
|
(44) |
Komise dospěla k závěru, že existují dostatečné důkazy, které odůvodňují zavedení celní evidence dovozu dotčeného výrobku podle čl. 14 odst. 5 základního antidumpingového nařízení. |
|
(45) |
Všechny zúčastněné strany se vyzývají, aby písemně sdělily svá stanoviska a poskytly příslušné důkazy. Komise může zúčastněné strany vyslechnout, pokud o to písemně požádají a uvedou zvláštní důvody pro takové slyšení. |
5. CELNÍ EVIDENCE
|
(46) |
Podle čl. 14 odst. 5 základního nařízení by u dotčeného výrobku měla být zavedena celní evidence dovozu, aby v případě, že výsledkem šetření budou zjištění, jež povedou k uložení antidumpingových cel, a pokud budou splněny nezbytné podmínky, mohla být tato cla uložena na celně evidovaný dovoz se zpětnou působností v souladu s platnými právními ustanoveními. |
|
(47) |
Případný budoucí celní dluh by vycházel ze zjištění antidumpingového šetření. |
|
(48) |
Tvrzení v podnětu, na jejichž základě bylo zahájeno antidumpingové šetření, odhadují pro dotčený výrobek dumpingové rozpětí od 4 % do 8 % a úrovně odstranění újmy od 10 % do 25 %. Výši možného budoucího celního dluhu lze odhadnout na úrovni nejvyššího dumpingového rozpětí odhadnutého na základě podnětu, tj. 8 % jako podíl dovozní hodnoty CIF dotčeného výrobku. |
6. ZPRACOVÁNÍ OSOBNÍCH ÚDAJŮ
|
(49) |
S veškerými osobními údaji shromážděnými v souvislosti s celní evidencí bude nakládáno v souladu s nařízením Evropského parlamentu a Rady (EU) 2018/1725 (18), |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
1. Celní orgány se vyzývají, aby podle čl. 14 odst. 5 nařízení (EU) 2016/1036 přijaly vhodná opatření k zavedení celní evidence dovozu plochých válcovaných výrobků ze železa, nelegované oceli nebo ostatní legované oceli, též ve svitcích (včetně výrobků „zkracovaných na míru“ a „úzkých pásů“), po válcování za tepla již dále neopracovaných, neplátovaných, nepokovených ani nepotažených, do Unie. Tyto výrobky mají v současnosti kódy KN 7208 10 00, 7208 25 00, 7208 26 00, 7208 27 00, 7208 36 00, 7208 37 00, 7208 38 00, 7208 39 00, 7208 40 00, 7208 52 10, 7208 52 99, 7208 53 10, 7208 53 90, 7208 54 00, 7211 13 00, 7211 14 00, 7211 19 00, ex 7225 19 10 (kód TARIC 7225191090), 7225 30 90, ex 7225 40 60 (kód TARIC 7225406090), 7225 40 90, ex 7226 19 10 (kód TARIC 7226191090), 7226 91 91 a 7226 91 99 a pocházejí z Turecka.
2. Celní evidence končí po uplynutí devíti měsíců ode dne vstupu tohoto nařízení v platnost.
3. Všechny zúčastněné strany se vyzývají, aby písemně sdělily svá stanoviska a poskytly příslušné důkazy nebo požádaly o slyšení do 21 dnů ode dne vyhlášení tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost prvním dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 12. listopadu 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 176, 30.6.2016, s. 21.
(2) Úř. věst. C 166, 14.5.2020, s. 9.
(3) Viz rozsudek Tribunálu (druhého senátu) ze dne 8. května 2019 ve věci T-749/16, Stemcor v. Evropská komise, bod 56.
(4) Viz rozsudek Tribunálu (druhého senátu) ze dne 8. května 2019 ve věci T-749/16, Stemcor v. Evropská komise, bod 33.
(5) Období šetření zahrnovalo období od 1. ledna 2019 do 31. prosince 2019.
(6) Dovoz dotčeného výrobku z Turecka je předmětem ochranných opatření od poloviny července 2018 (v rámci kategorie výrobků 1). Celní kvóty jsou na základě ochranných opatření spravovány čtvrtletně. Porovnáním stejných období je tak trend méně ovlivněn četnými změnami správy celních kvót, k nimž došlo v průběhu období šetření, což je celý rok (2019), neboť na Turecko se v průběhu roku 2019 v rámci systému správy celních kvót vztahovaly tři různé režimy.
(7) Komise uvedla, že u dotčeného výrobku ukazuje letní období soustavný pokles spotřeby v porovnání s předchozím obdobím. Období, jež Komise v tomto případě použila, by tak vyloučila zkreslení, pokud jde o případné sezónní vlivy.
(8) Průměrné objemy dovozu v těchto měsících jsou ve skutečnosti více než dvojnásobné v porovnání s průměrnými objemy dovozu ve zbývajících devíti měsících roku 2019.
(9) Toto srovnání je považováno za vhodnější, viz výše uvedený 17.–21. bod odůvodnění.
(10) Do doby, kdy byla k dispozici další tranše celní kvóty pro Turecko.
(11) Konsorcium uživatelů ploché za tepla válcované oceli.
(12) Skupiny Colakoglu a Erdemir.
(13) V žádosti Evropského ocelářského svazu o celní evidenci byly uvedeny údaje pouze za měsíce červen a červenec 2020.
(14) To znamená, až budou k dispozici údaje o dovozu za příslušné období, které je třeba posoudit, aby mohlo být rozhodnuto, zda je vybírání cel se zpětnou působností opodstatněné.
(15) Prováděcí nařízení Komise (EU) 2020/894 ze dne 29. června 2020, kterým se mění prováděcí nařízení (EU) 2019/159 o zavedení konečných ochranných opatření proti dovozu některých výrobků z oceli (Úř. věst. L 206, 30.6.2020, s. 27).
(16) S výhradou 25 % cla až do otevření další tranše celní kvóty v následujícím čtvrtletí.
(17) Období odpovídající čtvrtletím od října do prosince 2020, respektive od ledna do března 2021.
(18) Nařízení Evropského parlamentu a Rady (EU) 2018/1725 ze dne 23. října 2018 o ochraně fyzických osob v souvislosti se zpracováním osobních údajů orgány, institucemi a jinými subjekty Unie a o volném pohybu těchto údajů a o zrušení nařízení (ES) č. 45/2001 a rozhodnutí č. 1247/2002/ES (Úř. věst. L 295, 21.11.2018, s. 39).
SMĚRNICE
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/55 |
SMĚRNICE KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2020/1687
ze dne 2. září 2020,
kterou se mění příloha rámcového rozhodnutí Rady 2004/757/SVV, pokud jde o zahrnutí nové psychoaktivní látky N,N-diethyl-2-[[4-(1-methylethoxy)fenyl]methyl]-5-nitro-1H-benzimidazol-1-ethanamin (isotonitazen) do definice drogy
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na rámcové rozhodnutí Rady, kterou se mění definice drogy v rámcovém rozhodnutí Rady 2004/757/SVV ze dne 25. října 2004, kterým se stanoví minimální ustanovení týkající se znaků skutkových podstat trestných činů a sankcí v oblasti nedovoleného obchodu s drogami (1), a zejména na články 1a a 8a uvedeného rozhodnutí,
vzhledem k těmto důvodům:
|
(1) |
Zpráva o hodnocení rizik nové psychoaktivní látky N,N-diethyl-2-[[4-(1-methylethoxy)fenyl]methyl]-5-nitro-1H-benzimidazol-1-ethanamin (isotonitazen) byla vypracována dne 26. května 2020 v souladu s článkem 5c nařízení Evropského parlamentu a Rady (ES) č. 1920/2006 (2) vědeckým výborem Evropského monitorovacího centra pro drogy a drogovou závislost (EMCDDA, dále jen „centrum EMCDDA“) rozšířeným v souladu s postupem podle čl. 5c odst. 4 téhož nařízení. Dne 29. května 2020 předložilo centrum EMCDDA dotčenou zprávu o hodnocení rizik Komisi a členským státům. |
|
(2) |
Isotonitazen je syntetické opioidní analgetikum a je velmi podobný látkám etonitazen a klonitazen, které obě podléhají mezinárodní kontrole podle Jednotné úmluvy OSN o omamných látkách z roku 1961 ve znění protokolu z roku 1972. |
|
(3) |
Isotonitazen je v Unii dostupný přinejmenším od dubna 2019 a byl zjištěn v pěti členských státech i ve Spojeném království. Čtyři členské státy ohlásily 24 případů zabavení této látky; kromě toho jeden členský stát ohlásil jeden odebraný vzorek a Spojené království ohlásilo biologické vzorky odebrané post mortem. Obecně platí, že isotonitazen není pravděpodobně dostatečně odhalován, jelikož se kvůli svému novému výskytu na trhu běžně nezjišťuje. Ve většině případů byla tato látka zabavena ve formě prášku, avšak byla rovněž identifikována v kapalné formě. Ačkoliv jsou zjištěná množství poměrně malá, musí být posuzována v kontextu vysoké účinnosti isotonitazenu. |
|
(4) |
Německo a Spojené království už v souvislosti s isotonitazenem ohlásily dva případy úmrtí, ke kterým došlo v roce 2019. O případu úmrtí v Německu nejsou k dispozici žádné podrobné informace. V případě ohlášeném Spojeným královstvím bylo v biologických vzorcích odebraných post mortem identifikováno několik dalších látek. (3) Dosud nebyly hlášeny žádné akutní intoxikace, u nichž by se potvrdila expozice isotonitazenu. Je pravděpodobné, že při otravě způsobené isotonitazenem působí jako antidotum naloxon, stejně jako u jiných syntetických opioidů. Jak případy intoxikace, tak případy úmrtí nejsou pravděpodobně dostatečně odhalovány ani ohlašovány, protože tato látka se běžně nezjišťuje a na trhu Unie se objevila teprve nedávno. |
|
(5) |
Nejsou k dispozici žádné přímé důkazy svědčící o účasti organizovaného zločinu na výrobě a distribuci isotonitazenu či na nedovoleném obchodu s ním a na jeho dodávkách v rámci Unie. Z dostupných informací vyplývá, že isotonitazen vyrábějí chemické podniky sídlící mimo Unii. |
|
(6) |
Isotonitazen se obvykle prodává on-line v malých a velkoobchodních množstvích, zejména ve formě prášku; prodává se také jako nosní spreje připravené k použití. Informace získané při zabavení naznačují, že se isotonitazen možná prodával také na nelegálním trhu s opioidy. Uživatelé si proto nemusí být vědomi, že užívají isotonitazen. |
|
(7) |
Isotonitazen nemá v Unii a zdá se, že ani jinde ve světě, žádné uznávané humánní lékařské nebo veterinární využití. Nic nenasvědčuje tomu, že by tato látka mohla být používána k jiným účelům než jako analytický referenční standard a ve vědeckém výzkumu. |
|
(8) |
Ze zprávy o hodnocení rizik vyplývá, že na řadu otázek souvisejících s isotonitazenem, jež vyvstávají z důvodu nedostatku údajů o rizicích pro zdraví osob, rizicích pro veřejné zdraví a o společenských rizicích, by bylo možné najít odpověď prostřednictvím dalšího výzkumu. Neexistují žádné konkrétní informace o společenských rizicích souvisejících s isotonitazenem. Dostupné důkazy a informace o zdravotních rizicích, které tato látka představuje, rovněž s ohledem na skutečnost, že dotčená látka je relativně neznámá, však poskytují dostatečný důvod pro zahrnutí isotonitazenu do definice drogy. |
|
(9) |
Isotonitazen není uveden na seznamu látek podléhajících kontrole podle Jednotné úmluvy OSN o omamných látkách z roku 1961 ve znění protokolu z roku 1972 ani podle Úmluvy OSN o psychotropních látkách z roku 1971. Isotonitazen není v současné době předmětem hodnocení v rámci systému OSN. |
|
(10) |
Vzhledem k tomu, že čtyři členské státy kontrolují isotonitazen podle vnitrostátních právních předpisů o kontrole drog a jeden členský stát, jakož i Spojené království a Norsko, kontrolují isotonitazen podle jiných právních předpisů, by zahrnutí této látky do definice drogy, aby se na ni vztahovala ustanovení o trestných činech a sankcích podle definice v rámcovém rozhodnutí Rady 2004/757/SVV, pomohlo zamezit vzniku překážek při přeshraničním prosazování práva a v justiční spolupráci a přispělo by k ochraně před riziky, která mohou představovat dostupnost a užívání této látky. |
|
(11) |
K zajištění rychlé a odborně podložené reakce na úrovni Unie na výskyt nových psychoaktivních látek, které zjistily a ohlásily členské státy, svěřuje článek 1a rámcového rozhodnutí 2004/757/SVV Komisi pravomoc přijímat akty v přenesené pravomoci za účelem změny přílohy uvedeného rámcového rozhodnutí a zahrnutí takových látek do definice drogy. |
|
(12) |
Dostupné informace naznačují, že užívání isotonitazenu způsobuje poškození zdraví ve spojení s jeho akutní toxicitou a náchylností ke zneužívání nebo jeho potenciálem k rozvoji závislosti. Toto poškození zdraví je považováno za život ohrožující. Kromě toho existuje potenciál pro závažné fyzické nebo duševní poruchy a významné šíření nemocí, včetně přenosu virů přenášených krví. Tyto účinky, včetně závislosti, jsou srovnatelné s jinými opioidními analgetiky, které podléhají mezinárodní kontrole. |
|
(13) |
Podmínky a postup pro výkon pravomoci přijmout akt v přenesené pravomoci jsou splněny, a proto by měla být přijata směrnice v přenesené pravomoci za účelem zahrnutí isotonitazenu do přílohy rámcového rozhodnutí 2004/757/SVV, aby se na něj v důsledku toho vztahovaly trestněprávní předpisy Unie o nedovoleném obchodu s drogami. |
|
(14) |
Irsko je vázáno rámcovým rozhodnutím 2004/757/SVV ve znění směrnice (EU) 2017/2103 (4), a tudíž se účastní přijímání a používání tohoto rozhodnutí. |
|
(15) |
Dánsko je vázáno rámcovým rozhodnutím 2004/757/SVV ve znění použitelném do 21. listopadu 2018, není však vázáno směrnicí (EU) 2017/2103. Dánsko se tedy nepodílí na přijímání a používání této směrnice a tato směrnice pro ně není závazná ani použitelná. |
|
(16) |
Členské státy se v souladu se společným politickým prohlášením členských států a Komise ze dne 28. září 2011 o informativních dokumentech (5) zavázaly, že v odůvodněných případech doplní oznámení o opatřeních přijatých za účelem provedení směrnice ve vnitrostátním právu o jeden či více dokumentů s informacemi o vztahu mezi jednotlivými složkami směrnice a příslušnými částmi vnitrostátních nástrojů přijatých za účelem provedení směrnice ve vnitrostátním právu. |
|
(17) |
Rámcové rozhodnutí 2004/757/SVV by proto mělo být odpovídajícím způsobem změněno, |
PŘIJALA TUTO SMĚRNICI:
Článek 1
Změna rámcového rozhodnutí 2004/757/SVV
V příloze rámcového rozhodnutí 2004/757/SVV se doplňuje nový bod 17, který zní:
|
„17. |
N,N-diethyl-2-[[4-(1-methylethoxy)fenyl]methyl]-5-nitro-1H-benzimidazol-1-ethanamin (isotonitazen). (*1) |
Článek 2
Provedení
1. Členské státy uvedou v účinnost právní a správní předpisy nezbytné pro dosažení souladu s touto směrnicí nejpozději do 3. června 2021. Neprodleně sdělí Komisi jejich znění.
Tyto předpisy přijaté členskými státy musí obsahovat odkaz na tuto směrnici nebo musí být takový odkaz učiněn při jejich úředním vyhlášení. Způsob odkazu si stanoví členské státy.
2. Členské státy sdělí Komisi znění hlavních ustanovení vnitrostátních právních předpisů, které přijmou v oblasti působnosti této směrnice.
Článek 3
Vstup v platnost
Tato směrnice vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Článek 4
Tato směrnice je určena členským státům v souladu se Smlouvami.
V Bruselu dne 2. září 2020.
Za Komisi
Ursula VON DER LEYEN
předsedkyně
(1) Úř. věst. L 335, 11.11.2004, s. 8.
(2) Nařízení Evropského parlamentu a Rady (ES) č. 1920/2006 ze dne 12. prosince 2006 o Evropském monitorovacím centru pro drogy a drogovou závislost (Úř. věst. L 376, 27.12.2006, s. 1).
(3) Tři případy úmrtí ohlásila také Kanada a 18 případů Spojené státy.
(4) Směrnice Evropského parlamentu a Rady (EU) 2017/2103 ze dne 15. listopadu 2017, kterou se mění rámcové rozhodnutí Rady 2004/757/SVV s cílem zahrnout do definice drogy nové psychoaktivní látky a zrušuje rozhodnutí Rady 2005/387/SVV (Úř. věst. L 305, 21.11.2017, s. 12).
ROZHODNUTÍ
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/58 |
ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2020/1688
ze dne 25. září 2020,
kterým se mění rozhodnutí (EU) 2020/187 o provádění třetího programu nákupu krytých dluhopisů (ECB/2020/48)
RADA GUVERNÉRŮ EVROPSKÉ CENTRÁLNÍ BANKY,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 127 odst. 2 první odrážku této smlouvy,
s ohledem na statut Evropského systému centrálních bank a Evropské centrální banky, a zejména na druhý pododstavec článku 12.1 ve spojení s čl. 3.1 první odrážkou a článkem 18.1 tohoto statutu,
vzhledem k těmto důvodům:
|
(1) |
Rozhodnutím Evropské centrální banky (ECB) 2014/40 (1) byl zaveden třetí program nákupu krytých dluhopisů (third covered bond purchase programme – CBPP3); uvedené rozhodnutí bylo přepracováno rozhodnutím Evropské centrální banky (EU) 2020/187 (ECB/2020/8) (2). CBPP3 je spolu s programem nákupu cenných papírů krytých aktivy, programem nákupu aktiv veřejného sektoru na sekundárních trzích a programem nákupu cenných papírů podnikového sektoru součástí rozšířeného programu nákupu aktiv (asset purchase programme – APP) Evropské centrální banky (ECB). Cílem APP je zlepšit transmisi měnové politiky, usnadnit poskytování úvěrů hospodářství eurozóny, uvolnit úvěrové podmínky pro domácnosti a podniky a přispět k návratu míry inflace ve střednědobém horizontu pod 2 %, ale blízko této úrovně, což je v souladu s prvořadým cílem ECB udržovat cenovou stabilitu. |
|
(2) |
Rada guvernérů dne 5. března 2020 v zásadě rozhodla o automatickém omezení přístupu způsobilé protistrany k operacím měnové politiky Eurosystému za určitých předem stanovených okolností. V návaznosti na to Rada guvernérů rovněž rozhodla, že pokud se na základě obecných zásad Evropské centrální banky (EU) 2015/510 (ECB/2014/60) (3) uplatňuje takové automatické omezení, pozastavení či vyloučení přístupu, mělo by se po dobu tohoto omezení, pozastavení nebo vyloučení přístupu uplatňovat též odpovídající automatické vyloučení dluhopisů vydaných dotčenou protistranou z nákupů v rámci programu CBPP3. Rada guvernérů dále rozhodla, že změny, kterými se zohlední tato rozhodnutí, by se měly uplatňovat ode dne použití příslušné každoroční změny obecných zásad (EU) 2015/510 (ECB/2014/60). |
|
(3) |
Rozhodnutí (EU) 2020/187 (ECB/2020/8) je proto třeba příslušným způsobem změnit, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Změna
Rozhodnutí (EU) 2020/187 (ECB/2020/8) se mění takto:
V čl. 3 odst. 3 se písmeno d) nahrazuje tímto:
|
„d) |
Kryté dluhopisy vydané úvěrovými institucemi, jejichž přístup k operacím měnové politiky Eurosystému byl omezen, pozastaven či vyloučen podle obecných zásad (EU) 2015/510 (ECB/2014/60), jsou po dobu tohoto omezení, pozastavení nebo vyloučení automaticky vyloučeny z nákupů v rámci programu CBPP3. Odchylně od první věty písm. d) si Rada guvernérů ponechává pravomoc na základě posouzení v jednotlivých případech znovu posoudit vyloučení krytých dluhopisů vydaných úvěrovou institucí, jejíž přístup k operacím měnové politiky Eurosystému byl omezen, pozastaven či vyloučen podle obecných zásad (EU) 2015/510 (ECB/2014/60), a považuje-li to za vhodné, toto vyloučení zrušit.“ |
Článek 2
Vstup v platnost
Toto rozhodnutí vstupuje v platnost dvacátým dnem po zveřejnění v Úředním věstníku Evropské unie.
Použije se ode dne 1. ledna 2021.
Ve Frankfurtu nad Mohanem dne 25. září 2020.
Za Radu guvernérů ECB
prezidentka ECB
Christine LAGARDE
(1) Rozhodnutí Evropské centrální banky ECB/2014/40 ze dne 15. října 2014 o provádění třetího programu nákupu krytých dluhopisů (Úř. věst. L 335, 22.11.2014, s. 22).
(2) Rozhodnutí Evropské centrální banky (EU) 2020/187 ze dne 3. února 2020 o provádění třetího programu nákupu krytých dluhopisů (ECB/2020/8) (Úř. věst. L 39, 12.2.2020, s. 6).
(3) Obecné zásady Evropské centrální banky (EU) 2015/510 ze dne 19. prosince 2014 o provádění rámce měnové politiky Eurosystému (obecné zásady o obecné dokumentaci) (ECB/2014/60) (Úř. věst. L 91, 2.4.2015, s. 3).
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/60 |
ROZHODNUTÍ EVROPSKÉHO ORGÁNU PRO CENNÉ PAPÍRY A TRHY (EU) 2020/1689
ze dne 16. září 2020,
kterým se obnovuje dočasný požadavek, aby fyzické nebo právnické osoby, které mají čisté krátké pozice, dočasně snížily prahové hodnoty pro oznamování čistých krátkých pozic ve vztahu k upsanému akciovému kapitálu společností, jejichž akcie jsou přijaty k obchodování na regulovaném trhu, a podaly příslušným orgánům oznámení o překročení určité prahové hodnoty v souladu s čl. 28 odst. 1 písm. a) nařízení Evropského parlamentu a Rady (EU) č. 236/2012
RADA ORGÁNŮ DOHLEDU EVROPSKÉHO ORGÁNU PRO CENNÉ PAPÍRY A TRHY,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na Dohodu o Evropském hospodářském prostoru, zejména na přílohu IX uvedené dohody,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 1095/2010 ze dne 24. listopadu 2010 o zřízení Evropského orgánu dohledu (Evropského orgánu pro cenné papíry a trhy), o změně rozhodnutí č. 716/2009/ES a o zrušení rozhodnutí Komise 2009/77/ES (1), a zejména na čl. 9 odst. 5, čl. 43 odst. 1 a čl. 44 odst. 1 uvedeného nařízení,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 236/2012 ze dne 14. března 2012 o prodeji na krátko a některých aspektech swapů úvěrového selhání (2), a zejména na čl. 28 odst. 1 uvedeného nařízení,
s ohledem na nařízení Komise v přenesené pravomoci (EU) č. 918/2012 ze dne 5. července 2012, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 236/2012 o prodeji na krátko a některých aspektech swapů úvěrového selhání, pokud jde o definice, výpočet čistých krátkých pozic, kryté swapy úvěrového selhání na státní dluhopisy, prahové hodnoty pro oznamovací povinnost, prahové hodnoty likvidity pro pozastavení omezení, významný pokles hodnoty finančních nástrojů a nepříznivé události (3), a zejména na článek 24 uvedeného nařízení,
s ohledem na rozhodnutí orgánu ESMA (EU) 2020/525 ze dne 16. března 2020, kterým vyžaduje, aby fyzické nebo právnické osoby, které mají čisté krátké pozice, dočasně snížily prahové hodnoty pro oznamování čistých krátkých pozic ve vztahu k upsanému akciovému kapitálu společností, jejichž akcie jsou přijaty k obchodování na regulovaném trhu, a podaly příslušným orgánům oznámení v souladu s čl. 28 odst. 1 písm. a) nařízení Evropského parlamentu a Rady (EU) č. 236/2012 (4),
s ohledem na rozhodnutí Evropského orgánu pro cenné papíry a trh (EU) 2020/1123 ze dne 10. června 2020, kterým se obnovuje dočasný požadavek, aby fyzické nebo právnické osoby, které mají čisté krátké pozice, dočasně snížily prahové hodnoty pro oznamování čistých krátkých pozic ve vztahu k upsanému akciovému kapitálu společností, jejichž akcie jsou přijaty k obchodování na regulovaném trhu, a podaly příslušným orgánům oznámení o překročení určité prahové hodnoty v souladu s čl. 28 odst. 1 písm. a) nařízení Evropského parlamentu a Rady (EU) č. 236/2012 (5),
vzhledem k těmto důvodům:
1. ÚVOD
|
(1) |
V souladu s rozhodnutím (EU) 2020/525 požadoval orgán ESMA, aby fyzické nebo právnické osoby, které mají čisté krátké pozice ve vztahu k upsanému akciovému kapitálu společností, jejichž akcie jsou přijaty k obchodování na regulovaném trhu, oznámily příslušným orgánům v souladu s čl. 28 odst. 1 písm. a) nařízení (EU) č. 236/2012 podrobné informace o veškerých takových pozicích, které dosáhly nebo překročily 0,1 % upsaného základního kapitálu nebo poklesly pod tuto hranici. |
|
(2) |
Opatření uložené rozhodnutím (EU) 2020/525 se týkalo nutnosti, aby příslušné vnitrostátní orgány byly s ohledem na výjimečné okolnosti na finančních trzích schopny monitorovat čisté krátké pozice, které účastníci trhu uzavřeli ve vztahu k akciím přijatým k obchodování na regulovaném trhu. |
|
(3) |
Rozhodnutím (EU) 2020/1123 obnovil orgán ESMA dočasný požadavek, neboť bez ohledu na částečné oživení finančních trhů EU ze ztrát zaznamenaných od vypuknutí pandemie zůstal výhled na budoucí oživení nejistý a přetrvávaly hrozby pro řádné fungování a integritu finančních trhů a stabilitu finančního systému. |
|
(4) |
V souladu s čl. 28 odst. 10 nařízení (EU) č. 236/2012 musí orgán ESMA toto opatření přezkoumávat ve vhodných intervalech a alespoň jednou za tři měsíce. |
|
(5) |
Orgán ESMA provedl tento přezkum na základě analýzy ukazatelů výkonnosti, včetně cen, volatility, indexů rozpětí swapů úvěrového selhání, jakož i vývoje čistých krátkých pozic, zejména pozic mezi 0,1 a 0,2 %. Podle provedené analýzy orgán ESMA rozhodl, že by měl toto opatření obnovit na další tři měsíce. |
2. SCHOPNOST OPATŘENÍ REAGOVAT NA RELEVANTNÍ HROZBY A PŘESHRANIČNÍ DŮSLEDKY (ČL. 28 ODST. 2 PÍSM. a) NAŘÍZENÍ (EU) č. 236/2012)
a) Ohrožení správného fungování a integrity finančních trhů
|
(6) |
Pandemie COVID-19 má i nadále nepříznivý dopad na reálnou ekonomiku, přičemž celkové vyhlídky na budoucí oživení zůstávají nejisté, zejména s ohledem na nedávný vývoj v EU i mimo ni. Orgán ESMA konstatuje, že počet případů onemocnění COVID-19 se v několika jurisdikcích v posledních několika týdnech výrazně zvýšil, což vyvolává obavy ohledně možnosti druhé vlny nákaz COVID-19 a zvyšuje nejistotu jakéhokoli výhledu do budoucna. |
|
(7) |
Akciové trhy v EU, jak dokládá index Eurostoxx 50, v období od 20. února do 3. září 2020 ztratily 14 % v porovnání se ztrátou hodnoty ve výši 13 % mezi 20. únorem a 4. červnem (tabulka 1). Došlo k významnému zlepšení indexu Eurostoxx 50 oproti úrovni dosahované v březnu (kdy pokles činil přibližně 30 % ve srovnání s únorem 2020, jak je uvedeno v rozhodnutí (EU) 2020/525), aniž by se však vrátil na úroveň před pandemií COVID-19. |
|
(8) |
Volatilita měřená na základě VSTOXX (6) zůstává ve srovnání s únorem 2020 rovněž poměrně vysoká. Úroveň naměřená v září (+15 %) je mírně vyšší než v červnu (+13 %). Totéž platí, a to i ve větší míře, pro VIX (7) (+18 % v září oproti +9 % v červnu) (tabulka 1 a tabulka 2). |
|
(9) |
Úroveň swapů úvěrového selhání klesla od 4. června do 3. září v rozmezí od 17 % do 28 % (tabulka 1). Aby však bylo možné lépe pochopit vypovídací schopnost swapů úvěrového selhání v tomto okamžiku, musí být údaje posouzeny v kontextu rozhodnutí Evropské centrální banky (ECB) o nouzovém pandemickém programu nákupu aktiv (PEPP). Od začátku března začala být rozpětí swapů úvěrového selhání vysoce kolísavá a svědčí o vysokém finančním riziku. Obnovení rozhodnutí (EU) 2020/525 orgánem ESMA na základě údajů do 4. června bylo rovněž založeno na skutečnosti, že rozpětí swapů úvěrového selhání byla v té době vysoká a volatilní a byla považována za ukazatel vnímání rizika na trhu. |
|
(10) |
Navýšení PEPP o dalších 600 miliard EUR, o kterém bylo rozhodnuto 4. června, však vedlo k celkovému oznámenému měnovému stimulu ECB ve výši 1,35 bilionu EUR, čímž se snížila výpovědní hodnota rozpětí swapů úvěrového selhání v souvislosti s vnímáním rizika na trhu. |
|
(11) |
Podobné úvahy lze uvést ve vztahu k výpovědní hodnotě trhů se státními dluhopisy, které jsou stejně jako v případě rozpětí swapů úvěrového selhání ovlivněny měnovou politikou centrálních bank. Jak je patrné z tabulky 1, výnosy desetiletých státních dluhopisů DE, FR, GB a IT vykazují pokles oproti červnovým úrovním v průměru o 22 bazických bodů. |
|
(12) |
V důsledku toho se orgán ESMA domnívá, že vývoj akciových trhů, který je výrazně méně ovlivněn měnovou politikou centrálních bank, by měl poskytnout lepší přehled o současné úrovni rizika na finančních trzích EU. |
|
(13) |
Podobně jako Eurostoxx 50 ztratil index STOXX EUROPE 800 bez Švýcarska od 20. února 2020 přibližně 17 % ve srovnání s poklesem o 16 % v červnu. Index STOXX Europe Total Market Banks (odkaz na evropské banky) se od února snížil o 37 %, zatímco v červnu činila ztráta přibližně 30 %. |
|
(14) |
Jak je uvedeno ve zprávě orgánu ESMA o trendech, rizicích a zranitelnostech č. 2 ze září 2020, ve 2. čtvrtletí 2020 se objevily známky diferenciace mezi odvětvími, což mělo dopad zejména na úvěrové instituce. Ke konci června byly indexy leteckých společností a bankovního sektoru EU stále 36 % resp. 30 %, což je méně než na začátku ledna. Tabulka 3 navíc ukazuje, že bankovní sektor a pojišťovnictví jsou od června poměrně stabilní, ale výkonnost v období od 20. února do 3. září ve srovnání s obdobím od 20. února do 4. června vykazuje zhoršení: –38 % oproti –33 % pro bankovní sektor a –21 % oproti –20 % pro pojišťovnictví. Naopak výkonnost nefinančních (8) sektorů se v malé míře zlepšila: –9 % oproti –11 %. |
|
(15) |
K oživení cen v některých odvětvích došlo v kontextu dalšího zhoršování makroekonomického prostředí a hluboké a celosvětově synchronizované recese. Jak je uvedeno ve zprávě o trendech, rizicích a zranitelnostech, současné zjevné oddělení výkonnosti finančního trhu od související hospodářské činnosti vyvolává otázku ohledně další udržitelnosti oživení trhu. |
|
(16) |
Vzhledem k souhrnné vnitrostátní úrovni nebo úrovni EU se zdá, že k oživení cen nedošlo: Tabulka 5 ukazuje, že snižování cen je v celé Unii rozšířené, od června do září nedošlo k žádnému významnému zlepšení a výkonnost akciových indexů na 22 trzích EU naznačuje, že pokles od 20. února do 3. září byl horší než pokles od 20. února do 4. června. Kromě toho akciové trhy 25 jurisdikcí (ve srovnání s 24. červnem) ztratily při srovnání cen ze dne 3. září s cenami ze dne 20. února 2020 nejméně 10 % své hodnoty. Ve stejném období klesly ceny akcií evropských úvěrových institucí o 10 % až 59 % ve srovnání se ztrátami hodnoty v rozmezí od 9 % do 48 % zaznamenanými v období od února do června. |
|
(17) |
Procentní podíl akcií s čistou krátkou pozicí mezi 0,1 a 0,2 % se v období od 16. března do 11. června 2020 stabilně zvyšoval a poté zůstal stabilní až do 4. září 2020 (9), přičemž průměr činil 13 % celkových čistých krátkých pozic (tabulka 6). Nižší prahová hodnota pro vykazování navíc prokázala, že v některých zemích představovaly čisté krátké pozice mezi 0,1 % až 0,2 % přibližně 50 % celkových vykázaných pozic. Závěrem lze říci, že procentní podíl čistých krátkých pozic mezi 0,1 a 0,2 %, které musely být vykázány kvůli dočasné nižší prahové hodnotě pro oznamovací povinnost, zůstává významnou částí celkových čistých krátkých pozic a má pro regulační orgány v současné situaci silnou vypovídací hodnotu. |
|
(18) |
Celkově významný pokles cen v klíčových odvětvích, relativně vysoká volatilita, potenciální oddělení výkonnosti finančního trhu od související hospodářské činnosti a trvale vysoká úroveň čistých krátkých pozic spolu s nejistotou ohledně vývoje pandemie COVID-19 a jejího dopadu na reálnou ekonomiku signalizují, že finanční trhy EU zůstávají v křehkém stavu. Tento stav zvyšuje pravděpodobnost, že by tlaky na prodej na krátko mohly v nadcházejících měsících iniciovat nebo zhoršovat negativní vývoj, což může zase negativně ovlivnit důvěru trhu nebo integritu mechanismu určování cen. |
|
(19) |
Orgán ESMA se tedy domnívá, že kombinace okolností popsaných výše představuje vážné ohrožení řádného fungování a integrity finančních trhů. |
b) Ohrožení stability celého finančního systému Unie nebo jeho části
|
(20) |
Jak vysvětlila ECB ve svém přezkumu finanční stability (10), finanční stabilita je předpokladem, při němž je finanční systém – který zahrnuje finanční zprostředkovatele, trhy a tržní infrastruktury – schopen odolat šokům a vyřešit finanční nerovnováhu. |
|
(21) |
Pandemie COVID-19 má i nadále vážný dopad na reálnou ekonomiku v Unii. Jak se uvádí ve zprávě orgánu ESMA o trendech, rizicích a zranitelnostech, bez ohledu na oživení trhu zůstává tržní prostředí křehké a orgán ESMA předpokládá „dlouhé období rizika pro institucionální a retailové investory vyplývající z dalších – případně významných – korekcí trhu a (…) velmi vysokých rizik v celém rozsahu působnosti orgánu ESMA“ (11). V tomto ohledu orgán ESMA upozornil veřejnost na potenciální oddělování výsledků na finančním trhu a související hospodářské činnosti. |
|
(22) |
Výše uvedený oddíl 2 písm. a) obsahuje další informace o výkonnosti bankovnictví, pojišťovnictví a finančních trhů. |
|
(23) |
Tyto rozsáhlé poklesy cen způsobily, že většina akcií EU ve všech odvětvích se nachází v křehké situaci, kdy by další poklesy cen, které nejsou vyvolány dodatečnými základními informacemi, mohly mít velmi škodlivé důsledky. |
|
(24) |
V dosud nejasné situaci se orgán ESMA domnívá, že by značný prodejní tlak a neobvyklá volatilita cen akcií mohly být vyvolány různými faktory, včetně rostoucího počtu účastníků trhu, kteří prodávají na krátko a budují významné čisté krátké pozice. |
|
(25) |
Orgán ESMA zejména konstatuje, že rozsáhlé cenové ztráty úvěrových institucí, které představovaly jeden z parametrů pro rozhodnutí o obnovení přijaté v červnu, se nezlepšily. To naznačuje, že úvěrové instituce, které jsou v určitých případech systematicky důležité, jsou i nadále potenciálně zranitelné vůči strategiím prodeje na krátko a vytváření významných čistých krátkých pozic bez ohledu na to, zda jsou tyto strategie a pozice podloženy základními informacemi. |
|
(26) |
Přetrvává riziko, že kumulace strategií prodeje na krátko a vytváření významných čistých krátkých pozic by mohly vést k chaotickým spirálovým poklesům cen pro určité emitenty s potenciálními efekty přelévání v témže členském státě nebo v celé EU, které by pak mohly případně ohrozit finanční systém jednoho nebo několika členských států. |
|
(27) |
Bez ohledu na částečné oživení pozorované v určitých odvětvích evropských finančních trhů se orgán ESMA domnívá, že současná situace na trhu nadále vážně ohrožuje stabilitu finančního systému v Unii. |
|
(28) |
V rámci pověření orgánu ESMA navrhované obnovení opatření ukládá fyzickým nebo právnickým osobám, které mají čistou krátkou pozici v akciích přijatých k obchodování na regulovaném trhu, povinnost zaslat hlášení příslušným vnitrostátním orgánům při dosažení nižší prahové hodnoty, než jakou stanoví článek 5 nařízení (EU) č. 236/2012. |
|
(29) |
Obnovené opatření by mělo zachovat zlepšující se schopnost příslušných vnitrostátních orgánů a orgánu ESMA posoudit vyvíjející se situaci odpovídajícím způsobem, rozlišovat mezi pohyby na trhu, které vedou ze základních informací, od pohybů na trhu, které by mohly být iniciovány nebo prohloubeny prodejem na krátko, a reagovat, jestliže integrita, řádné fungování a stabilita trhů vyžadují přísnější opatření. |
c) Přeshraniční důsledky
|
(30) |
Další podmínkou pro to, aby orgán ESMA mohl toto opatření přijmout, je skutečnost, že zjištěné hrozby mají přeshraniční dopad. |
|
(31) |
Jak bylo popsáno výše, akciové trhy v celé EU se s ohledem na vnitrostátní i celoevropské indexy plně nezotavily z výrazného poklesu cen zaznamenaného v březnu. |
|
(32) |
Vzhledem ke skutečnosti, že ohroženy jsou finanční trhy většiny členských států EU, ačkoliv různou měrou, jsou přeshraniční dopady i nadále obzvláště závažné, neboť vzájemná provázanost finančních trhů v EU zvyšuje pravděpodobnost potenciálního efektu přelévání nebo dominového efektu na trzích v případě tlaku na prodej na krátko. |
|
(33) |
Orgán ESMA se proto domnívá, že výše popsané ohrožení integrity trhu, řádného fungování a finanční stability má přeshraniční dopady. Z důvodu povahy krize COVID-19 mají ve skutečnosti celoevropský a celosvětový charakter. |
3. ŽÁDNÝ PŘÍSLUŠNÝ ORGÁN NEPŘIJAL OPATŘENÍ K ŘEŠENÍ DANÉ HROZBY NEBO JEDEN NEBO VÍCE PŘÍSLUŠNÝCH ORGÁNŮ PŘIJALY OPATŘENÍ, KTERÁ NA TUTO HROZBU NEREAGUJÍ ODPOVÍDAJÍCÍM ZPŮSOBEM (ČL. 28 ODST. 2 PÍSM. b) NAŘÍZENÍ (EU) č. 236/2012)
|
(34) |
Další z podmínek, aby orgán ESMA mohl přijmout opatření uvedené v tomto rozhodnutí, je, že příslušný orgán nebo příslušné orgány nepřijaly opatření k řešení dané hrozby nebo že přijatá opatření na tuto hrozbu nereagují dostatečně. |
|
(35) |
Integrita trhu, řádné fungování a obavy týkající se finanční stability, které jsou popsány v rozhodnutí (EU) 2020/525 a které zůstávají v platnosti pro toto rozhodnutí, vedly některé vnitrostátní příslušné orgány k tomu, aby přijaly vnitrostátní opatření s cílem omezit prodej akcií na krátko ve Španělsku, Francii, v Rakousku, Belgii, Řecku a Itálii (12), jejichž platnost skončila dne 18. května. |
|
(36) |
Po skončení platnosti nebo zrušení těchto dočasných opatření nebyla v EU přijata žádná další opatření na základě nařízení (EU) č. 236/2012 a ke dni přijetí tohoto rozhodnutí nejsou žádná taková opatření v platnosti. |
|
(37) |
V době přijetí tohoto rozhodnutí žádné příslušné orgány nepřijaly opatření ke zviditelnění vývoje čistých krátkých pozic stanovením nižších prahových hodnot pro zasílání hlášení, jelikož se mohou opřít o rozhodnutí (EU) 2020/1123. |
|
(38) |
Nutnost většího zviditelnění čistých krátkých pozic je ještě naléhavější v situaci, kdy platnost výše uvedených omezení uložených podle článku 20 nařízení (EU) č. 236/2012 skončila a nejistota ve vztahu k pokračujícímu dopadu COVID-19 přetrvává. Vzhledem k tomu, že prodej na krátko a transakce s rovnocenným účinkem již nepodléhají jiným vnějším omezením, musí být příslušné vnitrostátní orgány v celé EU schopny předem určit, zda dochází k vytváření čistých krátkých pozic v míře, která může vést k výše popsanému ohrožení finančních trhů a finanční stability, které se zhoršuje v důsledku tlaku na prodej na krátko. |
|
(39) |
S ohledem na výše uvedené hrozby pro celou EU zůstává zřejmé, že informace získané příslušnými vnitrostátními orgány v rámci běžné prahové hodnoty pro zasílání hlášení stanovené v čl. 5 odst. 2 nařízení (EU) č. 236/2012 nejsou za stávajících krizových tržních podmínek dostatečné. Orgán ESMA se domnívá, že zachování nižších prahových hodnot pro zasílání hlášení by mělo zajistit, aby všechny příslušné vnitrostátní orgány v celé EU a orgán ESMA měly k dispozici co nejlepší soubor údajů pro monitorování tržních trendů a aby se ony samy a orgán ESMA v případě potřeby připravily na přijetí dalších opatření. |
4. ÚČINNOST OPATŘENÍ (ČL. 28 ODST. 3 PÍSM. a) NAŘÍZENÍ (EU) č. 236/2012)
|
(40) |
Orgán ESMA musí také vzít v úvahu, do jaké míry obnovené opatření výrazně řeší zjištěné hrozby. |
|
(41) |
Orgán ESMA se domnívá, že navzdory mimořádným ztrátám, které vznikly při obchodování s akciemi na regulovaných trzích od 20. února 2020, trhy fungovaly řádně a že integrita trhů byla do značné míry zachována. |
|
(42) |
Orgán ESMA tudíž analyzoval současné okolnosti, zejména s odkazem na to, do jaké míry představují hrozby pro integritu trhů a finanční stabilitu v Unii a zda by obnovené opatření orgánu ESMA bylo účinné při řešení těchto hrozeb pomocí výhledového přístupu. |
a) Opatření výrazně řeší ohrožení řádného fungování a integrity finančních trhů
|
(43) |
Za výše popsaných okolností může jakýkoli náhlý nárůst prodejních tlaků a volatility trhu způsobený prodejem na krátko a vytvářením krátkých pozic umocnit trendy poklesu na finančních trzích. Zatímco prodej na krátko v jiné době může posloužit pozitivním funkcím, pokud jde o stanovení správného ocenění emitentů, za současných podmínek na trhu však může představovat další ohrožení řádného fungování a integrity trhů. |
|
(44) |
Zejména s ohledem na horizontální dopad pokračující krizové situace, která ovlivňuje širokou škálu akcií v celé Unii, může být náhlý pokles cen akcií zhoršen dalším tlakem na prodej vyplývajícím z prodeje na krátko a nárůst čistých krátkých pozic, pokud jsou pod úrovní běžné prahové hodnoty pro oznamování příslušným vnitrostátním orgánům podle článku 5 nařízení (EU) č. 236/2012, by proto bez obnoveného opatření nebyl zjištěn. |
|
(45) |
Z výše uvedených důvodů si příslušné vnitrostátní orgány a orgán ESMA musí být co nejdříve vědomy účastníků trhu, kteří se zabývají prodejem na krátko a budováním významných čistých krátkých pozic, aby v případě potřeby zabránily tomu, aby se tyto pozice staly signály vedoucími k záplavě příkazů k prodeji a následnému významnému poklesu cen. |
|
(46) |
Orgán ESMA má za to, že pokud by toto opatření nebylo obnoveno o další tři měsíce, příslušné vnitrostátní orgány a orgán ESMA by nebyly schopny odpovídajícím způsobem monitorovat trh v současném nejistém a křehkém prostředí. To je zdůrazněno zjevným oddělením výkonnosti finančního trhu od související hospodářské činnosti ve spojení s vyvíjející se povahou pandemie COVID-19. Tyto faktory by mohly vyvolat náhlý a významný tlak na prodej a neobvyklou dodatečnou volatilitu cen akcií Unie, která by mohla být dále zesílena kumulací krátkých pozic. |
|
(47) |
Orgán ESMA zároveň považuje za vhodné zachovat prahovou hodnotu pro zveřejňování stanovenou v článku 6 nařízení (EU) č. 236/2012, která se rovná 0,5 % upsaného akciového kapitálu společnosti, jelikož snížení této prahové hodnoty se nejeví jako nezbytné z hlediska zachování řádných trhů a řešení rizik pro finanční stabilitu. Orgán ESMA nadále průběžně monitoruje tržní podmínky a v případě potřeby přijme další opatření. |
b) Opatření významně řeší ohrožení stability celého finančního systému Unie nebo jeho části
|
(48) |
Jak je popsáno výše, výkonnost velké většiny akciových trhů v EU se v období od června do září 2020 ve srovnání s 20. únorem zhoršila. Celkově pro obchodování s akciemi od 20. února 2020 byl a stále je typický tlak na prodej a poměrně vysoká míra volatility. Jak je uvedeno výše, různé rizikové faktory mají i nadále dopad na mnohá odvětví reálné ekonomiky a na finanční trhy EU. V tomto prostředí může zapojení do prodeje na krátko a budování významných čistých krátkých pozic zesílit tlak na prodej a klesající trendy, jež zase mohou zvýšit hrozbu, která může mít velmi škodlivé účinky na finanční stabilitu finančních institucí a společností z jiných odvětví. |
|
(49) |
V této souvislosti by zúžení údajů pro příslušné vnitrostátní orgány a orgán ESMA omezilo jejich schopnost řešit případné negativní dopady na hospodářství a v konečném důsledku na finanční stabilitu Unie jako celku. |
|
(50) |
Obnovené opatření orgánu ESMA s cílem dočasně snížit prahové hodnoty čistých krátkých pozic pro zasílání hlášení příslušným vnitrostátním orgánům proto účinně řeší tuto hrozbu pro stabilitu částí finančního systému Unie nebo v konečném důsledku celého finančního systému Unie tím, že snižuje omezení údajů a zlepšuje schopnost příslušných vnitrostátních orgánů řešit nadcházející hrozby v rané fázi. |
c) Zlepšení schopnosti příslušných orgánů monitorovat hrozbu
|
(51) |
Za běžných tržních podmínek příslušné vnitrostátní orgány monitorují jakoukoli hrozbu, která může vyplývat z prodeje na krátko a z vytváření čistých krátkých pozic pomocí nástrojů dohledu stanovených v právních předpisech Unie, zejména povinností zasílat hlášení týkající se čistých krátkých pozic stanovených v nařízení (EU) č. 236/2012 (13). |
|
(52) |
Stávající tržní podmínky však vyžadují zintenzivnění monitorovací činnosti příslušných vnitrostátních orgánů a orgánu ESMA, pokud jde o agregované čisté krátké pozice v akciích přijatých k obchodování na regulovaných trzích. Za tímto účelem a s ohledem na přetrvávající nejistotu spojenou s pandemií COVID-19 je stále důležité, aby příslušné vnitrostátní orgány nadále dostávaly informace o vytváření čistých krátkých pozic v co nejranější fázi, dříve než dosáhnou úrovně 0,2 % upsaného akciového kapitálu podle čl. 5 odst. 2 nařízení (EU) č. 236/2012. |
|
(53) |
To je zdůrazněno procentním podílem akcií s čistou krátkou pozicí mezi 0,1 a 0,2 %, který se v období od 16. března do 11. června 2020 postupně zvyšoval a od té doby zůstal stabilní až do 4. září 2020 (14), a to v průměru 13 % za celé sledované období. Lze proto vyvodit závěr, že procentní podíl čistých krátkých pozic mezi 0,1 a 0,2 %, které musely být vykázány kvůli nižší prahové hodnotě pro oznamovací povinnost stanovené orgánem ESMA, zůstává významnou částí celkových čistých krátkých pozic. |
|
(54) |
Obnovené opatření orgánu ESMA proto zachová vylepšenou schopnost příslušných vnitrostátních orgánů vypořádat se s veškerými zjištěnými hrozbami v dřívější fázi, aby jim a orgánu ESMA umožnily včasné řízení rizik ohrožujících řádné fungování trhů a finanční stabilitu, pokud by se projevila jakákoli známka napětí na trhu. |
5. OPATŘENÍ NEVEDOU KE VZNIKU RIZIKA REGULATORNÍ ARBITRÁŽE (ČL. 28 ODST. 3 PÍSM. b) NAŘÍZENÍ (EU) č. 236/2012)
|
(55) |
Za účelem přijetí nebo obnovení opatření podle článku 28 nařízení (EU) č. 236/2012 by měl orgán ESMA vzít v úvahu, zda opatření vede ke vzniku rizika regulatorní arbitráže. |
|
(56) |
Vzhledem k tomu, že se obnovené opatření ESMA týká povinnosti účastníků trhu zasílat hlášení, pokud jde o všechny akcie přijaté k obchodování na regulovaných trzích v Unii, zajistí pro všechny příslušné vnitrostátní orgány jednotnou prahovou hodnotu pro zasílání hlášení a zajistí rovné podmínky pro všechny účastníky trhu z Unie i mimo ni, pokud jde o obchodování s akciemi přijatými k obchodování na regulovaných trzích v Unii. |
6. OPATŘENÍ ORGÁNU ESMA NEMÁ ŠKODLIVÝ ÚČINEK NA EFEKTIVNOST FINANČNÍCH TRHŮ, MIMO JINÉ TÍM, ŽE SNÍŽÍ LIKVIDITU NA TĚCHTO TRZÍCH NEBO VYVOLÁ NEJISTOTU MEZI ÚČASTNÍKY TRHU, KTERÝ BY BYL NEÚMĚRNÝ VZHLEDEM K PŘÍNOSŮM OPATŘENÍ (ČL. 28 ODST. 3 PÍSM. c) NAŘÍZENÍ (EU) č. 236/2012)
|
(57) |
Orgán ESMA musí posoudit, zda má opatření škodlivé účinky, které by byly ve srovnání s jeho přínosy považovány za neúměrné. |
|
(58) |
Orgán ESMA považuje za vhodné, aby příslušné vnitrostátní orgány před zvážením přijetí jakýchkoli více narušujících opatření pozorně monitorovaly vývoj čistých krátkých pozic. Orgán ESMA poznamenává, že běžné prahové hodnoty pro zasílání hlášení (0,2 % upsaného akciového kapitálu) nemusí být v přetrvávajících výjimečných tržních podmínkách dostatečné pro včasnou identifikaci trendů a naplňujících se hrozeb. |
|
(59) |
Zavedení posílené povinnosti zasílat hlášení sice mohlo znamenat další zátěž pro vykazující subjekty, ty však již nyní upravily své vnitřní systémy na základě uplatňování rozhodnutí (EU) 2020/525 a (EU) 2020/1123, a neočekává se tudíž, že toto obnovené opatření bude mít další dopad na náklady na dodržování předpisů ze strany vykazujících subjektů. Kromě toho nebude omezovat schopnost účastníků trhu uzavírat nebo zvyšovat své krátké pozice v akciích. V důsledku toho nebude ovlivněna efektivnost trhu. |
|
(60) |
V porovnání s jinými možnými a více narušujícími opatřeními by toto obnovené opatření nemělo mít vliv na likviditu na trhu, neboť posílená povinnost zasílat hlášení pro omezený soubor účastníků trhu by neměla změnit jejich obchodní strategie, a tudíž ani jejich účast na trhu. Zachovaná výjimka stanovená pro činnosti spojené s tvorbou trhu a pro stabilizační programy navíc nemá za cíl zvyšovat zátěž subjektů, které nabízejí důležité služby, pokud jde o poskytování likvidity a snižování volatility, což je zvláště důležité v současné situaci. |
|
(61) |
Pokud jde o rozsah obnoveného opatření, domnívá se orgán ESMA, že jeho omezení na jedno nebo několik odvětví nebo na jakoukoli podskupinu emitentů nemusí dosáhnout požadovaného výsledku. Rozsah poklesu cen zaznamenaný po propuknutí pandemie COVID-19, široký rozsah dotčených akcií (a odvětví) a stupeň propojení mezi ekonomikami EU a obchodními systémy naznačují, že v poskytování včasných informacích o trhu příslušným vnitrostátním orgánům je opatření na úrovni EU pravděpodobně účinnější než odvětvová opatření. |
|
(62) |
Pokud jde o vyvolání nejistoty na trhu, toto opatření nezavádí nové regulační povinnosti, neboť pouze snižuje běžnou prahovou hodnotu pro zasílání hlášení, která je v platnosti od roku 2012. Orgán ESMA rovněž zdůrazňuje, že obnovené opatření zůstává omezeno na vykazování akcií, které jsou přijaty k obchodování na regulovaném trhu v Unii, k zachycení těch pozic, u nichž se zdá být nejvýznamnější další vykazování. |
|
(63) |
Orgán ESMA se proto domnívá, že taková zvýšená povinnost týkající se transparentnosti by neměla mít nepříznivý účinek na efektivnost finančních trhů ani na investory, který by byl neúměrný přínosům opatření, a neměla by vytvářet nejistotu na finančních trzích. |
|
(64) |
Pokud jde o dobu trvání opatření, orgán ESMA se domnívá, že obnovení opatření na tři měsíce je opodstatněné s ohledem na informace, které jsou v tuto chvíli k dispozici, a na přetrvávající celkový nejistý výhled v souvislosti s pandemií COVID-19. Orgán ESMA má v úmyslu se vrátit k povinnosti pravidelného zasílání hlášení, jakmile se situace zlepší, ale zároveň se nemůže zbavit možnosti rozšířit opatření, pokud by se situace zhoršila nebo pokud by trhy měly zůstat v křehkém stavu. |
|
(65) |
Na tomto základě a od tohoto data má orgán ESMA za to, že toto rozhodnutí obnovit dočasné zvýšení transparentnosti, pokud jde o čisté krátké pozice, je vzhledem k přetrvávajícím nepříznivým okolnostem přiměřené. |
7. KONZULTACE A OZNÁMENÍ (ČL. 28 ODST. 4 A 5 NAŘÍZENÍ (EU) č. 236/2012)
|
(66) |
Orgán ESMA provedl konzultaci s ESRB. ESRB neuvedla žádné námitky proti přijetí navrhovaného rozhodnutí. |
|
(67) |
Orgán ESMA informoval o zamýšleném rozhodnutí příslušné vnitrostátní orgány. |
|
(68) |
Obnovené opatření orgánu ESMA se použije ode dne 18. září 2020, |
PŘIJAL TOTO ROZHODNUTÍ:
Článek 1
Definice
Pro účely tohoto rozhodnutí se „regulovaným trhem“ rozumí regulovaný trh podle čl. 4 odst. 1 bodu 21 směrnice Evropského parlamentu a Rady 2014/65/EU (15).
Článek 2
Dočasné dodatečné povinnosti týkající se transparentnosti
1. Fyzická nebo právnická osoba, která má čistou krátkou pozici ve vztahu k upsanému akciovému kapitálu společnosti, jejíž akcie jsou přijaty k obchodování na regulovaném trhu, podá dotčenému příslušnému orgánu oznámení v souladu s články 5 a 9 nařízení (EU) č. 236/2012, jestliže tato pozice dosáhne příslušné prahové hodnoty pro oznamovací povinnost uvedené v odstavci 2 tohoto článku, nebo pod tuto hodnotu poklesne.
2. Příslušnou prahovou hodnotou pro oznamovací povinnost je procentní podíl rovný 0,1 % upsaného akciového kapitálu dotčené společnosti a dále každých 0,1 %.
Článek 3
Výjimky
1. V souladu s článkem 16 nařízení (EU) č. 236/2012 se dočasné dodatečné povinnosti týkající se transparentnosti uvedené v článku 2 nevztahují na akcie přijaté k obchodování na regulovaném trhu, jestliže se hlavní obchodní systém pro obchodování s těmito akciemi nachází ve třetí zemi.
2. V souladu s článkem 17 nařízení (EU) č. 236/2012 se dočasné dodatečné povinnosti týkající se transparentnosti uvedené v článku 2 nevztahují na transakce prováděné u činností v rámci tvorby trhu.
3. Dočasné dodatečné povinnosti týkající se transparentnosti uvedené v článku 2 se nevztahují na čistou krátkou pozici v souvislosti s provedením stabilizace podle článku 5 nařízení Evropského parlamentu a Rady (EU) č. 596/2014 (16).
Článek 4
Vstup v platnost a použitelnost
Toto rozhodnutí vstupuje v platnost dnem 18. září 2020. Použije se ode dne jeho vstupu v platnost po dobu tří měsíců.
V Paříži dne 16. září 2020.
Za radu orgánů dohledu
Steven MAIJOOR
předseda
(1) Úř. věst. L 331, 15.12.2010, s. 84.
(2) Úř. věst. L 86, 24.3.2012, s. 1.
(3) Úř. věst. L 274, 9.10.2012, s. 1.
(4) Úř. věst. L 116, 15.4.2020, s. 5.
(5) Úř. věst. L 245, 30.7.2020, s. 17.
(6) VSTOXX měří implikovanou volatilitu na základě cen opcí Eurostoxx 50.
(7) Index VIX se vypočítá pomocí středního bodu kupní/prodejní ceny opce indexu S&P 500 (SPX) v reálném čase.
(8) Z nefinančních sektorů jsou vyloučeny následující dílčí sektory: banky, pojišťovací a finanční služby.
(9) Zprávy o denních čistých krátkých pozicích z Dánska v období od 31. srpna do 4. září v důsledku technického problému chybí.
(10) https://www.ecb.europa.eu/pub/financial-stability/fsr/html/ecb.fsr201911~facad0251f.en.html.
(11) Zpráva o trendech, rizicích a zranitelnostech, Shrnutí, strana 4.
(12) V Itálii bylo opatření dne 18. května zrušeno.
(13) Viz článek 5 nařízení (EU) č. 236/2012.
(14) Zprávy o denních čistých krátkých pozicích z Dánska v období od 31. srpna do 4. září v důsledku technického problému chybí.
(15) Směrnice Evropského parlamentu a Rady 2014/65/EU ze dne 15. května 2014 o trzích finančních nástrojů a o změně směrnic 2002/92/ES a 2011/61/EU (Úř. věst. L 173, 12.6.2014, s. 349).
(16) Nařízení Evropského parlamentu a Rady (EU) č. 596/2014 ze dne 16. dubna 2014 o zneužívání trhu (nařízení o zneužívání trhu) a o zrušení směrnice Evropského parlamentu a Rady 2003/6/ES a směrnic Komise 2003/124/ES, 2003/125/ES a 2004/72/ES (Úř. věst. L 173, 12.6.2014, s. 1).
PŘÍLOHA
V této příloze se „rozhodnutí orgánu ESMA“ vztahuje k rozhodnutí (EU) 2020/525.
Tabulka 1
Finanční ukazatele
|
Výkonnost akciového trhu |
Změny od 20.2.2020 do 3.9.2020 (v %) |
Úroveň indexu ke dni 3.9.2020 |
Změny od 20.2.2020 do 4.6.2020 (v %) |
Úroveň indexu ke dni 4.6.2020 |
|
STOXX EUROPE 800 ex. Švýcarsko |
–17 |
116 |
–16 |
117 |
|
EURO STOXX INDEX |
–13 |
362 |
–13 |
364 |
|
EURO STOXX 50 |
–14 |
3 304 |
–13 |
3 323 |
|
US S&P500 |
2 |
3 451 |
–8 |
3 112 |
|
JP Nikkei |
0 |
23 466 |
–3 |
22 864 |
|
Celosvětově |
–1 |
228 |
–9 |
211 |
|
Evropské banky |
–37 |
93 |
–30 |
104 |
|
IT akcie finančních společností |
–30 |
27 |
–29 |
28 |
|
ES akcie finančních společností |
–48 |
34 |
–35 |
42 |
|
DE akcie finančních společností |
–13 |
123 |
–11 |
126 |
|
FR akcie finančních společností |
–34 |
118 |
–28 |
130 |
|
Volatilita |
Změny od 20.2.2020 do 3.9.2020 (v %) |
Úroveň indexu ke dni 3.9.2020 |
Změny od 20.2.2020 do 4.6.2020 (v %) |
Úroveň indexu ke dni 4.6.2020 |
|
VSTOXX |
15 |
29 |
13 |
28 |
|
VIX |
18 |
33 |
9 % |
25 |
|
Swapy úvěrového selhání |
Změny v bps od 20.2.2020 do 3.9.2020 |
Rozpětí swapů úvěrového selhání v bps ke dni 3.9.2020 |
Změny v bps od 20.2.2020 do 4.6.2020 |
Rozpětí swapů úvěrového selhání v bps ke dni 4.6.2020 |
|
Evropa korporát |
5 |
45 |
22 |
62 |
|
Evropa vysoký výnos |
92 |
290 |
157 |
355 |
|
Evropa finanční instituce |
15 |
59 |
29 |
73 |
|
Evropa finanční instituce podřízený dluh |
38 |
124 |
62 |
149 |
|
10Y státní dluhopisy |
Změny v bps od 20.2.2020 do 3.9.2020 |
Výnosy dluhopisů v % ke dni 3.9.2020 |
Změny v bps od 20.2.2020 do 4.6.2020 |
Výnosy dluhopisů v % ke dni 4.6.2020 |
|
DE10Y |
–5 |
–0,49 |
15 |
–0,29 |
|
ES10Y |
9 |
0,33 |
32 |
0,55 |
|
FR10Y |
2 |
–0,19 |
23 |
0,01 |
|
IT10Y |
15 |
1,06 |
51 |
1,42 |
|
US10Y |
–90 |
0,62 |
–67 |
0,86 |
|
GB10Y |
–34 |
0,24 |
–24 |
0,34 |
|
JP10Y |
8 |
0,04 |
9 |
0,05 |
|
Poznámka: Změny akciového trhu vyjádřené v relativních hodnotách, ostatní změny v absolutních hodnotách. Zdroje: Refinitiv EIKON, ESMA. |
||||
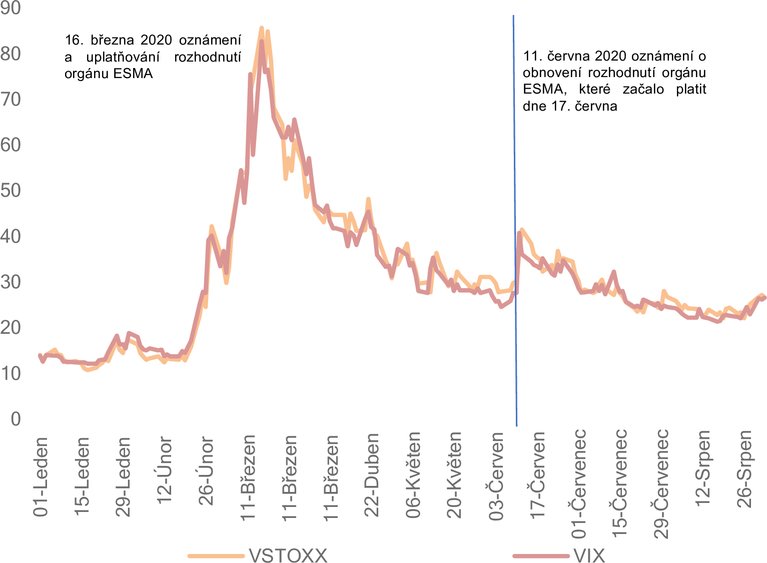
Poznámka: Implicitní volatility indexů EURO STOXX 50 (VSTOXX) a S&P 500 (VIX), v %.
Zdroje: Refinitiv Datastream, ESMA.

Poznámka: Ceny kapitálu. 20.2.2020 = 100.
Zdroje: Refinitiv Datastream, ESMA.
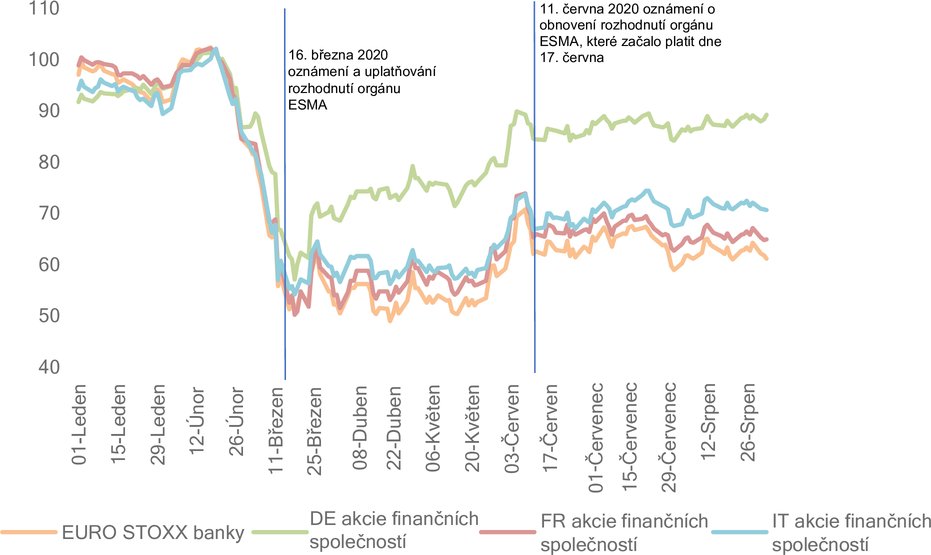
Poznámka: Ceny kapitálu. 20.2.2020 = 100.
Zdroje: Refinitiv Datastream, ESMA.
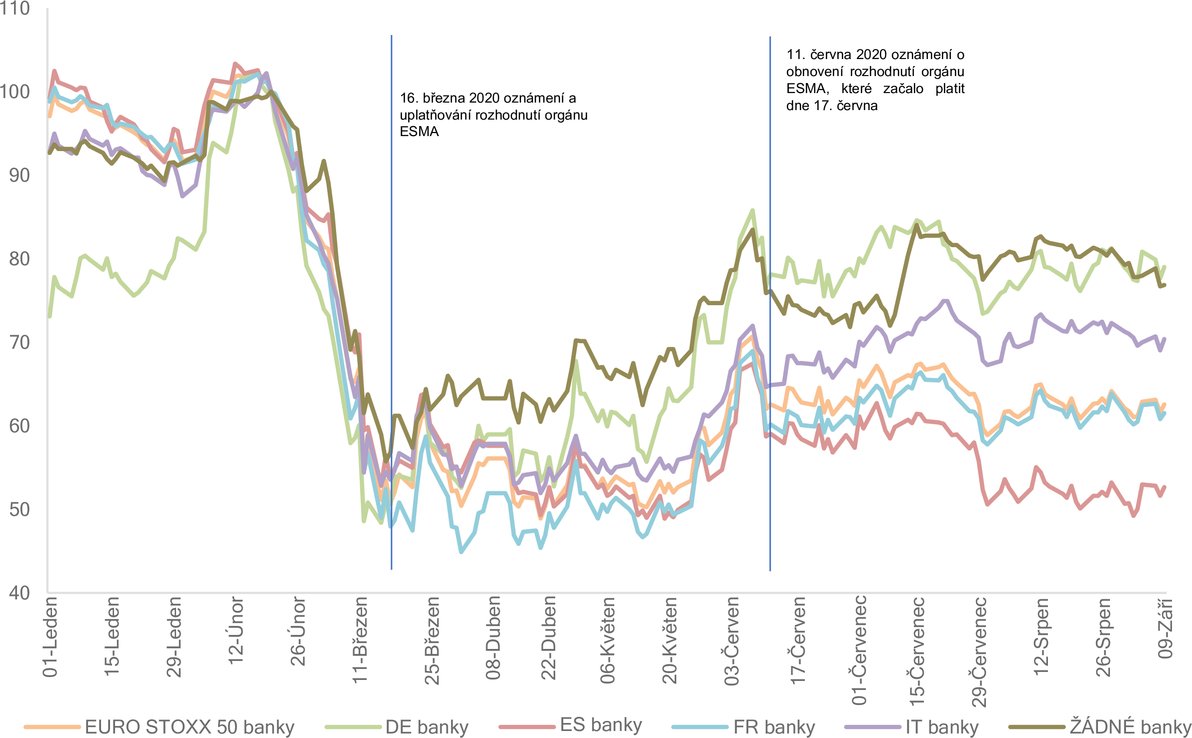
Poznámka: Ceny kapitálu. 20.2.2020 = 100.
Zdroje: Refinitiv Datastream, ESMA.
Tabulka 4
Indexy rozpětí swapů úvěrového selhání EU
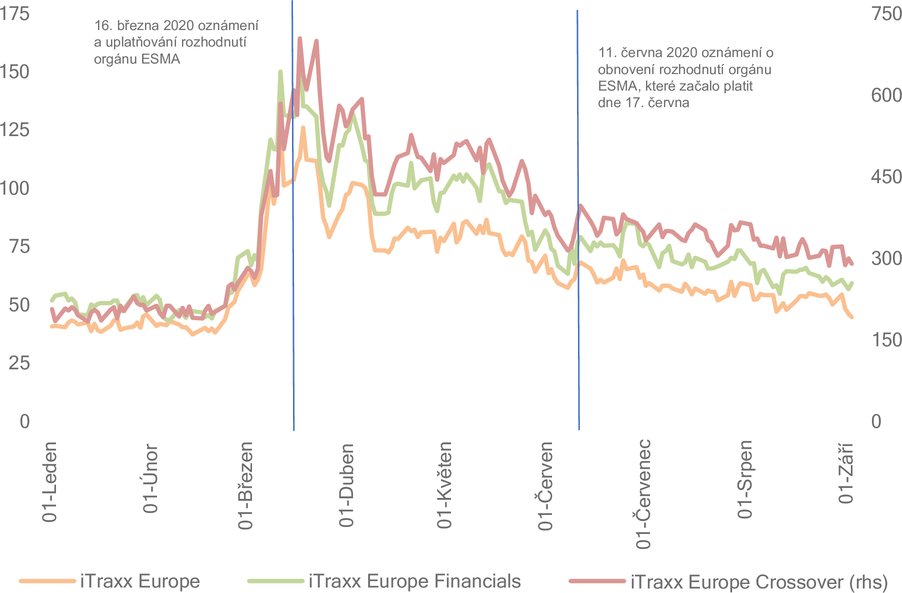
Poznámka: rozpětí swapů úvěrového selhání u evropských korporátů investičního stupně (iTraxx Europe), evropských vysoce výnosových korporátů (iTraxx Europe Crossover) a evropských finančních společností, v bps.
Zdroje: Refinitiv EIKON, ESMA.
Tabulka 5
Výkonnost evropských akciových indexů podle země
|
|
Změna v procentech od 20.2.2020 do 3.9.2020 |
Změna v procentech od 20.2.2020 do 4.6.2020 |
|
STOXX EUROPE 800 ex. Švýcarsko |
–16,67 |
–15,78 |
|
EURO STOXX INDEX |
–13,22 |
–12,72 |
|
EURO STOXX 50 |
–13,57 |
–13,07 |
|
AT |
–30,21 |
–23,30 |
|
BE |
–19,22 |
–14,86 |
|
BG |
–20,67 |
–15,69 |
|
CY |
–39,52 |
–34,73 |
|
CZ |
–17,81 |
–13,94 |
|
DE |
–4,44 |
–7,32 |
|
DK |
4,24 |
–2,48 |
|
EE |
–13,55 |
–13,16 |
|
ES |
–29,45 % |
–21,88 |
|
FI |
–5,35 |
–8,66 |
|
FR |
–17,37 |
–15,91 |
|
GB |
–21,32 |
–13,93 |
|
GR |
–29,24 |
–26,64 |
|
HR |
–19,61 |
–17,16 |
|
HU |
–24,05 |
–17,83 |
|
IE |
–13,00 |
–12,90 |
|
IS |
–1,50 |
–4,44 |
|
IT |
–22,04 |
–20,01 |
|
LT |
5,06 |
–1,98 |
|
LU |
–25,92 |
–21,60 |
|
LV |
5,53 |
–1,81 |
|
MT |
–20,80 |
–12,92 |
|
NL |
–11,66 |
–9,17 |
|
NO |
–11,80 |
–10,22 |
|
PL |
–15,75 |
–13,47 |
|
PT |
–20,09 |
–13,64 |
|
RO |
–10,73 |
–11,45 |
|
SE |
–7,28 |
–9,47 |
|
SI |
–13,01 |
–10,83 |
|
SK |
–7,05 |
0,07 |
|
Zdroje: Refinitiv EIKON, ESMA. |
||
Tabulka 6
Čisté krátké pozice mezi 0,1 % a 0,2 % v období od 16. března do 4. září 2020 (1)

OBECNÉ ZÁSADY
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/77 |
OBECNÉ ZÁSADY EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2020/1690
ze dne 25. září 2020,
kterými se mění obecné zásady (EU) 2015/510 o provádění rámce měnové politiky Eurosystému
(ECB/2020/45)
RADA GUVERNÉRŮ EVROPSKÉ CENTRÁLNÍ BANKY,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 127 odst. 2 první odrážku této smlouvy,
s ohledem na statut Evropského systému centrálních bank a Evropské centrální banky, a zejména na první odrážku článku 3.1, články 9.2, 12.1, 14.3, 18.2 a první odstavec článku 20 tohoto statutu,
vzhledem k těmto důvodům:
|
(1) |
Dosažení jednotné měnové politiky vyžaduje vymezení nástrojů a postupů, jež má Eurosystém využívat za účelem provádění této politiky jednotným způsobem ve všech členských státech, jejichž měnou je euro. |
|
(2) |
Obecné zásady Evropské centrální banky (EU) 2015/510 (ECB/2014/60) (1) by měly být změněny, aby zahrnovaly potřebné technické a redakční úpravy týkající se určitých aspektů operací měnové politiky. |
|
(3) |
Aby se snížila celková složitost rámce zajištění Eurosystému, expozice Eurosystému vůči riziku a provozní zátěž při posuzování způsobilosti, neměly by být jako zajištění Eurosystému nadále přijímány neregulované kryté dluhopisy (tj. smluvní kryté dluhopisy). Proto by definice a ustanovení týkající se krytých dluhopisů v rámci Eurosystému pro zajištění měly být změněny tak, aby omezily druh způsobilých krytých dluhopisů na regulované kryté dluhopisy a na multi cédulas. |
|
(4) |
S cílem zohlednit dvouřádový systém Eurosystému pro úročení přebytečných rezerv, který na základě rozhodnutí Evropské centrální banky (EU) 2019/1743 (ECB/2019/31) (2) platí od 30. října 2019, by mělo být upřesněno, který právní rámec se vztahuje na úročení minimálních rezerv a přebytečných rezerv. |
|
(5) |
S cílem dále snížit složitost rámce zajištění Eurosystému by obchodovatelné dluhové nástroje emitované nebo zaručené nefinančními podniky, pro něž není k dispozici náležité úvěrové hodnocení, již neměly být po uplynutí přechodného období přijímány jako zajištění Eurosystému, a to i s přihlédnutím k tomu, že byly používány pouze v omezeném rozsahu. |
|
(6) |
S cílem zohlednit nejnovější finanční inovace v oblasti udržitelného financování má Eurosystém v úmyslu přijímat některé obchodovatelné dluhové nástroje s kupónovými strukturami vázanými na plnění předem stanovených cílů udržitelnosti ze strany emitenta. |
|
(7) |
Mělo by být vyjasněno, že aktiva s kupóny vázanými na interpolované referenční sazby jsou způsobilá pouze za určitých podmínek, a tyto podmínky by měly být specifikovány. |
|
(8) |
S cílem zavést jednotný a transparentní přístup ke kategoriím zajištěných obchodovatelných aktiv, která jsou způsobilá jako zajištění pro úvěrové operace Eurosystému, by jako zajištění Eurosystému neměla být nadále přijímána zajištěná obchodovatelná aktiva s výjimkou cenných papírů krytých aktivy a krytých dluhopisů. |
|
(9) |
Požadavky na údaje o úvěrech pro cenné papíry kryté aktivy, které jsou způsobilé jako zajištění Eurosystému, by měly být upraveny pro ty cenné papíry kryté aktivy, u nichž se údaje o úvěrech vykazují v souladu s nařízením Evropského parlamentu a Rady (EU) 2017/2402 (3). |
|
(10) |
S cílem zlepšit dostupnost informací o úvěrových pohledávkách v rámci zajištění, zvýšit jednoznačnost pravidel, která určují způsobilost úvěrové pohledávky jako zajištění, a vyjasnit postupy ověřování těchto aktiv by měla být pozměněna některá ustanovení týkající se způsobilosti úvěrových pohledávek jako zajištění Eurosystému a vykazování údajů, pokud jde o úvěrové pohledávky. |
|
(11) |
V zájmu zajištění větší transparentnosti, konzistentnosti a právní jistoty by měla být vyjasněna obecná kritéria pro akceptaci externích ratingových agentur v rámci Eurosystému pro hodnocení úvěrového rizika. |
|
(12) |
Pravidla týkající se používání nezajištěných dluhových nástrojů vydaných protistranou nebo s ní úzce propojenými subjekty by měla být zjednodušena. |
|
(13) |
V zájmu zvýšení transparentnosti rámce Eurosystému pro protistrany by měly být objasněny podrobnosti týkající se délky dodatečné lhůty pro protistrany, které nesplňují minimální kapitálové požadavky. |
|
(14) |
Finanční postih za porušení související s využíváním způsobilých aktiv jako zajištění Eurosystému by měl být upraven tak, aby protistrany motivoval k tomu, aby o těchto porušeních proaktivně informovaly. |
|
(15) |
Obecné zásady (EU) 2015/510 (ECB/2014/60) je proto třeba příslušným způsobem změnit, |
PŘIJALA TYTO OBECNÉ ZÁSADY:
Článek 1
Změny
Obecné zásady (EU) 2015/510 (ECB/2014/60) se mění takto:
|
1. |
Článek 2 se mění takto:
|
|
2. |
Článek 54 se mění takto:
|
|
3. |
V článku 61 se v odstavci 1 doplňuje nová věta, která zní: „Tato aktiva jsou způsobilá pouze do dne, kdy začne fungovat systém řízení zajištění Eurosystému („den spuštění“).“; |
|
4. |
V článku 63 se odstavec 1 mění takto:
|
|
5. |
Vkládá se nový článek 64a, který zní: „Článek 64a Obchodovatelná aktiva s výjimkou cenných papírů krytých aktivy a krytých dluhopisů 1. Aby byla způsobilá, musí být obchodovatelná aktiva jiná než cenné papíry kryté aktivy, regulované kryté dluhopisy a multi cédulas nezajištěnými závazky jak emitenta, tak ručitele. V případě obchodovatelných aktiv s více než jedním emitentem nebo s více než jedním ručitelem se požadavek uvedený v tomto odstavci použije na všechny emitenty a všechny ručitele. 2. Obchodovatelná aktiva, která jsou zajištěna a byla způsobilá před 1. lednem 2021, avšak nesplňují požadavky na způsobilost stanovené v tomto článku, zůstávají způsobilá do 1. ledna 2026 za předpokladu, že splňují všechna ostatní kritéria způsobilosti pro obchodovatelná aktiva. Odchylně od první věty tohoto odstavce se kryté dluhopisy, které nejsou ani regulovanými krytými dluhopisy, ani multi cédulas, stávají nezpůsobilými od 1. ledna 2021.“; |
|
6. |
Článek 78 se mění takto:
|
|
7. |
Článek 80 se nahrazuje tímto: „Článek 80 Kritéria způsobilosti krytých dluhopisů zajištěných cennými papíry krytými aktivy 1. Aniž by byla dotčena způsobilost regulovaných krytých dluhopisů ve smyslu článku 64a, aby byly kryté dluhopisy regulované v EHP a zajištěné cennými papíry krytými aktivy způsobilé, obsahuje soubor zajišťovacích aktiv těchto dluhopisů (pro účely odstavců 1 až 4 „soubor zajišťovacích aktiv“) pouze cenné papíry kryté aktivy, které splňují všechny tyto podmínky.
2. S výhradou odstavce 4 národní centrální banky k ověření skutečnosti, že soubor zajišťovacích aktiv neobsahuje cenné papíry kryté aktivy, které nejsou v souladu s odstavcem 1, používají tato opatření.
3. Pokud emitent příslušné žádosti nevyhoví nebo má-li Eurosystém za to, že obsah potvrzení je natolik nesprávný nebo nedostatečný, že nelze ověřit, zda soubor zajišťovacích aktiv splňuje kritéria uvedená v odstavci 1, Eurosystém rozhodne o tom, že kryté dluhopisy regulované v EHP nepřijme jako způsobilé zajištění, nebo o pozastavení jejich způsobilosti. 4. Pokud příslušná legislativa nebo prospekt vylučují, aby cenné papíry kryté aktivy, které nejsou v souladu s odstavcem 1, byly zahrnuty do souboru zajišťovacích aktiv, ověření podle odstavce 2 se nevyžaduje. 5. Pro účely odst. 1 písm. b) se úzké propojení určuje v době, kdy jsou cenné papíry kryté aktivy s přednostním vypořádáním převáděny do souboru zajišťovacích aktiv krytého dluhopisu regulovaného v EHP. 6. Soubor zajišťovacích aktiv krytých dluhopisů regulovaných v zemi G10 mimo EHP nesmí obsahovat cenné papíry kryté aktivy.“; |
|
8. |
Článek 87 se mění takto:
|
|
9. |
Článek 90 se mění takto:
|
|
10. |
Článek 100 se nahrazuje tímto: „Článek 100 Ověření postupů a systémů pro předložení úvěrových pohledávek Národní centrální banky, orgány dohledu nebo externí auditoři před první mobilizací úvěrových pohledávek protistranou prověří vhodnost postupů a systémů, které protistrana používá, když Eurosystému překládá informace o úvěrových pohledávkách. Ověřování postupů a systémů se následně provádí nejméně jednou za pět let. V případě podstatných změn těchto postupů nebo systémů je možné provést nové ověření.“; |
|
11. |
V čl. 101 se za písmeno a) vkládá nové písmeno aa), které zní:
(*5) Nařízení Evropské centrální banky (EU) 2016/867 ze dne 18. května 2016 o shromažďování podrobných údajů o úvěrech a o úvěrovém riziku (ECB/2016/13) (Úř. věst. L 144, 1.6.2016, s. 44).“;" |
|
12. |
V článku 102 se druhá věta nahrazuje tímto: „Protistrana a/nebo případně nabyvatel musí splňovat všechny právní náležitosti nezbytné k zajištění platnosti smlouvy a mobilizace úvěrové pohledávky jako zajištění.“; |
|
13. |
V článku 120 se odstavce 2 a 2a nahrazují tímto: „2. V návaznosti na postup pro podávání žádostí ve smyslu přílohy IXc si Eurosystém vyhrazuje právo rozhodnout, zda na žádost ratingové agentury zahájí postup akceptace pro účely rámce Eurosystému pro hodnocení úvěrového rizika. Při rozhodování Eurosystém zohlední mimo jiné to, zda ratingová agentura poskytuje relevantní pokrytí pro účely účinného provádění rámce Eurosystému pro hodnocení úvěrového rizika v souladu s požadavky uvedenými v příloze IXa. 2a. Po zahájení postupu akceptace pro účely rámce Eurosystému pro hodnocení úvěrového rizika Eurosystém prošetří všechny dodatečné informace, které považuje za relevantní k zajištění účinného provádění rámce Eurosystému pro hodnocení úvěrového rizika, včetně schopnosti externí ratingové agentury i) splňovat kritéria a dodržovat pravidla procesu monitorování výsledků hodnocení úvěrového rizika v rámci Eurosystému pro hodnocení úvěrového rizika v souladu s požadavky obsaženými v příloze IX, jakož případně i zvláštní kritéria uvedená v příloze IXb (jsou-li relevantní) a ii) splňovat akceptační kritéria uvedená v příloze IXc. Eurosystém si vyhrazuje právo rozhodnout o akceptaci externí ratingové agentury pro účely rámce Eurosystému pro hodnocení úvěrového rizika na základě poskytnutých informací a na základě provedení vlastního hloubkového auditu.“; |
|
14. |
Článek 138 se mění takto:
|
|
15. |
Článek 139 se mění takto:
|
|
16. |
V článku 148 se odstavec 2 nahrazuje tímto: „2. Protistrany mohou způsobilá aktiva s výjimkou termínovaných vkladů mobilizovat pro přeshraniční užití takto:
|
|
17. |
Článek 155 se nahrazuje tímto: „Článek 155 Finanční postih za nedodržování určitých provozních pravidel 1. Pokud protistrana nesplní jakoukoli povinnost uvedenou v čl. 154 odst. 1, uloží Eurosystém za každý případ neplnění finanční postih. Příslušný finanční postih se vypočte v souladu s přílohou VII. 2. Pokud protistrana napraví nesplnění povinnosti uvedené v čl. 154 odst. 1 písm. c) a oznámí to národní centrální bance před tím, než národní centrální banka, ECB nebo externí auditor oznámí toto neplnění protistraně („porušení oznámené protistranou“), příslušný finanční postih vypočtený v souladu s přílohou VII se sníží o 50 %. Finanční postih se sníží rovněž v případech, kdy protistrana národní centrální bance oznámí porušení, které nebylo zjištěno ze strany ECB nebo národní centrální banky, a pokud se týká aktiv, která byla demobilizována. Finanční postih se nesnižuje, pokud jde o aktiva, u nichž probíhá postup ověřování, jehož si je protistrana vzhledem k oznámení národní centrální banky, ECB nebo externího auditora vědoma.“; |
|
18. |
V čl. 156 odst. 4 se písmeno a) nahrazuje tímto:
|
|
19. |
Článek 158 se mění takto:
|
|
20. |
v čl. 159 odst. 4 se písmeno b) nahrazuje tímto:
|
|
21. |
Přílohy I, VIII, IXa a XII se mění v souladu s přílohou I těchto obecných zásad; |
|
22. |
Text uvedený v příloze II těchto obecných zásad se doplňuje jako nová příloha IXc. |
Článek 2
Nabytí účinku a provádění
1. Tyto obecné zásady nabývají účinku dnem oznámení národním centrálním bankám členských států, jejichž měnou je euro.
2. Národní centrální banky členských států, jejichž měnou je euro, přijmou opatření nezbytná k dosažení souladu s těmito obecnými zásadami a použijí je ode dne 1. ledna 2021. Nejpozději do 6. listopadu 2020 informují Evropskou centrální banku o textech a prostředcích, které se týkají těchto opatření.
Článek 3
Určení
Tyto obecné zásady jsou určeny všem centrálním bankám Eurosystému.
Ve Frankfurtu nad Mohanem dne 25. září 2020.
prezidentka ECB
Za Radu guvernérů ECB
Christine LAGARDE
(1) Obecné zásady Evropské centrální banky (EU) 2015/510 ze dne 19. prosince 2014 o provádění rámce měnové politiky Eurosystému (obecné zásady o obecné dokumentaci) (ECB/2014/60) (Úř. věst. L 91, 2.4.2015, s. 3).
(2) Rozhodnutí Evropské centrální banky (EU) 2019/1743 ze dne 15. října 2019 o úročení přebytečných rezerv a některých vkladů (ECB/2019/31) (Úř. věst. L 267, 21.10.2019, s. 12).
(3) Nařízení Evropského parlamentu a Rady (EU) 2017/2402 ze dne 12. prosince 2017, kterým se stanoví obecný rámec pro sekuritizaci a vytváří se zvláštní rámec pro jednoduchou, transparentní a standardizovanou sekuritizaci a kterým se mění směrnice 2009/65/ES, 2009/138/ES, 2011/61/EU a nařízení (ES) č. 1060/2009 a (EU) č. 648/2012 (Úř. věst. L 347, 28.12.2017, s. 35).
PŘÍLOHA I
Přílohy I, VIII, IXa a XII obecných zásad (EU) 2015/510 (ECB/2014/60) se mění takto:
|
1. |
V příloze I v odstavci 5 se druhá věta nahrazuje tímto: „Mezi tyto instituce patří mimo jiné instituce, v nichž jsou prováděna reorganizační opatření, a instituce, vůči nimž Unie podle článku 75 Smlouvy nebo členský stát zavedly opatření spočívající ve zmrazení peněžních prostředků a/nebo jiná opatření, která omezují používání jejich peněžních prostředků, nebo jejichž přístup k operacím na volném trhu či ke stálým facilitám Eurosystému byl na základě rozhodnutí Eurosystému pozastaven či zrušen.“; |
|
2. |
Příloha VIII se mění takto:
|
|
3. |
V příloze IXa oddílu 2 se odstavec 1 nahrazuje tímto:
|
|
4. |
V příloze XII se pojem „krytý dluhopis typu Jumbo v souladu se směrnicí o SKIPCP“ nahrazuje pojmem „krytý dluhopis typu Jumbo“. |
PŘÍLOHA II
Doplňuje se nová příloha IXc, která zní:
„PŘÍLOHA IXc
KRITÉRIA PRO AKCEPTACI EXTERNÍ RATINGOVÉ AGENTURY A POSTUP PRO PODÁVÁNÍ ŽÁDOSTÍ
Tato příloha podrobně stanoví kritéria pro akceptaci externích ratingových agentur a postup, jak může ratingová agentura žádat o akceptaci jako externí ratingová agentura pro účely rámce Eurosystému pro hodnocení úvěrového rizika, jak jsou uvedeny v článku 120 těchto obecných zásad.
I. POSTUP PRO PODÁVÁNÍ ŽÁDOSTÍ O AKCEPTACI JAKO EXTERNÍ RATINGOVÁ AGENTURA V RÁMCI EUROSYSTÉMU PRO HODNOCENÍ ÚVĚROVÉHO RIZIKA
|
1. |
Žádost ratingové agentury o akceptaci jako externí ratingová agentura v rámci Eurosystému pro hodnocení úvěrového rizika musí být předložena ředitelství ECB pro řízení rizik (DRMSecretariat@ecb.europa.eu). Žádost musí obsahovat náležité odůvodnění a podklady, jak je stanoveno v oddílu II, které prokazují, že žadatel splňuje požadavky na externí ratingové agentury stanovené v těchto obecných zásadách. Žádost, odůvodnění a podklady musí být předloženy písemně v angličtině s využitím příslušných vzorů a v elektronické podobě. |
|
2. |
V první fázi postupu podávání žádosti musí ratingová agentura prokázat, že plní příslušné požadavky na pokrytí stanovené v článku 120 a v příloze IXa těchto obecných zásad, jakož i v této příloze, a jak řešila své předchozí neplnění příslušných požadavků v případě, že její žádost o akceptaci v rámci Eurosystému pro hodnocení úvěrového rizika Eurosystém předtím zamítl. Jednotlivé kroky v této první fázi jsou následující.
|
|
3. |
Pokud ECB rozhodne, že ratingová agentura splňuje příslušné požadavky na pokrytí, případně že napravila předchozí neplnění příslušných požadavků, a ECB rozhodne, že zahájí postup akceptace pro účely rámce Eurosystému pro hodnocení úvěrového rizika, může ratingová agentura postoupit do druhé fáze postupu podávání žádosti. Ve druhé fázi musí ratingová agentura prokázat, že splňuje všechny ostatní příslušné požadavky stanovené v těchto obecných zásadách. Jednotlivé kroky v této druhé fázi jsou následující.
|
II. INFORMACE VYŽADOVANÉ K TOMU, ABY BYLA ŽÁDOST O AKCEPTACI V RÁMCI EUROSYSTÉMU PRO HODNOCENÍ ÚVĚROVÉHO RIZIKA POVAŽOVÁNA ZA ÚPLNOU
|
1. |
Pokud jde o první fázi postupu podávání žádostí, musí ratingová agentura poskytnout následující informace.
|
|
2. |
ECB může například požadovat doplňující informace k prokázání stability pokrytí ratingové agentury v průběhu času, jejích postupů pro vydávání ratingů a kvality ratingů ratingové agentury v průběhu příslušného období pokrytí. |
|
3. |
Pokud jde o druhou fázi postupu podávání žádosti, musí ratingová agentura poskytnout následující dokumentaci a informace:
|
|
4. |
ECB může od ratingové agentury požadovat příslušné doplňující informace, například v souvislosti s ratingy aktiv, emitentů a ručitelů vypracovaných ratingovou agenturou, které nejsou způsobilé pro účely rámce Eurosystému pro hodnocení úvěrového rizika, například z důvodu zeměpisných omezení. |
III. KRITÉRIA AKCEPTACE PRO ÚČELY RÁMCE EUROSYSTÉMU PRO HODNOCENÍ ÚVĚROVÉHO RIZIKA
|
1. |
Aby mohla být ratingová agentura akceptována v rámci Eurosystému pro hodnocení úvěrového rizika, musí splňovat příslušné požadavky stanovené v těchto obecných zásadách, včetně relevantního pokrytí, aby se zajistilo účinné provádění rámce Eurosystému pro hodnocení úvěrového rizika, provozních kritérií, dostupnosti informací o úvěrovém hodnocení ze strany externích ratingových agentur a pro účely procesů sledování výkonnosti a schopnosti plnit kritéria a pravidla procesu monitorování výsledků v rámci Eurosystému pro hodnocení úvěrového rizika. |
|
2. |
Pokud jde o požadavek příslušného pokrytí:
|
|
3. |
Pokud jde o dostupnost informací o úvěrovém hodnocení ze strany externích ratingových agentur a pro účely procesů sledování výkonnosti:
|
|
4. |
Pokud jde o schopnost ratingové agentury plnit kritéria a pravidla procesu monitorování výsledků v rámci Eurosystému pro hodnocení úvěrového rizika, musí být výsledky ratingů ratingové agentury a její přidělení statusu selhání v průběhu času konzistentní s cílem a) zajistit náležité přiřazení informací o úvěrovém hodnocení poskytnutých systémem hodnocení úvěrového rizika na harmonizovanou ratingovou stupnici Eurosystému a b) zachovat srovnatelnost výsledků úvěrových hodnocení ratingové agentury napříč systémy a zdroji v rámci Eurosystému pro hodnocení úvěrového rizika. Tabulky pozorovaných změn v ratingu příslušné ratingové agentury a její statistika selhání by měly být v souladu s očekávanými hodnotami založenými na vlastní ratingové stupnici ratingové agentury, neboť, jak je stanoveno v příloze IX těchto obecných zásad, odchylky mezi dosaženými mírami selhání a přidělenou pravděpodobností selhání mohou zpochybnit kvalitu úvěrových hodnocení, což brání účinnému provádění rámce Eurosystému pro hodnocení úvěrového rizika. |
|
5. |
Pokud jde o provozní kritéria:
|
|
6. |
Aby mohla být ratingová agentura v rámci Eurosystému pro hodnocení úvěrového rizika akceptována, musí být splněna všechna kritéria pro akceptaci pro účely rámce Eurosystému pro hodnocení úvěrového rizika. Vzhledem k tomu, že akceptace na základě žádosti pro účely rámce Eurosystému pro hodnocení úvěrového rizika vyžaduje vysoce technické kvalitativní a kvantitativní posouzení, může Eurosystém v případě potřeby posoudit další relevantní faktory, které souvisejí s požadavky těchto obecných zásad, jež se týkají rámce Eurosystému pro hodnocení úvěrového rizika. |
IV. KRITÉRIA PRO AKCEPTACI EXTERNÍCH RATINGOVÝCH AGENTUR V RÁMCI EUROSYSTÉMU PRO HODNOCENÍ ÚVĚROVÉHO RIZIKA A JEJICH TRVALÉ PLNĚNÍ
|
1. |
Kritéria pro akceptaci jako externí ratingová agentura musí ratingová agentura splňovat v době podání žádosti o akceptaci a po celou dobu poté, co je akceptována v rámci Eurosystému pro hodnocení úvěrového rizika. |
|
2. |
Eurosystém může uplatňovat opatření podle článku 126 těchto obecných zásad vůči ratingové agentuře, která:
Když Eurosystém ratingovou agenturu informuje o svém rozhodnutí uplatnit opatření podle článku 126, toto rozhodnutí odůvodní. |
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/92 |
OBECNÉ ZÁSADY EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2020/1691
ze dne 25. září 2020,
kterými se mění obecné zásady ECB/2014/31 o dodatečných dočasných opatřeních týkajících se refinančních operací Eurosystému a způsobilosti zajištění
(ECB/2020/47)
RADA GUVERNÉRŮ EVROPSKÉ CENTRÁLNÍ BANKY,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 127 odst. 2 první odrážku této smlouvy,
s ohledem na statut Evropského systému centrálních bank a Evropské centrální banky, a zejména na čl. 3.1 první odrážku a články 5.1, 12.1, 14.3 a 18.2 tohoto statutu,
vzhledem k těmto důvodům:
|
(1) |
Cenné papíry kryté aktivy, jejichž podkladová aktiva zahrnují hypoteční úvěry na bydlení nebo úvěry malým a středním podnikům anebo oba druhy úvěrů a které nesplňují určité požadavky uvedené v čl. 3 odst. 5 obecných zásad ECB/2014/31 (1), by již neměly být způsobilým zajištěním Eurosystému, jelikož tato kategorie aktiv nebyla nikdy použita. |
|
(2) |
Způsob výpočtu finančních postihů v případech, kdy jsou do souboru dalších úvěrových pohledávek podle článku 4 obecných zásad ECB/2014/31 zahrnuty úvěrové pohledávky, které nejsou v souladu s čl. 154 odst. 1 písm. c) obecných zásad Evropské centrální banky (EU) 2015/510 (ECB/2014/60) (2), je třeba změnit, aby se zabránilo ukládání nepřiměřených finančních postihů. |
|
(3) |
Obecné zásady ECB/2014/31 je proto třeba odpovídajícím způsobem změnit, |
PŘIJALA TYTO OBECNÉ ZÁSADY:
Článek 1
Změny
Obecné zásady ECB/2014/31 se mění takto:
|
1. |
V článku 3 se zrušuje odstavec 5; |
|
2. |
Článek 4 se mění takto:
|
Článek 2
Nabytí účinku a provádění
1. Tyto obecné zásady nabývají účinku dnem oznámení národním centrálním bankám členských států, jejichž měnou je euro.
2. Národní centrální banky členských států, jejichž měnou je euro, přijmou opatření nezbytná k dosažení souladu s těmito obecnými zásadami a použijí je ode dne 1. ledna 2021. Nejpozději do 6. listopadu 2020 informují Evropskou centrální banku o textech a prostředcích, které se týkají těchto opatření.
Článek 3
Určení
Tyto obecné zásady jsou určeny všem centrálním bankám Eurosystému.
Ve Frankfurtu nad Mohanem dne 25. září 2020.
Za Radu guvernérů ECB
prezidentka ECB
Christine LAGARDE
(1) Obecné zásady ECB/2014/31 ze dne 9. července 2014 o dodatečných dočasných opatřeních týkajících se refinančních operací Eurosystému a způsobilosti zajištění a o změně obecných zásad ECB/2007/9 (Úř. věst. L 240, 13.8.2014, s. 28).
(2) Obecné zásady Evropské centrální banky (EU) 2015/510 ze dne 19. prosince 2014 o provádění rámce měnové politiky Eurosystému (obecné zásady o obecné dokumentaci) (ECB/2014/60) (Úř. věst. L 91, 2.4.2015, s. 3).
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/94 |
OBECNÉ ZÁSADY EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2020/1692
ze dne 25. září 2020,
kterými se mění obecné zásady (EU) 2016/65 o srážkách při ocenění uplatňovaných při provádění rámce měnové politiky Eurosystému
(ECB/2020/46)
RADA GUVERNÉRŮ EVROPSKÉ CENTRÁLNÍ BANKY,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 127 odst. 2 první odrážku této smlouvy,
s ohledem na statut Evropského systému centrálních bank a Evropské centrální banky, a zejména na první odrážku článku 3.1, články 9.2, 12.1, 14.3, 18.2 a první odstavec článku 20 tohoto statutu,
vzhledem k těmto důvodům:
|
(1) |
Rámec Eurosystému pro kontrolu rizika a oceňování je třeba upravit, aby se zohlednila skutečnost, že neregulované kryté dluhopisy (tj. smluvní kryté dluhopisy) by již neměly být akceptovány jako zajištění Eurosystému. |
|
(2) |
Obecné zásady Evropské centrální banky (EU) 2016/65 (ECB/2015/35) (1) je proto třeba příslušným způsobem změnit, |
PŘIJALA TYTO OBECNÉ ZÁSADY:
Článek 1
Změny
Obecné zásady (EU) 2016/65 (ECB/2015/35) se mění takto:
|
(1) |
Článek 2 se mění takto:
|
|
(2) |
V příloze se tabulka 1 nahrazuje tímto: „Tabulka 1 Kategorie srážek pro způsobilá obchodovatelná aktiva podle druhu emitenta a/nebo druhu aktiva
|
Článek 2
Nabytí účinku a provádění
1. Tyto obecné zásady nabývají účinku dnem oznámení národním centrálním bankám členských států, jejichž měnou je euro.
2. Národní centrální banky členských států, jejichž měnou je euro, přijmou opatření nezbytná pro dosažení souladu s těmito obecnými zásadami a použijí je ode dne 1. ledna 2021. Nejpozději do 6. listopadu 2020 informují Evropskou centrální banku o textech a prostředcích, které se týkají těchto opatření.
Článek 3
Určení
Tyto obecné zásady jsou určeny národním centrálním bankám členských států, jejichž měnou je euro.
Ve Frankfurtu nad Mohanem dne 25. září 2020.
Za Radu guvernérů ECB
prezidentka ECB
Christine LAGARDE
(1) Obecné zásady Evropské centrální banky (EU) 2016/65 ze dne 18. listopadu 2015 o srážkách při ocenění uplatňovaných při provádění rámce měnové politiky Eurosystému (ECB/2015/35) (Úř. věst. L 14, 21.1.2016, s. 30).
JEDNACÍ ŘÁDY
|
13.11.2020 |
CS |
Úřední věstník Evropské unie |
L 379/96 |
ROZHODNUTÍ SPRÁVNÍ RADY SPOLEČNÉHO PODNIKU PRO PRŮMYSL ZALOŽENÉHO NA BIOTECHNOLOGIÍCH
ze dne 26. března 2020,
kterým se stanoví vnitřní předpisy týkající se omezení některých práv subjektů údajů, pokud jde o zpracování osobních údajů v rámci fungování společného podniku BBI
SPRÁVNÍ RADA SPOLEČNÉHO PODNIKU PRO PRŮMYSL ZALOŽENÉHO NA BIOTECHNOLOGIÍCH (dále jen „společný podnik BBI“),
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) 2018/1725 ze dne 23. října 2018 o ochraně fyzických osob v souvislosti se zpracováním osobních údajů orgány, institucemi a jinými subjekty Unie a o volném pohybu těchto údajů a o zrušení nařízení (ES) č. 45/2001 a rozhodnutí č. 1247/2002/ES (1), a zejména na článek 25 tohoto nařízení,
s ohledem na nařízení Rady (EU) č. 560/2014 ze dne 6. května 2014 o založení společného podniku pro průmysl založený na biotechnologiích (2), a zejména na čl. 7 odst. 3 písm. s) tohoto nařízení,
s ohledem na pokyny evropského inspektora ochrany údajů (EIOÚ) k článku 25 nového nařízení a vnitřní předpisy,
po konzultaci s evropským inspektorem ochrany údajů v souladu s čl. 41 odst. 2 nařízení (EU) 2018/1725,
vzhledem k těmto důvodům:
|
(1) |
Společný podnik BBI vykonává svoji činnost v souladu s nařízením (EU) č. 560/2014. |
|
(2) |
V souladu s čl. 25 odst. 1 nařízení (EU) 2018/1725 by měla omezení použití článků 14 až 22, 35 a 36, jakož i článku 4 uvedeného nařízení v rozsahu, v jakém jeho ustanovení odpovídají právům a povinnostem stanoveným v článcích 14 až 22, vycházet z vnitřních předpisů přijatých společným podnikem BBI, pokud nevycházejí z právních aktů přijatých na základě Smluv. |
|
(3) |
Tyto vnitřní předpisy, včetně ustanovení o posouzení nezbytnosti a přiměřenosti daného omezení, by se neměly použít v případě, kdy omezení práv subjektů údajů stanoví právní akt přijatý na základě Smluv. |
|
(4) |
V případech, kdy společný podnik BBI vykonává své povinnosti s ohledem na práva subjektu údajů podle nařízení (EU) 2018/1725, zváží, zda se neuplatní kterákoliv z výjimek uvedených v tomto nařízení. |
|
(5) |
V rámci svého správního fungování může společný podnik BBI vést správní šetření či disciplinární řízení, vykonávat předběžné činnosti související s případy možných nesrovnalostí oznámených úřadu OLAF, zpracovávat případy whistleblowingu, vyřizovat (formální a neformální) řízení v případě obtěžování, vyřizovat interní a externí stížnosti, provádět interní audity, provádět šetření ze strany pověřence pro ochranu osobních údajů v souladu s čl. 45 odst. 2 nařízení (EU) 2018/1725 a šetření interní (IT) bezpečnosti. |
|
(6) |
Společný podnik BBI zpracovává několik kategorií osobních údajů, včetně „tvrdých“ údajů („objektivních“ údajů, jako jsou údaje o totožnosti, kontaktní údaje, profesní údaje, administrativní údaje, údaje získané ze zvláštních zdrojů, elektronická komunikace a provozní údaje) a „měkkých“ údajů („subjektivních“ údajů týkajících se daného případu, např. odůvodnění, údaje o chování, hodnocení, údaje o výkonu a jednání a údaje související nebo předložené v souvislosti s předmětem řízení nebo činnosti) (3). |
|
(7) |
Společný podnik BBI, zastoupený výkonným ředitelem, vystupuje jako správce údajů, a to i v případě dalšího přenesení pravomocí spojených s úlohou správce v rámci společného podniku BBI s cílem zohlednit provozní odpovědnost za konkrétní operace zpracování osobních údajů. |
|
(8) |
Osobní údaje jsou bezpečně uloženy v elektronickém prostředí nebo v papírové podobě tak, aby bylo zabráněno protiprávnímu přístupu nebo předání údajů osobám, které je nepotřebují znát. Zpracovávané osobní údaje nejsou uchovávány déle, než je nezbytné a přiměřené pro účely, pro které se zpracovávají, po dobu stanovenou v oznámeních o ochraně údajů, prohlášeních o ochraně soukromí nebo v záznamech společného podniku BBI. |
|
(9) |
Vnitřní předpisy by měly platit pro všechny operace zpracování provedené společným podnikem BBI v rámci správních šetření, disciplinárních řízení, předběžných činností souvisejících s případy možných nesrovnalostí oznámených úřadu OLAF, řízení v případě whistleblowingu, (formálních a neformálních) řízení v případech obtěžování, vyřizování interních a externích stížností, interních auditů, šetření prováděných pověřencem pro ochranu osobních údajů v souladu s čl. 45 odst. 2 nařízení (EU) 2018/1725, (IT) šetření bezpečnosti prováděných interně nebo se zapojením externích subjektů (např. skupiny CERT-EU). |
|
(10) |
Měly by platit pro operace zpracování provedené před zahájením výše uvedených řízení, během těchto řízení a během sledování opatření v návaznosti na výsledky řízení. Součástí by rovněž měla být pomoc a spolupráce, kterou společný podnik BBI nabízí vnitrostátním orgánům a mezinárodním organizacím nad rámec svých správních šetření. |
|
(11) |
V případech, kdy se použijí tyto vnitřní předpisy, je společný podnik BBI povinen uvést odůvodnění vysvětlující, proč jsou daná omezení v demokratické společnosti naprosto nezbytná a přiměřená, a respektovat podstatu základních práv a svobod. |
|
(12) |
V této souvislosti je společný podnik BBI v průběhu výše uvedených řízení povinen dodržovat v maximální možné míře základní práva subjektů údajů, zejména ta, která se týkají práva na poskytování informací, práva na přístup k osobním údajům, práva na jejich opravu, výmaz, a omezení zpracování, práva na oznamování případů porušení zabezpečení osobních údajů subjektu údajů nebo na důvěrnost komunikace, jak je zakotveno v nařízení (EU) 2018/1725. |
|
(13) |
Je však možné, že společný podnik BBI bude muset omezit informace poskytované subjektu údajů a jiná práva subjektu údajů, a to zejména s cílem chránit vlastní šetření, šetření a řízení jiných veřejných orgánů a rovněž práva jiných osob v souvislosti se svými šetřeními či jinými řízeními. |
|
(14) |
Společný podnik BBI je tedy oprávněn omezit informace pro účely ochrany šetření a základních práv a svobod jiných subjektů údajů. |
|
(15) |
Společný podnik BBI by měl pravidelně sledovat, že platí podmínky odůvodňující dané omezení, a omezení zrušit, pokud podmínky již neplatí. |
|
(16) |
Správce údajů by měl informovat pověřence pro ochranu osobních údajů v případě odkladu a během přezkumů, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Předmět a oblast působnosti
1. Tímto rozhodnutím se stanoví předpisy týkající se podmínek, za nichž může společný podnik BBI v rámci svých řízení uvedených v odstavci 2 omezit uplatňování práv zakotvených v článcích 14 až 21, 35 a 36, jakož i v článku 4 nařízení (EU) 2018/1725, a to v souladu s článkem 25 tohoto nařízení.
2. V rámci správního fungování společného podniku BBI platí toto rozhodnutí pro operace zpracování osobních údajů prováděné programovou kanceláří pro účely vedení správních šetření, disciplinárních řízení, předběžných činností souvisejících s případy možných nesrovnalostí oznámených úřadu OLAF, projednávání případů whistleblowingu, (formálních a neformálních) řízení v případech obtěžování, vyřizování interních a externích stížností, vedení interních auditů, šetření prováděných pověřencem pro ochranu osobních údajů v souladu s čl. 45 odst. 2 nařízení (EU) 2018/1725, šetření (IT) bezpečnosti prováděných interně nebo se zapojením externích subjektů (např. skupiny CERT-EU).
3. Dotčenými kategoriemi údajů jsou „tvrdé“ údaje („objektivní“ údaje, jako jsou údaje o totožnosti, kontaktní údaje, profesní údaje, administrativní údaje, údaje získané ze zvláštních zdrojů, elektronické komunikace a provozní údaje) a „měkké“ údaje („subjektivní“ údaje týkající se daného případu, např. odůvodnění, údaje o chování, hodnocení, údaje o výkonu a jednání a údaje související nebo předložené v souvislosti s předmětem řízení nebo činnosti).
4. V případech, kdy společný podnik BBI vykonává své povinnosti s ohledem na práva subjektu údajů podle nařízení (EU) 2018/1725, zváží, zda se neuplatní kterákoliv z výjimek uvedených v tomto nařízení.
5. V závislosti na podmínkách stanovených v tomto rozhodnutí mohou platit omezení pro tato práva: poskytování informací subjektům údajů, právo na přístup, opravu, výmaz, omezení zpracování, oznamování případů porušení zabezpečení osobních údajů subjektu údajů nebo důvěrnost komunikace.
Článek 2
Specifikace správce
Správcem operací zpracování je společný podnik BBI, zastoupený výkonným ředitelem, který může funkci správce delegovat. Subjekty údajů jsou o delegovaném správci informovány formou oznámení o ochraně osobních údajů nebo prostřednictvím záznamů zveřejněných na internetových stránkách a/nebo na intranetu společného podniku BBI.
Článek 3
Specifikace záruk
1. Společný podnik BBI zavede následující záruky, jejichž cílem je zabránit zneužití či předání osobních údajů nebo nezákonnému přístupu k nim (4):
|
a) |
papírové dokumenty se uchovávají v zabezpečených skříních a přístup k nim mají pouze oprávnění zaměstnanci; |
|
b) |
veškeré údaje v elektronické podobě se uchovávají v zabezpečené IT aplikaci podle bezpečnostních norem společného podniku BBI a ve zvláštních elektronických adresářích, k nimž mají přístup pouze oprávnění zaměstnanci. Vhodné úrovně přístupu se udělují individuálně; |
|
c) |
databáze je chráněna heslem v rámci jednotného systému přihlašování a propojena automaticky s uživatelským jménem a heslem daného uživatele. Nahrazování uživatelů je přísně zakázáno. Elektronické záznamy jsou uchovávány zabezpečeným způsobem, aby se zajistila důvěrnost a soukromí údajů v nich obsažených; |
|
d) |
všechny osoby, které mají přístup k údajům, jsou vázány povinností zachovávat důvěrnost. |
2. Období uchovávání osobních údajů uvedených v čl. 1 odst. 3 nesmí být delší, než je nezbytné a vhodné pro účely, pro něž se údaje zpracovávají. Každopádně však nesmí být delší než období uchovávání uvedené v oznámení o ochraně údajů, prohlášení o ochraně soukromí nebo v záznamech podle článku 6.
3. Pokud společný podnik BBI uvažuje o uplatnění omezení, zváží riziko pro práva a svobody subjektu údajů především ve srovnání s rizikem pro práva a svobody jiných subjektů údajů a s rizikem maření účinku šetření nebo řízení vedených společným podnikem BBI, například formou likvidace důkazů. Rizika pro práva a svobody subjektu údajů se týkají především, ale nikoliv výlučně, ohrožení dobrého jména a práva na obhajobu a práva být vyslechnut.
Článek 4
Omezení
1. Jakékoli omezení společný podnik BBI uplatní výhradně za účelem zabezpečení:
|
a) |
národní bezpečnosti, veřejné bezpečnosti nebo obrany členských států; |
|
b) |
prevence, vyšetřování, odhalování a stíhání trestných činů nebo výkonu trestů, včetně ochrany před hrozbami pro veřejnou bezpečnost a jejich předcházení; |
|
c) |
jiných důležitých cílů obecného veřejného zájmu Unie nebo některého členského státu, zejména cílů společné zahraniční a bezpečnostní politiky Unie nebo důležitých hospodářských nebo finančních zájmů Unie nebo některého členského státu, včetně měnových, rozpočtových a daňových záležitostí, veřejného zdraví a sociálního zabezpečení; |
|
d) |
vnitřní bezpečnosti orgánů a subjektů Unie, včetně jejich sítí elektronických komunikací; |
|
e) |
prevence, vyšetřování, odhalování a stíhání porušování etických pravidel regulovaných povolání; |
|
f) |
monitorovací, inspekční nebo regulační funkce spojené, i pouze příležitostně, s výkonem veřejné moci v případech uvedených v písmenech a) až c); |
|
g) |
ochrany subjektu údajů nebo práv a svobod druhých; |
|
h) |
vymáhání občanskoprávních nároků. |
2. V rámci zvláštního uplatnění účelů uvedených v odstavci 1 výše je společný podnik BBI oprávněn uplatnit omezení za těchto okolností:
|
a) |
v souvislosti s osobními údaji, které byly vyměněny s útvary Komise nebo s jinými orgány, institucemi a subjekty Unie,
|
|
b) |
v souvislosti s osobními údaji, které byly vyměněny s příslušnými orgány členských států,
|
|
c) |
v souvislosti s osobními údaji, které byly vyměněny s třetími zeměmi nebo s mezinárodními organizacemi, pokud existují jasné důkazy, že by výkon těchto práv a povinností pravděpodobně ohrozil spolupráci společného podniku BBI s třetími zeměmi nebo mezinárodními organizacemi při provádění jeho úkolů. |
Před uplatněním omezení za okolností uvedených v písmenech a) a b) prvního pododstavce se společný podnik BBI obrátí na příslušné útvary Komise, orgány, instituce a jiné subjekty Unie nebo příslušné orgány členských států, pokud nebude společnému podniku BBI zřejmé, že uplatnění daného omezení umožňuje jeden z aktů uvedených v těchto písmenech.
Článek 5
Omezení práv subjektů údajů
1. V řádně odůvodněných případech a za podmínek stanovených v tomto rozhodnutí může správce omezit následující práva, pokud je to nezbytné a přiměřené, v souvislosti s operacemi zpracování uvedenými v odstavci 2 níže:
|
a) |
právo na informace; |
|
b) |
právo na přístup; |
|
c) |
právo na opravu, výmaz a omezení zpracování; |
|
d) |
právo na oznamování případů porušení zabezpečení osobních údajů subjektu údajů; |
|
e) |
právo na důvěrnost elektronické komunikace. |
2. V souladu s čl. 25 odst. 2 písm. a) nařízení (EU) 2018/1725 může správce v řádně odůvodněných případech a za podmínek stanovených v tomto rozhodnutí použít omezení v souvislosti s těmito operacemi zpracování:
|
a) |
provádění správních šetření a disciplinárních řízení; |
|
b) |
předběžné činnosti související s případy možných nesrovnalostí oznámených úřadu OLAF; |
|
c) |
řízení v případě whistleblowingu; |
|
d) |
(formální a neformální) řízení v případech obtěžování (7); |
|
e) |
vyřizování interních a externích stížností; |
|
f) |
interní audity; |
|
g) |
šetření prováděná pověřencem pro ochranu osobních údajů v souladu s čl. 45 odst. 2 nařízení (EU) 2018/1725; |
|
h) |
šetření (IT) bezpečnosti prováděná interně nebo se zapojením externích subjektů (např. skupiny CERT-EU); |
|
i) |
v rámci řízení grantů nebo zadávání veřejných zakázek po uplynutí lhůty pro předkládání návrhů nebo nabídek (8). |
Omezení platí, dokud nepominou důvody, které jeho platnost odůvodňují.
3. Pokud společný podnik BBI zcela nebo zčásti omezí uplatňování práv uvedených v odstavci 1 výše, učiní kroky stanovené v článcích 6 a 7 tohoto rozhodnutí.
4. Pokud subjekty údajů požádají o přístup ke svým osobním údajům zpracovávaným v souvislosti s jedním nebo více konkrétními případy nebo ke konkrétní operaci zpracování v souladu s článkem 17 nařízení (EU) 2018/1725, omezí se společný podnik BBI v rámci posuzování této žádosti jen na tyto osobní údaje.
Článek 6
Nezbytnost a přiměřenost omezení
1. Všechna omezení uvedená v článku 5 musí být nezbytná a přiměřená vzhledem k rizikům pro práva a svobody subjektů údajů a musí respektovat podstatu základních práv a svobod v demokratické společnosti.
2. Zvažuje-li se použití omezení, provede se na základě těchto pravidel test nezbytnosti a přiměřenosti. Test se provádí také v rámci pravidelného přezkumu po posouzení toho, zda věcné a právní důvody omezení stále platí. Test se v každém jednotlivém případě zdokumentuje prostřednictvím oznámení o interním posouzení za účelem vyvození odpovědnosti.
3. Omezení jsou dočasná a zruší se, jakmile pominou okolnosti, které tato omezení odůvodňují. Zejména pak v případě, kdy se má za to, že výkon omezeného práva by již nemařil účinek uloženého omezení ani nepříznivě neovlivňoval práva nebo svobody jiných subjektů údajů.
Společný podnik BBI přezkoumá použití omezení každých šest měsíců ode dne jejich přijetí a při uzavření příslušného šetření, řízení nebo vyšetřování. Následně správce každých šest měsíců kontroluje, zda je třeba omezení nadále uplatňovat.
4. Pokud společný podnik BBI použije zcela nebo zčásti omezení uvedená v článku 5 tohoto rozhodnutí, zaznamená důvody omezení a právní základ v souladu s odstavcem 1 výše, včetně posouzení nezbytnosti a přiměřenosti omezení.
Tento záznam a v příslušných případech dokumenty obsahující věcné a právní prvky, z nichž omezení vycházejí, se zaregistrují. Na žádost se zpřístupní evropskému inspektorovi ochrany údajů.
Článek 7
Povinnost informovat
1. Společný podnik BBI v oznámeních o ochraně údajů, prohlášeních o ochraně soukromí nebo v záznamech ve smyslu článku 31 nařízení (EU) 2018/1725 zveřejněných na jeho internetových stránkách a/nebo na intranetu, kde informuje subjekty údajů o jejich právech v rámci daného řízení, uvede informace související s možným omezením těchto práv. Součástí těchto informací je i to, která práva mohou být omezena, důvody omezení a případná délka jeho trvání.
Aniž jsou dotčena ustanovení čl. 6 odst. 4, informuje společný podnik BBI, je-li to přiměřené, jednotlivě všechny subjekty údajů, o nichž se domnívá, že jsou dotčenými osobami v rámci konkrétní operace zpracování, neprodleně a písemně o jejich právech v souvislosti se stávajícími nebo budoucími omezeními.
2. Pokud společný podnik BBI zčásti nebo zcela omezí práva uvedená v článku 5, informuje dotčený subjekt údajů o uplatněném omezení a o jeho hlavních důvodech a také o možnosti podat stížnost u evropského inspektora ochrany údajů nebo požádat o soudní ochranu u Soudního dvora Evropské unie.
Poskytnutí informací uvedených v odstavci 2 výše lze odložit, neprovést nebo odepřít, pokud by mařilo účinek omezení uloženého podle čl. 25 odst. 8 nařízení (EU) 2018/1725.
Článek 8
Přezkum pověřencem pro ochranu osobních údajů
1. Společný podnik BBI neprodleně informuje svého pověřence pro ochranu osobních údajů, kdykoli správce v souladu s tímto rozhodnutím omezí uplatňování práv subjektů údajů nebo prodlouží platnost omezení. Správce poskytne pověřenci pro ochranu osobních údajů přístup k záznamům obsahujícím posouzení nezbytnosti a přiměřenosti omezení a v záznamu uvede datum informování pověřence.
2. Pověřenec pro ochranu osobních údajů může správce písemně požádat, aby použití omezení přezkoumal. Správce pověřence písemně informuje o výsledku vyžádaného přezkumu.
3. Pověřenec pro ochranu osobních údajů je do celého řízení zapojen. Správce informuje pověřence pro ochranu osobních údajů o zrušení omezení.
Článek 9
Vstup v platnost
Toto rozhodnutí vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
V Bruselu dne 26. března 2020.
Za správní radu společného podniku BBI
předseda
Mat QUAEDVLIEG
(1) Úř. věst. L 295, 21.11.2018, s. 39.
(2) Úř. věst. L 169, 7.6.2014, s. 130.
(3) V případě společné správy údajů se údaje zpracovávají v souladu s prostředky a účely stanovenými v příslušné dohodě společných správců, jak je stanoveno v článku 28 nařízení (EU) 2018/1725.
(4) Tento seznam není úplný.
(5) Nařízení Evropského parlamentu a Rady (EU) 2016/679 ze dne 27. dubna 2016 o ochraně fyzických osob v souvislosti se zpracováním osobních údajů a o volném pohybu těchto údajů a o zrušení směrnice 95/46/ES (obecné nařízení o ochraně osobních údajů) (Úř. věst. L 119, 4.5.2016, s. 1).
(6) Směrnice Evropského parlamentu a Rady (EU) 2016/680 ze dne 27. dubna 2016 o ochraně fyzických osob v souvislosti se zpracováním osobních údajů příslušnými orgány za účelem prevence, vyšetřování, odhalování či stíhání trestných činů nebo výkonu trestů, o volném pohybu těchto údajů a o zrušení rámcového rozhodnutí Rady 2008/977/SVV (Úř. věst. L 119, 4.5.2016, s. 89).
(7) Tato operace zpracování se nevztahuje na čl. 5 odst. 1 písm. d).
(8) Tato operace zpracování se vztahuje pouze na čl. 5 odst. 1 písm. c).