ISSN 1977-0626
Úřední věstník
Evropské unie
L 115

České vydání
Právní předpisy
Ročník 60
4. května 2017
|
ISSN 1977-0626 |
||
|
Úřední věstník Evropské unie |
L 115 |
|

|
||
|
České vydání |
Právní předpisy |
Ročník 60 |
|
Obsah |
|
II Nelegislativní akty |
Strana |
|
|
|
MEZINÁRODNÍ DOHODY |
|
|
|
* |
||
|
|
|
||
|
|
* |
||
|
|
* |
||
|
|
|
NAŘÍZENÍ |
|
|
|
* |
Nařízení Komise (EU) 2017/771 ze dne 3. května 2017, kterým se mění nařízení (ES) č. 152/2009, pokud jde o metody pro stanovení obsahu dioxinů a polychlorovaných bifenylů ( 1 ) |
|
|
|
* |
||
|
|
|
||
|
|
|
SMĚRNICE |
|
|
|
* |
Směrnice Komise (EU) 2017/774 ze dne 3. května 2017, kterou se za účelem přijetí zvláštních limitních hodnot pro chemické látky použité v hračkách mění dodatek C přílohy II směrnice Evropského parlamentu a Rady 2009/48/ES o bezpečnosti hraček, pokud jde o fenol ( 1 ) |
|
|
|
|
ROZHODNUTÍ |
|
|
|
* |
|
|
|
|
|
(1) Text s významem pro EHP. |
|
CS |
Akty, jejichž název není vyti_těn tučně, se vztahují ke každodennímu řízení záležitostí v zemědělství a obecně platí po omezenou dobu. Názvy všech ostatních aktů jsou vytištěny tučně a předchází jim hvězdička. |
II Nelegislativní akty
MEZINÁRODNÍ DOHODY
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/1 |
ROZHODNUTÍ RADY (EU) 2017/768
ze dne 18. července 2016
o podpisu jménem Evropské unie a jejích členských států a prozatímním provádění Protokolu k Evropsko-středomořské dohodě zakládající přidružení mezi Evropskými společenstvími a jejich členskými státy na jedné straně a Egyptskou arabskou republikou na straně druhé s ohledem na přistoupení Chorvatské republiky k Evropské unii
RADA EVROPSKÉ UNIE,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na článek 217 ve spojení s čl. 218 odst. 5 této smlouvy,
s ohledem na akt o přistoupení Chorvatské republiky, a zejména na čl. 6 odst. 2 uvedeného aktu,
s ohledem na návrh Evropské komise,
vzhledem k těmto důvodům:
|
(1) |
Dne 25. června 2001 byla podepsána Evropsko-středomořská dohoda, kterou se zakládá přidružení mezi Evropskými společenstvími a jejich členskými státy na jedné straně a Egyptskou arabskou republikou na straně druhé (1) (dále jen „dohoda“). Tato dohoda vstoupila v platnost dnem 1. června 2004. |
|
(2) |
Chorvatská republika se stala dne 1. července 2013 členským státem Evropské unie. |
|
(3) |
Podle čl. 6 odst. 2 aktu o přistoupení Chorvatské republiky má být její přistoupení k dohodě schváleno prostřednictvím protokolu k dohodě uzavřeným mezi Radou jednající jednomyslně jménem členských států a Egyptskou arabskou republikou. |
|
(4) |
Rada dne 14. září 2012 pověřila Komisi, aby zahájila jednání s Egyptskou arabskou republikou. Tato jednání byla úspěšně uzavřena parafováním protokolu dne 29. října 2015 v Bruselu. |
|
(5) |
Ustanovení čl. 8 odst. 3 protokolu stanoví prozatímní provádění protokolu do okamžiku, než vstoupí v platnost. |
|
(6) |
Protokol by měl být podepsán s výhradou uzavření a měl by být prozatímně prováděn, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Podpis Protokolu k Evropsko-středomořské dohodě zakládající přidružení mezi Evropskými společenstvími a jejich členskými státy na jedné straně a Egyptskou arabskou republikou na straně druhé s ohledem na přistoupení Chorvatské republiky k Evropské unii jménem Unie a jejích členských států se schvaluje s výhradou uzavření uvedeného protokolu.
Znění protokolu je připojeno k tomuto rozhodnutí.
Článek 2
Předseda Rady je oprávněn jmenovat osobu nebo osoby zmocněné podepsat protokol jménem Evropské unie a jejích členských států.
Článek 3
Protokol je prováděn prozatímně v souladu s čl. 8 odst. 3 protokolu ode dne 1. července 2013 do okamžiku, než budou dokončeny postupy nezbytné pro jeho uzavření.
Článek 4
Toto rozhodnutí vstupuje v platnost dnem přijetí.
V Bruselu dne 18. července 2016.
Za Radu
předsedkyně
F. MOGHERINI
(1) Úř. věst. L 304, 30.9.2004, s. 39.
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/3 |
PROTOKOL
k Evropsko-středomořské dohodě zakládající přidružení mezi Evropskými společenstvími a jejich členskými státy na jedné straně a Egyptskou arabskou republikou na straně druhé s ohledem na přistoupení Chorvatské republiky k Evropské unii
BELGICKÉ KRÁLOVSTVÍ,
BULHARSKÁ REPUBLIKA,
ČESKÁ REPUBLIKA,
DÁNSKÉ KRÁLOVSTVÍ,
SPOLKOVÁ REPUBLIKA NĚMECKO,
ESTONSKÁ REPUBLIKA,
IRSKO,
ŘECKÁ REPUBLIKA,
ŠPANĚLSKÉ KRÁLOVSTVÍ,
FRANCOUZSKÁ REPUBLIKA,
CHORVATSKÁ REPUBLIKA,
ITALSKÁ REPUBLIKA,
KYPERSKÁ REPUBLIKA,
LOTYŠSKÁ REPUBLIKA,
LITEVSKÁ REPUBLIKA,
LUCEMBURSKÉ VELKOVÉVODSTVÍ,
MAĎARSKO,
REPUBLIKA MALTA,
NIZOZEMSKÉ KRÁLOVSTVÍ,
RAKOUSKÁ REPUBLIKA,
POLSKÁ REPUBLIKA,
PORTUGALSKÁ REPUBLIKA,
RUMUNSKO,
REPUBLIKA SLOVINSKO,
SLOVENSKÁ REPUBLIKA,
FINSKÁ REPUBLIKA,
ŠVÉDSKÉ KRÁLOVSTVÍ,
SPOJENÉ KRÁLOVSTVÍ VELKÉ BRITÁNIE A SEVERNÍHO IRSKA,
smluvní strany Smlouvy o Evropské unii a Smlouvy o fungování Evropské unie, dále jen „členské státy“, a
EVROPSKÁ UNIE, dále též „Unie“,
na jedné straně a
EGYPTSKÁ ARABSKÁ REPUBLIKA, dále jen „Egypt“,
na straně druhé,
pro účely tohoto protokolu dále jen „smluvní strany“,
vzhledem k těmto důvodům:
|
(1) |
Evropsko-středomořská dohoda zakládající přidružení mezi Evropskými společenstvími a jejich členskými státy na jedné straně a Egyptskou arabskou republikou na straně druhé (dále jen „dohoda“) byla podepsána v Lucemburku dne 25. června 2001 a vstoupila v platnost dne 1. června 2004. |
|
(2) |
Smlouva o přistoupení Chorvatské republiky k Evropské unii byla podepsána v Bruselu dne 9. prosince 2011 a vstoupila v platnost dne 1. července 2013. |
|
(3) |
V souladu s čl. 6 odst. 2 aktu o přistoupení Chorvatské republiky má být její přistoupení k dohodě schváleno uzavřením protokolu k dohodě. |
|
(4) |
Proběhly konzultace v souladu s čl. 21 odst. 2 dohody, aby se zajistilo zohlednění vzájemných zájmů Unie i Egypta, |
SE DOHODLY TAKTO:
Článek 1
Chorvatská republika přistupuje jako smluvní strana k Evropsko-středomořské dohodě zakládající přidružení mezi Evropskými společenstvími a jejich členskými státy na jedné straně a Egyptskou arabskou republikou na straně druhé a přijímá a bere na vědomí, stejně jako ostatní členské státy Unie, znění dohody i společných prohlášení, prohlášení a výměn dopisů.
KAPITOLA I
ZMĚNY DOHODY VČETNĚ JEJÍCH PŘÍLOH A PROTOKOLŮ
Článek 2
Zemědělské produkty, zpracované zemědělské produkty, ryby a produkty rybolovu
Tabulka, která tvoří přílohu protokolu č. 1 k dohodě, se mění v souladu s tabulkou uvedenou v příloze tohoto protokolu.
Článek 3
Pravidla původu
Pro období mezi 1. červencem 2013 a 31. lednem 2016 se protokol č. 4 mění takto:
|
1) |
Příloha IVa se nahrazuje tímto: „PŘÍLOHA IVa ZNĚNÍ PROHLÁŠENÍ NA FAKTUŘE Prohlášení na faktuře, jehož znění je uvedeno níže, musí být vyhotoveno v souladu s poznámkami pod čarou. Text poznámek pod čarou však není třeba uvádět. Bulharské znění Износителят на продуктите, обхванати от този документ (митническо разрешение № … (1)) декларира, че освен където е отбелязано друго, тези продукти са с … преференциален произход (2). Španělské znění El exportador de los productos incluidos en el presente documento [autorización aduanera no … (1)] declara que, salvo indicación expresa en sentido contrario, estos productos gozan de un origen preferencial … (2). České znění Vývozce výrobků uvedených v tomto dokumentu (číslo povolení … (1)) prohlašuje, že kromě zřetelně označených mají tyto výrobky preferenční původ v … (2). Dánské znění Eksportøren af varer, der er omfattet af nærværende dokument, (toldmyndighedernes tilladelse nr. … (1)), erklærer, at varerne, medmindre andet tydeligt er angivet, har præferenceoprindelse i … (2). Německé znění Der Ausführer (Ermächtigter Ausführer; Bewilligungs-Nr. … (1)) der Waren, auf die sich dieses Handelspapier bezieht, erklärt, dass diese Waren, soweit nicht anders angegeben, präferenzbegünstigte … (2) Ursprungswaren sind. Estonské znění Käesoleva dokumendiga hõlmatud toodete eksportija (tolli luba nr … (1)) deklareerib, et need tooted on … (2) sooduspäritoluga, välja arvatud juhul, kui on selgelt näidatud teisiti. Řecké znění Ο εξαγωγέας των προϊόντων που καλύπτονται από το παρόν έγγραφο [άδεια τελωνείου υπ' αριθ. … (1)] δηλώνει ότι, εκτός εάν δηλώνεται σαφώς άλλως, τα προϊόντα αυτά είναι προτιμησιακής καταγωγής … (2). Anglické znění The exporter of the products covered by this document (customs authorisation No … (1)) declares that, except where otherwise clearly indicated, these products are of … (2) preferential origin. Francouzské znění L'exportateur des produits couverts par le présent document [autorisation douanière no … (1)] déclare que, sauf indication claire du contraire, ces produits ont l'origine préférentielle … (2). Chorvatské znění Izvoznik proizvoda obuhvaćenih ovom ispravom (carinsko ovlaštenje br. … (1)) izjavljuje da su, osim ako je drugačije izričito navedeno, ovi proizvodi … (2) preferencijalnog podrijetla. Italské znění L'esportatore delle merci contemplate nel presente documento [autorizzazione doganale n. … (1)] dichiarache, salvo indicazione contraria, le merci sono di origine preferenziale … (2). Lotyšské znění To produktu eksportētājs, kuri ietverti šajā dokumentā (muitas atļauja Nr. … (1)), deklarē, ka, izņemot tur, kur ir citādi skaidri noteikts, šiem produktiem ir preferenciāla izcelsme … (2). Litevské změní Šiame dokumente išvardintų produktų eksportuotojas (muitinės liudijimo Nr … (1)) deklaruoja, kad, jeigu kitaip nenurodyta, tai yra … (2) preferencinės kilmės produktai. Maďarské znění A jelen okmányban szereplő áruk exportőre (vámfelhatalmazási szám: … (1)) kijelentem, hogy egyértelmű eltérő jelzés hiányában az áruk preferenciális … (2) származásúak. Maltské znění L-esportatur tal-prodotti koperti b'dan id-dokument (awtorizzazzjoni tad-dwana nru … (1)) jiddikjara li, ħlief fejn indikat b'mod ċar li mhux hekk, dawn il-prodotti huma ta' oriġini preferenzjali … (2). Nizozemské znění De exporteur van de goederen waarop dit document van toepassing is (douanevergunning nr. … (1)), verklaart dat, behoudens uitdrukkelijke andersluidende vermelding, deze goederen van preferentiële … oorsprong zijn (2). Polské znění Eksporter produktów objętych tym dokumentem (upoważnienie władz celnych nr … (1)) deklaruje, że z wyjątkiem gdzie jest to wyraźnie określone, produkty te mają … (2) preferencyjne pochodzenie. Portugalské znění O exportador dos produtos abrangidos pelo presente documento [autorização aduaneira n.o … (1)], declara que, salvo declaração expressa em contrário, estes produtos são de origem preferencial … (2). Rumunské znění Exportatorul produselor ce fac obiectul acestui document [autorizația vamală nr. … (1)] declară că, exceptând cazul în care în mod expres este indicat altfel, aceste produse sunt de origine preferențială … (2). Slovinské znění Izvoznik blaga, zajetega s tem dokumentom (pooblastilo carinskih organov št. … (1)) izjavlja, da, razen če ni drugače jasno navedeno, ima to blago preferencialno poreklo … (2). Slovenské znění Vývozca výrobkov uvedených v tomto dokumente [číslo povolenia … (1)] vyhlasuje, že okrem zreteľne označených, majú tieto výrobky preferenčný pôvod v … (2). Finské znění Tässä asiakirjassa mainittujen tuotteiden viejä (tullin lupa nro … (1)) ilmoittaa, että nämä tuotteet ovat, ellei toisin ole selvästi merkitty, etuuskohteluun oikeutettuja … (2) alkuperätuotteita. Švédské znění Exportören av de varor som omfattas av detta dokument (tullmyndighetens tillstånd nr … (1)) försäkrar att dessa varor, om inte annat tydligt markerats, har förmånsberättigande … ursprung (2). Arabské znění
… (3) (Místo a datum) … (Podpis vývozce; dále musí být čitelně uvedeno jméno osoby, která prohlášení podepisuje.) (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (1) Činí-li prohlášení na faktuře schválený vývozce ve smyslu článku 23 protokolu, uvede se na tomto místě číslo povolení schváleného vývozce. Nečiní-li prohlášení na faktuře schválený vývozce, slova v závorkách se musí vynechat nebo musí místo zůstat prázdné." (2) Je třeba uvést původ produktů. Týká-li se prohlášení na faktuře zcela nebo zčásti produktů pocházejících z Ceuty a Melilly ve smyslu článku 38 protokolu, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, pomocí zkratky „CM“." (3) Tyto údaje lze vypustit, je-li informace uvedena v samotném dokladu." |
|
2) |
Příloha IVb se nahrazuje tímto: „PŘÍLOHA IVb ZNĚNÍ PROHLÁŠENÍ NA FAKTUŘE EUR-MED Prohlášení na faktuře EUR-MED, jehož znění je uvedeno níže, musí být vyhotoveno v souladu s poznámkami pod čarou. Text poznámek pod čarou však není třeba uvádět. Bulharské znění Износителят на продуктите, обхванати от този документ (митническо разрешение № … (4)) декларира, че освен където ясно е отбелязано друго, тези продукти са с … преференциален произход (5).
Španělské znění El exportador de los productos incluidos en el presente documento [autorización aduanera no … (4)] declara que, salvo indicación expresa en sentido contrario, estos productos gozan de un origen preferencial … (5).
České znění Vývozce výrobků uvedených v tomto dokumentu (číslo povolení … (4)) prohlašuje, že kromě zřetelně označených mají tyto výrobky preferenční původ v … (5).
Dánské znění Eksportøren af varer, der er omfattet af nærværende dokument, (toldmyndighedernes tilladelse nr. … (4)), erklærer, at varerne, medmindre andet tydeligt er angivet, har præferenceoprindelse i … (5).
Německé znění Der Ausführer (Ermächtigter Ausführer; Bewilligungs-Nr. … (4)) der Waren, auf die sich dieses Handelspapier bezieht, erklärt, dass diese Waren, soweit nicht anderes angegeben, präferenzbegünstigte … (5) Ursprungswaren sind.
Estonské znění Käesoleva dokumendiga hõlmatud toodete eksportija (tolli luba nr. … (4)) deklareerib, et need tooted on … (5) sooduspäritoluga, välja arvatud juhul kui on selgelt näidatud teisiti.
Řecké znění Ο εξαγωγέας των προϊόντων που καλύπτονται από το παρόν έγγραφο (άδεια τελωνείου υπ'αριθ. … (4)) δηλώνει ότι, εκτός εάν δηλώνεται σαφώς άλλως, τα προϊόντα αυτά είναι προτιμησιακής καταγωγής … (5).
Anglické znění The exporter of the products covered by this document (customs authorization No … (4)) declares that, except where otherwise clearly indicated, these products are of … (5) preferential origin.
Francouzské znění L'exportateur des produits couverts par le présent document (autorisation douanière no … (4)) déclare que, sauf indication claire du contraire, ces produits ont l'origine préférentielle … (5)).
Chorvatské znění Izvoznik proizvoda obuhvaćenih ovom ispravom (carinsko ovlaštenje br. … (4)) izjavljuje da su, osim ako je to drugačije izričito navedeno, ovi proizvodi … (5) preferencijalnog podrijetla.
Italské znění L'esportatore delle merci contemplate nel presente documento (autorizzazione doganale n. … (4)) dichiara che, salvo indicazione contraria, le merci sono di origine preferenziale … (5).
Lotyšské znění To produktu eksportētājs, kuri ietverti šajā dokumentā (muitas atļauja Nr. … (4)), deklarē, ka, izņemot tur, kur ir citādi skaidri noteikts, šiem produktiem ir preferenciāla izcelsme … (5).
Litevské změní Šiame dokumente išvardytų produktų eksportuotojas (muitinės liudijimo Nr … (4)) deklaruoja, kad, jeigu kitaip nenurodyta, tai yra … (5) preferencinės kilmės produktai.
Maďarské znění A jelen okmányban szereplő áruk exportőre (vámfelhatalmazási szám: … (4)) kijelentem, hogy egyértelmű eltérő jelzés hiányában az áruk preferenciális … (5) származásúak.
Maltské znění L-esportatur tal-prodotti koperti b'dan id-dokument (awtorizzazzjoni tad-dwana nru … (4)) jiddikjara li, ħlief fejn indikat b'mod ċar li mhux hekk, dawn il-prodotti huma ta' oriġini preferenzjali … (5).
Nizozemské znění De exporteur van de goederen waarop dit document van toepassing is (douanevergunning nr. … (4)), verklaart dat, behoudens uitdrukkelijke andersluidende vermelding, deze goederen van preferentiële … oorsprong zijn (5).
Polské znění Eksporter produktów objętych tym dokumentem (upoważnienie władz celnych nr … (4)) deklaruje, że z wyjątkiem gdzie jest to wyraźnie określone, produkty te mają … (5) preferencyjne pochodzenie.
Portugalské znění O exportador dos produtos abrangidos pelo presente documento (autorização aduaneira no. … (4)) declara que, salvo declaração expressa em contrário, estes produtos são de origem preferencial … (5).
Rumunské znění Exportatorul produselor ce fac obiectul acestui document (autorizația vamală nr. … (4)) declară că, exceptând cazul în care în mod expres este indicat altfel, aceste produse sunt de origine preferențială … (5).
Slovinské znění Izvoznik blaga, zajetega s tem dokumentom (pooblastilo carinskih organov št … (4)) izjavlja, da, razen če ni drugače jasno navedeno, ima to blago preferencialno … (5) poreklo.
Slovenské znění Vývozca výrobkov uvedených v tomto dokumente (číslo povolenia … (4)) vyhlasuje, že okrem zreteľne označených, majú tieto výrobky preferenčný pôvod v … (5).
Finské znění Tässä asiakirjassa mainittujen tuotteiden viejä (tullin lupa n:o … (4)) ilmoittaa, että nämä tuotteet ovat, ellei toisin ole selvästi merkitty, etuuskohteluun oikeutettuja … alkuperätuotteita (5).
Švédské znění Exportören av de varor som omfattas av detta dokument (tullmyndighetens tillstånd nr. … (4)) försäkrar att dessa varor, om inte annat tydligt markerats, har förmånsberättigande … ursprung (5).
Arabské znění
… (7) (Místo a datum) … (Podpis vývozce; dále musí být čitelně uvedeno jméno osoby, která prohlášení podepisuje.) (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (4) Je-li prohlášení o původu vyhotoveno schváleným vývozcem, musí zde být uvedeno číslo oprávnění schváleného vývozce. Nečiní-li prohlášení o původu schválený vývozce, slova v závorkách se vynechají nebo se místo nechá prázdné." (5) Je třeba uvést původ produktů. Týká-li se prohlášení o původu zcela nebo zčásti produktů pocházejících z Ceuty a Melilly, musí je vývozce zřetelně vyznačit na dokladu, na němž je prohlášení činěno, uvedením zkratky „CM“." (6) Vyplňte podle potřeby a nehodící se škrtněte." (6) Vyplňte podle potřeby a nehodící se škrtněte." (7) Tyto údaje lze vypustit, je-li informace uvedena v samotném dokladu." |
KAPITOLA II
PŘECHODNÁ USTANOVENÍ
Článek 4
Zboží v režimu tranzitu
1. Ustanovení dohody mohou být použita na zboží vyvážené z Egypta do Chorvatska nebo z Chorvatska do Egypta, které je v souladu s ustanoveními protokolu č. 4 k dohodě a které bylo ke dni přistoupení Chorvatska buď na cestě, v dočasném uskladnění nebo v celním skladu nebo ve svobodném celním pásmu v Egyptě nebo v Chorvatsku.
2. V takových případech lze přiznat preferenční zacházení, je-li celním orgánům dovážející země do čtyř měsíců ode dne přistoupení Chorvatska předložen doklad o původu vystavený dodatečně celními orgány vyvážející země.
KAPITOLA III
ZÁVĚREČNÁ A OBECNÁ USTANOVENÍ
Článek 5
Egypt se zavazuje, že v souvislosti s tímto rozšířením Unie nevznese žádný nárok, požadavek či žalobu, ani nezmění či neodejme žádnou koncesi podle čl. XXIV odst. 6 a článku XXVIII GATT 1994.
Článek 6
V přiměřené lhůtě po parafování tohoto protokolu sdělí Unie svým členským státům a Egyptu chorvatské znění dohody. S výhradou vstupu tohoto protokolu v platnost se jazykové znění uvedené v první větě tohoto článku stává platným za stejných podmínek jako anglické, bulharské, české, dánské, estonské, finské, francouzské, italské, litevské, lotyšské, maďarské, maltské, německé, nizozemské, polské, portugalské, rumunské, řecké, slovenské, slovinské, španělské, švédské a arabské znění dohody.
Článek 7
Protokol a jeho příloha tvoří nedílnou součást dohody.
Článek 8
1 Tento protokol schválí Rada Evropské unie jménem Unie a jejích členských států a Egypt v souladu se svými postupy. Strany si vzájemně oznámí dokončení postupů potřebných k tomuto účelu. Listiny o schválení se uloží u Generálního sekretariátu Rady Evropské unie.
2. Tento protokol vstupuje v platnost prvním dnem druhého měsíce následujícího po dni, kdy si všechny strany navzájem oznámí, že byly dokončeny postupy k tomu nezbytné.
3. Do okamžiku, než protokol vstoupí v platnost, bude prováděn prozatímně ode dne 1. července 2013.
Článek 9
Tento protokol je sepsán ve dvou vyhotoveních v jazyce anglickém, bulharském, českém, dánském, estonském, finském, francouzském, chorvatském, italském, litevském, lotyšském, maďarském, maltském, německém, nizozemském, polském, portugalském, rumunském, řeckém, slovenském, slovinském, španělském, švédském a arabském, přičemž všechna znění mají stejnou platnost.
NA DŮKAZ ČEHOŽ připojili níže podepsaní a řádně zplnomocnění zástupci k tomuto protokolu své podpisy.
Съставено в Брюксел на десети април през две хиляди и седемнадесета година.
Hecho en Bruselas, el diez de abril de dos mil diecisiete.
V Bruselu dne desátého dubna dva tisíce sedmnáct.
Udfærdiget i Bruxelles den tiende april to tusind og sytten.
Geschehen zu Brüssel am zehnten April zweitausendsiebzehn.
Kahe tuhande seitsmeteistkümnenda aasta aprillikuu kümnendal päeval Brüsselis.
Έγινε στις Βρυξέλλες, στις δέκα Απριλίου δύο χιλιάδες δεκαεπτά.
Done at Brussels on the tenth day of April in the year two thousand and seventeen.
Fait à Bruxelles, le dix avril deux mille dix-sept.
Sastavljeno u Bruxellesu desetog travnja godine dvije tisuće sedamnaeste.
Fatto a Bruxelles, addì dieci aprile duemiladiciassette.
Briselē, divi tūkstoši septiņpadsmitā gada desmitajā aprīlī.
Priimta Briuselyje du tūkstančiai septynioliktųjų metų balandžio dešimtą dieną.
Kelt Brüsszelben, a kétezer-tizenhetedik év április havának tizedik napján.
Magħmul fi Brussell, fl-għaxar jum ta' April fis-sena elfejn u sbatax.
Gedaan te Brussel, tien april tweeduizend zeventien.
Sporządzono w Brukseli dnia dziesiątego kwietnia roku dwa tysiące siedemnastego.
Feito em Bruxelas, em dez de abril de dois mil e dezassete.
Întocmit la Bruxelles la zece aprilie două mii șaptesprezece.
V Bruseli desiateho apríla dvetisícsedemnásť.
V Bruslju, dne desetega aprila leta dva tisoč sedemnajst.
Tehty Brysselissä kymmenentenä päivänä huhtikuuta vuonna kaksituhattaseitsemäntoista.
Som skedde i Bryssel den tionde april år tjugohundrasjutton.

За държавите-членки
Por los Estados miembros
Za členské státy
For medlemsstaterne
Für die Mitgliedstaaten
Liikmesriikide nimel
Για τα κράτη μέλη
For the Member States
Pour les États membres
Za države članice
Per gli Stati membri
Dalībvalstu vārdā –
Valstybių narių vardu
A tagállamok részéről
Għall-Istati Membri
Voor de lidstaten
W imieniu Państw Członkowskich
Pelos Estados-Membros
Pentru statele membre
Za členské štáty
Za države članice
Jäsenvaltioiden puolesta
För medlemsstaterna
![]()
![]()
За Европейския съюз
Рог la Unión Europea
Za Evropskou unii
For Den Europæiske Union
Für die Europäische Union
Euroopa Liidu nimel
Για την Ευρωπαϊκή Ένωση
For the European Union
Pour l'Union européenne
Za Europsku uniju
Per l'Unione europea
Eiropas Savienības vārdā –
Europos Sąjungos vardu
Az Európai Unió részéről
Għall-Unjoni Ewropea
Voor de Europese Unie
W imieniu Unii Europejskiej
Pela União Europeia
Pentru Uniunea Europeană
Za Európsku úniu
Za Evropsko unijo
Euroopan unionin puolesta
För Europeiska unionen


За Арабска република Египет
Por la República Árabe de Egipto
Za Egyptskou arabskou republiku
For Den Arabiske Republik Egypten
Für die Arabische Republik Ägypten
Egiptuse Araabia Vabariigi nimel
Για την Αραβική Δημοκρατία της Αιγύπτου
For the Arab Republic of Egypt
Pour la République arabe d'Égypte
Za Arapsku Republiku Egipat
Per la Repubblica araba d'Egitto
Ēģiptes Arābu Republikas vārdā –
Egipto Arabų Respublikos vardu
az Egyiptomi Arab Köztársaság részéről
Għar-Repubblika Għarbija tal-Eġittu
Voor de Arabische Republiek Egypte
W imieniu Arabskiej Republiki Egiptu
Pela República Árabe do Egipto
Pentru Republica Arabă Egipt
Za Egyptskú arabskú republiku
Za Arabsko republiko Egipt
Egyptin arabitasavallan puolesta
För Arabrepubliken Egypten
![]()

PŘÍLOHA
ZEMĚDĚLSKÉ PRODUKTY, ZPRACOVANÉ ZEMĚDĚLSKÉ PRODUKTY, RYBY A PRODUKTY RYBOLOVU
ZMĚNY PROTOKOLU Č. 1DOHODY O REŽIMECH DOVOZU PROZEMĚDĚLSKÉ PRODUKTY, ZPRACOVANÉ ZEMĚDĚLSKÉ PRODUKTY, RYBY A PRODUKTY RYBOLOVU POCHÁZEJÍCÍ Z EGYPTA DO UNIE
Koncese uvedené v této příloze u produktů podpoložky 0810 10 00 nahrazují koncese v současnosti uplatňované v rámci dohody o přidružení (protokol č. 1). Pro všechny výrobky, které nejsou v této příloze uvedeny, se koncese uplatňované v současnosti nemění.
|
Kód KN |
Popis |
Snížení cla podle doložky nejvyšších výhod v (%) |
Celní kvóta (čistá hmotnost v tunách) |
Snížení cla nad existující celní kvótu v (%) |
Zvláštní ustanovení |
|
0810 10 00 |
Čerstvé jahody, od 1. října do 30. dubna |
100 % |
10 000 |
— |
|
|
100 % |
94 |
— |
Zvláštní ustanovení v bodě 5 protokolu č. 1 se nepoužijí |
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/15 |
ROZHODNUTÍ RADY (EU) 2017/769
ze dne 25. dubna 2017
o ratifikaci členskými státy a jejich přistoupení v zájmu Evropské unie k Protokolu z roku 2010 k Mezinárodní úmluvě o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři, s výjimkou aspektů týkajících se justiční spolupráce v občanských věcech
RADA EVROPSKÉ UNIE,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 100 odst. 2 ve spojení s čl. 218 odst. 6 písm. a) bodem v) této smlouvy,
s ohledem na návrh Evropské komise,
s ohledem na souhlas Evropského parlamentu (1),
vzhledem k těmto důvodům:
|
(1) |
Mezinárodní úmluva o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři z roku 1996 (dále jen „úmluva HNS z roku 1996“) má za cíl zajistit odpovídající, rychlé a účinné poskytnutí náhrady osobám, které utrpí škodu způsobenou únikem nebezpečných a škodlivých látek při přepravě po moři. Úmluva HNS z roku 1996 zaplnila podstatnou mezeru v mezinárodní úpravě odpovědnosti v oblasti námořní dopravy. |
|
(2) |
V roce 2002 přijala Rada rozhodnutí 2002/971/ES (2). V souladu s uvedeným rozhodnutím byla členským státům uložena povinnost učinit kroky potřebné k ratifikaci úmluvy HNS z roku 1996 nebo k přistoupení k této úmluvě v přiměřené lhůtě a pokud možno do 30. června 2006. Následně tuto úmluvu ratifikovaly čtyři členské státy. Úmluva HNS z roku 1996 dosud nevstoupila v platnost. |
|
(3) |
Úmluva HNS z roku 1996 byla pozměněna Protokolem z roku 2010 k úmluvě HNS z roku 1996 („protokol z roku 2010“). Podle článku 2 a čl. 18 odst. 1 protokolu z roku 2010 jsou úmluva HNS z roku 1996 a protokol z roku 2010 stranami protokolu z roku 2010 chápány, vykládány a uplatňovány společně jako jediná listina. |
|
(4) |
Konsolidované znění úmluvy HNS z roku 1996 a protokolu z roku 2010 (dále jen „úmluva HNS z roku 2010“) vypracoval sekretariát Mezinárodní námořní organizace (dále jen „IMO“) a schválil ho její právní výbor na svém 98. zasedání. Úmluva HNS z roku 2010 není listinou určenou k podpisu nebo ratifikaci. Tato úmluva nabude účinku, jakmile vstoupí v členských státech v platnost protokol z roku 2010. |
|
(5) |
Jestliže stát vyjádří souhlas být vázán protokolem z roku 2010 ruší se tím v souladu s čl. 20 odst. 8 tohoto protokolu všechna předchozí vyjádření souhlasu tohoto státu být vázán úmluvou HNS z roku 1996. Státy, které jsou smluvními stranami úmluvy HNS z roku 1996, jimi tedy přestanou být v okamžiku, kdy vyjádří souhlas, aby byly vázány protokolem z roku 2010 v souladu s článkem 20 tohoto protokolu, zejména s odstavci 2, 3 a 4 tohoto článku. |
|
(6) |
Cílem směrnice Evropského parlamentu a Rady 2004/35/ES (3) je předcházet škodám na životním prostředí způsobeným pracovními činnostmi, včetně přepravy nebezpečného zboží po moři, a napravovat je. Nepoužije se však na případy zranění osob, na škody na soukromém majetku nebo na jakékoli hospodářské ztráty a nemá vliv na jakákoli práva na náhradu těchto škod. Předmět uvedené směrnice a předmět úmluvy HNS z roku 2010 se tedy částečně překrývají, avšak nikoli ve velké míře. Členské státy si ponechávají pravomoc v záležitostech, na něž se vztahuje úmluva HNS z roku 2010 a pro něž nebyla stanovena společná pravidla. |
|
(7) |
Stejně jako její předchůdkyně je i úmluva HNS z roku 2010 zvláště důležitá s ohledem na zájmy Unie a jejích členských států, protože poskytuje větší ochranu obětem škod způsobených přepravou nebezpečných a škodlivých látek po moři, a to i v oblasti škod na životním prostředí, v souladu s Úmluvou Organizace spojených národů o mořském právu z roku 1982. |
|
(8) |
Pro to, aby se státy staly smluvními stranami protokolu z roku 2010, a tím i úmluvy HNS z roku 2010, musí předložit generálnímu tajemníkovi IMO zároveň se schvalovací listinou příslušné údaje o celkovém množství nákladu podléhajícím příspěvku podle úmluvy HNS z roku 2010, který byl přijat během předcházejícího kalendářního roku, a to v souladu s čl. 20 odst. 4 této úmluvy. Dříve, než státy vyjádří souhlas, aby byly vázány protokolem z roku 2010, mají povinnost za tímto účelem vytvořit systém podávání zpráv o nákladu podléhajícím příspěvku podle úmluvy HNS z roku 2010. |
|
(9) |
V roce 2013 právní výbor IMO na svém 100. zasedání potvrdil pokyny k podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku, jež byly vypracovány s cílem usnadnit přijetí právních předpisů o podávání zpráv ratifikujícími státy před vstupem protokolu z roku 2010 v platnost a podpořit globální, jednotné a účinné provádění příslušných požadavků úmluvy HNS z roku 2010. |
|
(10) |
K zajištění právní jistoty pro všechny příslušné zúčastněné strany by členské státy měly náležitě informovat sebe navzájem, jakož i Radu a Komisi o svých systémech podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku. Tyto informace mohou být zpřístupněny neformálně prostřednictvím stávajících informačních kanálů, jako jsou přípravné orgány Rady. |
|
(11) |
Úsilí členských států o vytvoření systémů podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku podle úmluvy HNS z roku 2010, by mohlo být podpořeno výměnou osvědčených postupů mezi členskými státy, pokud jde o zřizování těchto systémů. |
|
(12) |
V případě neexistence doložky o organizacích regionální hospodářské integrace, jako tomu bylo v případě úmluvy HNS z roku 1996, mohou být smluvními stranami protokolu z roku 2010 pouze svrchované státy. Unie proto nemůže ratifikovat protokol z roku 2010 ani k němu přistoupit, a tudíž nemůže přistoupit ani k úmluvě HNS z roku 2010. |
|
(13) |
Ratifikace protokolu z roku 2010 všemi členskými státy v daném časovém rámci by měla zajistit všem dotčeným subjektům při uplatňování úmluvy HNS z roku 2010 rovné podmínky v rámci Unie. |
|
(14) |
S ohledem na mezinárodní povahu režimu HNS by mělo být při uplatňování úmluvy HNS z roku 2010 usilováno o rovné podmínky na celosvětové úrovni pro všechny dotčené subjekty. Je proto potřeba zajistit celosvětovou působnost protokolu z roku 2010. |
|
(15) |
Členské státy by proto měly být zmocněny k tomu, aby v případě částí spadajících do výhradní pravomoci Unie ratifikovaly protokol z roku 2010, nebo případně k němu přistoupily, s výjimkou aspektů souvisejících s justiční spoluprací v občanských věcech. Ustanovení úmluvy HNS z roku 2010 spadající do oblasti pravomoci svěřené Unii v rámci justiční spolupráce v občanských věcech budou předmětem rozhodnutí, jež bude přijato souběžně s tímto rozhodnutím, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Členské státy jsou tímto zmocněny, aby v zájmu Unie v případě částí spadajících do výhradní pravomoci Unie ratifikovaly protokol z roku 2010 nebo k němu případně přistoupily, s výjimkou aspektů souvisejících s justiční spoluprací v občanských věcech, a to za podmínek stanovených v tohoto rozhodnutí.
Článek 2
1. Členské státy by měly vyvinout úsilí, aby učinily kroky potřebné k tomu, aby uložily ratifikační listinu protokolu z roku 2010 nebo listinu o přistoupení k tomuto protokolu v přiměřené lhůtě a pokud možno do 6. května 2021.
2. Členské státy vhodným způsobem informují sebe navzájem, jakož i Radu a Komisi o zprovoznění systému podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku podle úmluvy HNS z roku 2010.
3. Členské státy budou usilovat o výměnu osvědčených postupů, zejména pokud jde o systém podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku podle úmluvy HNS z roku 2010, podle protokolu z roku 2010.
Článek 3
Členské státy při ratifikaci protokolu z roku 2010 nebo při přistoupení k němu informují písemně generálního tajemníka Mezinárodní námořní organizace o tom, že se tato ratifikace nebo přistoupení uskutečnily v souladu s tímto rozhodnutím a rozhodnutím Rady (EU) 2017/770 (4).
Článek 4
Toto rozhodnutí vstupuje v platnost prvním dnem po vyhlášení v Úředním věstníku Evropské unie.
Článek 5
Toto rozhodnutí je určeno členským státům v souladu se Smlouvami.
V Lucemburku dne 25. dubna 2017.
Za Radu
předseda
I. BORG
(1) Souhlas ze dne 5. dubna 2017 (dosud nezveřejněný v Úředním věstníku).
(2) Rozhodnutí Rady 2002/971/ES ze dne 18. listopadu 2002, kterým se členské státy zmocňují, aby v zájmu Společenství ratifikovaly Mezinárodní úmluvu o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři z roku 1996 nebo aby k této úmluvě přistoupily (Úmluva HNS) (Úř. věst. L 337, 13.12.2002, s. 55).
(3) Směrnice Evropského parlamentu a Rady 2004/35/ES ze dne 21. dubna 2004 o odpovědnosti za životní prostředí v souvislosti s prevencí a nápravou škod na životním prostředí (Úř. věst. L 143, 30.4.2004, s. 56).
(4) Rozhodnutí Rady (EU) 2017/770 ze dne 25. dubna 2017 o ratifikaci členskými státy a jejich přistoupení v zájmu Evropské unie k protokolu z roku 2010 k Mezinárodní úmluvě o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři, pokud jde o aspekty týkající se justiční spolupráce v občanských věcech (viz strana 18 v tomto čísle Úředního věstníku).
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/18 |
ROZHODNUTÍ RADY (EU) 2017/770
ze dne 25. dubna 2017
o ratifikaci členskými státy a jejich přistoupení v zájmu Evropské unie k Protokolu z roku 2010 k Mezinárodní úmluvě o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři, pokud jde o aspekty týkající se justiční spolupráce v občanských věcech
RADA EVROPSKÉ UNIE,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 81 ve spojení s čl. 218 odst. 6 písm. a) bodem v) této smlouvy,
s ohledem na návrh Evropské komise,
s ohledem na souhlas Evropského parlamentu (1),
vzhledem k těmto důvodům:
|
(1) |
Mezinárodní úmluva o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři z roku 1996 (dále jen „úmluva HNS z roku 1996“) má za cíl zajistit odpovídající, rychlé a účinné poskytnutí náhrady osobám, které utrpí škodu způsobenou únikem nebezpečných a škodlivých látek při přepravě po moři. Úmluva HNS z roku 1996 zaplnila podstatnou mezeru v mezinárodní úpravě odpovědnosti v oblasti námořní dopravy. |
|
(2) |
V roce 2002 přijala Rada rozhodnutí 2002/971/ES (2). V souladu s uvedeným rozhodnutím měly členské státy učinit kroky potřebné k ratifikaci úmluvy HNS z roku 1996 nebo k přistoupení k této úmluvě v přiměřené lhůtě a pokud možno do 30. června 2006. Následně tuto úmluvu ratifikovaly čtyři členské státy. Úmluva HNS z roku 1996 nevstoupila v platnost. |
|
(3) |
Úmluva HNS z roku 1996 byla pozměněna Protokolem z roku 2010 k úmluvě HNS z roku 1996 („protokol z roku 2010“). Podle článku 2 a čl. 18 odst. 1 protokolu z roku 2010 jsou úmluva HNS z roku 1996 a protokol z roku 2010 stranami protokolu z roku 2010 chápány, vykládány a uplatňovány společně jako jediná listina. |
|
(4) |
Konsolidované znění úmluvy HNS z roku 1996 a protokolu z roku 2010 (dále jen „úmluva HNS z roku 2010“) vypracoval sekretariát Mezinárodní námořní organizace (dále jen „IMO“) a schválil ho její právní výbor na svém 98. zasedání. Úmluva HNS z roku 2010 není listinou určenou k podpisu nebo ratifikaci. Tato úmluva nabude účinku, jakmile vstoupí v členských státech v platnost protokol z roku 2010. |
|
(5) |
Jestliže stát vyjádří souhlas být vázán protokolem z roku 2010, ruší se tím v souladu s čl. 20 odst. 8 tohoto protokolu všechna předchozí vyjádření souhlasu tohoto státu být vázán úmluvou HNS z roku 1996. Státy, které jsou smluvními stranami úmluvy HNS z roku 1996, jimi tedy přestanou být v okamžiku, kdy vyjádří souhlas, aby byly vázány protokolem z roku 2010 v souladu s článkem 20 tohoto protokolu, zejména s odstavci 2, 3 a 4 tohoto článku. |
|
(6) |
Stejně jako její předchůdkyně je i úmluva HNS z roku 2010 zvláště důležitá s ohledem na zájmy Unie a jejích členských států, protože poskytuje větší ochranu obětem škod způsobených přepravou nebezpečných a škodlivých látek po moři, a to i v oblasti škod na životním prostředí, v souladu s Úmluvou Organizace spojených národů o mořském právu z roku 1982. |
|
(7) |
Pro to, aby se státy staly smluvními stranami protokolu z roku 2010, a tím i úmluvy HNS z roku 2010, musí předložit generálnímu tajemníkovi IMO zároveň se schvalovací listinou příslušné údaje o celkovém množství nákladu podléhajícího příspěvku podle úmluvy HNS z roku 2010, který byl přijat během předcházejícího kalendářního roku, a to v souladu s čl. 20 odst. 4 této úmluvy. Dříve, než státy vyjádří souhlas, aby byly vázány protokolem z roku 2010, mají povinnost za tímto účelem vytvořit systém podávání zpráv o nákladu podléhajícím příspěvku podle úmluvy HNS. |
|
(8) |
Články 38, 39 a 40 úmluvy HNS z roku 2010 ovlivňují sekundární právní předpisy Unie o soudní příslušnosti a uznávání a výkonu soudních rozhodnutí v občanských a obchodních věcech, stanovené v nařízení Evropského parlamentu a Rady (EU) č. 1215/2012 (3). |
|
(9) |
Unie má proto výlučnou pravomoc ve vztahu k článkům 38, 39 a 40 úmluvy HNS z roku 2010, protože tato úmluva se dotýká pravidel stanovených v nařízení (EU) č. 1215/2012. |
|
(10) |
Úsilí členských států o vytvoření systémů podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku podle úmluvy HNS, by mohlo být podpořeno výměnou osvědčených postupů mezi členskými státy, pokud jde o zřizování těchto systémů. |
|
(11) |
V případě neexistence doložky o organizacích regionální hospodářské integrace, jak tomu bylo v případě úmluvy HNS z roku 1996, mohou být smluvními stranami protokolu z roku 2010 pouze svrchované státy. Unie proto nemůže ratifikovat protokol z roku 2010 ani k němu přistoupit, a tudíž nemůže přistoupit ani k úmluvě HNS z roku 2010. |
|
(12) |
Ratifikace protokolu z roku 2010 všemi členskými státy v daném časovém rámci by měla zajistit všem dotčeným subjektům při uplatňování úmluvy HNS z roku 2010 rovné podmínky v rámci Unie. |
|
(13) |
S ohledem na mezinárodní povahu režimu HNS by mělo být při uplatňování úmluvy HNS z roku 2010 usilováno o rovné podmínky na celosvětové úrovni pro všechny dotčené subjekty. Je proto potřeba zajistit celosvětovou působnost protokolu z roku 2010. |
|
(14) |
Členské státy by proto měly být zmocněny k tomu, aby ratifikovaly protokol z roku 2010, pokud jde o aspekty související s justiční spoluprací v občanských věcech, spadající do výlučné pravomoci Unie, nebo aby k tomuto protokolu přistoupily. Ustanovení úmluvy HNS z roku 2010 spadající do oblasti pravomoci svěřené Unii, s výjimkou ustanovení týkajících se justiční spolupráce v občanských věcech, budou předmětem rozhodnutí, jež bude přijato souběžně s tímto rozhodnutím. |
|
(15) |
Členské státy by měly při ratifikaci protokolu z roku 2010 nebo při přistoupení k tomuto protokolu učinit prohlášení o uznávání a výkonu soudních rozhodnutí spadajících do oblasti působnosti úmluvy HNS z roku 2010. |
|
(16) |
Spojené království a Irsko jsou vázány nařízením (EU) č. 1215/2012, a proto se účastní přijímání a používání tohoto rozhodnutí. |
|
(17) |
V souladu s články 1 a 2 Protokolu č. 22 o postavení Dánska připojeného ke Smlouvě o Evropské unii a Smlouvě o fungování Evropské unie se Dánsko neúčastní přijímání tohoto rozhodnutí a toto rozhodnutí pro ně není závazné ani použitelné, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Členské státy jsou tímto zmocněny, aby v zájmu Unie ratifikovaly protokol z roku 2010 nebo k němu případně přistoupily, pokud jde o aspekty týkající se justiční spolupráce v občanských věcech a spadající do výlučné pravomoci Unie, a to za podmínek stanovených v tomto rozhodnutí.
Článek 2
1. Členské státy by měly vyvinout úsilí, aby učinily kroky potřebné k tomu, aby uložily ratifikační listinu protokolu z roku 2010 nebo listinu o přistoupení k tomuto protokolu v přiměřené lhůtě a pokud možno do 6. května 2021.
2. Členské státy vhodným způsobem informují sebe navzájem, jakož i Radu a Komisi o zprovoznění systému podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku podle úmluvy HNS z roku 2010.
3. Členské státy budou usilovat o výměnu osvědčených postupů, zejména pokud jde o systém podávání zpráv o nákladu nebezpečných a škodlivých látek, který podléhá příspěvku podle úmluvy HNS z roku 2010, podle protokolu z roku 2010.
Článek 3
Členské státy při ratifikaci protokolu z roku 2010 nebo při přistoupení k němu rovněž uloží prohlášení uvedené v příloze tohoto rozhodnutí.
Článek 4
Toto rozhodnutí vstupuje v platnost prvním dnem po vyhlášení v Úředním věstníku Evropské unie.
Článek 5
Toto rozhodnutí je určeno členským státům v souladu se Smlouvami.
V Lucemburku dne 25. dubna 2017.
Za Radu
předseda
I. BORG
(1) Souhlas ze dne 5. 4. 2017.
(2) Rozhodnutí Rady 2002/971/ES ze dne 18. listopadu 2002, kterým se členské státy zmocňují, aby v zájmu Společenství ratifikovaly Mezinárodní úmluvu o odpovědnosti a náhradě za škodu v souvislosti s přepravou nebezpečných a škodlivých látek po moři z roku 1996 nebo aby k této úmluvě přistoupily (Úmluva HNS) (Úř. věst. L 337, 13.12.2002, s. 55).
(3) Nařízení Evropského parlamentu a Rady (EU) č. 1215/2012 ze dne 12. prosince 2012 o příslušnosti a uznávání a výkonu rozhodnutí v občanských a obchodních věcech (Úř. věst. L 351, 20.12.2012, s. 1).
PŘÍLOHA
Prohlášení, které mají členské státy při ratifikaci nebo přistoupení k protokolu z roku 2010 uložit v souladu s článkem 3:
„Soudní rozhodnutí ve věcech, na něž se vztahuje tato úmluva ve znění protokolu z roku 2010, vydaná soudem v… (1), jsou uznávána a vykonávána v… (2) podle příslušných pravidel Evropské unie týkajících se daného předmětu (3).
Pokud soudní rozhodnutí ve věcech, na něž se vztahuje tato úmluva ve znění protokolu z roku 2010, vydá soud Dánského království, jsou uznávána a vykonávána v … (4) v souladu s Dohodou mezi Evropským společenstvím a Dánským královstvím z roku 2005 o příslušnosti a uznávání a výkonu soudních rozhodnutí v občanských a obchodních věcech (5).
Pokud soudní rozhodnutí ve věcech, na něž se vztahuje tato úmluva ve znění protokolu z roku 2010, vydá soud třetího státu vázaného Luganskou úmluvou o příslušnosti a uznávání a výkonu soudních rozhodnutí v občanských a obchodních věcech ze dne 30. října 2007 (6), jsou uznávána a vykonávána v… (7) v souladu s uvedenou úmluvou.
NAŘÍZENÍ
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/22 |
NAŘÍZENÍ KOMISE (EU) 2017/771
ze dne 3. května 2017,
kterým se mění nařízení (ES) č. 152/2009, pokud jde o metody pro stanovení obsahu dioxinů a polychlorovaných bifenylů
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 882/2004 ze dne 29. dubna 2004 o úředních kontrolách za účelem ověření dodržování právních předpisů týkajících se krmiv a potravin a pravidel o zdraví zvířat a dobrých životních podmínkách zvířat (1), a zejména na čl. 11 odst. 4 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Nařízení Komise (ES) č. 152/2009 (2) obsahuje metody pro stanovení obsahu polychlorovaných dibenzo-p-dioxinů (PCDD), polychlorovaných dibenzofuranů (PCDF), polychlorovaných bifenylů (PCB) s dioxinovým efektem a polychlorovaných bifenylů (PCB) bez dioxinového efektu v krmivech. |
|
(2) |
Referenční laboratoř EU pro dioxiny a PCB v potravinách a krmivech poskytla důkazy o tom, že analytické výsledky pro dioxiny a PCB nejsou v některých případech spolehlivé, pokud laboratoře, které provádějí analýzy vzorků odebraných provozovateli krmivářských podniků v souladu s nařízením Evropského parlamentu a Rady (ES) č. 183/2005 (3), nepoužívají pracovní kritéria stanovená v příloze V části B nařízení (ES) č. 152/2009. Je proto vhodné stanovit, aby se používání pracovních kritérií stalo závazným pro analýzu těchto vzorků. |
|
(3) |
Vzhledem k tomu, že se přístup používání rozhodovací meze pro zajištění toho, aby analytický výsledek překročil maximální úroveň s určitou pravděpodobností, jak je stanoveno v rozhodnutí Komise 2002/657/ES (4), pro analýzu dioxinů, furanů a PCB v krmivech již nepoužívá, je vhodné tento přístup zrušit a zachovat pouze přístup rozšířené nejistoty při použití faktoru pokrytí 2, který odpovídá hladině spolehlivosti asi 95 %. |
|
(4) |
Byly vypracovány pokyny k měření nejistoty a odhadování meze detekce (LOD) a meze kvantifikace (LOQ). Je vhodné na tyto pokyny odkazovat. |
|
(5) |
V souladu s požadavky na podávání zpráv o bioanalytických screeningových metodách stanovených v příloze V části B nařízení (ES) č. 152/2009 je vhodné stanovit rovněž fyzikálně-chemické metody používané pro screening specifických požadavků na podávání zpráv v kapitole II uvedené části. |
|
(6) |
Vzhledem k tomu, že se analýzy dioxinů, PCB s dioxinovým efektem a PCB bez dioxinového efektu ve většině případů provádějí společně, je vhodné sladit pracovní kritéria pro PCB bez dioxinového efektu uvedená v příloze V části B kapitole III bodě 3.3 nařízení (ES) č. 152/2009 s pracovními kritérii pro dioxiny a PCB s dioxinovým efektem. Jedná se o zjednodušení bez podstatných změn v praxi, jelikož je v případě PCB bez dioxinového efektu relativní intenzita identifikačních iontů v porovnání s cílovými ionty > 50 %. |
|
(7) |
Na základě získaných zkušeností je třeba upravit některé technické specifikace, jako jsou výtěžnosti izotopicky značených standardů stanovené v příloze V části B kapitole III bodech 7.3 a 7.5 nařízení (ES) č. 152/2009. |
|
(8) |
Kromě toho se navrhuje několik dalších drobných změn stávajících ustanovení s cílem zvýšit jednotnost použité terminologie, kvůli kterým je třeba celou část B přílohy V nařízení (ES) č. 152/2009 nahradit, aby se zachovala srozumitelnost textu. |
|
(9) |
Nařízení (ES) č. 152/2009 by proto mělo být odpovídajícím způsobem změněno. |
|
(10) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro potravinový řetězec a zdraví zvířat, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Příloha V část B nařízení (ES) č. 152/2009 se mění v souladu s přílohou tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 3. května 2017.
Za Komisi
předseda
Jean-Claude JUNCKER
(1) Úř. věst. L 165, 30.4.2004, s. 1.
(2) Nařízení Komise (ES) č. 152/2009 ze dne 27. ledna 2009, kterým se stanoví metody odběru vzorků a laboratorního zkoušení pro úřední kontrolu krmiv (Úř. věst. L 54, 26.2.2009, s. 1).
(3) Nařízení Evropského parlamentu a Rady (ES) č. 183/2005 ze dne 12. ledna 2005, kterým se stanoví požadavky na hygienu krmiv (Úř. věst. L 35, 8.2.2005, s. 1).
(4) Rozhodnutí Komise 2002/657/ES ze dne 14. srpna 2002, kterým se provádí směrnice Rady 96/23/ES, pokud jde o provádění analytických metod a interpretaci výsledků (Úř. věst. L 221, 17.8.2002, s. 8).
PŘÍLOHA
V příloze V nařízení (ES) č. 152/2009 se část B „STANOVENÍ OBSAHU DIOXINŮ (PCDD/PCDF) A PCB“ nahrazuje tímto:
„B. STANOVENÍ OBSAHU DIOXINŮ (PCDD/PCDF) A PCB
KAPITOLA I
Metody odběru vzorků a interpretace výsledků analýz
1. Oblast působnosti a definice
Vzorky určené pro úřední kontrolu obsahu polychlorovaných dibenzo-p-dioxinů (PCDD), polychlorovaných dibenzofuranů (PCDF), polychlorovaných bifenylů (PCB) s dioxinovým efektem (1) a PCB bez dioxinového efektu v krmivech se odebírají v souladu s ustanoveními přílohy I. Musí být použity kvantitativní požadavky týkající se kontroly látek nebo produktů obsažených rovnoměrně v krmivech, jak je stanoveno v bodě 5.1 přílohy I. Takto získané souhrnné vzorky se považují za reprezentativní pro šarže nebo části šarže. Dodržení maximálních limitů stanovených ve směrnici 2002/32/ES se posuzuje na základě obsahů zjištěných v laboratorních vzorcích.
Pro účely této části B se použijí definice stanovené v příloze I rozhodnutí Komise 2002/657/ES (2).
Kromě zmíněných definic se pro účely této části B použijí tyto definice:
|
|
„Screeningovými metodami“ se rozumí metody používané k identifikaci vzorků s obsahem PCDD/PCDF a PCB s dioxinovým efektem převyšujícím maximální limity nebo akční prahy. Tyto metody musí umožňovat nákladově efektivní analýzu velkého množství vzorků, čímž se zvyšuje možnost zjistit nové případy vysoké expozice a ohrožení zdraví spotřebitelů. Screeningové metody musí být založeny na bioanalytických metodách nebo metodách GC-MS. Výsledky u vzorků, které překročily mezní hodnotu pro kontrolu dodržení maximálních limitů, musí být ověřeny úplnou opětovnou analýzou z původního vzorku pomocí konfirmační metody. |
|
|
„Konfirmačními metodami“ se rozumí metody, které poskytují úplné nebo doplňující informace pro jednoznačnou identifikaci a kvantifikaci PCDD/PCDF a PCB s dioxinovým efektem u maximálního limitu nebo, v případě potřeby, u akčního prahu. Tyto metody využívají plynovou chromatografii/hmotnostní spektrometrii s vysokým rozlišením (GC-HRMS) nebo plynovou chromatografii/tandemovou hmotnostní spektrometrii (GC-MS/MS). |
2. Dodržení maximálního limitu v šarži nebo části šarže
2.1. Pokud jde o PCB bez dioxinového efektu
Šarže nebo část šarže vyhovuje maximálnímu limitu, pokud výsledek analýzy pro sumu PCB 28, PCB 52, PCB 101, PCB 138, PCB 153 a PCB 180 (dále jen „PCB bez dioxinového efektu“) nepřekračuje maximální limit stanovený ve směrnici 2002/32/ES, s přihlédnutím k rozšířené nejistotě měření (3). Šarže nebo část šarže nevyhovuje maximálnímu limitu stanovenému ve směrnici 2002/32/ES, pokud střední hodnota dvou horních odhadů (4) výsledků analýzy získaná opakovanou analýzou (5) při zohlednění rozšířené nejistoty měření takřka nepochybně překračuje maximální limit, tj. k posouzení shody se použije zkoušená koncentrace poté, co byla odečtena rozšířená nejistota měření.
Rozšířená nejistota měření se vypočítá za použití faktoru pokrytí 2, který odpovídá míře spolehlivosti přibližně 95 %. Šarže nebo část šarže nevyhovuje, pokud je střední hodnota naměřených hodnot minus rozšířená nejistota měření střední hodnoty vyšší než maximální limit.
Pravidla zmíněná ve výše uvedených odstavcích tohoto bodu se použijí na výsledky analýzy získané u vzorku pro úřední kontrolu. V případě analýzy za účelem obhajoby nebo rozhodčího řízení se použijí vnitrostátní předpisy.
2.2. Pokud jde o PCDD/PCDF a PCB s dioxinovým efektem
Šarže nebo část šarže je v souladu s maximálním limitem, pokud výsledek jedné zkoušky
|
— |
provedené screeningovou metodou s mírou falešně vyhovujících výsledků nižší než 5 % naznačuje, že obsah nepřesahuje příslušný maximální limit pro PCDD/PCDF a pro sumu PCDD/PCDF a PCB s dioxinovým efektem stanovený ve směrnici 2002/32/ES, |
|
— |
provedené konfirmační metodou nepřekročí příslušný maximální limit pro PCDD/PCDF a pro sumu PCDD/PCDF a PCB s dioxinovým efektem stanovený ve směrnici 2002/32/ES, při zohlednění rozšířené nejistoty měření. |
U screeningových zkoušek se pro rozhodnutí o souladu vzorku s příslušnými maximálními limity stanovenými buď pro PCDD/PCDF, nebo pro sumu PCDD/PCDF a PCB s dioxinovým efektem stanoví mezní hodnota.
Šarže nebo část šarže nevyhovuje maximálnímu limitu stanovenému směrnicí 2002/32/ES, pokud střední hodnota dvou horních odhadů (6) výsledků zkoušky získaná opakovanou analýzou (7) s použitím konfirmační metody při zohlednění rozšířené nejistoty měření takřka nepochybně překračuje maximální limit, tj. k posouzení shody se použije zkoušená koncentrace poté, co byla odečtena rozšířená nejistota měření.
Rozšířená nejistota měření se vypočítá za použití faktoru pokrytí 2, který odpovídá míře spolehlivosti přibližně 95 %. Šarže nebo část šarže nevyhovuje, pokud je střední hodnota naměřených hodnot minus rozšířená nejistota měření střední hodnoty vyšší než maximální limit.
Pro sumu PCDD/PCDF a PCB s dioxinovým efektem se použije součet odhadované rozšířené nejistoty měření samostatných výsledků analýz u PCDD/PCDF a PCB s dioxinovým efektem.
Pravidla zmíněná ve výše uvedených odstavcích tohoto bodu se použijí na výsledky analýz získané u vzorku pro úřední kontrolu. V případě analýzy za účelem obhajoby nebo rozhodčího řízení se použijí vnitrostátní předpisy.
3. Výsledky překračující akční prahy stanovené v příloze II směrnice 2002/32/ES
Akční prahy slouží jako nástroj pro výběr vzorků v případech, kdy je nezbytné zjistit zdroj kontaminace a přijmout opatření pro jeho omezení nebo odstranění. Screeningové metody stanoví vhodné mezní hodnoty pro výběr těchto vzorků. V případě, kdy je zjištění zdroje a omezení nebo odstranění kontaminace velmi náročné, je účelné potvrdit překročení akčního prahu opakovanou analýzou s použitím konfirmační metody s přihlédnutím k rozšířené nejistotě měření (8).
KAPITOLA II
Příprava vzorků a požadavky na metody zkoušení použité při úřední kontrole obsahu dioxinů (PCDD/PCDF) a PCB s dioxinovým efektem v krmivech
1. Oblast působnosti
Požadavky stanovené v této kapitole se použijí tam, kde jsou zkoušena krmiva pro úřední kontrolu obsahu PCDD/PCDF substituovaných v polohách 2,3,7,8 a PCB s dioxinovým efektem a pro přípravu vzorků a analytické požadavky k jiným regulačním účelům, včetně kontrol prováděných provozovatelem krmivářského podniku k zajištění dodržování ustanovení nařízení Evropského parlamentu a Rady (ES) č. 183/2005 (9).
Sledování přítomnosti PCDD/PCDF a PCB s dioxinovým efektem v krmivech může být provedeno dvěma různými druhy analytických metod:
|
a) |
Screeningové metody Cílem screeningových metod je identifikovat vzorky s obsahem PCDD/PCDF a PCB s dioxinovým efektem převyšujícím maximální limity nebo akční prahy. Screeningové metody zajistí nákladově efektivní analýzu velkého množství vzorků, čímž se zvyšuje možnost zjistit nové případy vysoké expozice a ohrožení zdraví spotřebitelů. Cílem jejich použití je zabránit falešně vyhovujícím výsledkům. Tyto metody mohou zahrnovat bioanalytické metody a metody GC-MS. Screeningové metody porovnávají analytický výsledek s mezní hodnotou, a umožňují tak jednoznačné rozhodnutí (ano/ne) o případném překročení maximálního limitu nebo akčního prahu. Koncentraci PCDD/PCDF a sumu PCDD/PCDF a PCB s dioxinovým efektem ve vzorcích, u nichž panuje podezření, že jsou nevyhovující, pokud jde o maximální limit, je třeba stanovit nebo potvrdit konfirmační metodou. Kromě toho mohou screeningové metody udávat orientační obsah PCDD/PCDF a PCB s dioxinovým efektem přítomných ve vzorku. V případě použití bioanalytických screeningových metod se výsledek vyjádří v bioanalytických ekvivalentech (BEQ), zatímco v případě použití fyzikálně-chemických metod GC-MS se vyjádří v toxických ekvivalentech (TEQ). Numericky vyjádřené výsledky screeningových metod jsou vhodné k prokázání souladu nebo podezření na nedodržení nebo překročení akčních prahů a udávají rozmezí úrovní v případě následné zkoušky pomocí konfirmačních metod. Nejsou vhodné pro účely, jako je hodnocení úrovní pozadí, odhad příjmu, sledování vývoje úrovní v čase nebo přehodnocení akčních prahů a maximálních limitů. |
|
b) |
Konfirmační metody Konfirmační metody umožňují jednoznačnou identifikaci a kvantifikaci PCDD/PCDF a PCB s dioxinovým efektem přítomných ve vzorku a poskytují úplné informace o úrovni kongeneru. Uvedené metody proto umožňují kontrolu maximálních limitů a akčních prahů, včetně konfirmace výsledků získaných pomocí screeningových metod. Kromě toho mohou být výsledky použity i pro jiné účely, jako je stanovení nízkých úrovní pozadí při sledování krmiv, sledování vývoje v čase, posouzení expozice a vytvoření databáze za účelem případného přehodnocení akčních prahů a maximálních limitů. Rovněž jsou významné pro stanovení zastoupení kongenerů za účelem zjištění zdroje možné kontaminace. Tyto metody využívají GC-HRMS. Pro konfirmaci souladu nebo nesouladu s maximálními limity lze rovněž použít GC-MS/MS. |
2. Souvislosti
Pro výpočet koncentrací TEQ se koncentrace jednotlivých látek v daném vzorku vynásobí jejich příslušnými faktory toxické ekvivalence (TEF) (viz poznámka 1 v kapitole I), sečtou se a výsledná suma je celkovou koncentrací sloučenin s dioxinovým efektem vyjádřenou v TEQ.
Pro účely této části B se schválenou specifickou mezí kvantifikace jednotlivého kongeneru rozumí nejnižší obsah analytu, který lze měřit s rozumnou mírou statistické jistoty, splňující kritéria pro identifikaci, jež jsou popsána v mezinárodně uznávaných normách, například v normě EN 16215:2012 (Krmiva – stanovení dioxinů a PCB s dioxinovým efektem pomocí plynové chromatografie/hmotnostní spektrometrie s vysokým rozlišením (GC-HRMS) a indikátorových PCB pomocí GC-HRMS) a/nebo v metodách EPA 1613 a 1668 ve znění pozdějších revizí.
Mez kvantifikace jednotlivého kongeneru může být identifikována jako:
|
a) |
koncentrace analytu v extraktu vzorku, jež dává instrumentální odezvu na dvou různých iontech, které mají být monitorovány při poměru signál–šum 3:1 pro méně intenzivní signál, nebo |
|
b) |
pokud výpočet signál-šum z technických důvodů neposkytuje spolehlivé výsledky, jako nejnižší bod koncentrace na kalibrační křivce, který vykazuje přijatelnou (≤ 30 %) a stálou (měřeno alespoň na začátku a na konci analytické série vzorků) odchylku od průměrného relativního odezvového faktoru vypočteného pro všechny body na kalibrační křivce v každé sérii vzorků. Mez kvantifikace (LOQ) se vypočte z nejnižšího bodu koncentrace, přičemž se zohlední výtěžnost vnitřních standardů a množství vzorku. |
Bioanalytické screeningové metody neposkytnou výsledky na úrovni kongeneru, ale pouze orientační (10) hodnoty úrovně TEQ, vyjádřené v BEQ, aby byla zohledněna skutečnost, že ne všechny sloučeniny přítomné v extraktu vzorku, který při zkoušce dává odezvu, nutně splňují všechny požadavky principu TEQ.
Screeningové a konfirmační metody mohou být použity pouze pro kontrolu určité matrice, pokud jsou tyto metody dostatečně citlivé, aby spolehlivě zjistily hladiny na úrovni akčního prahu nebo maximálního limitu.
3. Požadavky na zabezpečení kvality
3.1. Na každém stupni odběru vzorků a zkoušky se přijmou opatření k zamezení křížové kontaminace.
3.2. Vzorky musí být uchovávány a přepravovány ve skleněných, hliníkových, polypropylenových nebo polyethylenových nádobách vhodných pro skladování bez jakéhokoli vlivu na úrovně PCDD/PCDF a PCB s dioxinovým efektem ve vzorcích. Z nádoby na vzorky se odstraní stopy papírového prachu.
3.3. Vzorky se uchovávají a přepravují tak, aby byla zachována integrita vzorku krmiv.
3.4. Pokud je to relevantní, jednotlivé laboratorní vzorky se jemně rozemelou a důkladně promísí postupem, u něhož je prokázáno, že se jím dosáhne úplné homogenizace (např. rozemletím a proséváním přes síto s průměrem oček 1 mm). Je-li vlhkost vzorků příliš vysoká, musí se vzorky před rozemletím sušit.
3.5. Je vždy důležité zkontrolovat činidla, pomůcky ze skla a vybavení z hlediska možného vlivu na výsledky založené na TEQ nebo BEQ.
3.6. Provede se slepý pokus, při němž se provede celý analytický postup bez vzorku.
3.7. U bioanalytických metod se u veškerých při zkoušce použitých pomůcek ze skla a rozpouštědel potvrdí, že jsou prosty sloučenin, které mohou bránit zjištění cílových sloučenin v pracovním rozsahu. Skleněné pomůcky se vypláchnou rozpouštědly nebo zahřejí na teploty vhodné pro odstranění stop PCDD/PCDF, sloučenin s dioxinovým efektem a interferujících sloučenin z jejich povrchu.
3.8. Množství vzorku použité pro extrakci musí být dostatečné, aby byly splněny požadavky s ohledem na dostatečně nízký pracovní rozsah včetně koncentrací maximálních limitů nebo akčního prahu.
3.9. Specifické postupy přípravy vzorku použité pro zkoumané produkty musí splňovat mezinárodně uznávané metodiky.
4. Požadavky na laboratoře
4.1. V souladu s nařízením (ES) č. 882/2004 musí být laboratoře akreditovány uznaným subjektem působícím v souladu s pokyny ISO Guide 58, aby bylo zaručeno, že uplatňují postupy zajištění analytické kvality. Laboratoře musí být akreditovány podle normy EN ISO/IEC 17025. V příslušném případě je třeba se řídit zásadami popsanými v technických pokynech pro odhad nejistoty měření a meze kvantifikace pro analýzu PCDD/PCDF a PCB (11).
4.2. Odbornost laboratoře prokazuje soustavná úspěšná účast v mezilaboratorních studiích týkajících se stanovení PCDD/PCDF a PCB s dioxinovým efektem v příslušných matricích krmiv a koncentračních rozpětích.
4.3. Laboratoře, které pro rutinní kontrolu vzorků používají screeningové metody, musí úzce spolupracovat s laboratořemi používajícími konfirmační metodu, za účelem jak kontroly kvality, tak konfirmace výsledku analýzy podezřelých vzorků.
5. Základní požadavky, které musí splňovat analytický postup u dioxinů (PCDD/PCDF) a PCB s dioxinovým efektem
5.1. Nízký pracovní rozsah a meze kvantifikace
V případě PCDD/PCDF musí být zjistitelná množství z důvodu extrémní toxicity některých těchto sloučenin na horní úrovni femtogramů (10– 15 g). V případě většiny kongenerů PCB je dostatečná již mez kvantifikace na úrovni nanogramů (10– 9 g). Pro měření toxičtějších kongenerů PCB s dioxinovým efektem (zejména non-ortho substituovaných kongenerů) musí nejspodnější část pracovního rozsahu dosahovat nízkých úrovní pikogramů (10– 12 g). U všech ostatních kongenerů PCB je dostatečná již mez kvantifikace na úrovni nanogramů (10– 9 g).
5.2. Vysoká selektivita (specifičnost)
5.2.1. Je třeba rozlišit PCDD/PCDF a PCB s dioxinovým efektem a řadu jiných sloučenin, které se extrahují společně s těmito látkami, mohou rušit při jejich stanovování a jsou přítomny v koncentracích až o několik řádů vyšších než koncentrace sledovaných analytů. Pro metody GC-MS je třeba rozlišení mezi různými kongenery, např. mezi toxickými kongenery (např. sedmnácti PCDD/PCDF substituovanými v polohách 2,3,7,8 a dvanácti PCB s dioxinovým efektem) a ostatními kongenery.
5.2.2. Bioanalytické metody musí být schopny detekovat cílové sloučeniny jako sumu PCDD/PCDF a/nebo PCB s dioxinovým efektem. Přečištění vzorku se zaměří na odstranění sloučenin způsobujících falešně nevyhovující výsledky nebo sloučenin, které mohou způsobovat snížení odezvy vedoucí k falešně vyhovujícím výsledkům.
5.3. Vysoká správnost (pravdivost a přesnost, zjevná výtěžnost biologické zkoušky)
5.3.1. U metod GC-MS musí stanovení poskytovat správný odhad skutečné koncentrace ve vzorku. Vysoká správnost je nezbytná k tomu, aby nedošlo k zamítnutí výsledku analýzy vzorku na základě malé spolehlivosti stanovené úrovně TEQ. Správnost je vyjádřena pravdivostí (rozdílem mezi střední naměřenou hodnotou analytu v certifikovaném materiálu a jeho certifikovanou hodnotou, vyjádřeným v procentech této hodnoty) a přesností (RSDR je relativní směrodatná odchylka vypočtená z výsledků získaných za podmínek reprodukovatelnosti).
5.3.2. Pro bioanalytické metody se určí zjevná výtěžnost biologické zkoušky. Zjevnou výtěžností biologické zkoušky se rozumí úroveň BEQ vypočtená z kalibrační křivky TCDD nebo PCB 126 upravená o hodnoty slepého stanovení a poté vydělená hodnotou TEQ určenou konfirmační metodou. Jejím účelem je korekce činitelů, jako je ztráta PCDD/PCDF a sloučenin s dioxinovým efektem během extrakce a čištění, současně extrahované sloučeniny zesilující nebo tlumící odezvu (agonistické a antagonistické účinky), kvalita kalibrace nebo rozdíly mezi hodnotami TEF a relativní účinnosti (REP). Zjevná výtěžnost biologické zkoušky se vypočte z vhodných referenčních vzorků s reprezentativním zastoupením kongenerů kolem sledované úrovně.
5.4. Validace v rozsahu maximálního limitu a obecná opatření pro kontrolu kvality
5.4.1. Laboratoře musí prokázat spolehlivost metody v rozsahu kolem maximálního limitu, např. v polovině, jednonásobku nebo dvojnásobku maximálního limitu, a to s přijatelným variačním koeficientem pro opakovanou analýzu, a sice během validace a během rutinní analýzy.
5.4.2. Jako opatření v rámci vnitřní kontroly kvality se provádějí pravidelná slepá kontrolní stanovení, stanovení s obohacenými vzorky nebo analýzy kontrolních vzorků (nejlépe certifikovaného referenčního materiálu, je-li k dispozici). Ze slepých kontrolních stanovení, stanovení s obohacenými vzorky nebo analýz kontrolních vzorků se vyhotoví a ověří grafy kontroly kvality, aby bylo zajištěno, že analytická výkonnost je v souladu s požadavky.
5.5. Mez kvantifikace
5.5.1. Pro bioanalytické screeningové metody není stanovení meze kvantifikace (LOQ) nezbytné, příslušná metoda však musí prokázat, že umožňuje rozlišení mezi hodnotou slepého stanovení a mezní hodnotou. Při poskytování úrovně BEQ se stanoví oznamovací mez pro vzorky s odezvou nižší než tato úroveň. Musí být prokázáno, že se oznamovací mez významně (nejméně trojnásobně) liší od slepých vzorků odrážejících celý pracovní postup s odezvou nižší než pracovní rozsah. Vypočte se proto ze vzorků obsahujících cílové sloučeniny přibližně v požadované minimální úrovni, a nikoli z poměru signál–šum nebo ze slepé zkoušky.
5.5.2. Mez kvantifikace u konfirmační metody činí přibližně jednu pětinu maximálního limitu.
5.6. Analytická kritéria
Pro spolehlivé výsledky konfirmačních nebo screeningových metod musí být v rozsahu maximálního limitu splněna následující kritéria pro hodnotu TEQ nebo BEQ, ať už je určena jako celkový TEQ nebo celkový BEQ (jako suma PCDD/PCDF a PCB s dioxinovým efektem), nebo samostatně pro PCDD/PCDF a PCB s dioxinovým efektem.
|
|
Screening pomocí bioanalytických nebo fyzikálně-chemických metod |
Konfirmační metody |
|
Míra falešně vyhovujících výsledků (*1) |
< 5 % |
|
|
Pravdivost |
|
– 20 % až + 20 % |
|
Opakovatelnost (RSDr) |
< 20 % |
|
|
Mezilehlá preciznost (RSDR) |
< 25 % |
< 15 % |
5.7. Zvláštní požadavky na screeningové metody
5.7.1. Pro screening mohou být použity jak metody GC-MS, tak bioanalytické metody. Metody GC/MS musí splňovat požadavky stanovené v bodě 6. Pro buněčné bioanalytické metody jsou zvláštní požadavky stanoveny v bodě 7.
5.7.2. Laboratoře, které pro rutinní kontrolu vzorků používají screeningové metody, musí úzce spolupracovat s laboratořemi používajícími konfirmační metodu.
5.7.3. Během rutinní analýzy je nutné ověřovat výkonnost příslušné screeningové metody, a to kontrolou kvality při analýzách a průběžnou validací metody. Zavede se stálý program kontroly vyhovujících výsledků.
5.7.4. Kontrola možného potlačení buněčné odezvy a cytotoxicity:
20 % extraktů vzorků se změří při rutinním screeningu bez přidání a s přidáním 2,3,7,8-TCDD v množství odpovídajícím maximálnímu limitu nebo akčnímu prahu, aby se zjistilo, zda odezva není potlačována interferujícími látkami přítomnými v extraktu vzorku. Naměřená koncentrace u obohaceného vzorku se porovná se sumou koncentrace neobohaceného extraktu a koncentrace obohacující látky. Pokud je tato naměřená koncentrace o více než 25 % nižší než vypočtená (souhrnná) koncentrace, svědčí to o tom, že možná dochází k potlačení odezvy, a dotčený vzorek musí být podroben konfirmační analýze pomocí GC-HRMS. Výsledky musí být zaznamenány v grafech kontroly kvality.
5.7.5. Kontrola kvality u vyhovujících vzorků
Přibližně 2 až 10 % vyhovujících vzorků, v závislosti na matrici vzorků a zkušenostech laboratoře, musí být potvrzeno pomocí GC/HRMS.
5.7.6. Určení míry falešně vyhovujících vzorků na základě údajů z kontroly kvality:
Určí se míra falešně vyhovujících výsledků na základě screeningu vzorků nižších a vyšších než maximální limit nebo akční práh. Skutečný podíl falešně vyhovujících výsledků musí být nižší než 5 %. Je-li k dispozici nejméně 20 potvrzených výsledků z kontroly kvality vyhovujících vzorků na matrici/matricovou skupinu, vyvodí se z těchto výsledků závěry ohledně míry falešně vyhovujících výsledků. Do minimálního počtu 20 výsledků pro hodnocení míry falešně vyhovujících výsledků se mohou zahrnout i výsledky ze vzorků analyzovaných pomocí kruhových testů nebo při kontaminačních aférách, které pokrývají rozpětí koncentrace až např. do dvojnásobku maximálního limitu. Vzorky musí zahrnovat nejčastější zastoupení kongenerů, které představují různé zdroje.
Ačkoli se mají screeningové testy přednostně zaměřit na zjištění vzorků přesahujících akční práh, je kritériem pro stanovení míry falešně vyhovujících vzorků maximální limit, s přihlédnutím k rozšířené nejistotě měření konfirmační metody.
5.7.7. Případné nevyhovující vzorky ze screeningu musí být vždy ověřeny úplnou opakovanou analýzou původního vzorku pomocí konfirmační metody analýzy. Tyto vzorky mohou být také použity pro vyhodnocení podílu falešně nevyhovujících výsledků. U screeningových metod je mírou falešně nevyhovujících výsledků podíl výsledků, které konfirmační analýza potvrdí jako vyhovující, zatímco při předchozím screeningu byl vzorek prohlášen za potenciálně nevyhovující. Hodnocení výhodnosti použití screeningové metody musí vycházet z porovnání falešně nevyhovujících výsledků a celkového počtu kontrolovaných vzorků. Tento poměr musí být dostatečně nízký, aby bylo možné považovat používání příslušného screeningového nástroje za výhodné.
5.7.8. Bioanalytické metody musí při validačních podmínkách poskytovat platné údaje o úrovni TEQ, vypočtené a vyjádřené jako BEQ.
Pro bioanalytické metody prováděné za podmínek opakovatelnosti je vnitrolaboratorní RSDr obvykle menší než za podmínek reprodukovatelnosti RSDR.
6. Zvláštní požadavky, které musí splňovat metody GC-MS, aby vyhovovaly pro účely screeningu nebo konfirmace
6.1. Přijatelné rozdíly mezi horním a dolním odhadem výsledků WHO-TEQ
Rozdíl mezi horním odhadem a dolním odhadem nesmí překročit 20 % pro konfirmaci překročení maximálního limitu nebo, v případě potřeby, akčních prahů.
6.2. Kontrola výtěžnosti
6.2.1. Vnitřní standardy 2,3,7,8-chlor-substituovaných PCDD/PCDF značené izotopem 13C a standardy PCB s dioxinovým efektem značené izotopem13C musí být přidány na samém začátku analýzy, např. před extrakcí, aby bylo možné validovat analytický postup. Alespoň jeden kongener musí být přidán pro každou z tetra- až okta-chlorovaných homologických skupin PCDD/PCDF a alespoň jeden kongener pro každou z homologických skupin PCB s dioxinovým efektem (nebo alespoň jeden kongener pro každou skupinu vybraných iontů při použití hmotnostní spektrometrie v režimu registrace vybraných iontů použitou pro sledování PCDD/PCDF a PCB s dioxinovým efektem). V případě konfirmačních metod se použije všech 17 vnitřních standardů 2,3,7,8-substituovaných PCDD/PCDF značených izotopem 13C a všech 12 vnitřních standardů PCB s dioxinovým efektem značených izotopem 13C.
6.2.2. Relativní faktory odezvy se s pomocí vhodných kalibračních roztoků stanoví také pro kongenery, pro něž nebyly přidány sloučeniny značené izotopem 13C.
6.2.3. U krmiv rostlinného původu a krmiv živočišného původu s obsahem tuku nižším než 10 % je přidání vnitřních standardů před extrakcí povinné. U krmiv živočišného původu s obsahem tuku vyšším než 10 % lze vnitřní standardy přidat buď před extrakcí, nebo po extrakci tuku. Vhodným způsobem se validuje účinnost extrakce, a to v závislosti na fázi, ve které se přidávají vnitřní standardy.
6.2.4. Před analýzou metodou GC-MS musí být přidány 1 nebo 2 obohacené standardy (recovery standardy) pro stanovení výtěžnosti.
6.2.5. Kontrola výtěžnosti je nezbytná. U konfirmačních metod se výtěžnost jednotlivých vnitřních standardů musí pohybovat v rozmezí 60 až 120 %. Nižší nebo vyšší hodnota výtěžnosti u jednotlivých kongenerů, zejména některých hepta- a okta-chlorovaných dibenzo-p-dioxinů a dibenzofuranů, je přípustná pod podmínkou, že jejich příspěvek k hodnotě TEQ nepřesáhne 10 % celkové hodnoty TEQ (na základě sumy PCDD/PCDF a PCB s dioxinovým efektem). Hodnota výtěžnosti u screeningových metod GC-MS se musí pohybovat mezi 30 a 140 %.
6.3. Odstranění interferujících látek
|
— |
Oddělení PCDD/PCDF od interferujících chlorovaných sloučenin, jako jsou PCB bez dioxinového efektu a chlorované difenylethery, se provede vhodnými chromatografickými technikami (nejlépe na florisilové, aluminové a/nebo uhlíkové koloně). |
|
— |
Oddělení izomerů pomocí plynové chromatografie musí být < 25 % překryvu mezi píky 1,2,3,4,7,8-HxCDF a 1,2,3,6,7,8-HxCDF. |
6.4. Kalibrace pomocí standardní křivky
Rozsah kalibrační křivky musí pokrývat odpovídající rozpětí maximálních limitů nebo akčních prahů.
6.5. Zvláštní kritéria pro konfirmační metody
|
— |
Pro GC-HRMS:
|
|
— |
Pro GC-MS/MS:
|
7. Zvláštní požadavky na bioanalytické metody
Bioanalytické metody jsou metody založené na využití biologických principů, jako jsou buněčné testy, receptorové testy nebo imunologické testy. V tomto bodě 7 se stanoví obecné požadavky na bioanalytické metody.
Screeningové metody v zásadě klasifikují vzorky jako vyhovující nebo vzorky podezřelé jako nevyhovující. Za tímto účelem se vypočtená úroveň BEQ porovnává s mezní hodnotou (viz bod 7.3). Vzorky nižší než mezní hodnota se považují za vyhovující, vzorky rovnající se mezní hodnotě nebo vyšší se považují za podezřelé jako nevyhovující a je nutné provést jejich analýzu pomocí konfirmační metody. Prakticky může jako mezní hodnota sloužit úroveň BEQ odpovídající 2/3 maximálního limitu, pokud je zajištěna míra falešně vyhovujících vzorků nižší než 5 % a přijatelná míra falešně nevyhovujících vzorků. Při různém maximálním limitu pro PCDD/PCDF a pro sumu PCDD/PCDF a PCB s dioxinovým efektem vyžaduje kontrola souladu vzorků bez frakcionace vhodné mezní hodnoty pro biologickou zkoušku pro PCDD/PCDF. Pro kontrolu vzorků překračujících akční prahy je vhodnou mezní hodnotou přiměřené procento příslušného akčního prahu.
Je-li orientační úroveň vyjádřena v BEQ, musí být výsledky vzorku vyjádřeny v pracovním rozsahu a přesahovat oznamovací mez (viz body 7.1.1 a 7.1.6).
7.1. Hodnocení odezvy zkoušky
7.1.1.
|
— |
Při výpočtu koncentrace z kalibrační křivky TCDD vykáží hodnoty na horním konci křivky velký křivkový rozptyl (vysoký variační koeficient (CV)). Pracovní rozsah je oblast, kde je tento CV menší než 15 %. Nejspodnější část pracovního rozsahu (oznamovací mez) musí být stanovena tak, aby nejméně trojnásobně přesahovala hodnoty slepých vzorků odrážejících celý pracovní postup. Horní část pracovního rozsahu obvykle představuje hodnota EC70 (70 % maximální účinné koncentrace), je však nižší, pokud je CV v tomto rozpětí vyšší než 15 %. Pracovní rozsah se stanoví během validace. Mezní hodnoty (viz bod 7.3) musí být uvnitř pracovního rozsahu. |
|
— |
Standardní roztoky a extrakty vzorku se zkouší třikrát nebo alespoň duplicitně. Při duplicitních zkouškách musí standardní roztok nebo kontrolní extrakt zkoušený ve 4–6 jamkách rozložených na destičce poskytnout odezvu nebo koncentraci (možné pouze v pracovním rozsahu) vycházející z CV < 15 %. |
7.1.2.
7.1.2.1. Kalibrace pomocí standardní křivky
|
— |
Za účelem výpočtu úrovně BEQ v extraktu a následně ve vzorku lze úroveň ve vzorcích odhadnout porovnáním jejich odezvy s odezvou kalibrační křivky TCDD (nebo PCB 126 nebo standardní směsi PCDD/PCDF/PCB s dioxinovým efektem). |
|
— |
Kalibrační křivky musí obsahovat 8 až 12 koncentrací (alespoň duplicitních), s dostatečným počtem koncentrací ve spodní části křivky (pracovním rozsahu). Zvláštní pozornost musí být věnována kvalitě proložení kalibračních bodů křivkou v pracovním rozsahu. Hodnota R2 sama o sobě má pouze zanedbatelný nebo žádný význam při hodnocení kvality proložení kalibračních bodů křivkou při nelineární regresi. Lepšího proložení se dosáhne minimalizací rozdílu mezi vypočtenými a zjištěnými úrovněmi v pracovním rozsahu křivky (např. minimalizací sumy druhých mocnin reziduí). |
|
— |
Od odhadované úrovně v extraktu vzorku se následně odečte úroveň BEQ vypočtená pro slepý vzorek matrice nebo rozpouštědla (aby se zohlednily nečistoty z použitých rozpouštědel a chemikálií) a provede se korekce na zjevnou výtěžnost (vypočtenou na základě úrovně BEQ vhodných referenčních vzorků s reprezentativním zastoupením kongenerů kolem maximálního limitu nebo akčního prahu). Pro provedení korekce na výtěžnost musí být zjevná výtěžnost v požadovaném rozmezí (viz bod 7.1.4). Referenční vzorky použité pro korekci na výtěžnost musí splňovat požadavky stanovené v bodě 7.2. |
7.1.2.2. Kalibrace pomocí referenčních vzorků
Případně lze použít kalibrační křivku zhotovenou alespoň ze čtyř referenčních vzorků (viz bod 7.2.4): jednoho matričního slepého vzorku plus tří referenčních vzorků na polovině, jednonásobku a dvojnásobku maximálního limitu nebo akčního prahu, čímž odpadne nutnost odečtu hodnoty slepého stanovení a korekce na výtěžnost, pokud se vlastnosti matrice referenčních vzorků kryjí s vlastnostmi neznámých vzorků. V tomto případě lze odezvu odpovídající 2/3 maximálního limitu (viz bod 7.3) vypočítat přímo z těchto vzorků a použít ji jako mezní hodnotu. Pro kontrolu vzorků překračujících akční prahy je vhodnou mezní hodnotou přiměřené procento těchto akčních prahů.
7.1.3.
Extrakty lze rozdělit do frakcí obsahujících PCDD/PCDF a PCB s dioxinovým efektem, což umožňuje získání oddělených údajů o úrovni TEQ pro PCDD/PCDF a PCB s dioxinovým efektem (v BEQ). Pro hodnocení výsledků pro frakci obsahující PCB s dioxinovým efektem se přednostně použije kalibrační křivka standardu PCB 126.
7.1.4.
„Zjevná výtěžnost biologické zkoušky“ se vypočte z vhodných referenčních vzorků s reprezentativním zastoupením kongenerů kolem maximálního limitu nebo akčního prahu a vyjádří se jako procento úrovně BEQ v porovnání s úrovní TEQ. V závislosti na použitém typu zkoušky a použitých TEF (12) mohou rozdíly mezi faktory TEF a REP pro PCB s dioxinovým efektem způsobit nízkou zjevnou výtěžnost u PCB s dioxinovým efektem v porovnání s PCDD/PCDF. Proto při samostatném stanovení PCDD/PCDF a PCB s dioxinovým efektem musí být zjevná výtěžnost biologických zkoušek následující: u PCB s dioxinovým efektem 20 % až 60 %, u PCDD/PCDF 50 % až 130 % (rozmezí platná pro kalibrační křivku TCDD). Jelikož podíl PCB s dioxinovým efektem na sumě PCDD/PCDF a PCB s dioxinovým efektem se může u různých matric a vzorků lišit, odráží se tyto rozdíly i ve zjevné výtěžnosti biologických zkoušek pro sumu PCDD/PCDF a PCB s dioxinovým efektem, která se má pohybovat v rozmezí 30 % až 130 %. Důsledky případné podstatné revize hodnot TEF pro právní předpisy Unie týkající se PCDD/PCDF a PCB s dioxinovým efektem budou vyžadovat revizi těchto rozmezí.
7.1.5.
Při validaci je nutné zkontrolovat ztrátu sloučenin během čištění. Slepý vzorek obohacený směsí různých kongenerů se podrobí čištění (alespoň n = 3) a výtěžnost a variabilita se ověří konfirmační metodou. Výtěžnost musí být v rozmezí 60 % až 120 %, zejména u kongenerů s podílem na množství TEQ v různých směsích, který je vyšší než 10 %.
7.1.6.
Při vydávání úrovní BEQ musí být stanovena oznamovací mez z příslušných matričních vzorků zahrnujících typická zastoupení kongenerů, avšak vzhledem k nízké přesnosti v dolním rozsahu křivky nikoli z kalibrační křivky standardů. Je třeba vzít v úvahu účinky extrakce a čištění. Oznamovací mez musí být stanovena nejméně trojnásobně vyšší než hodnoty slepých vzorků odrážejících celý pracovní postup.
7.2. Použití referenčních vzorků
7.2.1. Referenční vzorky musí představovat matrice vzorku, zastoupení kongenerů a rozpětí koncentrací pro PCDD/PCDF a PCB s dioxinovým efektem kolem maximálního limitu nebo akčního prahu.
7.2.2. Každá série zkoušek musí zahrnovat slepý vzorek odrážející celý pracovní postup, či nejlépe slepý matriční vzorek, a referenční vzorek na maximálním limitu nebo akčním prahu. Tyto vzorky musí být extrahovány a zkoušeny současně a za stejných podmínek. Referenční vzorek musí vykázat jasně vyšší odezvu v porovnání s odezvou slepého vzorku, čímž je zajištěna vhodnost zkoušky. Tyto vzorky mohou být použity pro korekci o hodnoty slepého stanovení a korekci na výtěžnost.
7.2.3. Referenční vzorky vybrané pro provedení korekce na výtěžnost musí být reprezentativní pro zkušební vzorky, což znamená, že zastoupení kongenerů nesmí vést k podhodnocení úrovní.
7.2.4. Pro prokázání odpovídající výkonnosti zkoušky ve sledovaném rozsahu pro kontrolu maximálního limitu nebo akčního prahu lze kromě toho zahrnout ještě referenční vzorky o např. poloviční a dvojnásobné koncentraci, než je maximální limit nebo akční práh. Dohromady mohou být tyto vzorky použity pro výpočet úrovní BEQ ve zkušebních vzorcích (viz bod 7.1.2.2).
7.3. Stanovení mezních hodnot
Je nutné určit vztah mezi výsledky biologické zkoušky v BEQ a výsledky konfirmační metody v TEQ (např. pomocí kalibračních pokusů, které zohledňují vliv matrice, s referenčními vzorky obohacenými na nule, polovině, jednonásobku a dvojnásobku maximálního limitu s šesti opakováními na každé úrovni (n = 24)). Na základě tohoto vztahu lze odhadnout korekční faktory (odečtení hodnoty slepého stanovení a korekce na výtěžnost), je však nutno je ověřit v souladu s bodem 7.2.2.
Je nutné stanovit mezní hodnoty pro účely rozhodnutí ohledně souladu vzorku s maximálními limity nebo pro kontrolu akčních prahů, jsou-li sledovanou hodnotou, a rovněž s příslušnými maximálními limity nebo akčními prahy, stanovenými buď zvlášť pro PCDD/PCDF a PCB s dioxinovým efektem, nebo pro sumu PCDD/PCDF a PCB s dioxinovým efektem. Tyto hodnoty jsou zastoupeny nižším cílovým bodem distribuce výsledků biologické zkoušky (upravených o hodnoty slepého stanovení a korigovaných na výtěžnost) odpovídajícím rozhodovací mezi u příslušné konfirmační metody na základě 95 % spolehlivosti, z čehož vyplývá míra falešně vyhovujících výsledků < 5 %, a na základě RSDR < 25 %. Rozhodovací mezí u konfirmační metody je maximální limit při zohlednění rozšířené nejistoty měření.
Mezní hodnotu (v BEQ) lze vypočítat v souladu s jedním z postupů uvedených v bodech 7.3.1, 7.3.2 a 7.3.3 (viz graf 1).
7.3.1. S použitím nižší části 95 % predikčního intervalu ve výši rozhodovací meze konfirmační metody:
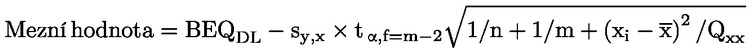
kde:
|
BEQDL |
je BEQ odpovídající rozhodovací mezi u konfirmační metody, což je maximální limit včetně rozšířené nejistoty měření |
|
sy,x |
je reziduální směrodatná odchylka |
|
tα,f = m-2 |
je kvantil Studentova t-rozdělení (α = 5 %, f = stupně volnosti, jednostranný) |
|
m |
je celkový počet kalibračních bodů (index j) |
|
n |
je počet opakování na každé úrovni |
|
xi |
je koncentrace vzorku (v TEQ) v kalibračním bodě i stanovená konfirmační metodou |
|
|
je průměr koncentrací (v TEQ) všech kalibračních vzorků |
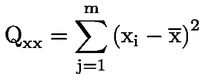 je parametr sumy čtverců, i = index pro kalibrační bod i
je parametr sumy čtverců, i = index pro kalibrační bod i
7.3.2. Z výsledků biologické zkoušky (upravených o hodnoty slepého stanovení a korigovaných na výtěžnost) získaných z vícenásobných analýz vzorků (n ≥ 6) kontaminovaných na úrovni rozhodovací meze konfirmační metody, jakožto nižší část rozdělení výsledků na odpovídající průměrné hodnotě BEQ:
Mezní hodnota = BEQDL – 1,64 × SDR
kde:
|
SDR |
je směrodatná odchylka výsledků biologické zkoušky na BEQDL, měřeno za podmínek vnitrolaboratorní reprodukovatelnosti. |
7.3.3. Výpočet jako střední hodnota výsledků bioanalýzy (v BEQ, upravených o hodnoty slepého stanovení a korigovaných na výtěžnost) z vícenásobné analýzy vzorků (n ≥ 6) kontaminovaných na 2/3 maximálního limitu nebo akčního prahu, na základě poznatku, že tato úroveň se bude pohybovat kolem mezní hodnoty určené v bodech 7.3.1 nebo 7.3.2:
Výpočet mezních hodnot vycházející z 95 % míry spolehlivosti, z níž vyplývá míra falešně vyhovujících výsledků < 5 %, a z RSDR < 25 %:
|
1. |
z nižší části 95 % predikčního intervalu na úrovni rozhodovací meze konfirmační metody; |
|
2. |
z vícenásobné analýzy vzorků (n ≥ 6) kontaminovaných na úrovni rozhodovací meze konfirmační metody jakožto nižší část distribuce údajů (v grafu je znázorňuje křivka ve tvaru zvonu) na odpovídající průměrné hodnotě BEQ. |
Graf 1

7.3.4. Omezení mezních hodnot
Mezní hodnoty vycházející z BEQ a vypočtené z RSDR dosažené při validaci s použitím omezeného počtu vzorků s různým zastoupením matrice/kongenerů mohou být vyšší než maximální limity nebo akční prahy vycházející z TEQ, vzhledem k větší přesnosti, než je přesnost, jíž lze běžně dosáhnout s neznámým spektrem zastoupení kongenerů. V takových případech se mezní hodnoty vypočtou z RSDR = 25 % nebo se dá přednost dvěma třetinám maximálního limitu nebo akčního prahu.
7.4. Kritéria výkonnosti
7.4.1. Vzhledem k tomu, že při bioanalytických metodách nelze použít žádné vnitřní standardy, provedou se zkoušky opakovatelnosti bioanalytických metod pro získání informací o směrodatné odchylce v rámci zkoušek a mezi sériemi zkoušek. Opakovatelnost musí být nižší než 20 %, vnitrolaboratorní reprodukovatelnost pak nižší než 25 %. To musí vycházet z vypočtených úrovní v BEQ po odečtení hodnot slepého stanovení a korekci na výtěžnost.
7.4.2. Jako součást postupu validace musí být prokázáno, že zkouška umožňuje rozlišit slepý vzorek a úroveň ve výši mezní hodnoty, a umožňuje tak identifikovat vzorky nad příslušnou mezní hodnotou (viz bod 7.1.2).
7.4.3. Je třeba určit cílové sloučeniny, možné interference a nejvyšší přípustný obsah ve slepém vzorku.
7.4.4. Procentní směrodatná odchylka odezvy nebo koncentrace vypočtená z odezvy (možné pouze v pracovním rozsahu) trojnásobného stanovení extraktu vzorku nesmí být vyšší než 15 %.
7.4.5. Pro hodnocení výkonnosti bioanalytické metody v konstantním časovém období se použijí nekorigované výsledky referenčního vzorku (referenčních vzorků) vyjádřené v BEQ (pro slepý vzorek a maximální limit nebo akční práh).
7.4.6. Pro slepé vzorky odrážející celý pracovní postup a pro každý typ referenčního vzorku se zaznamenávají a ověřují grafy kontroly kvality, aby bylo zajištěno, že analytická výkonnost je v souladu s příslušnými požadavky, u slepých vzorků odrážejících celý pracovní postup zejména s ohledem na požadovanou minimální odlišnost v nejspodnější části pracovního rozsahu a u referenčních vzorků zejména s ohledem na vnitrolaboratorní reprodukovatelnost. Slepé vzorky odrážející celý pracovní postup musí být důkladně kontrolovány, aby se zamezilo falešně vyhovujícím výsledkům po jejich odečtení.
7.4.7. Výsledky konfirmačních metod u podezřelých vzorků a 2 až 10 % vyhovujících vzorků (minimálně 20 vzorků na jednu matrici) se zaznamenají a použijí se pro hodnocení výkonnosti screeningové metody a vztahu mezi BEQ a TEQ. Tuto databázi lze použít pro přehodnocení mezních hodnot platných pro běžné vzorky pro validované matrice.
7.4.8. Dobrou výkonnost metody lze rovněž prokázat v kruhových testech. Výsledky vzorků analyzovaných v kruhových testech, které pokrývají rozsah koncentrací až do např. dvojnásobku maximálního limitu, se rovněž mohou zahrnout do hodnocení podílu falešně vyhovujících výsledků, je-li laboratoř schopna prokázat dobrou výkonnost. Vzorky musí zahrnovat nejčastější zastoupení kongenerů, které představují různé zdroje.
7.4.9. Při incidentech lze mezní hodnoty přehodnotit, aby odrážely konkrétní matrici a zastoupení kongenerů tohoto konkrétního incidentu.
8. Vydávání výsledků
8.1. Konfirmační metody
8.1.1. Analytické výsledky musí obsahovat hodnoty jednotlivých kongenerů PCDD/PCDF a PCB s dioxinovým efektem a hodnoty TEQ se vydávají jako dolní, horní a střední odhad, aby se do vydávání výsledků zahrnulo co nejvíce informací, a umožnil se tak výklad výsledků podle příslušných zvláštních požadavků.
8.1.2. Protokol musí také zahrnovat metodu použitou pro extrakci PCDD/PCDF a PCB s dioxinovým efektem.
8.1.3. Pokud výtěžnost leží mimo rozpětí uvedené v bodě 6.2.5, je-li překročen maximální limit (v tomto případě výtěžnosti pro jednu ze dvou opakovaných analýz), nebo v ostatních případech na žádost, musí být dány k dispozici hodnoty výtěžnosti pro jednotlivé vnitřní standardy.
8.1.4. Protože se má při rozhodování o souladu vzorku přihlédnout také k rozšířené nejistotě měření, je třeba poskytnout tento parametr. Analytické výsledky se proto vydají ve tvaru „x +/– U“, kde x je výsledek analýzy a U je rozšířená nejistota měření, přičemž se použije faktor pokrytí 2, který odpovídá míře spolehlivosti přibližně 95 %. V případě samostatného stanovení PCDD/PCDF a PCB s dioxinovým efektem se pro sumu PCDD/PCDF a PCB s dioxinovým efektem musí použít suma odhadované rozšířené nejistoty měření samostatných výsledků analýzy pro PCDD/PCDF a PCB s dioxinovým efektem.
8.1.5. Výsledky se vyjádří ve stejných jednotkách a (alespoň) se stejným počtem platných číslic jako maximální limity stanovené ve směrnici 2002/32/ES.
8.2. Bioanalytické screeningové metody
8.2.1. Výsledek screeningu se vyjádří jako „vyhovující“ nebo „podezřelý jako nevyhovující“ („podezřelý“).
8.2.2. Kromě toho je možné vydat orientační výsledek pro PCDD/PCDF a/nebo PCB s dioxinovým efektem vyjádřený v BEQ, nikoli TEQ.
8.2.3. Vzorky s odezvou nižší než oznamovací mez musí být vyjádřeny jako „nižší než oznamovací mez“. Vzorky s odezvou vyšší než pracovní rozsah se vydávají jako „vzorky překračující pracovní rozsah“ a úroveň odpovídající horní části pracovního rozsahu se uvede v BEQ.
8.2.4. Pro každý typ matrice vzorku musí protokol uvádět maximální limit nebo akční práh, z něhož hodnocení vychází.
8.2.5. Protokol musí uvádět použitý typ zkoušky, základní principy zkoušky a druh kalibrace.
8.2.6. Protokol musí také zahrnovat metodu použitou pro extrakci PCDD/PCDF a PCB s dioxinovým efektem.
8.2.7. V případě vzorků podezřelých jako nevyhovující musí protokol obsahovat poznámku o tom, jaká opatření mají být učiněna. Koncentraci PCDD/PCDF a sumu PCDD/PCDF a PCB s dioxinovým efektem v těchto vzorcích se zvýšeným obsahem je třeba stanovit/potvrdit konfirmační metodou.
8.2.8. Nevyhovující výsledky se vydávají pouze tehdy, pokud byly zjištěny konfirmační analýzou.
8.3. Fyzikálně-chemické screeningové metody
8.3.1. Výsledek screeningu se vyjádří jako „vyhovující“ nebo „podezřelý jako nevyhovující“ („podezřelý“).
8.3.2. Pro každý typ matrice vzorku musí protokol uvádět maximální limit nebo akční práh, z něhož hodnocení vychází.
8.3.3. Kromě toho mohou být hodnoty jednotlivých kongenerů PCDD/PCDF a/nebo PCB s dioxinovým efektem a hodnoty TEQ udávány jako dolní, horní a střední odhad. Výsledky se vyjádří ve stejných jednotkách a (alespoň) se stejným počtem platných číslic jako maximální limity stanovené ve směrnici 2002/32/ES.
8.3.4. Pokud výtěžnost leží mimo rozpětí uvedené v bodě 6.2.5, je-li překročen maximální limit (v tomto případě výtěžnosti pro jednu ze dvou opakovaných analýz), nebo v ostatních případech na žádost, musí být dány k dispozici hodnoty výtěžnosti pro jednotlivé vnitřní standardy.
8.3.5. V protokolu musí být uvedeno, která metoda GC-MS byla použita.
8.3.6. Protokol musí také zahrnovat metodu použitou pro extrakci PCDD/PCDF a PCB s dioxinovým efektem.
8.3.7. V případě vzorků podezřelých jako nevyhovující musí protokol obsahovat poznámku o tom, jaká opatření mají být učiněna. Koncentraci PCDD/PCDF a sumu PCDD/PCDF a PCB s dioxinovým efektem v těchto vzorcích se zvýšeným obsahem je třeba stanovit/potvrdit konfirmační metodou.
8.3.8. O tom, zda hodnota nebyla dodržena, může být rozhodnuto pouze konfirmační analýzou.
KAPITOLA III
Příprava vzorků a požadavky na analytické metody používané při úřední kontrole obsahu PCB bez dioxinového efektu v krmivech
1. Oblast působnosti
Požadavky stanovené v této kapitole se vztahují na analýzu krmiv pro úřední kontrolu obsahu PCB bez dioxinového efektu a pro přípravu vzorků a analytické požadavky k jiným regulačním účelům, včetně kontrol prováděných provozovatelem krmivářského podniku k zajištění dodržování ustanovení nařízení (ES) č. 183/2005.
2. Použitelné metody detekce
Plynová chromatografie v tandemu s detektorem elektronového záchytu (GC-ECD), GC-LRMS, GC-MS/MS, GC-HRMS nebo rovnocenné metody.
3. Identifikace a konfirmace sledovaných analytů
3.1. Relativní retenční čas ve vztahu k vnitřním standardům nebo referenčním standardům (s přijatelnou odchylkou ± 0,25 %).
3.2. Separace PCB bez dioxinového efektu plynovou chromatografií od interferujících látek, zejména současně se eluujících PCB, zvláště jsou-li úrovně vzorků v rozmezí limitů stanovených právními předpisy a případný nesoulad má být teprve potvrzen (13).
3.3. Požadavky na techniky GC-MS:
Sledování alespoň následujícího počtu molekulárních iontů nebo charakteristických iontů z molekulárních klastrů:
|
a) |
dvou specifických iontů u HRMS; |
|
b) |
tří specifických iontů u LRMS; |
|
c) |
dvou specifických prekurzorových iontů, každý s jedním odpovídajícím specifickým přechodovým produktovým iontem pro MS-MS. |
Nejvyšší přípustné tolerance intenzity vybraných hmotnostních fragmentů:
Relativní odchylka intenzity vybraných hmotnostních fragmentů od teoretické intenzity nebo kalibračního standardu pro cílový iont (nejintenzivnější sledovaný iont) a identifikační iont (ionty): ± 15 %
3.4. Požadavky na techniky GC-ECD
Konfirmace výsledků překračujících maximální limit s dvěma kolonami GC se stacionární fází jiné polarity.
4. Prokazování výkonnosti metody
Výkonnost metody se prokáže v rozsahu maximálního limitu (polovina až dvojnásobek maximálního limitu) s přijatelným variačním koeficientem pro opakovanou analýzu (viz požadavky na mezilehlou preciznost uvedené v bodě 9).
5. Mez kvantifikace
Suma mezí kvantifikace (14) PCB bez dioxinového efektu nesmí překročit jednu třetinu maximálního limitu (15).
6. Kontrola kvality
Pravidelné slepé kontrolní vzorky, analýzy obohacených vzorků, vzorky pro kontrolu kvality, účast v mezilaboratorních studiích o příslušných matricích.
7. Kontrola výtěžnosti
7.1. Použijí se vhodné vnitřní standardy s fyzikálně-chemickými vlastnostmi porovnatelnými se sledovanými analyty.
7.2. Přidání vnitřních standardů:
přidání k produktům (před extrakcí a čištěním).
7.3. Požadavky na metody s využitím všech šesti izotopicky značených kongenerů PCB bez dioxinového efektu
|
a) |
korekce výsledků na výtěžnost vnitřních standardů; |
|
b) |
výtěžnosti izotopicky značených vnitřních standardů mají být mezi 60 a 120 %; |
|
c) |
nižší nebo vyšší výtěžnosti jednotlivých kongenerů, které se na sumě PCB bez dioxinového efektu podílejí méně než 10 %, jsou přijatelné. |
7.4. Požadavky na metody, které nevyužívají všech šesti izotopicky značených vnitřních standardů nebo jiných vnitřních standardů:
|
a) |
kontrola výtěžnosti vnitřního standardu (vnitřních standardů) pro každý vzorek; |
|
b) |
výtěžnost vnitřních standardů má být mezi 60 a 120 %; |
|
c) |
výsledky se opraví na výtěžnost vnitřních standardů. |
7.5. Výtěžnosti neoznačených kongenerů se ověří pomocí obohacených vzorků nebo vzorků pro kontrolu kvality s koncentracemi v rozsahu maximálního limitu. Výtěžnost těchto kongenerů se považuje za přijatelnou, pokud je mezi 60 a 120 %.
8. Požadavky na laboratoře
V souladu s nařízením (ES) č. 882/2004 musí být laboratoře akreditovány uznaným subjektem působícím v souladu s pokyny ISO Guide 58, aby bylo zaručeno, že uplatňují postupy zajištění analytické kvality. Laboratoře musí být akreditovány podle normy EN ISO/IEC 17025. Kromě toho je v příslušném případě třeba řídit se zásadami popsanými v technických pokynech pro odhad nejistoty měření a meze kvantifikace pro analýzu PCB (16).
9. Kritéria výkonnosti: kritéria pro sumu PCB bez dioxionového efektu při maximálním limitu
|
|
Hmotnostní spektrometrie s izotopovým zřeďováním (17) |
Jiné techniky |
|
Pravdivost |
– 20 % až + 20 % |
– 30 % až + 30 % |
|
Mezilehlá preciznost (% RSD) |
≤ 15 % |
≤ 20 % |
|
Rozdíl mezi výpočtem horního a dolního odhadu |
≤ 20 % |
≤ 20 % |
10. Vydávání výsledků
10.1. Analytické výsledky musí obsahovat hodnoty jednotlivých PCB bez dioxinového efektu a sumu těch kongenerů PCB vydávaných jako dolní, horní a střední odhad, aby se do vydávání výsledků zahrnulo co nejvíce informací, a umožnil se tak výklad výsledků podle příslušných zvláštních požadavků.
10.2. Protokol musí také zahrnovat metodu použitou pro extrakci PCB.
10.3. Pokud výtěžnost leží mimo rozpětí uvedené v bodě 7, je-li překročen maximální limit nebo v ostatních případech na žádost musí být dány k dispozici hodnoty výtěžnosti pro jednotlivé vnitřní standardy.
10.4. Protože se má při rozhodování o souladu vzorku přihlédnout také k rozšířené nejistotě měření, je třeba poskytnout také tento parametr. Analytické výsledky se proto vydají ve tvaru „x +/– U“, kde x je výsledek analýzy a U je rozšířená nejistota měření, přičemž se použije faktor pokrytí 2, který odpovídá míře spolehlivosti přibližně 95 %.
10.5. Výsledky se vyjádří ve stejných jednotkách a (alespoň) se stejným počtem platných číslic jako maximální limity stanovené ve směrnici 2002/32/ES.“
(1) Tabulka faktorů toxické ekvivalence (TEF) pro PCDD, PCDF a PCB s dioxinovým efektem: WHO-TEF (faktory toxické ekvivalence Světové zdravotnické organizace) pro hodnocení nebezpečnosti pro člověka vycházející ze závěrů zasedání odborníků Světové zdravotnické organizace (WHO) Mezinárodní program chemické bezpečnosti (IPCS), které se konalo v Ženevě v červnu 2005 (Martin Van den Berg et al., The 2005 World Health Organization Re-evaluation of Human and Mammalian Toxic Equivalency Factors for Dioxins and Dioxin-like Compounds. Toxicological Sciences 93(2), 223–241 (2006)).
|
Kongener |
Hodnota TEF |
Kongener |
Hodnota TEF |
|
Dibenzo-p-dioxiny („PCDD“) a dibenzofurany („PCDF“) |
|
PCB „s dioxinovým efektem“ Non-ortho PCB + Mono-ortho PCB |
|
|
2,3,7,8-TCDD |
1 |
|
|
|
1,2,3,7,8-PeCDD |
1 |
Non-ortho PCB |
|
|
1,2,3,4,7,8-HxCDD |
0,1 |
PCB 77 |
0,0001 |
|
1,2,3,6,7,8-HxCDD |
0,1 |
PCB 81 |
0,0003 |
|
1,2,3,7,8,9-HxCDD |
0,1 |
PCB 126 |
0,1 |
|
1,2,3,4,6,7,8-HpCDD |
0,01 |
PCB 169 |
0,03 |
|
OCDD |
0,0003 |
Mono-ortho PCB |
|
|
2,3,7,8-TCDF |
0,1 |
PCB 105 |
0,00003 |
|
1,2,3,7,8-PeCDF |
0,03 |
PCB 114 |
0,00003 |
|
2,3,4,7,8-PeCDF |
0,3 |
PCB 118 |
0,00003 |
|
1,2,3,4,7,8-HxCDF |
0,1 |
PCB 123 |
0,00003 |
|
1,2,3,6,7,8-HxCDF |
0,1 |
PCB 156 |
0,00003 |
|
1,2,3,7,8,9-HxCDF |
0,1 |
PCB 157 |
0,00003 |
|
2,3,4,6,7,8-HxCDF |
0,1 |
PCB 167 |
0,00003 |
|
1,2,3,4,6,7,8-HpCDF |
0,01 |
PCB 189 |
0,00003 |
|
1,2,3,4,7,8,9-HpCDF |
0,01 |
|
|
|
OCDF |
0,0003 |
|
|
Použité zkratky: „T“ = tetra; „Pe“ = penta; „Hx“ = hexa; „Hp“ = hepta; „O“ = okta; „CDD“ = chlordibenzo-p-dioxin; „CDF“ = chlordibenzofuran; „CB“ = chlorbifenyl.
(2) Rozhodnutí Komise 2002/657/ES ze dne 14. srpna 2002, kterým se provádí směrnice Rady 96/23/ES, pokud jde o provádění analytických metod a interpretaci výsledků (Úř. věst. L 221, 17.8.2002, s. 8).
(3) V příslušném případě je třeba se řídit zásadami popsanými v dokumentu Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry (http://ec.europa.eu/food/safety/animal-feed_en).
(4) Koncept „horního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru použití hodnoty meze kvantifikace. Koncept „dolního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru použití nulové hodnoty. Koncept „středního odhadu“ vyžaduje pro výpočet příspěvku každého nekvantifikovaného kongeneru použití poloviny hodnoty meze kvantifikace.
(5) Opakovanou analýzou se rozumí samostatná analýza sledovaných analytů na základě druhého alikvotu téhož homogenizovaného vzorku. Obecně se použijí požadavky na opakovanou analýzu stanovené v příloze II kapitole C bodu 3. Avšak u metod s použitím vnitřního standardu značeného izotopem 13C pro příslušné analyty je opakovaná analýza nezbytná pouze tehdy, pokud výsledek prvního stanovení není vyhovující. Opakovaná analýza je nezbytná k vyloučení možnosti vnitřní křížové kontaminace nebo náhodného promíchání vzorků. Je-li analýza prováděna v rámci kontaminační aféry, lze od potvrzení opakovanou analýzou upustit, pokud lze zpětně vysledovat spojitost vzorků vybraných pro analýzu s danou kontaminační aférou a zjištěný obsah je výrazně vyšší než maximální limit.
(6) Koncept „horního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru k hodnotě toxického ekvivalentu (TEQ) použití hodnoty meze kvantifikace. Koncept „dolního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru k hodnotě TEQ použití nulové hodnoty. Koncept „středního odhadu“ vyžaduje pro výpočet příspěvku každého nekvantifikovaného kongeneru k hodnotě TEQ použití poloviny hodnoty meze kvantifikace.
(7) Obecně se použijí požadavky na opakovanou analýzu stanovené v příloze II kapitole C bodu 2. Avšak u konfirmačních metod s použitím vnitřního standardu značeného izotopem 13C pro příslušné analyty je opakovaná analýza nezbytná pouze tehdy, pokud výsledek prvního stanovení za použití takové konfirmační metody není vyhovující. Opakovaná analýza je nezbytná k vyloučení možnosti vnitřní křížové kontaminace nebo náhodného promíchání vzorků. Je-li analýza prováděna v rámci kontaminační aféry, lze od potvrzení opakovanou analýzou upustit, pokud lze zpětně vysledovat spojitost vzorků vybraných pro analýzu s danou kontaminační aférou a zjištěný obsah je výrazně vyšší než maximální limit.
(8) Totožné vysvětlení a požadavky na provedení opakované analýzy pro kontrolu akčních prahů jako v poznámce 2 výše pro maximální limity.
(9) Nařízení Evropského parlamentu a Rady (ES) č. 183/2005 ze dne 12. ledna 2005, kterým se stanoví požadavky na hygienu krmiv (Úř. věst. L 35, 8.2.2005, s. 1).
(10) Bioanalytické metody nejsou specifické pro kongenery zahrnuté v systému TEF. V extraktu vzorku mohou být přítomny jiné strukturně příbuzné AhR-aktivní sloučeniny, které přispívají k celkové reakci. Proto bioanalytické výsledky nelze považovat za odhad, ale spíše za orientační úroveň TEQ ve vzorku.
(11) Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry (http://ec.europa.eu/food/safety/animal-feed_en), Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food (http://ec.europa.eu/food/safety/animal-feed_en).
(*1) S ohledem na maximální limity.
(12) Současné požadavky vycházejí z TEF vydaných v: M. Van den Berg et al, Toxicol Sci 93 (2), 223–241 (2006).
(13) Mezi kongenery, u nichž je často zjištěno, že se eluují zároveň, patří např. PCB 28/31, PCB 52/69 a PCB 138/163/164. U GC-MS je rovněž nutné vzít v úvahu možné interference z fragmentů vyšších chlorovaných kongenerů.
(14) V příslušném případě je třeba se řídit zásadami popsanými v dokumentu Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food (http://ec.europa.eu/food/safety/animal-feed_en).
(15) Velmi se doporučuje, aby hodnoty slepého stanovení činidla byly nižší, než je obsah kontaminující látky ve vzorku. Je povinností laboratoře kontrolovat rozptyl hodnot slepých stanovení, zejména v případě, kdy se hodnoty slepého stanovení odečítají.
(16) Současné požadavky vycházejí z TEF vydaných v: M. Van den Berg et al, Toxicol Sci 93 (2), 223–241 (2006).
(17) Jako vnitřní standardy musí být použito všech šest sloučenin značených izotopem 13C.
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/43 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/772
ze dne 3. května 2017,
kterým se mění prováděcí nařízení (EU) č. 908/2014, pokud jde o seznam opatření, u nichž mají být zveřejněny některé údaje o příjemcích
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 1306/2013 ze dne 17. prosince 2013 o financování, řízení a sledování společné zemědělské politiky a o zrušení nařízení Rady (EHS) č. 352/78, (ES) č. 165/94, (ES) č. 2799/98, (ES) č. 814/2000, (ES) č. 1290/2005 a (ES) č. 485/2008 (1), a zejména na článek 114 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Podle čl. 111 odst. 1 nařízení (EU) č. 1306/2013 jsou členské státy povinny zveřejňovat údaje o příjemcích finančních prostředků z Evropského zemědělského záručního fondu a Evropského zemědělského fondu pro rozvoj venkova, a to mimo jiné včetně výše vyplacených částek, které příjemce obdržel za každé opatření financované z těchto fondů, a povahy a popisu každého opatření. |
|
(2) |
Článek 57 prováděcího nařízení Komise (EU) č. 908/2014 (2) stanoví podrobnější údaje, které musí být v souvislosti s těmito opatřeními zveřejněny, a odkazuje na přílohu XIII uvedeného nařízení, která obsahuje seznam příslušných opatření. |
|
(3) |
V důsledku ruského zákazu dovozu zemědělských produktů a potravin pocházejících z Unie a nižšího růstu celosvětové poptávky po mléce a mléčných výrobcích, zejména v důsledku poklesu vývozu do Číny, přijala Komise opatření v odvětví živočišné výroby nezbytná k řešení situace na trhu podle čl. 219 odst. 1 nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 (3). Tato opatření jsou stanovena v nařízeních Komise v přenesené pravomoci (EU) 2015/1853 (4), (EU) 2016/1612 (5) a (EU) 2016/1613 (6). Tato opatření byla poskytnuta jako opatření na podporu zemědělských trhů v souladu s čl. 4 odst. 1 písm. a) nařízení (EU) č. 1306/2013 a vztahují se na rozpočtový rok 2016 nebo 2017, ale nejsou zahrnuta do seznamu v příloze XIII prováděcího nařízení (EU) č. 908/2014. Proto je vhodné je do uvedeného seznamu zařadit. |
|
(4) |
Prováděcí nařízení (EU) č. 908/2014 by proto mělo být odpovídajícím způsobem změněno. |
|
(5) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Výboru zemědělských fondů, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
V příloze XIII prováděcího nařízení (EU) č. 908/2014 se doplňuje nový bod 10, který zní:
|
„10. |
Opatření poskytnutá v odvětví živočišné výroby podle čl. 219 odst. 1 nařízení (EU) č. 1308/2013 jako opatření na podporu zemědělských trhů v souladu s čl. 4 odst. 1 písm. a) nařízení (EU) č. 1306/2013.“ |
Článek 2
Toto nařízení vstupuje v platnost třetím dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 3. května 2017.
Za Komisi
předseda
Jean-Claude JUNCKER
(1) Úř. věst. L 347, 20.12.2013, s. 549.
(2) Prováděcí nařízení Komise (EU) č. 908/2014 ze dne 6. srpna 2014, kterým se stanoví pravidla pro uplatňování nařízení Evropského parlamentu a Rady (EU) č. 1306/2013, pokud jde o platební agentury a další subjekty, finanční řízení, schvalování účetní závěrky, pravidla pro kontroly, jistoty a transparentnost (Úř. věst. L 255, 28.8.2014, s. 59).
(3) Nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 ze dne 17. prosince 2013, kterým se stanoví společná organizace trhů se zemědělskými produkty a zrušují nařízení Rady (EHS) č. 922/72, (EHS) č. 234/79, (ES) č. 1037/2001 a (ES) č. 1234/2007 (Úř. věst. L 347, 20.12.2013, s. 671).
(4) Nařízení Komise v přenesené pravomoci (EU) 2015/1853 ze dne 15. října 2015, kterým se stanoví dočasná mimořádná podpora pro zemědělce v odvětví živočišné výroby (Úř. věst. L 271, 16.10.2015, s. 25).
(5) Nařízení Komise v přenesené pravomoci (EU) 2016/1612 ze dne 8. září 2016 o poskytování podpory na snížení produkce mléka (Úř. věst. L 242, 9.9.2016, s. 4).
(6) Nařízení Komise v přenesené pravomoci (EU) 2016/1613 ze dne 8. září 2016, kterým se stanoví mimořádná podpora na přizpůsobení pro producenty mléka a zemědělce v dalších odvětvích živočišné výroby (Úř. věst. L 242, 9.9.2016, s. 10).
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/45 |
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/773
ze dne 3. května 2017
o stanovení paušálních dovozních hodnot pro určení vstupní ceny některých druhů ovoce a zeleniny
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (EU) č. 1308/2013 ze dne 17. prosince 2013, kterým se stanoví společná organizace trhů se zemědělskými produkty a zrušují nařízení Rady (EHS) č. 922/72, (EHS) č. 234/79, (ES) č. 1037/2001 a (ES) č. 1234/2007 (1),
s ohledem na prováděcí nařízení Komise (EU) č. 543/2011 ze dne 7. června 2011, kterým se stanoví prováděcí pravidla k nařízení Rady (ES) č. 1234/2007 pro odvětví ovoce a zeleniny a odvětví výrobků z ovoce a zeleniny (2), a zejména na čl. 136 odst. 1 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Prováděcí nařízení (EU) č. 543/2011 stanoví na základě výsledků Uruguayského kola mnohostranných obchodních jednání kritéria, podle kterých má Komise stanovit paušální hodnoty pro dovoz ze třetích zemí, pokud jde o produkty a lhůty uvedené v části A přílohy XVI uvedeného nařízení. |
|
(2) |
Paušální dovozní hodnota se vypočítá každý pracovní den v souladu s čl. 136 odst. 1 prováděcího nařízení (EU) č. 543/2011, a přitom se zohlední proměnlivé denní údaje. Toto nařízení by proto mělo vstoupit v platnost dnem zveřejnění v Úředním věstníku Evropské unie, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Paušální dovozní hodnoty uvedené v článku 136 prováděcího nařízení (EU) č. 543/2011 jsou stanoveny v příloze tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dnem zveřejnění v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 3. května 2017.
Za Komisi,
jménem předsedy,
Jerzy PLEWA
generální ředitel
Generální ředitelství pro zemědělství a rozvoj venkova
(1) Úř. věst. L 347, 20.12.2013, s. 671.
(2) Úř. věst. L 157, 15.6.2011, s. 1.
PŘÍLOHA
Paušální dovozní hodnoty pro určení vstupní ceny některých druhů ovoce a zeleniny
|
(EUR/100 kg) |
||
|
Kód KN |
Kód třetích zemí (1) |
Paušální dovozní hodnota |
|
0702 00 00 |
EG |
288,4 |
|
MA |
90,1 |
|
|
TR |
118,3 |
|
|
ZZ |
165,6 |
|
|
0707 00 05 |
MA |
79,4 |
|
TR |
142,5 |
|
|
ZZ |
111,0 |
|
|
0709 93 10 |
TR |
138,1 |
|
ZZ |
138,1 |
|
|
0805 10 22 , 0805 10 24 , 0805 10 28 |
EG |
54,3 |
|
IL |
80,7 |
|
|
MA |
57,7 |
|
|
TR |
65,5 |
|
|
ZA |
43,6 |
|
|
ZZ |
60,4 |
|
|
0805 50 10 |
TR |
54,0 |
|
ZZ |
54,0 |
|
|
0808 10 80 |
AR |
92,9 |
|
BR |
119,5 |
|
|
CL |
122,6 |
|
|
NZ |
140,7 |
|
|
ZA |
84,4 |
|
|
ZZ |
112,0 |
|
(1) Klasifikace zemí podle nařízení Komise (EU) č. 1106/2012 ze dne 27. listopadu 2012, kterým se provádí nařízení Evropského parlamentu a Rady (ES) č. 471/2009 o statistice Společenství týkající se zahraničního obchodu se třetími zeměmi, pokud jde o aktualizaci klasifikace zemí a území (Úř. věst. L 328, 28.11.2012, s. 7). Kód „ZZ“ znamená „jiného původu“.
SMĚRNICE
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/47 |
SMĚRNICE KOMISE (EU) 2017/774
ze dne 3. května 2017,
kterou se za účelem přijetí zvláštních limitních hodnot pro chemické látky použité v hračkách mění dodatek C přílohy II směrnice Evropského parlamentu a Rady 2009/48/ES o bezpečnosti hraček, pokud jde o fenol
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na směrnici Evropského parlamentu a Rady 2009/48/ES ze dne 18. června 2009 o bezpečnosti hraček (1), a zejména na čl. 46 odst. 2 uvedené směrnice,
vzhledem k těmto důvodům:
|
(1) |
Za účelem zajištění vysoké úrovně ochrany dětí proti rizikům, která představují chemické látky v hračkách, stanoví směrnice 2009/48/ES určité požadavky, pokud jde o chemické látky klasifikované jako karcinogenní, mutagenní nebo toxické pro reprodukci (CMR) podle nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 (2), alergenní vonné látky a některé prvky. Kromě toho směrnice 2009/48/ES zmocňuje Komisi přijmout zvláštní limitní hodnoty pro chemické látky použité v hračkách určených pro děti mladší 36 měsíců a v jiných hračkách určených ke vkládání do úst, aby byla zajištěna odpovídající ochrana v případě hraček s vysokou úrovní expozice. Přijetí těchto limitních hodnot má podobu zařazení do dodatku C přílohy II směrnice 2009/48/ES. |
|
(2) |
U řady chemických látek jsou v současnosti platné limitní hodnoty s ohledem na dostupné vědecké důkazy buď příliš vysoké, nebo neexistují. Proto by pro ně měly být přijaty zvláštní limitní hodnoty, při zohlednění požadavků na balení potravin, jakož i rozdílů mezi hračkami a materiály určenými pro styk s potravinami. |
|
(3) |
Evropská komise zřídila skupinu odborníků pro bezpečnost hraček, aby jí tato skupina poskytovala poradenství při přípravě legislativních návrhů a politických iniciativ v oblasti bezpečnosti hraček. Úkolem její podskupiny „chemické látky“ je poskytovat takové poradenství ohledně chemických látek, které mohou být použity v hračkách. |
|
(4) |
Fenol (číslo CAS 108-95-2) se používá jako monomer fenolových pryskyřic při výrobě desek pro hračky pojených pryskyřicemi (3). Rozklad fenolických antioxidantů na polymery může být dalším zdrojem fenolu v hračkách (4). Fenol byl zjištěn v emisích z herních konzolí (5), v jednom ze šesti analyzovaných stanů nebo tunelů pro děti (6) a v balicí fólii (7), byl testován u hraček do vany a jiných nafukovacích hraček (8) a byla zjištěna jeho přítomnost v polyvinylchloridu (PVC) (9). Fenol by dále mohl být použit jako konzervační látka v některých hračkách obsahujících tekutinu na bázi vody, jako jsou bublifuky nebo tekuté inkousty na bázi vody (například fixy) (10). |
|
(5) |
Podskupina „chemické látky“ přijala při svých jednáních o fenolu jako základ evropské normy EN 71-9:2005+A1:2007, EN 71-10:2005 a EN 71-11:2005. Tyto normy odkazují na přítomnost fenolu v materiálech hraček (EN 71-9:2005+A1:2007) a poskytují specifické metody přípravy vzorku (EN 71-10:2005) a měření (EN 71-11:2005). Norma EN 71-11:2005 znovu uvádí a poskytuje podrobnosti pro limitní hodnoty pro fenol v materiálech hraček stanovené v normě EN 71-9:2005+A1:2007, a to 15 mg/l (migrační limit) pro fenol jako monomer a 10 mg/kg (limit obsahu) pro fenol jako konzervační látku v některých materiálech hraček obsahujících tekutinu. |
|
(6) |
Podskupina „chemické látky“ rovněž vzala v úvahu doporučení Vědeckého výboru pro zdravotní a environmentální rizika (SCHER), že by hodnota migračního limitu 15 mg/l pro fenol stanovená ve stávající evropské normě měla být snížena přinejmenším o faktor 2, aby se dosáhlo rozpětí expozice 100, které by mohlo být považováno za dostatečně široké (11). |
|
(7) |
Podskupina „chemické látky“ kromě toho přihlédla ke stanovisku vědecké komise pro materiály přicházející do styku s potravinami, enzymy, aromata a pomocné látky (CEF) a Evropského úřadu pro bezpečnost potravin (EFSA), kterým byl snížen tolerovatelný denní příjem pro fenol z 1,5 mg/kg tělesné hmotnosti denně na 0,5 mg/kg tělesné hmotnosti denně (12). |
|
(8) |
Podle nařízení (ES) č. 1272/2008 je fenol klasifikován jako mutagenní látka kategorie 2. Podle bodu 5 části III přílohy II směrnice 2009/48/ES mohou být mutagenní látky kategorie 2, jako je fenol, obsaženy v hračkách v koncentracích stejných nebo nižších, než je příslušná koncentrace stanovená pro klasifikaci směsí s obsahem těchto látek, konkrétně 1 %, což se rovná 10 000 mg/kg (limit obsahu). Směrnice 2009/48/ES v současné době nestanoví migrační limit pro fenol. |
|
(9) |
Podskupina „chemické látky“ proto na svých zasedáních dne 26. března 2014 a 18. února 2015 doporučila, aby byl fenol v hračkách omezen na 5 mg/l (migrační limit), je-li analyzován v polymerických materiálech, a na maximální koncentraci 10 mg/kg (limit obsahu), je-li analyzován jako konzervační látka, čímž se rozumí to, že 10 mg/kg (limit obsahu) fakticky představuje zákaz používání. Analýzy by měly být prováděny v souladu s evropskými normami EN 71-10:2005 a EN 71-11:2005. |
|
(10) |
Ačkoli existuje obecný migrační limit pro fenol jako monomer pro použití v určitých materiálech určených pro styk s potravinami, základní předpoklady pro odvození tohoto migračního limitu se liší od požadavků na migrační limit pro fenol jako monomer v hračkách. Používání fenolu jako konzervační látky není u materiálů určených pro styk s potravinami regulováno. |
|
(11) |
S ohledem na výše uvedené by měl být dodatek C přílohy II směrnice 2009/48/ES změněn tak, aby obsahoval migrační limit a rovněž limit obsahu pro fenol v hračkách. |
|
(12) |
Opatření stanovená touto směrnicí jsou v souladu se stanoviskem výboru zřízeného článkem 47 směrnice 2009/48/ES, |
PŘIJALA TUTO SMĚRNICI:
Článek 1
V dodatku C přílohy II směrnice 2009/48/ES se doplňuje nová položka, která zní:
|
Látka |
Číslo CAS |
Limitní hodnota |
|
„Fenol |
108-95-2 |
5 mg/l (migrační limit) v polymerických materiálech v souladu s metodami stanovenými v normách EN 71-10:2005 a EN 71-11:2005. 10 mg/kg (limit obsahu) jako konzervační látka v souladu s metodami stanovenými v normách EN 71-10:2005 a EN 71-11:2005.“ |
Článek 2
1. Členské státy přijmou a zveřejní právní a správní předpisy nezbytné pro dosažení souladu s touto směrnicí do 4. listopadu 2018 Neprodleně sdělí Komisi jejich znění.
Použijí tyto předpisy ode dne 4. listopadu 2018.
Tyto předpisy přijaté členskými státy musí obsahovat odkaz na tuto směrnici nebo musí být takový odkaz učiněn při jejich úředním vyhlášení. Způsob odkazu si stanoví členské státy.
2. Členské státy sdělí Komisi znění hlavních ustanovení vnitrostátních právních předpisů, které přijmou v oblasti působnosti této směrnice.
Článek 3
Tato směrnice vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Článek 4
Tato směrnice je určena členským státům.
V Bruselu dne 3. května 2017.
Za Komisi
předseda
Jean-Claude JUNCKER
(1) Úř. věst. L 170, 30.6.2009, s. 1.
(2) Nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 ze dne 16. prosince 2008 o klasifikaci, označování a balení látek a směsí, o změně a zrušení směrnic 67/548/EHS a 1999/45/ES a o změně nařízení (ES) č. 1907/2006 (Úř. věst. L 353, 31.12.2008, s. 1).
(3) E. Edmonds (2013), Occurrence of Phenol and Formaldehyde in Toys. Zpráva, kterou zadala společnost Toy Industries of Europe, s. 4.
(4) Viz pozn. pod čarou 3, s. 5 a 8.
(5) Dánská agentura na ochranu životního prostředí (2003), Survey of chemical substances in consumer products, Survey no. 32–2003: Emission and evaluation of chemical substances from selected electrical and electronic products, s. 47. http://eng.mst.dk/media/mst/69115/32.pdf
(6) Dánská agentura na ochranu životního prostředí (2004), Mapping of Chemical Substances in Consumer Products, nr. 46, 2004: Release of chemical substances from tents and tunnels for children. http://eng.mst.dk/media/mst/69127/46.pdf
(7) Bundesinstitut für Risikobewertung (2009), Limit values for phenol in food-contact articles and toys are to be updated. Stanovisko č. 038/2009 ze dne 18. srpna 2009. http://www.bfr.bund.de/cm/349/limit_values_for_phenol_in_food_contact_articles_and_toys_are_to_be_updated.pdf
(8) Voedsel en Waren Autoriteit (2004), Market Surveillances on Toy Safety. Zpráva č. ND04o063/01. https://www.nvwa.nl/binaries/nvwa/documenten/communicatie/inspectieresultaten/consument/2016m/market-surveillances-on-toy-safety/ND04o063-01_speelgoed.pdf
(9) Suortti T (1990), Determination of phenol in poly(vinyl chloride). J Chromatogr. 16. května 1990; 507:417-20. http://www.ncbi.nlm.nih.gov/pubmed/2380304
(10) CEN TC 52 (2002), Final report of the work of CEN/TC 52/WG 9 – Risk assessment. Smlouva BC/CEN/97/29.1.1. srpen 2002, s. 85.
(11) Vědecký výbor pro zdravotní a environmentální rizika (SCHER), Opinion on CEN's response to the opinion of the CSTEE on the assessment of CEN report on the risk assessment of organic chemicals in toys. Stanovisko přijaté 29. května 2007, s. 8 a 9.
(12) Evropský úřad pro bezpečnost potravin (EFSA), Scientific Opinion on the toxicological evaluation of phenol, EFSA Journal 2013;11(4):3189 [44 s.]. http://www.efsa.europa.eu/en/efsajournal/pub/3189.htm
ROZHODNUTÍ
|
4.5.2017 |
CS |
Úřední věstník Evropské unie |
L 115/50 |
ROZHODNUTÍ RADY (EU) 2017/775
ze dne 25. dubna 2017
o jmenování jedné náhradnice Výboru regionů, navržené Finskou republikou
RADA EVROPSKÉ UNIE,
s ohledem na Smlouvu o fungování Evropské unie, a zejména na článek 305 této smlouvy,
s ohledem na návrh finské vlády,
vzhledem k těmto důvodům:
|
(1) |
Dne 26. ledna 2015, dne 5. února 2015 a dne 23. června 2015 přijala Rada rozhodnutí (EU) 2015/116 (1), (EU) 2015/190 (2) a (EU) 2015/994 (3) o jmenování členů a náhradníků Výboru regionů na období od 26. ledna 2015 do 25. ledna 2020. |
|
(2) |
Po skončení funkčního období paní Katri KULMUNIOVÉ se uvolnilo jedno místo náhradníka Výboru regionů, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Do Výboru regionů je na zbývající část funkčního období, tedy do 25. ledna 2020, jmenována jako náhradnice:
|
— |
paní Merja LAHTINENOVÁ, Jämsän kaupunginvaltuuston jäsen. |
Článek 2
Toto rozhodnutí vstupuje v platnost dnem přijetí.
V Lucemburku dne 25. dubna 2017.
Za Radu
předseda
I. BORG
(1) Rozhodnutí Rady (EU) 2015/116 ze dne 26. ledna 2015 o jmenování členů a náhradníků Výboru regionů na období od 26. ledna 2015 do 25. ledna 2020 (Úř. věst. L 20, 27.1.2015, s. 42).
(2) Rozhodnutí Rady (EU) 2015/190 ze dne 5. února 2015 o jmenování členů a náhradníků Výboru regionů na období od 26. ledna 2015 do 25. ledna 2020 (Úř. věst. L 31, 7.2.2015, s. 25).
(3) Rozhodnutí Rady (EU) 2015/994 ze dne 23. června 2015 o jmenování členů a náhradníků Výboru regionů na období od 26. ledna 2015 do 25. ledna 2020 (Úř. věst. L 159, 25.6.2015, s. 70).