EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32012R0278
Commission Regulation (EU) No 278/2012 of 28 March 2012 amending Regulation (EC) No 152/2009 as regards the determination of the levels of dioxins and polychlorinated biphenyls Text with EEA relevance
Nařízení Komise (EU) č. 278/2012 ze dne 28. března 2012 , kterým se mění nařízení (ES) č. 152/2009, pokud jde o stanovení obsahu dioxinů a polychlorovaných bifenylů Text s významem pro EHP
Nařízení Komise (EU) č. 278/2012 ze dne 28. března 2012 , kterým se mění nařízení (ES) č. 152/2009, pokud jde o stanovení obsahu dioxinů a polychlorovaných bifenylů Text s významem pro EHP
OJ L 91, 29.3.2012, p. 8–22
(BG, ES, CS, DA, DE, ET, EL, EN, FR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
Special edition in Croatian: Chapter 03 Volume 071 P. 19 - 33
 In force
In force
- Date of document:
- 28/03/2012
- Date of effect:
- 18/04/2012; Vstoupení v platnost Den vyhlášení + 20 Viz Čl. 2
- Date of effect:
- 18/04/2012; Použitelnost Viz Čl. 2
- Date of end of validity:
- No end date
- Author:
- Evropská komise
- Form:
- Nařízení
- Additional information:
- Význam pro EHP
- Treaty:
- Smlouvy o fungování Evropské unie
- Legal basis:
-
- 32004R0882 - A11P4
- Link
- Link
- Link
- Select all documents mentioning this document No data available in the table
- Modifies:
-
Relation Act Comment Subdivision concerned From To Modifies 32009R0152 Nahrazení příloha 5 P.B 18/04/2012 - Instruments cited:
- Link
- EUROVOC descriptor:
- Subject matter:
- Directory code:
-
- 03.50.10.00 Zemědělství / Sbližování práva a opatření na ochranu zdraví / Krmiva
|
29.3.2012 |
CS |
Úřední věstník Evropské unie |
L 91/8 |
NAŘÍZENÍ KOMISE (EU) č. 278/2012
ze dne 28. března 2012,
kterým se mění nařízení (ES) č. 152/2009, pokud jde o stanovení obsahu dioxinů a polychlorovaných bifenylů
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 882/2004 ze dne 29. dubna 2004 o úředních kontrolách za účelem ověření dodržování právních předpisů týkajících se krmiv a potravin a pravidel o zdraví zvířat a dobrých životních podmínkách zvířat (1), a zejména na čl. 11 odst. 4 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Směrnice Evropského parlamentu a Rady 2002/32/ES ze dne 7. května 2002 o nežádoucích látkách v krmivech (2) stanoví maximální obsahy dioxinů, furanů a polychlorovaných bifenylů (PCB) v krmivech a akční prahy, při jejichž překročení vedou členské státy šetření s cílem určit zdroje těchto látek. |
|
(2) |
Nařízení Komise (ES) č. 152/2009 ze dne 27. ledna 2009, kterým se stanoví metody odběru vzorků a laboratorního zkoušení pro úřední kontrolu krmiv (3), obsahuje metody pro stanovení obsahu polychlorovaných dibenzo-p-dioxinů (PCDD) a polychlorovaných dibenzofuranů (PCDF)) a polychlorovaných bifenylů s dioxinovým efektem (PCB) v krmivech. |
|
(3) |
Pro identifikaci vzorků s významným obsahem PCDD/PCDF a PCB s dioxinovým efektem (nejlépe výběrem vzorků přesahujících akční prahy a zajištěním výběru vzorků překračujících maximální obsahy) lze použít vysoce výkonnou screeningovou analytickou metodu s obecně uznanou validací. Obsah PCDD/PCDF a PCB s dioxinovým efektem v těchto vzorcích je třeba určit konfirmační analytickou metodou. Proto je vhodné stanovit příslušné požadavky na screeningovou metodu, která zajistí, že míra falešně vyhovujících výsledků, pokud jde o maximální obsahy, je nižší než 5 %, a přísné požadavky na konfirmační analytické metody. Konfirmační metody navíc umožňují stanovení nízkých úrovní pozadí. To je důležité pro sledování vývoje v čase, posouzení expozice a pro přehodnocení maximálních obsahů a akčních prahů. |
|
(4) |
V důsledku změny maximálních obsahů pro dioxiny a PCB s dioxinovým efektem a stanovení PCB bez dioxinového efektu ve směrnici 2002/32/ES a potřeby aktualizovat kritéria pro screeningové metody je nezbytné změnit pravidla pro stanovení dioxinů a PCB v krmivech, jak jsou stanovena v části B přílohy V nařízení (ES) č. 152/2009. Z důvodů jasnosti a srozumitelnosti je vhodné přílohu V část B nahradit. |
|
(5) |
Je velice důležité, aby byly výsledky analýzy vydávány a interpretovány jednotným způsobem s cílem zajistit harmonizované postupy prosazování předpisů v celé Unii. |
|
(6) |
Příloha V nařízení (ES) č. 152/2009 by tedy měla být odpovídajícím způsobem změněna. |
|
(7) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem Stálého výboru pro potravinový řetězec a zdraví zvířat a ani Evropský parlament ani Rada nevyjádřily s těmito opatřeními nesouhlas, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
Příloha V část B nařízení (ES) č. 152/2009 se mění v souladu s přílohou tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie.
Použije se ode dne vstupu v platnost.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 28. března 2012.
Za Komisi
José Manuel BARROSO
předseda
(1) Úř. věst. L 165, 30.4.2004, s. 1.
(2) Úř. věst. L 140, 30.5.2002, s. 10.
(3) Úř. věst. L 54, 26.2.2009, s. 1.
PŘÍLOHA
V příloze V nařízení (ES) č. 152/2009 se část B „STANOVENÍ OBSAHU DIOXINŮ (PCDD/PCDF) A PCB S DIOXINOVÝM EFEKTEM“ nahrazuje tímto:
„B. STANOVENÍ OBSAHU DIOXINŮ (PCDD/PCDF) A PCB
KAPITOLA I
Metody odběru vzorků a interpretace výsledků zkoušek
1. Účel a rozsah
Vzorky určené pro úřední kontrolu obsahu polychlorovaných dibenzo-p-dioxinů (PCDD), polychlorovaných dibenzofuranů (PCDF), polychlorovaných bifenylů (PCB) s (1) dioxinovým efektem a PCB bez dioxinového efektu v krmivech se odebírají v souladu s ustanoveními přílohy I. Musí být použity kvantitativní požadavky týkající se kontroly látek nebo produktů obsažených rovnoměrně v krmivech, jak je stanoveno v bodě 5.A přílohy I. Takto získané souhrnné vzorky se považují za reprezentativní pro vzorkované partie nebo části vzorkované partie. Dodržení maximálních hodnot stanovených ve směrnici 2002/32/ES se posuzuje na základě obsahů určených v laboratorních vzorcích.
Pro účely této části přílohy V se použijí definice uvedené v příloze I rozhodnutí Komise 2002/657/ES ze dne 14. srpna 2002, kterým se provádí směrnice Rady 96/23/ES, pokud jde o provádění analytických metod a interpretaci výsledků (2).
2. Dodržení maximálního obsahu ve vzorkované partii nebo v části vzorkované partie
2.1 Pokud jde o PCB bez dioxinového efektu
Vzorkovaná partie je v souladu se specifikací, pokud výsledek zkoušky nepřekročí příslušný maximální obsah pro PCB bez dioxinového efektu stanovený ve směrnici 2002/32/ES při zohlednění nejistoty měření.
Vzorkovaná partie nevyhovuje specifikaci, pokud horní (3) odhad výsledku zkoušky konfirmovaný opakovanou zkouškou (4) překračuje příslušný maximální obsah stanovený ve směrnici 2002/32/ES při současném zohlednění nejistoty měření.
Nejistotu měření lze zohlednit jedním z těchto způsobů:
|
— |
započtením rozšířené nejistoty při použití faktoru pokrytí 2, který odpovídá hladině spolehlivosti asi 95 %. Vzorkovaná partie nebo její část nesplňuje podmínky, pokud naměřená hodnota, od níž se odečte U, přesahuje maximální obsah, |
|
— |
stanovením rozhodovací meze (CCα) v souladu s bodem 3.1.2.5 přílohy I rozhodnutí 2002/657/ES. Vzorkovaná partie nebo její část nesplňuje podmínky, pokud se naměřená hodnota rovná CCα, nebo je vyšší. |
Uvedená pravidla interpretace se použijí pro výsledky zkoušek získané u vzorků pro úřední kontrolu. U zkoušek pro účely obhajoby nebo rozhodčího řízení se použijí vnitrostátní předpisy.
2.2 Pokud jde o PCDD/PCDF a PCB s dioxinovým efektem
Vzorkovaná partie je v souladu se specifikací, pokud výsledek jedné zkoušky
|
— |
provedené screeningovou metodou s mírou falešně vyhovujících výsledků nižší než 5 % naznačuje, že obsah nepřesahuje příslušný maximální obsah pro PCDD/PCDF a pro součet PCDD/PCDF a PCB s dioxinovým efektem stanovené ve směrnici 2002/32/ES, |
|
— |
provedené konfirmační metodou nepřekročí příslušný maximální obsah pro PCDD/PCDF a pro součet PCDD/PCDF a PCB s dioxinovým efektem stanovený ve směrnici 2002/32/ES, při zohlednění nejistoty měření. |
U screeningových zkoušek se pro rozhodnutí o souladu vzorku s příslušnými sledovanými úrovněmi stanovenými buď pro PCDD/PCDF nebo pro součet PCDD/PCDF a PCB s dioxinovým efektem stanoví mezní hodnoty.
Vzorkovaná partie nevyhovuje specifikaci, pokud horní (5) odhad výsledku zkoušky získaný konfirmační metodou a konfirmovaný opakovanou zkouškou překračuje příslušný maximální obsah stanovený ve směrnici 2002/32/ES při současném zohlednění nejistoty měření (6).
Nejistotu měření lze zohlednit jedním z těchto způsobů:
|
— |
započtením rozšířené nejistoty při použití faktoru pokrytí 2, který odpovídá hladině spolehlivosti asi 95 %. Vzorkovaná partie nebo její část nesplňuje podmínky, pokud naměřená hodnota, od níž se odečte U, přesahuje maximální obsah, v případě samostatného stanovení PCDD/PCDF a PCB s dioxinovým efektem se součet odhadované rozšířené nejistoty měření samostatných výsledků zkoušek u PCDD/PCDF a PCB s dioxinovým efektem musí použít pro součet PCDD/PCDF a PCB s dioxinovým efektem, |
|
— |
stanovením rozhodovací meze (CCα) v souladu s bodem 3.1.2.5 přílohy I rozhodnutí 2002/657/ES. Vzorkovaná partie nebo její část nesplňuje podmínky, pokud se naměřená hodnota rovná CCα, nebo je vyšší. |
Uvedená pravidla interpretace se použijí na výsledky zkoušek získané u vzorků pro úřední kontrolu. U zkoušek pro účely obhajoby nebo rozhodčího řízení se použijí vnitrostátní předpisy.
3. Výsledky překračující akční prahy stanovené v příloze II směrnice 2002/32/ES
Akční prahy slouží jako nástroj pro výběr vzorků v případech, kdy je třeba zjistit zdroj kontaminace a přijmout opatření pro jeho omezení nebo odstranění. Screeningové metody stanoví vhodné mezní hodnoty pro výběr těchto vzorků. Zjišťování zdroje a omezení nebo odstranění kontaminace se provede, pouze pokud překročení akčních prahů konfirmuje opakovaná zkouška s použitím konfirmační metody a s přihlédnutím k nejistotě měření (7).
KAPITOLA II
Příprava vzorků a požadavky na analytické metody používané při úřední kontrole obsahu dioxinů (PCDD/PCDF) a PCB s dioxinovým efektem v krmivech
1. Oblast použití
Požadavky stanovené v této příloze se použijí tam, kde jsou zkoušena krmiva za účelem úřední kontroly obsahu polychlorovaných dibenzo-p-dioxinů substituovaných v polohách 2,3,7,8 (PCDD) a polychlorovaných dibenzofuranů (PCDD/F)) a polychlorovaných bifenylů s dioxinovým efektem (PCB s dioxinovým efektem) a pro účely regulace.
Sledování přítomnosti PCDD/PCDF a PCB s dioxinovým efektem v krmivech může mít dva různé cíle:
|
a) |
výběr vzorků s obsahem PCDD/PCDF a PCB s dioxinovým efektem převyšujícím maximální obsahy nebo akční hodnoty. Tento přístup může zahrnovat screeningovou metodu umožňující nákladově efektivní analýzu velkého množství vzorků, čímž se zvyšuje možnost zjistit nové případy vysoké expozice a ohrožení zdraví spotřebitelů. Screeningové metody mohou zahrnovat bioanalytické metody a metody GC/MS. Cílem jejich použití je zabránit falešně vyhovujícím výsledkům. Koncentraci PCDD/PCDF a součet PCDD/PCDF a PCB s dioxinovým efektem v těchto vzorcích s významným obsahem je třeba stanovit/potvrdit konfirmační metodou. |
|
b) |
stanovení obsahu PCDD/PCDF a PCB s dioxinovým efektem ve vzorcích krmiva v rozmezí nízké úrovně pozadí. To je důležité pro sledování vývoje v čase, posouzení expozice populace a pro vytvoření databáze za účelem případného přehodnocení akčních hodnot a maximálních obsahů. Tohoto cíle se dosahuje pomocí konfirmačních metod umožňujících jednoznačnou identifikaci a kvantifikaci PCDD/PCDF a PCB s dioxinovým efektem na sledované úrovni. Tyto metody lze použít při monitoringu krmiv pro konfirmaci výsledků získaných screeningovými metodami a pro stanovení nízkých úrovní pozadí. Rovněž jsou významné pro stanovení zastoupení kongenerů za účelem zjištění zdroje možné kontaminace. V současnosti tyto metody využívají plynovou chromatografii s vysokým rozlišením v tandemu s hmotnostní spektrometrií s vysokým rozlišením (HRGC/HRMS). |
2. Klasifikace metod podle stupně kvantifikace (8)
2.1 Kvalitativní metody dávají jednoznačnou odpověď (ano/ne), co se týče přítomnosti sledovaných analytů, avšak bez kvantitativních údajů o koncentraci domnělého analytu. Kvalitativní metody mohou mít potenciál pro poskytování semikvantitativních výsledků, avšak používají se výhradně pro účely rozhodnutí, zda úrovně překračují určitá rozpětí, např. mez detekce, mez kvantifikace nebo mezní hodnoty, či nikoliv.
Pro kontrolu maximálních obsahů a akčních hodnot PCDD/PCDF a PCB s dioxinovým efektem v krmivech mohou být použity screeningové metody založené na porovnání výsledku zkoušky s mezní hodnotou, které dávají odpověď ano/ne, pokud jde o možné překročení sledovaného obsahu.
2.2 Semikvantitativní metody poskytují přibližné údaje o koncentraci domnělého analytu, přičemž numerické výsledky nesplňují požadavky na kvantitativní metody. Mohou se použít ke zjištění rozsahu koncentrace analytu, na jehož základě osoba provádějící analýzu rozhodne o kalibračním rozsahu pro následně prováděnou konfirmační zkoušku a pro účely kontroly kvality. Za semikvantitativní metody se například považují tyto metody:
|
a) |
metody založené na využití biologických principů, jako jsou zkoušky na buněčné bázi, receptorové zkoušky nebo imunologické zkoušky (dále jen „bioanalytické metody“), které jsou schopny odhalit sledované analyty, zahrnují kalibrační křivku, umožňují jednoznačné rozhodnutí (ano/ne) o případném překročení sledovaného limitu a umožňují uvést výsledek jako bioanalytické ekvivalenty (BEQ), přičemž poskytují údaj o hodnotě TEQ ve vzorku, |
|
b) |
fyzikálně-chemické zkoušky (např. plynová chromatografie – hmotnostní spektrometrie / hmotnostní spektrometrie (GC-MS/MS) nebo plynová chromatografie / hmotnostní spektrometrie s nízkým rozlišením GC/LRMS)), u nichž zjištěná přesnost metody nesplňuje požadavky na kvantitativní zkoušky. |
2.3 Kvantitativní metody splňují stejné požadavky na správnost, dynamický rozsah a přesnost jako konfirmační metody. Požaduje-li se kvantifikace, validují se kvantitativní metody jako konfirmační metody.
3. Souvislosti
Pro výpočet koncentrací toxických ekvivalentů (TEQ) se koncentrace jednotlivých látek v daném vzorku vynásobí jejich příslušnými toxickými ekvivalenčními faktory (TEF), které jsou stanoveny Světovou zdravotnickou organizací a jsou uvedeny v dodatku k této příloze, sečtou se a výsledný součet je celkovou koncentrací sloučenin s dioxinovým efektem vyjádřenou v toxických ekvivalentech (TEQ).
Pro účely části B přílohy V je schválenou specifickou mezí kvantifikace jednotlivého kongeneru koncentrace analytu v extraktu vzorku, jež dává instrumentální odezvu na dvou různých iontech, které mají být monitorovány při poměru signál–šum 3:1 pro méně intenzivní signál a při splnění základních kritérií pro identifikaci, jako jsou například kritéria popsaná v normě prEN 16215 (Krmiva – stanovení dioxinů a PCB s dioxinovým efektem pomocí plynové chromatografie / hmotnostní spektrometrie s vysokým rozlišením (GC/HRMS) a indikátorových PCB pomocí GC/HRMS) a/nebo v metodě EPA 1613 revize B.
Bioanalytické screeningové metody neposkytnou výsledky na úrovni kongeneru, ale pouze orientační hodnoty (9) úrovně TEQ, vyjádřené v bioanalytických ekvivalentech (BEQ), aby byla zohledněna skutečnost, že ne všechny sloučeniny přítomné v extraktu vzorku, který při zkoušce dává odezvu, nutně splňují všechny požadavky principu TEQ.
Screeningové a konfirmační metody mohou být použity pouze pro kontrolu určité matrice, pokud jsou tyto metody dostatečně citlivé, aby spolehlivě zjistily hodnoty na sledované úrovni (akční práh nebo maximální obsah).
4. Požadavky na zabezpečení kvality
4.1 Na každém stupni odběru vzorků a analýzy se přijmou opatření k zamezení křížové kontaminace.
4.2 Vzorky musí být uchovávány a přepravovány ve skleněných, hliníkových, polypropylenových nebo polyethylenových nádobách vhodných pro skladování bez jakéhokoli vlivu na obsahy PCDD/PCDF a PCB s dioxinovým efektem ve vzorcích. Z nádoby na vzorky se odstraní stopy papírového prachu.
4.3 Vzorky se uchovávají a přepravují tak, aby byla zachována integrita vzorku krmiv.
4.4 Pokud je to relevantní, jednotlivé laboratorní vzorky se jemně rozemelou a důkladně promísí postupem, u něhož je prokázáno, že se jím dosáhne úplné homogenizace (např. rozemletím a proséváním přes síto s průměrem ok 1 mm). Je-li vlhkost vzorků příliš vysoká, musí se vzorky před rozemletím sušit.
4.5 Je vždy důležité zkontrolovat činidla, pomůcky ze skla a vybavení z hlediska možného vlivu na výsledky založené na TEQ nebo BEQ.
4.6 Provede se slepá analýza, při níž se provede celý postup laboratorního zkoušení bez vzorku.
4.7 U bioanalytických metod se u veškerých při zkoušce použitých pomůcek ze skla a rozpouštědel potvrdí, že jsou prosty sloučenin, které mohou bránit zjištění cílových sloučenin v pracovním rozsahu. Skleněné pomůcky se vypláchnou rozpouštědly nebo zahřejí na teploty vhodné pro odstranění stop PCDD/PCDF, sloučenin s dioxinovým efektem a interferujících sloučenin z jejich povrchu.
4.8 Množství vzorku použité pro extrakci musí být dostatečné, aby byly splněny požadavky s ohledem na dostatečně nízký pracovní rozsah včetně sledovaných koncentrací.
4.9 Specifické postupy přípravy vzorku použité pro zkoumané produkty musí splňovat mezinárodně uznávané metodiky.
5. Požadavky na laboratoře
5.1 V souladu s nařízením (ES) č. 882/2004 musí být laboratoře akreditovány uznávaným subjektem působícím v souladu s ISO Guide 58, aby bylo zaručeno, že uplatňují postupy zajištění kvality při zkouškách. Laboratoře musí být akreditovány podle normy EN ISO/IEC 17025.
5.2 Odbornost laboratoře prokazuje soustavná úspěšná účast v mezilaboratorních studiích týkajících se stanovení PCDD/PCDF a PCB s dioxinovým efektem v příslušných matricích krmiv a koncentračních rozpětích.
5.3 Laboratoře, které pro běžnou kontrolu vzorků používají screeningové metody, musí úzce spolupracovat s laboratořemi používajícími konfirmační metodu, za účelem jak kontroly kvality, tak konfirmace výsledku analýzy podezřelých vzorků.
6. Základní Požadavky, které musí splňovat analytická metoda pro dioxiny (PCDD/PCDF) a PCB s dioxinovým efektem
6.1 Nízký pracovní rozsah a meze kvantifikace
V případě PCDD/PCDF musí být zjistitelné množství z důvodu extrémní toxicity některých těchto sloučenin na horní úrovni femtogramů (10–15g). V případě většiny kongenerů PCB je dostatečná již mez kvantifikace na úrovni nanogramů (10–9g). Pro měření toxičtějších kongenerů PCB s dioxinovým efektem (zejména non-ortho substituovaných kongenerů) však musí nejspodnější část pracovního rozsahu dosahovat nízkých úrovní pikogramů (10–12g). U všech ostatních kongenerů PCB je dostatečná již mez kvantifikace na úrovni nanogramů (10–9g).
6.2 Vysoká selektivita (specifičnost)
6.2.1 Je třeba rozlišovat PCDD/PCDF a PCB s dioxinovým efektem od řady jiných sloučenin, které se extrahují společně s těmito látkami, mohou rušit při jejich stanovení a jsou přítomny v koncentracích až o několik řádů vyšších než koncentrace sledovaných analytů. Pro GC/MS je třeba rozlišení mezi různými kongenery, např. mezi toxickými kongenery (např. sedmnácti PCCC/PCDF substituovanými v polohách 2,3,7,8 a dvanácti PCB s dioxinovým efektem) a ostatními kongenery.
6.2.2 Bioanalytické metody musí být schopny detekovat cílové sloučeniny jako součet PCDD/PCDF a/nebo PCB s dioxinovým efektem. Přečištění vzorku se zaměří na odstranění sloučenin způsobujících falešně nevyhovující výsledky nebo sloučenin, které mohou způsobovat snížení odezvy vedoucí k falešně vyhovujícím výsledkům.
6.3 Vysoká správnost (pravdivost a přesnost, zjevná výtěžnost biologické zkoušky)
6.3.1 U GC/MS musí stanovení poskytovat správný odhad skutečné koncentrace ve vzorku. Vysoká správnost je nezbytná k tomu, aby nedošlo k zamítnutí výsledku zkoušky vzorku na základě malé spolehlivosti stanovení TEQ. Správnost je vyjádřena pravdivostí (rozdílem mezi střední naměřenou hodnotou analytu v certifikovaném materiálu a jeho certifikovanou hodnotou, vyjádřeným v procentech této hodnoty) a přesností (RSDR je relativní směrodatná odchylka vypočtená z výsledků získaných za podmínek reprodukovatelnosti).
6.3.2 Pro bioanalytické metody se určí zjevná výtěžnost biologické zkoušky. Zjevnou výtěžností biologické zkoušky se rozumí hodnota BEQ vypočtená z kalibrační křivky TCDD nebo PCB 126 upravená o hodnoty slepého stanovení a poté vydělená hodnotou TEQ určenou pomocí GC/HRMS. Jejím účelem je korekce činitelů, jako je ztráta PCDD/PCDF a sloučenin s dioxinovým efektem během extrakce a čištění, současně extrahované sloučeniny zesilující nebo tlumící odezvu (agonistické a antagonistické účinky), kvalita kalibrace nebo rozdíly mezi hodnotami toxické ekvivalence (TEF) a relativní účinnosti (REP). Zjevná výtěžnost biologické zkoušky se vypočte z vhodných referenčních vzorků s reprezentativním zastoupením kongenerů kolem sledované úrovně.
6.4 Validace v rozsahu sledovaného obsahu a obecná opatření pro kontrolu kvality
6.4.1 Laboratoře musí prokázat spolehlivost metody v rozsahu kolem sledované úrovně, např. v polovině, jednonásobku nebo dvojnásobku sledované úrovně, a to s přijatelným variačním koeficientem pro opakovanou zkoušku, a sice během validace a/nebo během rutinní zkoušky.
6.4.2 Jako opatření v rámci vnitřní kontroly kvality se provádějí pravidelná slepá kontrolní stanovení, stanovení s obohacenými vzorky nebo zkoušky kontrolních vzorků (nejlépe certifikovaného referenčního materiálu, je-li k dispozici). Ze slepých kontrolních stanovení, stanovení s obohacenými vzorky nebo zkoušek kontrolních vzorků se vyhotoví a ověří grafy kontroly kvality, aby bylo zajištěno, že analytická výkonnost metody je v souladu s požadavky.
6.5 Mez kvantifikace
6.5.1 Pro bioanalytické screeningové metody není stanovení meze kvantifikace nezbytné, příslušná metoda však musí prokázat, že umožňuje rozlišení mezi hodnotou slepého stanovení a mezní hodnotou. Pokud se vydává hodnota BEQ, musí být stanovena oznamovací mez pro vzorky s odezvou nižší než tato úroveň. Musí být prokázáno, že se oznamovací mez významně (nejméně trojnásobně) liší od slepých vzorků odrážejících celý pracovní postup s odezvou nižší než pracovní rozsah. Vypočte se proto ze vzorků obsahujících cílové sloučeniny přibližně v požadované minimální úrovni, a nikoli z poměru S/N nebo ze slepé zkoušky.
6.5.2 Mez kvantifikace u konfirmačních metod činí přibližně jednu pětinu sledované úrovně.
6.6 Analytická kritéria
Pro spolehlivé výsledky konfirmačních nebo screeningových metod musí být splněna následující kritéria pro hodnotu TEQ, případně BEQ, ať už je určena jako celkový TEQ (jako součet PCDD/PCDF a PCB s dioxinovým efektem), nebo samostatně pro PCDD/PCDF a PCB s dioxinovým efektem:
|
|
Screening pomocí bioanalytických nebo fyzikálně-chemických metod |
Konfirmační metody |
|
Míra falešně vyhovujících výsledků (10) |
< 5 % |
|
|
Pravdivost |
|
20 % až + 20 % |
|
Opakovatelnost (RSDr) |
< 20 % |
|
|
Vnitrolaboratorní reprodukovatelnost (RSDR) |
< 25 % |
< 15 % |
6.7 Zvláštní požadavky na screeningové metody
6.7.1 Pro screening mohou být použity jak GC/MS, tak bioanalytické metody. Metody GC/MS musí splňovat požadavky stanovené v bodě 7. Pro buněčné bioanalytické metody jsou zvláštní požadavky stanoveny v bodě 8.
6.7.2 Laboratoře, které pro rutinní kontrolu vzorků používají screeningové metody, musí úzce spolupracovat s laboratořemi používajícími konfirmační metodu.
6.7.3 Během rutinní zkoušky je nutné ověřovat výkonnost příslušné screeningové metody, a to kontrolou kvality při zkouškách a průběžnou validací metody. Zavede se stálý program kontroly vyhovujících výsledků.
6.7.4 Kontrola možného potlačení buněčné odezvy a cytotoxicity:
20 % extraktů vzorků se změří při rutinním screeningu bez přidání a s přidáním 2,3,7,8-TCDD v množství odpovídajícím sledovanému obsahu, aby se zjistilo, zda odezva není potlačována interferujícími látkami přítomnými v extraktu vzorku. Naměřená koncentrace u obohaceného vzorku se porovná se součtem koncentrace neobohaceného extraktu a koncentrace obohacující látky. Pokud je tato naměřená koncentrace o více než 25 % nižší než vypočtená (souhrnná) koncentrace, svědčí to o tom, že možná dochází k potlačení odezvy, a dotčený vzorek musí být podroben konfirmační zkoušce pomocí GC/HRMS. Výsledky musí být zaznamenány v grafech kontroly kvality.
6.7.5 Kontrola kvality u vyhovujících vzorků
Přibližně 2 až 10 % vyhovujících vzorků, v závislosti na matrici vzorků a zkušenostech laboratoře, musí být potvrzeno pomocí GC/HRMS.
6.7.6 Stanovení míry falešně vyhovujících vzorků na základě údajů z kontroly kvality
|
|
Stanoví se míra falešně vyhovujících výsledků na základě screeningu nižších a vyšších než maximální obsah nebo akční práh. Skutečný podíl falešně vyhovujících výsledků musí být nižší než 5 %. Je-li k dispozici nejméně 20 potvrzených výsledků z kontroly kvality vyhovujících vzorků na matrici / matricovou skupinu, vyvodí se z těchto výsledků závěry ohledně míry falešně vyhovujících výsledků. Do minimálního počtu 20 výsledků pro hodnocení míry falešně vyhovujících výsledků se mohou zahrnout i výsledky ze vzorků vyhodnocených pomocí okružních rozborů nebo při kontaminačních aférách, které pokrývají rozpětí koncentrace až např. do dvojnásobku maximálního obsahu. Vzorky musí zahrnovat nejčastější zastoupení kongenerů, které představují různé zdroje. |
|
|
Ačkoli se mají screeningové testy přednostně zaměřit na zjištění vzorků přesahujících akční práh, je kritériem pro stanovení míry falešně vyhovujících výsledků maximální obsah, s přihlédnutím k nejistotě měření konfirmační metody. |
6.7.7 Výsledky ze screeningu považované za nevyhovující musí být vždy ověřeny konfirmační metodou zkoušení (GC/HRMS). Tyto vzorky mohou být také použity pro vyhodnocení podílu falešně nevyhovujících výsledků. U screeningových metod je mírou falešně nevyhovujících výsledků podíl výsledků, které konfirmační zkouška pomocí GC/HRMS potvrdí jako vyhovující, zatímco při předchozím screeningu bylo vysloveno podezření, že je vzorek nevyhovující. Hodnocení výhodnosti použití screeningové metody však musí vycházet z porovnání falešně nevyhovujících výsledků a celkového počtu kontrolovaných vzorků. Tento poměr musí být dostatečně nízký, aby bylo možné považovat používání příslušného screeningového nástroje za výhodné.
6.7.8 Bioanalytické metody musí alespoň při validačních podmínkách poskytovat platné údaje o úrovni TEQ, vypočtené a vyjádřené jako BEQ.
Pro bioanalytické metody prováděné za podmínek reprodukovatelnosti je vnitrolaboratorní RSDr obvykle menší než reprodukovatelnost RSDR.
7. Zvláštní požadavky, které musí splňovat metody GC/MS, aby vyhovovaly pro účely screeningu nebo konfirmace
7.1 Obecné požadavky
U krmiv s úrovní kontaminace přibližně 1 ng WHO-TEQ na kilogram produktu o obsahu vlhkosti 12 % (na základě součtu PCDD/PCDF a PCB s dioxinovým efektem) nesmí rozdíl mezi horním odhadem a dolním odhadem překročit 20 %. Při nižších úrovních kontaminace, např. 0,5 ng WHO-TEQ na kilogram produktu, může být rozdíl mezi horním a dolním odhadem v rozpětí mezi 25 % a 40 %.
7.2 Kontrola výtěžnosti
7.2.1 Vnitřní standardy 2,3,7,8-chlor-substituovaných PCDD/PCDF značené isotopem 13C a standardy PCB s dioxinovým efektem značené isotopem 13C musí být přidány na samém začátku nebo při zahájení zkoušky, např. před extrakcí, aby bylo možné validovat postup laboratorního zkoušení. Alespoň jeden kongener musí být přidán pro každou z tetra až okta-chlorovaných homologických skupin PCDD/PCDF a alespoň jeden kongener pro každou z homologických skupin PCB s dioxinovým efektem (nebo alespoň jeden kongener pro každou skupinu vybraných iontů při použití hmotnostní spektrometrie v režimu registrace vybraných iontů, použitou pro sledování PCDD/PCDF a PCB s dioxinovým efektem). V případě konfirmačních metod se použije všech 17 vnitřních standardů 2,3,7,8-substituovaných PCDD/PCDF značených izotopem 13C a všech 12 vnitřních standardů PCB s dioxinovým efektem značených pomocí 13C.
7.2.2 Relativní odezvové faktory se s pomocí vhodných kalibračních roztoků stanoví také pro kongenery, pro něž nebyly přidány sloučeniny značené pomocí 13C.
7.2.3 U krmiv rostlinného původu nebo krmiv živočišného původu s obsahem tuku nižším než 10 % je přidání vnitřních standardů před extrakcí povinné. U krmiv živočišného původu s obsahem tuku vyšším než 10 % lze vnitřní standardy přidat buď před extrakcí, nebo po extrakci tuku. Vhodným způsobem se validuje účinnost extrakce, a to v závislosti na fázi, ve které se přidávají vnitřní standardy, a podle toho, zda se vydávané výsledky vztahují na výrobek nebo na tuk ve výrobku obsažený.
7.2.4 Před zkouškou metodou GC/MS musí být přidány 1 nebo 2 obohacené standardy (recovery standardy) pro stanovení výtěžnosti.
7.2.5 Kontrola výtěžnosti je nezbytná. U konfirmačních metod se výtěžnost jednotlivých vnitřních standardů musí pohybovat v rozmezí 60 až 120 %. Nižší nebo vyšší hodnota výtěžnosti jednotlivých kongenerů, zejména některých hepta- a okta-chlorovaných dibenzo-p-dioxinů a dibenzofuranů, je přípustná pod podmínkou, že jejich příspěvek k hodnotě TEQ nepřesáhne 10 % celkové hodnoty TEQ (na základě součtu PCDD/PCDF a PCB s dioxinovým efektem). Hodnota výtěžnosti u screeningových metod GC/MS se musí pohybovat mezi 30 a 140 %.
7.3 Odstranění interferujících látek
|
— |
Oddělení PCDD/PCDF od interferujících chlorovaných sloučenin, jako jsou PCB bez dioxinového efektu a chlorované difenylethery, se provede vhodnými chromatografickými technikami (nejlépe na florisilové, aluminové a/nebo uhlíkové koloně). |
|
— |
Rozdělení isomerů pomocí plynové chromatografie musí být dostatečné (< 25 % překryvu mezi píky 1,2,3,4,7,8-HxCDF a 1,2,3,6,7,8-HxCDF). |
7.4 Kalibrace pomocí standardní křivky
Rozsah kalibrační křivky musí pokrývat odpovídající rozpětí sledovaných úrovní.
8. Zvláštní požadavky na bioanalytické metody
Bioanalytické metody jsou metody založené na využití biologických principů, jako jsou buněčné testy, receptorové testy nebo imunologické testy. Tento bod 8 stanoví obecné požadavky na bioanalytické metody.
Screeningové metody v zásadě klasifikují vzorky jako vyhovující nebo vzorky podezřelé jako nevyhovující. Za tímto účelem se vypočtená hladina BEQ porovnává s mezní hodnotou (viz bod 8.3). Vzorky nižší než mezní hodnota se považují za vyhovující, vzorky rovnající se mezní hodnotě nebo vyšší se považují za podezřelé jako nevyhovující a je nutné provést jejich analýzu pomocí konfirmační metody. Prakticky může jako nejvhodnější mezní hodnota sloužit množství BEQ odpovídající 2/3 maximálního obsahu, přičemž taková mezní hodnota zajišťuje míru falešně vyhovujících vzorků nižší než 5 % a přijatelnou míru falešně nevyhovujících vzorků. Při různém maximálním obsahu pro PCDD/PCDF a pro součet PCDD/PCDF a PCB s dioxinovým efektem vyžaduje kontrola souladu vzorků bez frakcionace vhodné mezní hodnoty pro biologickou zkoušku pro PCDD/F. Pro kontrolu vzorků překračujících akční prahy je vhodnou mezní hodnotou přiměřené procento příslušné sledované úrovně.
V případě některých bioanalytických metod může být navíc stanovena orientační úroveň vyjádřená v BEQ pro vzorky v pracovním rozsahu, které přesahují oznamovací mez (viz 8.1.1. a 8.1.6.).
8.1 Hodnocení odezvy zkoušky
8.1.1
|
— |
Při výpočtu koncentrace z kalibrační křivky TCDD vykazují hodnoty na spodním a horním konci křivky velký křivkový rozptyl (CV). Pracovní rozsah je oblast, kde je tento rozptyl menší než 15 %. Spodní část pracovního rozsahu (oznamovací mez) musí být stanovena tak, aby výrazně (nejméně trojnásobně) přesahovala hodnoty slepých vzorků odrážejících celý pracovní postup. Horní část pracovního rozsahu obvykle představuje hodnota EC70 (70 % maximální efektivní koncentrace), je však nižší, pokud je CV v tomto rozpětí vyšší než 15 %. Pracovní rozsah se stanoví během validace. Mezní hodnoty (viz bod 8.3) musí být uvnitř pracovního rozsahu. |
|
— |
Standardní roztoky a extrakty vzorku se zkouší alespoň duplicitně. Při duplicitních zkouškách musí standardní roztok nebo kontrolní extrakt zkoušený ve 4–6 jamkách rozložených na destičce poskytnout odezvu nebo koncentraci (možné pouze v pracovním rozsahu) vycházející z CV < 15 %. |
8.1.2
8.1.2.1
|
— |
Za účelem výpočtu úrovně BEQ v extraktu a následně ve vzorku lze úroveň ve vzorcích odhadnout porovnáním jejich odezvy s odezvou kalibrační křivky TCDD (nebo PCB 126 nebo standardní směsi PCDD/PCDF / PCB s dioxinovým efektem). |
|
— |
Kalibrační křivky musí obsahovat 8 až 12 koncentrací (alespoň duplicitních), s dostatečným počtem koncentrací ve spodní části křivky (pracovním rozsahu). Zvláštní pozornost musí být věnována kvalitě proložení kalibračních bodů křivkou v pracovním rozsahu. Hodnota R2 sama o sobě má pouze zanedbatelný nebo žádný význam při hodnocení kvality proložení kalibračních bodů křivkou při nelineární regresi. Lepšího proložení se dosáhne minimalizací rozdílu mezi vypočtenými a zjištěnými úrovněmi v pracovním rozsahu křivky (např. minimalizací součtu druhých mocnin reziduí). |
|
— |
Od odhadované úrovně v extraktu vzorku se následně odečte úroveň BEQ vypočtená pro slepý vzorek matrice/rozpouštědla (aby se zohlednily nečistoty z použitých rozpouštědel a chemikálií) a provede se korekce na zjevnou výtěžnost (vypočtenou na základě úrovně BEQ vhodných referenčních vzorků s reprezentativním zastoupením kongenerů kolem sledované úrovně). Pro provedení korekce na výtěžnost musí být zjevná výtěžnost v požadovaném rozmezí (viz bod 8.1.4). Referenční vzorky použité pro korekci na výtěžnost musí splňovat požadavky stanovené v bodě 8.2. |
8.1.2.2
Případně lze použít kalibrační křivku zhotovenou alespoň ze čtyř referenčních vzorků (viz bod 8.2.4: jednoho matričního slepého vzorku plus tří referenčních vzorků na polovině, jednonásobku a dvojnásobku sledované úrovně) kolem sledované úrovně, čímž odpadne nutnost odečtu hodnoty slepého stanovení a korekce na výtěžnost. V tomto případě lze odezvu odpovídající 2/3 maximálního obsahu (viz bod 8.3) vypočítat přímo z těchto vzorků a použít ji jako mezní hodnotu. Pro kontrolu vzorků překračujících akční prahy je vhodnou mezní hodnotou přiměřené procento těchto akčních prahů.
8.1.3
Extrakty lze rozdělit do frakcí obsahujících PCDD/PCDF a PCB s dioxinovým efektem, což umožňuje získání oddělených údajů o hladinách TEQ pro PCDD/PCDF a PCB s dioxinovým efektem (v BEQ). Pro hodnocení výsledků pro frakci obsahující PCB s dioxinovým efektem se přednostně použije kalibrační křivka standardu PCB 126.
8.1.4
„Zjevná výtěžnost biologické zkoušky“ se vypočte z vhodných referenčních vzorků s reprezentativním zastoupením kongenerů kolem sledované úrovně a vyjádří se jako procento hladiny BEQ v porovnání s hladinou TEQ. V závislosti na použitém typu zkoušky a složení TEF (11) mohou rozdíly mezi faktory TEF a REP pro PCB s dioxinovým efektem způsobit nízkou zjevnou výtěžnost u PCB s dioxinovým efektem v porovnání s PCDD/PCDF. Proto při samostatném stanovení PCDD/PCDF a PCB s dioxinovým efektem musí být zjevná výtěžnost biologických zkoušek následující: u PCB s dioxinovým efektem 25 % až 60 %, u PCDD/PCDF 50 % až 130 % (rozmezí platná pro kalibrační křivku TCDD). Jelikož podíl PCB s dioxinovým efektem na součtu PCDD/PCDF a PCB s dioxinovým efektem se může u různých matric a vzorků lišit, odráží se tyto rozdíly i ve zjevné výtěžnosti biologických zkoušek pro součet PCDD/PCDF a PCB s dioxinovým efektem, která se má pohybovat v rozmezí 30 % až 130 %. Důsledky případné podstatné revize hodnot TEF pro právní předpisy Unie týkající se PCDD/PCDF a PCB s dioxinovým efektem budou vyžadovat revizi těchto rozmezí.
8.1.5
Při validaci je nutné zkontrolovat ztrátu sloučenin během čištění. Slepý vzorek obohacený směsí různých kongenerů se podrobí čištění (alespoň n = 3) a výtěžnost a variabilita se ověří zkouškou GC/HRMS. Výtěžnost musí být v rozmezí 60 % až 120 %, zejména u kongenerů s podílem na množství TEQ v různých směsích vyšším než 10 %.
8.1.6
Pokud se vydává hodnota BEQ, musí být stanovena oznamovací mez z příslušných matričních vzorků zahrnujících typická zastoupení kongenerů, avšak vzhledem k nízké přesnosti v dolním rozsahu křivky nikoli z kalibrační křivky standardů. Je třeba vzít v úvahu účinky extrakce a čištění. Oznamovací mez musí být stanovena nejméně trojnásobně vyšší než hodnoty slepých vzorků odrážejících celý pracovní postup.
8.2 Použití referenčních vzorků
8.2.1 Referenční vzorky musí představovat matrice vzorku, zastoupení kongenerů a rozpětí koncentrací pro PCDD/PCDF a PCB s dioxinovým efektem kolem sledované úrovně.
8.2.2 Každá série zkoušek musí zahrnovat slepý vzorek odrážející celý pracovní postup, či nejlépe slepý matriční vzorek, a referenční vzorek na sledované úrovni. Tyto vzorky musí být extrahovány a zkoušeny současně a za stejných podmínek. Referenční vzorek musí vykázat jasně vyšší odezvu v porovnání s odezvou slepého vzorku, čímž je zajištěna vhodnost zkoušky. Tyto vzorky mohou být použity pro odečtení blanku a korekci na výtěžnost.
8.2.3 Referenční vzorky vybrané pro provedení korekce na výtěžnost musí být reprezentativní pro zkušební vzorky, což znamená, že zastoupení kongenerů nesmí vést k podhodnocení úrovní.
8.2.4 Pro kontrolu sledované úrovně lze kromě toho zahrnout ještě referenční vzorky o např. poloviční a dvojnásobné koncentraci, než je sledovaná úroveň, aby byla prokázána odpovídající výkonnost zkoušky ve sledovaném rozsahu. Dohromady mohou být tyto vzorky použity pro výpočet úrovní BEQ ve zkušebních vzorcích (viz bod 8.1.2.2).
8.3 Stanovení mezních hodnot
Je nutné určit vztah mezi výsledky biologické zkoušky v BEQ a výsledky GC/HRMS v TEQ (např. pomocí kalibračních pokusů, které zohledňují vliv matrice, s referenčními vzorky uměle obohacenými na nule, polovině, jednonásobku a dvojnásobku maximálního obsahu s šesti opakováními na každé úrovni (n = 24)). Na základě tohoto vztahu lze odhadnout korekční faktory (odečtení blanku a korekce na výtěžnost), je však nutno je ověřit v souladu s bodem 8.2.2.
Je nutné stanovit mezní hodnoty pro účely rozhodnutí ohledně souladu vzorku s maximálními obsahy nebo pro kontrolu akčních prahů, jsou-li sledovanou hodnotou, a rovněž s příslušnými sledovanými úrovněmi buď zvlášť pro PCDD/PCDF a PCB s dioxinovým efektem, nebo pro součet PCDD/PCDF a PCB s dioxinovým efektem. Jsou zastoupeny nižším cílovým bodem distribuce výsledků biologické zkoušky (korigovaných o hodnoty slepého stanovení a korigovaných na výtěžnost) odpovídajícím rozhodovací mezi u GC/HRMS na základě 95 % jistoty, z čehož vyplývá míra falešně vyhovujících výsledků < 5 %, a na základě RSDR < 25 %. Rozhodovací mezí u GC/HRMS je maximální obsah při zohlednění nejistoty měření.
Mezní hodnotu (v BEQ) lze vypočítat v souladu s jedním z postupů uvedených v bodech 8.3.1, 8.3.2 a 8.3.3 (viz graf 1):
|
8.3.1 |
S použitím nižší části 95% predikčního intervalu ve výši rozhodovací meze GC/HRMS: 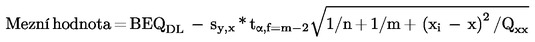
kde:
|
|
8.3.2 |
Z výsledků biologické zkoušky (korigovaných o hodnoty slepého stanovení a korigovaných na výtěžnost) získaných z vícenásobných zkoušek vzorků (n≥6) kontaminovaných na úrovni rozhodovací meze GC/HRMS, jakožto nižší část rozdělení výsledků na odpovídající průměrné hodnotě BEQ: Mezní hodnota = BEQDL – 1,64 × SDR kde
|
|
8.3.3 |
Výpočet jako střední hodnota výsledků bioanalýzy (v BEQ, korigovaných o hodnoty slepého stanovení a korigovaných na výtěžnost) z vícenásobné analýzy vzorků (n≥6) kontaminovaných na 2/3 sledované úrovně, na základě poznatku, že tato úroveň se bude pohybovat kolem mezní hodnoty určené v bodech 8.3.1 nebo 8.3.2: Graf č. 1
|
|
8.3.4 |
Omezení mezních hodnot: Mezní hodnoty vycházející z BEQ a vypočtené z RSDR dosažené při validaci s použitím omezeného počtu vzorků s různým zastoupením matrice/kongenerů mohou být vyšší než sledované úrovně vycházející z TEQ, vzhledem k větší přesnosti, než je přesnost, jíž lze běžně dosáhnout s neznámým spektrem zastoupení kongenerů. V takových případech se mezní hodnoty vypočtou z RSDR = 25 %, v ostatních případech se dá přednost dvěma třetinám sledované úrovně. |
8.4 Kritéria výkonnosti
8.4.1 Provedou se zkoušky opakovatelnosti bioanalytických metod, aby se získaly informace o směrodatné odchylce v rámci zkoušek a mezi sériemi zkoušek. Opakovatelnost musí být nižší než 20 %, vnitrolaboratorní reprodukovatelnost pak nižší než 25 %. To musí vycházet z vypočtených úrovní v BEQ po odečtení blanku a korekci na výtěžnost.
8.4.2 Jako součást postupu validace musí být prokázáno, že zkouška umožňuje rozlišit slepý vzorek a úroveň ve výši mezní hodnoty, a umožňuje tak identifikovat vzorky nad příslušnou mezní hodnotou (viz bod 8.1.2).
8.4.3 Je třeba určit cílové sloučeniny, možné interference a nejvyšší přípustný obsah ve slepém vzorku.
8.4.4 Procentní směrodatná odchylka odezvy nebo koncentrace vypočtená z odezvy (možné pouze v pracovním rozsahu) trojnásobného stanovení extraktu vzorku nesmí být vyšší než 15 %.
8.4.5 Pro hodnocení výkonnosti bioanalytické metody v konstantním časovém období se použijí nekorigované výsledky referenčního vzorku (referenčních vzorků) vyjádřené v BEQ (pro slepý vzorek a sledovanou úroveň).
8.4.6 Pro slepé vzorky odrážející celý pracovní postup a pro každý typ referenčního vzorku se zaznamenávají a ověřují grafy kontroly kvality, aby bylo zajištěno, že analytická výkonnost je v souladu s příslušnými požadavky, u slepých vzorků odrážející celý pracovní postup zejména s ohledem na požadovanou minimální odlišnost v nejnižší části pracovního rozsahu a u referenčních vzorků zejména s ohledem na vnitrolaboratorní reprodukovatelnost. Slepé vzorky odrážející celý pracovní postup musí být důkladně kontrolovány, aby se zamezilo falešně vyhovujícím výsledkům po jejich odečtení.
8.4.7 Výsledky zkoušek podezřelých vzorků a 2 až 10 % vyhovujících vzorků (minimálně 20 vzorků na jednu matrici) získané technikou GC/HRMS se zaznamenají a použijí se pro hodnocení výkonnosti screeningové metody a vztahu mezi BEQ a TEQ. Tuto databázi lze použít pro přehodnocení mezních hodnot platných pro běžné vzorky pro validované matrice.
8.4.8 Dobrou výkonnost metody lze rovněž prokázat v okružních rozborech. Výsledky vzorků analyzovaných v okružních rozborech, které pokrývají rozsah koncentrací až do např. dvojnásobku maximálního obsahu, se rovněž mohou zahrnout do hodnocení podílu falešně vyhovujících výsledků, je-li laboratoř schopna prokázat dobrou výkonnost. Vzorky musí zahrnovat nejčastější zastoupení kongenerů, které představují různé zdroje.
8.4.9 Při incidentech lze mezní hodnoty přehodnotit, aby odrážely konkrétní matrici a zastoupení kongenerů tohoto konkrétního incidentu.
9. Vydávání výsledků
9.1 Konfirmační metody
9.1.1 Pokud to použitý postup laboratorního zkoušení umožňuje, musí výsledky obsahovat hodnoty jednotlivých kongenerů PCDD/PCDF a PCB s dioxinovým efektem a vydávají se jako dolní, horní a střední odhad, aby se do vydávání výsledků zahrnulo co nejvíce informací, a umožnil se tak výklad výsledků podle příslušných zvláštních požadavků.
9.1.2 Zpráva musí také zahrnovat metodu použitou pro extrakci PCDD/PCDF, PCB s dioxinovým efektem a lipidů.
9.1.3 Pokud výtěžnost leží mimo rozpětí uvedené v bodě 7.2.5, je-li překročen maximální obsah nebo v ostatních případech na žádost, musí být dány k dispozici hodnoty výtěžnosti pro jednotlivé vnitřní standardy.
9.1.4 Protože se má při rozhodování o souladu vzorku přihlédnout také k nejistotě měření, je třeba poskytnout také tento parametr. Výsledek zkoušky se proto vydá ve tvaru „x +/– U“, kde x je výsledek zkoušky a U je rozšířená nejistota měření, přičemž se použije faktor pokrytí 2, který odpovídá hladině spolehlivosti přibližně 95 %. V případě samostatného stanovení PCDD/PCDF a PCB s dioxinovým efektem se pro součet PCDD/PCDF a PCB s dioxinovým efektem musí použít součet odhadované rozšířené nejistoty měření samostatných výsledků analýzy pro PCDD/PCDF a PCB s dioxinovým efektem.
9.1.5 Je-li nejistota měření zohledněna uplatněním rozhodovací meze (CCα) (jak je popsáno v bodě 2.2), tento parametr se uvede.
9.1.6 Výsledky se vyjádří ve stejných jednotkách a (alespoň) stejným počtem platných číslic, jako maximální obsahy stanovené ve směrnici 2002/32/ES.
9.2 Bioanalytické screeningové metody
9.2.1 Výsledek screeningu se vyjádří jako „vyhovující“ nebo „podezřelý jako nevyhovující“ („podezřelý“).
9.2.2 Kromě toho je možné vydat výsledek pro PCDD/PCDF a/nebo PCB s dioxinovým efektem vyjádřený v BEQ, nikoli TEQ.
9.2.3 Pokud je uvedena nejistota měření u vypočtené úrovně BEQ např. jako směrodatná odchylka, musí vycházet z nejméně trojnásobné analýzy vzorku, včetně extrakce, čištění a určení odezvy zkoušky.
9.2.4 Vzorky s odezvou nižší než oznamovací mez musí být vyjádřeny jako „nižší než oznamovací mez“.
9.2.5 Pro každý typ matrice vzorku musí zpráva uvádět sledovanou úroveň, z níž hodnocení vychází.
9.2.6 Zpráva musí uvádět použitý typ zkoušky, základní principy zkoušky a druh kalibrace.
9.2.7 Zpráva musí také zahrnovat metodu použitou pro extrakci PCDD/PCDF, PCB s dioxinovým efektem a lipidů.
KAPITOLA III
Příprava vzorků a požadavky na analytické metody používané při úřední kontrole obsahu PCB bez dioxinového efektu (PCB # 28, 52, 101, 138, 153, 180)
1. Použitelné metody detekce
Plynová chromatografie v tandemu s detektorem elektronového záchytu (GC/ECD), GC/LRMS, GC/MS-MS, GC/HRMS nebo rovnocenné metody.
2. Identifikace a konfirmace sledovaných analytů
2.1 Relativní retenční čas ve vztahu k vnitřním standardům nebo referenčním standardům (s přijatelnou odchylkou +/– 0,25 %).
2.2 Rozdělení všech šesti indikátorových PCB (PCB 28, PCB 52, PCB 101, PCB 138, PCB 153 a PCB 180) pomocí plynové chromatografie od interferujících látek, zejména současně se eluujících PCB, zvláště jsou-li úrovně vzorků v rozmezí limitů stanovených právními předpisy a případný nesoulad má být teprve potvrzen.
|
Poznámka: |
Mezi kongenery, u nichž je často zjištěno, že se eluují zároveň, patří např. PCB 28/31, PCB 52/69 a PCB 138/163/164. U GC/MS je rovněž nutné vzít v úvahu možné interference z fragmentů vyšších chlorovaných kongenerů. |
2.3 Požadavky na techniky GC/MS:
Sledování alespoň:
|
a) |
dvou specifických iontů u HRMS; |
|
b) |
dvou specifických iontů m/z > 200 nebo tří specifických iontů m/z > 100 u LRMS; |
|
c) |
1 prekurzorového a 2 produktových iontů u MS-MS. |
Nejvyšší přípustné tolerance intenzity vybraných hmotnostních fragmentů:
Relativní odchylka intenzity vybraných fragmentů od teoretické intenzity nebo kalibračního standardu pro cílový iont (nejintenzivnější sledovaný iont) a identifikační iont (ionty):
|
Relativní intenzita identifikačního iontu (iontů) v porovnání s cílovým iontem |
GC-EI-MS (relativní odchylka) |
GC-CI-MS, GC-MSn (relativní odchylka) |
|
> 50 % |
± 10 % |
± 20 % |
|
> 20 % až 50 % |
± 15 % |
± 25 % |
|
> 10 % až 20 % |
± 20 % |
± 30 % |
|
≤ 10 % |
± 50 % (12) |
± 50 % (12) |
2.4 Požadavky na techniky GC/ECD
Konfirmace výsledků překračujících toleranci s dvěma kolonami GC se stacionární fází jiné polarity.
3. Prokazování výkonnosti metody
Výkonnost metody se prokáže v rozsahu sledované úrovně (polovina až dvojnásobek sledované úrovně) s přijatelným variačním koeficientem pro opakovanou analýzu (viz požadavky na mezilehlou přesnost uvedené v bodě 8).
4. Mez kvantifikace
Hodnoty slepého stanovení nesmí být vyšší než 30 % úrovně kontaminace odpovídající maximální úrovni (13).
5. Kontrola kvality
Pravidelné slepé kontrolní vzorky, analýzy obohacených vzorků, vzorky pro kontrolu kvality, účast v mezilaboratorních studiích o příslušných matricích.
6. Kontrola výtěžnosti
6.1 Použijí se vhodné vnitřní standardy s fyzikálně-chemickými vlastnostmi porovnatelnými se sledovanými analyty.
6.2 Přidání vnitřních standardů:
Přidání k produktům (před extrakcí a čištěním).
6.3 Požadavky na metody s využitím všech šesti isotopicky značených indikátorových kongenerů:
|
a) |
korekce výsledků na výtěžnost vnitřních standardů; |
|
b) |
výtěžnost isotopicky značených vnitřních standardů má být mezi 50 a 120 %; |
|
c) |
nižší nebo vyšší výtěžnost jednotlivých kongenerů, které se na součtu všech šesti indikátorových PCB podílejí méně než 10 %, je přijatelná. |
6.4 Požadavky na metody, které nevyužívají všech šesti isotopicky značených vnitřních standardů nebo jiných vnitřních standardů:
|
a) |
výtěžnost vnitřních standardů se pro každý vzorek kontroluje; |
|
b) |
výtěžnost vnitřních standardů má být mezi 60 a 120 %; |
|
c) |
výsledky se opraví pro výtěžnost vnitřních standardů. |
6.5 Výtěžnost neoznačených kongenerů se ověří pomocí obohacených vzorků nebo vzorků pro kontrolu kvality s koncentracemi v rozsahu sledované úrovně. Výtěžnost těchto kongenerů se považuje za přijatelnou, pokud je mezi 70 a 120 %.
7. Požadavky na laboratoře
V souladu s nařízením (ES) č. 882/2004 musí být laboratoře akreditovány uznaným subjektem působícím v souladu s pokyny ISO Guide 58, aby bylo zaručeno, že uplatňují postupy zajištění analytické kvality. Laboratoře musí být akreditovány podle normy EN ISO/IEC 17025.
8. Kritéria výkonnosti: kritéria pro součet šesti indikátorových PCB na sledované úrovni
|
Pravdivost |
30 % až + 30 % |
|
Mezilehlá přesnost (% RSD) |
≤ 20 % |
|
Rozdíl mezi výpočtem horního a dolního odhadu |
≤ 20 % |
9. Vydávání výsledků
9.1 Pokud to analytický postup umožňuje, musí výsledky obsahovat hodnoty jednotlivých kongenerů PCB a vydávají se jako dolní, horní a střední odhad, aby se zahrnulo co nejvíce informací, a umožnil tak výklad podle příslušných zvláštních požadavků.
9.2 Protokol musí zahrnovat metodu použitou pro extrakci PCB a lipidů.
9.3 Pokud výtěžnost leží mimo rozpětí uvedené v bodě 6, je-li překročen maximální obsah nebo v ostatních případech na žádost, musí být dány k dispozici hodnoty výtěžnosti pro jednotlivé vnitřní standardy.
9.4 Protože se má při rozhodování o souladu vzorku přihlédnout také k nejistotě měření, je třeba poskytnout také tento parametr. Výsledky zkoušky se proto vydají ve tvaru „x +/– U“, kde x je výsledek zkoušky a U je rozšířená nejistota měření, přičemž se použije faktor pokrytí 2, který odpovídá hladině spolehlivosti přibližně 95 %.
9.5 Je-li nejistota měření zohledněna uplatněním rozhodovací meze (CCα) (jak je popsáno v bodě 2.1 kapitoly I), tento parametr se uvede.
9.6 Výsledky se vyjádří ve stejných jednotkách a (alespoň) se stejným počtem platných číslic jako maximální obsahy stanovené ve směrnici 2002/32/ES.“
(1) Tabulka koeficientů toxické ekvivalence (TEF) pro dioxiny, furany a PCB s dioxinovým efektem:
WHO-TEF (toxické ekvivalenční faktory Světové zdravotnické organizace) pro hodnocení nebezpečnosti pro člověka vycházející ze závěrů zasedání odborníků Světové zdravotnické organizace (WHO) - Mezinárodní program chemické bezpečnosti (IPCS), které se konalo v Ženevě v červnu 2005 (Martin Van den Berg et al., 2005. The 2005 World Health Organization Re-evaluation of Human and Mammalian Toxic Equivalency Factors for Dioxins and Dioxin-like Compounds. Toxicological Sciences 93(2), 223–241 (2006)).
|
Kongener |
Hodnota TEF |
|
Dibenzo-p-dioxiny („PCDD“) a dibenzofurany („PCDF“) |
|
|
2,3,7,8-TCDD |
1 |
|
1,2,3,7,8-PeCDD |
1 |
|
1,2,3,4,7,8-HxCDD |
0,1 |
|
1,2,3,6,7,8-HxCDD |
0,1 |
|
1,2,3,7,8,9-HxCDD |
0,1 |
|
1,2,3,4,6,7,8-HpCDD |
0,01 |
|
OCDD |
0,0003 |
|
|
|
|
2,3,7,8-TCDF |
0,1 |
|
1,2,3,7,8-PeCDF |
0,03 |
|
2,3,4,7,8-PeCDF |
0,3 |
|
1,2,3,4,7,8-HxCDF |
0,1 |
|
1,2,3,6,7,8-HxCDF |
0,1 |
|
1,2,3,7,8,9-HxCDF |
0,1 |
|
2,3,4,6,7,8-HxCDF |
0,1 |
|
1,2,3,4,6,7,8-HpCDF |
0,01 |
|
1,2,3,4,7,8,9-HpCDF |
0,01 |
|
OCDF |
0,0003 |
|
PCB „s dioxinovým efektem“ Non-orto PCB + Mono-orto PCB |
|
|
|
|
|
Non-orto PCB |
|
|
PCB 77 |
0,0001 |
|
PCB 81 |
0,0003 |
|
PCB 126 |
0,1 |
|
PCB 169 |
0,03 |
|
|
|
|
Mono-orto PCB |
|
|
PCB 105 |
0,00003 |
|
PCB 114 |
0,00003 |
|
PCB 118 |
0,00003 |
|
PCB 123 |
0,00003 |
|
PCB 156 |
0,00003 |
|
PCB 157 |
0,00003 |
|
PCB 167 |
0,00003 |
|
PCB 189 |
0,00003 |
|
|
|
|
|
|
|
Použité zkratky: „T“ = tetra; „Pe“ = penta; „Hx“ = hexa; „Hp“ = hepta; „O“ = okta; „CDD“ = chlordibenzo-p-dioxin; „CDF“ = chlordibenzofuran; „CB“ = chlorbifenyl. |
|
(2) Úř. věst. L 221, 17.8.2002, s. 8.
(3) Koncept „horního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru použití hodnoty meze kvantifikace. Koncept „dolního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru použití nulové hodnoty. Koncept „středního odhadu“ vyžaduje pro výpočet příspěvku každého nekvantifikovaného kongeneru použití poloviny hodnoty meze kvantifikace.
(4) Opakovaná zkouška je nutná k vyloučení možnosti vnitřní křížové kontaminace nebo náhodného promíchání vzorků. Vzhledem k nejistotě měření se pro ověření souladu použije první zkouška. Je-li zkouška prováděna v rámci kontaminační aféry, lze od konfirmace opakovanou zkouškou upustit, pokud lze zpětně vysledovat spojitost vzorků vybraných pro analýzu s danou kontaminační aférou.
(5) Koncept „horního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru použití hodnoty meze kvantifikace. Koncept „dolního odhadu“ vyžaduje pro příspěvek každého nekvantifikovaného kongeneru použití nulové hodnoty. Koncept „středního odhadu“ vyžaduje pro výpočet příspěvku každého nekvantifikovaného kongeneru použití poloviny hodnoty meze kvantifikace.
(6) Opakovaná zkouška je nutná k vyloučení možnosti vnitřní křížové kontaminace nebo náhodného promíchání vzorků. Vzhledem k nejistotě měření se pro ověření souladu použije první zkouška. Je-li zkouška prováděna v rámci kontaminační aféry, lze od konfirmace opakovanou zkouškou upustit, pokud lze zpětně vysledovat spojitost vzorků vybraných pro analýzu s danou kontaminační aférou.
(7) Totožné vysvětlení a požadavky na provedení opakované zkoušky pro kontrolu akčních prahů jako v poznámce pod čarou () pro maximální obsahy.
(8) Přizpůsobeno PCDD/PCDF a sloučeninám s dioxinovým efektem z „Pokynů pro validaci screeningových metod pro rezidua veterinárních léčivých přípravků“ referenčních laboratoří EU pro rezidua veterinárních léčivých přípravků a kontaminujících látek v potravinách živočišného původu ve Fougeres, Berlíně a Bilthovenu, 20.1.2010, http://ec.europa.eu/food/food/chemicalsafety/residues/lab_analysis_en.htm
(9) Bioanalytické metody nejsou specifické pro kongenery zahrnuté v systému TEF. V extraktu vzorku mohou být přítomny jiné strukturně příbuzné AhR-ativní sloučeniny, které přispívají k celkové reakci. Proto bioanalytické výsledky nelze považovat za odhad, ale spíše za orientační úroveň TEQ ve vzorku.
(10) s ohledem na maximální obsahy
(11) Současné požadavky vycházejí z TEF vydaného v: M. Van den Berg et al, Toxicol Sci 93 (2), 223–241 (2006).
(12) Je k dispozici dostatečný počet hmotnostních fragmentů s relativní intenzitou > 10 %, nedoporučuje se proto použít identifikační iont(y) s relativní intenzitou nižší než 10 % v porovnání s cílovým iontem.
(13) Velmi se doporučuje, aby hodnoty slepého stanovení činidla byly nižší než je obsah kontaminující látky ve vzorku. Je povinností laboratoře kontrolovat rozptyl hodnot slepých stanovení, zejména v případě, kdy se hodnoty slepého stanovení odečítají.



 je parametr sumy čtverců, i = index pro kalibrační bod i
je parametr sumy čtverců, i = index pro kalibrační bod i






