EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 31984L0539
Council Directive 84/539/EEC of 17 September 1984 on the approximation of the laws of the Member States relating to electro-medical equipment used in human or veterinary medicine
Директива на Съвета от 17 септември 1984 година за сближаване на законодателствата на държавите-членки относно използваното в хуманната и ветеринарна медицина електромедицинско оборудване
Директива на Съвета от 17 септември 1984 година за сближаване на законодателствата на държавите-членки относно използваното в хуманната и ветеринарна медицина електромедицинско оборудване
OJ L 300, 19.11.1984, p. 179–187
(DA, DE, EL, EN, FR, IT, NL)
Spanish special edition: Chapter 13 Volume 018 P. 133 - 141
Portuguese special edition: Chapter 13 Volume 018 P. 133 - 141
Special edition in Finnish: Chapter 13 Volume 014 P. 131 - 139
Special edition in Swedish: Chapter 13 Volume 014 P. 131 - 139
Special edition in Czech: Chapter 13 Volume 007 P. 272 - 280
Special edition in Estonian: Chapter 13 Volume 007 P. 272 - 280
Special edition in Latvian: Chapter 13 Volume 007 P. 272 - 280
Special edition in Lithuanian: Chapter 13 Volume 007 P. 272 - 280
Special edition in Hungarian Chapter 13 Volume 007 P. 272 - 280
Special edition in Maltese: Chapter 13 Volume 007 P. 272 - 280
Special edition in Polish: Chapter 13 Volume 007 P. 272 - 280
Special edition in Slovak: Chapter 13 Volume 007 P. 272 - 280
Special edition in Slovene: Chapter 13 Volume 007 P. 272 - 280
Special edition in Bulgarian: Chapter 13 Volume 006 P. 273 - 281
Special edition in Romanian: Chapter 13 Volume 006 P. 273 - 281
 No longer in force, Date of end of validity: 31/12/2008; отменен от 32008L0013
No longer in force, Date of end of validity: 31/12/2008; отменен от 32008L0013
- Date of document:
- 17/09/1984
- Date of effect:
- 26/09/1984; влизане в сила дата на оповестяване
- Date of notification:
- 26/09/1984
- Date of transposition:
- 26/09/1986; виж чл. 10
- Date of end of validity:
- 31/12/2008; отменен от 32008L0013
- Author:
- Съвет на Европейския съюз
- Responsible body:
- DG III – Industry, DG03/D/04
- Form:
- Директива
- Addressee:
- Десетте държави-членки: Белгия, Дания, Германия, Ирландия, Гърция, Франция, Италия, Люксембург, Нидерландия, Обединеното кралство
- Internal reference:
- COM/74/2178-01
- Additional information:
- разширяване на ЕИП от 21994A0103(01)
- Authentic language:
- датски, немски, гръцки, английски, френски, италиански, нидерландски, исландски, норвежки
- Procedure number:
- Co author:
- SJUR/X/00
- Treaty:
- Договор за създаване на Европейската икономическа общност
- Legal basis:
- Proposal:
- Link
- Link
- Link
- Select all documents mentioning this document No data available in the table
- Modified by:
-
Relation Act Comment Subdivision concerned From To Modified by 11985IN01/09/A поправка член 6.2 01/01/1986 Modified by 31993L0042 поправка заглавие Modified by 31993L0042 изпълнение член 2.1 Modified by 31993L0042 поправка член 1 Modified by 32003R0807 отменяне член 5.2 05/06/2003 Modified by 32003R0807 заместване член 6 05/06/2003 Repealed by 32008L0013 - Subsequent related instruments:
-
- Amendment proposed by 52001PC0789(04)
- Amendment proposed by 52007PC0465 отменяне, анулиране
- Affected by case:
-
- Proceedings concerning failure by Member States 61989CJ0310
- Instruments cited:
- Link
- EUROVOC descriptor:
- Subject matter:
- Directory code:
|
13/ 06 |
BG |
Официален вестник на Европейския съюз |
273 |
31984L0539
|
L 300/179 |
ОФИЦИАЛЕН ВЕСТНИК НА ЕВРОПЕЙСКИЯ СЪЮЗ |
ДИРЕКТИВА НА СЪВЕТА
от 17 септември 1984 година
за сближаване на законодателствата на държавите-членки относно използваното в хуманната и ветеринарна медицина електромедицинско оборудване
(84/539/ЕИО)
СЪВЕТЪТ НА ЕВРОПЕЙСКИТЕ ОБЩНОСТИ,
като взе предвид Договора за създаване на Европейската икономическа общност, и по-специално член 100 от него,
като взе предвид предложението на Комисията (1),
като взе предвид становището на Европейския парламент (2),
като взе предвид становището на Икономическия и социален комитет (3),
като има предвид, че във всяка държава-членка е необходимо да се постигне високо и ясно определено ниво на безопасност както при използването на електромедицинското оборудване в хуманната и ветеринарната медицина, така и при лечението с такова оборудване;
като има предвид, че много държави-членки се стремят да гарантират това ниво на безопасност чрез задължителни разпоредби, свързани с техническата безопасност и методите за контрол. Като има предвид, че тези разпоредби обаче се различават в отделните държави-членки;
като има предвид, че тези пречки пред установяването и безпрепятственото функциониране на общия пазар могат да бъдат намалени, дори премахнати, ако всички държави-членки приемат еднакви разпоредби в допълнение или на мястото на настоящото си законодателство;
като има предвид, че е целесъобразно в началото да бъде хармонизирано на общностно равнище една част от въпросното оборудване; като има предвид, че най-подходящият начин за това е да се вземат като основа за хармонизиране стандартите, изготвени от Европейския комитет по стандартизация в областта на електротехниката (Cenelec);
като има предвид, че производителят поема отговорност за съответствието на това оборудване с хармонизираните стандарти и го гарантира чрез поставяне на знак или чрез представяне на декларация за съответствие;
като има предвид, че техническият напредък изисква бързо привеждане в съответствие на разпоредбите в областта на техниката, които се съдържат съответно в директивите относно електромедицинското оборудване; като има предвид, че за да се улесни изпълнението на изискваните мерки, трябва да се създаде способ, който да предвижда тясно сътрудничество между държавите-членки и Комисията в рамките на Комитета за привеждане в съответствие с техническия прогрес на директивите за премахване на техническите пречки пред търговията с електромедицинско оборудване;
като има предвид, че би могло да се окаже, че определено електромедицинско оборудване застрашава сигурността или здравето на населението, въпреки че отговаря на изискванията на тези директиви; като има предвид следователно, че е целесъобразно да се предвиди процедура, която да способства за намаляване на тези рискове,
ПРИЕ НАСТОЯЩАТА ДИРЕКТИВА:
Член 1
Настоящата директива се отнася до посоченото в приложение II електромедицинско оборудване, наречено по-долу „оборудване“, което съгласно вида си е предназначено за използване в хуманната и ветеринарната медицина.
Член 2
1. Държавите-членки не могат да отказват, забраняват или ограничават продажбата, свободното движение или употребата, съответстваща на предназначението му, на посоченото в член 1 оборудване на основания, свързани с безопасността относно производството на модела, ако то отговаря на изискванията на настоящата директива.
Техническите предписания, на които трябва да отговаря оборудването, се съдържат в приложение I.
2. Съответствието на оборудването с изискванията на тази директива се удостоверява от производителя или вносителя на тяхна отговорност чрез поставянето на знак съгласно модела в приложение III или чрез подписване на декларация за съответствие съгласно модела в приложение IV.
Член 3
Държавите-членки гарантират, че осигуряват еднакви условия за заплащане на услугите, предоставени с помощта на оборудването, което отговаря на изискванията на тази директива, и на услугите, предоставени с помощта на оборудването, което отговаря на критериите, изискуеми съгласно разпоредбите в сила на тяхната територия по отношение на разрешените сфери на приложение и минималните изисквания за оборудване.
Член 4
Съгласно процедурата по член 6 се приемат следните изменения в приложение I:
|
— |
изменения, които са необходими вследствие на привеждане в съответствие с техническия прогрес на хармонизираните стандарти от съответния орган по стандартизация; |
|
— |
изменения, които са желателни вследствие на привеждане в съответствие с техническия прогрес, когато хармонизираният стандарт не е бил изменен от съответния орган по стандартизация. |
Във втория случай измененията се съобщават на компетентните органи по стандартизация.
Член 5
1. Учреден е комитет за привеждане в съответствие с техническия прогрес на директивите за премахване на техническите пречки пред търговията с електромедицинско оборудване, наречен по-долу „Комитет“, който е съставен от представители на държавите-членки и се председателства от представител на Комисията.
2. Комитетът изготвя свой процедурен правилник.
Член 6
1. Съгласно установената в този член процедура председателят внася въпроса пред комитета по своя инициатива или по искане на представител на държава-членка.
2. Представителят на Комисията изпраща на комитета проект във връзка с мерките, които трябва да се вземат. Комитетът дава становището си по този проект в определен срок, който председателят може да определи в зависимост от спешността на съответния въпрос. Становището се приема с мнозинство от 45 гласа, при което гласовете на държавите-членки се претеглят съгласно член 148, параграф 2 от Договора. Председателят не участва в гласуването.
|
3. |
|
Член 7
1. Ако някоя от държавите-членки установи въз основа на мотивирано потвърждение, че един или повече апарати, въпреки съответствието им с изискванията на настоящата директива, застрашават безопасността, то тогава тя може временно да забрани или да подчини на специални разпоредби продажбата, свободното движение или използването на този апарат или апарати на своята територия. Тя уведомява незабавно за това другите държави-членки и Комисията, като уточнява мотивите за това свое решение.
2. Комисията консултира в срок от 6 седмици заинтересованите държави-членки, след това незабавно представя своето становище и предприема необходимите мерки.
3. Ако Комисията е на мнение, че са необходими съответни технически промени на директивата, тези промени се правят или от Комисията, или от Съвета съгласно предвидената в член 6 процедура. В този случай държавата-членка, която е взела предпазни мерки, може да продължи действието им до влизането в сила на тези промени.
Член 8
1. Държавите-членки предприемат всички необходими мерки, за да може отличителният знак и декларацията за съответствие по смисъла на член 2 се изготвят от производителя или вносителя само при предвидените в директивата условия.
2. Държавите-членки предприемат всички необходими мерки, за да гарантират достатъчен контрол върху производството на оборудването.
Член 9
Държавите-членки предприемат всички подходящи мерки, за да предотвратят поставянето на знаци или надписи върху оборудването, които могат да бъдат объркани със знака на ЕИО, даден в приложение III.
Член 10
1. Държавите-членки въвеждат в сила необходимите разпоредби, за да се съобразят с настоящата директива в рамките на 24 месеца след нотификацията ѝ (4), и информират незабавно Комисията за това.
2. Държавите-членки съобщават на Комисията текстовете на разпоредбите от вътрешното законодателство, които приемат в областта, регулирана от настоящата директива.
Член 11
Адресати на настоящата директива са държавите-членки.
Съставено в Брюксел на 17 септември 1984 година.
За Съвета
Председател
P. BARRY
(1) ОВ С 33, 12.2.1975 г., стр. 5.
(2) ОВ С 76, 14.3.1975 г., стр. 37.
(3) ОВ С 233, 17.11.1975 г., стр. 39.
(4) Настоящата директива е нотифицирана на държавите-членки на 26 септември 1984 г.
ПРИЛОЖЕНИЕ I
Предвиденото в член 1 оборудване трябва да отговаря на следните технически предписания:
|
|
Документ за хармонизиране на Европейския комитет по стандартизация в областта на електротехниката (CENELEC) HD 395-1: Общи изисквания (издание 1979 – документ на базата на публикация IЕС № 601-1 на Международната електротехническа комисия). Този стандарт се прилага при условие че са направени следните изменения: |
Изискванията на HD 395-1 за оборудването, предвидено в приложение II, точка 2.2.1.1 се изменят както следва:
|
Точка 14.6, буква б): |
Оборудването е най-малко от тип BF; |
|
Точка 19.3: |
Спомагателен ток за пациенти: |
|
Нормални условия за работа — 1 mA |
|
|
Претоварване при обикновени условия — 5 mA. |
ПРИЛОЖЕНИЕ II
СПИСЪК НА ОБОРУДВАНЕТО, ПРЕДВИДЕНО В ЧЛЕН 1
1. ДИАГНОСТИЧНО ОБОРУДВАНЕ
(с изключение на оборудване с приспособление за защита срещу разреждане на дефибрилатори).
1.1. Оборудване за получаване на данни от живи организми, които са независими от външен източник.
1.1.1. Оборудване за определяне стойностите на биопотенциали.
1. Оборудване и принадлежности за диагноза или контролиране на изпитвания, или за контролиране на електрическата активност или електрическите характеристики на живи организми:
|
— |
електроенцефалографи и електрокортикографи, |
|
— |
електромиографи, |
|
— |
електроретинографи, |
|
— |
електронистагмографи. |
2. Оборудване и съответни принадлежности.
1.1.2. Оборудване за получаване на други параметри.
1. Оборудване и съответни принадлежности за изследване на инфрачервено лъчение от живи организми за диагностични цели:
|
— |
контактни топлинни датчици, |
|
— |
термографи, |
|
— |
термометри за излъчване. |
2. Оборудване и съответни принадлежности за изследване на акустичната активност или чувствителността на организмите:
|
— |
електронни стетоскопи; |
|
— |
фонокардиоскопи и фонокардиографи само в случаите, когато не са предвидени за интервенции в сърцето или кръвоносната система; |
|
— |
аудиометри, |
|
— |
аудиофони. |
3. Оборудване и съответни принадлежности:
|
— |
балистокардиографи, |
|
— |
електронни термометри само в случаите, когато са предвидени за интервенции в сърцето или кръвоносната система. |
1.2. Оборудване за получаване на данни от живи организми, зависещи от външен източник.
1.2.1. Оборудване, при което се използва електрически ток.
Оборудване и съответни принадлежности, при които се използва електрически ток непосредствено върху живия организъм:
|
— |
оборудване за измерване на електрическото съпротивление на кожата, |
|
— |
оборудване за импедансна реография на белите дробове или на кръвоносната система. |
1.2.2. Оборудване, при което се използва друг източник на енергия.
1. Оборудване и съответни принадлежности за офталмологична диагностика:
|
— |
оборудване за осветяване на очите: лампи с процеп, очни огледала, източници на спектрални линии, офталмоскопи, |
|
— |
оборудване за наблюдение, изобразяване и за измерване на окото: офталмометри, рефрактометри, тонометри, фотометри, ретиноскопи, корнеа-микроскопи, |
|
— |
офталмологични диагностични единици, които се състоят от посоченото офталмологично оборудване, комбинирано с необходимото помощно оборудване: стативи, стойки, столове. |
2. Оборудване и съответни принадлежности, които са предназначени да подобряват видимостта за диагностични цели чрез монокулярно или бинокулярно увеличаване, и които се използват за наблюдение при хирургически намеси (с изключение на високочестотно оборудване за хирургически цели):
|
— |
хирургически микроскопи, |
|
— |
колпоскопи, |
|
— |
отоскопи, |
|
— |
дерматоскопи. |
3. Оборудване и съответни принадлежности за локално осветяване на изследвани или лекувани области:
|
— |
лампи за глава, |
|
— |
осветително огледало за глава, |
|
— |
ръчни флуоресцентни лампи, |
|
— |
лампи за уста. |
2. ТЕРАПЕВТИЧНО ОБОРУДВАНЕ.
2.1. Специално терапевтично оборудване.
2.1.1. Оборудване, при което се използва електрическа енергия.
1. Оборудване и съответни принадлежности, които произвеждат електрически зареден или йонизиран въздух, пари или мъгла, при което може да се постигне зареждане или йонизация:
|
— |
чрез високо напрежение, |
|
— |
чрез електронна емисия от нагрят метал. |
2.1.2. Оборудване, при което се използват други видове енергии.
1. Оборудване и съответни принадлежности, които произвеждат определени механични ефекти в медицината:
|
— |
вибратори, |
|
— |
оборудване за масаж чрез водна струя, |
|
— |
оборудване за външен масаж на сърцето. |
2. Оборудване и съответни принадлежности, които произвеждат горещ въздух, пара или мъгла за терапевтични цели:
|
— |
оборудване, в което чрез нагряване или механично се изпаряват твърди или течни вещества с цел инхалации, |
|
— |
бани с горещ въздух. |
В тази точка не се включва ултразвуковото оборудване.
2.2. Електрохирургично оборудване.
2.2.1. Оборудване, при което се използва електрическа енергия.
1. Оборудване и съответни принадлежности, които използват нискочестотна електрическа енергия за произвеждане на топлина за електрокаутеризация:
|
— |
оборудване за електрокаутеризация, |
|
— |
части от комбинирано електромедицинско оборудване за електрокаутеризация. |
2.2.2. Оборудване, при което се използват други видове енергии.
1. Оборудване и принадлежности, които се използват за терапевтични цели в офталмологията:
|
— |
оборудване за лечение на очите, |
|
— |
магнити за очите. |
2. Оборудване и съответни принадлежности
3. Оборудване и съответни принадлежности, които произвеждат определени механични ефекти в медицината:
|
— |
бормашина (борапарат), триони, шлайфоборудване за зъболечение или в хирургията, |
|
— |
оборудване с водно задвижване. |
2.3. Оборудване за подпомагане или заместване на определени функции на тялото.
(С изключение на имплантирано оборудване за сърдечен ритъм и други имплантирани приспособления)
2.3.1. Оборудване за подпомагане или заместване чрез други средства.
1. Оборудване и съответни принадлежности за подпомагане или заместване на определени функции на тялото:
|
— |
изкуствени крайници, |
|
— |
приспособления за парализирани, |
|
— |
изкуствено говорно оборудване. |
2. Оборудване и съответни принадлежности за подпомагане на човешките зрителни органи:
|
— |
помощно оборудване за слепи. |
3. ДРУГИ ВИДОВЕ ОБОРУДВАНЕ:
Оборудване и съответни принадлежности за позициониране или движение на пациентите за хирургични или зъболекарски цели:
|
— |
операционни маси, |
|
— |
операционни столове, |
|
— |
операционни единици, |
|
— |
зъболекарски столове, |
|
— |
единици за зъболечение. |
ПРИЛОЖЕНИЕ III
МОДЕЛ НА ЗНАК ЗА СЪОТВЕТСТВИЕ, КОЙТО ТРЯБВА ДА СЕ ПОСТАВИ ОТ ПРОИЗВОДИТЕЛЯ
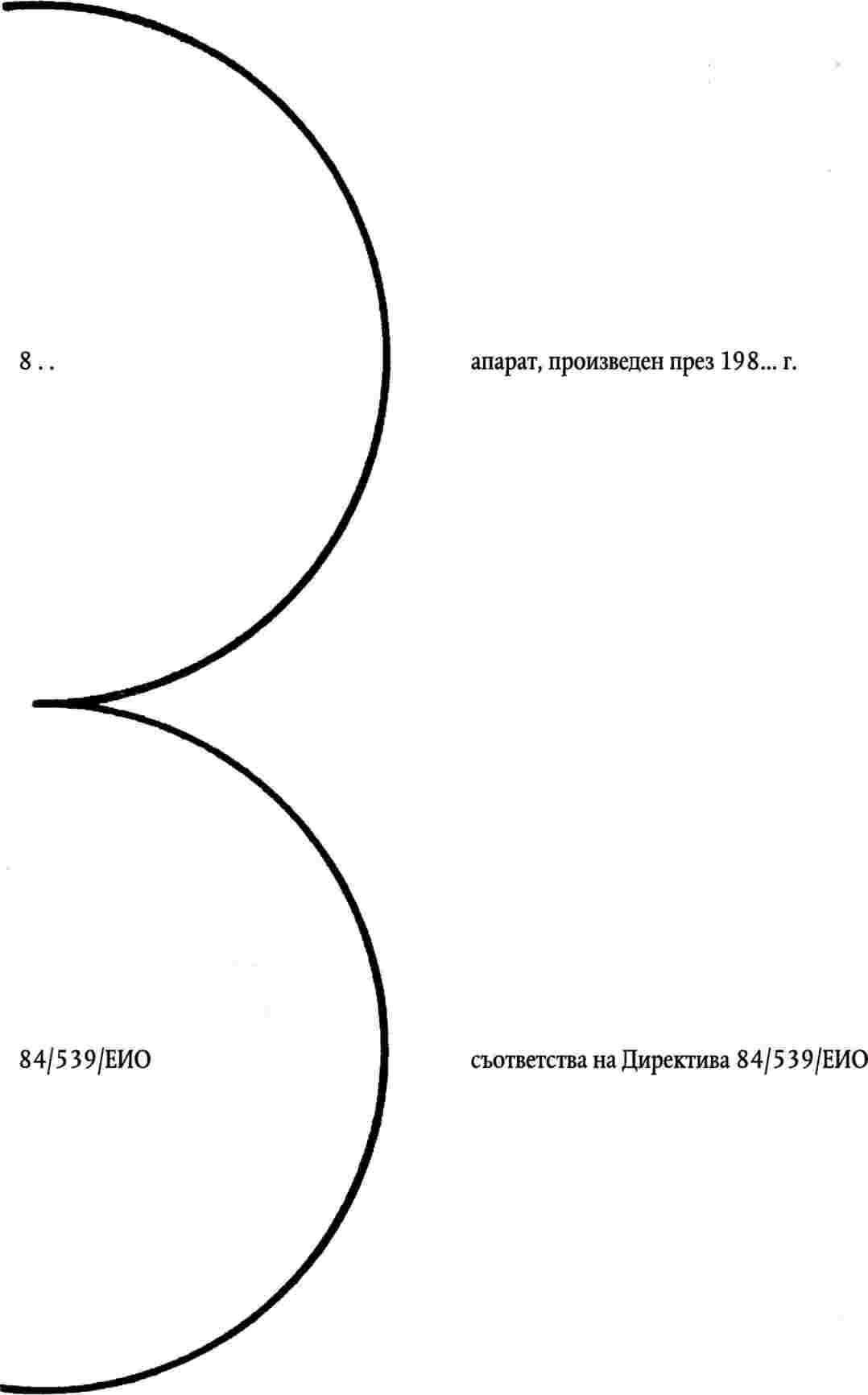
ПРИЛОЖЕНИЕ IV
МОДЕЛ НА ДЕКЛАРАЦИЯ ЗА СЪОТВЕТСТВИЕ
Прилагане съгласно Директива 84/539/ЕИО на Съвета от 17 септември 1984 г.

(Да се попълни и подпише от отговорен служител на посоченото в декларацията предприятие)








