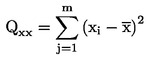EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32014R0709
Commission Regulation (EU) No 709/2014 of 20 June 2014 amending Regulation (EC) No 152/2009 as regards the determination of the levels of dioxins and polychlorinated biphenyls Text with EEA relevance
Nariadenie Komisie (EÚ) č. 709/2014 z 20. júna 2014 , ktorým sa mení nariadenie (ES) č. 152/2009, pokiaľ ide o stanovenie obsahu dioxínov a polychlórovaných bifenylov Text s významom pre EHP
Nariadenie Komisie (EÚ) č. 709/2014 z 20. júna 2014 , ktorým sa mení nariadenie (ES) č. 152/2009, pokiaľ ide o stanovenie obsahu dioxínov a polychlórovaných bifenylov Text s významom pre EHP
OJ L 188, 27.6.2014, p. 1–18
(BG, ES, CS, DA, DE, ET, EL, EN, FR, HR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
 In force
In force
|
27.6.2014 |
SK |
Úradný vestník Európskej únie |
L 188/1 |
NARIADENIE KOMISIE (EÚ) č. 709/2014
z 20. júna 2014,
ktorým sa mení nariadenie (ES) č. 152/2009, pokiaľ ide o stanovenie obsahu dioxínov a polychlórovaných bifenylov
(Text s významom pre EHP)
EURÓPSKA KOMISIA,
so zreteľom na Zmluvu o fungovaní Európskej únie,
so zreteľom na nariadenie Európskeho parlamentu a Rady (ES) č. 882/2004 z 29. apríla 2004 o úradných kontrolách uskutočňovaných s cieľom zabezpečiť overenie dodržiavania potravinového a krmivového práva a predpisov o zdraví zvierat a o starostlivosti o zvieratá (1), a najmä na jeho článok 11 ods. 4,
keďže:
|
(1) |
Nariadenie Komisie (ES) č. 152/2009 (2) obsahuje metódy stanovenia obsahu polychlórovaných dibenzo-p-dioxínov (PCDD), polychlórovaných dibenzofuránov (PCDF) a dioxínom podobných polychlórovaných bifenylov (PCB) v krmivách. |
|
(2) |
Mali by sa stanoviť požiadavky týkajúce sa vysoko výkonných skríningových metód na identifikáciu vzoriek s významným obsahom PCDD/F a dioxínom podobných PCB (prednostne by sa mali vyberať vzorky s prekročenými akčnými prahovými hodnotami a mal by byť zabezpečený výber vzoriek s prekročenými najvyššími prípustnými obsahmi). Pokiaľ ide o najvyššie prípustné obsahy, miera falošne vyhovujúcich výsledkov by mala byť v prípade uvedených skríningových metód pod 5 %. |
|
(3) |
Ak výsledky dosiahnuté skríningovou metódou prekračujú medznú hodnotu, pôvodná vzorka by sa mala analyzovať prostredníctvom metódy, ktorá umožnuje identifikáciu a stanovenie množstva PCDD/F a dioxínom podobných PCB vo vzorke. Takéto metódy sa ďalej uvádzajú ako „potvrdzujúce metódy“. Technický pokrok a vývoj ukázali, že okrem plynovej chromatografie/hmotnostnej spektrometrie s vysokým rozlíšením (GC-HRMS) by sa malo povoliť aj používanie plynovej chromatografie/tandemovej hmotnostnej spektrometrie (GC-MS/MS) ako potvrdzujúcej metódy na kontrolu dodržiavania najvyššieho prípustného obsahu. |
|
(4) |
Zo skúseností s uplatňovaním súčasných pravidiel vyplýva, že je vhodné zmeniť súčasné ustanovenia, pokiaľ ide o potrebu dvojnásobnej analýzy, stanovenie súladu v prípade dvojnásobnej analýzy a požiadavku o prijateľnom rozdiele medzi hornou a dolnou medzou výsledkov. |
|
(5) |
Nariadenie (ES) č. 152/2009 by sa preto malo zodpovedajúcim spôsobom zmeniť. |
|
(6) |
Opatrenia stanovené v tomto nariadení sú v súlade so stanoviskom Stáleho výboru pre potravinový reťazec a zdravie zvierat, |
PRIJALA TOTO NARIADENIE:
Článok 1
Časť B prílohy V k nariadeniu (ES) č. 152/2009 sa mení v súlade s prílohou k tomuto nariadeniu.
Článok 2
Toto nariadenie nadobúda účinnosť dvadsiatym dňom po jeho uverejnení v Úradnom vestníku Európskej únie.
Toto nariadenie je záväzné v celom rozsahu a priamo uplatniteľné vo všetkých členských štátoch.
V Bruseli 20. júna 2014
Za Komisiu
predseda
José Manuel BARROSO
(1) Ú. v. EÚ L 165, 30.4.2004, s. 1.
(2) Nariadenie Komisie (ES) č. 152/2009 z 27. januára 2009, ktorým sa stanovujú metódy odberu vzoriek a analýzy na účely úradných kontrol krmív (Ú. v. EÚ L 54, 26.2.2009, s. 1).
PRÍLOHA
V prílohe V k nariadeniu (ES) č. 152/2009 sa časť B „STANOVENIE OBSAHU DIOXÍNOV (PCDD/PCDF) A PCB“ nahrádza takto:
„B. STANOVENIE OBSAHU DIOXÍNOV (PCDD/PCDF) A PCB
KAPITOLA I
Metódy odberu vzoriek a interpretácia analytických výsledkov
1. Účel a rozsah
Vzorky určené na úradnú kontrolu obsahu polychlórovaných dibenzo-p-dioxínov (PCDD), polychlórovaných dibenzofuránov (PCDF) a dioxínom podobných polychlórovaných bifenylov (PCB) (1) a dioxínom nepodobných PCB v krmivách sa odoberajú v súlade s ustanoveniami v prílohe I. Uplatňujú sa kvantitatívne požiadavky ako na kontrolu látok alebo produktov rovnomerne rozložených v krmive uvedené v bode 5.1. prílohy I. Súhrnné vzorky, ktoré sa takto získajú, sa považujú za reprezentatívne pre šarže alebo podšarže, z ktorých sa odoberú. Dodržanie najvyšších prípustných obsahov stanovených v smernici 2002/32/ES sa zisťuje na základe obsahov stanovených v laboratórnych vzorkách.
Na účely tejto časti B sa uplatňuje vymedzenie pojmov stanovené v prílohe I k rozhodnutiu Komisie 2002/657/ES (2).
Okrem uvedeného vymedzenia pojmov sa na účely tejto časti B uplatňuje toto vymedzenie pojmov:
|
|
‚Skríningové metódy‘ sú metódy používané na výber vzoriek s obsahmi PCDD/F a dioxínom podobných PCB, ktoré prekračujú najvyššie prípustné obsahy alebo akčné prahové hodnoty. Tieto metódy umožňujú analyzovať vysoký počet vzoriek pri priaznivom pomere efektivity a nákladov, čím sa zvyšuje pravdepodobnosť zistenia nových prípadov vysokého vystavenia a zdravotných rizík pre spotrebiteľov. Skríningové metódy sú založené na bioanalytických metódach alebo metódach GC-MS. Výsledky vzoriek prekračujúcich medznú hodnotu na kontrolu súladu s najvyšším prípustným obsahom sa overujú opätovnou analýzou pôvodnej vzorky pomocou potvrdzujúcej metódy. |
|
|
‚Potvrdzujúce metódy‘ sú metódy, ktoré poskytujú úplné alebo doplňujúce informácie, na základe ktorých možno jednoznačne určiť a kvantifikovať PCDD/F a dioxínom podobné PCB na úrovni najvyššieho prípustného obsahu alebo, v prípade potreby, akčnej prahovej hodnoty. Pri týchto metódach sa využíva plynová chromatografia/hmotnostná spektrometria s vysokým rozlíšením (ďalej len ‚GC-HRMS‘) alebo plynová chromatografia/tandemová hmotnostná spektrometria (ďalej len ‚GC-MS/MS‘). |
2. Súlad šarže alebo podšarže s najvyšším prípustným obsahom
2.1. Pokiaľ ide o dioxínom nepodobné PCB
Šarža je v súlade s najvyšším prípustným obsahom, ak analytický výsledok nepresahuje najvyšší prípustný obsah dioxínom nepodobných PCB, stanovený v smernici 2002/32/ES, berúc do úvahy neistotu merania.
Šarža nie je v súlade s maximálnou hladinou, ak horná medza (3) analytického výsledku potvrdeného dvojnásobnou analýzou (4) presahuje maximálnu hladinu stanovenú v smernici 2002/32/ES, berúc do úvahy neistotu merania. Na overenie súladu sa použije stredná hodnota týchto dvoch stanovení s prihliadnutím na neistotu merania.
Neistota merania sa zohľadňuje podľa jedného z týchto postupov:
|
— |
výpočtom rozšírenej neistoty pomocou koeficientu pokrytia v hodnote 2, ktorý zabezpečuje približne 95 %-nú hladinu spoľahlivosti. Šarža alebo podšarža nie je v súlade, ak nameraná hodnota mínus U presahuje najvyšší prípustný obsah, |
|
— |
stanovením rozhodovacieho limitu (CCα) v súlade s bodom 3.1.2.5 prílohy I k rozhodnutiu 2002/657/ES. Šarža alebo podšarža nie je v súlade, ak sa nameraná hodnota rovná hodnote CCα alebo je vyššia. |
Odseky 1, 2 a 3 sa uplatňujú na výsledok analýzy vzorky určenej na úradnú kontrolu. V prípade analýzy na účely obhajoby alebo na referenčné účely sa uplatňujú pravidlá členského štátu.
2.2. Pokiaľ ide o PCDD/F a dioxínom podobné PCB
Šarža je v súlade s najvyššími prípustnými obsahmi, ak výsledok jednej analýzy
|
— |
vykonanej skríningovou metódou, ktorá má mieru falošne vyhovujúcich výsledkov pod 5 % indikuje, že príslušné najvyššie prípustné obsahy PCDD/PCDF a sumy PCDD/PCDF a dioxínom podobných PCB stanovené v smernici 2002/32/ES sa nepresahujú, |
|
— |
vykonanej potvrdzujúcou metódou nepresahuje príslušné najvyššie prípustné obsahy PCDD/PCDF a sumy PCDD/PCDF a dioxínom podobných PCB stanovené v smernici 2002/32/ES, s ohľadom na neistotu merania. |
V prípade skríningových testov sa stanovuje medzná hodnota pre rozhodnutia o súlade vzorky s príslušnými najvyššími prípustnými obsahmi stanovenými buď pre PCDD/PCDF, alebo pre sumu PCDD/PCDF a dioxínom podobných PCB.
Šarža nie je v súlade s najvyšším prípustným obsahom, ak horná medza (5) analytického výsledku získaného potvrdzujúcou metódou a potvrdeného dvojnásobnou analýzou presahuje najvyšší prípustný obsah stanovený v smernici 2002/32/ES, berúc do úvahy neistotu merania (6). Na overenie súladu sa použije stredná hodnota týchto dvoch stanovení s prihliadnutím na neistotu merania.
Neistota merania sa zohľadňuje podľa jedného z týchto postupov:
|
— |
výpočtom rozšírenej neistoty pomocou koeficientu pokrytia v hodnote 2, ktorý zabezpečuje približne 95 %-nú hladinu spoľahlivosti. Šarža alebo podšarža nie je v súlade, ak nameraná hodnota mínus U presahuje najvyšší prípustný obsah. V prípade oddeleného stanovovania PCDD/PCDF a dioxínom podobných PCB sa pre sumu PCDD/PCDF a dioxínom podobných PCB používa suma odhadovanej rozšírenej neistoty samostatných analytických výsledkov pre PCDD/PCDF a dioxínom podobné PCB, |
|
— |
stanovením rozhodovacieho limitu (CCα) v súlade s bodom 3.1.2.5 prílohy I k rozhodnutiu 2002/657/ES. Šarža alebo podšarža nie je v súlade, ak sa nameraná hodnota rovná hodnote CCα alebo je vyššia. |
Odseky 1 až 4 sa uplatňujú na výsledok analýzy vzorky určenej na úradnú kontrolu. V prípade analýzy na účely obhajoby alebo na referenčné účely sa uplatňujú pravidlá členského štátu.
3. Výsledky presahujúce akčné prahové hodnoty stanovené v prílohe II k smernici 2002/32/ES
Akčné prahové hodnoty slúžia ako nástroj na výber vzoriek v tých prípadoch, keď treba zistiť zdroj kontaminácie a prijať opatrenia na jej zníženie alebo eliminovanie. Pomocou skríningových metód sa stanovujú primerané medzné hodnoty na výber uvedených vzoriek. V prípade, že je potrebné vyvinúť značné úsilie na zistenie zdroja a zníženie alebo elimináciu kontaminácie, môže byť vhodné potvrdiť prekročenie akčnej prahovej hodnoty dvojnásobnou analýzou použitím potvrdzujúcej metódy zohľadňujúc neistotu merania (7).
KAPITOLA II
Príprava vzoriek a požiadavky na metódy analýzy, ktoré sa používajú pri úradnej kontrole obsahu dioxínov (PCDD/PCDF) a dioxínom podobných PCB v krmivách
1. Oblasť použitia
Požiadavky, ktoré sú stanovené v tejto kapitole, sa uplatňujú v prípadoch, keď sa vykonáva analýza krmív na úradnú kontrolu obsahu 2,3,7,8-substituovaných polychlórovaných dibenzo-p-dioxínov a polychlórovaných dibenzofuránov (PCDD/F) a dioxínom podobných polychlórovaných bifenylov (dioxínom podobných PCB) a na regulačné účely.
Monitorovanie prítomnosti PCDD/F a dioxínom podobných PCB v krmive sa môže vykonávať pomocou dvoch rozličných druhov analytických metód:
|
a) |
Skríningové metódy Cieľom skríningových metód je výber tých vzoriek, v ktorých obsah PCDD/F a dioxínom podobných PCB prekračuje najvyššie prípustné obsahy alebo akčné prahové hodnoty. Skríningové metódy by mali umožniť analýzu vysokého počtu vzoriek pri priaznivom pomere efektivity a nákladov, a zvýšiť tak pravdepodobnosť zistenia nových prípadov vysokej expozície a zdravotných rizík pre spotrebiteľov. Ich použitie by malo mať za cieľ predchádzať výsledkom vykazujúcim falošný súlad. Môžu zahŕňať bioanalytické metódy a metódy GC-MS. Skríningovými metódami sa porovnáva analytický výsledok s medznou hodnotou, na základe čoho sa určuje možné prekročenie/neprekročenie najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty. Koncentrácia PCDD/F a suma PCDD/F a dioxínom podobných PCB vo vzorkách, pri ktorých existuje podozrenie, že nie sú v súlade s najvyšším prípustným obsahom, sa musí stanoviť/potvrdiť potvrdzujúcou metódou. Skríningové metódy môžu navyše poskytnúť informáciu o obsahu PCDD/F a dioxínom podobných PCB prítomných vo vzorke. V prípade uplatňovania bioanalytických skríningových metód sa výsledok vyjadruje v bioanalytických ekvivalentoch (BEQ), zatiaľ čo v prípade uplatňovania fyzikálno-chemických metód GC-MS sa vyjadruje v toxických ekvivalentoch (TEQ). Číselné výsledky skríningových metód sú vhodné na preukázanie súladu, podozrenia na nesúlad alebo prekročenia akčných prahových hodnôt a poskytujú informáciu o rozsahu obsahu v prípade následného použitia potvrdzujúcich metód. Nie sú vhodné na hodnotenie obsahu pozadia, odhad príjmu, sledovanie dlhodobého trendu obsahov ani na prehodnotenie akčných prahových hodnôt a najvyšších prípustných obsahov. |
|
b) |
Potvrdzujúce metódy Potvrdzujúce metódy umožňujú jednoznačnú identifikáciu a kvantifikáciu PCDD/F a dioxínom podobných PCB prítomných vo vzorke a poskytujú úplné informácie o jednotlivých kongenéroch. Preto tieto metódy umožňujú kontrolu najvyšších prípustných obsahov a akčných prahových hodnôt vrátane potvrdenia výsledkov získaných skríningovými metódami. Okrem toho sa výsledky môžu použiť na iné účely, ako napríklad na stanovenie nízkych obsahov pozadia pri monitorovaní krmív, sledovanie dlhodobého trendu obsahov, posúdenie expozície obyvateľstva a vytváranie databázy na účely možného prehodnotenia akčných prahových hodnôt a najvyšších prípustných obsahov. Takisto sú dôležité z dôvodu stanovenia kongenérových profilov na účely identifikácie zdroja možnej kontaminácie. Pri týchto metódach sa používa GC-HRMS. Na potvrdenie súladu alebo nesúladu s najvyšším prípustným obsahom sa môže použiť aj metóda GC-MS/MS. |
2. Súvislosti
Pri výpočte koncentrácií toxických ekvivalentov (TEQ) sa vynásobia koncentrácie jednotlivých látok v predmetnej vzorke príslušným faktorom toxickej ekvivalencie (TEF) (pozri poznámku pod čiarou č. 1* v kapitole I), a následne sa spočítavajú, aby sa dospelo k celkovej koncentrácii dioxínom podobných zlúčenín, vyjadrenej v toxických ekvivalentoch (TEQ).
Na účely tejto časti B je akceptovaným špecifickým kvantifikačným limitom jednotlivého kongenéru najnižší obsah analytu, ktorý je možné merať s primeranou štatistickou istotou a ktorý spĺňa identifikačné kritériá opísané v medzinárodne uznávaných normách, napríklad v norme EN 16215:2012 (Krmivá pre zvieratá. Stanovenie dioxínov a dioxínom podobných PCB metódou GC-HRMS a indikátorových PCB metódou GC-HRMS) a/alebo v metódach EPA 1613 a 1668, v znení zmien.
Kvantifikačný limit jednotlivého kongenéru sa môže identifikovať ako:
|
a) |
koncentrácia analytu v extrakte vzorky, ktorá sa prejaví takou odozvou dvoch sledovaných rozličných iónov, pre ktorú platí pomer S/N (signál/šum) 3:1 pre signál menej intenzívneho iónu, alebo |
|
b) |
ak z technických príčin výpočet pomeru signál/šum neposkytuje spoľahlivé výsledky, najnižší koncentračný bod na kalibračnej krivke, ktorá poskytuje prijateľnú (≤ 30 %) a konzistentnú odchýlku (meranú aspoň na začiatku a konci analytickej série vzoriek) od priemerného relatívneho odozvového faktora vypočítaného pre všetky body kalibračnej krivky v každej sérii vzoriek. LOQ sa vypočíta z najnižšieho koncentračného bodu použitím výťažnosti vnútorných štandardov a množstva vzorky. |
Bioanalytické skríningové metódy neposkytujú výsledky na úrovni kongenéru, ale iba orientačné hodnoty (8) TEQ, vyjadrené v bioanalytických ekvivalentoch (ďalej len ‚BEQ‘), s prihliadnutím na skutočnosť, že nie všetky zložky prítomné v extrakte vzorky vykazujúcom pozitívny výsledok v teste zodpovedajú všetkým požiadavkám princípu TEQ.
Skríningové a potvrdzujúce metódy sa môžu použiť iba na kontrolu určitej matrice, ak príslušné metódy sú dostatočne citlivé na to, aby bola detekcia akčnej prahovej hodnoty alebo najvyššieho prípustného obsahu spoľahlivá.
3. Požiadavky na zabezpečenie kvality
3.1. Prijmú sa opatrenia, ktoré zabránia krížovej kontaminácii na každom stupni odberu vzoriek a procesov analýzy.
3.2. Vzorky sa skladujú a prepravujú v sklenených, hliníkových, polypropylénových alebo polyetylénových nádobách vhodných na skladovanie, ktoré nemajú žiadny vplyv na obsah PCDD/PCDF a dioxínom podobných PCB vo vzorkách. Z nádoby so vzorkami sa odstraňujú stopy po papierovom prachu.
3.3. Úschova a preprava vzorky sa vykonáva spôsobom, ktorý zabezpečí uchovanie integrity vzorky krmiva.
3.4. V prípade potreby sa každá laboratórna vzorka jemne zomelie a dôkladne premieša postupom, ktorý sa osvedčil na dosiahnutie dokonalej homogenizácie (napríklad vzorka sa zomelie tak, aby prešla okami sita s veľkosťou 1 mm). Ak je obsah vlhkosti vo vzorkách príliš vysoký, pred zomletím sa vysušia.
3.5. Vykonajú sa kontroly možného vplyvu reagentov, sklených pomôcok a vybavenia na výsledky založené na TEQ a BEQ.
3.6. Vykoná sa slepá skúška, a to uskutočnením celého postupu analýzy, pri ktorom sa vynechá iba vzorka.
3.7. Pokiaľ ide o bioanalytické metódy, testujú sa všetky sklené pomôcky a všetky rozpúšťadlá používané pri analýze, aby sa potvrdila neprítomnosť zlúčenín rušiacich detekciu cieľových zlúčenín v pracovnom rozsahu. Sklené pomôcky sa opláchnu rozpúšťadlami alebo zahrejú na teplotu vhodnú na odstránenie stôp PCDD/PCDF, dioxínom podobných zlúčenín a zlúčenín spôsobujúcich interferenciu z jeho povrchu.
3.8. Na extrakciu sa musí zvoliť také množstvo vzorky, aby sa splnili požiadavky dostatočne nízkeho pracovného rozsahu zahrňujúceho najvyššie prípustné obsahy alebo akčné prahové hodnoty.
3.9. Špecifické postupy prípravky vzoriek použité pri skúmaných produktoch spĺňajú medzinárodne prijaté usmernenia.
4. Požiadavky na laboratóriá
4.1. Akreditáciu laboratórií uskutočňuje v súlade s ustanoveniami nariadenia (ES) č. 882/2004 uznávaný orgán, ktorý pôsobí v súlade s pokynom ISO 58 s cieľom zaistiť, že laboratóriá zabezpečujú analytickú kvalitu. Akreditácia laboratórií sa uskutočňuje v súlade s normou EN ISO/IEC 17025.
4.2. Laboratórna spôsobilosť sa dokazuje nepretržitou úspešnou účasťou v medzilaboratórnych štúdiách na stanovenie PCDD/PCDF a dioxínom podobných PCB v príslušných krmivových matriciach a koncentračných rozsahoch.
4.3. Laboratóriá, ktoré používajú skríningové metódy na rutinnú kontrolu vzoriek, nadviažu úzku spoluprácu s laboratóriami, ktoré používajú potvrdzujúcu metódu, a to tak na účely kontroly kvality, ako aj na potvrdenie výsledku analýzy podozrivých vzoriek.
5. Základné požiadavky, ktoré má spĺňať analytický postup pre dioxíny (PCDD/PCDF) a dioxínom podobné PCB
5.1. Nízky pracovný rozsah a kvantifikačné limity
V prípade PCDD/PCDF sa stanoviteľné množstvá vzhľadom na mimoriadnu toxicitu niektorých z týchto zlúčenín musia nachádzať vo vyššom femtogramovom (10–15 g) rozpätí. V prípade väčšiny kongenérov PCB postačuje už kvantifikačný limit na úrovni nanogramov (10–9 g). Pri meraní toxickejších dioxínom podobných kongenérov PCB (predovšetkým non-orto-substituovaných kongenérov) musí nižšia hranica pracovného rozpätia dosiahnuť nízke pikogramové (10–12 g) obsahy. Pre všetky ostatné kongenéry PCB je kvantifikačný limit v rozsahu nanogramov (10–9g) dostatočný.
5.2. Vysoká selektívnosť (špecifickosť)
5.2.1. Žiada sa rozlíšenie PCDD/PCDF a dioxínom podobných PCB od množstva iných koextrahovaných a potenciálne interferujúcich zlúčenín prítomných v koncentráciách až niekoľkorádovo vyšších ako je koncentrácia skúmaných analytov. V prípade metód GC-MS je potrebné rozlišovať medzi rôznymi kongenérmi, ako napríklad medzi toxickými (napr. sedemnástimi 2,3,7,8-substituovanými PCDD/PCDF a dvanástimi dioxínom podobnými PCB) a ostatnými kongenérmi.
5.2.2. Pomocou bioanalytických metód je možná detekcia cieľových zlúčenín ako sumy PCDD/PCDF a/alebo dioxínom podobných PCB. Čistenie vzorky má za cieľ odstránenie zlúčenín spôsobujúcich výsledky vykazujúce falošný súlad alebo zlúčenín, ktoré môžu znížiť odozvu, čím spôsobujú výsledky vykazujúce falošný súlad.
5.3. Vysoká miera správnosti (pravdivosť výsledku merania a presnosť, zdanlivá výťažnosť biotestu)
5.3.1. V prípade metód GC-MS musí stanovenie poskytnúť právoplatný odhad skutočnej koncentrácie vo vzorke. Vyžaduje sa vysoká správnosť, aby sa predišlo odmietnutiu výsledku analýzy vzorky na základe nízkej spoľahlivosti stanoveného obsahu TEQ. Správnosť sa vyjadruje ako pravdivosť (rozdiel medzi nameranou priemernou hodnotou analytu v certifikovanom materiáli a jej certifikovanou hodnotou vyjadrenou ako percentuálny podiel tejto hodnoty) a presnosť (relatívna smerodajná odchýlka RSDR vypočítaná z výsledkov nameraných za podmienok reprodukovateľnosti).
5.3.2. V prípade bioanalytických metód sa stanovuje zdanlivá výťažnosť biotestu. Zdanlivá výťažnosť biotestu je hodnota BEQ vypočítaná z kalibračnej krivky TCDD alebo PCB 126 korigovaná na slepý pokus a následne vydelená hodnotou TEQ stanovenou pomocou potvrdzujúcej metódy. Jej cieľom je korekcia faktorov, ako sú strata PCDD/PCDF a dioxínom podobných zlúčenín počas extrakcie a procesu čistenia, spoluextrahované zlúčeniny zvyšujúce alebo znižujúce odpoveď (agonistické a antagonistické účinky), kvalita preloženia krivkou alebo rozdiely medzi hodnotami TEF a REP (relatívnej účinnosti, Relative Potency). Zdanlivá výťažnosť biotestu sa vypočíta z vhodných referenčných vzoriek s reprezentatívnym kongenérovým profilom v oblasti príslušných sledovaných obsahov.
5.4. Validácia v rozsahu najvyššieho prípustného obsahu a všeobecné opatrenia na kontrolu kvality
5.4.1. Laboratóriá musia počas validačného postupu a rutinnej analýzy preukázať účinnosť metódy v rozsahu najvyššieho prípustného obsahu, napríklad na úrovni 0,5–násobku, 1–násobku a 2–násobku najvyššieho prípustného obsahu s prijateľným variačným koeficientom pre opakovanú analýzu.
5.4.2. Pravidelné slepé kontroly a pokusy na vzorkách s prídavkom analytu alebo analýza kontrolných vzoriek (ak je to možné, tak najlepšie certifikovaného referenčného materiálu) sa vykonávajú v rámci vnútorných opatrení kontroly kvality. Vyhotovia a overia sa tabuľky kontroly kvality zo slepých kontrol, z pokusov na vzorkách s prídavkom analytu alebo analýz kontrolných vzoriek s cieľom zabezpečiť, aby bolo vykonanie analýzy v súlade s požiadavkami.
5.5. Kvantifikačný limit
5.5.1. Pri bioanalytickej skríningovej metóde nie je stanovenie kvantifikačného limitu (limit of quantification, ďalej len ‚LOQ‘) nevyhnutnou požiadavkou, ale pomocou tejto metódy musí byť možné rozlišovať medzi slepou a medznou hodnotou. Pri stanovovaní BEQ sa stanovuje medza oznamovania pre nakladanie so vzorkami vykazujúcimi odozvu pod touto hodnotou. Musí sa preukázať, že príslušná medza oznamovania sa aspoň trojnásobne odlišuje od slepých vzoriek použitých pri postupe, ktoré vykazujú odozvu pod pracovným rozsahom. Vypočíta sa preto zo vzoriek obsahujúcich cieľové zlúčeniny v koncentrácii približujúcej sa požadovanej minimálnej hladine, a nie na základe pomeru signál-šum (S/N) alebo testu naslepo.
5.5.2. LOQ pre potvrdzujúcu metódu musí byť približne jedna pätina najvyššieho prípustného obsahu.
5.6. Analytické kritériá
V záujme dosiahnutia spoľahlivých výsledkov pomocou potvrdzujúcich alebo skríningových metód je nutné splniť tieto kritériá v rozsahu najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty, pokiaľ ide o hodnotu TEQ a BEQ, či už stanovenú ako celkový TEQ (ako suma PCDD/PCDF a dioxínom podobných PCB), alebo samostatne pre PCDD/PCDFF a dioxínom podobné PCB:
|
|
Skríning pomocou bioanalytických alebo fyzikálno-chemických metód |
Konfirmačné metódy |
|
Miera výskytu meraní vykazujúcich falošný súlad (9) |
< 5 % |
|
|
Pravdivosť |
|
– 20 % až +20 % |
|
Opakovateľnosť (RSDr) |
< 20 % |
|
|
Vnútrolaboratórna opakovateľnosť (RSDR) |
< 25 % |
< 15 % |
5.7. Špecifické požiadavky na skríningové metódy
5.7.1. Pri skríningu je možné použiť metódy GC-MS, ako aj bioanalytické metódy. V prípade metód GC-MS musia byť splnené požiadavky stanovené v bode 6. Špecifické požiadavky na bunkové bioanalytické metódy sú stanovené v bode 7.
5.7.2. Laboratóriá používajúce skríningové metódy na rutinnú kontrolu vzoriek nadväzujú úzku spoluprácu s laboratóriami používajúcimi potvrdzujúcu metódu.
5.7.3. Overenie výkonnosti skríningovej metódy sa požaduje počas rutinnej analýzy kontrolou kvality analýzy a priebežnou validáciou metódy. Musí fungovať nepretržitý program kontroly výsledkov vykazujúcich súlad.
5.7.4. Kontrola možnej supresie bunkovej odozvy a cytotoxicity:
Uskutoční sa meraním 20 % extraktov vzoriek rutinným skríningom bez pridania a s pridaním 2,3,7,8-tetrachlórdibenzo-p-dioxínu v množstve zodpovedajúcom najvyššiemu prípustnému obsahu alebo akčnej prahovej hodnote s cieľom zistiť, či môže byť odozva potenciálne potlačená z dôvodu interferujúcich látok prítomných v extrakte vzorky. Meraná koncentrácia vzorky s pridanými analytmi sa porovnáva so sumou koncentrácie extraktu bez pridaných analytov a koncentrácie pridaného analytu. Ak je táto meraná koncentrácia nižšia o viac ako 25 % ako vypočítaná (sčítaná) koncentrácia, je to indikácia možného potlačenia (supresie) signálu a príslušná vzorka sa predkladá na potvrdzujúcu analýzu GC-HRMS. Výsledky sa monitorujú pomocou diagramov kontroly kvality.
5.7.5. Kontrola kvality vzoriek vykazujúcich súlad:
Približne 2 až 10 % vzoriek vykazujúcich súlad (v závislosti od vzorkovej matrice a laboratórnych skúseností) sa potvrdzuje analýzou GC-HRMS.
5.7.6. Stanovenie miery výskytu meraní vykazujúcich falošný súlad na základe údajov získaných v rámci kontroly kvality:
Stanovuje sa miera výskytu výsledkov vykazujúcich falošný súlad pri skríningu vzoriek pod a nad najvyšším prípustným obsahom alebo akčnou prahovou hodnotou. Skutočná miera výskytu meraní vykazujúcich falošný súlad musí byť nižšia ako 5 %. Ak sa získa aspoň 20 potvrdených výsledkov na matricu/skupinu matríc z kontroly kvality vzoriek vykazujúcich súlad, na základe tohto súboru údajov sa vyvodzujú závery o miere výskytu meraní vykazujúcich falošný súlad. Výsledky zo vzoriek analyzovaných v kruhových testoch alebo v prípadoch kontaminácie, ktoré sa nachádzajú v koncentračnom rozpätí až do napríklad dvojnásobku najvyššieho prípustného obsahu, môžu byť takisto zahrnuté medzi príslušné minimálne množstvo 20 výsledkov pre vyhodnocovanie miery výskytu meraní vykazujúcich falošný súlad. Vzorky musia pokryť najčastejšie kongenérové profily a reprezentovať rozličné zdroje.
Hoci skríningové testy majú v prvom rade za cieľ detekciu vzoriek prekračujúcich akčnú prahovú hodnotu, kritérium pre stanovenie miery výskytu meraní vykazujúcich falošný súlad je najvyšší prípustný obsah maximálna hladina, berúc do úvahy neistotu merania potvrdzujúcej metódy.
5.7.7. Vzorky potenciálne vykazujúce nesúlad pri skríningu sa vždy overujú úplnou opätovnou analýzou pôvodnej vzorky potvrdzujúcou metódou analýzy. Tieto vzorky sa môžu takisto použiť na hodnotenie miery výskytu výsledkov vykazujúcich falošný nesúlad. V prípade skríningových metód je mierou výskytu výsledkov vykazujúcich falošný nesúlad časť výsledkov, v prípade ktorých sa potvrdzujúcou analýzou potvrdil súlad, hoci vzorka bola na základe predchádzajúceho skríningu označená za vzorku, ktorá potenciálne vykazuje nesúlad. Vyhodnotenie výhodnosti skríningovej metódy sa zakladá na porovnaní vzoriek vykazujúcich falošný nesúlad s celkovým počtom skontrolovaných vzoriek. Táto miera musí byť dostatočne nízka nato, aby bolo možné považovať nástroj skríningu za výhodný.
5.7.8. Bioanalytické metódy poskytujú aspoň v podmienkach validácie platnú indikáciu hodnoty TEQ, vypočítanej a vyjadrenej ako BEQ.
Takisto v prípade bioanalytických metód vykonaných za podmienok opakovateľnosti by mala byť vnútrolaboratórna RSDr menšia ako RSDR (reprodukovateľnosť).
6. Špecifické požiadavky na metódy GC-MS, ktoré je potrebné splniť na účely skríningu a potvrdzovania
6.1. Prijateľné rozdiely medzi hornou a dolnou medzou výsledkov WHO-TEQ
Rozdiel medzi hornou a dolnou medzou nesmie presiahnuť 20 % na potvrdenie prekročenia najvyššieho prípustného obsahu alebo v prípade potreby akčných prahových hodnôt.
6.2. Kontrola výťažností
6.2.1. Na účely validácie analytického postupu sa musia na úplnom začiatku analytickej metódy, napr. pred extrakciou, pridať 13C-označené 2,3,7,8-chlórsubstituované vnútorné štandardy PCDD/PCDF a 13C-označené vnútorné štandardy dioxínom podobných PCB. Pre každú tetra- až okta-chlórovanú homológovanú skupinu PCDD/PCDF sa pridáva aspoň jeden kongenér a aspoň jeden kongenér pre každú homológovú skupinu dioxínom podobných PCB (prípadne aspoň jeden kongenér pre každý sledovaný hmotnostno-spektrometrický ión použitý na monitorovanie PCDD/PCDF a dioxínom podobných PCB). V prípade potvrdzujúcich metód je potrebné použiť všetkých 17 13C-označených 2,3,7,8-substituovaných vnútorných štandardov PCDD/PCDF a všetkých 12 13C-označených vnútorných štandardov dioxínom podobných PCB.
6.2.2. Použitím vhodných kalibračných roztokov sa stanovujú relatívne odozvové faktory aj pre tie kongenéry, pre ktoré nebol pridaný 13C-označený ekvivalent.
6.2.3. Ak ide o krmivá rastlinného pôvodu a krmivá živočíšneho pôvodu, ktoré obsahujú menej ako 10 % tuku, potom sa vnútorné štandardy pridávajú povinne pred extrakciou. V prípade krmív živočíšneho pôvodu obsahujúcich viac ako 10 % tuku sa vnútorné štandardy pridávajú pred extrakciou tuku alebo po nej. V závislosti od toho, v ktorej fáze sa pridávajú vnútorné štandardy a či sa výsledky uvádzajú na produkt alebo na tuk, sa vykoná vhodná validácia účinnosti extrakcie.
6.2.4. Pred analýzou pomocou GC-MS sa musia pridať 1 alebo 2 (náhradné) štandardy.
6.2.5. Vyžaduje sa kontrola výťažnosti. Výťažnosti jednotlivých vnútorných štandardov by sa mali v prípade potvrdzujúcich metód pohybovať v rozsahu 60 až 120 %. Vyššie alebo nižšie výťažnosti pre jednotlivé kongenéry, najmä pre niektoré hepta- a okta- chlórované dibenzo-p-dioxíny a dibenzofurány, sú prijateľné za podmienky, že ich podiel na hodnote TEQ neprekročí 10 % z celkovej hodnoty TEQ (vyjadrenej ako suma PCDD/PCDF a dioxínom podobných PCB). Pri skríningových metódach GC-MS sa musia výťažnosti pohybovať v rozpätí 30 až 140 %.
6.3. Odstránenie interferujúcich látok
|
— |
Separácia PCDD/PCDF od interferujúcich chlórovaných zlúčenín, ako sú dioxínom nepodobné PCB a chlórované difenylétery, sa vykonáva vhodnými chromatografickými postupmi (pokiaľ možno na kolóne s florisilom, oxidom hlinitým a/alebo aktívnym uhlím). |
|
— |
Separácia izomérov plynovou chromatografiou má byť < 25 % údolie medzi pikmi 1,2,3,4,7,8-HxCDF a 1,2,3,6,7,8-HxCDF. |
6.4. Kalibrácia na základe štandardnej krivky
Rozsah kalibračnej krivky musí pokrývať príslušnú oblasť najvyššieho prípustného obsahu alebo akčných prahových hodnôt.
6.5. Špecifické kritériá pre potvrdzujúce metódy
|
— |
Pre GC-HRMS:
|
|
— |
Pre GC-MS/MS:
|
7. Špecifické požiadavky na bioanalytické metódy
Bioanalytické metódy sú metódy založené na využívaní biologických princípov, ako sú bunkové testy, receptorové testy alebo imunologické testy. V tomto bode 7 sú stanovené požiadavky na bioanalytické metódy ako také.
Skríningová metóda klasifikuje v princípe vzorku ako vzorku, ktorá vykazuje súlad, alebo ako vzorku, v prípade ktorej existuje podozrenie na nesúlad. Na tieto účely sa vypočítaná hodnota BEQ porovná s medznou hodnotou (pozri bod 7.3). Vzorky pod medznou hodnotou sa vyhlásia za vzorky vykazujúce súlad, vzorky rovnajúce sa medznej hodnote alebo nad ňou sú vzorky, v prípade ktorých existuje podozrenie na nesúlad, a teda si vyžadujú analýzu pomocou potvrdzujúcej metódy. Hodnota BEQ zodpovedajúca 2/3 najvyššieho prípustného obsahu môže v praxi poslúžiť ako medzná hodnota, pokiaľ je zabezpečené, že miera výskytu meraní vykazujúcich falošný súlad je nižšia ako 5 % a miera výskytu výsledkov vykazujúcich falošný nesúlad je známa. Pri použití samostatných najvyšších prípustných obsahov pre PCDD/F a pre sumu PCDD/F a dioxínom podobných PCB si overenie súladu vzoriek bez frakcionácie vyžaduje vhodné medzné hodnoty pre biologické testy na PCDD/F. Na kontrolu vzoriek prekračujúcich akčné prahové hodnoty by bolo vhodné použiť ako medznú hodnotu primerané percento príslušnej akčnej prahovej hodnoty.
Okrem toho sa v prípade určitých bioanalytických metód môže pri vzorkách v pracovnom rozsahu, ktoré prekračujú medzu oznamovania (pozri 7.1.1 a 7.1.6), použiť indikatívna hodnota vyjadrená v BEQ.
7.1. Hodnotenie odozvy testu
7.1.1. Všeobecné požiadavky
|
— |
Pri výpočte koncentrácií z kalibračnej krivky TCDD vykážu dolné a horné medzné hodnoty krivky veľkú odchýlku (vysoký variačný koeficient – CV). Pracovný rozsah je oblasť, v ktorej je CV menší ako 15 %. Dolná hranica pracovného rozsahu (medza oznamovania) musí byť najmenej trojnásobne vyššia ako slepé vzorky. Hornú medzu pracovného rozsahu obvykle predstavuje hodnota EC70 (70 % maximálnej účinnej koncentrácie), ale je nižšia, ak je CV vyšší ako 15 % v tomto rozsahu. Pracovný rozsah sa stanovuje pri validácii. Medzné hodnoty (pozri bod 7.3) musia byť jasne v rámci pracovného rozsahu. |
|
— |
Štandardné roztoky a vzorkové extrakty sa testujú aspoň dvakrát. Odozva alebo koncentrácia štandardných roztokov alebo kontrolných extraktov pri dvojitom testovaní v 4 až 6 jamkách rozložených na platni by mala mať CV < 15 % (možnej len v rámci pracovného rozsahu). |
7.1.2. Kalibrácia
7.1.2.1. Kalibrácia na základe štandardnej krivky
|
— |
Odhad obsahov vo vzorkách sa vykonáva na základe porovnania odozvy testu s kalibračnou krivkou TCDD (alebo PCB 126 alebo štandardnej zmesi PCDD/PCDF/dioxínom podobných PCB) s cieľom vypočítať hodnotu BEQ v extrakte a následne vo vzorke. |
|
— |
Kalibračné krivky obsahujú 8 až 12 koncentrácií (aspoň dvojmo) s dostatočným počtom koncentrácií v nižšej časti krivky (pracovnom rozsahu). Osobitnú pozornosť treba venovať kvalite preloženia krivky v pracovnom rozsahu. Ako taká má hodnota R2 malú alebo žiadnu hodnotu pre odhad správnosti preloženia pri nelineárnej regresii. Lepšie preloženie krivky sa dosiahne minimalizáciou rozdielu medzi vypočítanými a pozorovanými hladinami v pracovnom rozsahu krivky, napríklad metódou najmenších štvorcov. |
|
— |
Pri odhade obsahu v extrakte vzorky sa následne vykoná korekcia na hodnotu BEQ vypočítanú pre slepú vzorku matrice/rozpúšťadla (aby sa zohľadnili nečistoty pochádzajúce z použitých rozpúšťadiel a chemikálií) a zdanlivú výťažnosť (vypočítanú z hodnoty BEQ vhodných referenčných vzoriek s reprezentatívnymi kongenérovými profilmi v oblasti najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty). Na vykonanie korekcie výťažnosti musí byť zdanlivá výťažnosť vždy v požadovanom rozsahu (pozri bod 7.1.4). Referenčné vzorky použité na korekciu výťažnosti musia byť v súlade s požiadavkami uvedenými v bode 7.2. |
7.1.2.2. Kalibrácia pomocou referenčných vzoriek
Alternatívne sa môže použiť kalibračná krivka zostrojená z aspoň štyroch referenčných vzoriek (pozri bod 7.2.4: jedna slepá matrica plus tri referenčné vzorky s 0,5-, 1,0- a 2,0-násobkom najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty), pričom nie je potrebné vykonať korekciu na slepú vzorku a výťažnosť. V tomto prípade môže byť odozva testu zodpovedajúca 2/3 najvyššieho prípustného obsahu (pozri bod 7.3) vypočítaná priamo z týchto vzoriek a použitá ako medzná hodnota. Na kontrolu vzoriek prekračujúcich akčné prahové hodnoty by ako medznú hodnotu bolo vhodné použiť primeraný percentuálny podiel z týchto akčných prahových hodnôt.
7.1.3. Oddelené stanovovanie PCDD/PCDF a dioxínom podobných PCB
Extrakty sa môžu rozdeliť do frakcií obsahujúcich PCDD/PCDF a diocínom podobné PCB, čím sa umožní samostatné stanovenie hodnôt TEQ (v BEQ) pre PCDD/PCDF a dioxínom podobné PCB. Na hodnotenie výsledkov pre frakciu obsahujúcu dioxínom podobné PCB sa prednostne používa štandardná kalibračná krivka PCB 126.
7.1.4. Zdanlivé výťažnosti biotestu
‚Zdanlivá výťažnosť biotestu‘ sa vypočítava z vhodných referenčných vzoriek s reprezentatívnymi kongenérovými profilmi v oblasti najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty a vyjadruje sa ako percentuálny podiel hodnoty BEQ v porovnaní s hodnotou TEQ. V závislosti od použitého typu testu a použitej schémy TEF (10) môžu rozdiely medzi faktormi TEF a REP pre dioxínom podobné PCB spôsobovať nízke zdanlivé výťažnosti pre dioxínom podobné PCB v porovnaní s PCDD/PCDF. Preto v prípade oddeleného stanovovania PCDD/PCDF a dioxínom podobných PCB sú zdanlivé výťažnosti biotestu: pre dioxínom podobné PCB na úrovni 20 až 60 %, pre PCDD/PCDF 50 až 130 % (rozsahy sa uplatňujú pri použití kalibračnej krivky TCDD). Keďže podiel dioxínom podobných PCB na sume PCDD/PCDF a dioxínom podobných PCB môže byť rôzny v prípade rôznych matríc a vzoriek, zdanlivé výťažnosti biotestu pre sumu PCDD/PCDF a dioxínom podobných PCB odzrkadľujú tieto rozsahy a nachádzajú sa medzi 30 a 130 %. Akýkoľvek vplyv do značnej miery zrevidovaných hodnôt TEF pre právne predpisy Únie týkajúce sa PCDD/PCDF a dioxínom podobných PCB si vyžaduje revíziu týchto rozsahov.
7.1.5. Kontrola výťažností čistenia
Pri validácii sa kontroluje strata zlúčenín, ku ktorej došlo pri čistení. Slepá vzorka s prídavkom zmesi rozličných kongenérov sa podrobuje čisteniu (aspoň n = 3) a pomocou potvrdzujúcej metódy sa overuje výťažnosť a variabilita. Výťažnosť sa musí nachádzať v rozpätí 60 až 120 % predovšetkým v prípade kongenérov s podielom na hodnote TEQ v rozličných zmesiach vyšším ako 10 %.
7.1.6. Medza oznamovania
Pri uvádzaní hodnôt BEQ sa medza oznamovania stanovuje z príslušných vzoriek matríc vykazujúcich typické kongenérové profily, nie však z kalibračnej krivky štandardov vzhľadom na malú presnosť v nižšej oblasti krivky. Musia sa zohľadniť účinky extrakcie a čistenia. Medza oznamovania musí byť stanovená aspoň trojnásobne nad slepými vzorkami.
7.2. Používanie referenčných vzoriek
7.2.1. Referenčné vzorky predstavujú vzorkovú matricu, kongenérové profily a koncentračné rozsahy pre PCDD/PCDF a dioxínom podobné PCB v oblasti najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty.
7.2.2. Do každej testovacej série sa zahrnie slepá matrica, alebo ak to nie je možné, slepá vzorka, ako aj referenčná vzorka vykazujúca najvyšší prípustný obsah alebo akčnú prahovú hodnotu. Tieto vzorky sa extrahujú a testujú súčasne a pri identických podmienkach. Referenčná vzorka musí vykázať zreteľne silnejšiu reakciu v porovnaní so slepou vzorkou, čím sa zabezpečí vhodnosť príslušného testu. Tieto vzorky sa môžu použiť na korekciu slepých vzoriek a výťažnosti.
7.2.3. Referenčné vzorky vybrané na korekciu výťažnosti musia byť reprezentatívne pre testovacie vzorky, čiže kongenérové profily nesmú viesť k podhodnoteniu obsahov.
7.2.4. Na preukázanie správnej funkcie testu v skúmanom rozsahu sa na kontrolu najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty môžu použiť dodatočné referenčné vzorky vykazujúce napr. 0,5- a 2,00-násobok najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty. Kombinácia týchto vzoriek môže poslúžiť na výpočet hodnôt BEQ v testovacích vzorkách (pozri bod 7.1.2.2).
7.3. Stanovenie medzných hodnôt
Stanovuje sa pomer medzi bioanalytickými výsledkami v BEQ a výsledkami potvrdzujúcej metódy v TEQ, napríklad pomocou kalibračných experimentov zohľadňujúc príslušnú matricu, pri použití referenčných vzoriek s prídavkom analytov v množstve 0-, 0,5-, 1,00- a 2,00-násobku najvyššieho prípustného obsahu (ML), so 6 opakovaniami pri každom obsahu (n = 24). Korekčné faktory (slepý pokus a výťažnosť) možno z tohto vzťahu odhadnúť, skontrolujú sa však podľa bodu 7.2.2.
Medzné hodnoty sa stanovujú na účely rozhodovania o tom, či sú vzorky v súlade s najvyššími prípustnými obsahmi, resp. na účely kontroly akčných prahových hodnôt, ak sú relevantné, a to s príslušnými najvyššími prípustnými obsahmi alebo akčnými prahovými hodnotami stanovenými buď zvlášť pre PCDD/PCDF a pre dioxínom podobné PCB, alebo pre sumu PCDD/PCDF a dioxínom podobných PCB. Predstavujú dolnú hranicu distribúcie bioanalytických výsledkov (korigovaných na slepý pokus a výťažnosť) zodpovedajúcich rozhodovaciemu limitu potvrdzujúcej metódy pri 95 % hladine spoľahlivosti, čiže pri nižšej ako 5 % miere výskytu meraní vykazujúcich falošný súlad, a pri RSDR < 25 %. Rozhodovací limit potvrdzujúcej metódy je najvyšší prípustný obsah berúc do úvahy neistotu merania.
Medzná hodnota (v BEQ) sa môže vypočítať v súlade s jedným z prístupov stanovených v bodoch 7.3.1, 7.3.2 a 7.3.3. (pozri obrázok 1).
7.3.1. Použitie dolného pásma 95 % predikčného intervalu rozhodovacieho limitu potvrdzujúcej metódy:

pričom:
|
BEQDL |
BEQ zodpovedajúce rozhodovaciemu limitu potvrdzujúcej metódy, ktorý je súčasne najvyšším prípustným obsahom pri zohľadnení neistoty merania |
|
sy,x |
smerodajná odchýlka rezíduí |
|
t α,f = m-2 |
Studentov koeficient (α = 5 %, f = počet stupňov voľnosti, jednostranný) |
|
m |
celkový počet kalibračných bodov (index j) |
|
n |
počet opakovaní pri každom obsahu |
|
xi |
koncentrácia vzorky (v TEQ) kalibračného bodu i stanovená potvrdzujúcou metódou |
|
|
priemerná hodnota koncentrácií (v TEQ) všetkých kalibračných vzoriek |
|
|
parameter súčtu štvorcov, i = index pre kalibračný bod i |
7.3.2. Výpočet z bioanalytických výsledkov (korigovaných na slepý pokus a výťažnosť) viacnásobne opakovaných analýz vzoriek (n≥ 6) kontaminovaných na úrovni rozhodovacieho limitu potvrdzujúcej metódy predstavujúceho dolnú hranicu distribúcie dát pri zodpovedajúcej priemernej hodnote BEQ:
medzná hodnota = BEQDL – 1.64xSDR
pričom:
|
SDR |
je smerodajná odchýlka výsledkov biotestu BEQDL nameraných za podmienok vnútrolaboratórnej reprodukovateľnosti |
7.3.3. Výpočet ako priemerná hodnota bioanalytických výsledkov (v BEQ, korigovaných vzhľadom na slepý pokus a výťažnosť) z mnohých analýz vzoriek (n ≥ 6) kontaminovaných na úrovni 2/3 najvyššieho prípustného obsahu alebo akčnej prahovej hodnoty, na základe poznatku, že tento obsah sa bude pohybovať okolo medznej hodnoty stanovenej v bode 7.3.1 alebo bode 7.3.2:
Obrázok 1

Obrázok 1. Výpočet medzných hodnôt pri 95 %-nej hladine spoľahlivosti, čiže pri 5 %-nej miere výskytu meraní vykazujúcich falošný súlad nižšej ako 5 % a pri RSDR < 25 %:
|
1. |
na základe dolného pásma 95 % predikčného intervalu pri rozhodovacom limite potvrdzujúcej metódy; |
|
2. |
na základe radu analýz vzoriek (n> 6) kontaminovaných na úrovni rozhodovacieho limitu potvrdzujúcej metódy ako dolná hranica dátovej distribúcie (znázornenej na obrázku zvonovitou krivkou) pri zodpovedajúcej priemernej hodnote BEQ. |
7.3.4. Obmedzenia týkajúce sa medzných hodnôt
Medzné hodnoty vychádzajúce z BEQ a vypočítané z RSDR získanej pri validácii použitím obmedzeného počtu vzoriek s rozličnými matricami/kongenérovými profilmi môžu byť vyššie ako najvyššie prístupné obsahy alebo akčné prahové hodnoty vyjadrené v TEQ z dôvodu vyššej presnosti, než akú možno bežne docieliť v prípade, že sa analyzuje neznáme spektrum možných kongenérových profilov. V takýchto prípadoch sa medzné hodnoty vypočítavajú z RSDR = 25 % alebo sa zvolí výpočet odvodený z dvoch tretín najvyššieho prístupného obsahu alebo akčnej prahovej hodnoty.
7.4. Charakteristiky účinnosti
7.4.1. Keďže pri biologických metódach nie je možné využívať žiadne vnútorné štandardy, je nutné vykonávať testy opakovateľnosti bioanalytických metód na získanie informácií o smerodajnej odchýlke v rámci jednej testovacej série, ako aj medzi jednotlivými testovacími sériami. Opakovateľnosť musí byť nižšia ako 20 %, vnútrolaboratórna reprodukovateľnosť nižšia ako 25 %. Vychádza sa z vypočítaných hodnôt v BEQ korigovaných na slepé vzorky a výťažnosť.
7.4.2. Súčasťou procesu validácie je preukázanie toho, že testy rozlišujú medzi slepou vzorkou a obsahom na úrovni medznej hodnoty, aby bolo možné identifikovať vzorky s vyšším obsahom ako je príslušná medzná hodnota (pozri bod 7.1.2).
7.4.3. Je nutné definovať cieľové zlúčeniny, možné interferencie a najvyššie prijateľné obsahy v slepých vzorkách.
7.4.4. Smerodajná odchýlka vyjadrená v percentách, ktorá sa týka odozvy alebo koncentrácie vypočítanej na základe odozvy (možnej len v pracovnom rozsahu), nesmie byť pri trojnásobnom stanovovaní extraktu vzorky vyššia ako 15 %.
7.4.5. Nekorigované výsledky referenčnej(-ých) vzorky(-iek) vyjadrené v BEQ (slepý pokus a najvyšší prípustný obsah alebo akčná prahová hodnota) sa používajú na vyhodnotenie účinnosti príslušnej bioanalytickej metódy počas konštantného časového obdobia.
7.4.6. Diagramy kontroly kvality pre slepé vzorky metódy a každý typ referenčnej vzorky sa zaznamenávajú a kontrolujú s cieľom zabezpečiť, aby bolo vykonanie analýzy v súlade s požiadavkami, predovšetkým pokiaľ ide o slepé vzorky a v súvislosti s nimi o požadovaný minimálny odstup od dolnej medze pracovného rozsahu, ako aj o referenčné vzorky a v súvislosti s nimi o vnútrolaboratórnu reprodukovateľnosť. Slepé vzorky metódy sa musia dôkladne skontrolovať s cieľom predísť výskytu výsledkov vykazujúcich falošný súlad po odpočítaní.
7.4.7. Výsledky analýz podozrivých vzoriek a 2 až 10 % vzoriek vykazujúcich súlad (minimálne 20 vzoriek na matricu), ktoré boli získané potvrdzujúcimi metódami, sa zhromažďujú a používajú na vyhodnotenie účinnosti skríningovej metódy a vzťahu medzi BEQ a TEQ. Tento súbor údajov sa môže použiť na prehodnotenie medzných hodnôt aplikovateľných na rutinné vzorky v prípade validovaných matríc.
7.4.8. Úspešnosť metódy sa môže preukázať takisto účasťou na kruhových testoch. Výsledky zo vzoriek analyzovaných v rámci kruhových testov, ktoré sa nachádzajú v koncentračnom rozpätí až do napr. dvojnásobku najvyššieho prípustného obsahu, sa môžu zahrnúť do vyhodnocovania miery výskytu meraní vykazujúcich falošný súlad, ak je laboratórium schopné preukázať svoju úspešnú výkonnosť. Vzorky musia pokryť najčastejšie kongenérové profily a reprezentovať rozličné zdroje.
7.4.9. V prípadoch kontaminácie sa môžu medzné hodnoty prehodnotiť tým spôsobom, že sa zohľadní špecifická matrica a kongenérové profily tohto konkrétneho prípadu.
8. Oznamovanie výsledkov
8.1. Potvrdzujúce metódy
8.1.1. Pokiaľ to umožňuje použitý analytický postup, analytické výsledky musia zahŕňať obsahy jednotlivých kongenérov PCDD/PCDF a dioxínom podobných PCB a musia byť uvedené ako dolná, horná a stredná medza, aby sa pri uvádzaní výsledkov zahrnulo čo najviac informácií, a tak umožnilo interpretovať výsledky v súlade s osobitnými požiadavkami.
8.1.2. Správa musí zahŕňať metódu použitú na extrahovanie PCDD/PCDF a dioxínom podobných PCB.
8.1.3. Údaje o výťažnostiach jednotlivých vnútorných štandardov sa musia poskytnúť v prípade, že výťažnosti sa pohybujú mimo oblasti uvedenej v bode 6.2.5, v prípade, že sa prekročí najvyšší prípustný obsah (v tomto prípade sa poskytujú údaje o výťažnosti jednej z dvoch dvojnásobných analýz), ako aj v ostatných prípadoch na požiadanie.
8.1.4. Keďže je pri rozhodovaní o súlade vzorky nutné zohľadniť nepresnosť merania, tento parameter musí byť k dispozícii. Preto sa analytické výsledky uvádzajú ako ‚x +/– U‘, pričom x je analytický výsledok a U je rozšírená neistota merania pri použití koeficientu pokrytia v hodnote 2, ktorý zabezpečuje približne 95 % hladinu spoľahlivosti. V prípade samostatného stanovenia PCDD/PCDF a dioxínom podobných PCB sa pre sumu PCDD/F a dioxínom podobných PCB používa suma odhadovanej rozšírenej neistoty samostatných analytických výsledkov PCDD/PCDF a dioxínom podobných PCB.
8.1.5. Ak sa nepresnosť merania zohľadní uplatnením CCα (ako je uvedené v bode 2.2 kapitoly I tejto časti B), je nutné uviesť tento parameter.
8.1.6. Výsledky sa vyjadrujú v rovnakých jednotkách a s najmenej rovnakým počtom číslic, ako sú najvyššie prístupné obsahy stanovené v smernici 2002/32/ES.
8.2. Bioanalytické skríningové metódy
8.2.1. Výsledok skríningu sa vyjadruje ako ‚v súlade‘ alebo ‚podozrenie na nesúlad‘ (‚podozrenie‘).
8.2.2. Okrem toho sa môže uvádzať výsledok pre PCDD/PCDF a/alebo dioxínom podobné PCB vyjadrené v BEQ (nie TEQ).
8.2.3. Vzorky vykazujúce odozvu pod medzou oznamovania sa musia označiť ako vzorky ‚pod medzou oznamovania‘.
8.2.4. Pre každý typ matrice sa v správe uvádza najvyšší prípustný obsah alebo akčná prahová hodnota, z ktorej vychádza hodnotenie.
8.2.5. V správe sa uvádza druh použitého testu, jeho základný princíp a druh kalibrácie.
8.2.6. Správa musí zahŕňať metódu použitú na extrahovanie PCDD/PCDF a dioxínom podobných PCB.
8.2.7. V prípade vzoriek, pri ktorých je podozrenie na nesúlad, musí správa obsahovať poznámku o opatreniach, ktoré je potrebné prijať. Prostredníctvom potvrdzujúcej metódy je potrebné stanoviť/potvrdiť koncentráciu PCDD/F a sumu koncentrácií PCDD/F a dioxínom podobných PCB vo vzorkách so zvýšenými obsahmi týchto látok.
KAPITOLA III
Príprava vzoriek a požiadavky na analytické metódy používané pri úradnej kontrole obsahov dioxínom nepodobných PCB (PCB # 28, 52, 101, 138, 153, 180)
1. Oblasť použitia
Požiadavky, ktoré sú stanovené v tejto kapitole, sa uplatňujú v prípadoch, keď sa vykonáva analýza krmív na úradnú kontrolu obsahu dioxínom nepodobných polychlórovaných bifenylov (dioxínom nepodobných PCB) a na iné regulačné účely.
2. Použiteľné detekčné metódy
Plynová chromatografia/detekcia elektrónového záchytu (GC-ECD), GC-LRMS, GC-MS/MS, GC-HRMS alebo rovnocenné metódy.
3. Identifikácia a potvrdzovanie skúmaných analytov:
3.1. Relatívny retenčný čas vo vzťahu k vnútorným štandardom alebo referenčným štandardom (prijateľná odchýlka +/– 0,25 %).
3.2. Separácia všetkých šiestich indikátorových PCB (PCB 28, PCB 52, PCB 101, PCB 138, PCB 153 a PCB 180) od interferujúcich látok, predovšetkým koeluovaných PCB, najmä ak sú obsahy vzoriek v oblasti zákonom stanovených medzí a nesúlad sa musí potvrdzovať.
[Kongenéry, v prípade ktorých je často zaznamenaná koeluácia, sú napr. PCB 28/31, PCB 52/69 a PCB 138/163/164. V prípade GC-MS je takisto nevyhnutné uvažovať o možných interferenciách fragmentov vyšších chlórovaných kongenérov.]
3.3. Požiadavky na techniky GC-MS
Monitorovanie aspoň:
|
a) |
dvoch špecifických iónov v prípade HRMS; |
|
b) |
dvoch špecifických iónov m/z > 200 alebo troch špecifických iónov m/z > 100 v prípade LRMS; |
|
c) |
jedného prekurzorového a dvoch produktových iónov v prípade MS-MS. |
Maximálne povolené tolerancie pomerov odoziev pre vybrané fragmenty hmoty:
Relatívna odchýlka pomeru odoziev vybraných fragmentov hmotností od teoretických pomerov odoziev alebo od pomerov odoziev kalibračných štandardov pre kvantifikačný ión (najintenzívnejší sledovaný ión) a dôkazový(-é) ión(-y):
|
Relatívna intenzita dôkazového(-ých) iónu(-ov) v porovnaní s kvantifikačným iónom |
GC-EI-MS (relatívna odchýlka) |
GC-CI-MS, GC-MSn (relatívna odchýlka) |
|
> 50 % |
± 10 % |
± 20 % |
|
> 20 % až 50 % |
± 15 % |
± 25 % |
|
> 10 % až 20 % |
± 20 % |
± 30 % |
|
≤ 10 % |
± 50 % (11) |
± 50 % (11) |
3.4. Požiadavky na techniky GC-ECD
Výsledky presahujúce toleranciu sa potvrdzujú na dvoch stĺpcoch GC so stacionárnymi fázami rozličnej polarity.
4. Preukázanie výkonnosti metódy
Účinnosť metódy sa validuje v rozsahu najvyššieho prípustného obsahu (0,5 až 2,00-násobok najvyššieho prípustného obsahu) s prijateľným variačným koeficientom pre opakovanú analýzu (pozri požiadavky na vnútrolaboratórnu presnosť v bode 9).
5. Kvantifikačný limit
Slepé hodnoty nesmú byť vyššie ako 30 % úrovne kontaminácie zodpovedajúcej najvyššiemu prípustnému obsahu (12).
6. Kontrola kvality
Pravidelné kontroly slepých vzoriek, analýzy vzoriek s prídavkom analytov, vzoriek na kontrolu kvality, účasť v medzilaboratórnych štúdiách relevantných matríc.
7. Kontrola výťažností
7.1. Použijú sa vhodné vnútorné štandardy s fyzikálno-chemickými vlastnosťami porovnateľnými so sledovanými analytmi.
7.2. Pridávanie vnútorných štandardov:
Pridanie k výrobkom (pred procesom extrakcie a čistenia).
7.3. Požiadavky na metódy používajúce všetkých šesť izotopom označených kongenérov PCB:
|
a) |
výsledky sa korigujú pre výťažnosti vnútorných štandardov; |
|
b) |
výťažnosti izotopom označených vnútorných štandardov sa musia pohybovať medzi 50 a 120 %; |
|
c) |
nižšie alebo vyššie výťažnosti individuálnych kongenérov s podielom na sume šiestich indikátorových PCB pod úrovňou 10 % sú prijateľné. |
7.4. Požiadavky na metódy, pri ktorých sa nepoužíva všetkých šesť izotopicky označených vnútorných štandardov alebo iné vnútorné štandardy:
|
a) |
výťažnosť vnútorného(-ých) štandardu(–ov) sa kontroluje pri každej vzorke; |
|
b) |
výťažnosti vnútorného(-ých) štandardu(-ov) sa musia pohybovať medzi 60 a 120 %; |
|
c) |
výsledky sa korigujú na výťažnosť vnútorných štandardov. |
7.5. Výťažnosti neoznačených kongenérov sa overujú vzorkami s prídavkom analytov alebo vzorkami kontroly kvality s koncentráciami v rozsahu najvyššieho prípustného obsahu. Výťažnosti týchto kongenérov sa považujú za prijateľné, ak sa pohybujú medzi 70 a 120 %.
8. Požiadavky na laboratóriá
Akreditáciu laboratórií uskutočňuje v súlade s ustanoveniami nariadenia (ES) č. 882/2004 uznávaný orgán, ktorý pôsobí v súlade s pokynom ISO 58 s cieľom zaistiť, že laboratóriá zabezpečujú analytickú kvalitu. Akreditácia laboratórií sa uskutočňuje v súlade s normou EN ISO/IEC 17025.
9. Výkonnostné charakteristiky: kritériá pre sumu šiestich indikátorových PCB pre najvyšší prípustný obsah
|
Pravdivosť |
– 30 až + 30 % |
|
Vnútrolaboratórna presnosť (RSD %) |
≤ 20 % |
|
Rozdiel medzi výpočtom hornej a dolnej medze |
≤ 20 % |
10. Oznamovanie výsledkov
10.1. Pokiaľ to použitý analytický postup umožňuje, analytické výsledky musia zahŕňať obsahy jednotlivých kongenérov PCB a musia byť uvedené ako dolná, horná a stredná medza, aby sa pri uvádzaní výsledkov zahrnulo čo najviac informácií, a tak umožnilo interpretovať výsledky v súlade s osobitnými požiadavkami.
10.2. Správa musí zahŕňať metódu použitú na extrahovanie PCB a lipidov.
10.3. Údaje o výťažnostiach jednotlivých vnútorných štandardov sa poskytujú v prípade, že výťažnosti sa pohybujú mimo rozsahu uvedeného v bode 7, v prípade, že sa prekročí najvyšší prípustný obsah, ako aj v ostatných prípadoch na požiadanie.
10.4. Keďže je nutné pri rozhodovaní o súlade vzorky zohľadniť neistotu merania, tento parameter musí byť tiež k dispozícii. Preto sa analytické výsledky uvádzajú ako ‚x +/– U‘, pričom x je analytický výsledok a U je rozšírená neistota merania pri použití koeficientu pokrytia v hodnote 2, ktorý zabezpečuje približne 95 %-nú hladinu spoľahlivosti.
10.5. Ak sa neistota merania zohľadní uplatnením CCα (ako je uvedené v bode 2.1. kapitoly I), je nutné uviesť tento parameter.
10.6. Výsledky sa vyjadrujú v rovnakých jednotkách a s najmenej rovnakým počtom číslic, ako sú najvyššie prípustné obsahy stanovené v smernici 2002/32/ES.
(9) Pokiaľ ide o najvyššie prípustné obsahy.
(11) Je dostupný dostatočný počet fragmentov hmotností s relatívnou intenzitou > 10 %, preto sa neodporúča používať dôkazový(-é) ión(-y) s relatívnou intenzitou menej ako 10 % v porovnaní s kvantifikačným iónom.