ANNESS
LINJI GWIDA DWAR L-ANNESS I TAR-REGOLAMENT (KE) Nru 1223/2009 DWAR IR-RAPPORT DWAR IS-SIKUREZZA TAL-PRODOTTI KOŻMETIĊI
1. INTRODUZZJONI
L-Artikolu 11 tar-Regolament (KE) Nru 1223/2009 jeħtieġ li jiġi fformulat fajl bl-informazzjoni dwar il-prodott għal kull prodott qabel ma jitqiegħed fis-suq. Il-fajl bl-informazzjoni dwar il-prodott għandu jiġi aġġornat meta jkun meħtieġ u jinżamm aċċessibbli faċilment, f’format elettroniku jew f’format ieħor, fl-indirizz tal-persuna responsabbli mogħti fuq it-tikketta, lill-awtoritajiet kompetenti għal finijiet ta’ sorveljanza tas-suq għal perjodu ta’ għaxar snin wara t-tqegħid fis-suq tal-aħħar lott tal-prodott.
L-element l-aktar importanti mill-fajl bl-informazzjoni dwar il-prodott, mill-perspettiva tas-sikurezza, huwa r-rapport dwar is-sikurezza tal-prodott kożmetiku msemmi fl-Artikolu 10(1). L-elementi l-oħra huma deskrizzjoni ċara tal-prodott kożmetiku, deskrizzjoni tal-metodu ta’ manifattura u dikjarazzjoni dwar il-konformità ma’ prattika ta’ manifattura tajba, il-prova tal-effetti ddikjarati, u dejta dwar l-ittestjar fuq l-annimali (1).
Meta l-persuna responsabbli li tfassal ir-rapport dwar is-sikurezza tal-prodott kożmetiku ma tkunx il-manifattur tal-prodott, din għandha tiżgura li jkollha aċċess għall-ħiliet tekniċi u xjentifiċi kollha meħtieġa biex tinkiseb informazzjoni affidabbli dwar is-sikurezza tal-prodott kożmetiku u valutazzjoni tas-sikurezza biex jintwera li l-prodott li huma responsabbli għalih huwa sikur, skont l-Artikolu 3 tar-Regolament (KE) Nru 1223/2009. Għalhekk, dan jistaħ jinvolvi mhux biss lill-eżaminatur tas-sikurezza, iżda wkoll lill-manifattur, lill-fornituri tal-materja prima, u esperti tekniċi oħra.
Fi kwalunkwe każ, il-persuna responsabbli għandha tiżgura li l-użu maħsub tal-prodott kożmetiku u l-esponiment sistemiku antiċipat għall-ingredjenti prinċipali f’formulazzjoni finali jitqiesu fil-valutazzjoni tas-sigurta; jintuża approċċ ibbażat fuq il-piż tal-evidenza fil-valutazzjoni tas-sikurezza għar-reviżjoni tad-dejta mis-sorsi eżistenti kollha; ir-rapport dwar is-sikurezza tal-prodott kożmetiku jinżamm aġġornat fid-dawl ta’ informazzjoni rilevanti addizzjonali ġġenerata wara t-tqegħid fis-suq (2).
Il-valutazzjoni tas-sikurezza tal-prodott kożmetiku, kif stabbilit fil-Parti B tal-Anness I tar-Regolament (KE) Nru 1223/2009, għandha titwetttaq minn eżaminatur tas-sikurezza kkwalifikat. Il-persuna responsabbli u l-eżaminatur tas-sikurezza għandhom jaħdmu flimkien mill-qrib biex jiżguraw li s-sikurezza tal-prodott tiġi vvalutata u ddokumentata kif xieraq filwaqt li l-valutazzjoni tinżamm aġġornata. Il-persuna responsabbli u l-eżaminatur tas-sikurezza għandhom jiġbru l-informazzjoni kollha meħtieġa kif meħtieġ mill-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009.
Ir-rapport dwar is-sikurezza tal-prodott kożmetiku għandu jitfassal b’mod trasparenti u għandu jkun argumentat sew u jinftiehem faċilment.
Ir-Rapport dwar is-Sikurezza tal-Prodott Kożmetiku huwa biċċa xogħol esperta magħmula minn moduli differenti u fejn l-informazzjoni meħtieġa skont il-Parti A tista’ tinħażen f’databases differenti. Ir-rapport, li għandu jkun jinkludi, bħala minimu, l-informazzjoni kollha indikata fl-Anness I tar-Regolament (KE) Nru 1223/2009, għandu jidher taħt l-istess intestaturi jew simili għal referenza faċili mill-awtoritajiet kompetenti. Madankollu, jista’ jkun suffiċjenti li taħt kull intestatura tiġi pprovduta referenza ċara għal dokument li jinkludi l-informazzjoni u li jkun faċilment disponibbli f’format elettroniku u stampat.
2. ANNESS I TAR-REGOLAMENT (KE) Nru 1223/2009 – RAPPORT DWAR IS-SIKUREZZA TAL-PRODOTT KOŻMETIKU
Skont l-Anness I tar-Regolament (KE) Nru 1223/2009, ir-Rapport dwar is-Sikurezza tal-Prodott Kożmetiku għandu “bħala minimu” jinkludi l-informazzjoni meħtieġa taħt kull waħda mill-intestaturi tal-Parti A u l-Parti B.
Il-Parti A għandha l-għan li tiġbor id-dejta kollha meħtieġa għall-valutazzjoni tas-sikurezza tal-prodott, filwaqt li l-Parti B tistabbilixxi r-raġunament, billi tibda mid-dejta, biex tfassal konklużjonijiet dwar is-sikurezza tal-prodott.
L-istruttura u l-kontenut tar-rapport dwar is-sikurezza għandhom jirriflettu r-rekwiżiti tal-Anness I tar-Regolament (KE) Nru 1223/2009. Madankollu, jekk ir-rapport ma jkunx jinkludi direttament l-informazzjoni meħtieġa, għandu jipprovdi referenza għal sors ieħor li jkun disponibbli faċilment.
Il-persuna responsabbli għandha tiżgura li r-Rapport dwar is-Sikurezza tal-Prodott Kożmetiku jinżamm aġġornat fid-dawl ta’ informazzjoni rilevanti addizzjonali li toħroġ wara li l-prodott ikun tqiegħed fis-suq (3).
3. PARTI A — INFORMAZZJONI DWAR IS-SIKUREZZA TAL-PRODOTT
Il-Parti A tar-rapport dwar is-sikurezza tal-prodott kożmetiku hija maħsuba biex tiġbor id-dejta meħtieġa biex jiġi ppruvat li l-prodott kożmetiku huwa sikur. L-informazzjoni għandha tippermetti lill-eżaminatur tas-sikurezza jidentifika u jikkwantifika b’mod ċar, abbażi tal-perikli identifikati, ir-riskji li jista’ jkollu prodott kożmetiku għas-saħħa tal-bniedem. Pereżempju, jista’ jiżviluppa periklu, mill-materja prima, il-proċess ta’ manifattura, l-ippakkjar, il-kundizzjonijiet ta’ użu tal-prodott, l-ispeċifikazzjonijiet mikrobijoloġiċi, il-kwantitajiet użati, il-profil tossikoloġiku tas-sustanzi, eċċ.
Peress li l-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009 teħtieġ li bħala minimu tiġi pprovduta d-dejta elenkata taħt l-intestatura tagħha, kwalunkwe diskrepanza fir-rigward tar-rekwiżiti tal-Parti A għandha tiġi ġġustifikata.
Il-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009 telenka d-dejta li “bħala minimu” għandha titqiegħed għad-dispożizzjoni tal-eżaminatur tas-sikurezza biex ikun jista’ jwettaq il-valutazzjoni tas-sikurezza.
Minbarra d-dejta minima elenkata fil-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009, l-eżaminatur tas-sikurezza jista’ juża kwalunkwe dejta addizzjonali, fejn ikun rilevanti. Min-naħa l-oħra, hu, jew il-persuna responsabbli, jista’ jikkunsidra li abbażi tat-tip ta’ prodott, xi parti mid-dejta meħtieġa ma tkunx rilevanti jew meħtieġa biex tiġi vvalutata s-sikurezza tal-prodott (eż. it-test tal-isfida tal-preżervazzjoni). F’dan il-każ, in-nuqqas ta’ dejta speċifika għandu jiġi ġġustifikat fil-Parti A u l-ġustifikazzjoni għandha tiġi rripetuta u vvalidata mill-eżaminatur tas-sikurezza fir-raġunament tal-Parti B. Il-persuna responsabbli għandha tivverifika l-preżenza tad-dejta meħtieġa jew il-ġustifikazzjoni għan-nuqqas tagħha.
Id-dejta meħtieġa mill-Parti A tista’ tittieħed minn kwalunkwe sors affidabbli. L-eżempji jinkludu: id-dejta mill-fornituri, id-dokumentazzjoni xjentifika, l-esperjenza miksuba b’kategoriji simili jew b’kategoriji ta’ prodotti oħra, ir-riżultati tal-istudji fuq il-prodott innifsu jew fuq is-sustanzi li fih, id-dejta disponibbli fuq formulazzjonijiet simili, jew il-mudelli tal-kompjuters. Ir-rapport dwar is-sikurezza għandu jenfasizza r-rilevanza tad-dejta fir-rigward tal-proġett.
Il-gwida ppubblikata mill-kumitati xjentifiċi tal-UE kkonċernati bil-valutazzjoni tar-riskju (4), kif ukoll ir-rakkomandazzjonijiet tal-awtoritajiet nazzjonali kompetenti jew l-organizzazzjonijiet professjonali, tista’ tipprovdi appoġġ utli ulterjuri.
3.1. Kompożizzjoni kwalitattiva u kwantitattiva tal-prodott kożmetiku
L-għan ta’ dik it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku huwa li tipprovdi l-kompożizzjoni kwalitattiva u kwantitattiva preċiża tal-prodott lest, billi tibda mill-materja prima. Il-materja prima hija sustanzi jew taħlitiet użati fil-manifattura tal-prodott kożmetiku. Il-funzjoni maħsuba ta’ kull sustanza għandha tiġi indikata.
Il-kompożizzjoni kompluta tal-prodott għandha tiġi speċifikata, billi tiddikjara l-isem u l-identità (kwalitattiva) ta’ kull materja prima (inkluż l-isem kimiku, l-INCI, is-CAS, l-EINECS/ELINCS, fejn ikun possibbli), u l-ammont minn kull materja prima, billi jiġi ddikjarat il-persentaġġ ta’ piż (kwantitattiv). Ma għandhomx jintużaw meded, sakemm dan ma jkunx jista’ jiġi ġġustifikat (eż.. viskożità jew aġġustaturi tal-pH). Jekk il-meded ta’ konċentrazzjoni jkunu inevitabbli, il-kunsiderazzjonijiet u l-kalkoli tossikoloġiċi għandhom ikunu bbażati fuq l-ogħla ċifra ta’ konċentrazzjoni. Jista’ jkun utli li jiġi/jiġu indikat(i) il-fornitur(i) tal-materja prima.
Is-sustanzi kollha li jidħlu fil-kompożizzjoni tat-taħlitiet kummerċjali pprovduti bħala materja prima (inkluż preżervattivi miżjuda direttament, antiossidanti, kelaturi, aġenti ta’ lqugħ, solventi, addittivi oħra, eċċ) għandhom jiġu identifikati u kkwantifikati fil-formula tal-prodott lest. Dan japplika wkoll għas-sustanzi kollha miżjuda indirettament mal-prodott, bħal preżervattivi użati għall-preżervazzjoni tal-materja prima. Il-funzjoni maħsuba ta’ kull sustanza għandha tiġi indikata.
Meta jkunu preżenti sustanzi ddefiniti sew kimikament, il-kwantità u l-formula molekulari tagħhom għandha tingħata flimkien mal-ispeċifikazzjonijiet analitiċi tagħhom (il-grad ta’ purità, l-identifikazzjoni ta’ impuritajiet ewlenin, il-kriterji u l-metodi ta’ ttestjar użati).
Meta jkunu preżenti ingredjenti kumplessi, għandha tingħata n-natura u l-kwalità tagħhom flimkien ma’ definizzjoni ċara tat-taħlita u l-materjal(i) użati sabiex jiġu identifikati s-sustanzi fir-rigward tal-kompożizzjoni u l-effetti tagħhom (il-proċess ta’ manifattura u purifikazzjoni, inklużi l-passi fiżiċi, kimiċi, enżimatiċi, bijoteknoloġiċi u mikrobijoloġiċi). Għandhom jiġu pprovduti l-kriterji ta’ purità u l-metodi ta’ ttestjar użati. L-eżempji ta’ ingredjenti kumplessi jinkludu dawk ta’ oriġini minerali, botanika, bijoteknoloġika jew mill-annimali. L-iskop tal-informazzjoni meħtieġa dwar l-ingredjenti kumplessi, abbażi tan-natura u l-oriġini tagħhom, hija elenkata espliċitament fin-Nota ta’ Gwida tal-Kumitat Xjentifiku dwar is-Sikurezza tal-Konsumatur (SCCS) (5).
Meta tkun preżenti taħlita kemm ta’ sustanzi ddefiniti sew kimikament kif ukoll ta’ ingredjenti kumplessi, tapplika wkoll il-gwida ta’ hawn fuq.
Meta xi kompost ta’ fwieħa (jew togħma) li jinkludi taħlita ta’ ingredjenti ta’ fwieħa (jew togħma) u l-komponenti funzjonali bi proprjetajiet olfattivi, li jsaħħu r-riħa, li jipproteġu r-riħa jew ta’ taħlit ikun fformulat u miżjud b’mod intenzjonali ma’ prodott kożmetiku biex tinħoloq fwieħa (jew togħma) jew biex ikopri riħa tinten, l-identifikazzjoni tiegħu għandha tinkludi l-isem u n-numru tal-kodiċi kif ukoll l-identità tal-fornitur. L-informazzjoni kwalitattiva u kwantitattiva dwar is-sustanzi rregolati fil-kompost tal-fwieħa (jew tat-togħma) u l-informazzjoni rilevanti għal valutazzjoni tas-sikurezza għandha tiġi żvelata lill-persuna responsabbli u l-eżaminatur tas-sikurezza, u għandha tiġi inkluża fir-rapport dwar is-sikurezza.
3.2. Karatteristiċi fiżiċi/kimiċi u l-istabbiltà tal-prodott kożmetiku
L-għan ta’ din it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku huwa li tiddeskrivi l-ispeċifikazzjonijiet fiżiċi u kimiċi tas-sustanzi jew it-taħlitiet użati u l-prodott kożmetiku nnifsu. Dawn l-ispeċifikazzjonijiet huma kruċjali għal valutazzjoni tas-sikurezza xierqa, peress li jistgħu jinfluwenzaw is-sikurezza tal-prodott kożmetiku. Pereżempju, il-proprjetajiet fiżikokimiċi, flimkien ma’ informazzjoni oħra, jistgħu jgħinu lill-eżaminatur tas-sikurezza biex jistabbilixxi l-ħtieġa li jiġu investigati l-parametri tossikoloġiċi rilevanti.
Minbarra dan, il-karatteristiċi fiżikokimiċi tas-sustanzi jew it-taħlitiet u l-prodotti lesti stabbilixxew il-parametru referenzjarju skont liema l-prodotti u l-materja prima jistgħu jiġu kkunsidrati aċċettabbli mill-perspettiva tal-kwalità (6) .
Din it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku teħtieġ ukoll valutazzjoni tal-istabbiltà tal-prodott kożmetiku, f’kundizzjonijiet ta’ ħżin raġonevolment prevedibbli. L-għan huwa li jiġi evalwat jekk l-istabbiltà tal-prodott kożmetiku taffettwax is-sikurezza u l-kwalità tal-prodott, u li l-informazzjoni tintuża biex tiġi stabbilita d-durabbiltà minima tiegħu u l-perjodu wara l-ftuħ (PAO).
3.2.1. Karatteristiċi fiżiċi/kimiċi tas-sustanzi jew taħlitiet
Din id-deskrizzjoni għandha tinkludi l-proprjetajiet fiżikokimiċi l-aktar rilevanti ta’ kull sustanza u t-taħlita inkluża fil-prodott, pereżempju: l-identifikazzjoni kimika, il-forma fiżika, il-piż molekulari, is-solubbiltà, il-koeffiċjent tal-partizzjoni, il-purità tas-sustanza, parametri oħra rilevanti għall-karatterizzazzjoni ta’ sustanzi u taħlitiet speċifiċi, u, għall-polimeri, il-piż molekulari u l-firxa medja.
Fejn ikun rilevanti, il-kurva tad-distribuzzjoni tad-daqs tal-partikoli tas-sustanzi għandha tiġi inkluża fil-karatteristiċi kimiċi rilevanti, speċjalment għan-nanomaterjali.
Il-manifatturi tal-prodotti kożmetiċi għandhom jiżguraw li l-ispeċifikazzjonijiet tal-materja prima jiġu ddokumentati sew mill-fornituri tagħhom. Għandhom ikunu disponibbli l-ispeċifikazzjonijiet għal kull materja prima li effettivament tintuża fil-prodott. Abbażi tal-funzjoni, jistgħu jkunu meħtieġa speċifikazzjonijiet addizzjonali. Pereżempju, għall-assorbituri tal-UV, għandu jiġi pprovdut l-ispektrum ta’ assorbiment.
Għal kull deskrizzjoni tal-proprjetajiet u l-ispeċifikazzjonijiet fiżikokimiċi (għal kull sustanza u taħlita inkluża fil-prodott), il-metodi ta’ referenza għandhom jiġu ddikjarati fir-rapport dwar is-sikurezza.
3.2.2. Karatteristiċi fiżiċi/kimiċi tal-prodott kożmetiku lest
Din id-deskrizzjoni għandha tinkludi l-ispeċifikazzjonijiet tal-prodott lest. Kull speċifikazzjoni għandha tingħata fil-limiti rilevanti, eż. pH bejn 5.5 u 6.5.
Għal kull deskrizzjoni tal-proprjetajiet u l-ispeċifikazzjonijiet fiżikokimiċi tal-prodott lest, il-metodi ta’ referenza għandhom jiġu ddikjarati fir-rapport dwar is-sikurezza tal-prodott kożmetiku.
3.2.3. Stabbiltà tal-prodott kożmetiku
Peress li r-rekwiżit huwa li tiġi vvalutata l-istabbiltà tal-prodott kożmetiku f’kundizzjonijiet ta’ ħżin raġonevolment prevedibbli, jekk l-istabbiltà tkun tiddependi fuq il-kundizzjonijiet ta’ ħżin, l-informazzjoni dwar dawn il-kundizzjonijiet għandha tiġi mgħoddija tul il-katina tal-provvista kollha, u jekk tkun rilevanti għall-utent aħħari, għandha tiġi indikata fuq it-tikketta tal-prodott.
Il-metodoloġija użata biex tiġi stabbilita d-durabbiltà minima tal-prodott għandha tiġi deskritta. Għandha tiġi indikata kwalunkwe prekawzjoni ta’ preżervazzjoni speċifika.
Id-dejta kollha disponibbli użata biex tiġi ġġustifikata d-durabbiltà minima indikata għandha tiġi elenkata fir-rapport dwar is-sikurezza. Sabiex tiġi stabbilita l-koerenza tal-istudju ta’ stabbiltà mwettaq, u biex tiġi vverifikata r-rilevanza tad-data ta’ durabbiltà minima magħżula għall-prodott, id-deskrizzjoni tat-testijiet speċifiċi għall-istudju ta’ stabbiltà u r-riżultati ta’ dawn it-testijiet għandhom jiġu inklużi fir-rapport dwar is-sikurezza tal-prodott kożmetiku. Barra minn hekk, għandhom jiġu pprovduti:
|
(1) |
Evidenza li l-kompożizzjoni tal-prodott użat għall-ittestjar tal-istabbiltà tikkorrispondi għall-prodott li tqiegħed effettivament fis-suq; |
|
(2) |
Ir-riżultati tal-istudju dwar l-effikaċja tal-preżervattiv, eż.. it-test tal-isfida, jekk ikun applikabbli (7); |
|
(3) |
Fejn ikun applikabbli, il-perjodu wara l-ftuħ (PAO) (8) u l-ġustifikazzjoni tiegħu. |
L-SCCS irrakkomanda li “għandhom jitwettqu testijiet tal-istabbiltà rilevanti, adattati għat-tip ta’ prodott kożmetiku u l-użu maħsub tiegħu. Biex jiġi żgurat li ma tiġi kkawżata l-ebda problema fl-istabbiltà mit-tip ta’ kontenitur u l-ippakkjar użat, fil-preżent it-testijiet għall-istabbiltà fiżika qegħdin jitwettqu b’kontenituri inerti u dawk maħsuba li jintużaw fis-suq.” (9)
3.3. Kwalità mikrobijoloġika
L-għan ta’ din it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku huwa li tistabbilixxi l-ispeċifikazzjonijiet mikrobijoloġiċi aċċettabbli tal-materja prima (is-sustanzi jew it-taħlitiet) u l-prodott lest minn perspettiva mikrobijoloġika. F’konformità mal-Anness I tar-Regolament (KE) Nru 1223/2009, għandha tingħata attenzjoni partikolari lill-ispeċifikazzjonijiet mikrobijoloġiċi tal-prodotti kożmetiċi maħsuba li jintużaw fuq partijiet tal-ġisem sensittivi u fuq popolazzjonijiet speċifiċi. Minbarra dan, l-informazzjoni dwar il-kwalità mikrobijoloġika hija essenzjali sabiex tiġi ġġustifikata l-effettività tas-sistema ta’ preżervazzjoni u tiġi ġġustifikata d-durabbiltà minima indikata tal-prodott kożmetiku maħżun f’kundizzjonijiet xierqa u l-perjodu wara l-ftuħ (PAO) (10) tal-prodott lest f’termini ta’ sikurezza.
L-ispeċifikazzjonijiet mikrobijoloġiċi tal-materja prima (is-sustanzi u t-taħlitiet) u l-prodott kożmetiku għandhom jiffurmaw parti mill-valutazzjoni tas-sikurezza. Għandha tingħata attenzjoni partikolari għall-ispeċifikazzjonijiet mikrobijoloġiċi tal-prodotti kożmetiċi maħsuba li jintużaw madwar l-għajnejn, fuq membrani mukużi b’mod ġenerali, fuq ġilda danneġġata (eż. prodotti għall-kura tal-ġilda xierqa għal ġilda atopika jew irritata), fuq tfal li għandhom anqas minn tliet snin, fuq persuni anzjani jew persuni b’risponsi immuni kompromessi.
3.3.1. Kwalità mikrobijoloġija tas-sustanzi u t-taħlitiet
Il-parametri ewlenin għall-kwalità mikrobijoloġika huma l-livell oriġinali ta’ kontaminazzjoni u l-possibbiltà ta’ tkabbir mikrobjali. Għandha tingħata attenzjoni partikolari għall-materja prima (sustanzi u taħlitiet) l-aktar suxxetibbli għat-tkabbir mikrobjali (eż. taħlitiet ibbażati fuq l-ilma, materjali li fihom ħafna proteini, pjanti jew materja prima mill-annimali). Min-naħa l-oħra, hemm materja prima li ma tappoġġjax it-tkabbir mikrobjali, eż. solventi organiċi.
3.3.2. Kwalità mikrobijoloġika tal-prodott kożmetiku lest
Rigward is-suxxettibbiltà mikrobijoloġika, hemm differenza bejn tliet kategoriji ta’ prodotti:
|
(1) |
Prodotti b’riskju mikrobijoloġiku baxx (eż. prodotti b’kontenut ta’ alkoħol > 20 %, prodotti bbażati fuq solventi organiċi, prodotti b’pH għoli/baxx), li għalihom ma huwa meħtieġ la test tal-isfida tal-preżervazzjoni u lanqas testijiet tal-kwalità mikrobijoloġika fuq il-prodott lest. Madankollu, għandha tiġi pprovduta ġustifikazzjoni xjentifika; |
|
(2) |
Il-prodotti b’użu uniku, u l-prodotti li ma jistgħux jinfetħu (eż. li l-ippakkjar tagħhom jippermetti d-dożaġġ tal-prodott mingħajr ma dan jiġi f’kuntatt mal-arja) li għalihom huma meħtieġa biss testijiet tal-kwalità mikrobijoloġika fuq il-prodott lest. Madankollu, għandha tiġi pprovduta ġustifikazzjoni xjentifika; |
|
(3) |
Il-prodotti l-oħra kollha, li għalihom huwa meħtieġ kemm test tal-isfida tal-preżervazzjoni kif ukoll testijiet tal-kwalità mikrobijoloġija fuq il-prodott lest. |
“Linji Gwida Speċifiċi dwar il-Kwalità Mikrobijoloġika tal-Prodott Lest” huma pprovduti fin-Noti ta’ Gwida tal-SCCS (11).
3.4. Impuritajiet, traċċi, informazzjoni dwar il-materjal tal-ippakkjar
L-għan ta’ din it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku huwa li tivvaluta jekk il-prodott kożmetiku jinkludix sustanzi li ma ġewx intenzjonalament miżjuda mal-formulazzjoni, u li jista’ jkollhom impatt fuq is-sikurezza tiegħu.
L-impuritajiet huma sustanzi mhux intenzjonati fil-materja prima.
Traċċa hija kwantità żgħira ta’ sustanza mhux intenzjonata fil-prodott lest. It-traċċi għandhom jiġu evalwati fir-rigward tas-sikurezza tal-prodott lest. Meta jkunu preżenti traċċi ta’ sustanzi pprojbiti, għandha tiġi pprovduta wkoll evidenza tal-inevitabbiltà teknika tagħhom.
It-traċċi jistgħu joriġinaw mis-sorsi li ġejjin: impuritajiet fil-materja prima/sustanzi; il-proċess ta’ manifattura; l-evoluzzjoni/interazzjoni kimika potenzjali u/jew il-migrazzjoni fil-prodott li jista’ jseħħ f’kundizzjoni ta’ ħżin normali u/jew permezz ta’ kuntatt mal-materjal tal-ippakkjar.
Peress li s-sustanzi jistgħu jimmigraw mill-ippakkjar għall-formulazzjoni, għandom jiġu kkunsidrati l-karatteristiċi rilevanti tal-materjal tal-ippakkjar.
F’konformità mal-punt 4 tal-Anness I tar-Regolament (KE) Nru 1223/2009, it-taqsima dwar l-“Impuritajiet, traċċi, informazzjoni dwar il-materjal tal-ippakkjar” għandha tindirizza tliet kwistjonijiet speċifiċi:
|
(a) |
Il-purità tas-sustanzi u t-taħlitiet; |
|
(b) |
F’każ ta’ traċċi ta’ sustanzi pprojbiti, evidenza tal-inevitabbiltà teknika tagħhom; |
|
(c) |
Il-karatteristiċi rilevanti tal-materjal tal-ippakkjar, b’mod partikolari l-purità u l-istabbiltà. |
F’termini prattiċi, dawn l-elementi jistgħu jiġu interpretati kif ġej:
|
(a) |
Definizzjoni preċiża tal-impuritajiet u t-traċċi (ara 3.4.1); |
|
(b) |
Evidenza tal-inevitabbiltà teknika tas-sustanzi pprojbiti (ara 3.4.2); |
|
(c) |
Ir-rilaxx potenzjali ta’ sustanzi mill-ippakkjar jew id-deterjorazzjoni possibbli tal-prodott f’kuntatt mal-ippakkjar (ara 3.4.3). |
Għall-analiżi tal-impuritajiet u l-materjal tal-ippakkjar, id-dejta mill-fornituri hija ta’ importanza kruċjali u għandha tkun ippreferuta.
3.4.1. Il-purità tas-sustanzi u t-taħlitiet
Il-preżenza ta’ sustanzi mhux intenzjonati, bħal impuritajiet u traċċi, jista’ jkollha impatt fuq is-sikurezza tal-prodott lest. Ir-rapport dwar is-sikurezza tal-prodott kożmetiku għandu jinkludi dejta dwar il-purità tal-materja prima (sustanzi u taħlitiet) u l-identifikazzjoni tas-sustanzi mhux intenzjonati rilevanti tossikoloġikament. Dawn is-sustanzi għandhom jitqiesu fil-valutazzjoni tas-sikurezza tal-prodott.
L-impuritajiet huma sustanzi mhux intenzjonati fil-materja prima.
Traċċa hija kwantità żgħira ta’ sustanza mhux intenzjonata fil-prodott lest.
Il-preżenza ta’ traċċi fil-prodott lest tista’ tkun evalwata b’żewġ modi:
|
(a) |
permezz tal-ispeċifikazzjonijiet/tad-dejta teknika għal kull materja prima, fuq il-bażi tal-għarfien dwar il-proċess għall-manifattura tal-materja prima (l-oriġini tas-sustanza, il-proċess tal-produzzjoni, ir-rotta ta’ sinteżi, il-proċess ta’ estrazzjoni, is-solvent użat, eċċ.); |
|
(b) |
permezz ta’ analiżi fiżikokimika għal impuritajiet possibbli fil-materja prima u, jekk ikun hemm bżonn, fil-prodott lest (eż. nitrosamini li potenzjalment ikunu ġġenerati matul jew wara l-proċess tal-manifattura). |
Traċċi ta’ sustanzi pprojbiti huma indirizzati fil-paragrafu 3.4.2 ta’ dawn il-Linji Gwida.
Ċerti traċċi għandhom limiti ta’ konċentrazzjoni regolatorji. Għall-preżenza ta’ traċċi ta’ sustanzi li mhumiex projbiti, u li għalihom ma hemm l-ebda limitu ta’ konċentrazzjoni regolatorju, iżda li jistgħu jkunu mistennija jħallu impatt fuq is-sikurezza tal-konsumatur, il-valutazzjoni dwar is-sikurezza trid titwettaq minn eżaminatur tas-sikurezza.
3.4.2. Evidenza tal-inevitabbiltà teknika ta’ traċċi ta’ sustanzi pprojbiti
Filwaqt li l-proċedura spjegata fil-paragrafu 3.4.1 għandha tkun segwita għall-impuritajiet u t-traċċi kollha magħrufin biex jiġi evalwat l-impatt tossikoloġiku tagħhom, hemm bżonn li ssir investigazzjoni oħra għal sustanzi pprojbiti preżenti bħala traċċi fil-prodott lest (12).
Meta dik il-preżenza ma tkun teknikament inevitabbli, il-manifatturi tal-prodotti kożmetiċi huma meħtieġa jipprovdu evidenza tal-inevitabbiltà teknika. Dan ifisser li jridu jiġġustifikaw il-preżenza ta’ dawk it-traċċi b’kull mezz neċessarju. Il-preżenza ta’ traċċi ta’ sustanzi pprojbiti għandha tinżamm kemm jista’ jkun baxxa permezz ta’ prassi tajba ta’ manifattura. Barra minn hekk, l-eżaminatur tas-sikurezza jrid jiddeċiedi jekk il-livelli tagħhom humiex tossikoloġikament aċċettabbli u jekk il-prodott għadux sikur.
Speċjalment fil-każ ta’ sustanzi ġenotossiċi u karċinoġeniċi mingħajr livell limitu (13), l-industrija kożmetika għandha tibqa’ ttejjeb l-aħjar prattiki tagħha sabiex telimina dawn is-sustanzi (il-prinċipju ALARA (14)) fil-prodott kożmetiku lest. It-tħassib ewlieni huwa l-iżgurar tal-protezzjoni tas-saħħa tal-bniedem, kif meħtieġ mill-Artikolu 3 tar-Regolament (KE) Nru 1223/2009.
Traċċi ġġenerati mid-degradazzjoni ta’ sustanzi fi ħdan il-prodott lest (problemi ta’ stabilità), minħabba problemi ta’ preżervazzjoni jew fit-trasport, jew minħabba l-interazzjoni tal-materja prima, għandhom ikunu evitati permezz ta’ prassi tajba ta’ manifattura, jew possibbilment permezz ta’ riformulazzjoni tal-prodott.
3.4.3. Evidenza tal-inevitabbiltà teknika ta’ traċċi ta’ sustanzi pprojbiti
Il-materjal tal-imballaġġ ifisser il-kontenitur (jew l-imballaġġ primarju) li huwa f’kuntatt dirett mal-formulazzjoni. Il-karatteristiċi relevanti tal-materjali tal-imballaġġ f’kuntatt dirett mal-prodott lest huma importanti għas-sikurezza tal-prodott kożmetiku. Referenza għar-Regolament (KE) Nru 1935/2004 tal-Parlament Ewropew u tal-Kunsill (15) tista’ tkun utli.
Esperjenza b’taħlitiet simili tal-formulazzjoni/imballaġġ diġà fis-suq tipprovdi indikazzjonijiet utli. Il-materjali li ġew żviluppati għall-imballaġġ tal-ikel spiss diġà jkunu ġew ittestjati, u b’hekk it-tagħrif relevanti dwar l-istabilità u l-migrazzjoni jista’ jkun disponibbli. Jista’ ma jkunx hemm bżonn li jsiru iktar testijiet. Madankollu, jista’ jkun hemm bżonn li jsiru evalwazzjonijiet oħrajn għal imballaġġ ġdid jew innovattiv.
It-taħlita ta’ materjal tal-imballaġġ, formulazzjoni tal-prodott kożmetiku u l-kuntatt mal-ambjent estern jista’ jkollha impatt fuq is-sikurezza tal-prodott lest, minħabba l-fatturi li ġejjin:
|
(a) |
interazzjoni bejn il-prodott u l-materjal tal-imballaġġ; |
|
(b) |
proprjetajiet xekkiela tal-materjal tal-imballaġġ; |
|
(c) |
migrazzjoni tas-sustanza minn/lejn il-materjal tal-imballaġġ. |
It-tagħrif dwar il-karatteristiċi relevanti tal-materjali tal-imballaġġ f’kuntatt dirett mal-prodott għandu jippermetti li ssir stima tar-riskji potenzjali. Il-karatteristiċi relevanti jistgħu jinkludu, pereżempju, dawn li ġejjin:
|
(a) |
il-kompożizzjoni tal-materjal tal-imballaġġ, inklużi sustanzi tekniċi bħal addittivi; |
|
(b) |
impuritajiet teknikament inevitabbli; |
|
(c) |
migrazzjoni possibbli mill-imballaġġ. |
Dan it-tagħrif jindika biss il-periklu. Huwa f’idejn l-eżaminatur tas-sikurezza li jevalwa r-riskju (16).
Studji dwar l-interazzjonijiet/l-adegwatezza bejn il-formulazzjoni u l-imballaġġ jippermettu li jsiru testijiet dwar il-migrazzjoni potenzjali ta’ ammonti żgħar ta’ sustanzi mill-materjal tal-imballaġġ primarju lejn il-prodott. Dawn it-testijiet isiru f’kundizzjonijiet speċifiċi u relevanti ta’ ttestjar. Madankollu, ma hemm l-ebda proċedura standard għall-prodotti kożmetiċi. Tista’ ssir valutazzjoni xierqa fuq il-bażi tal-għarfien tal-formulazzjoni u l-materjali tal-imballaġġ primarju u ġudizzju ta’ espert b’esperjenza.
Jekk il-migrazzjoni tkun tiddependi fuq il-kundizzjonijiet tal-ħżin, il-kundizzjonijiet korretti għandhom ikunu indikati fuq it-tikketta tal-prodott. Jekk il-formulazzjoni tkun sensittiva għad-dawl jew l-arja, u tiħżien b’mod li tħalli impatt fuq is-sikurezza tal-prodott jew l-effikaċja tiegħu, għandu jintuża l-imballaġġ xieraq.
3.5. Użu normali u raġonevolment prevedibbli
It-taqsima dwar l-użu normali u raġonevolment prevedibbli tal-prodott hija essenzjali biex l-eżaminatur tas-sikurezza jkun jista’ jiddetermina xenarju ta’ esponiment relevanti. L-użu maħsub għandu jkun komunikat kif xieraq lill-konsumatur biex jiġi evitat użu ħażin tal-prodott.
Barra minn hekk, it-twissijiet u spjegazzjonijiet oħrajn fuq it-tikketti għandhom ikunu konsistenti mal-użu normali u raġonevolment prevedibbli identifikat, u għandu jingħata r-raġunament li jiġġustifika l-inklużjoni tagħhom.
Għandha tiġi pprovduta spjegazzjoni ċara tal-użu normali maħsub u l-użu raġonevolment prevedibbli. Pereżempju, fil-każ ta’ xampù, l-użu normali maħsub ikun l-użu fuq ir-ras; użu raġonevolment prevedibbli (mhux maħsub) ikun li jintuża bħala ġell li tinħasel bih. Inġestjoni tkun użu evidentement ħażin.
Għal dan l-għan, jista’ jkun utli approċċ prattiku. Pereżempju, wieħed jista’ jinkludi ritratt tal-imballaġġ jew id-disinn fir-rapport dwar is-sikurezza tal-prodott kożmetiku biex juri l-preżentazzjoni tal-prodott u l-użu maħsub tiegħu. Ikun utli wkoll li jkun hemm ir-rabta mat-twissijiet u t-tikketti, kif enfasizzat fl-Anness I tar-Regolament (KE) Nru 1223/2009 dwar dan il-punt.
3.6. Esponiment għall-prodott kożmetiku
Il-valutazzjoni tal-esponiment hija element essenzjali ta’ valutazzjoni tar-riskju. L-għan ta’ din it-taqsima huwa li tikkwantifika l-ammont tal-prodott kożmetiku li jidħol f’kuntatt mal-partijiet esterni tal-ġisem tal-bniedem jew is-snien u l-membrani mukużi tal-kavità orali b’użu normali jew raġonevolment prevedibbli għal kull użu u l-frekwenza tal-użu.
Il-valutazzjoni tal-esponiment għall-prodott kożmetiku għandha tieħu f’kunsiderazzjoni s-sejbiet rigward l-“użu normali u raġonevolment prevedibbli” fit-taqsima 5 tal-Anness I tar-Regolament (KE) Nru 1223/2009 fir-rigward ta’ sett ta’ elementi li huma elenkati b’mod espliċitu fit-taqsima 6. Fejn xieraq, għandhom jittieħdu f’kunsiderazzjoni rotot ta’ esponiment sekondarji wkoll.
Id-deskrizzjoni tal-kundizzjonijiet konkreti tal-użu għall-fini tal-analiżi tal-esponiment għandha tieħdu f’kunsiderazzjoni wkoll il-parametri li ġejjin:
|
(a) |
it-tip ta’ prodott (eż. tħallih fuqek, tlaħalħu bl-ilma); |
|
(b) |
iż-żona tal-applikazzjoni (eż. ġisem sħiħ, għajnejn, kavità tal-ħalq); |
|
(c) |
l-ammont għal kull applikazzjoni fil-każ ta’ użu normali u raġonevolment prevedibbli, eż. inkluż meta xampù jintuża bħala ġell li tinħasel bih; |
|
(d) |
id-durata u l-frekwenza; |
|
(e) |
ir-rotot possibbli (prevedibbli) ta’ esponiment (eż. orali għal lipstick u toothpaste, jew teħid min-nifs għal aerosols u solventi); |
|
(f) |
grupp fil-mira għall-użu (eż. tfal taħt l-età ta’ tliet snin, adulti); |
|
(g) |
l-impatt tad-daqs tal-partikola fuq l-esponiment. |
In-Noti ta’ Gwida tas-SCCS jipprovdu tagħrif utli dwar il-kalkoli tal-esponiment u tabelli partikolarment relevanti (17).
Madankollu, peress li t-tabelli jista’ ma jkunx fihom il-valuri ta’ esponiment ta’ kuljum għal prodotti kożmetiċi speċifiċi, jistgħu jintużaw modi oħrajn ta’ kalkolu tal-esponiment. Huma possibbli bosta alternattivi. Pereżempju, jistgħu jsiru kalkoli fuq il-bażi ta’ dejta tal-wiċċ tal-ġilda jew ta’ esperjenza tal-utenti.
Jekk id-dejta disponibbli titqies li mhijiex biżżejjed, huwa rakkomandat li jiġi preżunt l-agħar esponiment possibbli filwaqt li jittieħdu f’kunsiderazzjoni l-kundizzjonijiet prevedibbli tal-użu.
Il-popolazzjoni speċifika fil-mira u l-popolazzjoijiet esposti b’xi mod ieħor għall-prodott għandhom jittieħdu f’kunsiderazzjoni. Pereżempju, fil-każ ta’ prodotti għal użu professjonali, ser ikun hemm xenarji ta’ esponiment differenti għall-konsumaturi fil-mira u l-professjonisti esposti f’termini ta’ frekwenza ta’ esponiment, durata tal-esponiment u d-daqs taż-żona tal-ġilda esposta, esponiment possibbli permezz ta’ teħid min-nifs (pereżempju, fil-każ ta’ xampujiet, meta jiġi vvalutat ir-riskju għall-konsumaturi, għandu jiġi kkunsidrat l-esponiment tan-naħa ta’ fuq tar-ras bi frekwenza ta’ madwar darba kuljum, filwaqt li għall-parrukkiera, għandu jittieħed f’kunsiderazzjoni l-esponiment tal-idejn bosta drabi kuljum).
3.7. Esponiment għas-sustanzi
Il-valutazzjoni tal-esponiment għal kull waħda mis-sustanzi li tinsab fil-prodott kożmetiku hija neċessarja sabiex jiġi vvalutat ir-riskju assoċjat ma’ kull sustanza individwali. L-għan ta’ dik it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku huwa li tiddetermina l-ammont ta’ kull sustanza li tidħol f’kuntatt mal-partijiet ta’ barra ta’ ġisem il-bniedem jew is-snien u l-membrani mukużi tal-kavità orali b’użu normali jew raġonevolment prevedibbli, għal kull użu.
L-esponiment għal kull waħda mis-sustanzi fil-prodott kożmetiku huwa kkalkolat mill-esponiment għall-prodott lest u l-konċentrazzjoni tas-sustanzi individwali fil-prodott lest. Hemm bżonn li jiġi kkalkolat dan l-esponiment sabiex jiġi vvalutat ir-riskju potenzjali li ġej minn kull sustanza.
L-esponiment għal sustanzi individwali huwa kkalkolata mill-kompożizzjoni kwantitattiva tal-prodott. Meta jiġu ġġenerati s-sustanzi matul l-użu tal-prodott, l-esponiment għandu jiġi stmat u jittieħed f’kunsiderazzjoni fil-valutazzjoni dwar is-sikurezza.
Il-kundizzjonijiet tal-esponiment għal kull sustanza individwali huma ddeterminati minn dawn għall-prodott kożmetiku lest fi 3.6.
3.8. Il-profil tossikoloġiku tas-sustanzi
L-għan ta’ din it-taqsima tar-rapport dwar is-sikurezza tal-prodott kożmetiku huwa li tiddeskrivi l-periklu tossikoloġiku ta’ kull waħda mis-sustanzi fil-prodott lest, tiddetermina l-esponiment potenzjali, u tfassal karatterizzazzjoni tar-riskju. Dawn l-aspetti huma ta’ importanza kruċjali sabiex issir valutazzjoni tar-riskju, peress li huma t-tliet passi essenzjali tal-proċess ta’ valutazzjoni tar-riskju (18) .
Il-punti ta’ tmiem li għandhom jitqiesu, kif ukoll id-dejta neċessarja, jiddependu fuq għadd ta’ fatturi, inklużi r-rotot tal-esponiment, il-kundizzjonijiet ta’ użu tal-prodott, il-karatteristiċi fiżiko/kimiċi u l-assorbiment possibbli tas-sustanza. L-għażla tal-punti ta’ tmiem relevanti għandha tkun ir-responsabilità tal-eżaminatur tas-sikurezza, li għandu jiġġustifika d-deċiżjonijiet tiegħu.
L-eżaminatur tas-sikurezza għandu jiżgura li d-dejta sperimentali tikkonforma mar-rekwiżiti tal-Artikolu 18 tar-Regolament (KE) Nru 1223/2009 dwar l-ittestjar fuq l-annimali. Dawk ir-rekwiżiti huma ċċarati fil-Komunikazzjoni tal-Kummissjoni dwar dwar l-ittestjar fuq l-annimali u l-projbizzjoni tal-kummerċjalizzazzjoni u dwar il-qagħda attwali fejn jidħlu metodi alternattivi fil-qasam tal-kożmetika (19) .
Il-punt 8 tal-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009 jistabbilixxi r-rekwiżiti ewlenin għar-rapport dwar is-sikurezza tal-prodott kożmetiku f’dak li għandu x’jaqsam mal-profil tossikoloġiku tas-sustanzi.
3.8.1. Kunsiderazzjonijiet ġenerali dwar il-profil tosiskoloġiku bħala parti mill-valutazzjoni dwar is-sikurezza
L-elementi relevanti tal-profil tossikoloġiku ta’ kull sustanza jew taħlita għandhom ikunu deskritti f’dettall fit-tagħrif dwar is-sikurezza tal-prodott kożmetiku (Parti A) u vvalutati fil-valutazzjoni dwar is-sikurezza (Parti B), filwaqt li jinżammu f’kunsiderazzjoni s-sitwazzjoni ta’ esponiment, it-tossiċità intrinsika (jew periklu) ta’ kull sustanza, u l-kundizzjonijiet ta’ użu speċifiċi tal-prodott.
L-esperjenzi umani, studji fuq annimali jew metodi alternattivi għall-ittestjar fuq l-annimali jgħinu biex jinftiehem ir-riskju għas-saħħa tal-bnedmin esposti għal sustanzi perikolużi. Għal profili tossikoloġiċi, jintużaw studji tossikoloġiċi biex jiġu identifikati l-perikli li jistgħu jkunu assoċjati ma’ riskju għall-bnedmin. Huwa essenzjali li jiġu kkunsidrati l-kwalità u l-limitazzjonijiet tal-istudji li saru. Il-validità ta’ studju għandha tittieħed f’kunsiderazzjoni meta jiġi ddeterminat jekk hemmx bżonn ta’ tagħrif ġdid biex jinftiehem ir-riskju għas-saħħa tal-bniedem (20). L-istudji li jsiru skont il-linji gwida internazzjonali huma l-iktar utli, iżda b’xorti ħażina mhux l-istudji kollha jissodisfaw dawn l-istandards. B’hekk, il-limitazzjonijiet ta’ dawk l-istudji għandhom jiġu kkunsidrati fil-valutazzjoni tal-profil tossikoloġiku għal kull sustanza.
L-eżaminatur tas-sikurezza għandu jiżgura li d-dejta sperimentali tikkonforma mar-rekwiżiti tal-Artikolu 18 tar-Regolament (KE) Nru 1223/2009 dwar l-ittestjar fuq l-annimali. Il-Komunikazzjoni mill-Kummissjoni lill-Parlament Ewropew u lill-Kunsill dwar l-ittestjar fuq l-annimali u l-projbizzjoni tal-kummerċjalizzazzjoni u dwar il-qagħda attwali fejn jidħlu metodi alternattivi fil-qasam tal-kożmetika tispjega l-interpretazzjoni tal-Kummissjoni ta’ dawk ir-rekwiżiti (21).
3.8.2. Il-profil tossikoloġiku tas-sustanzi għall-punti ta’ tmiem tossikoloġiċi relevanti kollha
Il-profil tossikoloġiku għal kull sustanza huwa ddeterminat mill-identifikazzjoni tal-periklu u l-karatterizzazzjoni tar-rispons għad-doża.
L-ewwel pass essenzjali fl-iżvilupp tal-profil tossikoloġiku huwa li jinġabar it-tagħrif kollu relevanti dwar il-proprjetajiet intrinsiċi tas-sustanza. Dak it-tagħrif għandu jinkludi dan li ġej:
|
(1) |
Bħala l-iktar tagħrif siewi dwar it-tossiċità, dejta propja ta’ testijiet minn studji in vivo jew in vitro miksubin skont ir-Regolament tal-Kummissjoni (KE) Nru 440/2008 tat-30 ta’ Mejju 2008 li jistabbilixxi metodi ta’ ttestjar skont ir-Regolament (KE) Nru 1907/2006 tal-Parlament Ewropew u tal-Kunsill dwar ir-reġistrazzjoni, il-valutazzjoni, l-awtorizzazzjoni u r-restrizzjoni ta’ sustanzi kimiċi (REACH) (22), linji gwida internazzjonali rikonoxxuti, jew standards (eż. Linji Gwida dwar it-Testijiet tal-OECD), u mwettqin skont prinċipji ta’ prattika tajba tal-laboratorju; |
|
(2) |
Id-dejta eżistenti minn testijiet li ma nkisbitx skont l-aħħar verżjoni adottata/aċċettata ta’ linja gwida dwar it-testijiet jew standards ta’ prattika tajba tal-laboratorju, iżda li titqies valida; |
|
(3) |
Dejta in vitro jew dejta alternattiva minn sistemi validi ta’ ttestjar, li għandhom jintużaw bħala studju ta’ tgħarbil biex titbassar it-tossiċità; |
|
(4) |
Dejta u/jew esperjenza ta’ bnedmin. B’mod ġenerali mhuwiex aċċettabbli li jsiru studji tossokoloġiċi fuq il-bniedem għall-identifikazzjoni tal-periklu, iżda, jekk teżisti dejta jew esperjenza, dawn għandhom jiddaħħlu fil-valutazzjoni finali; |
|
(5) |
Dejta (klinika) umana, inkluża dejta minn provi kliniċi u applikazzjonijiet f’industriji oħrajn bħal prodotti tal-ikel u mediċinali; |
|
(6) |
Dejta miġbura minn sorveljanza ta’ wara t-tqegħid fis-suq; |
|
(7) |
Studji dwar il-kumpatibbiltà fuq voluntiera bnedmin, li għandhom jintużaw biss biex jiġu kkonfermati livelli sikuri ta’ użu għal popolazzjoni fil-mira relevanti (23); |
|
(8) |
Approċċi ta’ read-across (24), ibbażati fuq l-istruttura u l-proprjetajiet kimiċi ta’ sustanzi relatati sabiex titbassar it-tossiċità tal-ingredjent, il-grupp ta’ sustanzi, u dejta mhux tat-testijiet minn eżiti tal-mudelli tal-QSAR. |
Fuq il-bażi ta’ dejta miksuba mis-sorsi kollha disponibbli, u filwaqt li titqies il-kwalità tad-dejta, l-eżaminatur tas-sikurezza jista’ jevalwa l-probabilità ta’ effetti avversi fil-bnedmin permezz ta’ approċċ ta’ “piż tal-evidenza” (25).
Prerekwiżit għal valutazzjoni tar-riskju xierqa huwa d-disponibilità ta’ dejta adegwata. Għal appoġġ addizzjonali fuq din il-kwistjoni, wieħed jista’ jikkonsulta l-gwida għat-tħejjija tad-dossiers tas-sikurezza għall-preżentazzjoni lill-Kumitat Xjentifiku dwar is-Sikurezza tal-Konsumatur (SCCS), imfassla mill-Kumitat innifsu fin-Noti ta’ Gwida tiegħu. Għad li dawn in-Noti ta’ Gwida huma pprovduti għal sustanzi fejn hemm bżonn ta’ awtorizzazzjoni, jiġifieri għal koloranti, preżervattivi u filtri tal-UV, jew li joħolqu tħassib b’xi mod ieħor, ir-rekwiżiti li jfasslu jistgħu jkunu ta’ għajnuna għall-valutazzjoni dwar is-sikurezza tas-sustanzi kollha użati fil-prodotti kożmetiċi. Barra minn hekk, taqsima tal-iktar Noti ta’ Gwida riċenti tiffoka fuq il-valutazzjoni dwar ir-sigurità ta’ prodotti kożmetiċi lesti (26).
Il-profil tossikoloġiku jista’ jindirizza għadd ta’ punti ta’ tmiem differenti. Deċiżjoni finali dwar liema punti ta’ tmiem huma relevanti tittieħed mill-eżaminatur tas-sikurezza fuq bażi ta’ każ b’każ, filwaqt li jittieħdu f’kunsiderazzjoni l-esponiment, l-użu tal-prodott, il-karatteristiċi fiżikokimiċi tas-sustanzi, l-esperjenza bis-sustanzi, eċċ (27). Għandha tingħata attenzjoni wkoll lill-effetti lokali (eż. irritazzjoni u fototossiċità), fejn dawn ikunu relevanti. Meta jitqies li ċertu punt ta’ tmiem mhuwiex relevanti, dan għandu jkun iġġustifikat.
Il-punti ta’ tmiem li jistgħu jkunu relevanti għall-profil tossikoloġiku huma:
|
(1) |
Tossiċità akuta permezz ta’ rotot ta’ esponiment relevanti; |
|
(2) |
Irritazzjoni u korrużjoni; |
|
(3) |
Irritazzjoni tal-ġilda u korrużjoni tal-ġilda; |
|
(4) |
Irritazzjoni tal-membrana mukuża (irritazzjoni tal-għajnejn); |
|
(5) |
Sensitizzazzjoni tal-ġilda; |
|
(6) |
Assorbiment dermali/perkutanju; |
|
(7) |
Tossiċità b’doża ripetuta (normalment studji ta’ 28 jew 90 jum) (28); |
|
(8) |
Mutaġeniċità/ġenotossiċità; |
|
(9) |
Karċinoġeniċità; |
|
(10) |
Tossiċità riproduttiva; |
|
(11) |
Tossikokinetika (Studji tal-ADME); |
|
(12) |
Tossiċità fotokkaġunata; |
Għall-punti ta’ tmiem xierqa, għandhom ikunu identifikati l-iktar konċentrazzjonijiet relevanti jew il-Livelli Bla Effett Ħażin Osservat (NOAEL) jew il-Livelli bl-Inqas Effett Ħażin Osservat (LOAEL) għal użu ulterjuri fil-proċess ta’ karatterizzazzjoni tar-riskju.
Tagħrif addizzjonali rigward dejta speċifika tal-punt ta’ tmiem u l-interpretazzjoni tagħha jista’ jinstab fil-gwida speċifika tal-punt ta’ tmiem (29) imħejjija mill-Aġenzija Ewropea għas-Sustanzi Kimiċi (ECHA) għall-implimentazzjoni tar-Regolament (KE) Nru 1907/2006 tal-Parlament Ewropew u tal-Kunsill (30) dwar ir-reġistrazzjoni, il-valutazzjoni, l-awtorizzazzjoni u r-restrizzjoni ta’ sustanzi kimiċi (REACH).
Għal xi ingredjenti kożmetiċi, eż. ta’ oriġini minerali, minn annimali, botanika u bijoteknoloġika (ara wkoll is-Sustanza ta’ kompożizzjoni mhux magħrufa jew varjabbli, Prodotti kumplessi ta’ reazzjoni jew Materjali bijoloġiċi jew “sustanzi UVCB” taħt ir-REACH) (31), l-identifikazzjoni tagħhom għandha tindirizza bir-reqqa s-sors, il-proċess, l-organiżmi involuti, eċċ. sabiex jiġi evalwat il-profil tossikoloġiku tagħhom.
Jekk ċerti perikli ma jistgħux ikunu indirizzati b’mod suffiċjenti, jew jekk jifdal xi dubji dwar is-sodezza tad-dejta, jistgħu jiddaħħlu fatturi ta’ inċertezza addizzjonali jew jista’ jkun hemm bżonn tiġi ġġenerata iktar dejta.
3.8.3. Kunsiderazzjoni tar-rotot importanti kollha ta’ assorbiment
Rotot ta’ esponiment dermali, orali u tat-teħid min-nifs huma potenzjalment relevanti għall-esponiment tal-bniedem għal prodotti kożmetiċi. Huwa essenzzjali li jiġi kkalkolat l-esponiment sistemiku sabiex jitqabbel man-NOAEL relevanti. Il-proporzjon bejn dawn it-tnejn huwa ddefinit bħala l-marġini ta’ sikurezza, li huwa indikatur ta’ jekk prodott jistax jitqies sikur jew le (ara wkoll it-taqsima 3.8.4 u wara).
L-assorbiment huwa marbut mal-bijodisponibbiltà ta’ sustanza, u huwa essenzjali għall-kalkolu tal-marġini ta’ sikurezza. L-esponiment sistemiku jista’ jiġi kkalkolat bħala:
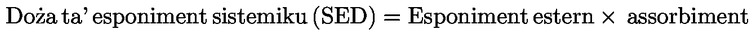
L-assorbiment jista’ jseħħ permezz ta’ bosta rotot esterni: dermali, orali u bit-teħid min-nifs.
Jekk l-esponiment maħsub għall-prodott kożmetiku mhuwiex konformi mar-rotta tal-esponiment fid-dejta ta’ sikurezza, għandha tiġi kkunsidrata estrapolazzjoni ta’ rotta għal rotta.
(a) Assorbiment wara esponiment dermali
L-assorbiment dermali (33) ta’ sustanza fi prodott jiddependi kemm fuq fatturi intrinsiċi (eż. LogPow, piż molekolari) u l-imġiba tagħha fil-veikolu. L-assorbiment dermali in vivo mill-bniedem ta’ sustanza jista’ jiġi stmat billi tintuża d-dejta minn studji in vivo eżistenti fuq annimali u studji in vitro fuq ġilda tal-annimali u tal-bniedem. Meta ma jkun hemm disponibbli ebda dejta ta’ kejl u ma tista’ tiġi ddeterminata l-ebda rata ta’ assorbiment bl-użu ta’ metodu in silico xjentifikament validu jew rati ta’ assorbiment predefiniti, għandu jintuża l-agħar valur possibbli ta’ 100 % għall-kalkolu tal-esponiment sistemiku (34). F’każ li MW > 500 Da u log Pow huwa iżgħar minn – 1 jew ogħla minn 4, jista’ jiġi kkunsidrat valur ta’ assorbiment dermali ta’ 10 %.
(b) Assorbiment wara esponiment orali
Meta użu raġonevolment prevedibbli jista’ jinvolvi inġestjoni, ir-rotta orali għandha tkun inkluża fix-xenarji ta’ esponiment.
(c) Assorbiment wara teħid min-nifs
Għas-sustanzi kollha użati f’applikazzjonijiet bi sprej u xi trabijiet, ir-rotta ta’ teħid min-nifs għandha tittieħed f’kunsiderazzjoni meta jiġi ddeterminat l-esponiment sistemiku.
Barra minn hekk, jista’ jkun hemm ukoll possibilità ta’ esponiment sekondarju tat-teħid min-nifs meta l-prodotti kożmetiċi jkun fihom sustanzi volatili li jistgħu jittieħdu min-nifs bla intenzjoni fil-każ ta’ użu dirett, eż. toluene f’żebgħa tad-dwiefer, bosta sustanzi li jinsabu f’ġellijiet ta’ fformar tad-dwiefer, eċċ.
3.8.4. Kunsiderazzjoni tal-effetti sistemiċi u kalkolu tal-marġini tas-sikurezza
Il-valutazzjoni tas-sikurezza ta’ prodott għat-tossiċità sistemika tiddependi ħafna fuq id-dejta dwar kull sustanza, peress li mhux se jkun hemm dejta dwar it-tossiċità sistemika għall-prodott kożmetiku finali.
Il-karatterizzazzjoni tar-riskji ġeneralment tinvolvi evalwazzjoni esperta tal-effetti negattivi potenzjali mhux kwantifikabbli, segwita b’kalkolu ta’ fattur ta’ inċertezza jew marġini ta’ sikurezza (35). Dan il-kalkolu jiddependi fuq esponiment sistemiku għas-sustanza u l-parametri tossikoloġiċi tagħha.
Skont il-Punt 8 parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009, l -effetti sistemiċi u l-marġini ta’ sikurezza għandhom jiġu kkunsidrati fil-Parti A tar-rapport tas-sikurezza. Peress li huma obbligatorji, l-ommissjoni ta’ dawn il-passi għandha tkun debitament ġustifikata. Eżempju fejn dan jista’ japplika huwa l-preżenza ta’ sustanza fil-prodott kożmetiku fuq livell baxx, bil-livelli ta’ esponiment mistennija (fl-agħar każ) li jkunu taħt il-valuri tal-limitu tat-tħassib tossikoloġiku (TTC) xierqa (36). Eżempju ieħor jista’ jkun l-inklużjoni ta’ materjali tal-ikel li għalihom huwa magħruf livell ħafna aktar għoli ta’ inġestjoni innokwa.
Meta l-ħtieġa għall-kalkolu tal-marġini tas-sikurezza ma tkunx tista’ tintlaħaq, jista’ jkun xieraq mod differenti ta’ kif tiġi espressa d-doża sikura għal kull sustanza, fejn ikun ġustifikat. Meta NOAEL ma jkunx disponibbli, valuri tossikoloġiċi ta’ referenza oħrajn bħall-Livell Bla Effett Osservat (NOEL), LOAEL, il-Livell bl-Inqas Effett Osservat (LOEL), jistgħu jintużaw biex tiġi kkalkulata l-marġini tas-sikurezza; Doża ta’ Riferiment (BMD) jew Doża Prattikament Sikura (VSD), użati biex jikkwalifikaw u jikkwantifikaw ir-riskju f’oqsma oħra, jistgħu jintużaw fil-kuntest ta’ valutazzjoni tas-sikurezza ta’ prodotti kożmetiċi, sakemm tiġi stabbilita relazzjoni mal-esponiment, billi l-esponiment mill-prodotti kożmetiċi jiġi mqabbel ma’ dawn id-dożi ta’ referenza.
Is-sikurezza ta’ sustanza partikolari fi prodott partikolari ma tistax tintwera mod ieħor.
Skont il-proċeduri deskritti fin-Noti ta’ Gwida tal-SCCS (37), il-marġini tas-sikurezza (MOS) għal rotta speċifika ta’ esponiment jista’ jiġi kkalkulat permezz tal-formola li ġejja:

fejn id-doża ta’ esponiment sistemika (SED) tinkiseb billi l-esponiment estern (mg/kg bw/jum) jiġi kkombinat mar-rata tal-assorbiment (tipikament espressa f’ % jew μg/cm2), il-frekwenza u l-fatturi ta’ kapaċità.
Huwa aċċettat b’mod ġenerali li l-marġini tas-sikurezza għandu jkun mill-inqas 100 biex sustanza tiġi ddikjarata sikura għall-użu fi prodott lest.
Fil-każ ta’ estrapolazzjoni minn rotta għal rotta, il-bijodisponibilità rispettiva permezz ta’ kull rotta idealment għandha tiġi kkunsidrata. L-assunzjoni ta’ 100 % bijodisponibilità orali tista’ twassal għal stima għolja ż-żejjed tal-esponiment sistemiku fi studju ta’ tossiċità permezz tar-rotta orali. Għalhekk, fin-nuqqas ta’ dejta, wieħed għandu jassumi li mhux aktar minn 50 % tad-doża mogħtija mill-ħalq tkun disponibbli sistemikament. Jekk ikun hemm prova li tissuġġerixxi bijodisponibilità orali ħażina, pereżempju jekk is-sustanza tkun partikulata li ma tinħallx sew, jista’ jkun aktar xieraq li wieħed jassumi li 10 % biss tad-doża mogħtija tkun disponibbli sistemikament (38). Kull meta tkun disponibbli dejta ta’ assorbiment orali, din għandha tiġi inkluża fil-kalkoli.
In-NOAEL magħżul għall-kalkolu tal-marġini tas-sikurezza jittieħed minn studji ta’ tossiċità b’doża ripetuta fit-tul (testijiet ta’ tossiċità subakuta, subkronika u/jew kronika, testijiet ta’ karċinoġenesi, testijiet ta’ teratoġenesi, tossiċità riproduttiva, eċċ.).
Il-valur użat se jkun l-iktar NOAEL baxx miksub mill-iktar studju pertinenti rigward il-kundizzjonijiet tal-użu tas-sustanza, għas-sensittività tal-ispeċi, eċċ.
Mill-profil tossikoloġiku sħiħ, NOAEL għandu jiġi stabbilit għall-effetti sistemiċi. B’mod ġenerali, l-inqas NOAEL rilevanti tal-iktar limitu rilevanti huwa magħżul għall-kalkolu tal-marġini tas-sikurezza.
Il-kalkolu tal-marġini tas-sikurezza bbażat biss fuq id-dejta tad-Doża Letali Medjana (LD50) miksuba minn testijiet ta’ doża waħda (minflok NOAEL minn mill-inqas testijiet sub-akuti) ma jistax jintuża biex jiġġustifika l-użu sikur.
Meta n-nuqqas ta’ bijodisponibbiltà jista’ jintwera b’mod ċar, il-kalkolu tal-marġini tas-sikurezza ma jkunx meħtieġ. F’dawn il-każijiet għandhom xorta jiġu kkunsidrati l-effetti lokali possibbli fuq il-ġilda jew il-membrani mukużi.
3.8.5. Impatt fuq il-profil tossikoloġiku ta’ ċerti karatteristiċi tas-sustanzi jew tal-prodott
(a) Id-daqs tal-partikoli
Id-daqs tal-partikola u l-kurva ta’ distribuzzjoni tagħha jistgħu jinfluwenzaw it-tossiċità ta’ sustanza. Meta ma jkunx jista’ jiġi eskluż li dawn ikollhom impatt fuq is-sikurezza tal-prodott lest, dawn għandhom jiġu inklużi fost il-karatteristiċi fiżiċi u kimiċi tiegħu, u jiġu kkunsidrati matul il-valutazzjoni tas-sikurezza. L-aktar opinjonijiet xjentifiċi riċenti dwar is-suġġett għandhom jiġu segwiti (SCENIHR, SCCS (39).
(b) Impuritajiet fis-sustanzi u l-materja prima
L-impuritajiet jista’ jkollhom impatt kbir fuq it-tossiċità totali ta’ kull sustanza. Huwa importanti ħafna li jiġi vverifikat il-profil tal-impuritajiet ta’ sustanza biex jiġi evitat, jew għall-inqas evalwat, kwalunkwe riskju addizzjonali mill-impuritajiet. Fin-nuqqas ta’ dejta ta’ sikurezza minn studji tossikoloġiċi, il-limitu tat-tħassib tossikoloġiku (TTC) (40) jista’ jkun għodda utli għall-valutazzjoni tas-sikurezza ta’ ċerti impuritajiet.
Meta l-istudji tossikoloġiċi jiġu użati biex jikkaratterizzaw il-profil tossikoloġiku ta’ sustanza, il-profil tal-purità u l-impuritajiet tas-sustanza użat fl-istudji tossikoloġiċi għandu jiġi deskritt. Jekk il-lottijiet attwalment użati fil-formulazzjoni tal-prodott kożmetiku ma jkollhomx profil ta’ impurità paragunabbli, jeħtieġ li jiġu evalwati d-differenzi.
3.8.6. L-użu ta’ read-across għandu jiġi sostanzjat u ġustifikat
Jeżistu diversi approċċi għat-teknika ta’ read-across. L-użu ta’ din it-teknika għandu jiġi sostanzjat u ġustifikat.
3.8.7. Identifikazzjoni tas-sorsi ta’ informazzjoni
Id-determinazzjoni tal-profil tossikoloġiku teħtieġ informazzjoni minima dwar is-sustanza li se tiġi evalwata.
Din l-informazzjoni tista’ tinġabar minn studji tossikoloġiċi. Jekk teżisti dejta minn esperjenza tal-bniedem, għandha tiġi kkunsidrata.
Għodod oħrajn bħar-relazzjoni kwantitattiva bejn l-istruttura u l-attività (QSAR) jew approċċi ta’ tqarrib huma biss stimi ta’ tossiċità, u l-piż tal-evidenza għandu jkun sostanzjat u ġustifikat.
Is-sorsi tad-dejta li ġejjin għandhom jiġu kkunsidrati:
|
(a) |
Dejta ta’ sikurezza u kwalità li tista’ tkun fil-fajl għand il-fornituri rispettivi tal-materja prima fil-formulazzjoni, u li l-fornitur għandu jaqsmu mal-manifattur tal-prodott kożmetiku. Dan huwa element importanti fil-kunsiderazzjoni tad-disponibbiltà tad-dejta rilevanti biex tintwera s-sikurezza ta’ kull ingredjent kożmetiku fil-formulazzjoni tal-prodott lest; |
|
(b) |
Jekk tkun teżisti opinjoni tal-SCCS, in-NOAEL użat fl-opinjoni għandu jintuża. L-eżaminatur tas-sikurezza għandu jqis l-aktar opinjoni xjentifika aġġornata; |
|
(c) |
Jekk tkun teżisti opinjoni ta’ kumitat xjentifiku awtorevoli ieħor, in-NOAEL użat fl-opinjoni jista’ jintuża, sakemm il-konklużjonijiet u l-limitazzjonijiet ikunu applikabbli għall-użu mistenni (l-użu kkunsidrat għall-kalkolu tal-marġini tas-sikurezza jista’ jkun differenti). L-eżaminatur tas-sikurezza għandu jqis l-iktar opinjoni xjentifika aġġornata; |
|
(d) |
Jekk ma tkun teżisti ebda opinjoni xjentifika, ikun meħtieġ li tingħata informazzjoni biex tikkaratterizza l-profil tossikoloġiku ta’ kull sustanza. Id-dejta tista’ tinkiseb minn diversi databases jew litteratura (ara l-Appendiċi) (41); |
|
(e) |
Il-klassifikazzjoni skont ir-Regolament (KE) Nru 1272/2008 tal-Parlament Ewropew u tal-Kunsill (42); |
|
(f) |
Studji mwettqa jew miksuba mill-manifattur tal-prodott; |
|
(g) |
Previżjoni in silico (QSAR); |
|
(h) |
L-approċċ ta’ tqarrib; |
|
(i) |
Il-valutazzjonijiet ta’ użi mhux kożmetiċi tas-sustanza (oġġetti tal-ikel, addittivi tal-ikel, materjali f’kuntatt mal-ikel, bijoċidi, ir-Reġistrazzjoni, il-Valutazzjoni, l-Awtorizzazzjoni u r-Restrizzjoni ta’ Sustanzi Kimiċi (REACH) …) jistgħu jintużaw ukoll sabiex tiġi kompluta l-informazzjoni dwar il-profil tossikoloġiku tas-sustanza. |
|
(j) |
Meta jkun disponibbli, is-CSR (Rapport dwar is-Sikurezza Kimika) jew is-sommarji robusti tal-istudji sottomessi skont ir-Regolament (KE) Nru 1907/2006 (REACH). |
Għadd ta’ sustanzi u/jew taħlitiet ma ġewx studjati biżżejjed biex jiddeterminaw il-parametri tossikoloġiċi pertinenti kollha. Għal dawn il-parametri neqsin, jew fejn il-karatterizzazzjoni tar-riskju tkun ibbażata fuq approċċ li juża dejta tossikoloġika miksuba għal sustanzi oħrajn (pereżempju strutturi simili) jew għal użi li mhumiex għal prodotti kożmetiċi (ikel, bijoċidi, prodotti farmaċewtiċi, eċċ.), il-ġustifikazzjonijiet għandhom jiġu inklużi fir-rapport.
3.9. Effetti mhux mixtieqa u effetti serji mhux mixtieqa
L-għan ta’ dik it-taqsima tar-rapport tas-sikurezza tal-prodott kożmetiku huwa li tiġi ssorveljata s-sikurezza tal-prodott wara li jkun tqiegħed fis-suq u li tittieħed azzjoni korrettiva, meta jkun meħtieġ. Għal dan il-għan, il-persuna responsabbli (b’kollaborazzjoni mad-distributuri) hija meħtieġa li twaqqaf sistema biex tiġbor, tiddokumenta, tistabbilixxi l- kawżalità u l-ġestjoni tal-effetti mhux mixtieqa kkawżati mill-prodott wara l-użu tiegħu fl-Unjoni (43). Meta l-effetti mhux mixtieqa jkunu serji, il-persuna responsabbli (u d-distributuri) għandhom jinnotifikaw lill-awtorità kompetenti tal-Istat Membru fejn seħħew l-effetti (44).
Informazzjoni dwar effetti mhux mixtieqa u effetti serji mhux mixtieqa għandha tiġi inkluża fir-rapport tas-sikurezza tal-prodott kożmetiku, tinżamm aġġornata u tkun magħmula disponibbli għall-eżaminatur tas-sikurezza, li jista’ jirrevedi l-valutazzjoni tagħhom jew jikkunsidra l-informazzjoni waqt li jivvaluta prodotti simili.
Ir-rapport tas-sikurezza tal-prodott kożmetiku għandu jinkludi l-informazzjoni disponibbli kollha, inkluża dejta statistika, dwar l-effetti mhux mixtieqa u effetti serji mhux mixtieqa tal-prodott kożmetiku jew, fejn rilevanti, ta’ prodotti kożmetiċi oħrajn.
B’mod partikolari, informazzjoni dwar effetti mhux mixtieqa li, skont il-valutazzjoni tal-kawżalità, instab li huma probabbli ħafna, probabbli, mhux attribwibbli b’mod ċar jew mhux probabbli li jkunu attribwibbli (45) għall-prodott kożmetiku inkwistjoni għandha tiġi inkluża fir-rapport tas-sikurezza.
Id-dejta dwar effetti mhux mixtieqa tista’ tiġi inkluża f’din il-parti tar-rapport tas-sikurezza fil-forma ta’ dejta statistika bħall-għadd u t-tip ta’ effetti mhux mixtieqa fis-sena.
Informazzjoni dwar effetti serji mhux mixtieqa li, skont il-valutazzjoni tal-kawżalità, instab li huma probabbli ħafna, probabbli, mhux attribwibbli b’mod ċar jew mhux probabbli li jkunu attribwibbli għall-prodott kożmetiku inkwistjoni għandha tiġi inkluża fir-rapport tas-sikurezza skont it-taqsima 9 tal-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009, u notifikata lill-awtoritajiet nazzjonali kompetenti, skont l-Artikolu 23 tal-istess Regolament (46). Il-formoli ta’ notifika li jintbagħtu lill-awtoritajiet kompetenti għalhekk għandhom jitwaħħlu mar-rapport tas-sikurezza tal-prodott kożmetiku.
Ir-reazzjoni u l-immaniġġjar tal-persuna responsabbli tal-effetti serji rrappurtati mhux mixtieqa għandhom jiġu ddikjarati. Il-miżuri korrettivi u preventivi li ttieħdu, jekk ikun hemm, għandhom jiġu deskritti.
L-informazzjoni dwar effetti mhux mixtieqa għandha tinżamm aġġornata u titpoġġa regolarment għad-dispożizzjoni tal-eżaminatur tas-sikurezza (47), li jista’ jikkunsidra li jkun meħtieġ li jirrevedi l-valutazzjoni tas-sikurezza, jipproponi titjib tal-formulazzjoni jew juża l-informazzjoni biex jistabbilixxi l-valutazzjoni tas-sikurezza għal prodotti simili.
Dejta addizzjonali ta’ kożmetoviġilanza, bħal effetti serji mhux mixtieqa ta’ użu mhux intenzjonat tista’ tipprovdi wkoll informazzjoni utli li l-eżaminatur tas-sikurezza għandu jikkunsidra.
3.10. Informazzjoni dwar il-prodott kożmetiku
Dik it-taqsima tar-rapport tas-sikurezza tal-prodott kożmetiku tippermetti l-inklużjoni ta’ kwalunkwe informazzjoni addizzjonali li mhix koperta taħt l-intestaturi l-oħrajn tal-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009, iżda hija kkunsidrata rilevanti biex titwettaq il-valutazzjoni tas-sikurezza tal-prodott.
Din it-taqsima tar-rapport tas-sikurezza tal-prodott kożmetiku għandha tinkludi informazzjoni rilevanti oħra, relatata mal-prodott jew formulazzjonijiet simili, bħal studji eżistenti dwar voluntiera umani, jew relatati ma’ sustanzi speċifiċi, bħas-sejbiet debitament ikkonfermati u sostanzjati ta’ valutazzjonijiet tar-riskju mwettqa f’oqsma rilevanti oħrajn.
Din it-taqsima tista’ tintuża biex issir referenza għal informazzjoni dwar sustanzi jew taħlitiet użati wkoll f’tipi ta’ prodotti oħrajn, bħal ikel u prodotti farmaċewtiċi.
4. PARTI B TAL-ANNESS I TAR-REGOLAMENT (KE) Nru 1223/2009 — VALUTAZZJONI TAS-SIKUREZZA TAL-PRODOTTI KOŻMETIĊI
Parti B tar-rapport hija l-valutazzjoni attwali tas-sikurezza tal-prodott. Fir-raġunament tiegħu, l-eżaminatur tas-sikurezza huwa meħtieġ li jikkunsidra l-perikli kollha identifikati għall-prodott u l-esponiment għalih.
Parti B tar-rapport tas-sikurezza tal-prodott kożmetiku tinkludi:
|
(1) |
Il-konklużjoni tal-valutazzjoni; |
|
(2) |
It-twissijiet fuq it-tikketta u l-istruzzjonijiet tal-użu; |
|
(3) |
Ir-raġunament; |
|
(4) |
Il-kredenzjali tal-eżaminatur tas-sikurezza u l-approvazzjoni finali tiegħu. |
4.1. Konklużjoni tal-valutazzjoni
Il-konklużjoni tal-valutazzjoni hija stqarrija dwar is-sikurezza tal-prodott kożmetiku rigward il-ħtieġa tas-sikurezza tal-Artikolu 3 tar-Regolament (KE) Nru 1223/2009.
Il-konklużjoni għandha tiddikjara jekk il-prodott huwiex sikur, sikur b’restrizzjonijiet jew mhux sikur għas-saħħa tal-bniedem meta jintuża f’kundizzjonijiet normali jew raġonevolment prevedibbli ta’ użu.
Il-qafas legali għall-valutazzjoni għandu jiġi msemmi espliċitament, b’mod partikolari r-Regolament (KE) Nru 1223/2009 dwar il-prodotti kożmetiċi.
Jekk il-prodott ikun ġie vvalutat bħala mhux sikur, ma jistax jitqies li jikkonforma mar-Regolament (KE) Nru 1223/2009 u għaldaqstant m’għandux jitqiegħed fis-suq.
4.2. Twissijiet fuq it-tikketta u struzzjonijiet tal-użu
L-għan ta’ dik it-taqsima tar-rapport tas-sikurezza tal-prodott kożmetiku huwa li tniżżel b’mod espliċitu l-prekawzjonijiet partikulari li għandhom jiġu osservati fl-użu, inkluż mill-inqas dawk elenkati fl-Annessi III sa VI tar-Regolament (KE) Nru 1223/2009 u kwalunkwe informazzjoni speċjali prekawzjonarja fuq prodotti kożmetiċi għall-użu professjonali, li għandha tidher fuq it-tikketta.
Skont l-Anness I tar-Regolament (KE) Nru 1223/2009, din it-taqsima għandha tkun stqarrija dwar il-ħtieġa li kwalunkwe twissijiet partikolari u struzzjonijiet tal-użu jitniżżlu fuq it-tikketta skont l-Artikolu 19(1)(d) tar-Regolament (KE) Nru 1223/2009.
Il-kompitu tal-eżaminatur tas-sikurezza huwa li jiddetermina liema twissijiet jew struzzjonijiet tal-użu, flimkien ma’ dawk elenkati fl-Annessi III sa VI, għandhom jitniżżlu fuq it-tikketta sabiex ikun żgurat l-użu sikur tal-prodott.
L-eżaminatur tas-sikurezza għandu jiddeċiedi x’għandu jidher fuq it-tikketta skont kull każ, b’kunsiderazzjoni tal-obbligi legali li joħorġu mill-Artikolu 19 u l-Annessi tar-Regolament (KE) Nru 1223/2009 u, fejn rilevanti, strumenti bħar-Rakkomandazzjoni tal-Kummissjoni 2006/647/KE (48) u linji gwida oħrajn ippubblikati mill-Kummissjoni, bħal dawk fuq it-tikketti ta’ “perjodu ta’ żmien wara l-ftuħ” (49) u t-tikketti tal-ingredjenti skont id-Direttiva 76/768/KEE (50).
4.3. Raġunament
Ir-raġunament huwa l-qalba tal-valutazzjoni tas-sikurezza, peress li l-għan tiegħu huwa li jispjega b’mod ċar u preċiż kif l-eżaminatur tas-sikurezza jasal għall-konklużjonijiet tiegħu dwar is-sikurezza tal-prodott kożmetiku mid-dejta miġbura skont il-Parti A tal-Anness I tar-Regolament (KE) Nru 1223/2009.
Il-valutazzjoni tas-sikurezza għandha ssir skont kull każ għal kull prodott kożmetiku individwali u tkun ir-riżultat ta’ evalwazzjoni esperta tad-dejta disponibbli. L-eżaminatur tas-sikurezza għandu jiżgura li l-informazzjoni kollha li jeħtieġ biex iwettaq valutazzjoni tas-sikurezza tkun disponibbli; għandu jivverifika r-rilevanza tad-dejta pprovduta fuq il-prodott li għandu jiġi vvalutat; u għandu jiġġustifika n-nuqqas ta’ dejta meħtieġa skont il-Parti A, meta jqis illi dawn mhumiex rilevanti jew meħtieġa.
Sabiex jasal għal konklużjonijiet dwar is-sikurezza ta’ prodott kożmetiku, l-eżaminatur tas-sikurezza huwa meħtieġ li jevalwa s-sikurezza tas-sustanzi individwali jew taħlitiet preżenti fil-formulazzjoni u s-sikurezza tal-prodott lest. Il-konklużjonijiet tiegħu għandhom ikunu bbażati fuq serje ta’ provi li juru li, minkejja l-perikli kollha identifikati, il-prodott jista’ jitqies sikur f’termini tas-saħħa tal-bniedem.
L-eżaminatur tas-sikurezza jista’ jaċċetta, jirrifjuta, jew jaċċetta taħt kundizzjonijiet speċifiċi l-formulazzjoni kkunsidrata. Prodott li ma jkunx konformi mar-Regolament (KE) Nru 1223/2009 għandu jiġi miċħud u ma jitqiegħedx fis-suq.
Ir-raġunament għall-valutazzjoni tas-sikurezza jistabbilixxi l-kunsiderazzjonijiet li jwasslu lill-eżaminatur tas-sikurezza, fuq il-bażi tal-informazzjoni kollha disponibbli relatata mas-sikurezza, għal konklużjoni ġenerali dwar is-sikurezza ta’ prodott.
Fir-raġunament tiegħu, l-eżaminatur tas-sikurezza huwa meħtieġ li jikkunsidra l-perikli kollha identifikati, il-kundizzjonijiet tal-esponiment maħsuba u raġonevolment prevedibbli tas-sustanzi individwali jew taħlitiet preżenti fil-formulazzjoni u tal-prodott kożmetiku lest.
Il-kompitu tal-eżaminatur tas-sikurezza huwa li jwettaq analiżi u evalwazzjoni tal-validità/affidabbiltà tal-informazzjoni eżistenti kollha. Billi jwettaq din l-analiżi, l-eżaminatur tas-sikurezza jista’ jiddeċiedi jekk id-dejta disponibbli hix biżżejjed biex issir valutazzjoni tas-sikurezza jew jekk għandhiex tiġi miksuba dejta addizzjonali fuq sustanza individwali jew il-prodott kożmetiku lest.
Ir-raġunament huwa bbażat fuq id-dejta miġbura fil-Parti A tar-rapport tas-sikurezza tal-prodott kożmetiku u jikkunsidra l-evalwazzjoni tas-sikurezza tas-sustanzi u t-taħlitiet, imwettqa mill-Kumitat Xjentifiku għas-Sikurezza tal-Konsumatur meta s-sustanzi jidhru fl-Annessi tar-Regolament (KE) Nru 1223/2009, minn kumitati xjentifiċi jew pannelli kompetenti oħrajn, jew mill-eżaminatur tas-sikurezza nnifsu, u l-evalwazzjoni tas-sikurezza tal-prodott kożmetiku.
4.3.1. Evalwazzjoni tas-Sikurezza tas-Sustanzi u/jew Taħlitiet
L-evalwazzjoni tas-sikurezza tas-sustanzi u/jew taħlitiet tikkonsisti fi tliet stadji ewlenin:
|
(1) |
karatterizzazzjoni tal-periklu tas-sustanzi u t-taħlitiet; |
|
(2) |
valutazzjoni tal-esponiment lokali u sistemiku (b’kunsiderazzjoni tad-dejta ta’ assorbiment); |
|
(3) |
valutazzjoni tar-riskju ta’ effetti sistemiċi (kalkolu tal-marġini tas-sikurezza) u valutazzjoni tar-riskju ta’ effetti lokali (bħal allerġija tal-ġilda, irritazzjoni tal-ġilda). |
Għal komposti ta’ fwieħa u togħma, meta l-informazzjoni dwar il-kompożizzjoni tagħhom tkun kunfidenzjali, tista’ tiġi pprovduta valutazzjoni tas-sikurezza lill-persuna responsabbli għall-prodott kożmetiku lest mill-manifattur ta’ dik it-taħlita. B’kunsiderazzjoni tal-konċentrazzjoni fil-prodott kożmetiku lest u x-xejra ta’ esponiment tiegħu, il-valutazzjoni tas-sikurezza tal-kompost tal-fwieħa u t-togħma għandha tiġi ppreparata skont il-prinċipji deskritti fl-Anness I tar-Regolament (KE) Nru 1223/2009 u dawn il-linji gwida. Dokument xieraq li juri s-sikurezza tal-kompost tal-fwieħa jew it-togħma għandu jiġi pprovdut mill-fornitur lill-persuna responsabbli għall-prodott kożmetiku lest.
4.3.2. Evalwazzjoni tas-Sikurezza tal-Prodott Kożmetiku
L-evalwazzjoni tas-sikurezza tal-prodott kożmetiku tkopri tliet aspetti ewlenin:
|
(1) |
Sommarju tal-valutazzjoni tar-riskju bbażat fuq l-effetti lokali u sistemiċi tas-sustanzi individwali/taħlitiet kollha (51); |
|
(2) |
Stima addizzjonali tas-sikurezza tal-prodott ifformulat, li ma jistax jiġi vvalutat permezz tal-valutazzjoni tas-sustanzi/taħlitiet separatament. Dan jista’ pereżempju jkun il-kumpatibbiltà tal-formulazzjoni mal-ġilda, il-valutazzjoni ta’ effetti possibbli ta’ kombinament, bħal ingredjent wieħed li jista’ jżid ir-rata ta’ assorbiment ta’ ingredjent ieħor, l-effetti possibbli li jistgħu jinqalgħu minn interazzjoni mal-materjal tal-ippakkjar, jew l-effetti possibbli minħabba reazzjonijiet kimiċi bejn is-sustanzi individwali/taħlitiet fil-prodott formulat (52); |
|
(3) |
Stima addizzjonali tas-sikurezza tal-prodott ifformulat, li ma jistax jiġi vvalutat permezz tal-valutazzjoni tas-sustanzi/taħlitiet separatament. Dan jista’ pereżempju jkun il-kumpatibbiltà tal-formulazzjoni mal-ġilda, il-valutazzjoni ta’ effetti possibbli ta’ kombinament, bħal ingredjent wieħed li jista’ jżid ir-rata ta’ assorbiment ta’ ingredjent ieħor, l-effetti possibbli li jistgħu jinqalgħu minn interazzjoni mal-materjal tal-ippakkjar, jew l-effetti possibbli minħabba reazzjonijiet kimiċi bejn is-sustanzi individwali/taħlitiet fil-prodott formulat. |
Il-valutazzjoni speċifika tal-prodotti kożmetiċi maħsuba għall-użu fuq it-tfal taħt l-età ta’ tliet snin li hija meħtieġa skont ir-Regolament (KE) Nru 1223/2009 għandha tikkunsidra r-rakkomandazzjonijiet speċifiċi fin-Noti ta’ Gwida tal-SCCS (53).
Fil-valutazzjoni speċifika meħtieġa skont ir-Regolament (KE) Nru 1223/2009 għall-prodotti kożmetiċi maħsuba esklussivament għall-użu fl-iġjene intima esterna, il-karatteristiċi partikolari tal-post tal-applikazzjoni għandhom jiġu kkunsidrati wkoll.
L-eżaminatur tas-sikurezza jista’ jaċċetta, jirrifjuta, jew jaċċetta taħt kundizzjonijiet speċifiċi l-formulazzjoni kkunsidrata. Prodott li ma jikkonformax mar-Regolament (KE) Nru 1223/2009 għandu jiġi miċħud u ma jitqiegħedx fis-suq. Ir-rakkomandazzjonijiet mill-eżaminatur tas-sikurezza dwar l-użu sikur tal-prodott għandhom jiġu segwiti.
Sabiex jiġi żgurat li r-rapport tas-sikurezza tal-prodott kożmetiku jinżamm aġġornat kif meħtieġ mill-Artikolu 10(1)(c) tar-Regolament (KE) Nru 1223/2009, is-sikurezza tal-prodott lest għandha tiġi evalwata mill-ġdid regolarment.
Meta jsiru bidliet fil-ħtiġijiet legali (eż. restrizzjonijiet ta’ waħda mis-sustanzi inklużi fil-formulazzjoni), għandu jiġi vverifikat, fost l-oħrajn (eż. tikkettar), jekk il-formulazzjoni għadhiex konformi mal-liġi, u l-valutazzjoni tas-sikurezza għandha tiġi riveduta u, jekk ikun meħtieġ, aġġornata.
Il-valutazzjoni tas-sikurezza għandha tiġi riveduta wkoll u, jekk meħtieġ, aġġornata, fejn tapplika waħda jew iktar minn waħda miċ-ċirkostanzi li ġejjin:
|
(a) |
sejbiet xjentifiċi ġodda u dejta tossikoloġika dwar is-sustanzi huma disponibbli li jistgħu jimmodifikaw ir-riżultat tal-valutazzjoni tas-sikurezza attwali; |
|
(b) |
bidliet li jseħħu fil-formulazzjoni jew l-ispeċifikazzjonijiet tal-materja prima; |
|
(c) |
bidliet li jseħħu fil-formulazzjoni jew l-ispeċifikazzjonijiet tal-materja prima; |
|
(d) |
tendenza li tiżdied f’termini tan-natura, is-severità u l-frekwenza ta’ effetti mhux mixtieqa, kemm taħt kundizzjonijiet raġonevolment prevedibbli ta’ użu kif ukoll fil-każ ta’ użu mhux korrett (54) |
Għandhom jiġu stabbiliti strutturi u proċessi li jiżguraw li l-informazzjoni rilevanti għall-aġġornament tar-rapport tas-sikurezza tal-prodott kożmetiku tiġi skambjata b’mod effiċjenti bejn il-persuna responsabbli u l-eżaminatur tas-sikurezza, u li l-eżaminatur tas-sikurezza jkun f’pożizzjoni li jintervjeni meta jkun meħtieġ aġġornament.
4.4. Kredenzjali tal-eżaminatur u approvazzjoni tal-Parti B
L-eżaminatur tas-sikurezza għandu jkun professjonist bl-għarfien u l-kompetenza meħtieġa biex ifassal valutazzjoni tas-sikurezza preċiża, kif indikat mill-ħtiġijiet ta’ kwalifika fl-Artikolu 10(2) tar-Regolament (KE) Nru 1223/2009. Dik it-taqsima tar-rapport tas-sikurezza ta’ prodott kożmetiku għandha l-għan li tiżgura li dan ir-rekwiżit jiġi sodisfatt u li tiġi pprovduta l-evidenza meħtieġa.
Dik it-taqsima tar-rapport tas-sikurezza għandha telenka l-isem u l-indirizz tal-eżaminatur tas-sikurezza u jkollha data u tkun iffirmata.
Ir-riżultat tal-valutazzjoni tas-sikurezza għandu jiġi ffirmat b’dikjarazzjoni tad-data ta’ preparazzjoni jew jinħareġ fuq il-bażi ta’ rilaxx elettroniku li jistabbilixxi relazzjoni ċara bejn l-eżaminatur, il-formulazzjoni u d-data tal-valutazzjoni. Il-verżjoni elettronika għandha tiġi protetta mill-abbuż minn persuni mhux awtorizzati.
Skont l-Artikolu 10(2) tar-Regolament (KE) Nru 1223/2009, l-eżaminatur tas-sikurezza huwa meħtieġ li jkun “persuna li jkollha diploma jew evidenza oħra ta’ kwalifiki formali mogħtija wara t-tlestija ta’ kors ta’ studju universitarju ta’ studju teoretiku u prattiku fil-farmaċija, it-tossikoloġija, il-mediċina jew dixxiplina simili, jew ta’ kors rikonoxxut bħala ekwivalenti minn Stat Membru”.
Persuna li tkun kisbet il-kwalifiki f’pajjiż terz tista’ taġixxi bħala eżaminaturtas-sikurezza jekk tkun lestiet “kors rikonoxxut bħala ekwivalenti [għal kors ta’ studju universitarju ta’ studju teoretiku u prattiku fil-farmaċija, it-tossikoloġija, il-mediċina jew dixxiplina simili] minn Stat Membru”.
Għandha tingħata prova tal-kwalifika tal-eżaminatur tas-sikurezza (jiġifieri kopja tad-diploma u, fejn meħtieġ, prova ta’ ekwivalenza) stipulata fl-Artikolu 10 tar-Regolament (KE) Nru 1223/2009.
Referenzi
|
— |
ATSDR (2004). Guidance Manual for the assessment of joint toxic action of chemical mixtures. Atlanta, GA: ATSDR, U.S. Department of Health and Human Services, Public Health Service. EFSA (2008) EFSA-Q-2006-160. |
|
— |
Bremmer H.J., Prud’homme de Lodder L.C.H., van Engelen J.G.M., Cosmetics Fact Sheet to Assess the Risks for the Consumer, Verżjoni aġġornata għall-ConsExpo 4, rapport RIVM 320104001/2006 (http://www.rivm.nl/bibliotheek/rapporten/320104001.pdf) |
|
— |
COSMED, Comment constituer le rapport de sécurité? (Règlement (CE) No 1223/2009), Collection: Les guides pratiques des entreprises - Editions 2011-2012., |
|
— |
CTFA & COLIPA, Guidelines On Stability Testing Of Cosmetic Products, Marzu 2004. |
|
— |
Aġenzija Ewropea għas-Sustanzi Kimiċi (ECHA), Gwida għall-identifikazzjoni u l-għoti ta’ ismijiet lis-sustanzi f’REACH u CLP, Novembru 2011. |
|
— |
Aġenzija Ewropea għas-Sustanzi Kimiċi (ECHA), Gwida dwar ir-rekwiżiti ta’ informazzjoni taħt REACH u Valutazzjonijiet tas-Sikurezza Kimika, Kapitolu R.4: Evalwazzjoni tal-informazzjoni disponibbli, Diċembru 2011. |
|
— |
Aġenzija Ewropea għas-Sustanzi Kimiċi (ECHA), Gwida dwar ir-rekwiżiti ta’ informazzjoni taħt REACH u Valutazzjonijiet tas-Sikurezza Kimika - Kapitolu R.7a: Gwida speċifika dwar il-punti ta’ tmiem, Mejju 2008. |
|
— |
Aġenzija Ewropea għas-Sustanzi Kimiċi (ECHA), Gwida dwar ir-rekwiżiti ta’ informazzjoni taħt REACH u Valutazzjonijiet tas-Sikurezza Kimika - Kapitolu R.7c: Gwida speċifika dwar il-punti ta’ tmiem, Mejju 2008. |
|
— |
ECHA, Gwida Prattika 2: How to report weight of evidence’, 2010, http://echa.europa.eu/documents/10162/13655/pg_report_weight_of_evidence_en.pdf |
|
— |
Kummissjoni Ewropea, Komunikazzjoni mill-Kummissjoni lill-Parlament Ewropew u lill-Kunsill dwar l-ittestjar fuq l-annimali u l-projbizzjoni tal-kummerċjalizzazzjoni u dwar il-qagħda attwali fejn jidħlu metodi alternattivi fil-qasam tal-kożmetika, COM(2013) 135 finali. |
|
— |
Kummissjoni Ewropea, Composition and undesirable effects of cosmetic products to be made easily accessible to the public — practical implementation of Article 7a(1)(h), second subparagraph, of Council Directive 76/768/KEE (http://ec.europa.eu/consumers/sectors/cosmetics/files/doc/guide_access_info_en.pdf) |
|
— |
Kummissjoni Ewropea, Serious Undesirable Effects (SUE) Reporting Guidelines, http://ec.europa.eu/consumers/sectors/cosmetics/files/pdf/sue_reporting_guidelines_en.pdf |
|
— |
Greim H. and Snyder R. (eds), Toxicology and Risk Assessment — A comprehensive Introduction. John Wiley & Sons Ltd., 2008. |
|
— |
Hall B., Tozer S., Safford B., Coroama M., Steiling W., Leneveu-Duchemin M.C., McNamara C. and Gibney M., European consumer exposure to cosmetic products, a framework for conducting population exposure assessments, Food and Chemical Toxicology, Volum 45, Ħarġa 11, Novembru 2007, Paġni 2097-2108. |
|
— |
IGHRC 2006, Guidelines on route-to-route extrapolation of toxicity data when assessing health risks of chemicals. The Interdepartmental Group on Health Risks from Chemicals (2006), http://www.silsoe.cranfield.ac.uk/ieh/ighrc/ighrc.html |
|
— |
Klimisch HJ, Andreae E u Tillmann U, A systematic approach for evaluating the quality of experimental and ecotoxicological data. Regulatory Toxicology and Pharmacology 25 (1997), p. 1-5. |
|
— |
Kroes R., Renwick A. G., Feron V., Galli C. L., Gibney M., Greim H., Guy R. H., Lhuguenot J. C., van de Sandt J. J. M., Application of the threshold of toxicological concern (TTC) to the safety evaluation of cosmetic ingredients, Food and Chemical Toxicology 45 (2007), 2533–2562. |
|
— |
Loretz L.J., Api A.M., Babcock L., Barraj L.M., Burdick J., Cater K.C., Jarrett G., Mann S., Pan Y.H., Re T.A., Renskers K.J., Scrafford C.G., Exposure data for cosmetic products: facial cleanser, hair conditioner, and eye shadow, Food Chem Toxicol. 2008 Mejju; 46(5):1516-24, Epub 2007 Diċembru 23. |
|
— |
Mildau G., Burkhard A., Daphi-Weber J., Große-Damhues J., Jung J., Schuster B., Walther C., Basic Requirements for Safety Assessment of Cosmetic Products, SOFW Journal, 133 6-2007, pp. 16-22. |
|
— |
Miljøstyrelsen, Guideline on Safety Assessment of Cosmetic Products, Environmental Guidelines No 10 2000. |
|
— |
OECD (2007), Guidance on Grouping of Chemicals. Series on Testing and Assessment, No. 80. Pariġi |
|
— |
OECD (2009), Guidance Document for using the OECD (Q)SAR Application Toolbox to Develop Chemical Categories According to the OECD Guidance on Grouping of Chemicals. Series on Testing and Assessment, No. 102. Pariġi |
|
— |
Pauwels M., Rogiers V., Human Health Safety Evaluation of Cosmetics in the EU: A Legally Imposed Challenge to Science, Toxicology and Applied Pharmacology, 243 (2010), pp. 260-274. |
|
— |
SCCS (Scientific Committee on Consumer Safety), Guidance on safety assessment of nanomaterials in cosmetics, SCCS/1484/12. |
|
— |
SCCS, The SCCS’s Notes of Guidance for the Testing of Cosmetic Ingredients and their Safety Evaluation, it-Tmien Reviżjoni, SCCS/1501/12. |
|
— |
SCCS, SCHER u SCENIHR, Opinion on Use of the Threshold of Toxicological Concern (TTC) Approach for Human Safety Assessment of Chemical Substances with focus on Cosmetics and Consumer Products, SCCP/1171/08. |
|
— |
SCCS, SCHER and SCENIHR, Toxicity and Assessment of Chemical Mixtures, 2012. |
|
— |
SCENIHR (Scientific Committee on Emerging and Newly Identified Health Risks), Opinion on the scientific basis for the definition of the term “nanomaterial”, 8 ta’ Diċembru 2010. |
|
— |
Rapport tal-Workshop “Assessment of undesirable events in cosmetic market surveillance: Background, description and use of a causality assessment method in cosmetovigilance”, Regulatory Toxicology and Pharmacology 58 (2010) 349–353. |
(1) Artikolu 11(2) tar-Regolament (KE) Nru 1223/2009.
(2) Artikolu 10(1) tar-Regolament (KE) Nru 1223/2009.
(3) Artikolu 10(1)(c) tar-Regolament (KE) Nru 1223/2009.
(4) In-Noti ta’ Gwida tal-SCCS għall-Ittestjar tal-Ingredjenti Kożmetiċi u l-Evalwazzjoni tas-Sikurezza tagħhom, it-Tmien Reviżjoni, SCCS/1501/12, u l-aġġornamenti sussegwenti tagħhom.
(5) Noti ta’ Gwida tal-SCCS, para. 3-6.2, p. 35-36.
(6) Dan il-punt huwa rilevanti fil-kuntest tal-Prattiki ta’ Manifattura Tajba, u huwa indirizzat espliċitament mill-istandard rilevanti EN ISO 22716.2007. B’mod aktar speċifiku, dan jaqbel mal-ħtiġijiet għall-ħruġ tal-materja prima u l-prodott lest.
(7) Ara t-taqsima 3.3 dwar il-Kwalità mikrobijoloġika.
(8) Ara l-“Implimentazzjoni prattika tal-Artikolu 6(1)(c) tad-Direttiva dwar il-Kożmetiċi (76/768/KEE): TIKKETTAR TAD-DURABBILTÀ TAL-PRODOTT: ‘PERJODU TA’ ŻMIEN WARA L-FTUĦ’ ” (Direttiva tal-Kunsill 76/768/KEE, ĠU L 262, 27.9.1976, p. 169) http://ec.europa.eu/consumers/sectors/cosmetics/files/doc/wd-04-entr-cos_28_rev_version_adoptee20040419_en.pdf
(9) Noti ta’ Gwida tal-SCCS, para. 4-3.3, p. 74.
(10) Id-“data tad-durabbiltà minima” hija d-data sa meta l-prodott kożmetiku, maħżun f’kundizzjonijiet xierqa, jibqa’ jissodisfa l-funzjoni inizjali tiegħu u, b’mod partikolari, jibqa’ sikur; il-PAO huwa l-perjodu ta’ żmien wara l-ftuħ li fih il-prodott jista’ jintuża mingħajr ebda periklu għall-konsumatur. Ara l-“Implimentazzjoni prattika tal-Artikolu 6(1)(c) tad-Direttiva dwar il-Kożmetiċi (76/768/KEE): TIKKETTAR TAD-DURABBILTÀ TAL-PRODOTT: ‘PERJODU TA’ ŻMIEN WARA L-FTUĦ’ ”.
(11) Noti ta’ Gwida tal-SCCS, para 4-4, p. 75–76.
(12) L-Artikolu 17 tar-Regolament (KE) Nru 1223/2009 jistabbilixxi li t-traċċi ta’ sustanzi pprojbiti huma permessi biss jekk ikunu teknikament inevitabbli u jekk ma jkollhom l-ebda impatt fuq is-sikurezza tal-prodotti kożmetiċi.
(13) Is-“sustanzi ġenotossiċi u karċinoġeniċi mingħajr livell limitu” huma s-sustanzi ġenotossiċi u karċinoġeniċi bla livell limitu għall-effetti karċinoġeniċi-ġenotossiċi.
(14) Opinjoni tal-Kumitat Xjentifiku fuq talba mill-EFSA relatata ma’ Approċċ Armonizzat għall-Valutazzjoni tar-Riskju ta’ Sustanzi Li huma kemm Ġenotossiċi kif ukoll Karċinoġeniċi, (traduzzjoni mhux uffiċjali) Il-Ġurnal tal-EFSA (2005) 282, pp. 1-31.
(15) ĠU L 338, 13.11.2004, p. 4.
(16) Biex jevalwa r-riskju, wieħed għandu jqis il-periklu flimkien mal-esponiment, u dan huwa d-dmir tal-eżaminatur tas-sikurezza.
(17) Noti ta’ Gwida tal-SCCS, para 4, p. 66 et seq.
(18) M. Pauwels, V. Rogiers, Human Health Safety Evaluation of Cosmetics in the EU: A Legally Imposed Challenge to Science, Toxicology and Applied Pharmacology, 243 (2010), p. 261.
(19) Komunikazzjoni mill-Kummissjoni lill-Parlament Ewropew u lill-Kunsill dwar l-ittestjar fuq l-annimali u l-projbizzjoni tal-kummerċjalizzazzjoni u dwar il-qagħda attwali fejn jidħlu metodi alternattivi fil-qasam tal-kożmetika, COM(2013) 135 finali.
(20) H.J. Klimisch, E. Andreae u U. Tillmann (1997), A systematic approach for evaluating the quality of experimental and ecotoxicological data. Regul Toxicol Pharmacol 25:1-5.
(21) Ara, b’mod partikolari, il-punt 3.1 tal-Komunikazzjoni.
(22) ĠU L 142, 31.5.2008, p. 1.
(23) Noti ta’ Gwida tal-SCCS, para. 3.4.11. Cf. ukoll l-opinjonijiet SCCNFP/0068/98, verżjoni preċedenti tan-Noti ta’ Gwida, u SCCNFP/0245/99 dwar Kriterji Bażiċi tal-Protokolli għall-Ittestjar tal-Kompatibilità mal-Ġilda ta’ Ingredjenti Kożmetiċi jew Taħlitiet ta’ Ingredjenti li Potenzjalment Jirritaw il-Ġilda fuq Voluntiera Bnedmin (traduzzjoni mhux uffiċjali).
(24) Read-across hija teknika għall-mili ta’ vojt fid-dejta li fiha t-tagħrif għal sustanza kimika waħda jew iktar jintuża biex isir tbassir għal sustanza kimika fil-mira, li titqies simili b’xi mod. Mill-ECHA, “Gwida dwar ir-rekwiżiti ta’ tagħrif u valutazzjoni dwar is-sikurezza kimika Kapitolu R.4: Evalwazzjoni tat-tagħrif disponibbli” (traduzzjoni mhux uffiċjali), Diċembru 2011, p. 12. http://echa.europa.eu/documents/10162/17235/information_requirements_r4_en.pdf
(25) Definizzjoni minnhom ta’ piż tal-evidenza hija: “l-proċess tal-konsiderazzjoni tas-saħħiet u n-nuqqasijiet ta’ diversi biċċiet ta’ informazzjoni biex tintlaħaq u tiġi sostnuta konklużjoni li tikkonċerna proprjetà tas-sustanza.” Mill-ECHA, “Gwida Prattika 2: Kif tirrapporta l-piż tal-evidenza” (traduzzjoni mhux uffiċjali), 2010, p. 2, http://echa.europa.eu/documents/10162/13655/pg_report_weight_of_evidence_mt.pdf
(26) Cfr. Noti ta’ Gwida tal-SCCS, Taqsima 3-6 Rekwiżiti Bażiċi għal Sustanzi Kożmetiċi Preżenti fi Prodotti Kożmetiċi Lesti (li għandhom ikunu evalwati minn eżaminaturi individwali tas-sikurezza) (traduzzjoni mhux uffiċjali).
(27) In-Noti ta’ Gwida tal-SCCS jindirizzaw biċ-ċar din il-kwistjoni fil-para. 3-6.1 Rekwiżiti tossikoloġiċi ġenerali (traduzzjoni mhux uffiċjali).
(28) Skont in-Noti ta’ Gwida tal-SCCS (para. 3-4.5), għandha tingħata prijorità lin-NOAEL fir-rigward ta’ tossiċità sottokronika (studju ta’ 90 jum). Huwa biss jekk it-tali valuri ma jkunux disponibbli li għandhom jintużaw ir-riżultati relatati mat-tossiċità sottoakuta (studju ta’ 28 jum).
(29) ECHA, Gwida dwar ir-rekwiżiti ta’ tagħrif u l-valutazzjoni tas-sikurezza kimika - Kapitolu R.7a: Gwida speċifika tal-punti ta’ tmiem, (traduzzjoni mhux uffiċjali) Mejju 2008.
(30) ĠU L 396, 30.12.2006, p. 1.
(31) Cfr. ECHA, Gwida għall-identifikazzjoni l-għoti ta’ ismijiet lil sustanzi taħt REACH u CLP, Novembru 2011, p. 29. http://echa.europa.eu/documents/10162/17235/substance_id_mt.pdf
(32) Jiġifieri“id-doża sistemikament disponibbli li tgħaddi l-ostakli fiżiċi relevanti (strutturi gastrointestinali, tal-ġilda jew tal-pulmun) u ssir disponibbli fid-demm għal distribuzzjoni sussegwenti fit-tessuti u l-organi”, ref. M. Pauwels, V. Rogiers, p. 262.
(33) Kriterji bażiċi għall-valutazzjoni in vitro tal-assorbiment dermali tal-ingredjenti kożmetiċi (SCCS/1358/10).
(34) Nota ta’ Gwida tal-SCCS, para 3-7.2, p. 49.
(35) M. Pauwels, V. Rogiers, p. 262.
(36) SCCS, SCHER and SCENIHR, Opinjoni dwar l-Użu tal-Approċċ tal-Limitu tat-Tħassib Tossikoloġiku (TTC) għall-Valutazzjoni għas-Sikurezza tal-Bniedem tas-Sustanzi Kimiċi b’attenzjoni fuq il-Prodotti Kożmetiċi u l-Prodotti tal-Konsumatur, SCCP/1171/08.
(37) Nota ta’ Gwida tal-SCCS, para 3-7, p. 46.
(38) IGHRC, Linji gwida dwar estrapolazzjoni minn rotta għal rotta ta’ dejta ta’ tossiċità fil-valutazzjoni tar-riskji tas-saħħa tas-sustanzi kimiċi. Il-Grupp Interdipartimentali dwar ir-Riskji tas-Saħħa mis-Sustanzi Kimiċi (2006), http://www.silsoe.cranfield.ac.uk/ieh/ighrc/ighrc.html
(39) Ara pereżempju: SCCS (il-Kumitat Xjentifiku dwar is-Sikurezza tal-Konsumatur, SCCS/1484/12; SCENIHR (il-Kumitat Xjentifiku dwar ir-Riskji Emerġenti għas-Saħħa u dawk Identifikati Reċentement), Opinjoni dwar il-bażi xjentifika għad-definizzjoni tat-terminu “nanomaterjal”, 8 ta’ Diċembru 2010.
(40) R. Kroes, A. G. Renwick, V. Feron, C. L. Galli, M. Gibney, H. Greim, R. H. Guy, J. C. Lhuguenot, J. J. M. van de Sandt, Applikazzjoni tal-limitu tat-tħassib tossikoloġiku (TTC) għall-evalwazzjoni tas-sikurezza tal-ingredjenti kożmetiċi, Tossikoloġija tal-Ikel u Kimika 45 (2007), pp. 2533–2562.
(41) Jeżistu diversi databases diponibbli pubblikament li fihom dejta tossikoloġika dwar sustanzi użati fil-kożmetika, u dawn huma elenkati fl-Appendiċi għal din il-Linja Gwida.
(42) ĠU L 353, 31.12.2008, p. 1, u l-websajt tar-reġistrazzjoni tal-ECHA: http://echa.europa.eu/mt/information-on-chemicals/registered-substances
(43) Din hija konsegwenza tar-rekwiżit tal-Artikolu 23 tar-Regolament (KE) Nru 1223/2009, li jistabbilixxi l-obbligu li l-persuni responsabbli jirrapportaw effetti serji mhux mixtieqa lill-awtoritajiet kompetenti fl-Istati Membri tal-UE.
(44) L-Artikolu 23 tar-Regolament (KE) Nru 1223/2009.
(45) Għal effetti mhux mixtieqa li huwa probabbli ħafna jew probabbli li jkunu attribwibbli għall-prodott kożmetiku, japplika l-Artikolu 21 tar-Regolament (KE) Nru 1223/2009, “Aċċess għall-informazzjoni għall-pubbliku”.
(46) Il-Kummissjoni Ewropea, Linji Gwida ta’ Rappurtar dwar Effetti Serji Mhux Mixtieqa (SUE), http://ec.europa.eu/consumers/sectors/cosmetics/files/pdf/sue_reporting_guidelines_en.pdf
(47) Dan huwa obbligu tal-persuna responsabbli skont l-Artikolu 10(1)(c) tar-Regolament (KE) Nru 1223/2009.
(48) ĠU L 265, 26.9.2006, p. 39.
(49) Disponibbli fuq http://ec.europa.eu/consumers/sectors/cosmetics/documents/guidelines/labelling/index_en.htm
(50) Disponibbli fuq http://ec.europa.eu/consumers/sectors/cosmetics/files/doc/guide_labelling200802_en.pdf
(51) Għal prodotti tal-istess iskala, fejn l-unika differenza fost prodotti differenti huwa l-aġent li jagħti kulur, u li m’għandu ebda impatt fuq is-sikurezza eż. għal lipsticks jew make-up ieħor tal-kulur, jista’ jiġi kkunsidrat rapport tas-sikurezza ta’ prodott ikkombinat, iżda għandu jkun ġustifikat.
(52) SCCS, SCHER, SCENIHR, Tossiċità u Valutazzjoni ta’ Taħlitiet Kimiċi, 2012 http://ec.europa.eu/health/scientific_committees/environmental_risks/docs/scher_o_155.pdf
(53) Noti ta’ Gwida tal-SCCS, para 3-7.3, p. 51.
(54) Il-Kummissjoni Ewropea, Linji Gwida ta’ Rappurtar dwar Effetti Serji Mhux Mixtieqa (SUE), http://ec.europa.eu/consumers/sectors/cosmetics/files/pdf/sue_reporting_guidelines_en.pdf
Appendiċi
Databases Magħrufa li Fihom Dejta Tossikoloġika dwar Sustanzi Użati fil-Prodotti Kosmetiċi
ChemIDPlus Light— http://chem.sis.nlm.nih.gov/chemidplus/chemidlite.jsp
ChemIDPlus Advanced— http://chem.sis.nlm.nih.gov/chemidplus/
Cosmetics Europe Recommendations— https://www.cosmeticseurope.eu/publications-cosmetics-europe-association/recommendations.html
IPCS Inchem— http://www.inchem.org/pages/jecfa.html
PubMed— http://www.ncbi.nlm.nih.gov/pubmed
ToxNet— http://toxnet.nlm.nih.gov/