ISSN 1725-518X
Az Európai Unió
Hivatalos Lapja
C 276

Magyar nyelvű kiadás
Tájékoztatások és közlemények
51. évfolyam
2008. október 31.
|
ISSN 1725-518X |
||
|
Az Európai Unió Hivatalos Lapja |
C 276 |
|

|
||
|
Magyar nyelvű kiadás |
Tájékoztatások és közlemények |
51. évfolyam |
|
Közleményszám |
Tartalom |
Oldal |
|
|
IV Tájékoztatások |
|
|
|
AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ TÁJÉKOZTATÁSOK |
|
|
|
Bizottság |
|
|
2008/C 276/01 |
||
|
2008/C 276/02 |
||
|
2008/C 276/03 |
||
|
|
TAGÁLLAMOKTÓL SZÁRMAZÓ TÁJÉKOZTATÁSOK |
|
|
2008/C 276/04 |
||
|
2008/C 276/05 |
A tagállamok tájékoztatása az EK-Szerződés 87. és 88. cikkének a kis- és középvállalkozásoknak nyújtott állami támogatásokra történő alkalmazásáról szóló 70/2001/EK bizottsági rendelet értelmében engedélyezett állami támogatásokról ( 1 ) |
|
|
2008/C 276/06 |
A tagállamok tájékoztatása az EK-Szerződés 87. és 88. cikkének a kis- és középvállalkozásoknak nyújtott állami támogatásokra történő alkalmazásáról szóló 70/2001/EK bizottsági rendelet értelmében engedélyezett állami támogatásokról ( 1 ) |
|
|
|
||
|
2008/C 276/12 |
||
|
|
|
|
|
(1) EGT-vonatkozású szöveg |
|
HU |
|
IV Tájékoztatások
AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ TÁJÉKOZTATÁSOK
Bizottság
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/1 |
Euro-átváltási árfolyamok (1)
2008. október 30.
(2008/C 276/01)
1 euro=
|
|
Pénznem |
Átváltási árfolyam |
|
USD |
USA dollár |
1,3035 |
|
JPY |
Japán yen |
128,73 |
|
DKK |
Dán korona |
7,4478 |
|
GBP |
Angol font |
0,7907 |
|
SEK |
Svéd korona |
9,811 |
|
CHF |
Svájci frank |
1,48 |
|
ISK |
Izlandi korona |
305 |
|
NOK |
Norvég korona |
8,52 |
|
BGN |
Bulgár leva |
1,9558 |
|
CZK |
Cseh korona |
24,48 |
|
EEK |
Észt korona |
15,6466 |
|
HUF |
Magyar forint |
257,24 |
|
LTL |
Litván litász/lita |
3,4528 |
|
LVL |
Lett lats |
0,7093 |
|
PLN |
Lengyel zloty |
3,565 |
|
RON |
Román lej |
3,6375 |
|
SKK |
Szlovák korona |
30,39 |
|
TRY |
Török líra |
1,9842 |
|
AUD |
Ausztrál dollár |
1,9204 |
|
CAD |
Kanadai dollár |
1,5697 |
|
HKD |
Hongkongi dollár |
10,1052 |
|
NZD |
Új-zélandi dollár |
2,2015 |
|
SGD |
Szingapúri dollár |
1,9141 |
|
KRW |
Dél-Koreai won |
1 665,72 |
|
ZAR |
Dél-Afrikai rand |
13,0194 |
|
CNY |
Kínai renminbi |
8,9133 |
|
HRK |
Horvát kuna |
7,1699 |
|
IDR |
Indonéz rúpia |
13 914,86 |
|
MYR |
Maláj ringgit |
4,6046 |
|
PHP |
Fülöp-szigeteki peso |
63,09 |
|
RUB |
Orosz rubel |
34,7912 |
|
THB |
Thaiföldi baht |
45,381 |
|
BRL |
Brazil real |
2,7521 |
|
MXN |
Mexikói peso |
16,6978 |
Forrás: Az Európai Központi Bank (ECB) átváltási árfolyama.
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/2 |
A forgalombahozatali engedélyekről szóló közösségi határozatok összefoglalása a gyógyszerkészítmények tekintetében 2008. szeptember 1-jétől2008. szeptember 30-ig
(Közzététel a 726/2004/EK európai parlamenti és tanácsi rendelet (1) 13. és 38. cikke értelmében)
(2008/C 276/02)
– Forgalombahozatali engedély kiadása (a 726/2004/EK rendelet 13. cikke): Elfogadva
|
Határozat időpontja |
Gyógyszerkészítmény neve |
INN (nemzetközi szabadnév) |
A forgalombahozatali engedély jogosultja |
Gyógyszerkészítmény száma a közösségi nyilvántartásban |
Gyógyszerforma |
ATC-kód (anatómiai és terápiás kémiai kód) |
Értesítés időpontja |
|||
|
2008.9.12. |
Oprymea |
Pramipexol |
|
EU/1/08/469/001-025 |
Tabletta |
NO4BC05 |
2008.9.15. |
|||
|
2008.9.15. |
Tevagrastim |
Filgrasztim |
|
EU/1/08/445/001-008 |
Injekcióhoz vagy infúzióhoz való oldat |
L03AA02 |
2008.9.17. |
|||
|
2008.9.15. |
Biograstim |
Filgrasztim |
|
EU/1/08/450/001-008 |
Injekcióhoz vagy infúzióhoz való oldat |
L03AA02 |
2008.9.17. |
|||
|
2008.9.15. |
Ratiograstim |
Filgrasztim |
|
EU/1/08/444/001-008 |
Injekcióhoz vagy infúzióhoz való oldat |
L03AA02 |
2008.9.17. |
|||
|
2008.9.15. |
Filgrastim ratiopharm |
Filgrasztim |
|
EU/1/08/449/001-008 |
Injekcióhoz vagy infúzióhoz való oldat |
L03AA02 |
2008.9.17. |
|||
|
2008.9.26. |
Prepandemic influenza vaccine (H5N1) (split virion inactivated adjuvanted) GlaxoSmithKline Biologicals |
Prepandémiás influenza (H5N1) vakcina (split virion, inaktivált, adjuvánshoz kötött) A/VietNam/1194/2004 NIBRG |
|
EU/1/08/478/001 |
Szuszpenzió és emulzió emulziós injekcióhoz |
J07BB02 |
2008.9.30. |
|||
|
2008.9.30. |
Xarelto |
Rivaroxaban |
|
EU/1/08/472/001-008 |
Filmtabletta |
B01AX06 |
2008.10.2. |
– Forgalombahozatali engedély módosítása (a 726/2004/EK rendelet 13. cikke): Elfogadva
|
Határozat időpontja |
Gyógyszerkészítmény neve |
A forgalombahozatali engedély jogosultja |
Gyógyszerkészítmény száma a közösségi nyilvántartásban |
Értesítés időpontja |
|||||
|
2008.9.1. |
Aranesp |
|
EU/1/01/185/001-073 |
2008.9.3. |
|||||
|
2008.9.1. |
Adenuric |
|
EU/1/08/447/001-004 |
2008.9.3. |
|||||
|
2008.9.3. |
||||||||
|
2008.9.1. |
Rotarix |
|
EU/1/05/330/001-011 |
2008.9.3. |
|||||
|
2008.9.1. |
Zostavax |
|
EU/1/06/341/001-013 |
2008.9.3. |
|||||
|
2008.9.2. |
Ziagen |
|
EU/1/99/112/001-002 |
2008.9.4. |
|||||
|
2008.9.2. |
Lucentis |
|
EU/1/06/374/001 |
2008.9.4. |
|||||
|
2008.9.2. |
Olanzapine Neopharma |
|
EU/1/07/426/001-011 |
2008.9.4. |
|||||
|
2008.9.2. |
SonoVue |
|
EU/1/01/177/002 |
2008.9.4. |
|||||
|
2008.9.2. |
Gardasil |
|
EU/1/06/357/001-021 |
2008.9.5. |
|||||
|
2008.9.2. |
Viramune |
|
EU/1/97/055/001-003 |
2008.9.4. |
|||||
|
2008.9.2. |
Ventavis |
|
EU/1/03/255/001-006 |
2008.9.4. |
|||||
|
2008.9.2. |
Silgard |
|
EU/1/06/358/001-021 |
2008.9.4. |
|||||
|
2008.9.2. |
Cetrotide |
|
EU/1/99/100/001-003 |
2008.9.5. |
|||||
|
2008.9.2. |
Olanzapine Teva - |
|
EU/1/07/427/001-057 |
2008.9.4. |
|||||
|
2008.9.2. |
Elaprase |
|
EU/1/06/365/001-003 |
2008.9.4. |
|||||
|
2008.9.3. |
Tysabri |
|
EU/1/06/346/001 |
2008.9.8. |
|||||
|
2008.9.3. |
Comtess |
|
EU/1/98/082/001-003 EU/1/98/082/005 |
2008.9.8. |
|||||
|
2008.9.3. |
Aldara |
|
EU/1/98/080/001 |
2008.9.5. |
|||||
|
2008.9.3. |
Tamiflu |
|
EU/1/02/222/001-004 |
2008.9.5. |
|||||
|
2008.9.3. |
Mirapexin |
|
EU/1/97/051/001-006 EU/1/97/051/009-012 |
2008.9.5. |
|||||
|
2008.9.3. |
Aldara |
|
EU/1/98/080/001 |
2008.9.5. |
|||||
|
2008.9.3. |
Comtan |
|
EU/1/98/081/001-004 |
2008.9.8. |
|||||
|
2008.9.3. |
Cialis |
|
EU/1/02/237/001-008 |
2008.9.5. |
|||||
|
2008.9.5. |
Mircera |
|
EU/1/07/400/017-021 |
2008.9.9. |
|||||
|
2008.9.5. |
Herceptin |
|
EU/1/00/145/001 |
2008.9.9. |
|||||
|
2008.9.5. |
Puregon |
|
EU/1/96/008/038-041 |
2008.9.9. |
|||||
|
2008.9.5. |
Epivir |
|
EU/1/96/015/001-005 |
2008.9.9. |
|||||
|
2008.9.8. |
Evra |
|
EU/1/02/223/001-003 |
2008.9.10. |
|||||
|
2008.9.9. |
Herceptin |
|
EU/1/00/145/001 |
2008.9.11. |
|||||
|
2008.9.12. |
Viread |
|
EU/1/01/200/001-002 |
2008.9.15. |
|||||
|
2008.9.15. |
Sustiva |
|
EU/1/99/110/001-009 |
2008.9.17. |
|||||
|
2008.9.15. |
Glubrava |
|
EU/1/07/421/001-009 |
2008.9.17. |
|||||
|
2008.9.15. |
Stalevo |
|
EU/1/03/260/001-023 |
2008.9.17. |
|||||
|
2008.9.16. |
Combivir |
|
EU/1/98/058/001-002 |
2008.9.18. |
|||||
|
2008.9.17. |
Optisulin |
|
EU/1/00/133/001-008 |
2008.9.19. |
|||||
|
2008.9.17. |
Lantus |
|
EU/1/00/134/001-037 |
2008.9.19. |
|||||
|
2008.9.22. |
Emtriva |
|
EU/1/03/261/001-003 |
2009.9.24. |
|||||
|
2008.9.22. |
Emend |
|
EU/1/03/262/001-008 |
2008.9.24. |
|||||
|
2008.9.26. |
Aclasta |
|
EU/1/05/308/001-002 |
2008.9.30. |
|||||
|
2008.9.26. |
Thelin |
|
EU/1/06/353/001-005 |
2008.9.30. |
|||||
|
2008.9.29. |
Mycamine |
|
EU/1/08/448/001-002 |
2008.10.1. |
|||||
|
2008.10.1. |
– Forgalombahozatali engedély visszavonása (a 726/2004/EK rendelet 13. cikke)
|
Határozat időpontja |
Gyógyszerkészítmény neve |
A forgalombahozatali engedély jogosultja |
Gyógyszerkészítmény száma a közösségi nyilvántartásban |
Értesítés időpontja |
|||||
|
2008.9.26. |
Exubera |
|
EU/1/05/327/001-018 |
2008.9.30. |
– Forgalombahozatali engedély kiadása (a 726/2004/EK rendelet 38. cikke): Elfogadva
|
Határozat időpontja |
Gyógyszerkészítmény neve |
INN (nemzetközi szabadnév) |
A forgalombahozatali engedély jogosultja |
Gyógyszerkészítmény száma a közösségi nyilvántartásban |
Gyógyszerforma |
ATC-kód (anatómiai és terápiás kémiai kód) |
Értesítés időpontja |
|||||
|
2008.9.9. |
Trocoxil |
Mavacoxib |
|
EU/2/08/084/001-005 |
Rágótabletta |
QM01AH92 |
2008.9.11. |
– Forgalombahozatali engedély módosítása (a 726/2004/EK rendelet 38. cikke): Elfogadva
|
Határozat időpontja |
Gyógyszerkészítmény neve |
A forgalombahozatali engedély jogosultja |
Gyógyszerkészítmény száma a közösségi nyilvántartásban |
Értesítés időpontja |
|||||
|
2008.9.2. |
Advocate |
|
EU/2/03/039/001-030 |
2008.9.4. |
|||||
|
2008.9.4. |
||||||||
|
2008.9.5. |
Profender |
|
EU/2/05/054/001-031 |
2008.9.9. |
|||||
|
2008.9.9. |
||||||||
|
2008.9.15. |
Oxyglobin |
|
EU/2/99/015/002 |
2008.9.17. |
|||||
|
2008.9.19. |
DRAXXIN |
|
EU/2/03/041/001-005 |
2008.9.23. |
|||||
|
2008.9.26. |
PRAC-TIC |
|
EU/2/06/066/001-012 |
2008.9.30. |
– Forgalombahozatali engedély módosítása (a 726/2004/EK rendelet 38. cikke): Elutasítva
|
Határozat időpontja |
Gyógyszerkészítmény neve |
A forgalombahozatali engedély jogosultja |
Gyógyszerkészítmény száma a közösségi nyilvántartásban |
Értesítés időpontja |
||||
|
2008.9.26. |
Porcilis Pesti |
|
EU/2/99/016/001-006 |
2008.9.30. |
Amennyiben betekintést kíván nyerni a szóban forgó gyógyszerkészítmények nyilvános értékelési jelentésébe és a kapcsolódó határozatokba, a következővel vegye fel a kapcsolatot:
|
The European Medicines Agency |
|
7 Westferry Circus |
|
Canary Wharf |
|
London E14 4HB |
|
United Kingdom |
(1) HL L 136., 2004.4.30., 1. o.
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/9 |
A forgalombahozatali engedélyekről szóló közösségi határozatok összefoglalása a gyógyszerkészítmények tekintetében 2008. szeptember 1-jétől2008. szeptember 30-ig
(A 2001/83/EK európai parlamenti és tanácsi irányelv (1) 34. cikke vagy a 2001/82/EK európai parlamenti és tanácsi irányelv (2) 38. cikke értelmében elfogadott határozatok)
(2008/C 276/03)
– A nemzeti forgalombahozatali engedély kiadása, fenntartása vagy módosítása
|
Határozat időpontja |
Gyógyszerkészítmény neve(i) |
A forgalombahozatali engedély jogosultja(i) |
Érintett tagállam |
Értesítés időpontja |
|||||
|
2008.9.3. |
Cozaar |
L. I. melléklet |
L. I. melléklet |
2008.9.8. |
|||||
|
2008.9.3. |
Cozaar Comp |
L. II. melléklet |
L. II. melléklet |
2008.9.8. |
|||||
|
2008.9.9. |
Arcoxia |
L. III. melléklet |
L. III. melléklet |
2008.9.11. |
|||||
|
2008.9.9. |
Etoricoxib |
L. IV. melléklet |
L. IV. melléklet |
2008.9.11. |
|||||
|
2008.9.11. |
Activelle |
L. V. melléklet |
L. V. melléklet |
2008.9.15. |
|||||
|
2008.9.11. |
Rapinyl |
L. VI. melléklet |
L. VI. melléklet |
2008.9.15. |
|||||
|
2008.9.15. |
Remeron |
L. VII. melléklet |
L. VII. melléklet |
2008.9.17. |
|||||
|
2008.9.23. |
Gemzar |
L. VIII. melléklet |
L. VIII. melléklet |
2008.9.24. |
|||||
|
2008.9.26. |
Nátrium-szalicilát |
L. IX. melléklet |
L. IX. melléklet |
2008.9.29. |
|||||
|
2008.9.26. |
Toltrazuril |
L. X. melléklet |
L. X. melléklet |
2008.9.29. |
|||||
|
2008.9.26. |
Aclasta |
|
Ennek a határozatnak a tagállamok a címzettjei |
2008.9.29. |
– A nemzeti forgalombahozatali engedély felfüggesztése
|
Határozat időpontja |
Gyógyszerkészítmény neve(i) |
A forgalombahozatali engedély jogosultja(i) |
Érintett tagállam |
Értesítés időpontja |
|
2008.9.9. |
Pulairmax |
L. XI. melléklet |
L. XI. melléklet |
2008.9.11. |
– A nemzeti forgalomba hozatali engedély felfüggesztésének hatályon kívül helyezése
|
Határozat időpontja |
Gyógyszerkészítmény neve(i) |
A forgalombahozatali engedély jogosultja(i) |
Érintett tagállam |
Értesítés időpontja |
|
2008.9.5. |
Suramox 15 % LA — Stabox 15 % LA |
L. XII. melléklet |
L. XII. melléklet |
2008.9.9. |
(1) HL L 311., 2001.11.28., 67. o.
(2) HL L 311., 2001.11.28., 1. o.
I. MELLÉKLET
A GYÓGYSZERKÉSZÍTMÉNYEK MEGNEVEZÉSEI, GYÓGYSZERFORMÁ(K), HATÁSERŐSSÉG(EK), AZ ALKALMAZÁS MÓDJAI, KÉRVÉNYEZŐ(K), A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA(I) A TAGÁLLAMOKBAN
|
Tagállam |
A forgalomba hozatali engedély jogosultja |
Kereskedelmi név Lozartán-kálium |
Hatáserősség |
Gyógyszerforma |
Az alkalmazás módja |
||||||
|
Ausztria |
|
Cosaar 12,5 mg — Filmtabletten |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Ausztria |
|
Cosaar 50 mg — Filmtabletten |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Ausztria |
|
Cosaar 100 mg — Filmtabletten |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Cozaar 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Cozaar 50 MG |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Cozaar 12,5 mg |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Cozaar Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Loortan 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Loortan 50 mg |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Loortan 12,50 mg |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Loortan Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Bulgária |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Ciprus |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Ciprus |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Dánia |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Dánia |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Dánia |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Dánia |
|
Cozaar Startpakke |
12,5 mg + 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Észtország |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Észtország |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Észtország |
|
Cozaar 12,5 mg |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Finnország |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Finnország |
|
Cozaar |
12,5 mg and 50 mg (initiation pack) |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Finnország |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Finnország |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Franciaország |
|
Cozaar 100 mg film-coated tablets |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Franciaország |
|
Cozaar 50 mg scored coated tablets |
50 mg |
Törésvonallal és bevonattal ellátott tabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Cardopal Start 12,5 mg Filmtabletten |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Lorzaar 100 mg Filmtabletten |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Lorzaar 50 mg Filmtabletten |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Lorzaar Protect 100 mg Filmtabletten |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Lorzaar Protect 50 mg Filmtabletten |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Lorzaar Start 12,5 mg Filmtabletten |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Pinzaar 100 mg Filmtabletten |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Pinzaar 50 mg Filmtabletten |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Lorzaar Varipharmstart 12,5 mg Filmtabletten |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Görögország |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Görögország |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Görögország |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Magyarország |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Magyarország |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Magyarország |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Írország |
|
Cozaar 50 mg Film-coated tablets |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Írország |
|
Cozaar 100 mg Film-coated tablets |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Írország |
|
Cozaar 12,5 mg Film-coated tablets |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Lortaan 50 mg compresse rivestite con film |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Lortaan 12,5 mg compresse rivestite con film |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Lortaan 100 mg compresse rivestite con film |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Neo-Lotan 50 mg compresse rivestite con film |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Neo-Lotan 12,5 mg compresse rivestite con film |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Neo-Lotan 100 mg compresse rivestite con film |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Losaprex 50 mg compresse rivestite con film |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Losaprex 12,5 mg compresse rivestite con film |
12.5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Losaprex 100 mg compresse rivestite con film |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lettország |
|
Cozaar 50 mg film-coated tablets |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lettország |
|
Cozaar 100 mg film-coated tablets |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Litvánia |
|
Cozaar (Losartan) |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Litvánia |
|
Cozaar (Losartan) |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Litvánia |
|
Cozaar (Losartan) |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Cozaar 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Cozaar 50 MG |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Cozaar 12,5 mg |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Cozaar Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Loortan 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Loortan 50 mg |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Loortan 12,50 mg |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Loortan Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Málta |
|
“Cozaar 100 mg” pilloli miksija b'rita |
10 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Málta |
|
“Cozaar 50 mg” pilloli miksija b'rita |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Hollandia |
|
Cozaar 50 |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Hollandia |
|
Cozaar 100 |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lengyelország |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lengyelország |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lengyelország |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Cozaar 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Cozaar IC |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Cozaar IC — Titulação |
12,5 mg + 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Lortaan IC |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Lortaan IC — Titulação |
12,5 mg + 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Lortaan |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Lortaan 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Románia |
|
Cozaar, comprimate filmate, 50 mg |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Szlovénia |
|
Cozaar 12,5 mg filmsko obložene tablete |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Szlovénia |
|
Cozaar 50 mg filmsko obložene tablete |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Szlovénia |
|
Cozaar 100 mg filmsko obložene tablete |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Spanyolország |
|
Cozaar 12,5 mg Inicio |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Spanyolország |
|
Cozaar 50 mg |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Spanyolország |
|
Cozaar 100 mg |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Svédország |
|
Cozaar 12,5 mg filmdragerade tabletter |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Svédország |
|
Cozaar 12,5 mg + 50 mg filmdragerade tabletter |
12,5 + 50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Svédország |
|
Cozaar 50 mg filmdragerade tabletter |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Svédország |
|
Cozaar 100 mg filmdragerade tabletter |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Egyesült Királyság |
|
Cozaar 50 mg Film-coated tablets |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Egyesült Királyság |
|
Cozaar 25 mg Film-coated tablets |
25 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Egyesült Királyság |
|
Cozaar 100 mg Film-coated tablets |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Izland |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Izland |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Izland |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Norvégia |
|
Cozaar |
12,5 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Norvégia |
|
Cozaar |
50 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Norvégia |
|
Cozaar |
100 mg |
Filmtabletta |
Szájon át történő alkalmazás |
II. MELLÉKLET
A GYÓGYSZERKÉSZÍTMÉNYEK MEGNEVEZÉSEI, GYÓGYSZERFORMÁ(K), HATÁSERŐSSÉG(EK), AZ ALKALMAZÁS MÓDJAI, KÉRVÉNYEZŐ(K), A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA(I) A TAGÁLLAMOKBAN
|
Tagállam |
A forgalomba hozatali engedély jogosultja |
Kereskedelmi név Lozartán-kálium és hidroklorotiazid |
Hatáserősség |
Gyógyszerforma |
Az alkalmazás módja |
|||||||
|
Ausztria |
|
Cosaar Plus — Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Ausztria |
|
Fortzaar-Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Belgium |
|
Cozaar Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Belgium |
|
Cozaar Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Belgium |
|
Loortan Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Belgium |
|
Loortan Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Bulgária |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Ciprus |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Ciprus |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Dánia |
|
Cozaar Comp. |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Dánia |
|
Cozaar Comp. Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Dánia |
|
Cozaar Comp. 100 mg/12,5 mg |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Dánia |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Észtország |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Észtország |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Finnország |
|
Cozaar Comp |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Finnország |
|
Cozaar Comp |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Finnország |
|
Cozaar Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Franciaország |
|
Fortzaar 100 mg/25 mg comprimé pelliculé |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Franciaország |
|
Hyzaar 100 mg/25 mg comprimé pelliculé |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Franciaország |
|
Fortzaar 50 mg/12,5 mg comprimé pelliculé |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Franciaország |
|
Hyzaar 50 mg/12,5 mg comprimé pelliculé |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Franciaország |
|
Fortzaar 100 mg/12,5 mg comprimé pelliculé |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Lorzaar Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Cardopal Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Lorzaar Varipharm Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Fortzaar 100/25 mg Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Fortzaar Varipharm 100/25 mg Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Lorzaar Plus Forte 100/12,5 mg Filmtabletten |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Görögország |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Görögország |
|
Hyzaar 100/25 |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Magyarország |
|
Hyzaar 50/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Magyarország |
|
Hyzaar Forte 100/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Írország |
|
Cozaar' Comp 50 mg/12,5 mg film-coated tablets |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Írország |
|
Cozaar' Comp 100 mg/25 mg film-coated tablets |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Hizaar 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Hizaar 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Forzaar 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Neo-Lotan Plus 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Neo-Lotan Plus 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Losazid 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Losazid 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Lettország |
|
Hyzaar 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Lettország |
|
Fortzaar 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Litvánia |
|
Fortzaar (Losartan/Hydrochlorothiazide) |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Litvánia |
|
Hyzaar (Losartan/Hydrochlorothiazide) |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Luxemburg |
|
Cozaar Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Luxemburg |
|
Cozaar Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Luxemburg |
|
Loortan Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Luxemburg |
|
Loortan Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Málta |
|
“Cozaar Comp” 50/12,5 mg pilloli miksija b'rita |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Málta |
|
“Cozaar Comp” 100/25 mg pilloli miksija b'rita |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Málta |
|
“Cozaar Comp” 100/12,5 mg pilloli miksija b'rita |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Hollandia |
|
Cozaar Plus 100/12,5 |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Hollandia |
|
Fortzaar 100/25 |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Hollandia |
|
Hyzaar 50/12,5 |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Lengyelország |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Lengyelország |
|
Hyzaar Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Cozaar Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Cozaar Plus |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Siaara |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Lortaan Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Lortaan Plus |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Losartan + Hidroclorotiazida Frosst |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Románia |
|
Hyzaar® 50 mg/12,5 mg comprimate filmate |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Románia |
|
Fortzaar® 100/25 mg comprimate filmate |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Szlovénia |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Szlovénia |
|
Hyzaar |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Szlovénia |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Spanyolország |
|
Cozaar Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Spanyolország |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Svédország |
|
Cozaar Comp 50 mg/12,5 mg filmdragerade tabletter |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Svédország |
|
Cozaar Comp 100 mg/12,5 mg filmdragerade tabletter |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Svédország |
|
Cozaar Comp Forte 100 mg/25 mg filmdragerade tabletter |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Egyesült Királyság |
|
Cozaar-Comp 50/12,5 mg film-coated tablets |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Egyesült Királyság |
|
Cozaar-Comp 100/25 mg film-coated tablets |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Egyesült Királyság |
|
Cozaar-Comp 100 mg/12,5 mg film-coated tablets |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Izland |
|
Cozaar-Comp 50/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Izland |
|
Cozaar-Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Izland |
|
Cozaar-Comp 100/12,5 mg |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Norvégia |
|
Cozaar Comp |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Norvégia |
|
Cozaar Comp |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Norvégia |
|
Cozaar Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Filmtabletta |
Szájon át történő alkalmazás |
III. MELLÉKLET
FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMÁK, GYÓGYSZERKÉSZÍTMÉNY-DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐK, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Név |
Dózis |
Gyógyszerforma |
Alkalmazási mód |
||||||
|
Ausztria |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Belgium |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Cseh Köztársaság |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Ciprus |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Dánia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Észtország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Finnország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Franciaország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Németország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Görögország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Magyarország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Izland |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Írország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Olaszország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lettország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Litvánia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Luxemburg |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Málta |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Hollandia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Norvégia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Lengyelország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Portugália |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Szlovákia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Szlovénia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Spanyolország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Svédország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
||||||
|
Egyesült Királyság |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
IV. MELLÉKLET
FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMÁK, GYÓGYSZERKÉSZÍTMÉNY-DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐK, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Név |
Dózis |
Gyógyszerforma |
Alkalmazási mód |
|||||||
|
Ausztria |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Auxib |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Belgium |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Ranacox |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Bulgária |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Cseh Köztársaság |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Ciprus |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Dánia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Észtország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Finnország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Turox |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Franciaország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Németország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Görögország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Magyarország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Izland |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Írország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Algix |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Recoxib |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Olaszország |
|
Tauxib |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Lettország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Litvánia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Luxemburg |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Ranacox |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Málta |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Hollandia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Auxib |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Norvégia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Lengyelország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Exxiv |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Portugália |
|
Turox |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Románia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Szlovákia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Szlovénia |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Spanyolország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Spanyolország |
|
Exxiv |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Svédország |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Turox |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Egyesült Királyság |
|
Arcoxia |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||
|
Auxib 90 |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Exxiv 90 |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
|||||||||
|
Turox 90 |
90 mg |
Filmtabletta |
Szájon át történő alkalmazás |
V. MELLÉKLET
FELSOROLÁS: MEGNEVEZÉSEK, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY-HATÁSERŐSSÉG(EK), ALKALMAZÁSI MÓD, KÉRELMEZŐK/FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Kérelmező |
(Kereskedelmi) név |
Hatáserősség |
Gyógyszerforma |
Alkalmazási mód |
|||||
|
Ausztria |
|
|
Noviana 0,5 mg/0,1 mg Filmtabletten |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Belgium |
|
|
Activelle minor comprimés pelliculés |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Bulgária |
|
|
Eviana филмирани таблетки |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Cseh Köztársaság |
|
|
Noviana potahované tablety |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Dánia |
|
|
Activelle low filmovertrukne tabletter |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Észtország |
|
|
Activelle |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Finnország |
|
|
Activelle 0,5 mg/0,1 mg tabl. |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Franciaország |
|
|
Activelle 0,5 mg/0,1 mg, comprimé pelliculé |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Németország |
|
|
Noviana |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Magyarország |
|
|
Noviana filmtabletta |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Izland |
|
|
Activelle low 0,5 mg/0,1 mg tablets filmuhúðaðar töflur |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Írország |
|
|
Activelle Tablets |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Olaszország |
|
|
Activelle 0,5 mg/0,1 mg compresse film-rivestite |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Lettország |
|
|
Noviana 0,5 mg/0,1 mg apvalkotās tabletes |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Litvánia |
|
|
Activelle |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Luxemburg |
|
|
Activelle comprimés pelliculés |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Hollandia |
|
|
Activelle filmomhulde tabletten |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Norvégia |
|
|
Noviana 0,5 mg/0,1 mg tablett filmdrasjert |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Portugália |
|
|
Activelle |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Románia |
|
|
Noviana comprimate filmate |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Szlovákia |
|
|
Noviana |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Szlovénia |
|
|
Noviana filmsko obložene tablete |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Spanyolország |
|
|
Activelle 0,5 mg/ 0,1 mg comprimidos recubiertos de película |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Svédország |
|
|
Activelle |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
|||||
|
Egyesült Királyság |
|
|
Noviana film-coated tablets |
0,5 mg ösztradiol (hemihidrát formájában) + 0,1 mg noretiszteron-acetát |
Filmtabletta |
Szájon át történő alkalmazás |
VI. MELLÉKLET
FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY-DÓZIS, ALKALMAZÁSI MÓD, KÉRELMEZŐ, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Kérelmező |
(Törzskönyvezett megnevezés) Név |
Dózis |
Gyógyszerforma |
Alkalmazási mód |
||||
|
Ausztria |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Belgium |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Ciprus |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Cseh Köztársaság |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Dánia |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Észtország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Finnország |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Franciaország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Németország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Görögország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Magyarország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Izland |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Írország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Olaszország |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Lettország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Litvánia |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Luxemburg |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Norvégia |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Lengyelország |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Portugália |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Szlovákia |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Szlovénia |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Spanyolország |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Svédország |
|
|
Abstral |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
||||
|
Egyesült Királyság |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Nyelvalatti tabletta |
Nyelvalatti alkalmazás |
(1) Név jóváhagyása függőben.
VII. MELLÉKLET
FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMÁK, GYÓGYSZERKÉSZÍTMÉNY-DÓZISOK, ALKALMAZÁSI MÓDOK, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
|
Tagállam |
A forgalomba hozatali engedély jogosultja |
INN (nemzetközi szabadnév) |
Törzskönyvezett megnevezés |
Hatáserősség |
Gyógyszerforma |
Alkalmazás módja |
Hatóanyagtartalom (koncentráció) |
|||||||
|
Ausztria |
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Belgium |
Delegation of power:
|
Mirtazapine |
Remergon |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remergon |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Ciprus |
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Cseh Köztársaság |
|
Mirtazapine |
REMERON 15 MG |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
REMERON 30 MG |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON 45 MG |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 15 MG |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 30 MG |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 45 MG |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Dánia |
|
Mirtazapine |
Mitazon Smelt |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Mitazon Smelt |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mitazon Smelt |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mitazon |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
||||||||
|
Mirtazapine |
Remeron Smelt |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Oral, opløsning |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Észtország |
|
Mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Finnország |
|
Mirtazapine |
Remeron Soltab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron Soltab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Soltab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazon |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
||||||||
|
Mirtazapine |
Mirtazon Smelt |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazon Smelt |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazon Smelt |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Franciaország |
|
Mirtazapine |
Norset |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Norset |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Norset |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Norset |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Norset |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Norset |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Németország |
|
Mirtazapine |
Remergil |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remergil |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergil |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergil |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazapin STADA |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
||||||||
|
Mirtazapine |
Mirtazapin STADA |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapin STADA |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Görögország |
|
Mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Magyarország |
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Izland |
|
Mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron 15 mg/ml |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Írország |
|
Mirtazapine |
Zispin® film-coated tablets |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Zispin® film-coated tablets |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Zispin® film-coated tablets |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Zispin® oral solution |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Olaszország |
|
mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Lettország |
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Litvánia |
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron Sol Tab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Sol Tab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron Sol Tab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Luxemburg |
Delegation of power:
|
Mirtazapine |
Remergon |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remergon |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remergon |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Hollandia |
|
Mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron drank |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Norvégia |
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron mikstur, oppløsning |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Lengyelország |
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Portugália |
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazon |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
||||||||
|
Mirtazapine |
Mirtazon |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazon |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Románia |
|
Mirtazapine |
Remeron SolTab 15 mg |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron SolTab 30 mg |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron SolTab 45 mg |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Szlovákia |
|
Mirtazapine |
REMERON 15 mg |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
REMERON 30 mg |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON 45 mg |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 15 mg |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 30 mg |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 45 mg |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Spanyolország |
|
Mirtazapine |
Rexer |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Rexer |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Rexer |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Rexer |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
||||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Svédország |
|
Mirtazapine |
Remeron |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron-S |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron-S |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Remeron-S |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Egyesült Királyság |
|
Mirtazapine |
Mirtazapine 15 mg tablets |
15 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||
|
Mirtazapine |
Mirtazapine 30 mg tablets |
30 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapine 45 mg tablets |
45 mg |
Filmtabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Mirtazapine 15 mg/ml oral solution |
15 mg/ml |
Belsőleges oldat |
Szájon át történő alkalmazásra |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Zispin SolTab 15 mg orodispersible tablet |
15 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Zispin SolTab 30 mg orodispersible tablet |
30 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
|||||||||
|
Mirtazapine |
Zispin SolTab 45 mg orodispersible tablet |
45 mg |
Szájban diszpergálódó tabletta |
Szájon át történő alkalmazásra |
|
VIII. MELLÉKLET
FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY-DÓZISOK, ALKALMAZÁSI MÓD, KÉRELMEZŐK, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Kereskedelmi név |
Hatáserősség |
Gyógyszerforma |
Az alkalmazás módja |
||||||
|
Ausztria |
|
Gemzar 200 mg — Trockensubstanz zur Infusionsbereitung |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Ausztria |
|
Gemzar 1 g — Trockensubstanz zur Infusionsbereitung |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Belgium |
|
Gemzar 1000 |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Belgium |
|
Gemzar 200 |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Bulgária |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Bulgária |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Cseh Köztársaság |
|
Gemzar 1 g |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Cseh Köztársaság |
|
Gemzar 200 mg |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Ciprus |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Ciprus |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Dánia |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Dánia |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Észtország |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Észtország |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Finnország |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Finnország |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Franciaország |
|
Gemzar 1 000 mg, poudre pour solution pour perfusion |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Franciaország |
|
Gemzar 200 mg, poudre pour solution pour perfusion |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Németország |
|
Gemzar 200 mg Pulver zur Herstellung einer Infusionslösung |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Németország |
|
Gemzar 1 g Pulver zur Herstellung einer Infusionslösung |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Görögország |
|
ΓΚΕΜΖΑΡ |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Görögország |
|
ΓΚΕΜΖΑΡ |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Magyarország |
|
Gemzar 1 g powder for injection |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Magyarország |
|
Gemzar 200 mg powder for injection |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Írország |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Írország |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Izland |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Izland |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Olaszország |
|
Gemzar 200 mg powder for solution for infusion and intravesical instillation |
200 mg |
Por oldatos infúzióhoz és intravesicalis alkalmazáshoz |
Intravénás alkalmazás és intravesicalis alkalmazás |
||||||
|
Olaszország |
|
Gemzar 1 g powder for solution for infusion and intravesical instillation |
1 g |
Por oldatos infúzióhoz és intravesicalis alkalmazáshoz |
Intravénás alkalmazás és intravesicalis alkalmazás |
||||||
|
Lettország |
|
Gemzar |
1 g |
Por oldatos infúzióhoz intravesicalis alkalmazás |
Intravénás alkalmazás |
||||||
|
Lettország |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Litvánia |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Litvánia |
|
Gemzar |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Luxemburg |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Luxemburg |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Málta |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Málta |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Hollandia |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Hollandia |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Norvégia |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Norvégia |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Lengyelország |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Lengyelország |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Portugália |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Portugália |
|
Gemzar |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Románia |
|
Gemzar 1 g |
1 000 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Románia |
|
Gemzar 200 mg |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Szlovákia |
|
Gemzar 1 g |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Szlovákia |
|
Gemzar 200 mg |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Szlovénia |
|
Gemzar 200 mg prašek za raztopino za infundiranje |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Szlovénia |
|
Gemzar 1 g prašek za raztopino za infundiranje |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Spanyolország |
|
Gemzar 1 g powder for solution for injection |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Spanyolország |
|
Gemzar 200 mg powder for solution for injection |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Svédország |
|
Gemzar |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Svédország |
|
Gemzar |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Egyesült Királyság |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
||||||
|
Egyesült Királyság |
|
Gemzar 1g powder for solution for infusion |
1 g |
Por oldatos infúzióhoz |
Intravénás alkalmazás |
IX. MELLÉKLET
MEGNEVEZÉS, GYÓGYSZERFORMA, HATÁSERŐSSÉG, ÁLLATFAJOK, ALKALMAZÁSI MÓDOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA/KÉRELMEZŐ
|
Tagállam/forgalomba hozatali engedély száma |
Forgalomba hozatali engedély jogosultja |
Termék törzskönyvezett neve |
Gyógyszerforma |
Hatáserősség/hatóanyag (INN) |
Állatfaj |
|
Ausztria (8-00694) |
Chevita Tierarzneimittel Ges.m.b.H. |
Asprimax 850 mg/g |
Por belsőleges oldathoz |
Nátrium-szalicilát |
Sertés |
|
Hollandia (REG NL 8913) |
Dopharma Research B.V. |
NA-SALICYLAAT, 100 %-os por belsőleges oldathoz |
Por belsőleges oldathoz |
Nátrium-szalicilát |
Borjak és sertés |
|
Hollandia (REG NL 10411) |
Dopharma Research B.V. |
NA-SALICYLAAT, 80 % WSP |
Por belsőleges oldathoz |
Nátrium-szalicilát |
Borjak és sertés |
|
A 33. cikk alapján benyújtott beterjesztés szerinti decentralizált eljárás (2008. április 17-i bizottsági határozat) |
Eurovet Animal Health B.V. |
SOLACYL 100 %, por belsőleges oldathoz borjak és malacok számára |
Por belsőleges oldathoz |
|
Borjak és sertés |
X. MELLÉKLET
AZ ÁLLATGYÓGYÁSZATI KÉSZÍTMÉNYEK MEGNEVEZÉSEI, GYÓGYSZERFORMÁI, HATÁSERŐSSÉGE, ÁLLATFAJOK, ALKALMAZÁSI MÓDOK, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI LISTÁJA A TAGÁLLAMOKBAN
|
Tagállam |
A termék törzskönyvezett neve |
Forgalomba hozatali engedély jogosultja Cég neve és címe |
Állatfaj |
Gyógyszerforma |
Hatáserősség |
Javallatok |
||||||||
|
Ausztria |
Baycox 25 mg/ml Lösung zum Eingeben für Hühner und Puten |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Belgium |
Baycox 2,5 % orale oplossing |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Bulgária |
Baycox 2,5 % solution |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Bulgária |
Cevazuril oral solution |
|
Brojlercsirkék, tenyészcsirkék, jércék és pulykák |
Belsőleges oldat |
25 mg/ml |
Coccidiosis megelőzése és kezelése |
||||||||
|
Ciprus |
Baycox 2,5 % oral solution |
|
Brojlercsirkék és pulykák |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Cseh Köztársaság |
Baycox 2,5 % sol. ad us. vet. |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Franciaország |
Baycox 2,5 % |
|
Csirke: brojlercsirkék, jércék és tenyészcsirkék |
Belsőleges oldat |
25 mg/ml |
Coccidiosis megelőzése és kezelése |
||||||||
|
Franciaország |
CEVAZURIL |
|
Csirke: brojlercsirkék, jércék és tenyészcsirkék |
Belsőleges oldat |
25 mg/ml |
Coccidiosis megelőzése és kezelése |
||||||||
|
Németország |
Baycox 2,5 % |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Görögország |
Baycox 2,5 % oral solution |
|
Brojlercsirkék és pulykák |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Magyarország |
Baycox 2,5 % solution A.U.V. |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Írország |
Baycox 2,5 % Solution |
|
Csirke |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése és az ellene való védekezés |
||||||||
|
Olaszország |
Baycox soluzione 2,5 % |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Olaszország |
Cevazuril (1) |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Lengyelország |
Baycox 2,5 % |
|
Brojlercsirkék, tenyészcsirkék, pulykák és galambok |
Belsőleges oldat |
25 mg/ml |
Csirke és pulyka: coccidiosis kezelése Galamb: Coccidiosis kezelése és megelőzése |
||||||||
|
Portugália |
Baycox 2,5 % oral solution |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Románia |
Cevazuril |
|
Brojlercsirkék, tenyészcsirkék, jércék és pulykák |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Szlovákia |
Baycox 2,5 % sol. a.u.v. |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Szlovénia |
Baycox 2,5 % w/v oral solution |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Hollandia |
Baycox 2,5 % |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Hollandia |
Baycox oplossing 2,5 % |
|
Csirke és pulyka |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
||||||||
|
Egyesült Királyság |
Baycox 2,5 % oral solution |
|
Brojlercsirkék és brojler tenyészcsirkék |
Belsőleges oldat |
25 mg/ml |
Coccidiosis kezelése |
(1) A forgalomba hozatali engedélyt 2007. június 12-én felfüggesztették.
XI. MELLÉKLET
MEGNEVEZÉS, GYÓGYSZERFORMÁK, GYÓGYSZERKÉSZÍTMÉNY-DÓZISOK, ALKALMAZÁSI MÓDOK, KÉRELMEZŐK, FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI A TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Kérelmező |
Törzskönyvezett megnevezés |
Dózis |
Gyógyszerforma |
Alkalmazási mód |
Tartalom (koncentráció) |
||||||
|
Ausztria |
|
|
Pulairmax 100 μg/Dosis Pulver zur Inhalation |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg/Dosis Pulver zur Inhalation |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg/Dosis Pulver zur Inhalation |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Belgium |
|
|
Pulairmax 100 μg inhalatiepoeder |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg inhalatiepoeder |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg inhalatiepoeder |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Ciprus |
|
|
Pulairmax 100 μg Σκόνη για εισπνοή |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg Σκόνη για εισπνοή |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg Σκόνη για εισπνοή |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Cseh Köztársaság |
|
|
Pulmax 100 μg Prášek k inhalaci |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulmax 200 μg Prášek k inhalaci |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulmax 400 μg Prášek k inhalaci |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Dánia |
|
|
Pulairmax |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Észtország |
|
|
Pulairmax |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Finnország |
|
|
Pulairmax 100 μg inhalaatiojauhe |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg inhalaatiojauhe |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg inhalaatiojauhe |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Németország |
|
|
Pulairmax 100 Mikrogramm/Dosis Pulver zur Inhalation |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 Mikrogramm/Dosis Pulver zur Inhalation |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 Mikrogramm/Dosis Pulver zur Inhalation |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Görögország |
|
|
Pulairmax 100 μg Κόνις για εισπνοή |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg Κόνις για εισπνοή |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg Κόνις για εισπνοή |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Írország |
|
|
Pulairmax 100 μg Inhalation Powder |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg Inhalation Powder |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg Inhalation Powder |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Olaszország |
|
|
Pulairmax 100 polvere per inalazione |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 mcg polvere per inalazione |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 mcg polvere per inalazione |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Lettország |
|
|
Pulairmax |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Litvánia |
|
|
Pulairmax |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Luxemburg |
|
|
Pulairmax 100 μg poudre pour inhalation |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg poudre pour inhalation |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg poudre pour inhalation |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Málta |
|
|
Pulairmax 100 μg Trab li jittiehed bin-nifs |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg Trab li jittiehed bin-nifs |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg Trab li jittiehed bin-nifs |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Hollandia |
|
|
Pulmax 100 mg, inhalatiepoeder |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulmax 200 mg, inhalatiepoeder |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulmax 400 mg, inhalatiepoeder |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Norvégia |
|
|
Pulairmax 100 μg inhalasjonspulver |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax 200 μg inhalasjonspulver |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax 400 μg inhalasjonspulver |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Lengyelország |
|
|
Pulmax 100 μg proszek do inhalacji |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulmax 200 μg proszek do inhalacji |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulmax 400 μg proszek do inhalacji |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Portugália |
|
|
Pulmax, 100 μg pó para inalação |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulmax, 200 μg pó para inalação |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulmax, 400 μg pó para inalação |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Szlovákia |
|
|
Pulmax 100 mcg Inhalačný prášok |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulmax 200 mcg Inhalačný prášok |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulmax 400 mcg Inhalačný prášok |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Spanyolország |
|
|
Budesonida TEVA 100 microgramos polvo para inhalación EFG |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Budesonida TEVA 200 microgramos polvo para inhalación EFG |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Budesonida TEVA 400 microgramos polvo para inhalación EFG |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
|||||||||
|
Svédország |
|
|
Pulairmax |
100 μg |
Inhalációs por |
Inhalációs alkalmazás |
100 mikrogramm |
||||||
|
Pulairmax |
200 μg |
Inhalációs por |
Inhalációs alkalmazás |
200 mikrogramm |
|||||||||
|
Pulairmax |
400 μg |
Inhalációs por |
Inhalációs alkalmazás |
400 mikrogramm |
XII. MELLÉKLET
MEGNEVEZÉSEK, GYÓGYSZERFORMÁK, HATÁSERŐSSÉGEK, ÁLLATFAJOK, ALKALMAZÁS GYAKORISÁGA ÉS MÓDJAI, AJÁNLOTT ADAGOK, VISSZATARTÁSI IDŐSZAKOK ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJAI AZ EZEN BETERJESZTÉS ÁLTAL ÉRINTETT TAGÁLLAMOKBAN
|
Tagállam |
Forgalomba hozatali engedély jogosultja |
Termék találmányi neve |
Gyógyszerforma |
Hatáserősség |
Állatfaj |
Alkalmazás gyakorisága és módja |
Ajánlott adag |
Élelmezésegészségügyi várakozási idő (hús és tej) |
||||
|
Cseh Köztársaság |
|
Suramox 15 % LA |
Szuszpenziós injekció |
150 mg/ml |
Szarvasmarha, sertés |
Két intramuscularis injekció 48 órás időközönként |
15 mg amoxicillin/tt kg (1 ml/10 kg mennyiséggel egyenértékű) |
Hús és egyéb ehető szövetek Szarvasmarha: 58 nap Sertés: 35 nap Tej: 2,5 nap |
||||
|
Spanyolország (1) |
|
Stabox 15 % LA |
Szuszpenziós injekció |
150 mg/ml |
Szarvasmarha, sertés |
Két intramuscularis injekció 48 órás időközönként |
15 mg amoxicillin/tt kg (1 ml/10 kg mennyiséggel egyenértékű) |
Hús és egyéb ehető szövetek Szarvasmarha: 58 nap Sertés: 35 nap Tej: 2,5 nap |
||||
|
Olaszország |
|
Stabox 15 % LA |
Szuszpenziós injekció |
150 mg/ml |
Szarvasmarha, sertés |
Két intramuscularis injekció 48 órás időközönként |
15 mg amoxicillin/tt kg (1 ml/10 kg mennyiséggel egyenértékű) |
Hús és egyéb ehető szövetek Szarvasmarha: 58 nap Sertés: 35 nap Tej: 2,5 nap |
||||
|
Franciaország (2) |
|
Suramox 15 % LA |
Szuszpenziós injekció |
150 mg/ml |
Szarvasmarha, sertés |
Két intramuscularis injekció 48 órás időközönként |
15 mg amoxicillin/tt kg (1 ml/10 kg mennyiséggel egyenértékű) |
Hús és egyéb ehető szövetek Szarvasmarha: 58 nap Sertés: 35 nap Tej: 2,5 nap |
(1) Forgalomba hozatal nem engedélyezett.
(2) Kölcsönös Elismerési Eljárás Referencia Tagállama.
TAGÁLLAMOKTÓL SZÁRMAZÓ TÁJÉKOZTATÁSOK
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/74 |
Kivonat a hitelintézetek reorganizációjáról és felszámolásáról szóló 2001/24/EK európai parlamenti és tanácsi irányelv 9. cikke szerint a Kaupthing Bank Luxembourg SA-val szemben elrendelt felszámolási eljárásról
(2008/C 276/04)
FIZETÉSI HALADÉK
A kereskedelmi ügyekben eljáró luxemburgi körzeti bíróság 2008. október 9-én 17 órakor hozott határozatával elrendelte a Kaupthing Bank Luxembourg SA részvénytársaság (a luxemburgi cégjegyzék (B. rész) szerinti cégjegyzékszáma: 63997; székhelye: 35a, avenue J-F Kennedy, L-1855 Luxembourg) tekintetében a pénzügyi ágazatról szóló 1993. április 5-i módosított törvény IV. része szerinti fizetési haladékra vonatkozó eljárás elindítását, valamint alkalmazandónak nyilvánítja az említett törvény 60–2. cikke (15) bekezdését, amelynek értelmében a Kaupthing Bank Luxembourg SA nevében hozott valamennyi olyan jogi aktus és határozat semmisnek tekintendő, amelyhez a vagyonfelügyelők írásban nem járultak hozzá. A vagyonfelügyelők bármely általuk szükségesnek ítélt javaslatot megvitatás céljából a Kaupthing Bank Luxembourg SA képviseleti szervei elé terjeszthetnek. Ezen kívül részt vehetnek a Kaupthing Bank Luxembourg SA részvénytársaság közgyűlésének, illetve igazgató, irányító, vezető vagy felügyeleti szerveinek tanácskozásain.
A határozat a Kaupthing Bank Luxembourg SA részvénytársaság vagyonkezelésének ellenőrzése céljából vagyonfelügyelőnek nevezi ki az Emmanuelle Caruel-Henniaux és Franz Fayot által képviselt PricewaterhouseCoopers SARL korlátolt felelősségű társaságot, valamint hat hónapra korlátozza a fizetési haladék időtartamát.
A pénzügyi felügyeleti hatóság (Commission de Surveillance du Secteur Financier) és a Kaupthing Bank Luxembourg SA részvénytársaság – a pénzügyi ágazatról szóló 1993. április 5-i módosított törvény 60–2. cikke (9) bekezdésével összhangban – a határozatról szóló értesítés, vagyis a kereskedelmi ügyekben eljáró luxemburgi körzeti bíróság jegyzője által ajánlott levélben elküldött értesítés kézhezvételének napjától számított 14 napon belül fellebbezhet. A fellebbezést a jegyzőnél nyilatkozat formájában kell benyújtani.
A határozattal szemben sem az érintett személyek, sem harmadik személy ellentmondással nem élhet.
A kivonat hiteléül:
A vagyonfelügyelők
A PricewaterhouseCoopers SARL képviseletében Emmanuelle Caruel-Henniaux és Franz Fayot
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/75 |
A tagállamok tájékoztatása az EK-Szerződés 87. és 88. cikkének a kis- és középvállalkozásoknak nyújtott állami támogatásokra történő alkalmazásáról szóló 70/2001/EK bizottsági rendelet értelmében engedélyezett állami támogatásokról
(EGT-vonatkozású szöveg)
(2008/C 276/05)
|
Támogatás száma |
XS 193/08 |
||||||||||
|
Tagállam |
Bolgár Köztársaság |
||||||||||
|
Régió |
Az EK-Szerződés 87. cikke (3) bekezdésének a) pontja szerinti régió |
||||||||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
Vissza nem térítendő támogatási program a 2007–2013 közötti vidékfejlesztési program „mezőgazdasági és erdészeti termékek értéknövelése” intézkedése keretében, a következő célkitűzések érdekében:
|
||||||||||
|
Jogalap |
Közösségi jogszabályok:
A Bolgár Köztársaság jogszabályai:
|
||||||||||
|
A támogatási program keretében tervezett éves kiadás, illetve a vállalkozásnak nyújtott egyedi támogatás összege |
Támogatási program |
Teljes éves összeg |
34,4 millió EUR (1) |
||||||||
|
Garantált kölcsönök |
|
||||||||||
|
Egyedi támogatás |
Teljes összeg |
|
|||||||||
|
Garantált kölcsönök |
|
||||||||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdése és 5. cikke alapján |
Igen (legfeljebb 50 %) |
|||||||||
|
Végrehajtás időpontja |
A végrehajtás azt követően kezdődik el, hogy az Európai Bizottság jóváhagyta a 2007–2013 közötti vidékfejlesztési program 9. fejezetének („A versenyszabályok szerinti értékelés elemei és a Szerződés 87., 88. és 89. cikke alapján engedélyezett támogatási programok jegyzéke”) módosítását, és a 9. fejezetet kiegészítették az állami támogatás nyilvántartási számával |
||||||||||
|
A támogatási program vagy egyedi támogatás nyújtásának időtartama |
Végrehajtás vége 2013.12.31. |
||||||||||
|
A támogatás célja |
Kis- és középvállalkozás támogatása |
Igen |
|||||||||
|
Érintett gazdasági ágazat |
Csak bizonyos ágazatokra vonatkozó támogatás |
Igen |
|||||||||
|
Egyéb feldolgozóipar |
Igen (2) |
||||||||||
|
A támogatást nyújtó hatóság neve és címe |
|
||||||||||
|
|||||||||||
|
Nagy összegű egyedi támogatás |
A rendelet 6. cikkével összhangban |
Nem |
|||||||||
|
Támogatás száma |
XS 201/08 |
||||||
|
Tagállam |
Olaszország |
||||||
|
Régió |
Sardegna |
||||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
Contributi per impianti fotovoltaici |
||||||
|
Jogalap |
Articolo 24, L.R. 29 maggio 2007, n. 2 Deliberazioni Giunta Regionale n. 21/37 del 8.4.2008 e n. 34/22 del 19.6.2008 DDS n. 366 del 25.6.2008 |
||||||
|
Az intézkedés típusa |
Támogatási program |
||||||
|
Költségvetés |
Tervezett éves kiadás: 10 millió EUR |
||||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban: A HL C 90., 2008.4.11-i számában közzétett 2007–2013-as regionális támogatási térkép szerint Szardínia támogatható részein található vállalatoknak megítélt támogatás a fényelektromossági berendezések megvalósítása támogatható költségének 20 %-át meg nem haladó tőketámogatásból áll. Azon vállalatok esetén, amelyek a 2007–2013-as regionális támogatási térkép szerint nem támogatható területen találhatóak, a maximális támogatási intenzitás a következőképpen alakul:
A támogatásnyújtás feltétele, hogy a beruházás legalább ötéves időtartamra fennmaradjon a régióban, illetve a kedvezményezett saját forrásaiból történő finanszírozás mértéke ne legyen kevesebb az elfogadott beruházás 25 %-ánál. A támogatás összhangban van a 2006. február 6-i, illetve a 2007. február 19-i miniszteri rendelettel módosított, az elektromos energia fényelektromos berendezések általi termelését ösztönző intézkedésekről szóló, 2005. július 28-i miniszteri rendelettel (ún. „conto energia”). A támogatás nem vonható össze más regionális, nemzeti vagy közösségi szintű támogatással |
||||||
|
A végrehajtás időpontja |
2008.7.18. |
||||||
|
Időtartam |
2008.9.18. |
||||||
|
Célkitűzés |
KKV-k |
||||||
|
Gazdasági ágazat |
A KKV-k részére nyújtott támogatásra jogosult valamennyi ágazat |
||||||
|
A támogatást nyújtó hatóság neve és címe |
|
||||||
|
Egyéb információ |
Az intézkedést nyilvános pályázati felhívás útján hajtják végre, a pályázatokat osztályozzák és rangsorolják. A 20 %-nál kisebb mértékű állami támogatást igénylők elsőbbséget élveznek. A regionális támogatásra nem jogosult területek esetében a támogatásintenzitás csökkentése a 70/2001/EK rendeletnek megfelelően történik |
|
Támogatás száma |
XS 209/08 |
|||||||||
|
Tagállam |
Görögország |
|||||||||
|
Régió |
— |
|||||||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
«ΕΝΙΣΧΥΣΗ ΤΗΣ ΑΝΤΑΓΩΝΙΣΤΙΚΟΤΗΤΑΣ ΚΑΙ ΤΗΣ ΚΑΙΝΟΤΟΜΙΑΣ ΤΩΝ ΜΙΚΡΟΜΕΣΑΙΩΝ ΕΠΙΧΕΙΡΗΣΕΩΝ ΣΤΟΥΣ ΤΟΜΕΙΣ ΤΗΣ ΜΕΤΑΠΟΙΗΣΗΣ ΚΑΙ ΤΟΥ ΤΟΥΡΙΣΜΟΥ» (3η προκήρυξη) [«ENISHYSI TIS ANTAGONISTIKOTITAS KAI TIS KAINOTOMIAS TON MIKROMESAION EPIHEIRISEON STOYS TOMEIS TIS METAPOIISIS KAI TOY TOYRISMOY» (3i prokiryksi)] |
|||||||||
|
Jogalap |
Άρθρο 35 του Ν. 3016/2002 (ΦΕΚ 110 Α'/17-05-2002) ΥΑ 41630/ΕΥΣ9450/7.11.2005 (ΦΕΚ 1651/B'/29.11.05) ΚΥΑ 14871/EYΣ3047/20.4.2005 (ΦΕΚ 575/ΤΒ/28.04.2005) ΥΑ 39059/ΕΥΣ9047/14.10.2005 (ΦΕΚ 1539/Β/8.11.2005) ΚΥΑ 1707/ΕΥΣ443/17.01.2006 (ΦΕΚ 42/Β/19.01.2006) |
|||||||||
|
Az intézkedés típusa |
Támogatási program |
|||||||||
|
Költségvetés |
Tervezett éves kiadás: 400 millió EUR |
|||||||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
|||||||||
|
Végrehajtás időpontja |
2006.3.15. |
|||||||||
|
Időtartam |
2007.6.30. |
|||||||||
|
Célkitűzés |
Kis- és középvállalkozások |
|||||||||
|
Gazdasági ágazat |
Feldolgozóipar, Idegenforgalom |
|||||||||
|
A támogatást nyújtó hatóság neve és címe |
|
|
Támogatás száma |
XS 211/08 |
|||
|
Tagállam |
Németország |
|||
|
Régió |
Freie und Hansestadt Hamburg |
|||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
|
|||
|
Jogalap |
Verordnung (EG) Nr. 70/2001 der Kommission vom 12. Januar 2001 über die Anwendung der Artikel 87 und 88 EG-Vertrag auf staatliche Beihilfen an kleine und mittlere Unternehmen (ABl. EG 13.1.2001 L 10/33 verlängert durch ABl. EU 23.12.2006 L 368/85); Gesetz über die Kreditkommission vom 29.4.1997 (Hamburgisches Gesetz- und Verordnungsblatt 1997, Nr. 18, S. 133) |
|||
|
Az intézkedés típusa |
Ad hoc |
|||
|
Költségvetés |
Tervezett támogatás teljes összege: 3 450 EUR |
|||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
|||
|
Végrehajtás időpontja |
2008.8.14. |
|||
|
Időtartam |
2009.2.14. |
|||
|
Célkitűzés |
Kis- és középvállalkozások |
|||
|
Gazdasági ágazat |
Egyéb szolgáltatások |
|||
|
A támogatást nyújtó hatóság neve és címe |
|
|
Támogatás száma |
XS 212/08 |
|||
|
Tagállam |
Németország |
|||
|
Régió |
Freie und Hansestadt Hamburg |
|||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
|
|||
|
Jogalap |
Verordnung (EG) Nr. 70/2001 der Kommission vom 12. Januar 2001 über die Anwendung der Artikel 87 und 88 EG-Vertrag auf staatliche Beihilfen an kleine und mittlere Unternehmen (ABl. EG 13.1.2001 L 10/33 verlängert durch ABl. EU 23.12.2006 L 368/85); Gesetz über die Kreditkommission vom 29.4.1997 (Hamburgisches Gesetz- und Verordnungsblatt 1997, Nr. 18, S. 133) |
|||
|
Az intézkedés típusa |
Ad hoc |
|||
|
Költségvetés |
Tervezett támogatás teljes összege: 6 750 EUR |
|||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
|||
|
Végrehajtás időpontja |
2008.7.31. |
|||
|
Időtartam |
2009.1.31. |
|||
|
Célkitűzés |
Kis- és középvállalkozások |
|||
|
Gazdasági ágazat |
Egyéb szolgáltatások |
|||
|
A támogatást nyújtó hatóság neve és címe |
|
(1) Az éves összeg indikatív jellegű, és a 2007–2013 vidékfejlesztési program 123. „mezőgazdasági és erdészeti termékek értéknövelése” intézkedés költségvetése alapján került meghatározásra (jelenértéken 241 millió EUR).
(2) Az EK-Szerződés I. mellékletében meghatározott termékek feldolgozásával és forgalmazásával kapcsolatos alábbi ágazatok támogathatók:
|
— |
tej és tejtermékek (elsősorban NACE 15.5), |
|
— |
hús és hústermékek (elsősorban NACE 15.1), |
|
— |
zöldség, gyümölcs, gomba (elsősorban NACE 15.3), |
|
— |
mézfeldolgozás (egyértelmű NACE-besorolása nincsen, de a NACE 15.89 alá tartozhat), |
|
— |
gabona, malomipari termékek és keményítőtermékek (elsősorban NACE 15.6), |
|
— |
növényi és állati eredetű olajok és zsírok (elsősorban NACE 15.4), |
|
— |
műszaki és orvosi célú növényfeldolgozás,ezen belül olajtartalmú rózsa, gyógynövények, nyers dohány (egyértelmű NACE-besorolása nincsen, de a NACE 24.63 alá tartozhat), |
|
— |
késztakarmány mezőgazdasági üzemekben tartott állatok számára (elsősorban NACE 15.71), |
|
— |
szőlőmust, bor és ecet (elsősorban NACE 15.87, 15.93). |
Az elsődleges és másodlagos biomassza növényi és állati termékeinek feldolgozásával foglalkozó, energiatermelésben érintett, az EK-Szerződés I. mellékletében felsorolt valamennyi ágazat a halászati termékek kivételével (egyértelmű NACE-besorolása nincsen).
|
— |
erdészeti termékek előállításával és forgalmazásával kapcsolatos ágazatok, a bútorgyártás kivételével (elsősorban NACE 20.10, 20.30, 20.40, 20.51). |
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/79 |
A tagállamok tájékoztatása az EK-Szerződés 87. és 88. cikkének a kis- és középvállalkozásoknak nyújtott állami támogatásokra történő alkalmazásáról szóló 70/2001/EK bizottsági rendelet értelmében engedélyezett állami támogatásokról
(EGT-vonatkozású szöveg)
(2008/C 276/06)
|
Támogatás száma |
XS 213/08 |
||||||
|
Tagállam |
Egyesült Királyság |
||||||
|
Régió |
East Midlands |
||||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
Hathersage Developments Ltd |
||||||
|
Jogalap |
RDA Act 1998 |
||||||
|
Az intézkedés típusa |
Ad hoc |
||||||
|
Költségvetés |
Tervezett támogatás teljes összege: 0,33 millió GBP |
||||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
||||||
|
Végrehajtás időpontja |
2008.1.14. |
||||||
|
Időtartam |
2009.3.31. |
||||||
|
Célkitűzés |
Kis- és középvállalkozások |
||||||
|
Gazdasági ágazat |
Szakmai, Tudományos, Műszaki Tevékenység |
||||||
|
A támogatást nyújtó hatóság neve és címe |
|
|
Támogatás száma |
XS 214/08 |
||||
|
Tagállam |
Egyesült Királyság |
||||
|
Régió |
North East England |
||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
Python Properties |
||||
|
Jogalap |
Industrial Development Act 1982 sections 7 and 11 Local Government Act 2000 section 2 |
||||
|
Az intézkedés típusa |
Támogatási program |
||||
|
Költségvetés |
Tervezett éves kiadás: 0,3 millió GBP |
||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
||||
|
Végrehajtás időpontja |
2008.3.3. |
||||
|
Időtartam |
2008.12.31. |
||||
|
Célkitűzés |
Kis- és középvállalkozások |
||||
|
Gazdasági ágazat |
Feldolgozóipar, Egyéb szolgáltatások |
||||
|
A támogatást nyújtó hatóság neve és címe |
|
|
Támogatás száma |
XS 215/08 |
||||||
|
Tagállam |
Egyesült Királyság |
||||||
|
Régió |
West Midlands |
||||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
Premium Vehicles Centres of Excellence Projects — Warwick University |
||||||
|
Jogalap |
Regional Development Agencies Act 1998 |
||||||
|
Az intézkedés típusa |
Támogatási program |
||||||
|
Költségvetés |
Tervezett éves kiadás: 2,2 millió GBP |
||||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
||||||
|
Végrehajtás időpontja |
2008.8.15. |
||||||
|
Időtartam |
2013.12.31. |
||||||
|
Célkitűzés |
Kis- és középvállalkozások |
||||||
|
Gazdasági ágazat |
Feldolgozóipar |
||||||
|
A támogatást nyújtó hatóság neve és címe |
|
|
Támogatás száma |
XS 219/08 |
||||
|
Tagállam |
Hollandia |
||||
|
Régió |
— |
||||
|
A támogatási program megnevezése vagy az egyedi támogatásban részesülő vállalkozás neve |
Subsidieregeling innovatiekredieten-module van de Experimentele kaderregeling subsidies innovatieprojecten |
||||
|
Jogalap |
Kaderwet EZ subsidies |
||||
|
Az intézkedés típusa |
Támogatási program |
||||
|
Költségvetés |
Tervezett éves kiadás: 20,3 millió EUR |
||||
|
Maximális támogatási intenzitás |
A rendelet 4. cikkének (2)–(6) bekezdésével és 5. cikkével összhangban |
||||
|
Végrehajtás időpontja |
2008.7.5. |
||||
|
Időtartam |
2012.7.5. |
||||
|
Célkitűzés |
Kis- és középvállalkozások |
||||
|
Gazdasági ágazat |
Kis- és középvállalkozások részére nyújtott támogatásra jogosult valamennyi ágazat |
||||
|
A támogatást nyújtó hatóság neve és címe |
|
V Vélemények
KÖZIGAZGATÁSI ELJÁRÁSOK
Bizottság
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/82 |
A 2408/92/EGK tanácsi rendelet 4. cikke (1) bekezdésének d) pontja értelmében Olaszország által közzétett ajánlattételi felhívás az Albenga–Roma Fiumicino útvonalon oda és vissza közlekedő menetrend szerinti légi járatok működtetésére
(EGT-vonatkozású szöveg)
(2008/C 276/07)
ELŐZMÉNYEK
Az olasz kormány Infrastruktúraügyi és Közlekedési Minisztériuma a 2408/92/EGK rendelet 4. cikkének rendelkezései értelmében és a légifuvarozók Liguria tartományban megrendezett konferenciája alkalmával hozott határozatokkal összhangban jóváhagyta az Albenga–Roma Fiumicino útvonalon oda és vissza közlekedő menetrend szerinti légi járatok működtetésére vonatkozó ezen ajánlattételi felhívást.
Az ezen közszolgáltatási kötelezettségek elrendelésével meghatározott előírások közzétételre kerültek az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában.
Abban az esetben, ha a fenti közszolgáltatási kötelezettség közzétételétől számított 30 napon belül egyetlen légifuvarozó sem jelezné azon szándékát, hogy az említett viszonylatban, a közszolgáltatási kötelezettségekkel összhangban, ellenszolgáltatás nélkül menetrendszerű járatokat indít, az olasz kormány Infrastruktúraügyi és Közlekedési Minisztériuma a 2408/92/EGK rendelet 4. cikke (1) bekezdésének d) pontjában meghatározott eljárással összhangban úgy határoz, hogy a hozzáférést egyetlen légifuvarozóra korlátozza, amelyet a közszolgáltatási kötelezettség alá eső járatoknak az említett rendeletben foglaltak szerinti biztosítása érdekében ajánlattételi eljárás keretében választ ki.
ÁLTALÁNOS RENDELKEZÉSEK
Ez a felhívás meghatározza az ajánlattételi eljárás tárgyát, az azon való részvétel módját, továbbá a szerződés időtartamára, módosítására és érvényességi idejére, a rendelkezések be nem tartása esetén alkalmazandó szankciókra, valamint az ajánlatot és a szerződés teljesítését alátámasztó biztosítékokra vonatkozó szabályokat.
A szóban forgó útvonalon a szolgáltatás működtetésére irányuló jog elnyerésének feltétele, hogy azt nyílt ajánlattételi eljárás keretében kell megszerezni, az ezen ajánlattételi felhívás 6. pontjában meghatározott pénzügyi ellentételezés összege szerinti legkedvezőbb ajánlat alapján.
1. Az ajánlattétel tárgya
Menetrend szerinti légi járatok működtetése az Albenga–Roma Fiumicino útvonalon oda és vissza az elrendelt közszolgáltatási kötelezettségeknek megfelelően, amelyek a 2408/92/EGK rendelet rendelkezéseivel összhangban az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában kerültek kihirdetésre.
2. Részvétel
Az ajánlattételi felhívásra a 2408/92/EGK rendelet (2) cikkének b) pontjában meghatározott valamennyi közösségi légifuvarozó nyújthat be ajánlatot amennyiben teljesíti az alábbi követelményeket.
Általános követelmények
|
1. |
nem fizetésképtelen, nincs kötelező felszámolás vagy hitelezőkkel való egyezségkötésre irányuló eljárás alatt, illetve nincs folyamatban ezen tényállások megállapítására irányuló eljárás; |
|
2. |
nem volt a működéstől való eltiltásra ítélve sem a 231/2001. számú törvényerejű rendelet 9. cikkének (2) bekezdése, sem olyan más ítélet szerint, amelynek értelmében nem köthet szerződést közigazgatási szervekkel; |
|
3. |
teljesítette a munkaviszonyhoz kapcsolódó társadalombiztosítási járulékfizetési kötelezettségét; |
|
4. |
nem tett hamis nyilatkozatot olyan korábbi ajánlattételi eljárásokban való részvételre vonatkozó feltételeket illetően, amelyek közszolgáltatási kötelezettségeknek megfelelően elrendelt légi járatok működtetésének elnyerésére irányultak. |
A fentiekben felsorolt feltételek teljesítését a pályázók a 3. pont vonatkozásában az INPS (Istituto Nazionale della Previdenza Sociale – Országos Társadalombiztosítási Intézet) vagy az INAIL (Istituto Nazionale Assicurazione contro gli Infortuni sul Lavoro – Országos Munkahelyi Balesetbiztosítási Intézet) által kibocsátott járulékfizetési igazolással, illetve az 1999. március 12-i 68. számú törvény („Norme per il diritto al lavoro dei disabili” – „A fogyatékkal élők munkához való jogára vonatkozó szabályok”) 17. cikke szerinti dokumentummal, az 1., 2. és 4. pont vonatkozásában pedig a köztársasági elnök 2000. december 28-i 445. számú rendelete 46. és 47. cikkének megfelelő helyettesítő nyilatkozattal igazolhatják.
Nem olaszországi, hanem az Európai Unió más tagországában működő pályázók esetében az illetőség szerinti ország közigazgatási és hatósági szerveinek kell kibocsátania ezeket az igazolásokat és nyilatkozatokat, és azokhoz az olasz konzulátus által hitelesített olasz fordítást is csatolni kell.
Műszaki követelmények
|
1. |
a 2407/92/EGK rendeletnek megfelelően kiadott légifuvarozói működési engedély; |
|
2. |
különösen az utasokra, a poggyászra, a rakományra és a harmadik felekre vonatkozó kötelező biztosítás, többek között a 785/2004/EK rendelet értelmében; |
|
3. |
a közösségi szabályokkal összhangban lévő üzemben tartási engedély (AOC); |
|
4. |
nem pályázhatnak olyan légitársaságok, amelyek szerepelnek a http://ec.europa.eu/transport/air-ban internetcímen közzétett, az európai biztonsági előírásokat nem teljesítő légitársaságokat tartalmazó úgynevezett „feketelistán”; |
|
5. |
a pályázóknak olyan analitikus könyveléssel kell rendelkezniük, amelyben szerepelnek a lényeges költségek (beleértve az állandó költségeket és a bevételeket). |
Azokat a pályázókat, amelyek az ajánlattételi eljárásban való részvételre irányuló kérelem beadását követően kerülnek olyan helyzetbe, hogy a fenti követelmények valamelyikét nem tudják teljesíteni, automatikusan kizárják az ajánlatok értékeléséből.
Azon pályázók esetében, amelyek az 5. pontban említett szerződés megkötését követően kerülnek olyan helyzetbe, hogy a fenti követelmények valamelyikét nem tudják teljesíteni, az ezen ajánlattételi felhívás 14. pontjában és 15. pontjának utolsó előtti bekezdésében foglalt rendelkezéseket kell alkalmazni.
3. Eljárás
Erre az ajánlattételi felhívásra a 2408/92/EGK rendelet 4. cikke (1) bekezdésének d), e), f), h) és i) pontjainak rendelkezései vonatkoznak.
4. Dokumentáció
Az ajánlattételi eljárásra érvényes egyedi szabályokat, az ajánlatok érvényességi idejét és minden egyéb hasznosnak vélt információt tartalmazó teljes ajánlattételi dokumentáció, illetve az 5. pontban említett mintaszerződés ezen ajánlattételi felhívásnak minden értelemben szerves részét képezi és ingyenesen beszerezhető az alábbi címen: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio, 118, I-00185 Roma vagy az alábbi e-mail címen: trasporto.aereo@enac.rupa.it.
5. A szolgáltatás nyújtását szabályozó szerződés
A szolgáltatást a légifuvarozó és az olaszországi Nemzeti Polgári Légiközlekedési Hatóság (ENAC) között létrejött, az ajánlattételi dokumentáció részét képező minta alapján szerkesztett szerződés szabályozza.
6. Pénzügyi ellentételezés
A szóban forgó útvonalon légi járatok üzemeltetéséért járó – a pályázati eljárás keretében meghatározott – pénzügyi ellentételezés legmagasabb összege évente 979 112,85 EUR (kilencszázhetvenkilencezer száztizenkettő euró és nyolcvanöt cent), amely tartalmazza a HÉÁ-t is.
Az ajánlattételi dokumentációban foglaltak szerint elkészített ajánlatokban az adatlap pénzügyi ajánlatra vonatkozó részénél egyértelműen meg kell jelölni a szóban forgó szolgáltatás működtetéséért ellentételezés címén igényelt legmagasabb összeget, az előzőekben rögzített felső határon belül.
Az ellentételezés pontos összege a szerződés egy éves érvényességi idejének lejártakor visszamenőleg kerül megállapításra a ténylegesen felmerült kiadások és a szolgáltatás során ténylegesen termelt jövedelem alapján, bizonylatok bemutatása ellenében és az ajánlatban megjelölt legmagasabb összeg mértékéig, az ajánlattételi dokumentációban meghatározottak szerint.
A légifuvarozó semmi esetre sem igényelhet pénzügyi ellentételezés címén a szerződésben megállapított felső határnál magasabb összeget, tekintettel arra, hogy a folyósított összeg nem díjazásnak, hanem a közszolgáltatási kötelezettségek keretében nyújtott szolgáltatás vállalásáért nyújtott ellentételezésnek minősül.
A szerződés egy éves érvényességi idejének lejártakor esedékes kifizetések – az ajánlattételi dokumentációban meghatározottak szerint – előlegek formájában történnek, majd ezt követi az elszámolás, kivéve azokat az eseteket, amikor az ENAC esetleges ellenőrzések keretében megvizsgálja a nyújtott ellentételezés tényleges rendeltetését, illetve azt, hogy az ajánlattételi eljárásban nyertes légifuvarozó továbbra is teljesíti-e az előírt követelményeket. Az elszámolásra azt követően kerül sor, hogy ellenőrizték az adott útvonal vonatkozásában a légifuvarozó által benyújtott részletes elszámolást, illetve azt, hogy a nyújtott szolgáltatás megfelel-e a szerződésben foglaltaknak.
7. Viteldíjak
A benyújtott ajánlatoknak – az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában közzétett, a közszolgáltatási kötelezettségekre vonatkozó közleménynek megfelelően – tartalmazniuk kell a várható viteldíjakat.
8. Az útvonal megindítása
A szóban forgó útvonalon a szerződés aláírásától számított 15 (tizenöt) napon belül meg kell kezdeni a szolgáltatást, amelynek tényét a nyertes légifuvarozó és az ENAC által aláírt jegyzőkönyv igazolja.
9. A szerződés időtartama
A szerződés a szolgáltatásnak a szóban forgó útvonalon történő tényleges elindításától számított egyéves időtartamra szól.
A légifuvarozó vállalja, hogy az ENAC rendelkezésére bocsátja alkalmazottait, műszaki és számviteli dokumentumait, berendezéseit, illetve minden egyebet, amely a Bizottság közleményében, a közszolgáltatási kötelezettséget elrendelő rendeletben, ezen ajánlattételi felhívásban, a szerződésben, valamint az ajánlattételi dokumentációban foglalt rendelkezések megfelelő teljesítésének, alkalmazásának és végrehajtásának ellenőrzésére irányuló felügyeleti tevékenység és ellenőrzés során szükségessé válik.
Az előző bekezdésben foglalt kötelezettségek be nem tartása esetén az ezen ajánlattételi felhívás 11. pontjában foglaltak szerint szankciók szabhatók ki.
10. Elállás a szerződéstől
A szerződő felek bármelyike hathónapos előzetes értesítést követően jogosult a szerződés felmondásra.
Előzetes értesítés nélküli elállásnak minősül, ha a légifuvarozó az általa működtetett, közszolgáltatási kötelezettség alá eső szolgáltatást megszakítja, és a vállalt kötelezettségek hiánytalan teljesítését az ENAC-tól kapott figyelmeztetés kézhezvételétől számított 30 (harminc) napon belül sem kezdi meg újra.
Amennyiben a légifuvarozó a szerződéstől eláll, az ENAC fenntartja a jogot arra, hogy elvégezze a szükséges elemzéseket annak érdekében, hogy az Infrastruktúraügyi és Közlekedési Minisztériumnak javaslatot tegyen új szerződés megkötésére az ajánlatok értékelésekor a következő helyre rangsorolt légifuvarozóval. A közszolgáltatási kötelezettség alá eső szolgáltatásnyújtás feltételei és az arányosan járó ellentételezés ugyanazok lesznek, mint a közszolgáltatási kötelezettség gyakorlásának eredeti odaítélésekor meghatározottak.
11. Mulasztások és szankciók
Nem tekinthető a légifuvarozónak felróható mulasztásnak a szolgáltatás következő okok miatt való megszakítása:
|
— |
veszélyes időjárási körülmények, |
|
— |
a működési programban megjelölt valamelyik repülőtér bezárása, |
|
— |
biztonsági problémák, |
|
— |
sztrájk, |
|
— |
vis maior esetek. |
Ha a szolgáltatás a fenti okok miatt szakad meg, a kimaradt járatok arányában csökken az ellentételezés összege.
A szerződésben foglalt szolgáltatások és az abban vállalt kötelezettségek be nem tartása esetén az ENAC jogosult büntetést kiszabni a légifuvarozóra, amely az elkövetett szerződésszegések számával arányosan növekszik. Ennek módja a mintaszerződésben részletesen rögzítésre kerül.
A büntetések összege semmi esetre sem haladhatja meg az ajánlat alapját képező, a 6. pontban említett pénzügyi ellentételezés maximális összegének 50 %-át, azzal a kikötéssel, hogy ezen határ átlépése esetén az ENAC jogosult a szerződés mulasztás miatti felmondására, aminek következtében a még folyósítandó ellentételezéseket azonnali hatállyal visszavonják.
A közvetlenül a légifuvarozónak felróható okokból bekövetkező járattörlések száma évente nem haladhatja meg a tervezett járatok 2 %-át.
Ezen tűréshatáron felül a légifuvarozó köteles az ENAC részére büntetés címén minden egyes, a 2 %-os határ fölötti járattörlés esetén 3 000,00 (háromezer) EUR-t fizetni. Erről előzőleg hivatalos értesítést kap, amelyet az esemény ismertté válását követő 10 napon belül kell megküldeni a légifuvarozónak. A légifuvarozónak a kifogás kézhezvételét követően legfeljebb hét nap áll rendelkezésére, hogy benyújtsa esetleges ellenérveit.
Ezenkívül az ENAC felülvizsgálja és az elindított járatokkal arányos mértékben módosítja a pénzügyi ellentételezés összegét. Az ilyen jogcímen befolyt összeget Albenga város területi folytonosságának finanszírozására különítik el.
A 10. cikkben említett előzetes értesítési kötelezettség figyelmen kívül hagyása esetén bírság szabható ki, amely az esedékes ellentételezés összege és az értesítés elmulasztásának a közszolgáltatási kötelezettség alá eső szolgáltatás megszakításától számított ideje alapján kerül kiszámításra, a 10. pontban meghatározott feltételek szerint, az alábbi képlet alapján:
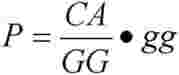
Ahol:
|
P |
= |
bírság |
|
CA |
= |
éves ellentételezés |
|
GG |
= |
a szóban forgó év napjainak száma (365 vagy 366) |
|
gg |
= |
az értesítés elmulasztásának napjai |
Az ebben a pontban meghatározott szankciók összevonhatók az ezen témakörre vonatkozó közösségi szabályozásban, valamint a nemzeti jogszabályokban és szabályozó rendelkezésekben meghatározott bírságokkal.
12. Az ajánlatot alátámasztó biztosítékok
Az ajánlat komolyságának és megbízhatóságának alátámasztására az ajánlattételi eljárásban részt vevő légifuvarozóknak a 6. pontban említett pénzügyi ellentételezés maximális összegének 2 %-ával megegyező összegű biztosítékot kell elhelyezniük, tetszés szerint kaució, illetve biztosítási vagy banki kezességvállalás formájában.
A fenti biztosíték elhelyezésének módjával kapcsolatos részleteket az ajánlattételi dokumentáció tartalmazza, illetve azok esetlegesen a szerződésben is rögzítésre kerülnek.
A biztosíték érvényességi idejének az ajánlatok beadási határidejétől számított legalább 180 (száznyolcvan) napnak kell lennie, és a légifuvarozónak vállalnia kell, hogy abban az esetben, ha szolgáltatásnyújtás jogának odaítélése határidőre nem történik meg, akkor a biztosíték érvényességi idejét az ENAC ugyanezen eljárás keretében tett kérésére meghosszabbítja.
Amikor az ENAC az ajánlattételi eljárásban nem nyertes légifuvarozókat tájékoztatja az eredményről, egyúttal az általuk elhelyezett biztosítékokat is felszabadítja.
13. A teljesítésre vonatkozó biztosítékok és a biztosítási fedezet
Az ezen ajánlattételi felhívás tárgyát képező közszolgáltatási kötelezettség alá eső járatok működtetésének jogát elnyerő légifuvarozó köteles – biztosítási vagy banki kezességvállalás révén – 400 000,00 (négyszázezer) EUR összegben biztosítékot letétbe helyezni az ENAC javára, amely ezt az összeget a közszolgáltatási kötelezettség alá eső szolgáltatás teljesítésének biztosítására használhatja fel.
A biztosíték felszabadítása automatikusan, az ENAC jóváhagyása nélkül történik, azt követően, hogy a 6. pont utolsó bekezdésében említett ellenőrzés kedvező eredménnyel zárul.
14. A pénzügyi ellentételezés hatályának megszűnése vagy annak visszavonása
Amennyiben a nyertes légifuvarozó olyan helyzetbe kerül, hogy az ezen ajánlattételi felhívás 2. pontjában, illetve az ajánlattételi dokumentációban említett általános és műszaki követelmények bármelyikét a szerződés megkötését követően nem tudja teljesíteni, az útvonalra vonatkozó megbízás hatályát veszti, a pénzügyi ellentételezést visszavonják és azokat a részleteket, amelyeket esetlegesen már folyósítottak, de amelyekre a légifuvarozó már nem volt jogosult, a jogos kamatokkal növelve behajtják.
Az útvonalra vonatkozó megbízás visszavonását követően az Infrastruktúraügyi és Közlekedési Minisztérium felhatalmazhatja az ENAC-ot arra, hogy az adott útvonalra vonatkozó szolgáltatás még hátralévő idejére új szerződést írjon alá az ajánlatok értékelésekor a következő helyen végzett légifuvarozóval.
Ebben az esetben a szerződés időtartama a szolgáltatás elindításának időpontjától a megszüntetett szerződésben foglalt eredeti időpontig tart, figyelembe véve az ajánlattételi eljárásban nyertes légifuvarozó által benyújtott ajánlat értékelésekor jóváhagyott működési programot.
15. A szerződés megszűnése
Amennyiben a légifuvarozó nem tartja be az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában közzétett, a kötelezettségekre vonatkozó közleményben, valamint a közszolgáltatási kötelezettséget elrendelő rendeletben, a szerződésben, az ezen ajánlattételi felhívásban vagy az ajánlattételi dokumentációban foglalt előírásokat, az ENAC a polgári törvénykönyv 1454. cikkének értelmében jogosult írásban felszólítani a légifuvarozót arra, hogy a felszólítás kézhezvételétől számítva 15 (tizenöt) napon belül szüntesse meg mulasztását.
A határidő lejárta után az ENAC a szerződést semmisnek tekintheti és a 13. pontban említett biztosíték összegét véglegesen visszatarthatja, továbbá a légifuvarozóval szemben eljárhat a kár megtérítése érdekében.
Továbbá ha a légifuvarozó a szerződésben, az ezen ajánlattételi felhívás rendelkezéseiben vagy az ajánlattételi dokumentációban foglalt kötelezettségeket és szolgáltatásokat nem teljesíti, az ENAC a polgári törvénykönyv 1456. cikkének értelmében előzetes írásbeli figyelmeztetést követően jogosult a szerződés felbontására.
A szerződés felbontása esetén a Infrastruktúraügyi és Közlekedési Minisztérium felhatalmazhatja az ENAC-ot arra, hogy az adott útvonalra vonatkozó szolgáltatás még hátralévő idejére új szerződést írjon alá az útvonalra vonatkozó megbízás odaítélésekor a következő helyen végzett légifuvarozóval.
Ebben az esetben a szerződés időtartama a szolgáltatás elindításának időpontjától a megszüntetett szerződésben foglalt eredeti időpontig tart, figyelembe véve az ajánlattételi eljárásban nyertes légifuvarozó által benyújtott ajánlat értékelésekor jóváhagyott működési programot.
16. Az ajánlatok benyújtása
Az ajánlatokat ezen ajánlattételi felhívásnak az Európai Unió Hivatalos Lapjában történő kihirdetésétől számított 30 (harminc) napon belül, az ajánlati dokumentációban foglaltaknak megfelelő formában, a kizárás terhe mellett, tértivevényes ajánlott küldemény útján vagy közvetlenül, megfelelő átvételi elismervény ellenében a következő címre kell eljuttatni: ENAC – Direzione Generale, viale del Castro Pretorio, 118, I-00185 Roma.
Az ajánlatokat a kizárás terhe mellett három lezárt és lepecsételt borítékban kell benyújtani.
A külső lezárt, lepecsételt és mindkét szélén szignált borítékon, amelyben a két másik, szintén lepecsételt és mindkét szélén szignált borítékot kell elhelyezni, az alábbiakat kell feltüntetni: „Offerta per la gara in oneri di servizio pubblico sulla rotta Albenga – Roma Fiumicino e viceversa”.
Az ezen ajánlattételi felhívás 4. pontjában említett ajánlattételi dokumentáció rögzíti, hogy milyen dokumentumokat kell az említett három borítékban elhelyezni.
A felek tudomásul veszik, hogy amennyiben bármilyen okból kifolyólag a küldemény a fenti határidőre nem érkezik meg a címre, az kizárólag a feladó felelőssége.
Az ajánlattételi eljárásban abban az esetben is lehet eredményt hirdetni, ha csak egy érvényes ajánlat érkezik.
17. Az ajánlatok érvényességi ideje
Az ajánlatok benyújtásának határidejétől számított 180 (száznyolcvan) nap.
18. A pályázati eljárás lefolytatása
Az ajánlatok elbírálásáról az ENAC gondoskodik, amely e célra bizottságot nevez ki: ennek tagja egy, az ENAC főigazgatója által delegált vezető, a Liguria tartomány által kinevezett légiközlekedési szakértő, valamint az ENAC és Liguria tartomány által egyetértésben megválasztott elnök. A titkársági teendőket az ENAC egy hivatalnoka végzi.
19. A személyes adatok kezelése
A személyes adatok kizárólag intézményi céllal kerülnek feldolgozásra, és a hatályos jogszabályok értelmében biztosítják azok védelmét és titkosságát. E célból, a 196/2003. számú törvényerejű rendeletben és annak módosításaiban és kiegészítéseiben foglaltak szerint a nyertes ajánlattevőnek alá kell írnia a személyes adatok kezelésére vonatkozó felhatalmazást.
20. Az érzékeny adatok kezelése
A benyújtott ajánlatokban található érzékeny adatok kezelése az ENAC igazgatótanácsának 2006. március 2-i ülésén jóváhagyott, az érzékeny és bűnüldözési adatok kezelésére vonatkozó rendeletben („Regolamento per il trattamento dei dati sensibili e giudiziari”) foglaltak szerint történik. A dokumentum elérhető az ENAC internetes oldalán, a www.enac-italia.it címen.
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/86 |
A 2408/92/EGK tanácsi rendelet 4. cikke (1) bekezdésének d) pontja értelmében Olaszország által közzétett ajánlattételi felhívás a Crotone–Milano Linate útvonalon oda és vissza közlekedő menetrend szerinti légi járatok működtetésére
(EGT-vonatkozású szöveg)
(2008/C 276/08)
ELŐZMÉNYEK
Az olasz kormány Infrastruktúraügyi és Közlekedési Minisztériuma a 2408/92/EGK rendelet 4. cikkének rendelkezései értelmében és a légifuvarozók Calabria tartományban megrendezett konferenciája alkalmával hozott határozatokkal összhangban jóváhagyta a Crotone–Milano Linate útvonalon oda és vissza közlekedő menetrend szerinti légi járatok működtetésére vonatkozó ezen ajánlattételi felhívást.
Az ezen közszolgáltatási kötelezettségek elrendelésével meghatározott előírások közzétételre kerültek az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában.
Abban az esetben, ha a fenti közszolgáltatási kötelezettség közzétételétől számított 30 napon belül egyetlen légifuvarozó sem jelezné azon szándékát, hogy az említett viszonylatban, a közszolgáltatási kötelezettségekkel összhangban, ellenszolgáltatás nélkül menetrendszerű járatokat indít, az olasz kormány Infrastruktúraügyi és Közlekedési Minisztériuma a 2408/92/EGK rendelet 4. cikke (1) bekezdésének d) pontjában meghatározott eljárással összhangban úgy határoz, hogy a hozzáférést egyetlen légifuvarozóra korlátozza, amelyet a közszolgáltatási kötelezettség alá eső járatoknak az említett rendeletben foglaltak szerinti biztosítása érdekében ajánlattételi eljárás keretében választ ki.
ÁLTALÁNOS RENDELKEZÉSEK
Ez a felhívás meghatározza az ajánlattételi eljárás tárgyát, az azon való részvétel módját, továbbá a szerződés időtartamára, módosítására és érvényességi idejére, a rendelkezések be nem tartása esetén alkalmazandó szankciókra, valamint az ajánlatot és a szerződés teljesítését alátámasztó biztosítékokra vonatkozó szabályokat.
A szóban forgó útvonalon a szolgáltatás működtetésére irányuló jog elnyerésének feltétele, hogy azt nyílt ajánlattételi eljárás keretében kell megszerezni, az ezen ajánlattételi felhívás 6. pontjában meghatározott pénzügyi ellentételezés összege szerinti legkedvezőbb ajánlat alapján.
1. Az ajánlattétel tárgya
Menetrend szerinti légi járatok működtetése a Crotone–Milano Linate útvonalon oda és vissza az elrendelt közszolgáltatási kötelezettségeknek megfelelően, amelyek a 2408/92/EGK rendelet rendelkezéseivel összhangban az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában kerültek kihirdetésre.
2. Részvétel
Az ajánlattételi felhívásra a 2408/92/EGK rendelet (2) cikkének b) pontjában meghatározott valamennyi közösségi légifuvarozó nyújthat be ajánlatot amennyiben teljesíti az alábbi követelményeket.
Általános követelmények
|
1. |
nem fizetésképtelen, nincs kötelező felszámolás vagy hitelezőkkel való egyezségkötésre irányuló eljárás alatt, illetve nincs folyamatban ezen tényállások megállapítására irányuló eljárás; |
|
2. |
nem volt a működéstől való eltiltásra ítélve sem a 231/2001. számú törvényerejű rendelet 9. cikkének (2) bekezdése, sem olyan más ítélet szerint, amelynek értelmében nem köthet szerződést közigazgatási szervekkel; |
|
3. |
teljesítette a munkaviszonyhoz kapcsolódó társadalombiztosítási járulékfizetési kötelezettségét; |
|
4. |
nem tett hamis nyilatkozatot olyan korábbi ajánlattételi eljárásokban való részvételre vonatkozó feltételeket illetően, amelyek közszolgáltatási kötelezettségeknek megfelelően elrendelt légi járatok működtetésének elnyerésére irányultak. |
A fentiekben felsorolt feltételek teljesítését a pályázók a 3. pont vonatkozásában az INPS (Istituto Nazionale della Previdenza Sociale – Országos Társadalombiztosítási Intézet) vagy az INAIL (Istituto Nazionale Assicurazione contro gli Infortuni sul Lavoro – Országos Munkahelyi Balesetbiztosítási Intézet) által kibocsátott járulékfizetési igazolással, illetve az 1999. március 12-i 68. számú törvény („Norme per il diritto al lavoro dei disabili” – „A fogyatékkal élők munkához való jogára vonatkozó szabályok”) 17. cikke szerinti dokumentummal, az 1., 2. és 4. pont vonatkozásában pedig a köztársasági elnök 2000. december 28-i 445. számú rendelete 46. és 47. cikkének megfelelő helyettesítő nyilatkozattal igazolhatják.
Nem olaszországi, hanem az Európai Unió más tagországában működő pályázók esetében az illetőség szerinti ország közigazgatási és hatósági szerveinek kell kibocsátania ezeket az igazolásokat és nyilatkozatokat, és azokhoz az olasz konzulátus által hitelesített olasz fordítást is csatolni kell.
Műszaki követelmények
|
1. |
a 2407/92/EGK rendeletnek megfelelően kiadott légifuvarozói működési engedély; |
|
2. |
különösen az utasokra, a poggyászra, a rakományra és a harmadik felekre vonatkozó kötelező biztosítás, többek között a 785/2004/EK rendelet értelmében; |
|
3. |
a közösségi szabályokkal összhangban lévő üzemben tartási engedély (AOC); |
|
4. |
nem pályázhatnak olyan légitársaságok, amelyek szerepelnek a http://ec.europa.eu/transport/air-ban internetcímen közzétett, az európai biztonsági előírásokat nem teljesítő légitársaságokat tartalmazó úgynevezett „feketelistán”; |
|
5. |
a pályázóknak olyan analitikus könyveléssel kell rendelkezniük, amelyben szerepelnek a lényeges költségek (beleértve az állandó költségeket és a bevételeket). |
Azokat a pályázókat, amelyek az ajánlattételi eljárásban való részvételre irányuló kérelem beadását követően kerülnek olyan helyzetbe, hogy a fenti követelmények valamelyikét nem tudják teljesíteni, automatikusan kizárják az ajánlatok értékeléséből.
Azon pályázók esetében, amelyek az 5. pontban említett szerződés megkötését követően kerülnek olyan helyzetbe, hogy a fenti követelmények valamelyikét nem tudják teljesíteni, az ezen ajánlattételi felhívás 14. pontjában és 15. pontjának utolsó előtti bekezdésében foglalt rendelkezéseket kell alkalmazni.
3. Eljárás
Erre az ajánlattételi felhívásra a 2408/92/EGK rendelet 4. cikke (1) bekezdésének d), e), f), h) és i) pontjainak rendelkezései vonatkoznak.
4. Dokumentáció
Az ajánlattételi eljárásra érvényes egyedi szabályokat, az ajánlatok érvényességi idejét és minden egyéb hasznosnak vélt információt tartalmazó teljes ajánlattételi dokumentáció, illetve az 5. pontban említett mintaszerződés ezen ajánlattételi felhívásnak minden értelemben szerves részét képezi és ingyenesen beszerezhető az alábbi címen: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio, 118, I-00185 Roma vagy az alábbi e-mail címen: trasporto.aereo@enac.rupa.it.
5. A szolgáltatás nyújtását szabályozó szerződés
A szolgáltatást a légifuvarozó és az olaszországi Nemzeti Polgári Légiközlekedési Hatóság (ENAC) között létrejött, az ajánlattételi dokumentáció részét képező minta alapján szerkesztett szerződés szabályozza.
6. Pénzügyi ellentételezés
A szóban forgó útvonalon légi járatok üzemeltetéséért járó – a pályázati eljárás keretében meghatározott – pénzügyi ellentételezés legmagasabb összege évente 1 258 178,33 EUR, amely tartalmazza a HÉÁ-t is.
Az ajánlattételi dokumentációban foglaltak szerint elkészített ajánlatokban az adatlap pénzügyi ajánlatra vonatkozó részénél éves bontásban, egyértelműen meg kell jelölni a szóban forgó szolgáltatás működtetéséért ellentételezés címén igényelt legmagasabb összeget, az előzőekben rögzített felső határon belül.
Az ellentételezés pontos összege minden évben visszamenőleg kerül megállapításra a ténylegesen felmerült kiadások és a szolgáltatás során ténylegesen termelt jövedelem alapján, bizonylatok bemutatása ellenében és az ajánlatban megjelölt legmagasabb összeg mértékéig, az ajánlattételi dokumentációban meghatározottak szerint.
A légifuvarozó semmi esetre sem igényelhet pénzügyi ellentételezés címén a szerződésben megállapított felső határnál magasabb összeget, tekintettel arra, hogy a folyósított összeg nem díjazásnak, hanem a közszolgáltatási kötelezettségek keretében nyújtott szolgáltatás vállalásáért nyújtott ellentételezésnek minősül.
Az éves kifizetések – az ajánlattételi dokumentációban meghatározottak szerint – előlegek formájában történnek, majd ezt követi az elszámolás, kivéve azokat az eseteket, amikor az ENAC esetleges ellenőrzések keretében megvizsgálja a nyújtott ellentételezés tényleges rendeltetését, illetve azt, hogy az ajánlattételi eljárásban nyertes légifuvarozó továbbra is teljesíti-e az előírt követelményeket. Az elszámolásra azt követően kerül sor, hogy ellenőrizték az adott útvonal vonatkozásában a légifuvarozó által benyújtott részletes elszámolást, illetve azt, hogy a nyújtott szolgáltatás megfelel-e a szerződésben foglaltaknak.
7. Viteldíjak
A benyújtott ajánlatoknak – az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában közzétett, a közszolgáltatási kötelezettségekre vonatkozó közleménynek megfelelően – tartalmazniuk kell a várható viteldíjakat.
8. Az útvonal megindítása
A szóban forgó útvonalon a szerződés aláírásától számított 15 napon belül meg kell kezdeni a szolgáltatást, amelynek tényét a nyertes légifuvarozó és az ENAC által aláírt jegyzőkönyv igazolja.
9. A szerződés időtartama
A szerződés a szolgáltatásnak a szóban forgó útvonalon történő tényleges elindításától számított kétéves időtartamra szól.
A légifuvarozó vállalja, hogy az ENAC rendelkezésére bocsátja alkalmazottait, műszaki és számviteli dokumentumait, berendezéseit, illetve minden egyebet, amely a Bizottság közleményében, a közszolgáltatási kötelezettséget elrendelő rendeletben, ezen ajánlattételi felhívásban, a szerződésben, valamint az ajánlattételi dokumentációban foglalt rendelkezések megfelelő teljesítésének, alkalmazásának és végrehajtásának ellenőrzésére irányuló felügyeleti tevékenység és ellenőrzés során szükségessé válik.
Az előző bekezdésben foglalt kötelezettségek be nem tartása esetén az ezen ajánlattételi felhívás 11. pontjában foglaltak szerint szankciók szabhatók ki.
10. Elállás a szerződéstől
A szerződő felek bármelyike hathónapos előzetes értesítést követően jogosult a szerződés határidejének lejárta előtti, díjfizetési vagy kártalanítási kötelezettség nélküli felmondásra, de minden esetben csak a szolgáltatás elindításától számított egy év eltelte után.
Előzetes értesítés nélküli elállásnak minősül, ha a légifuvarozó az általa működtetett, közszolgáltatási kötelezettség alá eső szolgáltatást megszakítja, és a vállalt kötelezettségek hiánytalan teljesítését az ENAC-tól kapott figyelmeztetés kézhezvételétől számított 30 napon belül sem kezdi meg újra.
Amennyiben a légifuvarozó a szerződéstől eláll, az ENAC fenntartja a jogot arra, hogy elvégezze a szükséges elemzéseket annak érdekében, hogy az Infrastruktúraügyi és Közlekedési Minisztériumnak javaslatot tegyen új szerződés megkötésére az ajánlatok értékelésekor a következő helyre rangsorolt légifuvarozóval. A közszolgáltatási kötelezettség alá eső szolgáltatásnyújtás feltételei és az arányosan járó ellentételezés ugyanazok lesznek, mint a közszolgáltatási kötelezettség gyakorlásának eredeti odaítélésekor meghatározottak.
11. Mulasztások és szankciók
Nem tekinthető a légifuvarozónak felróható mulasztásnak a szolgáltatás következő okok miatt való megszakítása:
|
— |
veszélyes időjárási körülmények, |
|
— |
a működési programban megjelölt valamelyik repülőtér bezárása, |
|
— |
biztonsági problémák, |
|
— |
sztrájk, |
|
— |
vis maior esetek. |
Ha a szolgáltatás a fenti okok miatt szakad meg, a kimaradt járatok arányában csökken az ellentételezés összege.
A szerződésben foglalt szolgáltatások és az abban vállalt kötelezettségek be nem tartása esetén az ENAC jogosult büntetést kiszabni a légifuvarozóra, amely az elkövetett szerződésszegések számával arányosan növekszik. Ennek módja a mintaszerződésben részletesen rögzítésre kerül.
A büntetések összege semmi esetre sem haladhatja meg az ajánlat alapját képező, a 6. pontban említett pénzügyi ellentételezés maximális összegének 50 %-át, azzal a kikötéssel, hogy ezen határ átlépése esetén az ENAC jogosult a szerződés mulasztás miatti felmondására, aminek következtében a még folyósítandó ellentételezéseket azonnali hatállyal visszavonják.
A közvetlenül a légifuvarozónak felróható okokból bekövetkező járattörlések száma évente nem haladhatja meg a tervezett járatok 2 %-át.
Ezen tűréshatáron felül a légifuvarozó köteles az ENAC részére büntetés címén minden egyes, a 2 %-os határ fölötti járattörlés esetén 3 000,00 EUR-t fizetni. Erről előzőleg hivatalos értesítést kap, amelyet az esemény ismertté válását követő 10 napon belül kell megküldeni a légifuvarozónak. A légifuvarozónak a kifogás kézhezvételét követően legfeljebb 7 nap áll rendelkezésére, hogy benyújtsa esetleges ellenérveit.
Ezenkívül az ENAC felülvizsgálja és az elindított járatokkal arányos mértékben módosítja a pénzügyi ellentételezés összegét. Az ilyen jogcímen befolyt összeget Crotone város területi folytonosságának finanszírozására különítik el.
A 10. cikkben említett előzetes értesítési kötelezettség figyelmen kívül hagyása esetén bírság szabható ki, amely az éves ellentételezés összege és az értesítés elmulasztásának a közszolgáltatási kötelezettség alá eső szolgáltatás megszakításától számított ideje alapján kerül kiszámításra, a 10. pontban meghatározott feltételek szerint, az alábbi képlet alapján:
P = CA/GG × gg
Ahol:
|
P |
= |
bírság |
|
CA |
= |
éves ellentételezés |
|
GG |
= |
a szóban forgó év napjainak száma (365 vagy 366) |
|
gg |
= |
az értesítés elmulasztásának napjai |
Az ebben a pontban meghatározott szankciók összevonhatók az ezen témakörre vonatkozó közösségi szabályozásban, valamint a nemzeti jogszabályokban és szabályozó rendelkezésekben meghatározott bírságokkal.
12. Az ajánlatot alátámasztó biztosítékok
Az ajánlat komolyságának és megbízhatóságának alátámasztására az ajánlattételi eljárásban részt vevő légifuvarozóknak a 6. pontban említett pénzügyi ellentételezés maximális összegének 2 %-ával megegyező összegű biztosítékot kell elhelyezniük, tetszés szerint kaució, illetve biztosítási vagy banki kezességvállalás formájában.
A fenti biztosíték elhelyezésének módjával kapcsolatos részleteket az ajánlattételi dokumentáció tartalmazza, illetve azok esetlegesen a szerződésben is rögzítésre kerülnek.
A biztosíték érvényességi idejének az ajánlatok beadási határidejétől számított legalább 180 napnak kell lennie, és a légifuvarozónak vállalnia kell, hogy abban az esetben, ha szolgáltatásnyújtás jogának odaítélése határidőre nem történik meg, akkor a biztosíték érvényességi idejét az ENAC ugyanezen eljárás keretében tett kérésére meghosszabbítja.
Amikor az ENAC az ajánlattételi eljárásban nem nyertes légifuvarozókat tájékoztatja az eredményről, egyúttal az általuk elhelyezett biztosítékokat is felszabadítja.
13. A teljesítésre vonatkozó biztosítékok és a biztosítási fedezet
Az ezen ajánlattételi felhívás tárgyát képező közszolgáltatási kötelezettség alá eső járatok működtetésének jogát elnyerő légifuvarozó köteles – biztosítási vagy banki kezességvállalás révén – 700 000,00 EUR összegben biztosítékot letétbe helyezni az ENAC javára, amely ezt az összeget a közszolgáltatási kötelezettség alá eső szolgáltatás teljesítésének biztosítására használhatja fel.
A biztosíték felszabadítása automatikusan, az ENAC jóváhagyása nélkül történik, azt követően, hogy a 6. pont utolsó bekezdésében említett ellenőrzés kedvező eredménnyel zárul.
14. A pénzügyi ellentételezés hatályának megszűnése vagy annak visszavonása
Amennyiben a nyertes légifuvarozó olyan helyzetbe kerül, hogy az ezen ajánlattételi felhívás 2. pontjában, illetve az ajánlattételi dokumentációban említett általános és műszaki követelmények bármelyikét a szerződés megkötését követően nem tudja teljesíteni, az útvonalra vonatkozó megbízás hatályát veszti, a pénzügyi ellentételezést visszavonják és azokat a részleteket, amelyeket esetlegesen már folyósítottak, de amelyekre a légifuvarozó már nem volt jogosult, a jogos kamatokkal növelve behajtják.
Az útvonalra vonatkozó megbízás visszavonását követően az Infrastruktúraügyi és Közlekedési Minisztérium felhatalmazhatja az ENAC-ot arra, hogy az adott útvonalra vonatkozó szolgáltatás még hátralévő idejére új szerződést írjon alá az ajánlatok értékelésekor a következő helyen végzett légifuvarozóval.
Ebben az esetben a szerződés időtartama a szolgáltatás elindításának időpontjától a megszüntetett szerződésben foglalt eredeti időpontig tart, figyelembe véve az ajánlattételi eljárásban nyertes légifuvarozó által benyújtott ajánlat értékelésekor jóváhagyott működési programot.
15. A szerződés megszűnése
Amennyiben a légifuvarozó nem tartja be az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában közzétett, a kötelezettségekre vonatkozó közleményben, valamint a közszolgáltatási kötelezettséget elrendelő rendeletben, a szerződésben, az ezen ajánlattételi felhívásban vagy az ajánlattételi dokumentációban foglalt előírásokat, az ENAC a polgári törvénykönyv 1454. cikkének értelmében jogosult írásban felszólítani a légifuvarozót arra, hogy a felszólítás kézhezvételétől számítva 15 napon belül szüntesse meg mulasztását.
A határidő lejárta után az ENAC a szerződést semmisnek tekintheti és a 13. pontban említett biztosíték összegét véglegesen visszatarthatja, továbbá a légifuvarozóval szemben eljárhat a kár megtérítése érdekében.
Továbbá ha a légifuvarozó a szerződésben, az ezen ajánlattételi felhívás rendelkezéseiben vagy az ajánlattételi dokumentációban foglalt kötelezettségeket és szolgáltatásokat nem teljesíti, az ENAC a polgári törvénykönyv 1456. cikkének értelmében előzetes írásbeli figyelmeztetést követően jogosult a szerződés felbontására.
A szerződés felbontása esetén a Infrastruktúraügyi és Közlekedési Minisztérium felhatalmazhatja az ENAC-ot arra, hogy az adott útvonalra vonatkozó szolgáltatás még hátralévő idejére új szerződést írjon alá az útvonalra vonatkozó megbízás odaítélésekor a következő helyen végzett légifuvarozóval.
Ebben az esetben a szerződés időtartama a szolgáltatás elindításának időpontjától a megszüntetett szerződésben foglalt eredeti időpontig tart, figyelembe véve az ajánlattételi eljárásban nyertes légifuvarozó által benyújtott ajánlat értékelésekor jóváhagyott működési programot.
16. Az ajánlatok benyújtása
Az ajánlatokat ezen ajánlattételi felhívásnak az Európai Unió Hivatalos Lapjában történő kihirdetésétől számított 30 napon belül, az ajánlati dokumentációban foglaltaknak megfelelő formában, a kizárás terhe mellett, tértivevényes ajánlott küldemény útján vagy közvetlenül, megfelelő átvételi elismervény ellenében a következő címre kell eljuttatni: ENAC – Direzione Generale, viale del Castro Pretorio, 118, I-00185 Roma.
Az ajánlatokat a kizárás terhe mellett három lezárt és lepecsételt borítékban kell benyújtani.
A külső lezárt, lepecsételt és mindkét szélén szignált borítékon, amelyben a két másik, szintén lepecsételt és mindkét szélén szignált borítékot kell elhelyezni, az alábbiakat kell feltüntetni:„Offerta per la gara in oneri di servizio pubblico sulla rotta Crotone – Milano Linate e viceversa”.
Az ezen ajánlattételi felhívás 4. pontjában említett ajánlattételi dokumentáció rögzíti, hogy milyen dokumentumokat kell az említett három borítékban elhelyezni.
A felek tudomásul veszik, hogy amennyiben bármilyen okból kifolyólag a küldemény a fenti határidőre nem érkezik meg a címre, az kizárólag a feladó felelőssége.
Az ajánlattételi eljárásban abban az esetben is lehet eredményt hirdetni, ha csak egy érvényes ajánlat érkezik.
17. Az ajánlatok érvényességi ideje
Az ajánlatok benyújtásának határidejétől számított 180 nap.
18. A pályázati eljárás lefolytatása
Az ajánlatok elbírálásáról az ENAC gondoskodik, amely e célra bizottságot nevez ki: ennek tagja egy, az ENAC főigazgatója által delegált vezető, a Calabria tartomány által kinevezett légiközlekedési szakértő, valamint az ENAC és Calabria tartomány által egyetértésben megválasztott elnök. A titkársági teendőket az ENAC egy hivatalnoka végzi.
19. A személyes adatok kezelése
A személyes adatok kizárólag intézményi céllal kerülnek feldolgozásra, és a hatályos jogszabályok értelmében biztosítják azok védelmét és titkosságát. E célból, a 196/2003. számú törvényerejű rendeletben és annak módosításaiban és kiegészítéseiben foglaltak szerint a nyertes ajánlattevőnek alá kell írnia a személyes adatok kezelésére vonatkozó felhatalmazást.
20. Az érzékeny adatok kezelése
A benyújtott ajánlatokban található érzékeny adatok kezelése az ENAC igazgatótanácsának 2006. március 2-i ülésén jóváhagyott, az érzékeny és bűnüldözési adatok kezelésére vonatkozó rendeletben („Regolamento per il trattamento dei dati sensibili e giudiziari”) foglaltak szerint történik. A dokumentum elérhető az ENAC internetes oldalán, a www.enac-italia.it címen.
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/90 |
A 2408/92/EGK tanácsi rendelet 4. cikke (1) bekezdésének d) pontja értelmében Olaszország által közzétett ajánlattételi felhívás a Crotone–Roma Fiumicino útvonalon oda és vissza közlekedő menetrend szerinti légi járatok működtetésére
(EGT-vonatkozású szöveg)
(2008/C 276/09)
ELŐZMÉNYEK
Az olasz kormány Infrastruktúraügyi és Közlekedési Minisztériuma a 2408/92/EGK rendelet 4. cikkének rendelkezései értelmében és a légifuvarozók Calabria tartományban megrendezett konferenciája alkalmával hozott határozatokkal összhangban jóváhagyta a Crotone–Roma Fiumicino útvonalon oda és vissza közlekedő menetrend szerinti légi járatok működtetésére vonatkozó ezen ajánlattételi felhívást.
Az ezen közszolgáltatási kötelezettségek elrendelésével meghatározott előírások közzétételre kerültek az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában.
Abban az esetben, ha a fenti közszolgáltatási kötelezettség közzétételétől számított 30 napon belül egyetlen légifuvarozó sem jelezné azon szándékát, hogy az említett viszonylatban, a közszolgáltatási kötelezettségekkel összhangban, ellenszolgáltatás nélkül menetrendszerű járatokat indít, az olasz kormány Infrastruktúraügyi és Közlekedési Minisztériuma a 2408/92/EGK rendelet 4. cikke (1) bekezdésének d) pontjában meghatározott eljárással összhangban úgy határoz, hogy a hozzáférést egyetlen légifuvarozóra korlátozza, amelyet a közszolgáltatási kötelezettség alá eső járatoknak az említett rendeletben foglaltak szerinti biztosítása érdekében ajánlattételi eljárás keretében választ ki.
ÁLTALÁNOS RENDELKEZÉSEK
Ez a felhívás meghatározza az ajánlattételi eljárás tárgyát, az azon való részvétel módját, továbbá a szerződés időtartamára, módosítására és érvényességi idejére, a rendelkezések be nem tartása esetén alkalmazandó szankciókra, valamint az ajánlatot és a szerződés teljesítését alátámasztó biztosítékokra vonatkozó szabályokat.
A szóban forgó útvonalon a szolgáltatás működtetésére irányuló jog elnyerésének feltétele, hogy azt nyílt ajánlattételi eljárás keretében kell megszerezni, az ezen ajánlattételi felhívás 6. pontjában meghatározott pénzügyi ellentételezés összege szerinti legkedvezőbb ajánlat alapján.
1. Az ajánlattétel tárgya
Menetrend szerinti légi járatok működtetése a Crotone–Roma Fiumicino útvonalon oda és vissza az elrendelt közszolgáltatási kötelezettségeknek megfelelően, amelyek a 2408/92/EGK rendelet rendelkezéseivel összhangban az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában kerültek kihirdetésre.
2. Részvétel
Az ajánlattételi felhívásra a 2408/92/EGK rendelet 2. cikkének b) pontjában meghatározott valamennyi közösségi légifuvarozó nyújthat be ajánlatot amennyiben teljesíti az alábbi követelményeket.
Általános követelmények
|
1. |
nem fizetésképtelen, nincs kötelező felszámolás vagy hitelezőkkel való egyezségkötésre irányuló eljárás alatt, illetve nincs folyamatban ezen tényállások megállapítására irányuló eljárás; |
|
2. |
nem volt a működéstől való eltiltásra ítélve sem a 231/2001. számú törvényerejű rendelet 9. cikkének (2) bekezdése, sem olyan más ítélet szerint, amelynek értelmében nem köthet szerződést közigazgatási szervekkel; |
|
3. |
teljesítette a munkaviszonyhoz kapcsolódó társadalombiztosítási járulékfizetési kötelezettségét; |
|
4. |
nem tett hamis nyilatkozatot olyan korábbi ajánlattételi eljárásokban való részvételre vonatkozó feltételeket illetően, amelyek közszolgáltatási kötelezettségeknek megfelelően elrendelt légi járatok működtetésének elnyerésére irányultak. |
A fentiekben felsorolt feltételek teljesítését a pályázók a 3. pont vonatkozásában az INPS (Istituto Nazionale della Previdenza Sociale – Országos Társadalombiztosítási Intézet) vagy az INAIL (Istituto Nazionale Assicurazione contro gli Infortuni sul Lavoro – Országos Munkahelyi Balesetbiztosítási Intézet) által kibocsátott járulékfizetési igazolással, illetve az 1999. március 12-i 68. számú törvény („Norme per il diritto al lavoro dei disabili” – „A fogyatékkal élők munkához való jogára vonatkozó szabályok”) 17. cikke szerinti dokumentummal, az 1., 2. és 4. pont vonatkozásában pedig a köztársasági elnök 2000. december 28-i 445. számú rendelete 46. és 47. cikkének megfelelő helyettesítő nyilatkozattal igazolhatják.
Nem olaszországi, hanem az Európai Unió más tagországában működő pályázók esetében az illetőség szerinti ország közigazgatási és hatósági szerveinek kell kibocsátania ezeket az igazolásokat és nyilatkozatokat, és azokhoz az olasz konzulátus által hitelesített olasz fordítást is csatolni kell.
Műszaki követelmények
|
1. |
a 2407/92/EGK rendeletnek megfelelően kiadott légifuvarozói működési engedély; |
|
2. |
különösen az utasokra, a poggyászra, a rakományra és a harmadik felekre vonatkozó kötelező biztosítás, többek között a 785/2004/EK rendelet értelmében; |
|
3. |
a közösségi szabályokkal összhangban lévő üzemben tartási engedély (AOC); |
|
4. |
nem pályázhatnak olyan légitársaságok, amelyek szerepelnek a http://ec.europa.eu/transport/air-ban internetcímen közzétett, az európai biztonsági előírásokat nem teljesítő légitársaságokat tartalmazó úgynevezett „feketelistán”; |
|
5. |
a pályázóknak olyan analitikus könyveléssel kell rendelkezniük, amelyben szerepelnek a lényeges költségek (beleértve az állandó költségeket és a bevételeket). |
Azokat a pályázókat, amelyek az ajánlattételi eljárásban való részvételre irányuló kérelem beadását követően kerülnek olyan helyzetbe, hogy a fenti követelmények valamelyikét nem tudják teljesíteni, automatikusan kizárják az ajánlatok értékeléséből.
Azon pályázók esetében, amelyek az 5. pontban említett szerződés megkötését követően kerülnek olyan helyzetbe, hogy a fenti követelmények valamelyikét nem tudják teljesíteni, az ezen ajánlattételi felhívás 14. pontjában és 15. pontjának utolsó előtti bekezdésében foglalt rendelkezéseket kell alkalmazni.
3. Eljárás
Erre az ajánlattételi felhívásra a 2408/92/EGK rendelet 4. cikke (1) bekezdésének d), e), f), h) és i) pontjainak rendelkezései vonatkoznak.
4. Dokumentáció
Az ajánlattételi eljárásra érvényes egyedi szabályokat, az ajánlatok érvényességi idejét és minden egyéb hasznosnak vélt információt tartalmazó teljes ajánlattételi dokumentáció, illetve az 5. pontban említett mintaszerződés ezen ajánlattételi felhívásnak minden értelemben szerves részét képezi és ingyenesen beszerezhető az alábbi címen: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio, 118, I-00185 Roma vagy az alábbi e-mail címen: trasporto.aereo@enac.rupa.it.
5. A szolgáltatás nyújtását szabályozó szerződés
A szolgáltatást a légifuvarozó és az olaszországi Nemzeti Polgári Légiközlekedési Hatóság (ENAC) között létrejött, az ajánlattételi dokumentáció részét képező minta alapján szerkesztett szerződés szabályozza.
6. Pénzügyi ellentételezés
A szóban forgó útvonalon légi járatok üzemeltetéséért járó – a pályázati eljárás keretében meghatározott – pénzügyi ellentételezés legmagasabb összege évente 1 724 666,00 EUR, amely tartalmazza a HÉÁ-t is.
Az ajánlattételi dokumentációban foglaltak szerint elkészített ajánlatokban az adatlap pénzügyi ajánlatra vonatkozó részénél éves bontásban, egyértelműen meg kell jelölni a szóban forgó szolgáltatás működtetéséért ellentételezés címén igényelt legmagasabb összeget, az előzőekben rögzített felső határon belül.
Az ellentételezés pontos összege minden évben visszamenőleg kerül megállapításra a ténylegesen felmerült kiadások és a szolgáltatás során ténylegesen termelt jövedelem alapján, bizonylatok bemutatása ellenében és az ajánlatban megjelölt legmagasabb összeg mértékéig, az ajánlattételi dokumentációban meghatározottak szerint.
A légifuvarozó semmi esetre sem igényelhet pénzügyi ellentételezés címén a szerződésben megállapított felső határnál magasabb összeget, tekintettel arra, hogy a folyósított összeg nem díjazásnak, hanem a közszolgáltatási kötelezettségek keretében nyújtott szolgáltatás vállalásáért nyújtott ellentételezésnek minősül.
Az éves kifizetések – az ajánlattételi dokumentációban meghatározottak szerint – előlegek formájában történnek, majd ezt követi az elszámolás, kivéve azokat az eseteket, amikor az ENAC esetleges ellenőrzések keretében megvizsgálja a nyújtott ellentételezés tényleges rendeltetését, illetve azt, hogy az ajánlattételi eljárásban nyertes légifuvarozó továbbra is teljesíti-e az előírt követelményeket. Az elszámolásra azt követően kerül sor, hogy ellenőrizték az adott útvonal vonatkozásában a légifuvarozó által benyújtott részletes elszámolást, illetve azt, hogy a nyújtott szolgáltatás megfelel-e a szerződésben foglaltaknak.
7. Viteldíjak
A benyújtott ajánlatoknak – az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában közzétett, a közszolgáltatási kötelezettségekre vonatkozó közleménynek megfelelően – tartalmazniuk kell a várható viteldíjakat.
8. Az útvonal megindítása
A szóban forgó útvonalon a szerződés aláírásától számított 15 napon belül meg kell kezdeni a szolgáltatást, amelynek tényét a nyertes légifuvarozó és az ENAC által aláírt jegyzőkönyv igazolja.
9. A szerződés időtartama
A szerződés a szolgáltatásnak a szóban forgó útvonalon történő tényleges elindításától számított kétéves időtartamra szól.
A légifuvarozó vállalja, hogy az ENAC rendelkezésére bocsátja alkalmazottait, műszaki és számviteli dokumentumait, berendezéseit, illetve minden egyebet, amely a Bizottság közleményében, a közszolgáltatási kötelezettséget elrendelő rendeletben, ezen ajánlattételi felhívásban, a szerződésben, valamint az ajánlattételi dokumentációban foglalt rendelkezések megfelelő teljesítésének, alkalmazásának és végrehajtásának ellenőrzésére irányuló felügyeleti tevékenység és ellenőrzés során szükségessé válik.
Az előző bekezdésben foglalt kötelezettségek be nem tartása esetén az ezen ajánlattételi felhívás 11. pontjában foglaltak szerint szankciók szabhatók ki.
10. Elállás a szerződéstől
A szerződő felek bármelyike hathónapos előzetes értesítést követően jogosult a szerződés határidejének lejárta előtti, díjfizetési vagy kártalanítási kötelezettség nélküli felmondásra, de minden esetben csak a szolgáltatás elindításától számított egy év eltelte után.
Előzetes értesítés nélküli elállásnak minősül, ha a légifuvarozó az általa működtetett, közszolgáltatási kötelezettség alá eső szolgáltatást megszakítja, és a vállalt kötelezettségek hiánytalan teljesítését az ENAC-tól kapott figyelmeztetés kézhezvételétől számított 30 napon belül sem kezdi meg újra.
Amennyiben a légifuvarozó a szerződéstől eláll, az ENAC fenntartja a jogot arra, hogy elvégezze a szükséges elemzéseket annak érdekében, hogy az Infrastruktúraügyi és Közlekedési Minisztériumnak javaslatot tegyen új szerződés megkötésére az ajánlatok értékelésekor a következő helyre rangsorolt légifuvarozóval. A közszolgáltatási kötelezettség alá eső szolgáltatásnyújtás feltételei és az arányosan járó ellentételezés ugyanazok lesznek, mint a közszolgáltatási kötelezettség gyakorlásának eredeti odaítélésekor meghatározottak.
11. Mulasztások és szankciók
Nem tekinthető a légifuvarozónak felróható mulasztásnak a szolgáltatás következő okok miatt való megszakítása:
|
— |
veszélyes időjárási körülmények, |
|
— |
a működési programban megjelölt valamelyik repülőtér bezárása, |
|
— |
biztonsági problémák, |
|
— |
sztrájk, |
|
— |
vis maior esetek. |
Ha a szolgáltatás a fenti okok miatt szakad meg, a kimaradt járatok arányában csökken az ellentételezés összege.
A szerződésben foglalt szolgáltatások és az abban vállalt kötelezettségek be nem tartása esetén az ENAC jogosult büntetést kiszabni a légifuvarozóra, amely az elkövetett szerződésszegések számával arányosan növekszik. Ennek módja a mintaszerződésben részletesen rögzítésre kerül.
A büntetések összege semmi esetre sem haladhatja meg az ajánlat alapját képező, a 6. pontban említett pénzügyi ellentételezés maximális összegének 50 %-át, azzal a kikötéssel, hogy ezen határ átlépése esetén az ENAC jogosult a szerződés mulasztás miatti felmondására, aminek következtében a még folyósítandó ellentételezéseket azonnali hatállyal visszavonják.
A közvetlenül a légifuvarozónak felróható okokból bekövetkező járattörlések száma évente nem haladhatja meg a tervezett járatok 2 %-át.
Ezen tűréshatáron felül a légifuvarozó köteles az ENAC részére büntetés címén minden egyes, a 2 %-os határ fölötti járattörlés esetén 3 000,00 EUR-t fizetni. Erről előzőleg hivatalos értesítést kap, amelyet az esemény ismertté válását követő 10 napon belül kell megküldeni a légifuvarozónak. A légifuvarozónak a kifogás kézhezvételét követően legfeljebb 7 nap áll rendelkezésére, hogy benyújtsa esetleges ellenérveit.
Ezenkívül az ENAC felülvizsgálja és az elindított járatokkal arányos mértékben módosítja a pénzügyi ellentételezés összegét. Az ilyen jogcímen befolyt összeget Crotone város területi folytonosságának finanszírozására különítik el.
A 10. cikkben említett előzetes értesítési kötelezettség figyelmen kívül hagyása esetén bírság szabható ki, amely az éves ellentételezés összege és az értesítés elmulasztásának a közszolgáltatási kötelezettség alá eső szolgáltatás megszakításától számított ideje alapján kerül kiszámításra, a 10. pontban meghatározott feltételek szerint, az alábbi képlet alapján:
P = CA/GG × gg
Ahol:
|
P |
= |
bírság |
|
CA |
= |
éves ellentételezés |
|
GG |
= |
a szóban forgó év napjainak száma (365 vagy 366) |
|
gg |
= |
az értesítés elmulasztásának napjai |
Az ebben a pontban meghatározott szankciók összevonhatók az ezen témakörre vonatkozó közösségi szabályozásban, valamint a nemzeti jogszabályokban és szabályozó rendelkezésekben meghatározott bírságokkal.
12. Az ajánlatot alátámasztó biztosítékok
Az ajánlat komolyságának és megbízhatóságának alátámasztására az ajánlattételi eljárásban részt vevő légifuvarozóknak a 6. pontban említett pénzügyi ellentételezés maximális összegének 2 %-ával megegyező összegű biztosítékot kell elhelyezniük, tetszés szerint kaució, illetve biztosítási vagy banki kezességvállalás formájában.
A fenti biztosíték elhelyezésének módjával kapcsolatos részleteket az ajánlattételi dokumentáció tartalmazza, illetve azok esetlegesen a szerződésben is rögzítésre kerülnek.
A biztosíték érvényességi idejének az ajánlatok beadási határidejétől számított legalább 180 napnak kell lennie, és a légifuvarozónak vállalnia kell, hogy abban az esetben, ha szolgáltatásnyújtás jogának odaítélése határidőre nem történik meg, akkor a biztosíték érvényességi idejét az ENAC ugyanezen eljárás keretében tett kérésére meghosszabbítja.
Amikor az ENAC az ajánlattételi eljárásban nem nyertes légifuvarozókat tájékoztatja az eredményről, egyúttal az általuk elhelyezett biztosítékokat is felszabadítja.
13. A teljesítésre vonatkozó biztosítékok és a biztosítási fedezet
Az ezen ajánlattételi felhívás tárgyát képező közszolgáltatási kötelezettség alá eső járatok működtetésének jogát elnyerő légifuvarozó köteles – biztosítási vagy banki kezességvállalás révén – 700 000,00 EUR összegben biztosítékot letétbe helyezni az ENAC javára, amely ezt az összeget a közszolgáltatási kötelezettség alá eső szolgáltatás teljesítésének biztosítására használhatja fel.
A biztosíték felszabadítása automatikusan, az ENAC jóváhagyása nélkül történik, azt követően, hogy a 6. pont utolsó bekezdésében említett ellenőrzés kedvező eredménnyel zárul.
14. A pénzügyi ellentételezés hatályának megszűnése vagy annak visszavonása
Amennyiben a nyertes légifuvarozó olyan helyzetbe kerül, hogy az ezen ajánlattételi felhívás 2. pontjában, illetve az ajánlattételi dokumentációban említett általános és műszaki követelmények bármelyikét a szerződés megkötését követően nem tudja teljesíteni, az útvonalra vonatkozó megbízás hatályát veszti, a pénzügyi ellentételezést visszavonják és azokat a részleteket, amelyeket esetlegesen már folyósítottak, de amelyekre a légifuvarozó már nem volt jogosult, a jogos kamatokkal növelve behajtják.
Az útvonalra vonatkozó megbízás visszavonását követően az Infrastruktúraügyi és Közlekedési Minisztérium felhatalmazhatja az ENAC-ot arra, hogy az adott útvonalra vonatkozó szolgáltatás még hátralévő idejére új szerződést írjon alá az ajánlatok értékelésekor a következő helyen végzett légifuvarozóval.
Ebben az esetben a szerződés időtartama a szolgáltatás elindításának időpontjától a megszüntetett szerződésben foglalt eredeti időpontig tart, figyelembe véve az ajánlattételi eljárásban nyertes légifuvarozó által benyújtott ajánlat értékelésekor jóváhagyott működési programot.
15. A szerződés megszűnése
Amennyiben a légifuvarozó nem tartja be az Európai Unió Hivatalos Lapja C sorozatának 2008. szeptember 20-i 241. számában közzétett, a kötelezettségekre vonatkozó közleményben, valamint a közszolgáltatási kötelezettséget elrendelő rendeletben, a szerződésben, az ezen ajánlattételi felhívásban vagy az ajánlattételi dokumentációban foglalt előírásokat, az ENAC a polgári törvénykönyv 1454. cikkének értelmében jogosult írásban felszólítani a légifuvarozót arra, hogy a felszólítás kézhezvételétől számítva 15 napon belül szüntesse meg mulasztását.
A határidő lejárta után az ENAC a szerződést semmisnek tekintheti és a 13. pontban említett biztosíték összegét véglegesen visszatarthatja, továbbá a légifuvarozóval szemben eljárhat a kár megtérítése érdekében.
Továbbá ha a légifuvarozó a szerződésben, az ezen ajánlattételi felhívás rendelkezéseiben vagy az ajánlattételi dokumentációban foglalt kötelezettségeket és szolgáltatásokat nem teljesíti, az ENAC a polgári törvénykönyv 1456. cikkének értelmében előzetes írásbeli figyelmeztetést követően jogosult a szerződés felbontására.
A szerződés felbontása esetén a Infrastruktúraügyi és Közlekedési Minisztérium felhatalmazhatja az ENAC-ot arra, hogy az adott útvonalra vonatkozó szolgáltatás még hátralévő idejére új szerződést írjon alá az útvonalra vonatkozó megbízás odaítélésekor a következő helyen végzett légifuvarozóval.
Ebben az esetben a szerződés időtartama a szolgáltatás elindításának időpontjától a megszüntetett szerződésben foglalt eredeti időpontig tart, figyelembe véve az ajánlattételi eljárásban nyertes légifuvarozó által benyújtott ajánlat értékelésekor jóváhagyott működési programot.
16. Az ajánlatok benyújtása
Az ajánlatokat ezen ajánlattételi felhívásnak az Európai Unió Hivatalos Lapjában történő kihirdetésétől számított 30 napon belül, az ajánlati dokumentációban foglaltaknak megfelelő formában, a kizárás terhe mellett, tértivevényes ajánlott küldemény útján vagy közvetlenül, megfelelő átvételi elismervény ellenében a következő címre kell eljuttatni: ENAC – Direzione Generale, viale del Castro Pretorio, 118, I-00185 Roma.
Az ajánlatokat a kizárás terhe mellett három lezárt és lepecsételt borítékban kell benyújtani.
A külső lezárt, lepecsételt és mindkét szélén szignált borítékon, amelyben a két másik, szintén lepecsételt és mindkét szélén szignált borítékot kell elhelyezni, az alábbiakat kell feltüntetni: „Offerta per la gara in oneri di servizio pubblico sulla rotta Crotone – Roma Fiumicino e viceversa”.
Az ezen ajánlattételi felhívás 4. pontjában említett ajánlattételi dokumentáció rögzíti, hogy milyen dokumentumokat kell az említett három borítékban elhelyezni.
A felek tudomásul veszik, hogy amennyiben bármilyen okból kifolyólag a küldemény a fenti határidőre nem érkezik meg a címre, az kizárólag a feladó felelőssége.
Az ajánlattételi eljárásban abban az esetben is lehet eredményt hirdetni, ha csak egy érvényes ajánlat érkezik.
17. Az ajánlatok érvényességi ideje
Az ajánlatok benyújtásának határidejétől számított 180 nap.
18. A pályázati eljárás lefolytatása
Az ajánlatok elbírálásáról az ENAC gondoskodik, amely e célra bizottságot nevez ki: ennek tagja egy, az ENAC főigazgatója által delegált vezető, a Calabria tartomány által kinevezett légiközlekedési szakértő, valamint az ENAC és Calabria tartomány által egyetértésben megválasztott elnök. A titkársági teendőket az ENAC egy hivatalnoka végzi.
19. A személyes adatok kezelése:
A személyes adatok kizárólag intézményi céllal kerülnek feldolgozásra, és a hatályos jogszabályok értelmében biztosítják azok védelmét és titkosságát. E célból, a 196/2003. számú törvényerejű rendeletben és annak módosításaiban és kiegészítéseiben foglaltak szerint a nyertes ajánlattevőnek alá kell írnia a személyes adatok kezelésére vonatkozó felhatalmazást.
20. Az érzékeny adatok kezelése
A benyújtott ajánlatokban található érzékeny adatok kezelése az ENAC igazgatótanácsának 2006. március 2-i ülésén jóváhagyott, az érzékeny és bűnüldözési adatok kezelésére vonatkozó rendeletben („Regolamento per il trattamento dei dati sensibili e giudiziari”) foglaltak szerint történik. A dokumentum elérhető az ENAC internetes oldalán, a www.enac-italia.it címen.
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/94 |
PÁLYÁZATI FELHÍVÁS – EACEA/29/08
Az oktatás és szakképzés terén európai uniós szinten aktív európai szövetségek
(2008/C 276/10)
1. A pályázati felhívás célja és leírása
A pályázati felhívás célja az oktatás és szakképzés terén működő, vagy az európai politika részét képező valamely célkitűzésért dolgozó európai szövetségek tevékenységének támogatása.
A támogatás jogalapja az élethosszig tartó tanulást célzó cselekvési program (az egész életen át tartó tanulás programja) (1), azon belül is annak „Jean Monnet alprogramja”.
A Jean Monnet program 3. kulcstevékenységének végrehajtása során e pályázati felhívás célkitűzései a következők:
|
— |
az oktatás és szakképzés terén aktív, magas minőségi szintet képviselő európai szövetségek támogatása, |
|
— |
az „Oktatás és szakképzés 2010” munkaprogramban közreműködő európai szövetségek támogatása (2), |
|
— |
az európai integrációs folyamattal kapcsolatos tudásnak és tudatosságnak az oktatáson és szakképzésen keresztüli növelésében közreműködő európai szövetségek támogatása. |
E pályázati felhívás keretében nyújtott közösségi támogatás a 2009. évre szóló, egyéves működési támogatás, mégpedig a kiválasztott európai szövetségek bizonyos működési és adminisztrációs kiadásainak finanszírozására.
Az ajánlattételi felhívás végrehajtásáért az Európai Bizottság („a Bizottság”) által felhatalmazott Oktatási, Audiovizuális és Kulturális Ügynökség („az Ügynökség”) felel.
2. Pályázásra jogosultak
Az az európai szövetség jogosult a pályázásra, amely megfelel a következő feltételeknek. A szervezet:
|
— |
non-profit szervezet, |
|
— |
a pályázásra jogosult országok (a 27 EU-tagállam, Izland, Liechtenstein, Norvégia és Törökország) valamelyikében található jogi személy, és ott (2008. december 23-án) több mint két éve székhellyel rendelkezik, |
|
— |
tevékenységének nagy részét az Európai Unió tagállamaiban, az Európai Gazdasági Térséghez tartozó országokban és/vagy a tagjelölt országokban végzi, |
|
— |
a költségvetési rendelet végrehajtási szabályairól szóló, a legutóbb a 478/2007/EK rendelettel módosított 2342/2002/EK, Euratom bizottsági rendelet 162. cikkének meghatározása szerinti általános európai érdeket szolgáló célt képviselő szervezetként működik (3), |
|
— |
európai uniós szinten tevékenykedik az oktatás és szakképzés területén, hivatalos alapokmányában lefektetett világos, pontosan meghatározott célok megvalósítása érdekében, |
|
— |
az „Oktatás és szakképzés 2010” munkaprogram prioritásainak megfelelő tevékenységet folytat, és/vagy hozzájárul az európai integrációs folyamattal kapcsolatos tudásnak és tudatosságnak az oktatáson és szakképzésen keresztüli növeléséhez, |
|
— |
vannak legalább 12 különböző EU-tagállamban székhellyel rendelkező tagszervezetei (4). Ezen tagszervezeteknek „teljes értékű tag” státusszal kell rendelkezniük (a társult tagok és a megfigyelők nem számítanak „teljes értékű tagnak”) transznacionális, nemzeti, regionális és helyi szinten. |
Megjegyzés: A magánszemélyek, egyéni ajánlattevők, egyes felsőoktatási intézmények, vagy államháztartási szervek és a tagállamok adminisztratív struktúráját képező intézmények nem tekintendők „szövetségnek”.
3. Odaítélési feltételek
A jogosult pályázatokat a 2009. évre szóló 12 hónapos, részletes munkaprogram minősége alapján fogják értékelni, a következő kritériumok szerint:
|
— |
a rövid távú (12 hónapos) célkitűzések fontossága, érthetősége és egységessége, |
|
— |
a munkaprogram lebonyolításának minősége (a tevékenységek, valamint a célkitűzések elérését szolgáló javasolt költségvetés világos és koherens volta, menetrend), |
|
— |
a tevékenységek valószínű hatása az európai szintű oktatásra és/vagy szakképzésre (különösen, hogy a pályázó európai szövetségek milyen mértékben járulnak hozzá az „Oktatás és szakképzés 2010” munkaprogramhoz és/vagy az európai integrációs folyamattal kapcsolatos ismeretek és tudatosság növeléséhez). |
A pályázók által az egyes odaítélési kritériumok vonatkozásában benyújtandó információk részletesebb leírását lásd: http://eacea.ec.europa.eu/index.htm. Kérjük, figyelmesen olvassák el a tájékoztatót.
4. Költségvetés és a projekt időtartama
A jelen ajánlattételi felhívás keretében az európai szövetségek társfinanszírozására előirányzott teljes közösségi költségvetés 600 000 EUR.
Az egy szövetségnek egy 12 hónapot felölelő (egy pénzügyi évnek megfelelő) éves munkaprogramra adható maximális működési támogatás nem haladhatja meg a 100 000 EUR-t.
A pályázó szervezetek két társfinanszírozási rendszer közül választhatnak.
|
a) |
költségvetés alapján történő támogatás: a támogatható költségek szokásos megtérítése, amely esetben a közösségi támogatás nem haladhatja meg a szövetség munkaprogramjának költségvetésében szereplő összes támogatható költség 75 %-át; |
|
b) |
átalányfinanszírozás: átalányfinanszírozás, amely esetben a közösségi támogatás nem haladhatja meg az adott évre vonatkozó előzetes pénzügyi eredménykimutatás főösszegének 75 %-át. |
A legfeljebb 12 hónapos munkaprogram költségei támogathatóságának időszaka 2009. január 1. és 2009. április 1. között kell, hogy elkezdődjön, és nem tarthat tovább, mint a kedvezményezett pénzügyi évének vége.
5. Határidő és az ajánlatok benyújtása
A pályázatok beadásának határideje 2008. december 23. (a postabélyegző dátuma számít). A pályázatokat az alábbi címre kell elküldeni:
|
Education, Audiovisual and Culture Executive Agency |
|
Lifelong Learning: Erasmus, Jean Monnet |
|
Call for Proposal EACEA/29/08 |
|
Mr. Ralf RAHDERS |
|
Office: BOUR 2/61 |
|
Avenue du Bourget 1 |
|
B-1140 Brussels |
Csak a hivatalos pályázati formanyomtatványon benyújtott, a pályázó szervezet nevében jogilag kötelező erejű kötelezettségek vállalására felhatalmazott személy által megfelelően aláírt, és a kiírás teljes szövegében meghatározott összes információt és mellékletet tartalmazó pályázatokat fogadják el. A faxon vagy e-mailben elküldött pályázatokat elutasítják.
6. További információk
A pályázók számára készült útmutató és a kitöltendő formanyomtatvány az Ügynökség honlapján érhető el: http://eacea.ec.europa.eu
További tájékoztatás az alábbi címen kérhető:
|
Education, Audiovisual & Culture Executive Agency |
|
Ilona POKORNA |
|
E-mail: Ilona.Pokorna@ec.europa.eu |
|
Tel.: közvetlen szám: (32-2) 295 83 94 |
(1) Lásd az Európai Parlamentnek és a Tanácsnak az egész életen át tartó tanulás terén egy cselekvési program létrehozásáról szóló, 2006. november 15-i 1720/2006/EK határozatát.
http://eur-lex.europa.eu/LexUriServ/site/en/oj/2006/c_327/c_32420061230en00590067.pdf
(2) Lásd: http://ec.europa.eu/education/policies/2010/et_2010_en.html
(3) E meghatározás szerint az általános európai érdeket szolgáló célt képviselő szervek a következők:
|
— |
az oktatás, képzés, tájékoztatás, valamint az európai politikák tanulmányozásának és kutatásának területén működő európai szerv, vagy európai szabványügyi testület, vagy |
|
— |
a tagállamokban, illetve a tagjelölt országokban működő nonprofit szerveket képviselő és a Szerződések célkitűzéseivel összhangban lévő elveket és politikákat támogató európai hálózatok. |
(4) Az európai szövetség továbbá rendelkezhet olyan tagszervezetekkel, amelyek székhelye más, az élethosszig tartó tanulás programjában részt vevő országokban (az Európai Unión kívüli országokban) található.
A VERSENYPOLITIKA VÉGREHAJTÁSÁRA VONATKOZÓ ELJÁRÁSOK
Bizottság
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/97 |
Összefonódás előzetes bejelentése
(Ügyszám COMP/M.5368 – MidAmerican/Constellation)
Egyszerűsített eljárás alá vont ügy
(EGT-vonatkozású szöveg)
(2008/C 276/11)
|
1. |
2008. október 23-án a Bizottság a 139/2004/EK tanácsi rendelet (1) 4. cikke szerint bejelentés kapott a Berkshire Hathaway irányítása alá tartozó MidAmerican Energy Holdings Company (a továbbiakban: MidAmerican, Amerikai Egyesült Államok) által tervezett összefonódásról, amely szerint e vállalkozás részesedés vásárlása útján a tanácsi rendelet 3. cikke (1) bekezdésének b) pontja értelmében irányítást szerez a Constellation Energy group Inc. (a továbbiakban: Constellation, Amerikai Egyesült Államok) felett. |
|
2. |
Az érintett vállalkozások üzleti tevékenysége a következő:
|
|
3. |
A Bizottság előzetes vizsgálatára alapozva megállapítja, hogy a bejelentett összefonódás a 139/2004/EK rendelet hatálya alá tartozhat, a végleges döntés jogát azonban fenntartja. A Bizottság a 139/2004/EK tanácsi rendelet szerinti egyes összefonódások kezelésére vonatkozó egyszerűsített eljárásáról szóló közleménye (2) szerint az ügyet egyszerűsített eljárásra utalhatja. |
|
4. |
A Bizottság felhívja az érdekelt harmadik feleket, hogy az ügylet kapcsán esetlegesen felmerülő észrevételeiket nyújtsák be a Bizottságnak. Az észrevételeknek a közzétételt követő 10 napon belül kell a Bizottsághoz beérkezniük. Az észrevételeket a COMP/M.5368 – MidAmerican/Constellation hivatkozási szám feltüntetése mellett lehet eljuttatni a Bizottsághoz faxon (fax: (32-2) 296 43 01 vagy 296 72 44) vagy postai úton a következő címre:
|
(1) HL L 24., 2004.1.29., 1. o.
(2) HL C 56., 2005.3.5., 32. o.
|
31.10.2008 |
HU |
Az Európai Unió Hivatalos Lapja |
C 276/s3 |
MEGJEGYZÉS AZ OLVASÓHOZ
Az intézmények úgy határoztak, hogy a jövőben nem tüntetik fel szövegeikben az idézett jogszabály utolsó módosítását.
Ellenkező jelzés hiányában, az itt megjelent szövegekben a jogszabályokra történő hivatkozást a hatályos változatukra történő hivatkozásként kell értelmezni.