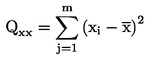EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32014R0709
Commission Regulation (EU) No 709/2014 of 20 June 2014 amending Regulation (EC) No 152/2009 as regards the determination of the levels of dioxins and polychlorinated biphenyls Text with EEA relevance
A Bizottság 709/2014/EU rendelete ( 2014. június 20. ) a 152/2009/EK rendeletnek a dioxinok és a poliklórozott bifenilek koncentrációjának meghatározása tekintetében történő módosításáról EGT-vonatkozású szöveg
A Bizottság 709/2014/EU rendelete ( 2014. június 20. ) a 152/2009/EK rendeletnek a dioxinok és a poliklórozott bifenilek koncentrációjának meghatározása tekintetében történő módosításáról EGT-vonatkozású szöveg
OJ L 188, 27.6.2014, p. 1–18
(BG, ES, CS, DA, DE, ET, EL, EN, FR, HR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
 In force
In force
|
27.6.2014 |
HU |
Az Európai Unió Hivatalos Lapja |
L 188/1 |
A BIZOTTSÁG 709/2014/EU RENDELETE
(2014. június 20.)
a 152/2009/EK rendeletnek a dioxinok és a poliklórozott bifenilek koncentrációjának meghatározása tekintetében történő módosításáról
(EGT-vonatkozású szöveg)
AZ EURÓPAI BIZOTTSÁG,
tekintettel az Európai Unió működéséről szóló szerződésre,
tekintettel a takarmány- és élelmiszerjog, valamint az állat-egészségügyi és az állatok kíméletére vonatkozó szabályok követelményeinek történő megfelelés ellenőrzésének biztosítása céljából végrehajtott hatósági ellenőrzésekről szóló, 2004. április 29-i 882/2004/EK európai parlamenti és tanácsi rendeletre (1) és különösen annak 11. cikke (4) bekezdésére,
mivel:
|
(1) |
A 152/2009/EK bizottsági rendelet (2) módszereket ír elő a takarmányokban előforduló poliklórozott dibenzo-p-dioxinok (PCDD-k), poliklórozott dibenzo-furánok (PCDF-ek) és dioxinjellegű poliklórozott bifenilek (PCB-k) koncentrációjának meghatározására. |
|
(2) |
Követelményeket kell meghatározni a PCDD-ket/PCDF-eket és dioxinjellegű PCB-ket jelentős mennyiségben tartalmazó minták beazonosítására szolgáló, nagy teljesítményű szűrőmódszerekre vonatkozóan (lehetőleg olyan mintákat kell választani, amelyekben a koncentráció meghaladja a beavatkozási küszöbértéket, és biztosítani kell a felső határértéket meghaladó koncentrációjú minták kiválasztását). A felső határértékek tekintetében a „hamis megfelelő” aránynak 5 % alatt kell lennie |
|
(3) |
Ahol a szűrőmódszerrel kapott eredmények meghaladják a cut-off értéket, ott az eredeti mintát egy olyan módszerrel kell elemezni, amely képes azonosítani és mennyiségileg meghatározni a mintában lévő PCDD-k/PCDF-eket és dioxinjellegű PCB-ket. A továbbiakban a „megerősítő módszer” kifejezés jelöli az ilyen módszereket. A műszaki fejlődésnek köszönhetően bebizonyosodott, hogy a gázkromatográfia/nagy felbontású tömegspektrometria (GC-HRMS) mellett a gázkromatográfia/tandem tömegspektometria (GC-MS/MS) is használható megerősítő módszerként a felső határértéknek való megfelelés ellenőrzése céljából. |
|
(4) |
A jelenleg érvényes szabályok alkalmazásával kapcsolatban nyert tapasztalatok alapján helyénvaló módosítani a hatályban lévő rendelkezéseket a két párhuzamos elemzés szükségessége, a megfelelés megítélése két párhuzamos elemzés esetében, valamint a megerősített felső és alsó határértékre vonatkozó eredmények közötti elfogadható különbség követelménye tekintetében. |
|
(5) |
A 152/2009/EK rendeletet ezért ennek megfelelően módosítani kell. |
|
(6) |
Az e rendeletben előírt intézkedések összhangban vannak az Élelmiszerlánc- és Állategészségügyi Állandó Bizottság véleményével, |
ELFOGADTA EZT A RENDELETET:
1. cikk
A 152/2009/EK rendelet V. mellékletének B. része e rendelet mellékletének megfelelően módosul.
2. cikk
Ez a rendelet az Európai Unió Hivatalos Lapjában való kihirdetését követő huszadik napon lép hatályba.
Ez a rendelet teljes egészében kötelező és közvetlenül alkalmazandó valamennyi tagállamban.
Kelt Brüsszelben, 2014. június 20-án.
a Bizottság részéről
az elnök
José Manuel BARROSO
(1) HL L 165., 2004.4.30., 1. o.
(2) A Bizottság 2009. január 27-i 152/2009/EK rendelete a takarmányok hatósági ellenőrzése során alkalmazott mintavételi és vizsgálati módszerek megállapításáról (HL L 54., 2009.2.26., 1. o.).
MELLÉKLET
A 152/2009/EK rendelet V. melléletében a „B. A DIOXIN- (PCDD/PCDF) ÉS PCB-TARTALOM MEGHATÁROZÁSA” című rész helyébe a következő szöveg lép:
„B DIOXINOK (PCDD-K/PCDF-EK) ÉS PCB-K KONCENTRÁCIÓJÁNAK MEGHATÁROZÁSA
I. FEJEZET
Mintavételi módszerek és az analitikai eredmények értelmezése
1. Cél és Alkalmazási kör
A takarmányokban előforduló poliklórozott dibenzo-p-dioxinok (PCDD-k), poliklórozott dibenzo-furánok (PCDF-ek), dioxinjellegű poliklórozott bifenilek (PCB-k) (1) és nem dioxinjellegű PCB-k koncentrációjának hatósági ellenőrzésére az I. mellékletnek megfelelően kell mintát venni. Alkalmazni kell az I. melléklet 5.1. pontjában a takarmányban egyenletesen eloszló anyagok vagy termékek ellenőrzésére vonatkozóan előírt mennyiségi követelményeket. Az így nyert egyesített minták reprezentatívnak tekintendők azon tételekre és altételekre, amelyekből a mintavétel történt. A 2002/32/EK irányelvben előírt felső határértékeknek való megfelelést a laboratóriumi minták elemzésével kapott koncentrációk alapján kell megállapítani.
E B. rész alkalmazásakor a 2002/657/EK bizottsági határozat (2) I. mellékletében meghatározott fogalommeghatározások alkalmazandók.
Az említett fogalommeghatározásokon kívül e B. rész alkalmazásában a következő fogalommeghatározásokat kell alkalmazni:
|
|
»Szűrőmódszerek«: azoknak a mintáknak a kiválasztására használt módszerek, melyekben a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k koncentrációja meghaladja a felső határértéket vagy a beavatkozási küszöbértéket. Segítségükkel költséghatékonyan lehet nagy mennyiségű mintát feldolgozni, és így nagyobb az esély az olyan új szennyeződési esetek felismerésére, amelyek nagy fogyasztói expozíciót és egészségi kockázatot jelenthetnek. A szűrőmódszerek bioanalitikai módszereken vagy gázkromatográfiás/tömegspektrometriás (GC/MS) módszereken alapszanak. A felső határértékeknek való megfelelés ellenőrzésekor a cut-off értéket meghaladó mintákból kapott eredményeket az eredeti minta megerősítő módszerrel történő teljes újbóli vizsgálata által kell ellenőrizni. |
|
|
»Megerősítő módszerek«: olyan teljes vagy kiegészítő információkkal szolgálnak, amelyek lehetővé teszik a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k maximális koncentrációban vagy szükség esetén a beavatkozási küszöbértéken történő azonosítását és egyértelmű mennyiségi meghatározását. E módszerek gázkromatográfiát/nagyfelbontású tömegspektrometriát (GC-HRMS) vagy gázkromatográfiát/tandem tömegspektrometriát (GC-MS/MS) alkalmaznak. |
2. A tétel vagy altétel megfelelése a felső határértéknek
2.1. A nem dioxinjellegű PCB-k tekintetében
A tétel akkor felel meg a felső határértéknek, ha az analitikai eredmény – a mérési bizonytalanságot is figyelembe véve – nem haladja meg a 2002/32/EK irányelvben a nem dioxinjellegű PCB-kre megállapított felső határértéket.
A tétel nem felel meg a felső határértéknek, ha a felfelé kerekített (3) analitikai eredmény két párhuzamos elemzéssel (4) megerősítve és a mérési bizonytalanságot is figyelembe véve meghaladja a 2002/32/EK irányelvben megállapított felső határértéket. A mérési bizonytalanságot is figyelembe véve, a két meghatározás számtani középértéke szolgál a megfelelőség ellenőrzésére.
A mérési bizonytalanságot a következő módszerek egyikével kell figyelembe venni:
|
— |
a kiterjesztett bizonytalanság kiszámítása 2-es kiterjesztési tényező alkalmazásával, ami megközelítőleg 95 %-os megbízhatósági szintet ad. A tétel vagy altétel nem megfelelő, ha az U-val csökkentett mért érték meghaladja a felső határértéket, |
|
— |
a 2002/657/EK határozat I. mellékletének 3.1.2.5. pontja szerinti döntési határérték (CCα) meghatározása. A tétel vagy altétel nem megfelelő, ha a mért érték egyenlő a CCα-val, vagy meghaladja azt. |
Az (1), (2) és (3) bekezdést a hatósági ellenőrzés céljából vett mintákkal kapott analitikai eredményekre kell alkalmazni. Az érdekvédelmi vagy szakértői célból végzett elemzések esetében a nemzeti szabályok alkalmazandók.
2.2. A PCDD-k/PCDF-ek és a dioxinjellegű PCB-k tekintetében
A tétel megfelel a felső határértékeknek, ha
|
— |
5 % alatti »hamis megfelelő« arányt biztosító szűrőmódszerrel végzett egyetlen elemzés eredménye azt mutatja, hogy a koncentráció nem haladja meg a 2002/32/EK irányelvben a PCDD-kre/PCDF-ekre, illetve a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegére megállapított felső határértéket; |
|
— |
a megerősítő módszerrel végzett egyetlen elemzés eredménye – a mérési bizonytalanságot is figyelembe véve – nem haladja meg a 2002/32/EK irányelvben a PCDD-kre/PCDF-ekre, illetve a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegére megállapított felső határértéket. |
A szűrőtesztekhez cut-off értéket kell megállapítani, amely alapján eldönthető, hogy a minta elérheti-e a PCDD-kre/PCDF-ekre, illetve a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegére megállapított vonatkozó felső határértékeket, vagy sem.
A tétel nem felel meg a felső határértéknek, ha megerősítő módszerrel kapott felfelé kerekített (5) analitikai eredmény, két párhuzamos elemzéssel megerősítve és a mérési bizonytalanságot is figyelembe véve meghaladja a 2002/32/EK irányelvben megállapított felső határértéket (6). A mérési bizonytalanságot is figyelembe véve, a két meghatározás számtani középértéke szolgál a megfelelőség ellenőrzésére.
A mérési bizonytalanságot a következő módszerek egyikével kell figyelembe venni:
|
— |
a kiterjesztett bizonytalanság kiszámítása 2-es kiterjesztési tényező alkalmazásával, ami megközelítőleg 95 %-os megbízhatósági szintet ad. A tétel vagy altétel nem megfelelő, ha az U-val csökkentett mért érték meghaladja a felső határértéket. A PCDD-k/PCDF-ek és a dioxinjellegű PCB-k külön történő meghatározása esetén a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k külön-külön kapott analitikai eredményeinél kapott kiterjesztett bizonytalanságok összegét kell használni a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegének kiszámításához; |
|
— |
a 2002/657/EK határozat I. mellékletének 3.1.2.5. pontja szerinti döntési határérték (CCα) meghatározása. A tétel vagy altétel nem megfelelő, ha a mért érték egyenlő a CCα-val, vagy meghaladja azt. |
Az (1)–(4) bekezdést a hatósági ellenőrzés céljából vett mintákkal kapott analitikai eredményekre kell alkalmazni. Az érdekvédelmi vagy szakértői célból végzett elemzések esetében a nemzeti szabályok alkalmazandók.
3. A 2002/32/EK irányelv ii. mellékletében megállapított beavatkozási küszöbértékeket meghaladó eredmények
A beavatkozási küszöbértékek eszközként használhatók a minták kiválasztásához azokban az esetekben, amikor azonosítani kell a szennyeződés forrását, és intézkedni kell a csökkentéséről vagy megszüntetéséről. A szűrőmódszereknél megfelelő cut-off értékeket kell meghatározni az ilyen minták kiválasztásához. Ha jelentős erőfeszítések szükségesek a szennyeződés forrásának beazonosításához és a szennyeződés csökkentéséhez vagy megszüntetéséhez, célszerű eljárás lehet két párhuzamos, megerősítő módszert alkalmazó elemzés végzése – a mérési bizonytalanságot is figyelembe véve – a beavatkozási küszöbérték túllépésének megerősítésére (7).
II. FEJEZET
A takarmányokban előforduló dioxinok (PCDD-k/PCDF-ek) és PCB-k koncentrációjának hatósági ellenőrzéséhez használt minta-előkészítés és az elemzési módszerekre vonatkozó követelmények
1. Alkalmazási kör
Az e fejezetben előírt követelményeket kell alkalmazni a takarmányoknak a 2,3,7,8-as szénatomokon helyettesített poliklórozott dibenzo-p-dioxinok és poliklórozott dibenzo-furánok (PCDD-k/PCDF-ek), és a dioxinjellegű poliklórozott bifenilek (dioxinjellegű PCB-k) koncentrációja tekintetében történő hatósági ellenőrzéséhez, valamint egyéb szabályozási célokra.
A takarmányokban előforduló PCDD-k/PCDF-ek és dioxinjellegű PCB-k koncentrációjának figyelemmel kísérése két különböző analitikai módszerrel történhet:
|
a) |
Szűrési módszerek A szűrési módszerek célja azoknak a mintáknak a kiválasztása, melyekben a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k koncentrációja meghaladja a felső határértéket vagy a beavatkozási küszöbértéket. A szűrési módszerek segítségével költséghatékonyan lehet nagy mennyiségű mintát feldolgozni, és így nagyobb az esély az olyan új szennyeződési esetek felismerésére, amelyek nagy fogyasztói expozíciót és egészségi kockázatot jelenthetnek. Alkalmazásuknak arra kell irányulnia, hogy ne forduljanak elő »hamis megfelelő« eredmények. A szűrőmódszerek közé tartozhatnak bioanalitikai módszerek és gázkromatográfiás/tömegspektrometriás (GC-MS) módszerek. A szűrőmódszerek az analitikai eredményt összehasonlítják egy cut-off értékkel, és igen/nem választ adnak a felső határérték vagy a beavatkozási küszöbérték lehetséges túllépéséről. Az olyan mintákban, amelyek esetében feltételezhető a felső határértéket meghaladó eredmény, a PCDD-k/PCDF-ek koncentrációját, valamint a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összkoncentrációját megerősítő módszerrel kell meghatározni/megerősíteni. Emellett a szűrőmódszerek jelezhetik a mintában lévő PCDD-k/PCDF-ek és dioxinjellegű PCB-k koncentrációját. Bioanalitikai szűrőmódszerek alkalmazása esetén az eredmény bioanalitikai egyenértékként (BEQ) fejezhető ki, míg fizikai-kémiai CG-MS módszerek alkalmazása esetén toxicitási egyenértékként (TEQ). A szűrőmódszerek számadattal megadott eredményei megfelelően mutatják a megfelelést, a feltételezett meg nem felelést vagy a beavatkozási küszöbérték túllépését, és amennyiben megerősítő módszerekkel történő nyomon követés szükséges, jelzik a koncentrációtartományt. Nem alkalmasak olyan célokra, mint például a háttér-koncentrációk értékelése, a bevitel becslése, a koncentráció időbeli tendenciáinak nyomon követése vagy a beavatkozási küszöbérték, illetve a felső határértékek felülvizsgálata. |
|
b) |
Megerősítő módszerek A megerősítő módszerek lehetővé teszik a mintában jelen lévő PCDD-k/PCDF-ek és dioxinjellegű PCB-k egyértelmű azonosítását és mennyiségi meghatározását, és teljes körű információt adnak kongénerszinten. Ezért e módszerek lehetővé teszik a felső határértékek és a beavatkozási küszöbértékek ellenőrzését, ideértve a szűrőmódszerekkel kapott eredmények megerősítését. Ezen túlmenően az eredmények egyéb célokra – például a takarmányellenőrzésben az alacsony háttér-koncentrációk meghatározására, az időbeli tendenciák követésére, az expozíció felmérésére, valamint a beavatkozási küszöbérték és a felső határértékek esetleges felülvizsgálatát szolgáló adatbázis létrehozására – is alkalmazhatók. Fontosak továbbá a kongénerkombinációk megállapításához, hogy azonosítani lehessen egy szennyeződés lehetséges forrását. Az ilyen módszerek GC-HRMS-t alkalmaznak. A felső határértéknek való megfelelés/meg nem felelés megerősítésére GC-MS/MS is alkalmazható. |
2. Háttér
A toxicitási egyenértékben (TEQ) kifejezett koncentráció kiszámításához az egyes anyagok adott mintában mért koncentrációját meg kell szorozni a hozzájuk tartozó toxicitási egyenérték-tényezővel (TEF) (lásd az I. fejezet (1)* lábjegyzetét), majd össze kell adni őket, és ez adja a dioxinjellegű vegyületek toxicitási egyenértékben (TEQ) kifejezett összkoncentrációját.
Az e B. rész alkalmazásában egy adott kongéner specifikus meghatározási határa a mintában az a legkisebb analittartalom, amely elfogadható statisztikai bizonyossággal mérhető, teljesítve a nemzetközileg elfogadott szabványokban, így például az EN 16215:2012 szabványban (Animal feed – Determination of dioxins and dioxin-like PCBs by GC/HRMS and of indicator PCBs by GC-HRMS; Állati takarmányok. Dioxinok és dioxinjellegű PCB-k meghatározása GC-HRMS módszerrel és indikátor PCB-k meghatározása GC/HRMS módszerrel) és/vagy a felülvizsgált EPA 1613 és 1668 módszerben leírt azonosítási kritériumokat.
Egy adott kongéner meghatározási határa a következőképpen azonosítható:
|
a) |
a mintakivonatban mért azon analitkoncentráció, amelynél két különböző vizsgált ion olyan analitikai jelet ad, amelynél a jel/zaj (S/N) arány a kisebb intenzitású jelre 3:1; vagy |
|
b) |
amennyiben technikai okokból a jel-zaj viszony számítása nem ad megbízható eredményt, egy kalibrációs görbe legkisebb koncentrációs pontja, amely elfogadható (≤ 30 %) és következetes (a minták analitikai sorozatának legalább a kezdetén és a végén mért) eltérést mutat az egyes mintasorozatokban a kalibrációs görbe valamennyi pontjára kiszámított átlagos relatív válaszfaktoroktól. A meghatározási határt a legkisebb koncentrációs pontból kell kiszámítani, figyelembe véve a belső standardok visszanyerését és a beviteli mintamennyiséget. |
A bioanalitikai szűrőmódszerek az eredményeket nem a kongénerek szintjén adják meg, hanem csupán bioanalitikai egyenértékként (BEQ) jelzik (8) a TEQ-értéket, ami azt jelenti, hogy a méréskor analitikai jelet adó, a mintakivonatban jelen lévő vegyületek közül esetleg nem felel meg mindegyik a TEQ-elv összes követelményének.
Egy adott mátrix ellenőrzésére csak akkor alkalmazhatók szűrési és megerősítő módszerek, ha azok kellően érzékenyek ahhoz, hogy megbízhatóan ki tudják mutatni a beavatkozási küszöbértéket vagy a felső határértéket.
3. Minőségbiztosítási előírások
3.1. Intézkedéseket kell hozni, hogy a mintavétel és az analitikai eljárás szakaszaiban ne fordulhasson elő a minták keresztszennyeződése.
3.2. A mintákat olyan üveg, alumínium, polipropilén vagy polietilén edényekben kell tárolni és szállítani, amelyek alkalmasak a minták olyan tárolására, hogy az azokban lévő PCDD-k/PCDF-ek és dioxinjellegű PCB-k koncentrációját semmilyen hatás ne érhesse. A papírpormaradékokat el kell távolítani a mintatartóból.
3.3. A minták tárolása és szállítása során gondoskodni kell a takarmányminta épségének megőrzéséről.
3.4. Adott esetben az egyes laboratóriumi mintákat finomra kell őrölni és alaposan össze kell keverni bizonyítottan teljes homogenizációt eredményező eljárással (például őrlés olyan finomságúra, hogy 1 mm-es szitán áthulljon). A túl nagy nedvességtartalmú mintákat őrlés előtt szárítani kell.
3.5. A reagenseket és a laboratóriumi eszközöket ellenőrizni kell, hogy nem befolyásolhatják-e a TEQ-értékre vagy BEQ-értékre alapozott eredményeket.
3.6. Vakpróbát kell végezni, azaz végre kell hajtani a teljes analitikai eljárást, a mintát kihagyva belőle.
3.7. Bioanalitikai módszereknél az elemzéshez használt összes laboratóriumi üvegeszközt és oldószert ellenőrizni kell, hogy mentesek legyenek olyan vegyületektől, melyek a munkatartományban zavarhatnák a keresett vegyületek kimutatását. Az üvegeszközöket ki kell öblíteni oldószerrel, vagy fel kell melegíteni olyan hőmérsékletre, amelyen a felületükről eltávoznak a nyomokban esetleg ott lévő PCDD-k/PCDF-ek, dioxinjellegű vegyületek és zavaró vegyületek.
3.8. Az extrakcióhoz használt minta mennyiségének elegendőnek kell lennie ahhoz, hogy teljesüljenek a felső határérték vagy a beavatkozási küszöbérték koncentrációit magában foglaló, kellően alacsony munkatartományra vonatkozó követelmények.
3.9. A vizsgált termékekre alkalmazott adott minta-előkészítési eljárásoknak nemzetközileg elfogadott iránymutatásokat kell követniük.
4. A laboratóriumokra vonatkozó követelmények
4.1. A 882/2004/EK rendeletnek megfelelően az analitikai minőségbiztosítás alkalmazásának biztosítása érdekében a laboratóriumokat az ISO 58 útmutató szerint működő elismert testületnek kell akkreditálnia. A laboratóriumokat az EN ISO/IEC 17025 szabvány szerint kell akkreditálni.
4.2. A laboratóriumok szakmai felkészültségét olyan laboratóriumközi körvizsgálatokban való folyamatos, sikeres részvétellel kell bizonyítani, amelyek a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k meghatározására irányulnak a megfelelő takarmánymátrixokban és koncentrációtartományokban.
4.3. A minták rutinszerű ellenőrzésére szűrőmódszereket alkalmazó laboratóriumoknak szoros együttműködést kell kialakítaniuk a megerősítő módszert alkalmazó laboratóriumokkal mind a minőség-ellenőrzés, mind a feltehetően nem megfelelő minták analitikai eredményének megerősítése terén.
5. A dioxinokhoz (PCDD-K/PCDF-ek) és dioxinjellegű PCB-khez használt analitikai eljárásokra vonatkozó alapkövetelmények
5.1. Alacsony munkatartomány és a mennyiségi meghatározás határértéke
A PCDD-k/PCDF-ek esetében a kimutatható mennyiségnek a femtogrammos (10-15 g) tartomány felső részébe kell esnie, mivel az említett vegyületek közül több rendkívül mérgező. A legtöbb PCB-kongéner esetében már az is elegendő, ha a meghatározási határ értéke a nanogrammos (10-9 g) tartományban van. A mérgezőbb dioxinjellegű PCB-kongénerek (és különösen a nem orto-helyzetben helyettesített kongénerek) méréséhez a munkatartomány aljának el kell érnie a pikogrammos (10-12 g) tartomány alját. Az összes többi PCB-kongéner esetében elegendő, ha a meghatározási határ értéke a nanogrammos (10-9 g) tartományba esik.
5.2. Nagy szelektivitás (specifikusság)
5.2.1. Meg kell tudni különböztetni a PCDD-ket/PCDF-eket és a dioxinjellegű PCB-ket azoktól a sokféle, együtt extrahálódó és a mérést esetleg zavaró más vegyülettől, amelyek több nagyságrenddel nagyobb koncentrációban lehetnek jelen, mint a keresett analitok. A GC-MS módszerekkel meg kell tudni különböztetni egymástól a különböző kongénereket, így például a mérgező vegyületeket (például a 2,3,7,8-as szénatomokon helyettesített tizenhét PCDD-ket/PCDF-eket és a tizenkét dioxinjellegű PCB-ket) a többi kongénertől.
5.2.2. A bioanalitikai módszerekkel ki kell tudni mutatni a keresett vegyületeket a PCDD-k/PCDF-ek és/vagy a dioxinjellegű PCB-k összegeként. A mintatisztítás célja az olyan vegyületek eltávolítása, amelyek »hamis nem megfelelő« eredményeket okoznak, vagy az olyanokét, amelyek a reakció gyengítésével »hamis megfelelő« eredményt okoznak.
5.3. Nagy adatpontosság (valódiság és módszerpontosság, biológiai próba során észlelt visszanyerés)
5.3.1. A GC-MS módszerekkel a meghatározásnak hiteles becslést kell adnia a minta valódi koncentrációjáról. Nagy adatpontosság szükséges ahhoz, hogy a mintaelemzés eredményét ne kelljen elutasítani a kapott TEQ-érték gyenge megbízhatósága miatt. Az adatpontosság a valódiság (egy hitelesített anyagban az adott analitra mért átlagérték és a hitelesített érték közötti különbség, ez utóbbi százalékában kifejezve) és a módszerpontosság (a reprodukálhatósági körülmények között kapott eredményekből kiszámított relatív szórás [RSDR]) összege.
5.3.2. A bioanalitikai módszereknél a biológiai próba során észlelt visszanyerést kell meghatározni. A biológiai próba során észlelt visszanyerés a TCDD vagy a PCB-126 kalibrációs görbéjéből számított, a vakminta eredményeivel korrigált BEQ-érték osztva a megerősítő módszerrel meghatározott TEQ-értékkel. Célja az olyan hatások korrigálása, mint például a PCDD-k/PCDF-ek és a dioxinjellegű vegyületek vesztesége az extrakció és a mintatisztítás során, az extrakcióval átmenő más vegyületek reakciót erősítő vagy gyengítő (agonisztikus és antagonisztikus) hatása, a görbeilleszkedés minősége vagy a toxikológiai egyenérték-tényező (TEF) és a relatív hatóképesség (REP) értékei közötti különbségek. A biológiai próba során észlelt visszanyerés kiszámítása reprezentatív kongénerkombinációkat a keresett koncentráció körüli koncentrációkban tartalmazó, alkalmas referenciamintákból történik.
5.4. Hitelesítés a felső határérték tartományában és általános minőség-ellenőrző intézkedések
5.4.1. A laboratóriumoknak a hitelesítés és a rutinszerű elemzés során igazolniuk kell a módszerek teljesítőképességét a felső határérték esetében – például a felső határérték felénél, egyszeresénél és kétszeresénél – azzal, hogy az ismételt elemzések variációs együtthatója elfogadható.
5.4.2. Belső minőség-ellenőrzési intézkedésként rendszeresen vakpróbákat, adalékolási kísérleteket vagy kontrollminta-elemzést (lehetőleg hitelesített referenciaanyaggal) kell végezni. A vakpróbákról, az adalékolási kísérletekről vagy a kontrollminta-elemzésekről minőség-ellenőrzési nyilvántartást kell vezetni, és ellenőrizni kell, hogy az analitikai teljesítőképesség valóban megfelel-e a követelményeknek.
5.5. Meghatározási határ
5.5.1. A bioanalitikai szűrőmódszereknél nem feltétlenül szükséges, hogy meg legyen határozva a meghatározási határ (LOQ), de a módszerről bizonyítani kell, hogy meg tudja különböztetni a vakmintával kapott eredményeket a cut-off értéktől. BEQ-érték megadásakor az e koncentráció alatti reakciót mutató minták kezelése céljából meg kell határozni egy jelentési határértéket. A jelentési határértéknek igazoltan az elemzési vakmintákkal kapott eredmény legalább 3-szorosának kell lennie úgy, hogy az érték a munkatartomány alá esik. Ezért ezt a keresett vegyületet az előírt minimumkoncentráció körüli koncentrációban tartalmazó mintákból, nem pedig a jel/zaj arányból vagy mérési vakmintából kell kiszámítani.
5.5.2. Megerősítő módszer esetében a mennyiségi meghatározás határértékének a felső határérték körülbelül egyötödénél kell lennie.
5.6. Analitikai kritériumok
Ahhoz, hogy a megerősítő vagy a szűrőmódszerek megbízható eredményeket adjanak, a következő kritériumoknak kell teljesülniük a felső határérték vagy a beavatkozási küszöbérték tartományában a TEQ-értékre, illetve a BEQ-értékre, függetlenül attól, hogy a meghatározás TEQ-összértékként (a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegéként) vagy külön a PCDD-kre/PCDF-ekre és külön a dioxinjellegű PCB-kre történik:
|
|
Szűrés bioanalitikai vagy fizikai-kémiai módszerekkel |
Megerősítő módszerek |
|
»Hamis megfelelő« arány (9) |
< 5 % |
|
|
Valódiság |
|
– 20 % és + 20 % között |
|
Ismételhetőség (RSDr) |
< 20 % |
|
|
Laboratóriumon belüli reprodukálhatóság (RSDR) |
< 25 % |
< 15 % |
5.7. A szűrőmódszerekre vonatkozó egyedi követelmények
5.7.1. A szűréshez mind GC-MS módszerek, mind bioanalitikai módszerek használhatók. A GC-MS módszerekre a 6. pontban előírt követelményeket kell alkalmazni. A sejtalapú bioanalitikai módszerekre vonatkozó egyedi követelményeket a 7. pont írja le.
5.7.2. A minták rutinszerű ellenőrzéséhez szűrőmódszereket alkalmazó laboratóriumoknak szoros együttműködést kell kialakítaniuk a megerősítő módszert alkalmazó laboratóriumokkal.
5.7.3. A szűrőmódszerek teljesítőképességét a rutinszerű elemzések során analitikai minőség-ellenőrzéssel és a módszer folyamatos hitelesítésével ellenőrizni kell. A »megfelelő« eredmények ellenőrzésére folyamatos programot kell alkalmazni.
5.7.4. A sejtreakció és a citotoxicitás esetleges elnyomásának ellenőrzése:
A mintakivonatok 20 %-át kell mérni rutinszerű szűréssel, a felső határértéknek vagy a beavatkozási küszöbértéknek megfelelően hozzáadott 2,3,7,8-TCDD-vel és anélkül, ellenőrizendő, hogy előfordulhat-e reakcióelnyomás a mintakivonatban jelen lévő zavaró anyagok miatt. Az adalékolt minta mért koncentrációját össze kell hasonlítani az adalékolás nélküli kivonat koncentrációjának és az adalékolási koncentráció összegével. Ha a mért koncentráció több mint 25 %-kal kisebb a számított (össz)koncentrációnál, akkor ez azt mutatja, hogy fennáll a reakcióelnyomás lehetősége, és az adott mintát meg kell vizsgálni GC-HRMS megerősítő elemzéssel. Az eredményeket figyelemmel kell kísérni a minőség-ellenőrző nyilvántartásban.
5.7.5. »Megfelelő« minták minőség-ellenőrzése:
A mintamátrixtól és a laboratóriumi gyakorlattól függően a »megfelelő« minták megközelítőleg 2–10 %-ával el kell végezni a megerősítést GC-HRMS módszerrel.
5.7.6. A »hamis megfelelő« arányok meghatározása a minőség-ellenőrzési adatokból:
A felső határérték vagy a beavatkozási küszöbérték alatti és feletti minták szűrése alapján meg kell határozni a »hamis megfelelő« eredmények arányát. A tényleges »hamis megfelelő« aránynak 5 % alatt kell lennie. Ha mátrixonként vagy mátrixcsoportonként van legalább 20 megerősített eredmény a »megfelelő« minták minőség-ellenőrzéséből, akkor a »hamis megfelelő« arányt ebből az adatbázisból kell megállapítani. A körvizsgálatokban vagy a szennyeződési esetek során elemzett minták eredményei, amelyek például akár a felső határérték (ML) kétszereséig terjedő koncentrációtartományokba is eshetnek, szintén felvehetők a »hamis megfelelő« arány kiszámításához minimumként használandó 20 eredmény közé. A mintáknak le kell fedniük a különféle forrásokat reprezentáló, leggyakoribb kongénerkombinációkat.
Noha a szűrőteszteknek lehetőleg azt kell célozniuk, hogy kimutassák a beavatkozási küszöbértéket meghaladó mintákat, a »hamis megfelelő« arányok meghatározásának kritériuma a felső határérték, figyelembe véve a megerősítő módszer mérési bizonytalanságát.
5.7.7. A szűrés alapján »feltehetően nem megfelelő« mintákat az eredeti mintának a teljes körű újraelemzése útján megerősítő módszerrel kell mindig ellenőrizni. Ezek a minták a »hamis nem megfelelő« eredmények arányának kiszámításához is használhatók. A szűrőmódszereknél a »hamis nem megfelelő« eredmények aránya a korábbi szűréskor »feltehetően nem megfelelő«-nek minősített minták megerősítő elemzéssel »megfelelő«-ként megerősített eredmények hányada. A szűrőmódszer előnyösségének értékelése a »hamis nem megfelelő« mintáknak az összes ellenőrzött mintával való összehasonlításán alapul. Ennek az aránynak elég kicsinek kell lennie ahhoz, hogy a szűrővizsgálati módszer alkalmazása előnyös legyen.
5.7.8. A bioanalitikai módszereknek, legalábbis a hitelesítési körülmények között, hitelesen kell jelezniük – a BEQ-érték kiszámításával és megadásával – a TEQ-értéket.
A megismételhetőségi körülmények között alkalmazott bioanalitikai módszerekre is igaz, hogy a laboratóriumon belüli RSDr jellemzően kisebb, mint az RSDR- reprodukálhatóság.
6. A szűrés és megerősítés céljából alkalmazott GC-MS módszerekre vonatkozó egyedi követelmények
6.1. A felfelé kerekített és a lefelé kerekített WHO-TEQ-koncentrációk közötti elfogadható különbség
A megerősített felső és alsó határ közötti különbség nem haladhatja meg a 20 %-ot a felső határérték vagy szükség esetén a beavatkozási küszöbérték túllépésének megerősítése céljából.
6.2. A visszanyerések ellenőrzése
6.2.1. Az elemzési eljárás hitelesítéséhez a 2,3,7,8-as szénatomokon helyettesített PCDD-kből/PCDF-ekből készített, 13C-jelölésű belső standardokat és a dioxinjellegű PCB-kből készített, 13C-jelölésű belső standardokat az analitikai eljárás legelején, például az extrakció előtt hozzá kell adni a mintákhoz. A tetraklórozottól az oktaklórozottig terjedő PCDD/PCDF homológ csoportok mindegyikéből legalább egy kongénert, továbbá a dioxinjellegű PCB homológ csoportok mindegyikéből legalább egy kongénert kell hozzáadni a mintához (más megoldásként legalább egy-egy kongénert a PCDD-k/PCDF-ek és dioxinjellegű PCB-k ellenőrzéséhez használt tömegspektrometriás szelektív ionkövetéses funkciókhoz). A megerősítő módszerek esetében a 2,3,7,8-as szénatomokon helyettesített mind a tizenhét PCDD-ből/PCDF-ből készített, 13C-jelölésű belső standardot és mind a tizenkét dioxinjellegű PCB-ből készített, 13C-jelölésű belső standardot használni kell.
6.2.2. Ezenkívül megfelelő kalibráló oldatok alkalmazásával relatív válaszfaktorokat kell meghatározni azon kongénerekre, amelyek 13C-jelölésű analógja nem lett hozzáadva a mintához.
6.2.3. A növényi eredetű takarmányok és a 10 %-nál kevesebb zsírt tartalmazó állati eredetű takarmányok esetében a belső standardokat kötelezően az extrahálás előtt kell a mintához adni. A 10 %-nál nagyobb zsírtartalmú állati eredetű takarmányok esetében a belső standardokat vagy a zsírextrakció előtt, vagy azt követően kell a mintához adni. Az extrakció hatékonyságát megfelelően hitelesíteni kell, figyelembe véve, hogy a belső standardok hozzáadása melyik szakaszban történt, illetve hogy az eredményeket termékre vagy zsírra kell-e megadni.
6.2.4. GC-MS elemzés előtt a visszanyerés mérésére egy vagy két (kísérő) standardot is hozzá kell adni a mintához.
6.2.5. A visszanyerést ellenőrizni kell. A megerősítő módszerek esetében az egyes belső standardoknál a visszanyerésnek a 60–120 %-os tartományban kell lennie. Egyes kongénereknél, különösen néhány 7, illetve 8 klóratomot tartalmazó dibenzo-p-dioxin és dibenzo-furán esetében ennél kisebb vagy nagyobb visszanyerés is elfogadható, feltéve, hogy TEQ-értékük részaránya a PCDD-k/PCDF-ek és dioxinjellegű PCB-k összegén alapuló TEQ-összértéken belül legfeljebb 10 %. GC-MS szűrőmódszerek esetében a visszanyerésnek 30–140 %-os tartományban kell lennie.
6.3. A zavaró anyagok eltávolítása
|
— |
A PCDD-ket/PCDF-eket megfelelő kromatográfiás eljárással (lehetőleg florisil-, alumínium-oxid- és/vagy szénoszlopon) el kell választani a zavaró klórozott vegyületektől, így például a nem dioxinjellegű PCB-ktől és a klórozott difenil-éterektől. |
|
— |
Izomerek gázkromatográfiás elválasztásánál az 1,2,3,4,7,8-HxCDF és az 1,2,3,6,7,8-HxCDF esetében az alapzajnak 25 %-nál kisebbnek kell lennie. |
6.4. Kalibrálás standard görbével
A kalibrációs görbe tartományának le kell fednie a felső határérték vagy a beavatkozási küszöbérték megfelelő tartományát.
6.5. A szűrőmódszerekre vonatkozó egyedi követelmények
|
— |
A GC-HRMS esetében:
|
|
— |
A GC-MS/MS esetében:
|
7. A bioanalitikai módszerekre vonatkozó egyedi követelmények
A bioanalitikai módszerek biológiai alapelveken alapuló módszerek, mint például sejtalapú tesztek, receptortesztek vagy immuntesztek. E 7. pont általánosságban leírja a bioanalitikai módszerekre vonatkozó követelményeket.
Egy szűrőmódszer alapvetően »megfelelő«-nek vagy »feltehetően nem megfelelő«-nek minősít egy mintát. Ehhez a számított BEQ-értéket össze kell hasonlítani a cut-off értékkel (lásd a 7.3. pontot). A cut-off küszöbérték alatti minták »megfelelő«-nek minősülnek, az azzal egyenlő vagy a feletti értékű minták pedig »feltehetően nem megfelelő«-nek, és ezeket megerősítő módszerrel elemezni kell. A gyakorlatban a felső határérték 2/3-ának megfelelő BEQ-érték alkalmazható a legalkalmasabb cut-off értékként, ami biztosítja, hogy a »hamis megfelelő« arány 5 % alatt legyen, és a »hamis nem megfelelő« eredmények aránya is elfogadható legyen. Mivel külön felső határértékek vonatkoznak a PCDD-kre/PCDF-ekre, illetve a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegére, a minták frakcionálás nélküli megfelelőség-ellenőrzéséhez a biológiai próbáknál megfelelő cut-off értékek szükségesek a PCDD-kre/PCDF-ek vonatkozásában. A beavatkozási küszöbértékeket meghaladó minták ellenőrzéséhez az adott beavatkozási küszöbértékek megfelelő százalékaránya lehet az alkalmas cut-off érték.
Egyes bioanalitikai módszereknél továbbá tájékoztató BEQ-érték adható meg a munkatartományba eső és a jelentési határértéket meghaladó mintákra (lásd a 7.1.1. és a 7.1.6. pontot).
7.1. A mérési reakciók kiértékelése
7.1.1. Általános követelmények
|
— |
Ha a koncentrációk kiszámítása TCDD-s kalibrációs görbével történik, akkor a görbe alsó és felső végénél lévő értékek nagy szórást (nagy variációs együtthatót [CV]) mutatnak. A munkatartomány az a terület, ahol ez a CV 15 %-nál kisebb. A munkatartomány alját (jelentési határérték) úgy kell meghatározni, hogy az legalább háromszorosa legyen a elemzési vakmintákkal kapott eredményeknek. A munkatartomány tetejét általában az EC70 érték jelenti (a legnagyobb hatásos koncentráció 70 %-a), de ennél kisebbnek kell lennie, ha ebben a tartományban a CV nagyobb, mint 15 %. A munkatartományt a hitelesítés során kell meghatározni. A cut-off értékeknek (lásd a 7.3. pontot) a munkatartomány belsejében kell lenniük. |
|
— |
A standard oldatokat és a mintakivonatokat legalább két párhuzamos elemzéssel kell mérni. Két párhuzamos elemzéskor a lemezen elosztva 4–6 cellában mért standard oldatnak vagy kontrollkivonatnak olyan reakciókat vagy koncentrációkat kell adnia (ez csak a munkatartományban lehetséges), amelyek variációs együtthatója (CV) < 15 %. |
7.1.2. Kalibrálás
7.1.2.1. Kalibrálás standard görbével
|
— |
A mintában lévő mennyiségeket a mérési reakció és a TCDD-vel (vagy a PCB-126-tal vagy pedig PCDD-ből/PCDF-ből/dioxinjellegű PCB-ből álló standard keverékkel) készített kalibrációs görbe összehasonlításával kell megbecsülni, és ez alapján lehet kiszámítani a kivonatra és ezt követően a mintára jellemző BEQ-értéket. |
|
— |
A kalibrációs görbéknek 8–12 (legalább két párhuzamos elemzéssel kapott) koncentrációt kell tartalmazniuk úgy, hogy elegendő koncentráció legyen a görbe alsó részén (a munkatartományban). Külön figyelmet kell fordítani a munkatartományban a görbeilleszkedés minőségére. Ennél az R2 érték kevéssé vagy egyáltalán nem használható az illeszkedés jóságának becslésére a nem lineáris regresszió esetében. Jobb illeszkedést kell elérni a görbe munkatartományában számított és mért koncentrációk közötti legkisebb különbségek, például a legkisebb maradék négyzetösszeg alkalmazásával. |
|
— |
A mintakivonat becsült koncentrációját ezután korrigálni kell egy vakmátrixra/vakoldószerre számított BEQ-értékkel (az alkalmazott oldószerek és vegyszerek szennyeződéseinek figyelembevétele céljából) és a látszólagos visszanyeréssel (ennek kiszámítása a reprezentatív kongénerkombinációkat a felső határérték vagy a beavatkozási küszöbérték körül tartalmazó, alkalmas referenciaminták BEQ-értékéből történik). A visszanyeréssel való korrigáláshoz a látszólagos visszanyerésnek az előírt tartományba kell esnie (lásd a 7.1.4. pontot). A visszanyeréssel való korrigáláshoz használt referenciamintáknak meg kell felelniük a 7.2. pontban ismertetett követelményeknek. |
7.1.2.2. Kalibrálás referenciamintákkal
Más megoldásként használható legalább négy referenciamintával (lásd a 7.2.4. pontot: egy vakmátrix, plusz három referenciaminta, mely a felső határérték vagy a beavatkozási küszöbérték 0,5-szerese, 1,0-szerese, illetve 2,0-szerese) készített kalibrációs görbe, így nincs szükség a vakminta eredményeivel és a visszanyeréssel történő korrigálásra. Ebben az esetben a felső határérték 2/3-ának megfelelő mérési reakció (lásd a 7.3. pontot) közvetlenül kiszámítható ezekből a mintákból és cut-off értékként használható. A beavatkozási küszöbértékeket meghaladó minták ellenőrzéséhez a beavatkozási küszöbértékek megfelelő százalékaránya lehet az alkalmas cut-off érték.
7.1.3. A PCDD-k/PCDF-ek és a dioxinjellegű PCB-k meghatározása külön-külön
A kivonatok szétválaszthatók olyan frakciókra, melyek PCDD-ket/PCDF-eket, illetve dioxinjellegű PCB-ket tartalmaznak, így külön-külön meghatározható a PCDD-k/PCDF-ek, illetve a dioxinjellegű PCB-k TEQ-értéke (BEQ-értékként). A dioxinjellegű PCB-ket tartalmazó frakció eredményeinek kiszámításához lehetőleg a PCB-126-tal készített standarddal felvett kalibrációs görbét kell használni.
7.1.4. Biológiai próbák során észlelt visszanyerések
A »biológiai próbák során észlelt visszanyerést« a felső határérték vagy a beavatkozási küszöbérték körüli reprezentatív kongénerkombinációkat tartalmazó alkalmas referenciamintákból kell kiszámítani és a BEQ-értéknek a TEQ-értékhez képesti százalékában kell megadni. A teszt típusától és az alkalmazott TEF-értékektől (10) függően a dioxinjellegű PCB-kre vonatkozó TEF- és REP-tényezők közötti különbségek a dioxinjellegű PCB-k esetében a PCDD-khez/PCDF-ekhez képest kis látszólagos visszanyerést okozhatnak. Ezért ha a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k meghatározása külön-külön történik, akkor a biológiai próba során észlelt visszanyeréseknek a következőnek kell lenniük: dioxinjellegű PCB-knél 20–60 %, PCDD-knél/PCDF-eknél pedig 50–130 % (a tartományok a TCDD-s kalibrációs görbére vonatkoznak). Mivel a dioxinjellegű PCB-k hozzájárulása a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegéhez a mátrixoktól és a mintáktól függően változhat, a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegére vonatkozóan a biológiai próba során észlelt visszanyerések tükrözik ezeket a tartományokat, és ezeknek 30 % és 130 % között kell lenniük. A PCDD-kre/PCDF-ekre és a dioxinjellegű PCB-kre vonatkozó uniós szabályozásban a TEF-értékek lényeges módosítása esetén ezeket a tartományokat is módosítani kell.
7.1.5. A visszanyerések ellenőrzése mintatisztításnál
A mintatisztítás során előforduló vegyületvesztést a hitelesítéskor ellenőrizni kell. A különböző kongénerek keverékével adalékolt vakmintán el kell végezni a mintatisztítást (n = legalább 3), és a visszanyerést és a variabilitást megerősítő módszerrel kell ellenőrizni. A visszanyerésnek 60 % és 120 % között kell lennie, főként olyan kongénereknél, amelyek 10 %-nál nagyobb mértékben járulnak hozzá a TEQ-értékhez a különféle keverékekben.
7.1.6. Jelentési határérték
A BEQ-értékeknek a jelentésben történő megadásához jelentési határértéket kell meghatározni jellemző kongénerkombinációkat tartalmazó adott mátrixmintákból (nem a standard kalibrációs görbéből, mivel a görbe alján kicsi a módszerpontosság). Figyelembe kell venni az extrakció és a mintatisztítás hatásait. A jelentési határértéket az elemzési vakmintákkal kapott érték legalább háromszorosaként kell megállapítani.
7.2. Referenciaminták használata
7.2.1. A referenciamintáknak reprezentálniuk kell a mintamátrixot, a kongénerkombinációkat és a PCDD-knek/PCDF-eknek és a dioxinjellegű PCB-knek a felső határérték vagy a beavatkozási küszöbérték körüli koncentrációtartományait.
7.2.2. Mindegyik méréssorozatban lennie kell vakmátrixnak vagy, ha ez nem lehetséges, elemzési vakmintának, valamint a felső határérték vagy a beavatkozási küszöbérték körüli koncentrációjú referenciamintának. Ezeket a mintákat egy időben és azonos körülmények között kell extrahálni és elemezni. A referenciamintának egyértelműen nagyobb reakciót kell adnia, mint a vakmintának, így biztosítva az elemzés alkalmasságát. Ezek a minták használhatók a vakminta eredményeivel és a visszanyeréssel való korrigáláshoz.
7.2.3. A visszanyeréssel való korrigáláshoz választott referenciamintáknak reprezentatívaknak kell lenniük az elemzett mintákra, ami azt jelenti, hogy a kongénerkombinációk nem okozhatják a koncentrációk alábecslését.
7.2.4. A felső határérték vagy a beavatkozási küszöbérték ellenőrzésére például a felső határérték vagy a beavatkozási küszöbérték felének és kétszeresének megfelelő további referenciamintákat is alkalmazni lehet annak igazolására, hogy az elemzés alkalmassága a keresett tartományban megfelelő. Ezek a minták együttesen használhatók az elemzett minták BEQ-értékeinek kiszámítására (lásd a 7.1.2.2. pontot).
7.3. A cut-off értékek meghatározása
Meg kell határozni a BEQ-értékként kapott bioanalitikai eredmények és a megerősítő módszerrel kapott TEQ-értékek közötti összefüggést, például egyeztetett mátrixokkal végzett kalibrálási kísérletekkel, a felső határérték (ML) 0-szorosával, 0,5-szeresével, 1-szeresével és 2-szeresével egyenlő koncentrációkra adalékolt referenciamintákat használva, mindegyik koncentrációnál hat-hat ismétléssel (n = 24). Ebből az összefüggésből meg lehet becsülni a korrigálási tényezőket (vakminta és visszanyerés), de azokat a 7.2.2. pont szerint ellenőrizni kell.
Cut-off értékeket kell megállapítani annak eldöntéséhez, hogy a minta megfelel-e a PCDD-kre/PCDF-ekre és a dioxinjellegű PCB-kre külön-külön, vagy pedig a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegére meghatározott felső határértéknek, illetve adott esetben a beavatkozási küszöbértéknek. Ezeket a (vakminta eredményeivel és a visszanyeréssel korrigált) bioanalitikai eredmények eloszlásának alsó végpontja jelenti, amely megfelel a megerősítő módszernél használt, 5 %-nál kisebb »hamis megfelelő« arányt és 25 %-nál kisebb RSDR-t feltételező 95 %-os megbízhatósági szinten alapuló döntési határértéknek. A megerősítő módszernél használt döntési határérték a felső határérték, figyelembe véve a mérési bizonytalanságot.
A (BEQ értékként kifejezett) cut-off érték a 7.3.1., a 7.3.2. és a 7.3.3. pontban ismertetett módszerek egyikével számítható ki (lásd az 1. ábrát).
7.3.1. A 95 %-os predikciós intervallum alsó sávja a megerősítő módszernél használt döntési határértéknél:

ahol:
|
BEQDL |
A megerősítő módszer döntési határértékének – amely a mérési bizonytalanságot is tartalmazó felső határérték – megfelelő BEQ |
|
sy,x |
maradék szórás |
|
t α,f = m–2 |
Student-tényező (α = 5 %, f = szabadságfok, egyoldali) |
|
m |
a kalibrációs pontok összesen (j index) |
|
n |
az ismétlések száma az egyes koncentrációknál |
|
xi |
az i. kalibrációs pontnál a minta megerősítő módszerrel mért koncentrációja (TEQ-értékként) |
|
|
az összes kalibrálási minta koncentrációjának (TEQ-érték) átlaga |
|
|
Qxx = négyzetösszeg-paraméter, i = az i. kalibrálási pont indexe |
7.3.2. A megerősítő módszer döntési határértékének megfelelő szennyezettségű minták párhuzamos elemzéseinek (n≥ 6) (a vakminta eredményeivel és a visszanyeréssel korrigált) bioanalitikai eredményeiből, az eloszlási görbének a megfelelő BEQ-átlagértéknél lévő alsó végpontjaként:
Cut-off érték = BEQDL – 1,64xSDR
ahol:
|
SDR |
a biológiai tesztek BEQDL-értékre kapott eredményeinek szórása, a laboratóriumon belüli reprodukálhatóság körülményei között mérve. |
7.3.3. A felső határérték vagy a beavatkozási küszöbérték 2/3-ának megfelelő szennyezettségű minták párhuzamos elemzéseivel (n≥ 6) kapott (BEQ-értékként kifejezett, a vakminta eredményeivel és a visszanyeréssel korrigált) bioanalitikai eredmények átlaga, annak a megfigyelésnek az alapján, hogy ez az érték a 7.3.1. vagy 7.3.2. pont szerint meghatározott cut-off érték körül lesz.
1. ábra

1. ábra 5 %-nál kisebb »hamis megfelelő« arányt és 25 %-nál kisebb RSDR-t feltételező 95 %-os megbízhatósági szinten alapuló cut-off értékek kiszámítása:
|
1. |
a 95 %-os predikciós intervallum alsó sávjából a megerősítő módszernél használt döntési határértéknél; |
|
2. |
a megerősítő módszer döntési határértékének megfelelő szennyezettségű minták párhuzamos elemzéseinek (n≥ 6) (a vakminta eredményeivel és a kihozatallal korrigált) bioanalitikai eredményeiből, az eloszlási görbének (az ábrán a harang alakú görbe) a megfelelő BEQ-átlagértéknél lévő alsó végpontjaként: |
7.3.4. A cut-off értékek korlátozásai:
A korlátozott számú, különböző mátrixú/kongénerkombinációjú mintákkal végzett hitelesítés során kapott RSDR-ből kiszámított, BEQ értéken alapuló cut-off értékek nagyobbak lehetnek a TEQ értéken alapuló felső határértéknél vagy beavatkozási küszöbértéknél, mivel hitelesítéskor nagyobb módszerpontosság érhető el, mint a rutinszerű elemzéseknél, ahol a lehetséges kongénerkombinációk ismeretlen skáláját kell ellenőrizni. Ilyen esetekben a cut-off értékek kiszámításához RSDR = 25 %-ot kell venni, vagy pedig a felső határérték vagy a beavatkozási küszöbérték kétharmadát célszerű cut-off értéknek tekinteni.
7.4. Alkalmasságjellemzők
7.4.1. Mivel a bioanalitikai módszereknél nem alkalmazható belső standard, a méréssorozatokon belüli és a sorozatok közötti szórás megállapításához vizsgálni kell a bioanalitikai módszerek megismételhetőségét. A megismételhetőségnek 20 % alatt, a laboratóriumon belüli reprodukálhatóságnak pedig 25 % alatt kell lennie. Ehhez a vakminta eredményeivel és a visszanyeréssel korrigált BEQ értékként számított koncentrációkat kell használni.
7.4.2. A hitelesítési eljárás részeként a tesztről ki kell mutatni, hogy különbséget tesz a vakminta eredménye és a cut-off érték között, és így lehetővé teszi a megfelelő cut-off érték felett lévő minták azonosítását (lásd a 7.1.2. pontot).
7.4.3. Meg kell határozni a keresett vegyületeket, az esetleges interferenciákat és a vakminták elfogadható legnagyobb értékeit.
7.4.4. Egy mintakivonat három párhuzamos meghatározásakor kapott reakciók vagy az ilyen reakcióból számított koncentrációk (csak a munkatartományban lehetséges) százalékos szórása nem lehet nagyobb 15 %-nál.
7.4.5. A referenciaminta/referenciaminták BEQ-értékként kifejezett, korrigálás (vakminta és felső határérték vagy beavatkozási küszöbérték) nélküli eredményeit kell használni a bioanalitikai módszer egy meghatározott időszak alatti alkalmasságának értékelésére.
7.4.6. Az elemzési vakmintákról és a referenciaminták egyes típusairól minőség-ellenőrzési nyilvántartást kell vezetni, és ellenőrizni kell, hogy az analitikai alkalmasság biztosan megfelel-e a követelményeknek, az elemzési vakminták esetében főként a munkatartomány aljához képest előírt legkisebb különbség, a referenciaminták esetében pedig főként a laboratóriumon belüli reprodukálhatóság tekintetében. Az elemzési vakmintáknál ügyelni kell arra, hogy a kivonás miatt ne keletkezhessenek »hamis megfelelő« eredmények.
7.4.7. A szűrőmódszer alkalmasságának, valamint a BEQ és a TEQ közötti összefüggés értékeléséhez a feltehetően nem megfelelő mintáknak és a megfelelő minták 2–10 %-ának (mátrixonként legalább 20 minta) megerősítő módszerrel végzett elemzéséből származó eredményeket kell összegyűjteni és felhasználni. Ez az adatbázis használható a hitelesített mátrixokkal végzett rutinszerű elemzésekre vonatkozó cut-off értékek újraértékeléséhez.
7.4.8. A módszerek alkalmassága igazolható körvizsgálatokban való részvétellel is. A körvizsgálatokban elemzett minták eredményei, a felső határérték kétszereséig terjedő koncentrációtartományokban, felhasználhatók a »hamis megfelelő« arány kiszámításához, ha a laboratórium igazolni tudja az alkalmasságot. A mintáknak le kell fedniük a különféle forrásokat reprezentáló, leggyakoribb kongénerkombinációkat.
7.4.9. Szennyeződési eseteknél a cut-off értékek átértékelhetők, hogy tükrözzék az adott külön esemény egyedi mátrix- és kongénerkombinációit.
8. Az eredmények jelentése
8.1. Megerősítő módszerek
8.1.1. Amennyire az alkalmazott analitikai eljárás lehetővé teszi, az analitikai eredmények között fel kell tüntetni az egyes PCDD-/PCDF- és dioxinjellegű PCB-kongénerek koncentrációit, és ezeket felfelé, lefelé és középre kerekített értékként kell a jelentésben megadni, hogy az az eredményekről a lehető legtöbb információt tartalmazza, lehetővé téve az eredményeknek a vonatkozó követelmények szerinti értelmezését.
8.1.2. A jelentésnek tartalmaznia kell a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k extrahálásához használt módszert.
8.1.3. Meg kell adni az egyes belső standardok visszanyeréseit abban az esetben, ha a visszanyerések kívül esnek a 6.2.5. pontban megadott tartományon, ha az eredmények meghaladják a felső határértéket (ebben az esetben meg kell adni a két párhuzamos elemzés egyikének visszanyeréseit) vagy kérésre más esetekben.
8.1.4. Mivel a minta megfelelőségéről való döntésnél figyelembe kell venni a mérési bizonytalanságot, ezt a paramétert is meg kell adni. Az analitikai eredményeket tehát x ± U formában kell megadni a jelentésben, ahol x az analitikai eredmény, U a kiterjesztett mérési bizonytalanság – a kiterjesztési tényező 2, amely körülbelül 95 %-os megbízhatósági szintet eredményez. A PCDD-k/PCDF-ek és a dioxinjellegű PCB-k külön meghatározása esetén a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k külön-külön kapott analitikai eredményeinél becsült kiterjesztett bizonytalanságok összegét kell használni a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összegének kiszámításához.
8.1.5. Ha a mérési bizonytalanság figyelembevétele a CCα alkalmazásával történik (az e B. rész I. fejezetének 2.2. pontjában leírt módon), akkor ezt a paramétert is meg kell adni a jelentésben.
8.1.6. Az eredményeket ugyanabban a mértékegységben és legalább ugyanannyi tizedesjeggyel kell megadni, ahogy a 2002/32/EK irányelv a felső határértékeket megadja.
8.2. Bioanalitikai szűrőmódszerek
8.2.1. A szűrés eredményét »megfelelő« vagy »feltehetően nem megfelelő« megjelöléssel kell megadni.
8.2.2. Ezenkívül az eredmény a PCDD-kre/PCDF-ekre és/vagy a dioxinjellegű PCB-kre megadható BEQ-értékként, nem pedig TEQ-értékként.
8.2.3. A jelentési határérték alatti reakciókat adó mintákat »jelentési határérték alatt« megjelöléssel kell feltüntetni.
8.2.4. A jelentésnek minden mintamátrix-típusnál tartalmaznia kell az értékelés alapját képező felső határértéket vagy beavatkozási küszöbértéket.
8.2.5. A jelentésnek tartalmaznia kell az alkalmazott teszt típusát, a teszt alapelvét és a kalibráció típusát.
8.2.6. A jelentésnek tartalmaznia kell a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k extrahálásához használt módszert.
8.2.7. Ha valamely mintával kapcsolatban felmerül, hogy feltehetően nem felel meg, a jelentésben szerepelnie kell a szükséges intézkedésre vonatkozó megjegyzésnek. A jelentős koncentrációt tartalmazó mintákban a PCDD-k/PCDF-ek koncentrációját, valamint a PCDD-k/PCDF-ek és a dioxinjellegű PCB-k összkoncentrációját megerősítő módszerrel kell meghatározni/megerősíteni.
III. FEJEZET
A nem dioxinjellegű PCB-k (PCB -28, -52, -101, -138, -153, -180) koncentrációjának hatósági ellenőrzéséhez használt minta-előkészítés és az elemzési módszerekre vonatkozó előírások
1. Alkalmazási kör
Az e fejezetben előírt követelményeket kell alkalmazni a takarmányoknak a nem dioxinjellegű poliklórozott bifenilek (nem dioxinjellegű PCB-k) koncentrációja tekintetében történő hatósági ellenőrzéséhez, valamint egyéb szabályozási célokra.
2. Az alkalmazandó kimutatási módszerek
Gázkromatográfia/elektronbefogásos kimutatás (GC-ECD), GC-LRMS, GC-MS/MS, GC-HRMS vagy hasonló módszerek.
3. A keresett analitok beazonosítása és megerősítése
3.1. A belső standardokhoz vagy referenciastandardokhoz viszonyított relatív retenciós idő (elfogadható eltérés: ± 0,25 %).
3.2. Gázkromatográfiás elválasztásnál meg kell erősíteni, hogy megtörtént-e mind a hat indikátor PCB (PCB-28, PCB-52, PCB-101, PCB-138, PCB-153 és PCB-180) elválasztása a zavaró anyagoktól, főként az együtt eluálódó PCB-ktől, különösen akkor, ha a minták koncentrációi a jogszabályi határértékek tartományában vagy a fölött vannak, és a meg nem felelést meg kell erősíteni.
[A tapasztalatok szerint a következő kongénereknél például gyakran előfordul az együttes eluáció: PCB-28/-31, PCB-52/-69 és PCB-138/-163/-164. A GC-MS módszernél figyelembe kell venni az esetleg a nagyobb mértékben klórozott kongénerek fragmentumai által okozott zavarást is.]
3.3. A GC-MS módszerekre vonatkozó előírások
Mérni kell legalább a következőket:
|
a) |
a HRMS-nél két meghatározott ion; |
|
b) |
az LRMS-nél két meghatározott m/z > 200 ion vagy három meghatározott m/z > 100 ion; |
|
c) |
az MS-MS-nél 1 elővegyület- és 2 termékion. |
Kiválasztott tömegfragmentumok gyakoriságára megengedett tűrések:
Kiválasztott tömegfragmentumok gyakoriságának relatív eltérése az elméleti gyakorisághoz vagy a keresett ion (a vizsgált ionok közül a leggyakoribb) és a minősítő ion(ok) kalibrációs standardjához képest:
|
A minősítő ion(ok) relatív intenzitása a keresett ionhoz képest |
GC-EI-MS (relatív eltérés) |
GC-CI-MS, GC-MSn (relatív eltérés) |
|
> 50 % |
± 10 % |
± 20 % |
|
> 20 % és 50 % között |
± 15 % |
± 25 % |
|
> 10 % és 20 % között |
± 20 % |
± 30 % |
|
≤ 10 % |
± 50 % (11) |
± 50 % (11) |
3.4. A GC-ECD módszerekre vonatkozó előírások
A tűrést meghaladó eredményeket különböző polaritású állófázist használó két gázkromatográfiás oszloppal meg kell erősíteni.
4. A módszerek alkalmasságának igazolása
A módszerek alkalmasságát a felső határérték tartományában (a felső határérték felétől a kétszereséig) kell hitelesíteni úgy, hogy az ismételt elemzések elfogadható variációs együtthatót adnak (a közbenső módszerpontosságra vonatkozó előírásokat lásd a 9. pontban).
5. A mennyiségi meghatározás határértéke
A vakmintákkal kapott eredmények nem lehetnek nagyobbak a felső határértéknek megfelelő szennyeződéskoncentráció 30 %-ánál (12).
6. Minőség-ellenőrzés
Rendszeres vakkontrollmérések, adalékolt minták elemzése, minőség-ellenőrzési minták, részvétel a vonatkozó mátrixokkal végzett laboratóriumközi körvizsgálatokban.
7. A visszanyerések ellenőrzése
7.1. A keresett analitokhoz hasonló fizikai-kémiai tulajdonságokkal rendelkező alkalmas belső standardokat kell használni.
7.2. Belső standardok hozzáadása:
Hozzáadás a termékekhez (extrahálás és mintatisztítás előtt).
7.3. A mind a hat izotópos jelölésű indikátor PCB-kongénert használó módszerekre vonatkozó előírások:
|
a) |
az eredményeket korrigálni kell a belső standardok visszanyeréseivel; |
|
b) |
az izotópjelölésű belső standardok visszanyeréseinek 50 % és 120 % között kell lenniük; |
|
c) |
a hat indikátor PCB összegéhez 10 %-nál kisebb mértékben hozzájáruló egyes kongénereknél elfogadhatók ennél kisebb vagy nagyobb visszanyerések. |
7.4. A nem mind a hat izotópos jelölésű indikátor PCB-ből készített belső standardokat vagy más belső standardokat használó módszerekre vonatkozó előírások:
|
a) |
a belső standard(ok) visszanyerését minden minta esetében ellenőrizni kell; |
|
b) |
a belső standard(ok) visszanyeréseinek 60 % és 120 % között kell lenniük; |
|
c) |
az eredményeket korrigálni kell a belső standardok visszanyeréseivel. |
7.5. Az izotóppal nem jelölt kongénerek visszanyerését olyan adalékolt mintákkal vagy minőség-ellenőrzési mintákkal kell ellenőrizni, amelyek koncentrációja a felső határérték körüli tartományba esik. Ezeknek a kongénereknek a visszanyeréseit elfogadhatónak kell tekinteni, ha 70 % és 120 % között vannak.
8. A laboratóriumokra vonatkozó követelmények
A 882/2004/EK rendelet rendelkezéseinek megfelelően az analitikai minőségbiztosítás alkalmazásának biztosítása érdekében a laboratóriumokat az ISO 58 útmutató szerint működő elismert testületnek kell akkreditálnia. A laboratóriumokat az EN ISO/IEC 17025 szabvány szerint kell akkreditálni.
9. Alkalmasságjellemzők: a felső határértékben jelen lévő hat indikátor PCB összegére vonatkozó kritériumok
|
Valódiság |
– 30 % és + 30 % között |
|
Közbenső módszerpontosság (RSD%) |
≤ 20 % |
|
A felfelé és a lefelé kerekítés közötti különbség |
≤ 20 % |
10. Az eredmények jelentése
10.1. Amennyire az alkalmazott analitikai eljárás lehetővé teszi, az analitikai eredmények között fel kell tüntetni az egyes PCB-kongénerek koncentrációit, és ezeket felfelé, lefelé és középre kerekített értékként kell a jelentésben megadni, hogy az az eredményekről a lehető legtöbb információt tartalmazza, lehetővé téve az eredményeknek a vonatkozó követelmények szerinti értelmezését.
10.2. A jelentésnek tartalmaznia kell a PCB-k és a lipidek extrahálásához használt módszert.
10.3. Meg kell adni az egyes belső standardok visszanyeréseit abban az esetben, ha a visszanyerések kívül esnek a 7. pontban megadott tartományon, ha az eredmények meghaladják a felső határértéket vagy kérésre más esetekben.
10.4. Mivel a minta megfelelőségéről való döntésnél figyelembe kell venni a mérési bizonytalanságot, ezt a paramétert is meg kell adni. Az analitikai eredményeket tehát x ± U formában kell megadni a jelentésben, ahol x az analitikai eredmény, U a kiterjesztett mérési bizonytalanság – a kiterjesztési tényező 2, amely körülbelül 95 %-os megbízhatósági szintet eredményez.
10.5. Ha a mérési bizonytalanság figyelembevétele a CCα alkalmazásával történik (az I. fejezet 2.1. pontjában leírt módon), akkor ezt a paramétert is meg kell adni a jelentésben.
10.6. Az eredményeket ugyanabban a mértékegységben és legalább ugyanannyi tizedesjeggyel kell megadni, ahogy a 2002/32/EK irányelv a felső határértékeket megadja.
(9) a felső határértékhez képest.
(11) Mivel van elég 10 %-nál nagyobb relatív intenzitású tömegfragmentum, a keresett ionhoz képest 10 %-nál kisebb relatív intenzitású minősítő ion(ok) használata nem ajánlott.