EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 02010R0605-20140326
Commission Regulation (EU) No 605/2010 of 2 July 2010 laying down animal and public health and veterinary certification conditions for the introduction into the European Union of raw milk, dairy products, colostrum and colostrum-based products intended for human consumption (Text with EEA relevance)
Consolidated text: Règlement (UE) n o 605/2010 de la Commission du 2 juillet 2010 arrêtant les conditions sanitaires et de police sanitaire ainsi que les exigences en matière de certification vétérinaire pour l’introduction dans l’Union européenne de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum destinés à la consommation humaine (Texte présentant de l'intérêt pour l'EEE)
Règlement (UE) n o 605/2010 de la Commission du 2 juillet 2010 arrêtant les conditions sanitaires et de police sanitaire ainsi que les exigences en matière de certification vétérinaire pour l’introduction dans l’Union européenne de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum destinés à la consommation humaine (Texte présentant de l'intérêt pour l'EEE)
2010R0605 — FR — 26.03.2014 — 005.001
Ce document constitue un outil de documentation et n’engage pas la responsabilité des institutions
|
RÈGLEMENT (UE) No 605/2010 DE LA COMMISSION du 2 juillet 2010 arrêtant les conditions sanitaires et de police sanitaire ainsi que les exigences en matière de certification vétérinaire pour l’introduction dans l’Union européenne de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum destinés à la consommation humaine (Texte présentant de l'intérêt pour l'EEE) (JO L 175, 10.7.2010, p.1) |
Modifié par:
|
|
|
Journal officiel |
||
|
No |
page |
date |
||
|
RÈGLEMENT D’EXÉCUTION (UE) No 914/2011 DE LA COMMISSION du 13 septembre 2011 |
L 237 |
1 |
14.9.2011 |
|
|
RÈGLEMENT D’EXÉCUTION (UE) No 957/2012 DE LA COMMISSION du 17 octobre 2012 |
L 287 |
5 |
18.10.2012 |
|
|
RÈGLEMENT D’EXÉCUTION (UE) No 300/2013 DE LA COMMISSION du 27 mars 2013 |
L 90 |
71 |
28.3.2013 |
|
|
RÈGLEMENT (UE) No 519/2013 DE LA COMMISSION du 21 février 2013 |
L 158 |
74 |
10.6.2013 |
|
|
RÈGLEMENT D’EXÉCUTION (UE) No 556/2013 DE LA COMMISSION du 14 juin 2013 |
L 164 |
13 |
18.6.2013 |
|
|
RÈGLEMENT D’EXÉCUTION (UE) No 209/2014 DE LA COMMISSION du 5 mars 2014 |
L 66 |
11 |
6.3.2014 |
|
RÈGLEMENT (UE) No 605/2010 DE LA COMMISSION
du 2 juillet 2010
arrêtant les conditions sanitaires et de police sanitaire ainsi que les exigences en matière de certification vétérinaire pour l’introduction dans l’Union européenne de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum destinés à la consommation humaine
(Texte présentant de l'intérêt pour l'EEE)
LA COMMISSION EUROPÉENNE,
vu le traité sur le fonctionnement de l’Union européenne,
vu la directive 2002/99/CE du Conseil du 16 décembre 2002 fixant les règles de police sanitaire régissant la production, la transformation, la distribution et l’introduction des produits d’origine animale destinés à la consommation humaine ( 1 ), et notamment son article 8, phrase introductive, son article 8, point 1, premier alinéa, et point 4, ainsi que son article 9, paragraphe 4,
vu le règlement (CE) no 852/2004 du Parlement européen et du Conseil du 29 avril 2004 relatif à l’hygiène des denrées alimentaires ( 2 ), et notamment son article 12,
vu le règlement (CE) no 853/2004 du Parlement européen et du Conseil du 29 avril 2004 fixant des règles spécifiques d'hygiène applicables aux denrées alimentaires d'origine animale ( 3 ), et notamment son article 9,
vu le règlement (CE) no 854/2004 du Parlement européen et du Conseil du 29 avril 2004 fixant les règles spécifiques d'organisation des contrôles officiels concernant les produits d'origine animale destinés à la consommation humaine ( 4 ), et notamment son article 11, paragraphe 1, son article 14, paragraphe 4, et son article 16,
vu le règlement (CE) no 882/2004 du Parlement européen et du Conseil du 29 avril 2004 relatif aux contrôles officiels effectués pour s'assurer de la conformité avec la législation sur les aliments pour animaux et les denrées alimentaires et avec les dispositions relatives à la santé animale et au bien-être des animaux ( 5 ), et notamment son article 48, paragraphe 1,
considérant ce qui suit:|
(1) |
La directive 92/46/CEE du Conseil du 16 juin 1992 arrêtant les règles sanitaires pour la production et la mise sur le marché de lait cru, de lait traité thermiquement et de produits à base de lait ( 6 ) prévoyait l’établissement d’une liste de pays tiers ou de parties de pays tiers en provenance desquels les États membres devaient autoriser l’importation de lait ou de produits à base de lait. Elle disposait également que ces denrées devaient être accompagnées d’un certificat sanitaire, satisfaire à certaines exigences, y compris en matière de traitement thermique, et offrir certaines garanties. |
|
(2) |
La décision 2004/438/CE de la Commission du 29 avril 2004 arrêtant les conditions sanitaires et de police sanitaire ainsi que la certification vétérinaire requises à l’introduction dans la Communauté de lait traité thermiquement, de produits à base de lait et de lait cru destinés à la consommation humaine ( 7 ) a été adoptée en conséquence. |
|
(3) |
Depuis l’adoption de cette décision, plusieurs nouvelles exigences sanitaires et de police sanitaire ont été établies, constituant un nouveau cadre réglementaire dans ce domaine que le présent règlement doit prendre en considération. Par ailleurs, la directive 92/46/CEE a été abrogée par la directive 2004/41/CE du Parlement européen et du Conseil du 21 avril 2004 abrogeant certaines directives relatives à l'hygiène des denrées alimentaires et aux règles sanitaires régissant la production et la mise sur le marché de certains produits d'origine animale destinés à la consommation humaine ( 8 ). |
|
(4) |
Le règlement (CE) no 178/2002 du Parlement européen et du Conseil du 28 janvier 2002 établissant les principes généraux et les prescriptions générales de la législation alimentaire, instituant l'Autorité européenne de sécurité des aliments et fixant des procédures relatives à la sécurité des denrées alimentaires ( 9 ) définit les principes généraux régissant les denrées alimentaires et les aliments pour animaux en général, et la sécurité de ces denrées et aliments en particulier, au niveau de l’Union européenne et au niveau national. |
|
(5) |
La directive 2002/99/CE fixe les règles régissant l'introduction, en provenance des pays tiers, de produits d'origine animale destinés à la consommation humaine. Elle prévoit que ces produits ne peuvent être introduits dans l’Union européenne que s'ils sont conformes aux exigences applicables à toutes les étapes de la production, de la transformation et de la distribution de tels produits dans l’Union européenne ou offrent des garanties équivalentes en matière de santé animale. |
|
(6) |
Le règlement (CE) no 852/2004 établit, à l'intention des exploitants du secteur alimentaire, des règles générales en matière d’hygiène des denrées alimentaires à toutes les étapes de la chaîne alimentaire, y compris celle de la production primaire. |
|
(7) |
Le règlement (CE) no 853/2004 établit, à l’intention des exploitants du secteur alimentaire, des règles spécifiques relatives à l’hygiène des denrées alimentaires d'origine animale. Il prévoit que les exploitants du secteur alimentaire qui produisent du lait cru et des produits laitiers destinés à la consommation humaine doivent respecter les dispositions applicables de son annexe III. |
|
(8) |
Le règlement (CE) no 854/2004 fixe des règles spécifiques pour l’organisation des contrôles officiels concernant les produits d’origine animale. |
|
(9) |
Le règlement (CE) no 2073/2005 de la Commission du 15 novembre 2005 concernant les critères microbiologiques applicables aux denrées alimentaires ( 10 ) établit les critères microbiologiques relatifs à certains micro-organismes et les règles d'application que les exploitants du secteur alimentaire doivent observer lorsqu'ils mettent en œuvre les mesures d'hygiène générales et spécifiques visées à l'article 4 du règlement (CE) no 852/2004. Il impose aux exploitants du secteur alimentaire de veiller à ce que les denrées alimentaires respectent les critères microbiologiques pertinents qu'il établit. |
|
(10) |
Le champ d’application de la directive 92/46/CEE du Conseil se limite au lait cru de vaches, de brebis, de chèvres et de bufflonnes et à ses produits dérivés. Toutefois, la définition du lait cru et des produits laitiers établie à l’annexe I du règlement (CE) no 853/2004 élargit le champ d’application des règles concernant l’hygiène du lait à toutes les espèces de mammifères et définit le lait cru comme le lait produit par la sécrétion de la glande mammaire d'animaux d'élevage et non chauffé à plus de 40 °C ni soumis à un traitement d'effet équivalent. En outre, ce règlement définit les produits laitiers comme des produits transformés résultant du traitement de lait cru ou d'un traitement ultérieur de ces produits transformés. |
|
(11) |
Étant donné l’entrée en application des règlements (CE) no 852/2004, (CE) no 853/2004 et (CE) no 854/2004, ainsi que des actes d’exécution de ces règlements, il est nécessaire de modifier et d’actualiser les conditions sanitaires et de police sanitaire de l’Union européenne ainsi que les exigences en matière de certification en vue de l’introduction dans l’Union européenne de lait cru et de produits laitiers destinés à la consommation humaine. |
|
(12) |
Dans un souci de cohérence de la législation de l’Union, le présent règlement doit aussi tenir compte des règles établies par le règlement (CE) no 470/2009 du Parlement européen et du Conseil du 6 mai 2009 établissant des procédures communautaires pour la fixation des limites de résidus des substances pharmacologiquement actives dans les aliments d’origine animale, abrogeant le règlement (CEE) no 2377/90 du Conseil et modifiant la directive 2001/82/CE du Parlement européen et du Conseil et le règlement (CE) no 726/2004 du Parlement européen et du Conseil ( 11 ), ainsi que de ses modalités d’application, fixées par le règlement (UE) no 37/2010 de la Commission du 22 décembre 2009 relatif aux substances pharmacologiquement actives et à leur classification en ce qui concerne les limites maximales de résidus dans les aliments d’origine animale ( 12 ). Il doit en outre tenir compte de la directive 96/23/CE du Conseil du 29 avril 1996 relative aux mesures de contrôle à mettre en œuvre à l'égard de certaines substances et de leurs résidus dans les animaux vivants et leurs produits et abrogeant les directives 85/358/CEE et 86/469/CEE et les décisions 89/187/CEE et 91/664/CEE ( 13 ). |
|
(13) |
La directive 96/93/CE du Conseil du 17 décembre 1996 concernant la certification des animaux et des produits animaux ( 14 ) établit les règles à respecter pour la délivrance des certificats requis par la législation vétérinaire, de façon à empêcher les certifications trompeuses ou frauduleuses. Il convient de veiller à ce que les autorités compétentes des pays tiers exportateurs appliquent des exigences en matière de certification au moins équivalentes à celles établies dans ladite directive. |
|
(14) |
Par ailleurs, la directive 90/425/CEE du Conseil du 26 juin 1990 relative aux contrôles vétérinaires et zootechniques applicables dans les échanges intracommunautaires de certains animaux vivants et produits dans la perspective de la réalisation du marché intérieur ( 15 ) prévoit l’instauration d’un système informatisé de liaison entre autorités vétérinaires, lequel a été mis en place dans l’Union européenne. Il est nécessaire de modifier le format de tous les modèles de certificats sanitaires en vue de les rendre compatibles avec une éventuelle certification électronique dans le cadre du système expert de contrôle des échanges (TRACES), prévu par la directive 90/425/CEE. En conséquence, les règles définies par le présent règlement doivent tenir compte du système TRACES. |
|
(15) |
La directive 97/78/CE du Conseil du 18 décembre 1997 fixant les principes relatifs à l'organisation des contrôles vétérinaires pour les produits en provenance des pays tiers introduits dans la Communauté ( 16 ) établit des règles relatives aux contrôles vétérinaires portant sur les produits d’origine animale introduits dans l’Union européenne en provenance des pays tiers en vue de leur importation ou de leur transit, y compris certaines exigences en matière de certification. Ces règles sont applicables aux denrées couvertes par le présent règlement. |
|
(16) |
Compte tenu de la situation géographique de Kaliningrad, il y a lieu de prévoir des conditions particulières de transit par l’Union européenne, concernant uniquement la Lettonie, la Lituanie et la Pologne, pour les lots à destination ou en provenance de Russie. |
|
(17) |
Par souci de clarté du droit européen, il convient d’abroger la décision 2004/438/CE de la Commission et de la remplacer par le présent règlement. |
|
(18) |
Afin d’éviter toute perturbation des échanges, il y a lieu d’autoriser l’utilisation des certificats sanitaires délivrés conformément à la décision 2004/438/CE pendant une période transitoire. |
|
(19) |
Les mesures prévues par le présent règlement sont conformes à l’avis du comité permanent de la chaîne alimentaire et de la santé animale, |
A ADOPTÉ LE PRÉSENT RÈGLEMENT:
Article premier
Objet et champ d'application
Le présent règlement arrête:
a) les conditions sanitaires et de police sanitaire ainsi que les exigences en matière de certification pour l’introduction dans l’Union européenne de lots de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum;
b) la liste des pays tiers à partir desquels l’introduction dans l’Union européenne de tels lots est autorisée.
Le présent règlement s’applique sans préjudice des exigences spécifiques en matière de certification prévues dans d’autres actes de l’Union ou dans des accords conclus par l’Union avec des pays tiers.
Article 2
Importations de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum en provenance de pays tiers ou de parties de pays tiers répertoriés dans la colonne A de l’annexe I
Les États membres autorisent l’importation de lots de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum en provenance de pays tiers ou de parties de pays tiers répertoriés dans la colonne A de l’annexe I.
Article 3
Importations de certains produits laitiers en provenance de pays tiers ou de parties de pays tiers répertoriés dans la colonne B de l’annexe I
Les États membres autorisent l’importation de lots de produits laitiers dérivés de lait cru de vaches, de brebis, de chèvres ou de bufflonnes, en provenance des pays tiers ou des parties de pays tiers non menacés par la fièvre aphteuse qui sont répertoriés dans la colonne B de l’annexe I, à condition que ces produits laitiers aient subi, ou aient été produits à partir de lait cru ayant subi, une pasteurisation impliquant un traitement unique par la chaleur
a) dont l’effet thermique est au moins équivalent à celui d’un processus de pasteurisation consistant à maintenir une température d’au moins 72 °C pendant 15 secondes;
b) qui, le cas échéant, est suffisant pour garantir une réaction négative au test de la phosphatase alcaline, réalisé immédiatement après le traitement thermique.
Article 4
Importations de certains produits laitiers en provenance de pays tiers ou de parties de pays tiers répertoriés dans la colonne C de l’annexe I
Les États membres autorisent l’importation de lots de produits laitiers dérivés de lait cru de vaches, de brebis, de chèvres et de bufflonnes ou, dans les cas spécifiquement autorisés à l’annexe I, de chamelles de l’espèce Camelus dromedarius en provenance des pays tiers ou des parties de pays tiers menacés par la fièvre aphteuse qui sont répertoriés dans la colonne C de l’annexe I, à condition que ces produits laitiers aient subi, ou aient été produits à partir de lait cru ayant subi, un traitement thermique impliquant:
◄
a) un processus de stérilisation permettant d’atteindre une valeur F0 égale ou supérieure à 3;
b) un traitement par ultra-haute température (UHT) à une température d'au moins 135 °C, maintenue pendant une durée appropriée;
i) pour le lait dont le pH est égal ou supérieur à 7,0, une pasteurisation ultra-rapide à haute température (HTST) pendant 15 secondes à 72 °C, effectuée à deux reprises, garantissant, le cas échéant, une réaction négative au test de la phosphatase alcaline, réalisé immédiatement après le traitement thermique, ou
ii) un traitement dont l’effet de pasteurisation est équivalent à celui du point i) et qui garantit, le cas échéant, une réaction négative au test de la phosphatase alcaline, réalisé immédiatement après le traitement thermique;
d) un traitement HTST simple du lait présentant un pH inférieur à 7,0; ou
e) un traitement HTST associé à un autre traitement physique, qui peut être:
i) soit un abaissement du pH en dessous de 6 pendant une heure,
ii) soit une exposition additionnelle à une température égale ou supérieure à 72 °C, combinée avec une dessiccation.
2. Les États membres autorisent l’importation de lots de produits laitiers dérivés de lait cru d’animaux autres que ceux visés au paragraphe 1, en provenance des pays tiers ou des parties de pays tiers menacés par la fièvre aphteuse qui sont répertoriés dans la colonne C de l’annexe I, à condition que ces produits laitiers aient subi, ou aient été produits à partir de lait cru ayant subi, un traitement impliquant:
a) un processus de stérilisation permettant d’atteindre une valeur F0 égale ou supérieure à 3; ou
b) un traitement par ultra-haute température (UHT) à une température d'au moins 135 °C, maintenue pendant une durée appropriée.
Article 5
Certificats
Les lots autorisés pour l’importation conformément aux articles 2, 3 et 4 sont accompagnés d’un certificat sanitaire établi pour le produit concerné conformément au modèle adéquat fourni à l’annexe II, partie 2. Ce certificat sanitaire est complété suivant les notes explicatives figurant dans la partie 1 de ladite annexe.
Toutefois, les dispositions du présent article n'excluent pas la possibilité de recourir à la certification électronique ou à d'autres systèmes agréés et harmonisés au niveau de l’Union européenne.
Article 6
Conditions de transit et d’entreposage
L’introduction dans l’Union européenne de lots de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum non destinés à être importés dans l’Union mais destinés à un pays tiers, soit après un transit direct par l’Union européenne, soit après un entreposage sur le territoire de celle-ci, conformément aux articles 11, 12 et 13 de la directive 97/78/CE, n’est autorisée que si les lots remplissent les conditions suivantes:
a) ils proviennent d’un pays tiers ou d’une partie de pays tiers répertoriés dans l’annexe I en provenance desquels l’introduction dans l’Union européenne de lots de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum est autorisée et ils respectent les conditions relatives au traitement thermique applicables à ce type de lots, telles qu’elles sont prévues aux articles 2, 3 et 4;
b) ils remplissent les conditions spécifiques de police sanitaire applicables aux importations dans l’Union européenne du lait cru, de produits laitiers, de colostrum ou de produits à base de colostrum concernés, telles qu’elles sont exposées dans l’attestation de santé animale figurant dans la section II.1 du modèle de certificat approprié, fourni à l’annexe II, partie 2;
c) ils sont accompagnés d’un certificat sanitaire établi pour le lot concerné suivant le modèle adéquat fourni à l’annexe II, partie 3. Ce certificat sanitaire est complété conformément aux notes explicatives figurant dans la partie 1 de ladite annexe;
d) ils sont certifiés acceptables pour le transit, y compris, le cas échéant, pour l’entreposage, dans le document vétérinaire commun d’entrée visé à l’article 2, paragraphe 1, du règlement (CE) no 136/2004 et signé par le vétérinaire officiel du poste d’inspection frontalier d’introduction dans l’Union européenne.
Article 7
Dérogation relative aux conditions de transit et d'entreposage
1. Par dérogation aux dispositions de l’article 6, le transit routier ou ferroviaire par l’Union européenne de lots acheminés en provenance ou à destination de la Russie, directement ou via un autre pays tiers, est autorisé entre les postes d’inspection frontaliers de Lettonie, de Lituanie et de Pologne mentionnés dans la décision 2009/821/CE de la Commission ( 17 ), lorsque les conditions suivantes sont remplies:
a) le lot est scellé par les services vétérinaires de l'autorité compétente au poste d'inspection frontalier d'introduction dans l’Union européenne, au moyen d'un cachet portant un numéro d'ordre;
b) les documents accompagnant le lot visés à l'article 7 de la directive 97/78/CE sont marqués sur chaque page, par le vétérinaire officiel de l'autorité compétente responsable du poste d'inspection frontalier d’introduction dans l’Union européenne, d'un cachet portant la mention «UNIQUEMENT POUR TRANSIT PAR L’UE À DESTINATION DE LA RUSSIE»;
c) les exigences procédurales prévues à l’article 11 de la directive 97/78/CE sont respectées;
d) le vétérinaire officiel du poste d'inspection frontalier d'introduction dans l’Union européenne a certifié que le lot était acceptable pour le transit sur le document vétérinaire commun d'entrée.
2. Le déchargement ou l’entreposage de tels lots sur le territoire de l’Union européenne, au sens de l'article 12, paragraphe 4, ou de l'article 13 de la directive 97/78/CE, ne sont pas autorisés.
3. L'autorité compétente effectue régulièrement des contrôles afin de vérifier que le nombre de lots et les quantités de produits quittant le territoire de l’Union européenne correspondent au nombre et aux quantités qui y ont été introduites.
Article 7 bis
Dérogation pour le transit par la Croatie de lots en provenance de Bosnie-Herzégovine destinés à des pays tiers
1. Par dérogation à l’article 6, le transit routier direct par l’Union, entre les postes d’inspection frontaliers de Nova Sela et de Ploče, de lots en provenance de Bosnie-Herzégovine à destination de pays tiers est autorisé si les conditions suivantes sont remplies:
a) le lot est scellé par le vétérinaire officiel au poste d’inspection frontalier d’entrée au moyen d’un sceau portant un numéro d’ordre;
b) les documents accompagnant le lot, visés à l’article 7 de la directive 97/78/CE, portent, sur chaque page, la mention «UNIQUEMENT POUR TRANSIT PAR L’Union européenne À DESTINATION DE PAYS TIERS», apposée au moyen d’un cachet par le vétérinaire officiel au poste d’inspection frontalier d’entrée;
c) les exigences procédurales prévues à l’article 11 de la directive 97/78/CE sont respectées;
d) le vétérinaire officiel du poste d’inspection frontalier d’entrée a certifié que le lot était acceptable pour le transit sur le document vétérinaire commun d’entrée prévu à l’article 2, paragraphe 1, du règlement (CE) no 136/2004.
2. Le déchargement et l’entreposage de ces lots, au sens de l’article 12, paragraphe 4, ou de l’article 13 de la directive 97/78/CE, ne sont pas autorisés sur le territoire de l’Union.
3. L’autorité compétente effectue régulièrement des contrôles afin de vérifier que le nombre de lots et les quantités de produits quittant le territoire de l’Union correspondent au nombre et aux quantités qui y ont été introduites.
Article 8
Traitements spécifiques
Les lots de produits laitiers et de produits à base de colostrum dont l’introduction dans l’Union européenne est autorisée conformément aux articles 2, 3, 4, 6 ou 7 et qui proviennent de pays tiers ou de parties de pays tiers dans lesquels un foyer de fièvre aphteuse est apparu au cours des douze mois précédant la date de délivrance du certificat sanitaire ou dans lesquels une campagne de vaccination a été menée contre cette maladie au cours de cette période ne sont effectivement autorisés sur le territoire de l’Union européenne que si ces produits ont subi un des traitements visés à l’article 4.
Article 9
Abrogation
La décision 2004/438/CE est abrogée.
Toute référence à la décision 2004/438/CE s’entend comme une référence au présent règlement.
Article 10
Dispositions transitoires
Pendant une période transitoire allant jusqu’au 30 novembre 2010, les lots de lait cru et de produits à base de lait visés dans la décision 2004/438/CE pour lesquels des certificats sanitaires adéquats ont été délivrés conformément à la décision 2004/438/CE peuvent continuer à être introduits sur le territoire de l’Union européenne.
Article 11
Entrée en vigueur et applicabilité
Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l'Union européenne.
Il s’applique à compter du 1er août 2010.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
ANNEXE I
Liste des pays tiers ou parties de pays tiers à partir desquels l’introduction dans l’Union européenne de lots de lait cru, de produits laitiers, de colostrum (1) et de produits à base de colostrum (1) est autorisée et indiquant le type de traitement thermique requis pour ces denrées
|
Code ISO du pays tiers |
Pays tiers ou partie de pays tiers |
Colonne A |
Colonne B |
Colonne C |
|
AE |
Émirat de Dubaï des Émirats arabes unis (5) |
0 |
0 |
+ (6) |
|
AD |
Andorre |
+ |
+ |
+ |
|
AL |
Albanie |
0 |
0 |
+ |
|
AR |
Argentine |
0 |
0 |
+ |
|
AU |
Australie |
+ |
+ |
+ |
|
BR |
Brésil |
0 |
0 |
+ |
|
BW |
Botswana |
0 |
0 |
+ |
|
BY |
Biélorussie |
0 |
0 |
+ |
|
BZ |
Belize |
0 |
0 |
+ |
|
BA |
Bosnie-Herzégovine |
0 |
0 |
+ |
|
CA |
Canada |
+ |
+ |
+ |
|
CH |
Suisse (2) |
+ |
+ |
+ |
|
CL |
Chili |
0 |
+ |
+ |
|
CN |
Chine |
0 |
0 |
+ |
|
CO |
Colombie |
0 |
0 |
+ |
|
CR |
Costa Rica |
0 |
0 |
+ |
|
CU |
Cuba |
0 |
0 |
+ |
|
DZ |
Algérie |
0 |
0 |
+ |
|
ET |
Éthiopie |
0 |
0 |
+ |
|
GL |
Groenland |
0 |
+ |
+ |
|
GT |
Guatemala |
0 |
0 |
+ |
|
HK |
Hong Kong |
0 |
0 |
+ |
|
HN |
Honduras |
0 |
0 |
+ |
|
IL |
Israël |
0 |
0 |
+ |
|
IN |
Inde |
0 |
0 |
+ |
|
IS |
Islande |
+ |
+ |
+ |
|
KE |
Kenya |
0 |
0 |
+ |
|
MA |
Maroc |
0 |
0 |
+ |
|
MG |
Madagascar |
0 |
0 |
+ |
|
MK (3) |
Ancienne République yougoslave de Macédoine |
0 |
+ |
+ |
|
MR |
Mauritanie |
0 |
0 |
+ |
|
MU |
Maurice |
0 |
0 |
+ |
|
MX |
Mexique |
0 |
0 |
+ |
|
NA |
Namibie |
0 |
0 |
+ |
|
NI |
Nicaragua |
0 |
0 |
+ |
|
NZ |
Nouvelle-Zélande |
+ |
+ |
+ |
|
PA |
Panama |
0 |
0 |
+ |
|
PY |
Paraguay |
0 |
0 |
+ |
|
RS (4) |
Serbie |
0 |
+ |
+ |
|
RU |
Russie |
0 |
0 |
+ |
|
SG |
Singapour |
0 |
0 |
+ |
|
SV |
El Salvador |
0 |
0 |
+ |
|
SZ |
Swaziland |
0 |
0 |
+ |
|
TH |
Thaïlande |
0 |
0 |
+ |
|
TN |
Tunisie |
0 |
0 |
+ |
|
TR |
Turquie |
0 |
0 |
+ |
|
UA |
Ukraine |
0 |
0 |
+ |
|
US |
États-Unis |
+ |
+ |
+ |
|
UY |
Uruguay |
0 |
0 |
+ |
|
ZA |
Afrique du Sud |
0 |
0 |
+ |
|
ZW |
Zimbabwe |
0 |
0 |
+ |
|
(1) Le colostrum et les produits à base de colostrum ne peuvent être introduits dans l’Union européenne qu’en provenance de pays autorisés dans la colonne A. (2) Certificats prévus par l’accord entre la Communauté européenne et la Confédération suisse relatif aux échanges de produits agricoles (JO L 114 du 30.4.2002, p. 132). (3) Ancienne République yougoslave de Macédoine: la nomenclature définitive pour ce pays sera adoptée après la conclusion des négociations actuellement en cours à cet égard aux Nations unies. (4) N’inclut pas le Kosovo, actuellement sous administration internationale suite à la résolution no 1244 du Conseil de sécurité des Nations unies du 10 juin 1999. (5) Uniquement les produits laitiers dérivés du lait de chamelles de l’espèce Camelus dromedarius. (6) Les produits laitiers dérivés du lait de chamelles de l’espèce Camelus dromedarius sont autorisés. |
||||
ANNEXE II
PARTIE 1
Modèles de certificats sanitaires
|
«Milk-RM» |
: |
certificat sanitaire pour le lait cru provenant des pays tiers ou des parties de pays tiers autorisés conformément à la colonne A de l’annexe I et destiné à être transformé dans l’Union européenne avant son utilisation pour la consommation humaine. |
|
«Milk-RMP» |
: |
certificat sanitaire pour les produits laitiers dérivés du lait cru qui proviennent des pays tiers ou des parties de pays tiers autorisés conformément à la colonne A de l’annexe I et destinés à être importés dans l’Union européenne en vue de la consommation humaine. |
|
«Milk-HTB» |
: |
certificat sanitaire pour les produits laitiers dérivés de lait de vaches, de brebis, de chèvres et de bufflonnes destinés à être importés dans l’Union européenne en vue de la consommation humaine, en provenance des pays tiers ou des parties de pays tiers autorisés conformément à la colonne B de l’annexe I. |
|
«Milk-HTC» |
: |
certificat sanitaire pour les produits laitiers destinés à être importés dans l’Union européenne en vue de la consommation humaine, en provenance des pays tiers ou des parties de pays tiers autorisés conformément à la colonne C de l’annexe I. |
|
«Colostrum-C/CPB» |
: |
certificat sanitaire pour le colostrum de vaches, de brebis, de chèvres et de bufflonnes et les produits dérivés de colostrum des mêmes espèces destinés à être importés dans l’Union européenne en vue de la consommation humaine, en provenance des pays tiers ou des parties de pays tiers autorisés conformément à la colonne A de l’annexe I. |
|
«Milk/ Colostrum-T/S» |
: |
certificat de police sanitaire pour le lait cru, le colostrum, les produits laitiers ou les produits à base de colostrum destinés à la consommation humaine après un transit ou un entreposage dans l’Union européenne. |
Notes explicatives
a) Les certificats sanitaires doivent être établis par les autorités compétentes du pays tiers d'origine, conformément au modèle approprié fourni dans la partie 2 de la présente annexe, suivant la présentation du modèle qui correspond au lait cru, au colostrum, aux produits laitiers ou aux produits à base de colostrum concernés. Ils contiennent, numérotées dans l'ordre indiqué dans le modèle, les attestations exigées pour tous les pays tiers et, le cas échéant, les garanties supplémentaires requises pour le pays tiers exportateur concerné.
b) L’original du certificat sanitaire se compose d’une seule feuille, imprimée recto verso; si l’espace disponible ne suffit pas, le certificat est présenté de façon à ce que toutes ses pages forment un tout indivisible.
c) Un certificat sanitaire distinct doit être présenté pour chacun des lots du produit concerné exportés à destination du même lieu en provenance d’un pays tiers figurant dans le tableau de l’annexe I et transportés dans le même wagon, véhicule routier, avion ou bateau.
d) L’original du certificat sanitaire et les étiquettes visées dans le modèle de certificat sont établis dans au moins une des langues officielles de l’État membre effectuant l’inspection aux frontières et de l’État membre de destination. Néanmoins, ces États membres peuvent autoriser qu'ils soient établis dans une autre langue officielle de l’Union européenne et accompagnés, si nécessaire, d'une traduction officielle.
e) Si des pages supplémentaires sont jointes au certificat sanitaire pour les besoins de l’identification des produits composant le lot, ces pages sont également considérées comme faisant partie du certificat original, pour autant que la signature et le cachet du vétérinaire officiel chargé de la certification figurent sur chacune d’elles.
f) Lorsque le certificat sanitaire comporte plus d’une page, chacune d’elles est numérotée comme suit dans sa partie inférieure: «–x (numéro de la page) sur y (nombre total de pages)–», le numéro de référence du certificat attribué par l’autorité compétente figurant en haut de page.
g) Le certificat sanitaire original doit être complété et signé par le représentant de l’autorité compétente responsable de vérifier et de certifier la conformité du lait cru, du colostrum, des produits laitiers ou des produits à base de colostrum avec les exigences sanitaires définies à l’annexe III, section IX, chapitre I, du règlement (CE) no 853/2004 ainsi que dans la directive 2002/99/CE.
h) Les autorités compétentes du pays tiers exportateur garantissent l'application de principes de certification équivalents à ceux établis dans la directive 96/93/CE du Conseil ( 18 ).
i) La couleur de la signature du vétérinaire officiel doit être différente de celle du texte imprimé sur le certificat sanitaire. Cette exigence s'applique également aux cachets, à l'exception des reliefs et des filigranes.
j) Le certificat sanitaire original doit accompagner le lot jusqu’au poste d’inspection frontalier d’introduction dans l’Union européenne.
k) Lorsque le modèle de certificat indique de choisir la mention qui convient, les mentions non pertinentes peuvent être biffées et paraphées, puis estampillées par le certificateur ou totalement effacées du certificat.
PARTIE 2
Modèle Milk-RM
Certificat sanitaire pour le lait cru provenant des pays tiers ou des parties de pays tiers autorisés conformément à la colonne A de l’annexe I du règlement (UE) no 605/2010 et destiné à être transformé dans l’Union européenne avant son utilisation pour la consommation humaine



Modèle Milk-RMP
Certificat sanitaire pour les produits laitiers dérivés du lait cru qui proviennent des pays tiers ou des parties de pays tiers autorisés conformément à la colonne A de l’annexe I du règlement (UE) no 605/2010 et qui sont destinés à être importés dans l’Union européenne en vue de la consommation humaine



Modèle Milk-HTB
Certificat sanitaire pour les produits laitiers dérivés de lait de vaches, de brebis, de chèvres et de bufflonnes destinés à être importés dans l’Union européenne en vue de la consommation humaine, en provenance des pays tiers ou des parties de pays tiers autorisés conformément à la colonne B de l’annexe I du règlement (UE) no 605/2010
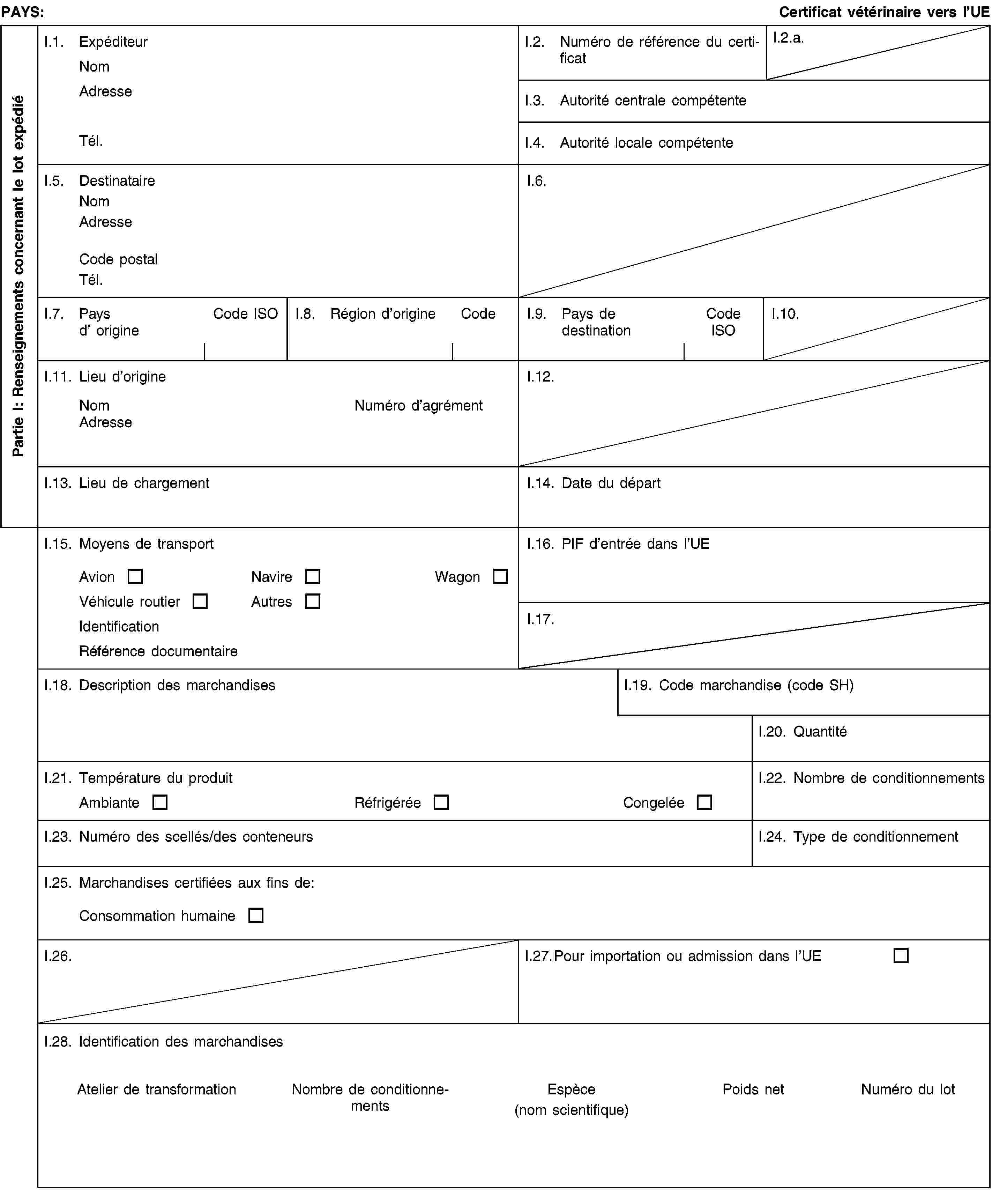


Modèle Milk-HTC
Certificat sanitaire pour les produits laitiers destinés à être importés dans l’Union européenne en vue de la consommation humaine, en provenance des pays tiers ou des parties de pays tiers autorisés conformément à la colonne C de l’annexe I du règlement (UE) no 605/2010

 soit [ii) un traitement par ultra-haute température (UHT) à une température d’au moins 135 °C, maintenue pendant une durée appropriée,](1) soit [iii) pour le lait dont le pH est égal ou supérieur à 7,0, une pasteurisation ultra-rapide à haute température (HTST) pendant 15 secondes à 72 °C, effectuée à deux reprises, garantissant, le cas échéant, une réaction négative au test de la phosphatase alcaline, réalisé immédiatement après le traitement thermique,](1) soit [iv) un traitement dont l’effet de pasteurisation est équivalent à celui du point iii) et garantissant, le cas échéant, une réaction négative au test de la phosphatase alcaline, réalisé immédiatement après le traitement thermique,](1) soit [v) un traitement HTST simple du lait présentant un pH inférieur à 7,0,](1) soit [vi) a un traitement HTST associé à un autre traitement physique:(1) soit [(1) un abaissement du pH en dessous de 6 pendant une heure,](1) soit [(2) une exposition additionnelle à une température égale ou supérieure à 72 °C, combinée avec une dessiccation;]](1) ou [(b) proviennent de lait cru d’animaux autres que des vaches, des brebis, des chèvres, des buflonnes ou des chamelles de l’espèce Camelus dromedarius et ont subi, préalablement à leur importation sur le territoire de l’Union européenne:(1) soit [i) un processus de stérilisation permettant d’atteindre une valeur F0 égale ou supérieure à 3,](1) soit [ii) un traitement par ultra-haute température (UHT) à une température d’au moins 135 °C, maintenue pendant une durée appropriée.]]II.2. Attestation de santé publiqueJe soussigné, inspecteur officiel, déclare avoir connaissance des dispositions applicables des règlements (CE) no 178/2002, (CE) no 852/2004, (CE) no 853/2004 et (CE) no 854/2004 et certifie que les produits laitiers décrits ci-dessus ont été produits conformément à ces dispositions, et en particulier:a) qu’ils ont été fabriqués avec du lait cru:i) qui provient d’exploitations enregistrées conformément au règlement (CE) no 852/2004 et contrôlées conformément aux dispositions de l’annexe IV du règlement (CE) no 854/2004,ii) qui a été produit, collecté, refroidi, entreposé et transporté dans le respect des conditions d’hygiène fixées à l’annexe III, section IX, chapitre I, du règlement (CE) no 853/2004,iii) qui respecte les critères relatifs à la teneur en germes et en cellules somatiques fixés à l’annexe III, section IX, chapitre I, du règlement (CE) no 853/2004,iv) qui respecte les garanties sur l’état du lait cru en ce qui concerne les résidus, prévues par les plans de surveillance pour la recherche des résidus ou des substances conformément à la directive 96/23/CE du Conseil, et notamment son article 29,](./../../../resource.html?uri=celex:02010R0605-20140326.FRA.xhtml.L_2013090FR.01007501.tif.jpg)




PARTIE 3

![Partie II: certificationPAYSModèle Milk/Colostrum-T/SLait cru, produits laitiers, colostrum ou produits à base de colostrum destinés à la consommation humaine après un transit ou un entreposageII. Renseignements sanitairesII.a. Numéro de référence du certificatII.b.II.1 Attestation de santé animaleJe soussigné, vétérinaire officiel, certifie que [le lait cru]/[les produits laitiers]/[le colostrum]/[les produits à base de colostrum] (1) (2) fdécrit(s) dans la partie I et destiné(s) [au transit par]/[à un entreposage dans] (2) l’Union européenne:a) provient (proviennent) d’un pays, ou d’une partie de pays, en provenance duquel les importations de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum sont autorisées dans l’Union européenne, conformément à l’annexe I du règlement (UE) no 605/2010;b) répond (répondent) aux conditions de police sanitaire applicables aux produits considérés, telles qu’elles sont fixées dans l’attestation de santé animale figurant dans la section II.1 du modèle de certificat [Milk-RM]/[Milk-RMP]/[Milk-HTB]/[Milk-HTC]/[Colostrum-C/CBP] (2) établi à l’annexe II, partie 2, du règlement (UE) no 605/2010;c) a (ont) été produit(s) le … (3) ou entre le … (3) et le … (3).NotesPartie I:Rubrique I.7: indiquer le nom et le code ISO du pays ou de la partie du pays tels qu’ils figurent à l’annexe I du règlement (UE) no 605/2010 du 2 juillet 2010 arrêtant les conditions sanitaires et de police sanitaire ainsi que les exigences en matière de certification vétérinaire pour l’introduction dans l’Union européenne de lait cru et de produits laitiers destinés à la consommation humaine (JO L 175 du 10.7.2010, p. 1).Rubrique I.11: nom, adresse et numéro d’agrément de l’établissement d’expédition. Le nom du pays d’origine doit être le même que celui du pays exportateur.Rubrique I.15: numéro d’immatriculation (wagons ou conteneurs et véhicules routiers), numéro de vol (avions) ou nom (navires). En cas de transport en conteneurs, indiquer le nombre total de conteneurs, leur numéro d’enregistrement et, le cas échéant, celui des scellés dans la case I.23. En cas de déchargement et de rechargement, l’expéditeur doit en informer le poste d’inspection frontalier d’introduction dans l’Union européenne.Rubrique I.19: utiliser le code approprié du système harmonisé (SH) sous les rubriques suivantes: 04.01, 04.02, 04.03, 04.04, 04.05, 04.06, 15.17, 17.02, 19.01, 21.05, 21.06, 22.02; 28.35, 30.01, 35.01, 35.02, 35.04 ou 04.10.Rubrique I.20: indiquer le poids brut total et le poids net total.Rubrique I.23: pour les conteneurs ou les boîtes, il convient d’indiquer le numéro du conteneur et, le cas échéant, celui des scellés.Rubrique I.28: atelier de fabrication: indiquer le numéro d’agrément de l’exploitation (ou des exploitations) de production, du centre de collecte ou du centre de standardisation agréé pour l’exportation vers l’Union européenne.Partie II:(1) Par “lait cru”, “produits laitiers”, “colostrum” ou “produits à base de colostrum”, on entend le lait cru, les produits laitiers, le colostrum et les produits à base de colostrum destinés à la consommation humaine qui sont en transit ou sont entreposés conformément à l'article 12, paragraphe 4, ou à l'article 13 de la directive 97/78/CE du Conseil du 18 décembre 1997 fixant les principes relatifs à l'organisation des contrôles vétérinaires pour les produits en provenance des pays tiers introduits dans la Communauté (JO L 24 du 30.1.1998, p. 9).(2) Choisir la mention qui convient.(3) Date(s) de production. Les importations de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum ne sont pas autorisées lorsque ce lait ou ces produits laitiers ou ce colostrum ou ces produits à base de colostrum ont été obtenus soit avant la date d'autorisation d'exportation vers l’Union européenne du pays tiers, ou de la partie de pays tiers, mentionné aux rubriques I.7 et I.8, soit à une période pendant laquelle l’Union européenne a adopté des mesures restrictives à l'importation de lait cru, de produits laitiers, de colostrum et de produits à base de colostrum provenant de ce pays tiers ou de cette partie de pays tiers.La couleur de la signature doit être différente de celle du texte imprimé. Cette règle vaut également pour les cachets, à l'exception des reliefs et des filigranes.](./../../../resource.html?uri=celex:02010R0605-20140326.FRA.xhtml.L_2014066FR.01002201.tif.jpg)

( 1 ) JO L 18 du 23.1.2003, p. 11.
( 2 ) JO L 139 du 30.4.2004, p. 1.
( 3 ) JO L 139 du 30.4.2004, p. 55.
( 4 ) JO L 139 du 30.4.2004, p. 206.
( 5 ) JO L 165 du 30.4.2004, p. 206.
( 6 ) JO L 268 du 14.9.1992, p. 1.
( 7 ) JO L 154 du 30.4.2004, p. 72.
( 8 ) JO L 157 du 30.4.2004, p. 33.
( 9 ) JO L 31 du 1.2.2002, p. 1.
( 10 ) JO L 338 du 22.12.2005, p. 1.
( 11 ) JO L 152 du 16.6.2009, p. 11.
( 12 ) JO L 15 du 20.1.2010, p. 1.
( 13 ) JO L 125 du 23.5.1996, p. 10.
( 14 ) JO L 13 du 16.1.1997, p. 28.
( 15 ) JO L 224 du 18.8.1990, p. 29.
( 16 ) JO L 24 du 30.1.1998, p. 9.
( 17 ) JO L 296 du 12.11.2009, p. 1.
( 18 ) JO L 13 du 16.1.1997, p. 28.


