EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 01988L0407-20111101
Council Directive of 14 June 1988 laying down the animal health requirements applicable to intra-Community trade in and imports of deep-frozen semen of domestic animals of the bovine species (88/407/EEC)
Consolidated text: Neuvoston direktiivi , annettu 14 päivänä kesäkuuta 1988 , eläinten terveyttä koskevista vaatimuksista yhteisön sisäisessä naudansukuisten kotieläinten pakastetun siemennesteen kaupassa ja tuonnissa (88/407/ETY)
Neuvoston direktiivi , annettu 14 päivänä kesäkuuta 1988 , eläinten terveyttä koskevista vaatimuksista yhteisön sisäisessä naudansukuisten kotieläinten pakastetun siemennesteen kaupassa ja tuonnissa (88/407/ETY)
 No longer in force
No longer in force
1988L0407 — FI — 01.11.2011 — 011.001
Tämä asiakirja on ainoastaan dokumentointitarkoituksiin. Toimielimet eivät vastaa sen sisällöstä.
|
NEUVOSTON DIREKTIIVI, annettu 14 päivänä kesäkuuta 1988, eläinten terveyttä koskevista vaatimuksista yhteisön sisäisessä naudansukuisten kotieläinten ►M3 ————— ◄ siemennesteen kaupassa ja tuonnissa (EYV L 194, 22.7.1988, p.10) |
Muutettu:
|
|
|
Virallinen lehti |
||
|
No |
page |
date |
||
|
NEUVOSTON DIREKTIIVI, 90/120/ETY annettu 5 päivänä maaliskuuta 1990, |
L 71 |
37 |
17.3.1990 |
|
|
NEUVOSTON DIREKTIIVI, 90/425/ETY annettu 26 päivänä kesäkuuta 1990, |
L 224 |
29 |
18.8.1990 |
|
|
NEUVOSTON DIREKTIIVI 93/60/ETY, annettu 30 päivänä kesäkuuta 1993, |
L 186 |
28 |
28.7.1993 |
|
|
NEUVOSTON ASETUS (EY) N:o 806/2003, annettu 14 päivänä huhtikuuta 2003, |
L 122 |
1 |
16.5.2003 |
|
|
NEUVOSTON DIREKTIIVI 2003/43/EY, annettu 26 päivänä toukokuuta 2003, |
L 143 |
23 |
11.6.2003 |
|
|
L 30 |
15 |
4.2.2004 |
||
|
L 11 |
21 |
17.1.2006 |
||
|
L 42 |
63 |
16.2.2008 |
||
|
L 219 |
40 |
14.8.2008 |
||
|
KOMISSION TÄYTÄNTÖÖNPANOPÄÄTÖS, annettu 20 päivänä syyskuuta 2011, |
L 247 |
22 |
24.9.2011 |
|
Muutettu:
|
C 241 |
21 |
29.8.1994 |
||
|
|
L 001 |
1 |
.. |
NEUVOSTON DIREKTIIVI,
annettu 14 päivänä kesäkuuta 1988,
eläinten terveyttä koskevista vaatimuksista yhteisön sisäisessä naudansukuisten kotieläinten ►M3 ————— ◄ siemennesteen kaupassa ja tuonnissa
(88/407/ETY)
EUROOPAN YHTEISÖJEN NEUVOSTO, joka
ottaa huomioon Euroopan talousyhteisön perustamissopimuksen ja erityisesti sen 43 artiklan,
ottaa huomioon komission ehdotuksen ( 1 ),
ottaa huomioon Euroopan parlamentin lausunnon ( 2 ),
ottaa huomioon talous- ja sosiaalikomitean lausunnon ( 3 ),
sekä katsoo, ettäsäännökset eläinten terveyteen liittyvistä ongelmista yhteisön sisäisessä nautaeläinten ja sikojen kaupassa sisältyvät direktiiviin 64/432/ETY ( 4 ), sellaisena kuin se on viimeksi muutettuna asetuksella (ETY) N:o 3768/85 ( 5 ); direktiivi 72/462/ETY ( 6 ), sellaisena kuin se on viimeksi muutettuna asetuksella (ETY) N:o 3768/85, sisältää lisäksi säännökset terveyttä koskevista ongelmista nautaeläinten ja sikojen tuonnissa kolmansista maista,
edellä mainituin säännöksin on yhteisön nautaeläinten ja sikojen yhteisön sisäisessä kaupassa ja niiden tuonnissa kolmansista maista huolehdittu siitä, että alkuperämaa takaa eläinten terveyttä koskevien periaatteiden noudattamisen, joten eläintautien leviämisen vaara on käytännöllisesti katsoen poistunut; tietty eläintautien leviämisen vaara siemennesteen kauppaan kuitenkin liittyy,
yhteisön sisäistä eläin- ja eläintuotekauppaa sääntelevien eläinten terveyttä koskevien kansallisten säännösten yhdenmukaistamista koskevassa yhteisön toimintaperiaatteissa on vastedes tarpeen aikaansaada yhdenmukainen järjestelmä sovellettavaksi nautojen siemennesteen yhteisön sisäisessä kaupassa ja sen tuonnissa yhteisön alueelle,
yhteisön sisäisessä siemennesteen kaupassa jäsenvaltio, jonka alueella siemenneste kerätään, on velvollinen huolehtimaan siitä, että siemenneste on kerätty ja käsitelty hyväksytyillä ja valvotuilla keinosiemennysasemilla, että luovuttajaeläinten terveydentila on sellainen kuin eläintautien leviämisvaaran torjumiseksi on edellytettävä, että siemennesteen terveydellisen tason turvaamiseksi annettuja määräyksiä on noudatettu sen keräyksessä, käsittelyssä, säilytyksessä ja kuljetuksessa ja että mukana on terveystodistus osoituksena näiden takeiden täyttämisestä, kun sitä kuljetetaan määrämaahan,
tiettyjä tauteja koskevien rokotuskäytäntöjen eroavuudet yhteisössä antavat aiheen pitää voimassa määräaikaisia poikkeuksia, joilla annetaan jäsenvaltioille tiettyjen tautien osalta oikeus vaatia lisäsuojaa näitä tauteja vastaan,
kolmansista maista yhteisön alueelle tapahtuvaa siemennesteen tuontia varten on syytä luetteloida kolmannet maat terveysvaatimusten mukaan; jäsenvaltiot saisivat sallia vain sellaisen siemennesteen maahantuonnin, joka on peräisin tietyt vaatimukset täyttäviltä ja virallisesti valvotuilta keinosiemennysasemilta, sanotun kuitenkaan rajoittamatta tämän luettelon käyttämistä; on lisäksi tarpeen luettelossa mainittujen maiden osalta määritellä olosuhteiden mukaiset erityiset terveysvaatimukset ja vaatimusten noudattaminen voidaan tarkastaa paikalla suoritettavin tarkastuksin,
on tarpeen aikaansaada menettelytapa jäsenvaltioiden välille mahdollisesti syntyvien erimielisyyksien sopimiseksi siitä, onko jonkin keinosiemennysaseman hyväksyminen perusteltua,
jäsenvaltiot voivat kieltäytyä vastaanottamasta siemennestelähetystä, jos osoitetaan, ettei se vastaa tämän direktiivin säännöksiä; tällainen siemenneste on voitava palauttaa, jos sille ei ole eläinten terveyteen perustuvia esteitä ja jos lähettäjä tai tämän edustaja sitä pyytää; lähettäjällä tai tämän edustajalla on oltava mahdollisuus saada tieto kiellon tai rajoituksen perusteista sekä hankkia asiantuntijan lausunto,
tiettyjen tartuntatautien leviämisen estämiseksi on tarpeen suorittaa tuontitarkastuksia siemennestelähetyksen saapuessa yhteisön alueelle, paitsi jos kyseessä on ulkoinen kauttakuljetus,
sisäistä kauttakuljetusta varten on määriteltävä toimenpiteet, jotka jäsenvaltioiden on kyseisten tarkastusten jälkeen toteutettava,
on tarpeen sallia jäsenvaltion ryhtyä kiireellisiin suojatoimenpiteisiin, jos toisessa jäsenvaltiossa tai kolmannessa maassa puhkeaa tarttuva tauti; tällaiseen tautiin liittyvät vaarat ja niiden edellyttämät suojatoimenpiteet on arvioitava samalla tavoin koko yhteisön alueella; tätä tarkastusta varten on tarpeen, että pysyvä eläinlääkintäkomitea laatii koko yhteisöä koskevan kiireellisen menettelyn, jota noudattaen tarvittavat toimenpiteet on annettava,
on tarpeen antaa komission tehtäväksi toteuttaa tietyt toimenpiteet tämän direktiivin täytäntöön panemiseksi; tätä varten on tarpeen säätää menettelystä komission ja jäsenvaltioiden välisen tiiviin ja tehokkaan yhteistyön aikaansaamiseksi pysyvässä eläinlääkintäkomiteassa, ja
tämä direktiivi ei vaikuta sellaisen siemennesteen kauppaan, joka on tuotettu ennen ajankohtaa, jolloin jäsenvaltioiden on noudatettava tätä direktiiviä,
ON ANTANUT TÄMÄN DIREKTIIVIN:
I LUKU
Yleiset säännökset
1 artikla
Tässä direktiivissä säädetään eläinten terveyttä koskevista vaatimuksista, joita sovelletaan yhteisön sisäiseen nautaeläinten ►M3 ————— ◄ siemennesteen kauppaan ja tuontiin kolmansista maista.
Tämä direktiivi ei vaikuta yhteisön ja/tai kansallisiin eläinjalostusalan säännöksiin, joilla säännellään yleisesti keinosiemennyksen järjestämistä ja erityisesti siemennesteen jakelua.
2 artikla
Tässä direktiivissä sovelletaan tarvittaessa direktiivin 64/432/ETY 2 artiklassa ja direktiivin 72/462/ETY 2 artiklassa olevia määritelmiä.
Lisäksi tarkoitetaan:
a) ”siemennesteellä” naudansukuisten kotieläimen käsiteltyä tai laimennettua siemennestettä;
— ”keinosiemennysasemalla” jäsenvaltion tai kolmannen maan alueella sijaitsevaa, virallisesti hyväksyttyä ja virallisesti valvottua laitosta, jossa tuotetaan siemennestettä keinosiemennystarkoituksiin,
— ”siemennesteen varastointiasemalla” jäsenvaltion tai kolmannen maan alueella sijaitsevaa, virallisesti hyväksyttyä ja virallisesti valvottua laitosta, jossa siemennestettä varastoidaan keinosiemennystarkoituksiin;
c) ”virkaeläinlääkärillä” jäsenvaltion tai kolmannen maan toimivaltaisen keskusviranomaisen nimeämää eläinlääkäriä;
d) ”asemaeläinlääkärillä” eläinlääkäriä, joka vastaa tässä direktiivissä säädettyjen vaatimusten noudattamisesta keinosiemennysaseman päivittäisessä toiminnassa;
e) ”siemennestelähetyksellä” yhden todistuksen kattamaa siemennestemäärää;
f) ”keräilymaalla” sitä jäsenvaltiota tai kolmatta maata, jossa siemenneste kerätään ja josta se lähetetään johonkin jäsenvaltioon;
g) ”hyväksytyllä laboratoriolla” jäsenvaltion tai kolmannen maan alueella sijaitsevaa laboratoriota, jonka toimivaltainen eläinlääkintäviranomainen on nimennyt suorittamaan tässä direktiivissä säädettyjä tutkimuksia;
h) ”keräyserällä” yhdeltä luovuttajaeläimeltä yhdellä kertaa saatua siemennestettä.
II LUKU
Yhteisön sisäinen kauppa
3 artikla
Jokaisen jäsenvaltion on huolehdittava, että ainoastaan seuraavat yleiset vaatimukset täyttävää siemennestettä lähetetään sen alueelta toisen jäsenvaltion alueelle:
a) siemenneste on kerätty ja käsitelty ja/tai varastoitu tapauksesta riippuen 5 artiklan 1 kohdan mukaisesti tähän tarkoitukseen hyväksytyllä keinosiemennys- tai varastointiasemalla tai -asemilla keinosiemennystä ja yhteisön sisäistä kauppaa varten;
b) siemenneste on kerätty naudansukuisilta kotieläimiltä, joiden terveydentila täyttää liitteen B vaatimukset;
c) siemennesteen keräys, käsittely, varastointi ja kuljetus on tapahtunut liitteiden A ja C mukaisesti;
d) kuljetuksen aikana määrämaahan saakka siemennesteen mukana on 6 artiklan 1 kohdan mukainen terveystodistus.
4 artikla
▼M5 —————
3 Jäsenvaltiot eivät saa estää suu- ja sorkkatautia vastaan rokotettujen sonnien siemennesteen tuontia maahan. Jos siemenneste on kuitenkin peräisin sonnilta, joka on rokotettu suu- ja sorkkatautia vastaan keräystä edeltävien 12 kuukauden aikana, 5 prosenttia (vähintään viisi olkea) kustakin toiseen jäsenvaltioon aiotusta keräyserästä on tutkittava suu- ja sorkkatautiviruksen eristyskokeella määrämaana olevassa jäsenvaltiossa sijaitsevassa tai sen nimeämässä laboratoriossa negatiivisin tuloksin.
5 artikla
1 Jäsenvaltion, jonka alueella ►M5 keinosiemennysasema tai siemennesteen varastointiasema ◄ sijaitsee, on huolehdittava, että 3 artiklan a alakohdassa tarkoitettu hyväksyntä annetaan vain, jos liitteen A vaatimukset täyttyvät ja jos ►M5 keinosiemennysasemalla tai siemennesteen varastointiasemalla ◄ on edellytykset noudattaa tämän direktiivin muita säännöksiä.
Jäsenvaltion on myös huolehdittava, että virkaeläinlääkäri valvoo mainittujen säännösten noudattamista, ja sen on peruutettava hyväksyntä, jos yhtä tai useampaa säännöstä ei enää noudateta.
2. Kaikki hyväksytyt keinosiemennysasemat tai siemennesteen varastointiasemat on rekisteröitävä ja kullekin on annettava eläinlääkinnällinen rekisterinumero. Jokaisen jäsenvaltion on laadittava ja päivitettävä luettelo hyväksytyistä keinosiemennysasemista tai siemennesteen varastointiasemista ja niiden eläinlääkinnällisistä rekisterinumeroista ja toimitettava luettelo muiden jäsenvaltioiden ja yleisön saataville.
3. Tämän artiklan yhtenäistä soveltamista koskevia yksityiskohtaisia sääntöjä voidaan antaa 18 artiklan 2 kohdassa tarkoitettua menettelyä noudattaen.
6 artikla
1 Jäsenvaltioiden on tehtävä siemennesteen maahan pääsy riippuvaksi siitä, että liitteessä D olevan mallin mukaiselle lomakkeelle laadittu ja keräyserän jäsenvaltion virkaeläinlääkärin antama terveystodistus esitetään.
Tämä todistus on:
a) laadittava ainakin yhdellä alkuperämaana olevan jäsenvaltion ja yhdellä määrämaalla olevan jäsenvaltion virallisista kielistä,
b) oltava alkuperäiskappaleena lähetyksen mukana määräpaikkaan saakka,
c) laadittava yhdelle liuskalle,
d) osoitettava yhdelle vastaanottajalle.
2
a) Määrämaana oleva jäsenvaltio voi kieltää lähetysten maahan pääsyn, jos asiakirjojen tarkastuksessa havaitaan, että 3 artiklan säännöksiä ei ole noudatettu.
b) Määrämaana oleva jäsenvaltio voi toteuttaa tarpeelliset toimenpiteet, mukaan lukien karanteenin asettaminen, kiistattoman näytön saamiseksi tapauksissa, joissa siemennesteen epäillään olevan taudinaiheuttajaorganismien tartuttamaa tai saastuttamaa.
c) Edellä a tai b kohdan mukaisesti tehdyissä päätöksissä on sallittava siemennesteen palauttaminen lähettäjän tai tämän edustajan pyynnöstä, jos sille eläinten terveyttä koskevien seikkojen perusteella ei ole esteitä.
3 Jos siemennesteen tuominen maahan on kielletty jollakin 2 kohdan a ja b alakohdassa tarkoitetulla perusteella ja alkuperämaana oleva jäsenvaltio ei 30 päivän kuluessa anna lupaa siemennesteen palauttamiseen, määrämaana olevan jäsenvaltion toimivaltainen eläinlääkintäviranomainen voi määrätä siemennesteen hävitettäväksi.
4 Toimivaltaisen eläinlääkintäviranomaisen 2 ja 3 kohdan mukaiset päätökset ja niiden perustelut on toimitettava lähettäjälle tai tämän edustajalle tiedoksi.
▼M2 —————
III LUKU
Tuonti kolmansista maista
8 artikla
1 Jäsenvaltio voi sallia siemennesteen tuonnin vain sellaisista kolmansista maista, jotka sisältyvät ►M5 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen ◄ laadittuun luetteloon.
Luetteloa voidaan täydentää tai muuttaa ►M5 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen ◄ .
2 Päätettäessä jonkin kolmannen maan sisällyttämisestä 1 kohdassa tarkoitettuun luetteloon, on erityisesti otettava huomioon:
a) karjan, muiden kotieläinten ja luonnonvaraisen eläimistön terveydentila kyseisessä kolmannessa maassa, erityisesti eksoottisten eläintautien esiintyminen, sekä eläintautitilanne ympäristössä, sikäli kun ne saattaisivat olla vaaraksi jäsenvaltioiden eläimistön terveydelle;
b) miten säännöllisesti ja nopeasti kolmas maa antaa tietoja alueellaan esiintyvistä eläinten tartuntataudeista, erityisesti Maailman eläintautijärjestön luetteloissa A ja B mainituista taudeista;
c) kolmannen maan säännökset eläintautien ehkäisystä ja torjunnasta;
d) kolmannen maan eläinlääkintäyksiköiden organisaatio ja toimivalta;
e) tarttuvien eläintautien ehkäisy- ja torjuntatoimenpiteiden organisaatio ja täytäntöönpano; sekä
f) takeet, jotka kolmas maa voi antaa tämän direktiivin noudattamisesta.
3 Edellä 1 kohdassa tarkoitettu luettelo ja kaikki siihen tehdyt muutokset julkaistaan Euroopan yhteisöjen virallisessa lehdessä.
9 artikla
1. Jäsenvaltioiden on hyväksyttävä ainoastaan sellaisen siemennesteen tuonti, joka on lähetetty kolmannessa maassa sijaitsevalta keinosiemennysasemalta tai siemennesteen varastointiasemalta, joka on merkitty 8 artiklassa tarkoitettuun luetteloon ja jonka osalta kyseisen kolmannen maan toimivaltainen viranomainen voi antaa takeet siitä, että
a) se täyttää seuraavat edellytykset:
i) liitteessä A olevassa I luvussa vahvistetut keinosiemennysasemien tai siemennesteen varastointiasemien hyväksymistä koskevat edellytykset;
ii) sen luvussa II vahvistetut tällaisten asemien valvontaa koskevat vaatimukset;
b) kyseisen kolmannen maan toimivaltainen viranomainen on virallisesti hyväksynyt sen yhteisöön tapahtuvaa vientiä varten;
c) se on asemaeläinlääkärin valvonnassa;
d) kyseisen kolmannen maan virkaeläinlääkäri tarkastaa sen vähintään kahdesti vuodessa.
2. Luettelo keinosiemennysasemista tai siemennesteen varastointiasemista, jotka 8 artiklassa tarkoitetussa luettelossa olevan kolmannen maan toimivaltainen viranomainen on hyväksynyt tämän artiklan 1 kohdassa vahvistettujen edellytysten mukaisesti ja joilta siemennestettä voidaan lähettää yhteisöön, on toimitettava komissiolle.
Kolmannen maan toimivaltaisen viranomaisen on välittömästi keskeytettävä tai peruutettava keinosiemennysaseman tai siemennesteen varastointiaseman hyväksyntä, jos se ei enää täytä 1 kohdassa vahvistettuja edellytyksiä, ja komissiolle on välittömästi ilmoitettava asiasta.
Komissio toimittaa jäsenvaltioille kaikki uudet ja päivitetyt luettelot, jotka se saa kolmannen maan toimivaltaiselta viranomaiselta tämän kohdan mukaisesti ja se toimittaa luettelon yleisölle tiedoksi.
3. Tämän artiklan yhtenäistä soveltamista koskevia yksityiskohtaisia sääntöjä voidaan antaa 18 artiklan 2 kohdassa tarkoitettua menettelyä noudattaen.
10 artikla
1 Siemennesteen on oltava peräisin eläimiltä, jotka ovat välittömästi ennen siemennesteen ottoa olleet ainakin kuuden kuukauden ajan 8 artiklan 1 kohdan mukaisesti laaditussa luettelossa mainitun kolmannen maan alueella.
2 Jäsenvaltiot saavat sallia siemennesteen tuonnin luettelossa mainitusta kolmannesta maasta vain, jos siemenneste täyttää eläinten terveyttä koskevat vaatimukset, jotka on ►M5 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen ◄ hyväksytty kyseisestä maasta tapahtuvaa siemennesteen tuontia varten, sanotun kuitenkaan rajoittamatta 8 artiklan 1 kohdan ja tämän artiklan 1 kohdan soveltamista.
Päätettäessä edellisessä alakohdassa tarkoitetuista vaatimuksista on otettava huomioon:
a) terveystilanne keinosiemennysasemaa ympäröivällä vyöhykkeellä erityisesti Maailman eläintautijärjestön luetteloon A sisältyvien tautien osalta;
b) keinosiemennysaseman karjan terveydentila, mukaan lukien tutkimuksia koskevat määräykset;
c) luovuttajaeläimen terveydentila ja tutkimuksia koskevat määräykset;
d) siemennesteen tutkimusta koskevat määräykset.
3 Määriteltäessä 2 kohdan mukaisia terveyttä koskevia vaatimuksia naudan tuberkuloosin ja luomistaudin osalta, on vertailuperusteena käytettävä direktiivin 64/432/ETY liitteessä A esitettyjä määräyksiä. Näistä säännöksistä tehtävistä poikkeuksista voidaan päättää tapauksittain ►M5 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen ◄ , jos kolmas maa, jota asia koskee, antaa samanlaiset terveystakeet; tällaisessa tapauksessa on samaa menettelyä noudattaen määriteltävä vähintään mainitun direktiivin liitteen A kanssa samanveroiset terveysvaatimukset, jotta kyseisten eläinten pääsy keinosiemennysasemille voidaan sallia.
4 Vastaavasti 4 artiklaa sovelletaan.
11 artikla
1 Jäsenvaltiot saavat antaa luvan siemennesteen tuontiin vain sillä edellytyksellä, että esitetään alkuperämaana olevan kolmannen maan virkaeläinlääkärin laatima ja allekirjoittama terveystodistus.
Tämä todistus on:
a) laadittava ainakin yhdellä määrämaana olevan jäsenvaltion ja yhdellä sen jäsenvaltion virallisista kielistä, jossa 12 artiklassa säädetty tuontitarkastus tapahtuu;
b) oltava alkuperäiskappaleena siemennestelähetyksen mukana;
c) laadittava yhdelle liuskalle;
d) osoitettava yhdelle vastaanottajalle.
2 Terveystodistuksen on oltava ►M5 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen ◄ laaditun mallin mukainen.
12 artikla
Direktiivissä 97/78/EY vahvistettuja sääntöjä noudatetaan erityisesti jäsenvaltioiden tekemien tarkastusten järjestämisen ja seurannan osalta sekä mainitun direktiivin 22 artiklassa tarkoitetun menettelyn mukaisesti noudatettavien suojatoimenpiteiden osalta.
▼M3 —————
IV LUKU
Suoja- ja tarkastustoimenpiteet
▼M2 —————
15 artikla
Eläinlääkärin- ja kotieläinjalostustarkastuksista ( 7 ) yhteisön sisäisessä tiettyjen elävien eläinten ja tuotteiden kaupassa 26 päivänä kesäkuuta 1990 annetussa neuvoston direktiivissä 90/425/ETY säädettyjä sääntöjä sovelletaan erityisesti alkuperäpaikassa suoritettaviin tarkastuksiin, määräpaikkana olevassa jäsenvaltiossa suoritettavien tarkastusten järjestämiseen ja seurantaan sekä täytäntöön pantaviin suojatoimenpiteisiin.
16 artikla
1 Komission eläinlääkintäasiantuntijat voivat yhteistyössä jäsenvaltioiden ja kolmansien maiden toimivaltaisten viranomaisten kanssa suorittaa tarkastuksia paikalla sikäli kuin ne tämän direktiivin yhdenmukaisen soveltamisen kannalta ovat tarpeen.
Alkuperämaan, jonka alueella tarkastus tapahtuu, on annettava kaikki tarpeellinen apu asiantuntijoille näiden suorittaessa tehtäviään. Komission on ilmoitettava tarkastuksen tuloksista jäsenvaltioille tai kyseiselle keräilymaalle.
Alkuperämaan on toteutettava kaikki tarkastusten tulosten huomioon ottamiseksi mahdollisesti tarpeelliset toimenpiteet. Jollei alkuperämaa toteuta mainittuja toimenpiteitä, komissio voi pysyvän eläinlääkintäkomitean tutkittua tilanteen soveltaa 5 artiklan 2 kohdan neljännen alakohdan ja 9 artiklan 1 kohdan säännöksiä.
2 Yleiset, erityisesti 1 kohdan ensimmäisessä alakohdassa tarkoitettujen tarkastusten tiheyttä ja suoritustapaa koskevat säännökset tämän artiklan täytäntöön panemiseksi annetaan ►M5 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen ◄ .
V LUKU
Loppusäännökset
17 artikla
Neuvosto muuttaa komission ehdotuksesta määräenemmistöllä liitettä A erityisesti sen mukauttamiseksi tekniikan kehitykseen.
Liitteitä B, C ja D muutetaan 18 artiklan 2 kohdassa säädettyä menettelyä noudattaen.
18 artikla
1. Komissiota avustaa asetuksella (EY) N:o 178/2002 ( 8 ) perustettu elintarvikeketjua ja eläinten terveyttä käsittelevä pysyvä komitea.
2. Jos tähän kohtaan viitataan, sovelletaan päätöksen 1999/468/EY ( 9 ) 5 ja 7 artiklaa.
Päätöksen 1999/468/EY 5 artiklan 6 kohdassa tarkoitettu määräaika vahvistetaan kolmeksi kuukaudeksi.
3. Komitea vahvistaa työjärjestyksensä.
▼M5 —————
20 artikla
1 Tätä direktiiviä ei sovelleta jäsenvaltiossa ennen 1 päivää tammikuuta 1990 kerättyyn ja käsiteltyyn siemennesteeseen.
2 Siihen asti kunnes 8, 9 ja 10 artiklassa säädetyt päätökset tulevat voimaan jäsenvaltiot eivät saa soveltaa siemennesteen tuontiin kolmansista maista suotuisampia ehtoja kuin II luvusta johtuvat ehdot.
21 artikla
Jäsenvaltioiden on saatettava voimaan tämän direktiivin noudattamisen edellyttämät lait, asetukset ja hallinnolliset määräykset viimeistään 1 päivänä tammikuuta 1990. Jäsenvaltioiden on ilmoitettava niistä komissiolle viipymättä.
22 artikla
Tämä direktiivi on osoitettu kaikille jäsenvaltioille.
LIITE A
I LUKU ASEMIEN VIRALLISEN HYVÄKSYMISEN EDELLYTYKSET
1. Keinosiemennysasemien on täytettävä seuraavat vaatimukset:
a) aseman on oltava toimivaltaisen viranomaisen valtuuttaman asemaeläinlääkärin pysyvässä valvonnassa;
b) asemalla on oltava ainakin:
i) eläintilat, mukaan luettuna eristystilat;
ii) tilat siemennesteen ottoon, mukaan luettuna erillinen huone välineiden puhdistusta ja desinfioimista tai sterilointia varten;
iii) siemennesteen käsittelyhuone, jonka ei välttämättä tarvitse sijaita samassa paikassa;
iv) siemennesteen varastointihuone, jonka ei välttämättä tarvitse sijaita samassa paikassa;
c) aseman on oltava rakennettu tai eristetty siten, että estetään kosketus ulkopuolella olevaan karjaan;
d) asema on oltava rakennettu siten, että eläintilat sekä siemennesteen keräily-, käsittely- ja varastointitilat voidaan helposti puhdistaa ja desinfioida;
e) asemalla on oltava eristystila, josta ei ole välitöntä yhteyttä normaaleihin eläintiloihin;
f) aseman on oltava suunniteltu siten, että eläintilat ovat fyysisesti erillään siemennesteen käsittelytiloista ja että molemmat ovat erillään siemennesteen varastointitiloista.
2. Siemennesteen varastointiasemien on täytettävä seuraavat vaatimukset:
a) aseman on oltava toimivaltaisen viranomaisen valtuuttaman asemaeläinlääkärin pysyvässä valvonnassa;
b) aseman on oltava rakennettu tai eristetty siten, että estetään kosketus ulkopuolella olevaan karjaan;
c) asema on oltava rakennettu siten, että varastointitilat voidaan puhdistaa ja desinfioida helposti.
II LUKU ASEMIEN VIRALLISTA VALVONTAA KOSKEVAT VAATIMUKSET
1. Keinosiemennysasemien on:
a) oltava valvottuja siten, että niillä säilytetään vain sen lajin eläimiä, joiden siemennestettä on tarkoitus kerätä. Muita aseman normaalin toiminnan kannalta ehdottoman tarpeellisia kotieläimiä voidaan kuitenkin tuoda asemalle edellyttäen, ettei niistä aiheudu tartunnan vaaraa siemennestettä luovuttaville lajeille ja että ne täyttävät aseman eläinlääkärin laatimat ehdot;
b) oltava valvottuja siten, että ne pitävät kaikista asemalla olevista nautaeläimistä kirjaa, josta ilmenee kunkin eläimen rotu, syntymäpäivä ja tunniste, ja että ne lisäksi pitävät kirjaa kaikista terveystarkastuksista ja kullekin eläimelle suoritetuista rokotuksista;
c) oltava virkaeläinlääkärin säännöllisesti vähintään kahdesti vuodessa tarkastamia. Nämä tarkastukset suoritetaan säännönmukaisten hyväksymistä ja valvontaa koskevien vaatimusten tarkastamisen yhteydessä;
d) oltava valvottuja siten, että asiattomien henkilöiden pääsy aseman tiloihin estyy. Lisäksi luvallisilta vierailijoilta on vaadittava aseman eläinlääkärin vahvistamien vaatimusten noudattamista;
e) pidettävä palveluksessaan teknisesti pätevää henkilöstöä, joka on asianmukaisesti koulutettu sairauksien torjunnassa tarvittaviin desinfiointimenetelmiin ja hygieenisiin menetelmiin;
f) oltava valvottuja siten, että:
i) hyväksytyillä asemilla käsitellään ja varastoidaan vain hyväksytyillä asemilla kerättyä siemennestettä, jota ei päästetä kosketuksiin muiden siemennestelähetysten kanssa. Muulla kuin hyväksytyllä keinosiemennysasemalla kerättyä siemennestettä voidaan kuitenkin käsitellä hyväksytyllä asemalla, jos
— tällainen siemenneste on peräisin sonneilta, jotka täyttävät liitteessä B olevan I luvun 1 kohdan d alakohdan vaatimukset,
— käsittely suoritetaan eri välineillä tai eri aikaan kuin yhteisön sisäiseen kauppaan tarkoitetun siemennesteen käsittely, jolloin jälkimmäisessä tapauksessa välineet käytön jälkeen puhdistetaan ja steriloidaan,
— tällaista siemennestettä ei päästetä yhteisön sisäiseen kauppaan eikä se missään vaiheessa saa tulla kosketuksiin tai olla varastoituna yhteisön sisäiseen kauppaan tarkoitetun siemennesteen kanssa,
— tällainen siemenneste on tunnistettavissa merkinnästä, joka erottuu vii alakohdassa säädetystä merkinnästä;
Hyväksytyillä asemilla voidaan varastoida myös pakastettuja alkioita, edellyttäen että:
— toimivaltainen viranomainen on antanut luvan tällaiseen varastointiin,
— alkiot täyttävät eläinten terveyttä koskevista vaatimuksista yhteisön sisäisessä naudansukuisten kotieläinten alkioiden kaupassa ja tuonnissa kolmansista maista 25 päivänä syyskuuta 1989 annetun neuvoston direktiivin 89/556/ETY ( 10 ) vaatimukset,
— alkiot varastoidaan erillisiin säilytysastioihin hyväksytyn siemennesteen varastointitiloissa;
ii) siemennesteen keräys, käsittely ja varastointi tapahtuu ainoastaan näihin tarkoituksiin varatuissa tiloissa ja ehdottoman hygieenisesti;
iii) kaikki siemennesteen keräyksen ja käsittelyn yhteydessä siemennesteen tai luovuttajaeläimen kanssa kosketuksiin joutuvat välineet, kertakäyttöisiä välineitä lukuun ottamatta, desinfioidaan tai steriloidaan asianmukaisesti ennen käyttöä;
iv) siemennesteen käsittelyssä käytetyt eläinperäiset tuotteet, mukaan luettuna lisä- tai laimennusaineet, hankitaan lähteistä, joista ei aiheudu eläintautien vaaraa, taikka käsitellään ennen käyttöä siten, että sellainen vaara torjutaan;
v) säilytys- ja kuljetusastiat, kertakäyttöisiä säiliöitä lukuun ottamatta, joko desinfioidaan tai steriloidaan asianmukaisesti ennen jokaista täyttöä;
vi) pakastusnesteenä käytettävää nestettä ei ole aiemmin käytetty muiden eläinperäisten tuotteiden käsittelyyn;
vii) kukin siemenneste-erä merkitään selvästi siten, että siemennesteen keräyspäivä, luovuttajaeläimen rotu ja tunniste sekä aseman hyväksymisnumero ovat helposti todettavissa. Kunkin jäsenvaltion on ilmoitettava komissiolle ja muille jäsenvaltioille alueellaan käyttöön otetun merkinnän ominaispiirteet ja muoto;
viii) varastointiyksikön on noudatettava 2 kohdassa säädettyjä siemennesteen varastointiaseman valvontaa koskevia erityisvaatimuksia.
2. Siemennesteen varastointiasemien on:
a) oltava valvottuja siten, että ne pitävät kirjaa kaikista siemennesteen siirroista (asemalle ja asemalta) sekä niiden luovuttajasonnien terveydentilasta, joiden siemennestettä on varastoitu, jonka on täytettävä tämän direktiivin vaatimukset;
b) oltava virkaeläinlääkärin säännöllisesti vähintään kahdesti vuodessa tarkastamia. Nämä tarkastukset suoritetaan säännönmukaisten hyväksymistä ja valvontaa koskevien vaatimusten tarkastamisen yhteydessä;
c) oltava valvottuja siten, että asiattomien henkilöiden pääsy aseman tiloihin estyy. Lisäksi luvallisilta vierailijoilta on vaadittava aseman eläinlääkärin vahvistamien vaatimusten noudattamista;
d) pidettävä palveluksessaan teknisesti pätevää henkilöstöä, joka on asianmukaisesti koulutettu sairauksien torjunnassa tarvittaviin desinfiointimenetelmiin ja hygieenisiin menetelmiin;
e) oltava valvottuja siten, että
i) hyväksytyillä varastointiasemilla varastoidaan vain tämän direktiivin mukaisesti hyväksytyillä asemilla kerättyä siemennestettä, joka ei ole ollut kosketuksissa muunlaisen siemenen kanssa.
Tämän lisäksi hyväksytylle varastointiasemalle voidaan tuoda vain siemennestettä, joka on peräisin hyväksytyltä keinosiemennysasemalta tai siemennesteen varastointiasemalta ja kuljetettu terveydellisesti täysin varmoissa olosuhteissa ja jota ei päästetä kosketuksiin muiden siemennestelähetysten kanssa.
Hyväksytyillä asemilla voidaan varastoida myös pakastettuja alkioita, edellyttäen että:
— toimivaltainen viranomainen on antanut luvan tällaiseen varastointiin,
— alkiot täyttävät eläinten terveyttä koskevista vaatimuksista yhteisön sisäisessä naudansukuisten kotieläinten alkioiden kaupassa ja tuonnissa kolmansista maista 25 päivänä syyskuuta 1989 annetun neuvoston direktiivin 89/556/ETY vaatimukset,
— alkiot varastoidaan erillisiin säilytysastioihin hyväksytyn siemennesteen varastointitiloissa;
ii) siemennesteen varastointi tapahtuu ainoastaan näihin tarkoituksiin varatuissa tiloissa ja ehdottoman hygieenisesti;
iii) kaikki siemennesteen kanssa kosketuksiin joutuvat välineet, kertakäyttöisiä välineitä lukuun ottamatta, desinfioidaan tai steriloidaan asianmukaisesti ennen käyttöä;
iv) säilytys- ja kuljetusastiat, kertakäyttöisiä säiliöitä lukuun ottamatta, joko desinfioidaan tai steriloidaan asianmukaisesti ennen jokaista täyttöä;
v) pakastusnesteenä käytettävää nestettä ei ole aiemmin käytetty muiden eläinperäisten tuotteiden käsittelyyn;
vi) kukin siemenneste-erä merkitään selvästi siten, että siemennesteen keräyspäivä, luovuttajaeläimen rotu ja tunniste sekä keinosiemennysaseman hyväksymisnumero ovat helposti todettavissa. Kunkin jäsenvaltion on ilmoitettava komissiolle ja muille jäsenvaltioille alueellaan käyttöön otetun merkinnän ominaispiirteet ja muoto.
LIITE B
I LUKU HYVÄKSYTYILLE KEINOSIEMENNYSASEMILLE TUOTAVIA ELÄIMIÄ KOSKEVAT VAATIMUKSET
1. Kaikkiin keinosiemennysasemalle tuotaviin nautaeläimiin sovelletaan seuraavia vaatimuksia:
a) eläimet ovat olleet karanteenissa vähintään 28 päivän ajan tiloissa, jotka jäsenvaltion toimivaltainen viranomainen on nimenomaan tähän tarkoitukseen hyväksynyt ja joissa niiden lisäksi on ollut vain vähintään yhtä hyvässä terveydentilassa olevia muita sorkkaeläimiä;
b) ennen siirtymistään a alakohdassa tarkoitettuihin karanteenitiloihin eläimet ovat kuuluneet karjoihin, jotka on todettu virallisesti vapaiksi tuberkuloosista ja luomistaudista direktiivin 64/432/ETY mukaisesti. Eläimiä ei ole aikaisemmin saanut pitää karjassa, jonka tautitilanne on huonompi;
c) eläimet ovat lähtöisin karjasta, joka on virallisesti vapaa naudan tarttuvasta leukoosista, sellaisena kuin se on määritetty direktiivissä 64/432/ETY, tai niiden emälle on tehty direktiivin 64/432/ETY liitteessä D olevan II luvun mukaisesti tutkimus negatiivisin tuloksin sen jälkeen kun ne on viety pois emältään. Alkionsiirtotapauksissa ’emällä’ tarkoitetaan alkion vastaanottajaa.
Jos tätä vaatimusta ei voida täyttää, siemennestettä ei saa myydä, ennen kuin luovuttajaeläin on saavuttanut kahden vuoden iän ja se on tutkittu II luvun 1 kohdan c alakohdan mukaisesti negatiivisin tuloksin;
d) eläinten on ollut käytävä a kohdassa määriteltyä karanteenia edeltävien 28 päivän aikana lävitse seuraavat tutkimukset negatiivisin tuloksin, lukuun ottamatta v kohdassa mainittua BVD/MD-vasta-ainetestiä:
i) naudan tuberkuloosin varalta nahansisäinen tuberkuliinikoe suoritettuna direktiivin 64/432/ETY liitteessä B vahvistetulla tavalla;
ii) nautojen luomistaudin varalta serologinen tutkimus suoritettuna direktiivin 64/432/ETY liitteessä C kuvatulla tavalla;
iii) naudan tarttuvan leukoosin varalta serologinen tutkimus suoritettuna direktiivin 64/432/ETY liitteessä D olevassa II luvussa säädetyllä tavalla;
iv) naudan tarttuvan rinotrakeiitin / tarttuvan pustulaarisen vulvovaginiitin (IBR/IPV) varalta verinäytteen serologinen tutkimus (koko virus), jos eläimet eivät tule IBR/IPV-vapaasta karjasta, siten kuin se on määritetty kansainvälisen eläinten terveyttä koskevan säännöstön 2.3.5.3 artiklassa;
v) naudan virusripulin (BVD/MD) varalta:
— virukseneristämistesti tai viruksen antigeenitesti, ja
— serologinen tutkimus vasta-aineiden selvittämiseksi.
Toimivaltainen viranomainen voi antaa luvan d alakohdassa tarkoitettujen tutkimusten suorittamiseen karanteenitiloissa kerätyistä näytteistä. Tällöin a alakohdassa tarkoitettu karanteeni ei voi alkaa ennen näytteidenottopäivää. Jos jokin d alakohdassa mainituista kokeista kuitenkin antaa positiivisen tuloksen, kyseinen eläin on viipymättä poistettava eristystiloista. Jos kyseessä on ryhmäeristys, a alakohdassa tarkoitettu karanteeni ei voi alkaa muiden eläinten osalta ennen kuin positiivisen näytteen antanut eläin on poistettu.
e) eläimille on tehty a alakohdassa säädetyn karanteenin aikana ja aikaisintaan 21 päivän kuluttua niiden karanteeniin otosta (Campylobacter fetus ssp. veneralis -tartunnan ja Trichomonas foetus -tartunnan etsimiseksi aikaisintaan 7 päivän kuluttua niiden karanteeniin otosta) seuraavat tutkimukset negatiivisin tuloksin, lukuun ottamatta BVD/MD-vasta-ainetestiä (jäljempänä iii alakohta):
i) nautojen luomistaudin varalta serologinen tutkimus suoritettuna direktiivin 64/432/ETY liitteessä C kuvatulla tavalla;
ii) naudan tarttuvan rinotrakeiitin / tarttuvan pustulaarisen vulvovaginiitin (IBR/IPV) varalta verinäytteen serologinen tutkimus (koko virus).
Jos jonkin edellä mainitun kokeen tulos on positiivinen, eläin on poistettava välittömästi karanteeniasemalta ja muut saman ryhmän eläimet on pidettävä karanteenissa ja niille on tehtävä uusi koe negatiivisin tuloksin vähintään 21 päivän kuluttua positiivisen eläimen tai positiivisten eläinten siirtämisestä;
iii) naudan virusripulin (BVD/MD) varalta:
— virukseneristämistesti tai viruksen antigeenitesti, ja
— serologinen tutkimus vasta-aineiden selvittämiseksi.
Siemennesteen keruutiloihin voidaan päästää eläimiä (seronegatiivisia taikka seropositiivisia) ainoastaan, jos ennen karanteeniasemalle tuloa seronegatiivisiksi todetuissa eläimissä ei esiinny serokonversiota.
Jos serokonversiota esiintyy, kaikki edelleen seronegatiiviset eläimet on pidettävä karanteenissa pidennetyn ajan, kunnes ryhmässä ei enää esiinny serokonversiota kolmen viikon aikana. Serologisesti positiivisiksi todettuja eläimiä voidaan päästää siemennesteen keruuaseman tiloihin;
iv) Campylobacter foetus ssp venerealis -tartunnan varalta:
— yksi koe esinahan näytteestä tai keinoemättimen huuhtelunestenäytteestä, jos eläimet ovat alle kuuden kuukauden ikäisiä tai niitä on pidetty tuosta iästä asti vain samaa sukupuolta olevien ryhmässä ennen karanteenia,
— kolme kertaa viikon välein esinahan näytteestä tai keinoemättimen huuhtelunestenäytteestä tehtävä koe, jos eläimet ovat yli kuuden kuukauden ikäisiä ja ovat voineet olla kosketuksissa naaraisiin ennen karanteenia;
v) Trichomonas foetus -tartunnan varalta
— yksi koe esinahan näytteestä, jos eläimet ovat alle kuuden kuukauden ikäisiä tai niitä on pidetty tuosta iästä asti vain samaa sukupuolta olevien ryhmässä ennen karanteenia,
— kolme kertaa viikon välein esinahan näytteestä tehtävä koe, jos eläimet ovat yli kuuden kuukauden ikäisiä ja ovat voineet olla kosketuksissa naaraisiin ennen karanteenia.
Jos jokin mainituista kokeista antaa positiivisen tuloksen, eläin on viipymättä poistettava eristystiloista. Jos kyseessä on ryhmäeristys, toimivaltaisen viranomaisen on toteutettava kaikki tarpeelliset toimenpiteet, jotta jäljellä olevat eläimet voidaan liittää aseman karjaan liitteen mukaisesti;
f) Ennen kuin serologisessa BVD/MD-testissä positiivisen tuloksen saaneiden sonnien siemennestettä lähetetään ensimmäisen kerran, kunkin eläimen siemennestenäytteestä on tehtävä virukseneristämistesti tai Elisa BVD/MD-antigeenitesti. Jos tulos on positiivinen, sonni on poistettava asemalta ja kaikki sen siemenneste on tuhottava.
2. Kaikki kokeet on suoritettava jäsenvaltion hyväksymässä laboratoriossa.
3. Eläimiä saa tuoda keinosiemennysasemalle ainoastaan aseman eläinlääkärin nimenomaisella luvalla. Eläinten saapumisesta asemalle ja poistamisesta sieltä on pidettävä kirjaa.
4. Keinosiemennysasemalle tuotu eläin ei saapumispäivänä saa osoittaa mitään kliinisiä sairauden oireita. Sen estämättä, mitä 5 kohdassa säädetään, kaikkien eläinten on oltava lähtöisin 1 kohdan a alakohdassa tarkoitetusta eristystilasta, joka lähetyspäivänä virallisesti täyttää seuraavat vaatimukset:
a) tila sijaitsee sellaisen alueen keskellä, jonka säde on 10 kilometriä ja jolla ei ainakaan 30 päivään ole esiintynyt suu- ja sorkkatautia;
b) tila on vähintään 3 kuukauden ajan ollut vapaa suu- ja sorkkataudista sekä luomistaudista;
c) tila on vähintään 30 päivän ajan ollut vapaa sellaisista karjan sairauksista, joista on tehtävä ilmoitus direktiivin 64/432/ETY liitteen E mukaisesti.
5. Jos 4 kohdassa säädetyt edellytykset on täytetty ja II luvussa tarkoitetut rutiinitutkimukset on suoritettu 12 edellisen kuukauden aikana, eläimiä voidaan ilman eristystä tai tutkimuksia siirtää yhdeltä hyväksytyltä keinosiemennysasemalta toiselle, jonka tautitilanne on samanlainen, jos siirto tapahtuu suoraan. Kyseessä oleva eläin ei saa päästä suoraan eikä välillisesti kosketuksiin sellaisten sorkkaeläinten kanssa, joiden tautitilanne on huonompi, ja kuljetuskalusto täytyy ennen käyttöä desinfioida. Jos siirto keinosiemennysasemalta toiselle tapahtuu jäsenvaltioiden välillä, se on suoritettava direktiivin 64/432/ETY mukaisesti.
II LUKU HYVÄKSYTYLLÄ KEINOSIEMENNYSASEMALLA PIDETTÄVILLE NAUTAELÄIMILLE PAKOLLISESTI SUORITETTAVAT TAVANOMAISET TUTKIMUKSET
1. Kaikille hyväksytyllä keinosiemennysasemalla pidettäville nautaeläimille on vähintään kerran vuodessa tehtävä seuraavat tutkimukset negatiivisin tuloksin:
a) naudan tuberkuloosin varalta nahansisäinen tuberkuliinikoe suoritettuna direktiivin 64/432/ETY liitteessä B vahvistetulla tavalla;
b) nautojen luomistaudin varalta serologinen tutkimus suoritettuna direktiivin 64/432/ETY liitteessä C vahvistetulla tavalla;
c) naudan tarttuvan leukoosin varalta serologinen tutkimus suoritettuna direktiivin 64/432/ETY liitteessä D olevassa II luvussa kuvatulla tavalla;
d) naudan tarttuvan rinotrakeiitin / tarttuvan pustulaarisen vulvovaginiitin (IBR/IPV) varalta verinäytteen serologinen tutkimus (koko virus);
e) naudan virusripulin (BVD/MD) varalta serologinen vasta-ainetesti ainoastaan seronegatiivisille eläimille.
Jos jonkin eläimen serologinen tulos on positiivinen, kaikki kyseisen eläimen viimeisen negatiivisen kokeen jälkeiset ejakulaatiot on joko hävitettävä tai niille on tehtävä virustesti negatiivisin tuloksin;
f) Campylobacter foetus ssp venerealis -tartunnan varalta koe esinahan näytteestä. Koe on tarpeen tehdä ainoastaan siemennesteen tuotannossa oleville sonneille tai sellaisten kanssa kosketuksiin joutuville sonneille. Keinosiemennysasemalle pidemmän kuin kuuden kuukauden ajanjakson jälkeen palaavat sonnit on testattava enintään 30 päivää ennen kuin ne aloittavat tuotannon uudelleen;
g) Trichomonas foetus -tartunnan varalta koe esinahan näytteestä. Koe on tarpeen tehdä ainoastaan siemennesteen tuotannossa oleville sonneille tai sellaisten kanssa kosketuksiin joutuville sonneille. Keinosiemennysasemalle pidemmän kuin kuuden kuukauden ajanjakson jälkeen palaavat sonnit on testattava enintään 30 päivää ennen kuin ne aloittavat tuotannon uudelleen.
2. Kaikki kokeet on suoritettava jäsenvaltion hyväksymässä laboratoriossa.
3. Jos jonkin edellä mainitun kokeen tulos on positiivinen, eläin on eristettävä, eikä sen viimeisen negatiivista tulosta osoittaneen kokeen jälkeen luovuttamaa siemennestettä saa päästää yhteisön sisäiseen kauppaan lukuun ottamatta ejakulaatioista, joiden BVD/MD -virustestin tulos on ollut negatiivinen, saatua siemennestettä.
Kaikilta muilta asemalla olevilta eläimiltä positiivista tulosta osoittaneen kokeen jälkeen kerätty siemenneste on säilytettävä erillisessä varastossa, eikä sitä saa päästää yhteisön sisäiseen kauppaan ennen kuin aseman tautitilanne on entisellään.
LIITE C
YHTEISÖN SISÄISEEN KAUPPAAN TARKOITETTUA TAI YHTEISÖÖN TUOTUA SIEMENNESTETTÄ KOSKEVAT VAATIMUKSET
1. Siemennesteen on oltava peräisin eläimiltä,
a) jotka eivät keräyspäivänä osoita mitään kliinisiä sairauden oireita;
i) joita ei ole rokotettu suu- ja sorkkatautia vastaan siemennesteen ottoa edeltäneiden 12 kuukauden tai
ii) jotka on rokotettu suu- ja sorkkatautia vastaan siemennesteen ottoa edeltäneiden 12 kuukauden aikana, jolloin viidelle prosentille (vähintään viisi olkea) kustakin keräyserästä on tehtävä virukseneristämistesti suu- ja sorkkataudin varalta negatiivisin tuloksin;
c) joita ei ole rokotettu suu- ja sorkkatautia vastaan siemennesteen ottoa välittömästi edeltäneiden 30 päivän aikana;
d) jotka ovat olleet hyväksytyllä keinosiemennysasemalla yhtäjaksoisesti vähintään siemennesteen ottoa välittömästi edeltäneiden 30 päivän ajan, jos kyseessä on tuore siemenneste;
e) joita ei käytetä luonnolliseen astutukseen;
f) joita pidetään vähintään kolmen kuukauden ajan ennen siemennesteen ottoa ja 30 päivän ajan sen jälkeen tai, jos kyseessä on tuore siemenneste, lähetyshetkeen asti suu- ja sorkkataudista vapaana olleella keinosiemennysasemalla, joka sijaitsee sellaisen alueen keskellä, jonka säde on 10 kilometriä ja jolla ei ainakaan 30 päivään ole esiintynyt suu- ja sorkkatautia;
g) joita on pidetty keinosiemennysasemalla, joka on vähintään 30 päivän ajan ennen siemennesteen ottoa ja 30 päivän ajan sen jälkeen tai, jos kyseessä on tuore siemenneste, lähetyshetkeen asti ollut vapaa direktiivin 64/432/ETY liitteen E (I) mukaan pakollisesti ilmoitettavista karjan sairauksista.
2. Siemennesteeseen on lisättävä seuraavia antibiootteja siten, että lopullisessa laimennetussa siemennesteessä niitä on jäljempänä mainitut pitoisuudet:
vähintään:
— 500 μg streptomysiiniä millilitraa kohden,
— 500 k.y. penisilliiniä millilitraa kohden,
— 150 μg linkomysiiniä millilitraa kohden,
— 300 μg spektinomysiiniä millilitraa kohden.
On myös mahdollista käyttää jotakin muuta antibioottiyhdistelmää, jolla on sama vaikutus kampylobakteereihin, leptospiraan ja mykoplasmoihin.
Laimennettua siemennestettä on välittömästi antibioottien lisäämisen jälkeen säilytettävä vähintään 5 oC:n lämpötilassa ainakin 45 minuutin ajan.
3. Yhteisön sisäiseen kauppaan tarkoitettu seimenneste on:
a) ennen lähetystä säilytettävä hyväksytyissä olosuhteissa vähintään 30 päivän ajan. Vaatimus ei koske tuoretta siemennestettä;
b) kuljetettava määrämaana olevaan jäsenvaltioon säiliöissä, jotka on ennen käyttöä puhdistettu ja desinfioitu tai steriloitu ja jotka on sinetöity ja numeroitu ennen kuin ne ovat lähteneet hyväksytystä varastosta.
LIITE D
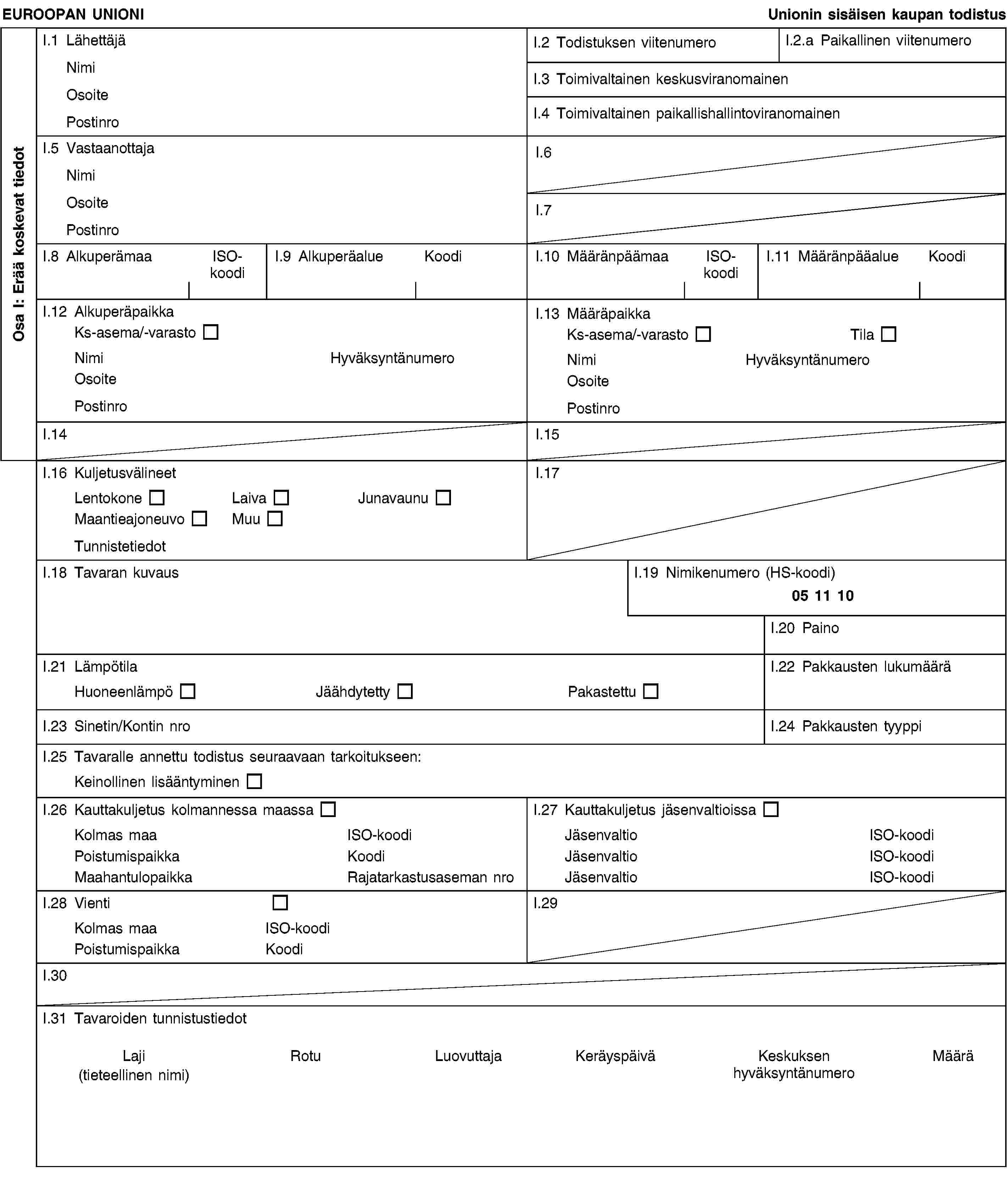
UNIONIN SISÄISESSÄ KAUPASSA KÄYTETTÄVÄT ELÄINTEN TERVEYSTODISTUSTEN MALLIT
LIITE D1
Eläinten terveystodistuksen malli, jota sovelletaan sellaisen naudansukuisten kotieläinten siemennesteen unionin sisäiseen kauppaan, joka on kerätty, käsitelty ja varastoitu neuvoston direktiivin 88/407/ETY, sellaisena kuin se on muutettuna direktiivillä 2003/43/EY, mukaisesti ja lähetetty siltä keinosiemennysasemalta, jolla siemenneste kerättiin

 tai II.1.2.2 [jotka on rokotettu suu- ja sorkkatautia vastaan siemennesteen keräystä edeltäneiden enintään 12 kuukauden ja vähintään 30 päivän aikana, jolloin viidelle prosentille (vähintään viisi olkea) kustakin keräyserästä on tehty virukseneristämistesti suu- ja sorkkataudin varalta negatiivisin tuloksin (…) (3) laboratoriossa, joka on määräjäsenvaltion osoittama tai sijaitsee määräjäsenvaltiossa;]II.1.3 on kerätty, käsitelty, varastoitu ja kuljetettu olosuhteissa, jotka täyttävät direktiivin 88/407/ETY liitteessä C vahvistetut vaatimukset;II.1.4 on välittömästi keräyksen jälkeen säilytetty hyväksytyissä olosuhteissa vähintään 30 päivän ajan (4).HuomautuksetOsa I:Kohta I.12: Alkuperäpaikan on vastattava sitä keinosiemennysasemaa (siten kuin se on määritelty direktiivin 88/407/ETY 2 artiklan b alakohdan ensimmäisessä luetelmakohdassa), jolla siemenneste kerättiin.Kohta I.13: Määräpaikan on vastattava keinosiemennysasemaa tai siemennesteen varastointiasemaa (siten kuin se on määritelty direktiivin 88/407/ETY 2 artiklan b alakohdassa) tai siemennesteen määränpäänä olevaa tilaa.Kohta I.23: Kontin tunnistetiedot ja sinetin numero on ilmoitettava.Kohta I.31: Luovuttajan on vastattava eläimen virallisia tunnistetietoja.Keräyspäivä on ilmoitettava seuraavassa muodossa: pp/kk/vvvvv.Aseman hyväksyntänumeron on vastattava kohdassa I.12 mainittua sen keinosiemennysaseman hyväksyntänumeroa, jolla siemenneste kerättiin.Osa II:(1) Tarpeeton yliviivataan.(2) Ainoastaan neuvoston direktiivin 88/407/ETY 5 artiklan 2 kohdan mukaisesti luetellut keinosiemennysasemat, jotka löytyvät seuraavalta komission www-sivustolta:http://ec.europa.eu/food/animal/approved_establishments/establishments_vet_field_en.htm(3) Laboratorion nimi.(4) Voidaan yliviivata, jos on kyse tuoreesta siemennesteestä.— Leima ja allekirjoitus on tehtävä eri värillä kuin muut todistuksen merkinnät.Virkaeläinlääkäri tai virallinen tarkastajaNimi (suuraakkosin):Virka-asema ja -nimike:Paikallinen eläinlääkintäyksikkö:Paikallisen eläinlääkintäyksikön nro:Päivämäärä:Allekirjoitus:Leima:](./../../../resource.html?uri=celex:01988L0407-20111101.FIN.xhtml.L_2011247FI.01002501.tif.jpg)
LIITE D2
Eläinten terveystodistuksen malli, jota sovelletaan 1. tammikuuta 2005 alkaen sellaisen siemennesteen varastojen unionin sisäiseen kauppaan, joka on kerätty, käsitelty ja varastoitu ennen 31. joulukuuta 2004 neuvoston direktiivin 88/407/ETY 1. heinäkuuta 2004 asti sovellettujen säännösten mukaisesti ja jota pidetään kaupan kyseisen päivän jälkeen direktiivin 2003/43/EY 2 artiklan 2 kohdan mukaisesti ja joka on lähetetty siltä keinosiemennysasemalta, jolla siemenneste kerättiin
 tai [nautaeläimille, joita ei ole rokotettu naudan tarttuvaa rinotrakeiittia vastaan, on tehty vähintään kerran vuodessa negatiivisin tuloksin seerumin neutralisaatiotesti tai Elisa-testi naudan tarttuvan rinotrakeiitin / tarttuvan pustulaarisen vulvovaginiitin varalta; naudan tarttuvaa rinotrakeiittia koskevia testejä ei tehdä sonneille, jotka ovat saneet ensimmäisen rokotuksen naudan tarttuvaa rinotrakeiittia vastaan keinosiemennysasemalla sen jälkeen, kun niille oli tehty negatiivisin tuloksin seerumin neutralisaatiotesti tai Elisa-testi naudan tarttuvan rinotrakeiitin / tarttuvan pustulaarisen vulvovaginiitin varalta, ja joita ensimmäisen rokotuksen jälkeen on rokotettu uudelleen säännöllisesti enintään kuuden kuukauden välein.]](./../../../resource.html?uri=celex:01988L0407-20111101.FIN.xhtml.L_2011247FI.01002701.tif.jpg)
 tai [jotka on rokotettu suu- ja sorkkatautia vastaan siemennesteen keräystä edeltäneiden enintään 12 kuukauden ja vähintään 30 päivän aikana, jolloin viidelle prosentille (vähintään viisi olkea) kustakin keräyserästä on tehty virukseneristämistesti suu- ja sorkkataudin varalta negatiivisin tuloksin (…) (2) laboratoriossa, joka on määräjäsenvaltion osoittama tai sijaitsee määräjäsenvaltiossa;]II.1.5.2(1) joko [joita ei ole rokotettu naudan tarttuvan rinotrakeiitin varalta;](1) tai [jotka on rokotettu naudan tarttuvan rinotrakeiitin varalta kohdan II.1.4. mukaisesti.]II.1.6 Edellä kuvattu siemenneste on välittömästi keräyksen jälkeen säilytetty hyväksytyissä olosuhteissa vähintään 30 päivän ajan (3).II.1.7 Edellä kuvattu siemenneste on toimitettu lastauspaikalle sinetöidyssä säiliössä, jonka numero on yksilöity kohdassa I.23.HuomautuksetOsa I:Kohta I.12: Alkuperäpaikan on vastattava sitä keinosiemennysasemaa (siten kuin se on määritelty direktiivin 88/407/ETY 2 artiklan b alakohdan ensimmäisessä luetelmakohdassa), jolla siemenneste kerättiin.Kohta I.13: Määräpaikan on vastattava keinosiemennysasemaa tai siemennesteen varastointiasemaa (siten kuin se on määritelty direktiivin 88/407/ETY 2 artiklan b alakohdassa) tai siemennesteen määränpäänä olevaa tilaa.Kohta I.23: Kontin tunnistetiedot ja sinetin numero on ilmoitettava.Kohta I.31: Luovuttajan on vastattava eläimen virallisia tunnistetietoja.Keräyspäivä on ilmoitettava seuraavassa muodossa: pp/kk/vvvv, ja sen on oltava aiemmin kuin 31. joulukuuta 2004.Aseman hyväksyntänumeron on vastattava kohdassa I.12 mainittua sen keinosiemennysaseman hyväksyntänumeroa, jolla siemenneste kerättiin.Osa II:(1) Tarpeeton yliviivataan.(2) Laboratorion nimi.(3) Voidaan yliviivata, jos on kyse tuoreesta siemennesteestä.— Leima ja allekirjoitus on tehtävä eri värillä kuin muut todistuksen merkinnät.Virkaeläinlääkäri tai virallinen tarkastajaNimi (suuraakkosin):Virka-asema ja -nimike:Paikallinen eläinlääkintäyksikkö:Paikallisen eläinlääkintäyksikön nro:Päivämäärä:Allekirjoitus:Leima:](./../../../resource.html?uri=celex:01988L0407-20111101.FIN.xhtml.L_2011247FI.01002801.tif.jpg)
LIITE D3
Eläinten terveystodistuksen malli, jota sovelletaan sellaisen naudansukuisten kotieläinten siemennesteen unionin sisäiseen kauppaan, joka on kerätty, käsitelty ja varastoitu neuvoston direktiivin 88/407/ETY, sellaisena kuin se on muutettuna direktiivillä 2003/43/EY, mukaisesti ja sellaisen siemennesteen varastojen unionin sisäiseen kauppaan, joka on kerätty, käsitelty ja varastoitu ennen 31. joulukuuta 2004 neuvoston direktiivin 88/407/ETY 1. heinäkuuta 2004 asti sovellettujen säännösten mukaisesti ja jota pidetään kaupan kyseisen päivän jälkeen direktiivin 2003/43/EY 2 artiklan 2 kohdan mukaisesti ja joka on lähetetty siemennesteen varastointiasemalta

![Osa II: TodistusEUROOPAN UNIONINaudan siemenneste – D3II Terveyttä koskevat tiedotII.a. Todistuksen viitenumeroII.b.II.1 Eläinten terveyttä koskeva vakuutusAllekirjoittanut virkaeläinlääkäri vakuuttaa, että edellä kuvattu siemenneste(1) joko [II.1 on kerätty, käsitelty ja varastoitu välittömästi keräyksen jälkeen vähintään 30 päivän ajan keinosiemennysasemalla (2) joka sijaitsee siinä jäsenvaltiossa, josta kyseinen siemenneste on peräisin, ja jota hallinnoidaan ja valvotaan direktiivin 88/407/ETY liitteessä A olevan I luvun 1 kohdan ja II luvun 1 kohdan mukaisesti ja josta kyseinen siemenneste hyväksyttiin kohdassa I.12 mainitulle siemennesteen varastointiasemalle, joka sijaitsee samassa jäsenvaltiossa, josta siemenneste on peräisin, sellaisten eläinten terveyttä ja terveystodistuksia koskevien vaatimusten nojalla, jotka ovat vähintään yhtä tiukat kuin ne, joista säädetään(1) joko [direktiivin 88/407/ETY liitteessä D1 (3);]](1) )ja/tai [direktiivin 88/407/ETY liitteessä D2 (4);]](1) ja/tai [direktiivin 88/407/ETY liitteessä D3 (3) (4);]](1) ja/tai [31. lokakuuta 2011 saakka direktiivin 88/407/ETY liitteessä D3 (3) (4) (5);]](1) ja/tai [II.1 on kerätty, käsitelty ja varastoitu välittömästi keräyksen jälkeen vähintään 30 päivän ajan keinosiemennysasemalla (2) joka sijaitsee Euroopan unionissa ja jota hallinnoidaan ja valvotaan direktiivin 88/407/ETY liitteessä A olevan I luvun 1 kohdan ja II luvun 1 kohdan mukaisesti, ja hyväksyttiin kohdassa I.12 mainitulle siemennesteen varastointiasemalle seuraavien mukaisesti:(1) joko [direktiivin 88/407/ETY liite D1 (3);]](1) ja/tai [direktiivin 88/407/ETY liite D2 (4);]](1) ja/tai [direktiivin 88/407/ETY liite D3 (3) (4);]](1) ja/tai [31. lokakuuta 2011 saakka direktiivin 88/407/ETY liite D3 (3) (4) (5);]](1) ja/tai [II.1 on kerätty, käsitelty ja varastoitu välittömästi keräyksen jälkeen vähintään 30 päivän ajan keinosiemennysasemalla (2) joka sijaitsee komission päätöksen 2011/630/EU liitteessä I luetellussa kolmannessa maassa tai kolmannen maan osassa tai osissa ja jota hallinnoidaan ja valvotaan direktiivin 88/407/ETY liitteessä A olevan I luvun 1 kohdan ja II luvun 1 kohdan mukaisesti, ja tuotiin Euroopan unioniin direktiivin 88/407/ETY 8–12 artiklan edellytysten nojalla seuraavien mukaisesti:(1) joko [päätöksen 2011/630/EU liitteessä II olevan 2 osan A jakso (3);]](1) ja/tai [31. lokakuuta 2011 saakka päätöksen 2004/639/EY liitteessä II oleva 1 osa (3);]](1) ja/tai [päätöksen 2011/630/EU liitteessä II olevan 2 osan B jakso (4);]](1) ja/tai [31. lokakuuta 2011 saakka päätöksen 2004/639/EY liitteessä II oleva 2 osa (4);]](1) ja/tai [päätöksen 2011/630/EU liitteessä II olevan 2 osan C jakso (3) (4);]](1) ja/tai [31. lokakuuta 2011 saakka päätöksen 2004/639/EY liitteessä II oleva 3 osa (3) (4);]]II.2 on varastoitu kohdassa I.12 mainitulla siemennesteen varastointiasemalla (2), jota hallinnoidaan ja valvotaan direktiivin 88/407/ETY liitteessä A olevan I luvun 2 kohdan ja II luvun 2 kohdan mukaisesti.HuomautuksetOsa I:Kohta I.6: Numeron on vastattava sen virallisen kansallisen asiakirjan (virallisten kansallisten asiakirjojen), INTRA-terveystodistuksen (-terveystodistusten) tai CVED-todistuksen (-todistusten) sarjanumeroa, joka seuraa edellä kuvatun siemennesteen mukana siltä keinosiemennysasemalta, jolta kyseinen siemenneste on peräisin, edellä kuvatulle siemennesteen varastointiasemalle.Kohta I.12: Alkuperäpaikan on vastattava sitä keinosiemennysasemaa tai siemennesteen varastointiasemaa (siten kuin se on määritelty direktiivin 88/407/ETY 2 artiklan b alakohdassa), jolta siemenneste on lähetetty.Kohta I.13: Määräpaikan on vastattava keinosiemennysasemaa tai siemennesteen varastointiasemaa (siten kuin se on määritelty direktiivin 88/407/ETY 2 artiklan b alakohdassa) tai siemennesteen määränpäänä olevaa tilaa.Kohta I.23: Kontin tunnistetiedot ja sinetin numero on ilmoitettava.Kohta I.31: Luovuttajan on vastattava eläimen virallisia tunnistetietoja.Keräyspäivä on ilmoitettava seuraavassa muodossa: pp/kk/vvvvv.Aseman hyväksyntänumeron on vastattava sen keinosiemennysaseman hyväksyntänumeroa, jolta siemenneste on peräisin.](./../../../resource.html?uri=celex:01988L0407-20111101.FIN.xhtml.L_2011247FI.01003001.tif.jpg)

( 1 ) EYVL N:o C 267, 6.10.1983, s. 5
( 2 ) EYVL N:o C 342, 19.12.1983, s. 11
( 3 ) EYVL N:o C 140, 28.5.1984, s. 6
( 4 ) EYVL N:o 121, 29.7.1964, s. 1977/64
( 5 ) EYVL N:o L 362, 31.12.1985, s. 8
( 6 ) EYVL N:o L 302, 31.12.1972, s. 28
( 7 ) EYVL N:o L 224, 18.8.1990, s. 29
( 8 ) EYVL L 31, 1.2.2002, s. 1.
( 9 ) EYVL L 184, 17.7.1999, s. 23.
( 10 ) EYVL L 302, 19.10.1989, s. 1, direktiivi sellaisena kuin se on viimeksi muutettuna komission päätöksellä 94/113/EY (EYVL L 53, 24.2.1994, s. 23).

