ISSN 1725-2415
Επίσημη Εφημερίδα
της Ευρωπαϊκής Ένωσης
C 276

Έκδοση στην ελληνική γλώσσα
Ανακοινώσεις και Πληροφορίες
51ό έτος
31 Οκτωβρίου 2008
|
ISSN 1725-2415 |
||
|
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276 |
|

|
||
|
Έκδοση στην ελληνική γλώσσα |
Ανακοινώσεις και Πληροφορίες |
51ό έτος |
|
Ανακοίνωση αριθ |
Περιεχόμενα |
Σελίδα |
|
|
IV Πληροφορίες |
|
|
|
ΠΛΗΡΟΦΟΡΙΕΣ ΠΡΟΕΡΧΟΜΕΝΕΣ ΑΠΟ ΤΑ ΟΡΓΑΝΑ ΚΑΙ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ ΤΗΣ ΕΥΡΩΠΑΪΚΗΣ ΕΝΩΣΗΣ |
|
|
|
Επιτροπή |
|
|
2008/C 276/01 |
||
|
2008/C 276/02 |
||
|
2008/C 276/03 |
||
|
|
ΠΛΗΡΟΦΟΡΙΕΣ ΠΡΟΕΡΧΟΜΕΝΕΣ ΑΠΟ ΤΑ ΚΡΑΤΗ ΜΕΛΗ |
|
|
2008/C 276/04 |
||
|
2008/C 276/05 |
Πληροφορίες που διαβιβάζουν τα κράτη μέλη για τις κρατικές ενισχύσεις που χορηγούνται βάσει του κανονισμού (ΕΚ) αριθ. 70/2001 της Επιτροπής σχετικά με την εφαρμογή των άρθρων 87 και 88 της συνθήκης EK στις κρατικές ενισχύσεις προς μικρές και μεσαίες επιχειρήσεις ( 1 ) |
|
|
2008/C 276/06 |
Πληροφορίες που διαβιβάζουν τα κράτη μέλη για τις κρατικές ενισχύσεις που χορηγούνται βάσει του κανονισμού (ΕΚ) αριθ. 70/2001 της Επιτροπής σχετικά με την εφαρμογή των άρθρων 87 και 88 της συνθήκης EK στις κρατικές ενισχύσεις προς μικρές και μεσαίες επιχειρήσεις ( 1 ) |
|
|
|
||
|
2008/C 276/12 |
||
|
|
|
|
|
(1) Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ |
|
EL |
|
IV Πληροφορίες
ΠΛΗΡΟΦΟΡΙΕΣ ΠΡΟΕΡΧΟΜΕΝΕΣ ΑΠΟ ΤΑ ΟΡΓΑΝΑ ΚΑΙ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ ΤΗΣ ΕΥΡΩΠΑΪΚΗΣ ΕΝΩΣΗΣ
Επιτροπή
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/1 |
Ισοτιμίες του ευρώ (1)
30 Οκτωβρίου 2008
(2008/C 276/01)
1 ευρώ=
|
|
Νομισματική μονάδα |
Ισοτιμία |
|
USD |
δολάριο ΗΠΑ |
1,3035 |
|
JPY |
ιαπωνικό γιεν |
128,73 |
|
DKK |
δανική κορόνα |
7,4478 |
|
GBP |
λίρα στερλίνα |
0,7907 |
|
SEK |
σουηδική κορόνα |
9,811 |
|
CHF |
ελβετικό φράγκο |
1,48 |
|
ISK |
ισλανδική κορόνα |
305 |
|
NOK |
νορβηγική κορόνα |
8,52 |
|
BGN |
βουλγαρικό λεβ |
1,9558 |
|
CZK |
τσεχική κορόνα |
24,48 |
|
EEK |
εσθονική κορόνα |
15,6466 |
|
HUF |
ουγγρικό φιορίνι |
257,24 |
|
LTL |
λιθουανικό λίτας |
3,4528 |
|
LVL |
λεττονικό λατ |
0,7093 |
|
PLN |
πολωνικό ζλότι |
3,565 |
|
RON |
ρουμανικό λέι |
3,6375 |
|
SKK |
σλοβακική κορόνα |
30,39 |
|
TRY |
τουρκική λίρα |
1,9842 |
|
AUD |
αυστραλιανό δολάριο |
1,9204 |
|
CAD |
καναδικό δολάριο |
1,5697 |
|
HKD |
δολάριο Χονγκ Κονγκ |
10,1052 |
|
NZD |
νεοζηλανδικό δολάριο |
2,2015 |
|
SGD |
δολάριο Σιγκαπούρης |
1,9141 |
|
KRW |
νοτιοκορεατικό γουόν |
1 665,72 |
|
ZAR |
νοτιοαφρικανικό ραντ |
13,0194 |
|
CNY |
κινεζικό γιουάν |
8,9133 |
|
HRK |
κροατικό κούνα |
7,1699 |
|
IDR |
ινδονησιακή ρουπία |
13 914,86 |
|
MYR |
μαλαισιανό ρίγκιτ |
4,6046 |
|
PHP |
πέσο Φιλιππινών |
63,09 |
|
RUB |
ρωσικό ρούβλι |
34,7912 |
|
THB |
ταϊλανδικό μπατ |
45,381 |
|
BRL |
ρεάλ Βραζιλίας |
2,7521 |
|
MXN |
μεξικανικό πέσο |
16,6978 |
Πηγή: Ισοτιμίες αναφοράς που δημοσιεύονται από την Ευρωπαϊκή Κεντρική Τράπεζα.
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/2 |
Σύνοψη των κοινοτικών αποφάσεων σχετικά με τις άδειες κυκλοφορίας των φαρμάκων από τη 1 Σεπτεμβρίου 2008 έως τις 30 Σεπτεμβρίου 2008
[Δημοσίευση δυνάμει του άρθρου 13 ή του άρθρου 38 του κανονισμού (ΕΚ) αριθ. 726/2004 του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου (1) ]
(2008/C 276/02)
— Έκδοση άδειας κυκλοφορίας [Άρθρο 13 του κανονισμού (ΕΚ) αριθ. 726/2004]: Εγκρίνεται
|
Ημερομηνία της απόφασης |
Ονομασία του φαρμάκου |
INN (Διεθνής κοινή ονομασία) |
Κάτοχος της άδειας κυκλοφορίας |
Αριθμός εγγραφής στο κοινοτικό μητρώο |
Φαρμακευτική μορφή |
ATC code (Ανατομικός Θεραπευτικός Χημικός Κωδικός) |
Ημερομηνία κοινοποίησης |
|||
|
12.9.2008 |
Oprymea |
Πραμιπεξόλη |
|
EU/1/08/469/001-025 |
Δισκίο |
NO4BC05 |
15.9.2008 |
|||
|
15.9.2008 |
Tevagrastim |
Φιλγραστίμη |
|
EU/1/08/445/001-008 |
Ενέσιμο διάλυμα ή διάλυμα προς έγχυση |
L03AA02 |
17.9.2008 |
|||
|
15.9.2008 |
Biograstim |
Φιλγραστίμη |
|
EU/1/08/450/001-008 |
Ενέσιμο διάλυμα ή διάλυμα προς έγχυση |
L03AA02 |
17.9.2008 |
|||
|
15.9.2008 |
Ratiograstim |
Φιλγραστίμη |
|
EU/1/08/444/001-008 |
Ενέσιμο διάλυμα ή διάλυμα προς έγχυση |
L03AA02 |
17.9.2008 |
|||
|
15.9.2008 |
Filgrastim ratiopharm |
Φιλγραστίμη |
|
EU/1/08/449/001-008 |
Ενέσιμο διάλυμα ή διάλυμα προς έγχυση |
L03AA02 |
17.9.2008 |
|||
|
26.9.2008 |
Prepandemic influenza vaccine (H5N1) (split virion inactivated adjuvanted) GlaxoSmithKline Biologicals |
Προπανδημικό εμβόλιο γρίπης (H5N1) (τμήμα ιού, αδρανοποιημένο, ανοσοενισχυμένο) A/VietNam/1194/2004 NIBRG |
|
EU/1/08/478/001 |
Εναιώρημα και γαλάκτωμα για ενέσιμο γαλάκτωμα |
J07BB02 |
30.9.2008 |
|||
|
30.9.2008 |
Xarelto |
Ριβαροξαβάνη |
|
EU/1/08/472/001-008 |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
B01AX06 |
2.10.2008 |
— Τροποποίηση άδειας κυκλοφορίας [Άρθρο 13 του κανονισμού (ΕΚ) αριθ. 726/2004]: Εγκρίνεται
|
Ημερομηνία της απόφασης |
Ονομασία του φαρμάκου |
Κάτοχος της άδειας κυκλοφορίας |
Αριθμός εγγραφής στο κοινοτικό μητρώο |
Ημερομηνία κοινοποίησης |
|||||
|
1.9.2008 |
Aranesp |
|
EU/1/01/185/001-073 |
3.9.2008 |
|||||
|
1.9.2008 |
Adenuric |
|
EU/1/08/447/001-004 |
3.9.2008 |
|||||
|
3.9.2008 |
||||||||
|
1.9.2008 |
Rotarix |
|
EU/1/05/330/001-011 |
3.9.2008 |
|||||
|
1.9.2008 |
Zostavax |
|
EU/1/06/341/001-013 |
3.9.2008 |
|||||
|
2.9.2008 |
Ziagen |
|
EU/1/99/112/001-002 |
4.9.2008 |
|||||
|
2.9.2008 |
Lucentis |
|
EU/1/06/374/001 |
4.9.2008 |
|||||
|
2.9.2008 |
Olanzapine Neopharma |
|
EU/1/07/426/001-011 |
4.9.2008 |
|||||
|
2.9.2008 |
SonoVue |
|
EU/1/01/177/002 |
4.9.2008 |
|||||
|
2.9.2008 |
Gardasil |
|
EU/1/06/357/001-021 |
5.9.2008 |
|||||
|
2.9.2008 |
Viramune |
|
EU/1/97/055/001-003 |
4.9.2008 |
|||||
|
2.9.2008 |
Ventavis |
|
EU/1/03/255/001-006 |
4.9.2008 |
|||||
|
2.9.2008 |
Silgard |
|
EU/1/06/358/001-021 |
4.9.2008 |
|||||
|
2.9.2008 |
Cetrotide |
|
EU/1/99/100/001-003 |
5.9.2008 |
|||||
|
2.9.2008 |
Olanzapine Teva - |
|
EU/1/07/427/001-057 |
4.9.2008 |
|||||
|
2.9.2008 |
Elaprase |
|
EU/1/06/365/001-003 |
4.9.2008 |
|||||
|
3.9.2008 |
Tysabri |
|
EU/1/06/346/001 |
8.9.2008 |
|||||
|
3.9.2008 |
Comtess |
|
EU/1/98/082/001-003 EU/1/98/082/005 |
8.9.2008 |
|||||
|
3.9.2008 |
Aldara |
|
EU/1/98/080/001 |
5.9.2008 |
|||||
|
3.9.2008 |
Tamiflu |
|
EU/1/02/222/001-004 |
5.9.2008 |
|||||
|
3.9.2008 |
Mirapexin |
|
EU/1/97/051/001-006 EU/1/97/051/009-012 |
5.9.2008 |
|||||
|
3.9.2008 |
Aldara |
|
EU/1/98/080/001 |
5.9.2008 |
|||||
|
3.9.2008 |
Comtan |
|
EU/1/98/081/001-004 |
8.9.2008 |
|||||
|
3.9.2008 |
Cialis |
|
EU/1/02/237/001-008 |
5.9.2008 |
|||||
|
5.9.2008 |
Mircera |
|
EU/1/07/400/017-021 |
9.9.2008 |
|||||
|
5.9.2008 |
Herceptin |
|
EU/1/00/145/001 |
9.9.2008 |
|||||
|
5.9.2008 |
Puregon |
|
EU/1/96/008/038-041 |
9.9.2008 |
|||||
|
5.9.2008 |
Epivir |
|
EU/1/96/015/001-005 |
9.9.2008 |
|||||
|
8.9.2008 |
Evra |
|
EU/1/02/223/001-003 |
10.9.2008 |
|||||
|
9.9.2008 |
Herceptin |
|
EU/1/00/145/001 |
11.9.2008 |
|||||
|
12.9.2008 |
Viread |
|
EU/1/01/200/001-002 |
15.9.2008 |
|||||
|
15.9.2008 |
Sustiva |
|
EU/1/99/110/001-009 |
17.9.2008 |
|||||
|
15.9.2008 |
Glubrava |
|
EU/1/07/421/001-009 |
17.9.2008 |
|||||
|
15.9.2008 |
Stalevo |
|
EU/1/03/260/001-023 |
17.9.2008 |
|||||
|
16.9.2008 |
Combivir |
|
EU/1/98/058/001-002 |
18.9.2008 |
|||||
|
17.9.2008 |
Optisulin |
|
EU/1/00/133/001-008 |
19.9.2008 |
|||||
|
17.9.2008 |
Lantus |
|
EU/1/00/134/001-037 |
19.9.2008 |
|||||
|
22.9.2008 |
Emtriva |
|
EU/1/03/261/001-003 |
24.9.2009 |
|||||
|
22.9.2008 |
Emend |
|
EU/1/03/262/001-008 |
24.9.2008 |
|||||
|
26.9.2008 |
Aclasta |
|
EU/1/05/308/001-002 |
30.9.2008 |
|||||
|
26.9.2008 |
Thelin |
|
EU/1/06/353/001-005 |
30.9.2008 |
|||||
|
29.9.2008 |
Mycamine |
|
EU/1/08/448/001-002 |
1.10.2008 |
|||||
|
1.10.2008 |
— Ανάκληση άδειας κυκλοφορίας [Άρθρο 13 του κανονισμού (ΕΚ) αριθ. 726/2004]
|
Ημερομηνία της απόφασης |
Ονομασία του φαρμάκου |
Κάτοχος της άδειας κυκλοφορίας |
Αριθμός εγγραφής στο κοινοτικό μητρώο |
Ημερομηνία κοινοποίησης |
|||||
|
26.9.2008 |
Exubera |
|
EU/1/05/327/001-018 |
30.9.2008 |
— Έκδοση άδειας κυκλοφορίας [Άρθρο 38 του κανονισμού (ΕΚ) αριθ. 726/2004]: Εγκρίνεται
|
Ημερομηνία της απόφασης |
Ονομασία του φαρμάκου |
INN (Διεθνής κοινή ονομασία) |
Κάτοχος της άδειας κυκλοφορίας |
Αριθμός εγγραφής στο κοινοτικό μητρώο |
Φαρμακευτική μορφή |
ATC code (Ανατομικός Θεραπευτικός Χημικός Κωδικός) |
Ημερομηνία κοινοποίησης |
|||||
|
9.9.2008 |
Trocoxil |
Mavacoxib |
|
EU/2/08/084/001-005 |
Μασώμενες ταμπλέτες |
QM01AH92 |
11.9.2008 |
— Τροποποίηση άδειας κυκλοφορίας [Άρθρο 38 του κανονισμού (ΕΚ) αριθ. 726/2004]: Εγκρίνεται
|
Ημερομηνία της απόφασης |
Ονομασία του φαρμάκου |
Κάτοχος της άδειας κυκλοφορίας |
Αριθμός εγγραφής στο κοινοτικό μητρώο |
Ημερομηνία κοινοποίησης |
|||||
|
2.9.2008 |
Advocate |
|
EU/2/03/039/001-030 |
4.9.2008 |
|||||
|
4.9.2008 |
||||||||
|
5.9.2008 |
Profender |
|
EU/2/05/054/001-031 |
9.9.2008 |
|||||
|
9.9.2008 |
||||||||
|
15.9.2008 |
Oxyglobin |
|
EU/2/99/015/002 |
17.9.2008 |
|||||
|
19.9.2008 |
DRAXXIN |
|
EU/2/03/041/001-005 |
23.9.2008 |
|||||
|
26.9.2008 |
PRAC-TIC |
|
EU/2/06/066/001-012 |
30.9.2008 |
— Τροποποίηση άδειας κυκλοφορίας [Άρθρο 38 του κανονισμού (ΕΚ) αριθ. 726/2004]: Απορρίπτεται
|
Ημερομηνία της απόφασης |
Ονομασία του φαρμάκου |
Κάτοχος της άδειας κυκλοφορίας |
Αριθμός εγγραφής στο κοινοτικό μητρώο |
Ημερομηνία κοινοποίησης |
||||
|
26.9.2008 |
Porcilis Pesti |
|
EU/2/99/016/001-006 |
30.9.2008 |
Οι ενδιαφερόμενοι που επιθυμούν να προμηθευτούν τη δημόσια έκθεση αξιολόγησης των εν λόγω φαρμάκων και των σχετικών αποφάσεων μπορούν να απευθυνθούν στην εξής διεύθυνση:
|
The European Medicines Agency |
|
7 Westferry Circus |
|
Canary Wharf |
|
London E14 4HB |
|
United Kingdom |
(1) ΕΕ L 136 της 30.4.2004, σ. 1.
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/9 |
Σύνοψη των κοινοτικών αποφάσεων σχετικά με τις άδειες κυκλοφορίας των φαρμάκων από τη 1 Σεπτεμβρίου 2008 έως τις 30 Σεπτεμβρίου 2008
[Αποφάσεις δυνάμει του άρθρου 34 της οδηγίας 2001/83/ΕΚ του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου (1) ή του άρθρου 38 της οδηγίας 2001/82/ΕΚ του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου (2) ]
(2008/C 276/03)
— Έκδοση, διατήρηση ή τροποποίηση εθνικής άδειας κυκλοφορίας
|
Ημερομηνία της απόφασης |
Ονομασία(-ες) του φαρμάκου |
Κάτοχος(-οι) της άδειας κυκλοφορίας |
Σχετικό κράτος μέλος |
Ημερομηνία κοινοποίησης |
|||||
|
3.9.2008 |
Cozaar |
Βλέπε παράρτημα I |
Βλέπε παράρτημα I |
8.9.2008 |
|||||
|
3.9.2008 |
Cozaar Comp |
Βλέπε παράρτημα II |
Βλέπε παράρτημα II |
8.9.2008 |
|||||
|
9.9.2008 |
Arcoxia |
Βλέπε παράρτημα III |
Βλέπε παράρτημα III |
11.9.2008 |
|||||
|
9.9.2008 |
Etoricoxib |
Βλέπε παράρτημα IV |
Βλέπε παράρτημα IV |
11.9.2008 |
|||||
|
11.9.2008 |
Activelle |
Βλέπε παράρτημα V |
Βλέπε παράρτημα V |
15.9.2008 |
|||||
|
11.9.2008 |
Rapinyl |
Βλέπε παράρτημα VI |
Βλέπε παράρτημα VI |
15.9.2008 |
|||||
|
15.9.2008 |
Remeron |
Βλέπε παράρτημα VII |
Βλέπε παράρτημα VII |
17.9.2008 |
|||||
|
23.9.2008 |
Gemzar |
Βλέπε παράρτημα VIII |
Βλέπε παράρτημα VIII |
24.9.2008 |
|||||
|
26.9.2008 |
Σαλικυλικό νάτριο |
Βλέπε παράρτημα IX |
Βλέπε παράρτημα IX |
29.9.2008 |
|||||
|
26.9.2008 |
Toltrazuril |
Βλέπε παράρτημα X |
Βλέπε παράρτημα X |
29.9.2008 |
|||||
|
26.9.2008 |
Aclasta |
|
Η παρούσα απόφαση απευθύνεται στα κράτη μέλη |
29.9.2008 |
— Αναστολή εθνικής άδειας κυκλοφορίας
|
Ημερομηνία της απόφασης |
Ονομασία(-ες) του φαρμάκου |
Κάτοχος(-οι) της άδειας κυκλοφορίας |
Σχετικό κράτος μέλος |
Ημερομηνία κοινοποίησης |
|
9.9.2008 |
Pulairmax |
Βλέπε παράρτημα XI |
Βλέπε παράρτημα XI |
11.9.2008 |
— Άρση της αναστολής της εθνικής άδειας
|
Ημερομηνία της απόφασης |
Ονομασία(-ες) του φαρμάκου |
Κάτοχος(-οι) της άδειας κυκλοφορίας |
Σχετικό κράτος μέλος |
Ημερομηνία κοινοποίησης |
|
5.9.2008 |
Suramox 15 % LA — Stabox 15 % LA |
Βλέπε παράρτημα XII |
Βλέπε παράρτημα XII |
9.9.2008 |
(1) ΕΕ L 311 της 28.11.2001, σ. 67.
(2) ΕΕ L 311 της 28.11.2001, σ. 1.
ΠΑΡΑΡΤΗΜΑ Ι
ΚΑΤΑΛΟΓΟΣ ΤΩΝ ΟΝΟΜΑΣΙΩΝ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗΣ(-ΩΝ) ΜΟΡΦΗΣ(-ΩΝ), ΠΕΡΙΕΚΤΙΚΟΤΗΤΑΣ(-ΩΝ) ΟΔΟΥ(-ΩΝ) ΧΟΡΗΓΗΣΗΣ ΤΟΥ (ΤΩΝ) ΦΑΡΜΑΚΕΥΤΙΚΟΥ(-ΩΝ) ΠΡΟΪΟΝΤΟΣ(-ΩΝ), ΚΑΤΟΧΟΣ(-ΟΙ) ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος άδειας κυκλοφορίας |
Επινοηθείσα ονομασία Losartan potassium |
Περιεκτικότητα |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
||||||
|
Αυστρία |
|
Cosaar 12,5 mg — Filmtabletten |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Αυστρία |
|
Cosaar 50 mg — Filmtabletten |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Αυστρία |
|
Cosaar 100 mg — Filmtabletten |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Cozaar 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Cozaar 50 MG |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Cozaar 12,5 mg |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Cozaar Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Loortan 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Loortan 50 mg |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Loortan 12,50 mg |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Loortan Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Βουλγαρία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Κύπρος |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Κύπρος |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Δανία |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Δανία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Δανία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Δανία |
|
Cozaar Startpakke |
12,5 mg + 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Εσθονία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Εσθονία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Εσθονία |
|
Cozaar 12,5 mg |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Φινλανδία |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Φινλανδία |
|
Cozaar |
12,5 mg and 50 mg (initiation pack) |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Φινλανδία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Φινλανδία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γαλλία |
|
Cozaar 100 mg film-coated tablets |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γαλλία |
|
Cozaar 50 mg scored coated tablets |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Cardopal Start 12,5 mg Filmtabletten |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Lorzaar 100 mg Filmtabletten |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Lorzaar 50 mg Filmtabletten |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Lorzaar Protect 100 mg Filmtabletten |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Lorzaar Protect 50 mg Filmtabletten |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Lorzaar Start 12,5 mg Filmtabletten |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Pinzaar 100 mg Filmtabletten |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Pinzaar 50 mg Filmtabletten |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Lorzaar Varipharmstart 12,5 mg Filmtabletten |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ελλάδα |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ελλάδα |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ελλάδα |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ουγγαρία |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ουγγαρία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ουγγαρία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιρλανδία |
|
Cozaar 50 mg Film-coated tablets |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιρλανδία |
|
Cozaar 100 mg Film-coated tablets |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιρλανδία |
|
Cozaar 12,5 mg Film-coated tablets |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Lortaan 50 mg compresse rivestite con film |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Lortaan 12,5 mg compresse rivestite con film |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Lortaan 100 mg compresse rivestite con film |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Neo-Lotan 50 mg compresse rivestite con film |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Neo-Lotan 12,5 mg compresse rivestite con film |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Neo-Lotan 100 mg compresse rivestite con film |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Losaprex 50 mg compresse rivestite con film |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Losaprex 12,5 mg compresse rivestite con film |
12.5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Losaprex 100 mg compresse rivestite con film |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λεττονία |
|
Cozaar 50 mg film-coated tablets |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λεττονία |
|
Cozaar 100 mg film-coated tablets |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λιθουανία |
|
Cozaar (Losartan) |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λιθουανία |
|
Cozaar (Losartan) |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λιθουανία |
|
Cozaar (Losartan) |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Cozaar 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Cozaar 50 MG |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Cozaar 12,5 mg |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Cozaar Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Loortan 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Loortan 50 mg |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Loortan 12,50 mg |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Loortan Cardio Start |
21 X 12,5 mg + 14 X 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Μάλτα |
|
“Cozaar 100 mg” pilloli miksija b'rita |
10 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Μάλτα |
|
“Cozaar 50 mg” pilloli miksija b'rita |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Κάτω Χώρες |
|
Cozaar 50 |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Κάτω Χώρες |
|
Cozaar 100 |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πολωνία |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πολωνία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πολωνία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Cozaar 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Cozaar IC |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Cozaar IC — Titulação |
12,5 mg + 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Lortaan IC |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Lortaan IC — Titulação |
12,5 mg + 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Lortaan |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Lortaan 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ρουμανία |
|
Cozaar, comprimate filmate, 50 mg |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σλοβενία |
|
Cozaar 12,5 mg filmsko obložene tablete |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σλοβενία |
|
Cozaar 50 mg filmsko obložene tablete |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σλοβενία |
|
Cozaar 100 mg filmsko obložene tablete |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ισπανία |
|
Cozaar 12,5 mg Inicio |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ισπανία |
|
Cozaar 50 mg |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ισπανία |
|
Cozaar 100 mg |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σοηδία |
|
Cozaar 12,5 mg filmdragerade tabletter |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σοηδία |
|
Cozaar 12,5 mg + 50 mg filmdragerade tabletter |
12,5 + 50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σοηδία |
|
Cozaar 50 mg filmdragerade tabletter |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Σοηδία |
|
Cozaar 100 mg filmdragerade tabletter |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ηνωμένο Βασίλειο |
|
Cozaar 50 mg Film-coated tablets |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ηνωμένο Βασίλειο |
|
Cozaar 25 mg Film-coated tablets |
25 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ηνωμένο Βασίλειο |
|
Cozaar 100 mg Film-coated tablets |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ισλανδία |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ισλανδία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Ισλανδία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Νορβηγία |
|
Cozaar |
12,5 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Νορβηγία |
|
Cozaar |
50 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
||||||
|
Νορβηγία |
|
Cozaar |
100 mg |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
ΠΑΡΑΡΤΗΜΑ ΙI
ΚΑΤΑΛΟΓΟΣ ΤΩΝ ΟΝΟΜΑΣΙΩΝ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗΣ(-ΩΝ) ΜΟΡΦΗΣ(-ΩΝ), ΠΕΡΙΕΚΤΙΚΟΤΗΤΑΣ(-ΩΝ) ΟΔΟΥ(-ΩΝ) ΧΟΡΗΓΗΣΗΣ ΤΟΥ (ΤΩΝ) ΦΑΡΜΑΚΕΥΤΙΚΟΥ(-ΩΝ) ΠΡΟΪΟΝΤΟΣ(-ΩΝ), ΚΑΤΟΧΟΣ(-ΟΙ) ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος άδειας κυκλοφορίας |
Επινοηθείσα ονομασία Losartan potassium και hydrochlorothiazide |
Περιεκτικότητα |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
|||||||
|
Αυστρία |
|
Cosaar Plus — Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Αυστρία |
|
Fortzaar-Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Βέλγιο |
|
Cozaar Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Βέλγιο |
|
Cozaar Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Βέλγιο |
|
Loortan Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Βέλγιο |
|
Loortan Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Βουλγαρία |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Κύπρος |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Κύπρος |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Δανία |
|
Cozaar Comp. |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Δανία |
|
Cozaar Comp. Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Δανία |
|
Cozaar Comp. 100 mg/12,5 mg |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Δανία |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Εσθονία |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Εσθονία |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Φινλανδία |
|
Cozaar Comp |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Φινλανδία |
|
Cozaar Comp |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Φινλανδία |
|
Cozaar Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γαλλία |
|
Fortzaar 100 mg/25 mg comprimé pelliculé |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γαλλία |
|
Hyzaar 100 mg/25 mg comprimé pelliculé |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γαλλία |
|
Fortzaar 50 mg/12,5 mg comprimé pelliculé |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γαλλία |
|
Hyzaar 50 mg/12,5 mg comprimé pelliculé |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γαλλία |
|
Fortzaar 100 mg/12,5 mg comprimé pelliculé |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Lorzaar Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Cardopal Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Lorzaar Varipharm Plus 50/12,5 mg Filmtabletten |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Fortzaar 100/25 mg Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Fortzaar Varipharm 100/25 mg Filmtabletten |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Lorzaar Plus Forte 100/12,5 mg Filmtabletten |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ελλάδα |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ελλάδα |
|
Hyzaar 100/25 |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ουγγαρία |
|
Hyzaar 50/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ουγγαρία |
|
Hyzaar Forte 100/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιρλανδία |
|
Cozaar' Comp 50 mg/12,5 mg film-coated tablets |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιρλανδία |
|
Cozaar' Comp 100 mg/25 mg film-coated tablets |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Hizaar 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Hizaar 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Forzaar 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Neo-Lotan Plus 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Neo-Lotan Plus 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Losazid 50 mg + 12,5 mg compresse rivestite con film |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Losazid 100 mg + 25 mg compresse rivestite con film |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λεττονία |
|
Hyzaar 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λεττονία |
|
Fortzaar 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λιθουανία |
|
Fortzaar (Losartan/Hydrochlorothiazide) |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λιθουανία |
|
Hyzaar (Losartan/Hydrochlorothiazide) |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λουξεμβούργο |
|
Cozaar Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λουξεμβούργο |
|
Cozaar Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λουξεμβούργο |
|
Loortan Plus Forte 100 mg/25 mg |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Λουξεμβούργο |
|
Loortan Plus 50 mg/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Μάλτα |
|
“Cozaar Comp” 50/12,5 mg pilloli miksija b'rita |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Μάλτα |
|
“Cozaar Comp” 100/25 mg pilloli miksija b'rita |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Μάλτα |
|
“Cozaar Comp” 100/12,5 mg pilloli miksija b'rita |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Κάτω Χώρες |
|
Cozaar Plus 100/12,5 |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Κάτω Χώρες |
|
Fortzaar 100/25 |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Κάτω Χώρες |
|
Hyzaar 50/12,5 |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πολωνία |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πολωνία |
|
Hyzaar Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Cozaar Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Cozaar Plus |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Siaara |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Lortaan Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Lortaan Plus |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Losartan + Hidroclorotiazida Frosst |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ρουμανία |
|
Hyzaar® 50 mg/12,5 mg comprimate filmate |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ρουμανία |
|
Fortzaar® 100/25 mg comprimate filmate |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Σλοβενία |
|
Hyzaar |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Σλοβενία |
|
Hyzaar |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Σλοβενία |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ισπανία |
|
Cozaar Plus |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ισπανία |
|
Fortzaar |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Σουηδία |
|
Cozaar Comp 50 mg/12,5 mg filmdragerade tabletter |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Σουηδία |
|
Cozaar Comp 100 mg/12,5 mg filmdragerade tabletter |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Σουηδία |
|
Cozaar Comp Forte 100 mg/25 mg filmdragerade tabletter |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ηνωμένο Βασίλειο |
|
Cozaar-Comp 50/12,5 mg film-coated tablets |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ηνωμένο Βασίλειο |
|
Cozaar-Comp 100/25 mg film-coated tablets |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ηνωμένο Βασίλειο |
|
Cozaar-Comp 100 mg/12,5 mg film-coated tablets |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ισλανδία |
|
Cozaar-Comp 50/12,5 mg |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ισλανδία |
|
Cozaar-Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Ισλανδία |
|
Cozaar-Comp 100/12,5 mg |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Νορβηγία |
|
Cozaar Comp |
50 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Νορβηγία |
|
Cozaar Comp |
100 mg losartan potassium — 12,5 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
|||||||
|
Νορβηγία |
|
Cozaar Comp Forte |
100 mg losartan potassium — 25 mg hydrochlorothiazide |
Επικαλυμμένο με λεπτό υμένιο δισκίο |
Από στόματος χρήση |
ΠΑΡΑΡΤΗΜΑ ΙII
ΚΑΤΑΣΤΑΣΗ ΜΕ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΗ ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ(-ΕΣ) ΜΟΡΦΗ(-ΕΣ), ΤΙΣ (ΤΗΝ) ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ(-Α) ΤΩΝ (ΤΟΥ) ΦΑΡΜΑΚΕΥΤΙΚΩΝ(-ΟΥ) ΠΡΟΪΟΝΤΩΝ(-ΟΣ), ΤΗΝ (ΤΙΣ) ΟΔΟ(-ΟΥΣ) ΧΟΡΗΓΗΣΗΣ, ΤΟΝ (ΤΟΥΣ) ΑΙΤΟΥΝΤΑ(-ΕΣ), ΤΟΝ (ΤΟΥΣ) ΚΑΤΟΧΟ(-ΟΥΣ) ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος της άδειας κυκλοφορίας |
Επινοηθείσα ονομασία |
Περιεκτικότητα |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
||||||
|
Αυστρία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Βέλγιο |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Τσεχική Δημοκρατία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Κύπρος |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Δανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Εσθονία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Φινλανδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Γαλλία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Γερμανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ελλάδα |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ουγγαρία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ισλανδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ιρλανδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ιταλία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Λεττονία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Λιθουανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Λουξεμβούργο |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Μάλτα |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Κάτω Χώρες |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Νορβηγία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Πολωνία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Πορτογαλία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Σλοβακία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Σλοβενία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ισπανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Σουηδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
||||||
|
Ηνωμένο Βασίλειο |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
ΠΑΡΑΡΤΗΜΑ ΙV
ΚΑΤΑΣΤΑΣΗ ΜΕ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΗ ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ(-ΕΣ) ΜΟΡΦΗ(-ΕΣ), ΤΙΣ (ΤΗΝ) ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ(-Α) ΤΩΝ (ΤΟΥ) ΦΑΡΜΑΚΕΥΤΙΚΩΝ(-ΟΥ) ΠΡΟΪΟΝΤΩΝ(-ΟΣ), ΤΗΝ (ΤΙΣ) ΟΔΟ(-ΟΥΣ) ΧΟΡΗΓΗΣΗΣ, ΤΟΝ (ΤΟΥΣ) ΑΙΤΟΥΝΤΑ(-ΕΣ), ΤΟΝ (ΤΟΥΣ) ΚΑΤΟΧΟ(-ΟΥΣ) ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος της άδειας κυκλοφορίας |
Επινοηθείσα ονομασία |
Περιεκτικότητα |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
|||||||
|
Αυστρία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Auxib |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Βέλγιο |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ranacox |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Βουλγαρία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Τσεχική Δημοκρατία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Κύπρος |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Δανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Εσθονία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Φινλανδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Turox |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Γαλλία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Γερμανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ελλάδα |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ουγγαρία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ισλανδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ιρλανδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Algix |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Recoxib |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ιταλία |
|
Tauxib |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Λεττονία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Λιθουανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Λουξεμβούργο |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ranacox |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Μάλτα |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Κάτω Χώρες |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Auxib |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Νορβηγία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Πολωνία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Exxiv |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Πορτογαλία |
|
Turox |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ρουμανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Σλοβακία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Σλοβενία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ισπανία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Ισπανία |
|
Exxiv |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Σουηδία |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Turox |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Ηνωμένο Βασίλειο |
|
Arcoxia |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||
|
Auxib 90 |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Exxiv 90 |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
|||||||||
|
Turox 90 |
90 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από στόματος χρήση |
ΠΑΡΑΡΤΗΜΑ V
ΚΑΤΑΛΟΓΟΣ ΕΜΠΟΡΙΚΩΝ ΟΝΟΜΑΤΩΝ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗΣ ΜΟΡΦΗΣ, ΠΕΡΙΕΚΤΙΚΟΤΗΤΑΣ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ, ΟΔΟΥ ΧΟΡΗΓΗΣΗΣ, ΑΙΤΟΥΝΤΩΝ/ΚΑΤΟΧΩΝ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΙΣ ΧΩΡΕΣ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος της άδειας κυκλοφορίας |
Αιτών |
Εμπορική ονομασία |
Περιεκτικότητα |
Φαρμακοτεκτική μορφή |
Οδός χορήγησης |
|||||
|
Αυστρία |
|
|
Noviana 0,5 mg/0,1 mg Filmtabletten |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Βέλγιο |
|
|
Activelle minor comprimés pelliculés |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Βουλγαρία |
|
|
Eviana филмирани таблетки |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Τσεχική Δημοκρατία |
|
|
Noviana potahované tablety |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Δανία |
|
|
Activelle low filmovertrukne tabletter |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Εσθονία |
|
|
Activelle |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Φινλανδία |
|
|
Activelle 0,5 mg/0,1 mg tabl. |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Γαλλία |
|
|
Activelle 0,5 mg/0,1 mg, comprimé pelliculé |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Γερμανία |
|
|
Noviana |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ουγγαρία |
|
|
Noviana filmtabletta |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ισλανδία |
|
|
Activelle low 0,5 mg/0,1 mg tablets filmuhúðaðar töflur |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ιρλανδία |
|
|
Activelle Tablets |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ιταλία |
|
|
Activelle 0,5 mg/0,1 mg compresse film-rivestite |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Λεττονία |
|
|
Noviana 0,5 mg/0,1 mg apvalkotās tabletes |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Λιθουανία |
|
|
Activelle |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Λουξεμβούργο |
|
|
Activelle comprimés pelliculés |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Κάτω Χώρες |
|
|
Activelle filmomhulde tabletten |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Νορβηγία |
|
|
Noviana 0,5 mg/0,1 mg tablett filmdrasjert |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Πορτογαλία |
|
|
Activelle |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ρουμανία |
|
|
Noviana comprimate filmate |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Σλοβακική Δημοκρατία |
|
|
Noviana |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Σλοβενία |
|
|
Noviana filmsko obložene tablete |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ισπανία |
|
|
Activelle 0,5 mg/ 0,1 mg comprimidos recubiertos de película |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Σουηδία |
|
|
Activelle |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
|||||
|
Ηνωμένο Βασίλειο |
|
|
Noviana film-coated tablets |
Οιστραδιόλη (ως ημιυδρική) 0.5 mg + Οξική νορεθιστερόνη 0.1 mg |
Δισκία επικαλυμμένα με υμένιο |
Από στόματος χρήση |
ΠΑΡΑΡΤΗΜΑ VΙ
ΛΙΣΤΑ ΟΝΟΜΑΣΙΩΝ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗΣ ΜΟΡΦΗΣ, ΠΕΡΙΕΚΤΙΚΟΤΗΤΩΝ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ, ΟΔΟΣ ΧΟΡΗΓΗΣΗΣ, ΑΙΤΟΥΝΤΕΣ ΚΑΙ ΚΑΤΟΧΟΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος άδειας κυκλοφορίας |
Αιτών |
(Επινοηθείσα) Ονομασία |
Περιεκτικότητα |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
||||
|
Αυστρία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Βέλγιο |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Κύπρος |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Τσεχική Δημοκρατία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Δανία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Εσθονία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Φινλανδία |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Γαλλία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Γερμανία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ελλάδα |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ουγγαρία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ισλανδία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ιρλανδία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ιταλία |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Λεττονία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Λιθουανία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Λουξεμβούργο |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Νορβηγία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Πολωνία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Πορτογαλία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Σλοβακία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Σλοβενία |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ισπανία |
|
|
Rapinyl (1) |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Σουηδία |
|
|
Abstral |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
||||
|
Ηνωμένο Βασίλειο |
|
|
Rapinyl |
50 μg 100 μg 200 μg 300 μg 400 μg 600 μg 800 μg |
Υπογλώσσιο δισκίο |
Υπογλώσσια χρήση |
(1) Αναμένεται έγκριση ονομασίας.
ΠΑΡΑΡΤΗΜΑ VII
ΚΑΤΑΣΤΑΣΗ ΜΕ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΙΣ ΦΑΡΜΑΚΟΤΕΧΝΙΚΕΣ ΜΟΡΦΕΣ, ΤΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ, ΤΙΣ ΟΔΟΥΣ ΧΟΡΗΓΗΣΗΣ, ΤΟΥΣ ΚΑΤΟΧΟΥΣ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος άδειας κυκλοφορίας |
INN |
Επινοηθείσα ονομασία |
Δυναμικότητα |
Φαρμακευτική μορφή |
Οδός χορήγησης |
Περιεκτικότητα (συγκέντρωση) |
|||||||
|
Αυστρία |
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab Schmelztabletten |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Βέλγιο |
Delegation of power:
|
Mirtazapine |
Remergon |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remergon |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Κύπρος |
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Τσεχική Δημοκρατία |
|
Mirtazapine |
REMERON 15 MG |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
REMERON 30 MG |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON 45 MG |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 15 MG |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 30 MG |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON SOLTAB 45 MG |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Δανία |
|
Mirtazapine |
Mitazon Smelt |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Mitazon Smelt |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mitazon Smelt |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mitazon |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
||||||||
|
Mirtazapine |
Remeron Smelt |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Oral, opløsning |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Εσθονία |
|
Mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Φινλανδία |
|
Mirtazapine |
Remeron Soltab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron Soltab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Soltab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazon |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
||||||||
|
Mirtazapine |
Mirtazon Smelt |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazon Smelt |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazon Smelt |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Γαλλία |
|
Mirtazapine |
Norset |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Norset |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Norset |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Norset |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Norset |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Norset |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Γερμανία |
|
Mirtazapine |
Remergil |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remergil |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergil |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergil SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergil |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazapin STADA |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
||||||||
|
Mirtazapine |
Mirtazapin STADA |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapin STADA |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Ελλάδα |
|
Mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Ουγγαρία |
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Ισλανδία |
|
Mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Smelt |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron 15 mg/ml |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Ιρλανδία |
|
Mirtazapine |
Zispin® film-coated tablets |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Zispin® film-coated tablets |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Zispin® film-coated tablets |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Zispin® Soltab® orodispersible tablets |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Zispin® oral solution |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Ιταλία |
|
mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Λεττονία |
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Λιθουανία |
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron Sol Tab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Sol Tab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron Sol Tab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Λουξεμβούργο |
Delegation of power:
|
Mirtazapine |
Remergon |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remergon |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remergon |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Κάτω Χώρες |
|
Mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron drank |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapine orodispergeerbare tabletten |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Νορβηγία |
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron-S smeltetabletter |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron mikstur, oppløsning |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Πολωνία |
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Πορτογαλία |
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazon |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
||||||||
|
Mirtazapine |
Mirtazon |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazon |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Ρουμανία |
|
Mirtazapine |
Remeron SolTab 15 mg |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron SolTab 30 mg |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron SolTab 45 mg |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Σλοβακική Δημοκρατία |
|
Mirtazapine |
REMERON 15 mg |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
REMERON 30 mg |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON 45 mg |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 15 mg |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 30 mg |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
REMERON Soltab 45 mg |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Ισπανία |
|
Mirtazapine |
Rexer |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Rexer |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Rexer |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Rexer Flas |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Rexer |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
||||||||
|
Mirtazapine |
Mirtazapina Organon |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapina Organon |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Σουηδία |
|
Mirtazapine |
Remeron |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Remeron |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Remeron-S |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron-S |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Remeron-S |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapin IP |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Ηνωμένο Βασίλειο |
|
Mirtazapine |
Mirtazapine 15 mg tablets |
15 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||
|
Mirtazapine |
Mirtazapine 30 mg tablets |
30 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapine 45 mg tablets |
45 mg |
Επικαλυμμένα με λεπτό υμένιο δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Mirtazapine 15 mg/ml oral solution |
15 mg/ml |
Πόσιμο διάλυμα |
Από του στόματος χρήση |
990 mg/66 ml |
|||||||||
|
Mirtazapine |
Zispin SolTab 15 mg orodispersible tablet |
15 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Zispin SolTab 30 mg orodispersible tablet |
30 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
|||||||||
|
Mirtazapine |
Zispin SolTab 45 mg orodispersible tablet |
45 mg |
Διασπειρόμενα στο στόμα δισκία |
Από του στόματος χρήση |
|
ΠΑΡΑΡΤΗΜΑ VIII
ΚΑΤΑΣΤΑΣΗ ΜΕ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΙΣ ΦΑΡΜΑΚΟΤΕΧΝΙΚΕΣ ΜΟΡΦΕΣ, ΤΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ, ΤΗΝ ΟΔΟ ΧΟΡΗΓΗΣΗΣ, ΤΟΥΣ ΑΙΤΟΥΝΤΕΣ, ΤΟΥΣ ΚΑΤΟΧΟΥΣ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος άδειας κυκλοφορίας |
Επινοηθείσα ονομασία |
Συγκέντρωση |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
||||||
|
Αυστρία |
|
Gemzar 200 mg — Trockensubstanz zur Infusionsbereitung |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Αυστρία |
|
Gemzar 1 g — Trockensubstanz zur Infusionsbereitung |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Βέλγιο |
|
Gemzar 1000 |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Βέλγιο |
|
Gemzar 200 |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Βουλγαρία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Βουλγαρία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Τσεχική Δημοκρατία |
|
Gemzar 1 g |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Τσεχική Δημοκρατία |
|
Gemzar 200 mg |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Κύπρος |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Κύπρος |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Δανία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Δανία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Εσθονία |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Εσθονία |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Φινλανδία |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Φινλανδία |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Γαλλία |
|
Gemzar 1 000 mg, poudre pour solution pour perfusion |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Γαλλία |
|
Gemzar 200 mg, poudre pour solution pour perfusion |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Γερμανία |
|
Gemzar 200 mg Pulver zur Herstellung einer Infusionslösung |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Γερμανία |
|
Gemzar 1 g Pulver zur Herstellung einer Infusionslösung |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ελλάδα |
|
ΓΚΕΜΖΑΡ |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ελλάδα |
|
ΓΚΕΜΖΑΡ |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ουγγαρία |
|
Gemzar 1 g powder for injection |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ουγγαρία |
|
Gemzar 200 mg powder for injection |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ιρλανδία |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ιρλανδία |
|
Gemzar 1 g powder for solution for infusion |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ισλανδία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ισλανδία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ιταλία |
|
Gemzar 200 mg powder for solution for infusion and intravesical instillation |
200 mg |
Kόνις για διάλυμα προς έγχυση και ενδοκυστική ενστάλαξη |
Eνδοφλέβια χρήση και ενδοκυστική χρήση |
||||||
|
Ιταλία |
|
Gemzar 1 g powder for solution for infusion and intravesical instillation |
1 g |
Kόνις για διάλυμα προς έγχυση και ενδοκυστική ενστάλαξη |
Eνδοφλέβια χρήση και ενδοκυστική χρήση |
||||||
|
Λεττονία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Λεττονία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Λιθουανία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Λιθουανία |
|
Gemzar |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Λουξεμβούργο |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Λουξεμβούργο |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Μάλτα |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Μάλτα |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Κάτω Χώρες |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Κάτω Χώρες |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Νορβηγία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Νορβηγία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Πολωνία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Πολωνία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Πορτογαλία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Πορτογαλία |
|
Gemzar |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ρουμανία |
|
Gemzar 1 g |
1 000 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ρουμανία |
|
Gemzar 200 mg |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Σλοβακία |
|
Gemzar 1 g |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Σλοβακία |
|
Gemzar 200 mg |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Σλοβενία |
|
Gemzar 200 mg prašek za raztopino za infundiranje |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Σλοβενία |
|
Gemzar 1 g prašek za raztopino za infundiranje |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ισπανία |
|
Gemzar 1 g powder for solution for injection |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ισπανία |
|
Gemzar 200 mg powder for solution for injection |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Σουηδία |
|
Gemzar |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Σουηδία |
|
Gemzar |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ηνωμένο Βασίλειο |
|
Gemzar 200 mg powder for solution for infusion |
200 mg |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
||||||
|
Ηνωμένο Βασίλειο |
|
Gemzar 1g powder for solution for infusion |
1 g |
Kόνις για διάλυμα προς έγχυση |
Eνδοφλέβια χρήση |
ΠΑΡΑΡΤΗΜΑ ΙX
ΟΝΟΜΑΣΙΑ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ, ΠΕΡΙΕΚΤΙΚΟΤΗΤΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ, ΖΩΙΚΑ ΕΙΔΗ, ΟΔΟΙ ΧΟΡΗΓΗΣΗΣ, ΚΑΙ ΚΑΤΟΧΟΣ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ/ΑΙΤΩΝ
|
Κράτος μέλος/αριθμός άδειας κυκλοφορίας |
Κάτοχος της άδειας κυκλοφορίας |
Επινοηθείσα ονομασία προϊόντος |
Φαρμακοτεχνική μορφή |
Περιεκτικότητα/δραστική ουσία (κοινόχρηστη διεθνής ονομασία) |
Ζωικό είδος |
|
Αυστρία (8-00694) |
Chevita Tierarzneimittel Ges.m.b.H. |
Asprimax 850 mg/g |
Κόνις για πόσιμο διάλυμα |
Σαλικυλικό νάτριο |
Χοίροι |
|
Κάτω Χώρες (REG NL 8913) |
Dopharma Research B.V. |
NA-SALICYLAAT, 100 %, κόνις για πόσιμο διάλυμα για χορήγηση από το στόμα |
Κόνις για πόσιμο διάλυμα |
Σαλικυλικό νάτριο |
Μόσχοι και Χοίροι |
|
Κάτω Χώρες (REG NL 10411) |
Dopharma Research B.V. |
NA-SALICYLAAT, 80 % WSP |
Κόνις για πόσιμο διάλυμα |
Σαλικυλικό νάτριο |
Μόσχοι και Χοίροι |
|
Αποκεντρωμένη διαδικασία που υπόκειται στο άρθρο 33 της διαδικασίας παραπομπής (CD 17 Απριλίου 2008) |
Eurovet Animal Health B.V. |
SOLACYL 100 %, κόνις για πόσιμο διάλυμα για μόσχους και χοίρους |
Κόνις για πόσιμο διάλυμα |
|
Μόσχοι και Χοίροι |
ΠΑΡΑΡΤΗΜΑ X
ΚΑΤΑΣΤΑΣΗ ΠΕΡΙΕΧΟΥΣΑ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΙΣ ΦΑΡΜΑΚΟΤΕΧΝΙΚΕΣ ΜΟΡΦΕΣ, ΤΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ ΚΤΗΝΙΑΤΡΙΚΗΣ ΧΡΗΣΗΣ, ΤΑ ΖΩΙΚΑ ΕΙΔΗ, ΤΙΣ ΟΔΟΥΣ ΧΟΡΗΓΗΣΗΣ ΚΑΙ ΤΟΥΣ ΚΑΤΟΧΟΥΣ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Επινοηθείσα ονομασία |
Κάτοχος της άδειας κυκλοφορίας Όνομα εταιρείας και Διεύθυνση |
Ζωικό είδος |
Φαρμακοτεχνική μορφή |
Περιεκτικότητα |
Ενδείξεις |
||||||||
|
Αυστρία |
Baycox 25 mg/ml Lösung zum Eingeben für Hühner und Puten |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Βέλγιο |
Baycox 2,5 % orale oplossing |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Βουλγαρία |
Baycox 2,5 % solution |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Βουλγαρία |
Cevazuril oral solution |
|
Ορνίθια κρεατοπαραγωγής, όρνιθες αναπαραγωγής, νεαρές όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Πρόληψη και θεραπεία της κοκκιδίωσης |
||||||||
|
Κύπρος |
Baycox 2,5 % oral solution |
|
Ορνίθια κρεατοπαραγωγής και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Τσεχική Δημοκρατία |
Baycox 2,5 % sol. ad us. vet. |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Γαλλία |
Baycox 2,5 % |
|
Όρνιθες: ορνίθια κρεατοπαραγωγής, νεαρές όρνιθες και ορνίθια αναπαραγωγής |
Πόσιμο διάλυμα |
25 mg/ml |
Πρόληψη και θεραπεία της κοκκιδίωσης |
||||||||
|
Γαλλία |
CEVAZURIL |
|
Όρνιθες: ορνίθια κρεατοπαραγωγής, νεαρές όρνιθες και ορνίθια αναπαραγωγής |
Πόσιμο διάλυμα |
25 mg/ml |
Πρόληψη και θεραπεία της κοκκιδίωσης |
||||||||
|
Γερμανία |
Baycox 2,5 % |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Ελλάδα |
Baycox 2,5 % oral solution |
|
Ορνίθια κρεατοπαραγωγής και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Ουγγαρία |
Baycox 2,5 % solution A.U.V. |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Ιρλανδία |
Baycox 2,5 % Solution |
|
Όρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία και ελεγχος της κοκκιδίωσης |
||||||||
|
Ιταλία |
Baycox soluzione 2,5 % |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Ιταλία |
Cevazuril (1) |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Πολωνία |
Baycox 2,5 % |
|
Ορνίθια κρεατοπαραγωγής, ορνίθια αναπαραγωγής, ινδόρνιθες και περιστέρια |
Πόσιμο διάλυμα |
25 mg/ml |
Όρνιθες και ινδόρνιθες: Θεραπεία της κοκκιδίωσηςΠεριστέρια: Θεραπεία και πρόληψη της κοκκιδίωσης |
||||||||
|
Πορτογαλία |
Baycox 2,5 % oral solution |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Ρουμανία |
Cevazuril |
|
Ορνίθια κρεατοπαραγωγής, ορνίθια αναπαραγωγής, νεαρές όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Σλοβακία |
Baycox 2,5 % sol. a.u.v. |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Σλοβενία |
Baycox 2,5 % w/v oral solution |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Κάτω Χώρες |
Baycox 2,5 % |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Κάτω Χώρες |
Baycox oplossing 2,5 % |
|
Όρνιθες και ινδόρνιθες |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
||||||||
|
Ηνωμένο Βασίλειο |
Baycox 2,5 % oral solution |
|
Ορνίθια κρεατοπαραγωγής και ορνίθια αναπαραγωγής |
Πόσιμο διάλυμα |
25 mg/ml |
Θεραπεία της κοκκιδίωσης |
(1) Η άδεια κυκλοφορίας ανεστάλη στις 12 Ιουνίου 2007.
ΠΑΡΑΡΤΗΜΑ XΙ
ΚΑΤΑΣΤΑΣΗ ΜΕ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΗ ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ, ΤΗΝ (ΤΙΣ) ΠΕΡΙΕΚΤΙΚΟΤΗΤΑ(-ΕΣ) ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ, ΤΗΝ ΟΔΟ ΧΟΡΗΓΗΣΗΣ, ΤΟΝ ΑΙΤΟΥΝΤΑ ΚΑΙ ΤΟΝ ΚΑΤΟΧΟ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
Κράτος μέλος |
Κάτοχος της άδειας κυκλοφορίας |
Αιτών |
Επινοηθείσα ονομασία |
Περιεκτικότητα |
Φαρμακοτεχνική μορφή |
Οδός χορήγησης |
Περιεκτικότητα (συγκέντρωση) |
||||||
|
Αυστρία |
|
|
Pulairmax 100 μg/Dosis Pulver zur Inhalation |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg/Dosis Pulver zur Inhalation |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg/Dosis Pulver zur Inhalation |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Βέλγιο |
|
|
Pulairmax 100 μg inhalatiepoeder |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg inhalatiepoeder |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg inhalatiepoeder |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Κύπρος |
|
|
Pulairmax 100 μg Σκόνη για εισπνοή |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg Σκόνη για εισπνοή |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg Σκόνη για εισπνοή |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Τσεχική Δημοκρατία |
|
|
Pulmax 100 μg Prášek k inhalaci |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulmax 200 μg Prášek k inhalaci |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulmax 400 μg Prášek k inhalaci |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Δανία |
|
|
Pulairmax |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Εσθονία |
|
|
Pulairmax |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Φινλανδία |
|
|
Pulairmax 100 μg inhalaatiojauhe |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg inhalaatiojauhe |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg inhalaatiojauhe |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Γερμανία |
|
|
Pulairmax 100 Mikrogramm/Dosis Pulver zur Inhalation |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 Mikrogramm/Dosis Pulver zur Inhalation |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 Mikrogramm/Dosis Pulver zur Inhalation |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Ελλάδα |
|
|
Pulairmax 100 μg Κόνις για εισπνοή |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg Κόνις για εισπνοή |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg Κόνις για εισπνοή |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Ιρλανδία |
|
|
Pulairmax 100 μg Inhalation Powder |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg Inhalation Powder |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg Inhalation Powder |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Ιταλία |
|
|
Pulairmax 100 polvere per inalazione |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 mcg polvere per inalazione |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 mcg polvere per inalazione |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Λεττονία |
|
|
Pulairmax |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Λιθουανία |
|
|
Pulairmax |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Λουξεμβούργο |
|
|
Pulairmax 100 μg poudre pour inhalation |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg poudre pour inhalation |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg poudre pour inhalation |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Μάλτα |
|
|
Pulairmax 100 μg Trab li jittiehed bin-nifs |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg Trab li jittiehed bin-nifs |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg Trab li jittiehed bin-nifs |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Κάτω Χώρες |
|
|
Pulmax 100 mg, inhalatiepoeder |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulmax 200 mg, inhalatiepoeder |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulmax 400 mg, inhalatiepoeder |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Νορβηγία |
|
|
Pulairmax 100 μg inhalasjonspulver |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax 200 μg inhalasjonspulver |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax 400 μg inhalasjonspulver |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Πολωνία |
|
|
Pulmax 100 μg proszek do inhalacji |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulmax 200 μg proszek do inhalacji |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulmax 400 μg proszek do inhalacji |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Πορτογαλία |
|
|
Pulmax, 100 μg pó para inalação |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulmax, 200 μg pó para inalação |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulmax, 400 μg pó para inalação |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Σλοβακική Δημοκρατία |
|
|
Pulmax 100 mcg Inhalačný prášok |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulmax 200 mcg Inhalačný prášok |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulmax 400 mcg Inhalačný prášok |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Ισπανία |
|
|
Budesonida TEVA 100 microgramos polvo para inhalación EFG |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Budesonida TEVA 200 microgramos polvo para inhalación EFG |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Budesonida TEVA 400 microgramos polvo para inhalación EFG |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
|||||||||
|
Σουηδία |
|
|
Pulairmax |
100 μg |
Σκόνη για εισπνοή |
Εισπνοή |
100 μικρογραμμάρια |
||||||
|
Pulairmax |
200 μg |
Σκόνη για εισπνοή |
Εισπνοή |
200 μικρογραμμάρια |
|||||||||
|
Pulairmax |
400 μg |
Σκόνη για εισπνοή |
Εισπνοή |
400 μικρογραμμάρια |
ΠΑΡΑΡΤΗΜΑ XII
ΚΑΤΑΣΤΑΣΗ ΜΕ ΤΙΣ ΟΝΟΜΑΣΙΕΣ, ΤΙΣ ΦΑΡΜΑΚΟΤΕΧΝΙΚΕΣ ΜΟΡΦΕΣ, ΤΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ, ΤΑ ΖΩΙΚΑ ΕΙΔΗ, ΤΗ ΣΥΧΝΟΤΗΤΑ ΚΑΙ ΤΙΣ ΟΔΟΥΣ ΧΟΡΗΓΗΣΗΣ, ΤΙΣ ΣΥΝΙΣΤΩΜΕΝΕΣ ΔΟΣΕΙΣ, ΤΟΥΣ ΧΡΟΝΟΥΣ ΑΝΑΜΟΝΗΣ ΚΑΙ ΤΟΥΣ ΚΑΤΟΧΟΥΣ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΑ ΚΡΑΤΗ ΜΕΛΗ ΠΟΥ ΑΦΟΡΑ Η ΠΑΡΑΠΟΜΠΗ
|
Κράτος μέλος |
Κάτοχος της άδειας κυκλοφορίας |
Έπινοηθείσα ονομασία |
Φαρμακοτεχνική μορφή |
Περιεκτικότητα |
Ζωικό είδος |
Συχνότητα και οδός χορήγησης |
Συνιστώμενη δόση |
Χρόνος αναμονής (Κρέας και γάλα) |
||||
|
Τσεχική Δημοκρατία |
|
Suramox 15 % LA |
Ενέσιμο εναιώρημα |
150 mg/ml |
Βοοειδή, χοίροι |
Δύο ενδομυϊκές ενέσεις σε διάστημα 48 ωρών |
15 mg αμοξικιλλίνης/kg σωματικού βάρους (ισοδυναμεί με 1ml/10 kg) |
Κρέας και εδώδιμοι ιστοί: Βοοειδή: 58 ημέρες Χοίροι: 35 ημέρες Γάλα: 2,5 ημέρες |
||||
|
Ισπανία (1) |
|
Stabox 15 % LA |
Ενέσιμο εναιώρημα |
150 mg/ml |
Βοοειδή, χοίροι |
Δύο ενδομυϊκές ενέσεις σε διάστημα 48 ωρών |
15 mg αμοξικιλλίνης/kg σωματικού βάρους (ισοδυναμεί με 1ml/10 kg) |
Κρέας και εδώδιμοι ιστοί: Βοοειδή: 58 ημέρες Χοίροι: 35 ημέρες Γάλα: 2,5 ημέρες |
||||
|
Ιταλία |
|
Stabox 15 % LA |
Ενέσιμο εναιώρημα |
150 mg/ml |
Βοοειδή, χοίροι |
Δύο ενδομυϊκές ενέσεις σε διάστημα 48 ωρών |
15 mg αμοξικιλλίνης/kg σωματικού βάρους (ισοδυναμεί με 1ml/10 kg) |
Κρέας και εδώδιμοι ιστοί: Βοοειδή: 58 ημέρες Χοίροι: 35 ημέρες Γάλα: 2,5 ημέρες |
||||
|
Γαλλία (2) |
|
Suramox 15 % LA |
Ενέσιμο εναιώρημα |
150 mg/ml |
Βοοειδή, χοίροι |
Δύο ενδομυϊκές ενέσεις σε διάστημα 48 ωρών |
15 mg αμοξικιλλίνης/kg σωματικού βάρους (ισοδυναμεί με 1ml/10 kg) |
Κρέας και εδώδιμοι ιστοί: Βοοειδή: 58 ημέρες Χοίροι: 35 ημέρες Γάλα: 2,5 ημέρες |
(1) Δεν χορηγήθηκε η άδεια κυκλοφορίας.
(2) Κράτος μέλος αναφοράς για τη διαδικασία αμοιβαίας αναγνώρισης.
ΠΛΗΡΟΦΟΡΙΕΣ ΠΡΟΕΡΧΟΜΕΝΕΣ ΑΠΟ ΤΑ ΚΡΑΤΗ ΜΕΛΗ
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/74 |
Αντίγραφο του μέτρου εκκαθάρισης που αποφασίσθηκε βάσει του άρθρου 9 της οδηγίας 2001/24/ΕΚ του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου για την εξυγίανση και την εκκαθάριση των πιστωτικών ιδρυμάτων στην υπόθεση της Kaupthing Bank Luxembourg SA
(2008/C 276/04)
Αναστολή πληρωμών
Με απόφαση που εξέδωσε στις 9 Οκτωβρίου 2008 και ώρα 17.00 το περιφερειακό δικαστήριο του Λουξεμβούργου με έδρα το Λουξεμβούργο, το οποίο είναι αρμόδιο για την εκδίκαση εμπορικών υποθέσεων, διέταξε να υπαχθεί η ανώνυμη εταιρεία Kaupthing Bank Luxembourg SA, που είναι εγγεγραμμένη στο εμπορικό μητρώο και το μητρώο εταιρειών του Λουξεμβούργου, μέρος B, με αύξοντα αριθμό 63997, η οποία έχει την έδρα της στη διεύθυνση 35a, avenue J.F. Kennedy, L-1855 Luxembourg, στην ευεργετική διαδικασία αναστολής της διαδικασίας πληρωμών που ορίζεται στο μέρος IV του νόμου της 5ης Απριλίου 1993 για τον χρηματοπιστωτικό τομέα, όπως αυτός έχει τροποποιηθεί, και κηρύσσει εφαρμοστέο το άρθρο 60-2 (15) του εν λόγω νόμου, βάσει του οποίου απαιτείται, επί ποινή ακυρότητας, η γραπτή έγκριση των διαχειριστών για όλες τις πράξεις και αποφάσεις που αφορούν την τράπεζα Kaupthing Bank Luxembourg SA και δυνάμει του οποίου οι διαχειριστές δύνανται να υποβάλουν προς συζήτηση στα εταιρικά όργανα της τράπεζας Kaupthing Bank Luxembourg SA κάθε πρόταση που κρίνουν κατάλληλη, ενώ δύνανται να παρίστανται στις διαβουλεύσεις της γενικής συνέλευσης των μετόχων και των διοικητικών, διευθυντικών, διαχειριστικών ή εποπτικών οργάνων της εταιρείας Kaupthing Bank Luxembourg SA.
Με την ίδια απόφαση διορίζεται διαχειριστής η εταιρία περιορισμένης ευθύνης PricewaterhouseCoopers SARL, η οποία εκπροσωπείται από την κυρία Emmanuelle Caruel-Henniaux και τον κύριο Franz Fayot, στην οποία ανατίθενται καθήκοντα διαχείρισης των περιουσιακών στοιχείων της ανώνυμης εταιρείας Kaupthing Bank Luxembourg SA και περιορίζεται η διαδικασία αναστολής των πληρωμών σε έξι μήνες.
Η Επιτροπή Εποπτείας του Χρηματοπιστωτικού Τομέα (Commission de Surveillance du Secteur Financier) και η ανώνυμη εταιρεία Kaupthing Bank Luxembourg SA έχουν τη δυνατότητα να υποβάλουν προσφυγή, εντός προθεσμίας δεκαπέντε ημερών από τη στιγμή της κοινοποίησης της απόφασης, βάσει του άρθρου 60-2 παράγραφος 9 του νόμου της 5ης Απριλίου 1993 για τον χρηματοπιστωτικό τομέα όπως αυτός έχει τροποποιηθεί, δηλαδή από τη στιγμή της κοινοποίησης της προαναφερθείσας απόφασης, με συστημένη επιστολή, από τον Γραμματέα του περιφερειακού δικαστηρίου του Λουξεμβούργου με έδρα το Λουξεμβούργο, το οποίο είναι αρμόδιο για την εκδίκαση εμπορικών υποθέσεων. Η προσφυγή υποβάλλεται με δήλωση στον εν λόγω Γραμματέα.
Δεν είναι δυνατόν να ασκηθεί ανακοπή ή τριτανακοπή κατά της απόφασης.
Ακριβές επικυρωμένο αντίγραφο,
Οι διαχειριστές
PricewaterhouseCoopers SARL, εκπροσωπούμενη από την κυρία Emmanuelle Caruel-Henniaux και τον κύριο Franz Fayot
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/75 |
Πληροφορίες που διαβιβάζουν τα κράτη μέλη για τις κρατικές ενισχύσεις που χορηγούνται βάσει του κανονισμού (ΕΚ) αριθ. 70/2001 της Επιτροπής σχετικά με την εφαρμογή των άρθρων 87 και 88 της συνθήκης EK στις κρατικές ενισχύσεις προς μικρές και μεσαίες επιχειρήσεις
(Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ)
(2008/C 276/05)
|
Αριθμός ενίσχυσης |
XS 193/08 |
||||||||||
|
Κράτος μέλος |
Δημοκρατία της Βουλγαρίας |
||||||||||
|
Περιφέρεια |
Περιφέρεια του άρθρου 87 παράγραφος 3 στοιχείο α) της συνθήκης ΕΚ |
||||||||||
|
Τίτλος του καθεστώτος ενισχύσεων ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
Καθεστώς χορήγησης μη επιστρεπτέας οικονομικής ενίσχυσης στο πλαίσιο του μέτρου «Προστιθέμενη αξία στα γεωργικά και δασοκομικά προϊόντα» του προγράμματος αγροτικής ανάπτυξης 2007-2013 για την:
|
||||||||||
|
Νομική βάση |
Νομοθεσία ΕΕ
Νομοθεσία της Δημοκρατίας της Βουλγαρίας:
|
||||||||||
|
Ετήσιες δαπάνες που προβλέπονται στο πλαίσιο του καθεστώτος |
Καθεστώς ενίσχυσης |
Ετήσιο συνολικό ποσό |
34,4 εκατ. EUR (1) |
||||||||
|
Εγγυημένα δάνεια |
|
||||||||||
|
Μεμονωμένη ενίσχυση |
Συνολικό ποσό ενίσχυσης |
|
|||||||||
|
Εγγυημένα δάνεια |
|
||||||||||
|
Μέγιστη ένταση της ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και με το άρθρο 5 του κανονισμού |
Ναι (50 % κατ' ανώτατο όριο) |
|||||||||
|
Ημερομηνία εφαρμογής |
Μετά την έγκριση από την Ευρωπαϊκή Επιτροπή της τροποποίησης του κεφαλαίου 9 («Στοιχεία που χρειάζονται για την αξιολόγηση βάσει των κανόνων περί ανταγωνισμού και κατάλογος των καθεστώτων ενίσχυσης που εγκρίθηκαν δυνάμει των άρθρων 87, 88 και 89 της συνθήκης») του προγράμματος αγροτικής ανάπτυξης 2007-2013 και τη συμπερίληψη του αριθμού καταχώρησης της παρούσας κρατικής ενίσχυσης στο κεφάλαιο 9 |
||||||||||
|
Διάρκεια του καθεστώτος ενίσχυσης |
Έως την 31.12.2013 |
||||||||||
|
Σκοπός της ενίσχυσης |
Ενισχύσεις προς μικρομεσαίες επιχειρήσεις (ΜMΕ) |
Ναι |
|||||||||
|
Οικείοι οικονομικοί τομείς |
Περιορίζεται σε συγκεκριμένους τομείς |
Ναι |
|||||||||
|
Άλλος μεταποιητικός τομέας |
Ναι (2) |
||||||||||
|
Ονομασία και διεύθυνση της χορηγούσας αρχής |
|
||||||||||
|
|||||||||||
|
Μεγάλες μεμονωμένες ενισχύσεις |
Σύμφωνα με το άρθρο 6 του κανονισμού |
Όχι |
|||||||||
|
Αριθμός ενίσχυσης |
XS 201/08 |
||||||
|
Κράτος μέλος |
Ιταλία |
||||||
|
Περιφέρεια |
Sardegna |
||||||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
Contributi per impianti fotovoltaici |
||||||
|
Νομική βάση |
Articolo 24, L.R. 29 maggio 2007, n. 2 Deliberazioni Giunta Regionale n. 21/37 del 8.4.2008 e n. 34/22 del 19.6.2008 DDS n. 366 del 25.6.2008 |
||||||
|
Είδος μέτρου |
Καθεστώς ενισχύσεων |
||||||
|
Προϋπολογισμός |
Προβλεπόμενη ετήσια δαπάνη: 10 εκατ. EUR |
||||||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού: Η χορηγούμενη ενίσχυση, υπέρ των επιχειρήσεων που είναι εγκατεστημένες στις περιοχές της Περιφέρειας οι οποίες είναι επιλέξιμες σύμφωνα με το χάρτη κρατικών ενισχύσεων περιφερειακού χαρακτήρα 2007-2013, που έχει δημοσιευθεί στην ΕΕ C 90 της 11.4.2008, συνίσταται σε εισφορά κεφαλαίου μέγιστου ύψους 20 % της δαπάνης υλοποίησης της φωτοβολταϊκής εγκατάστασης. Όσον αφορά τις επιχειρήσεις που βρίσκονται στις συγκεκριμένες περιοχές του κτηματολογίου της Περιφέρειας που δεν είναι επιλέξιμες και προσδιορίζονται στο χάρτη κρατικών ενισχύσεων 2007-2013, η μέγιστη ένταση ενίσχυσης περιορίζεται σε:
Η ενίσχυση χορηγείται υπό τον όρο ότι η επένδυση θα διατηρηθεί στην περιφέρεια για περίοδο τουλάχιστον 5 ετών και ότι η συνεισφορά ιδίων πόρων από μέρους του δικαιούχου δεν θα είναι κατώτερη του 25 % της επένδυσης. Η ενίσχυση είναι συμβατή με τα μέτρα δημιουργίας κινήτρων για την παραγωγή ηλεκτρικής ενέργειας μέσω φωτοβολταϊκών εγκαταστάσεων που προβλέπονται στο D.M. 28.7.2005, όπως τροποποιήθηκε με το D.M. 6.2.2006 και το D.M. 19.2.2007 (αποκαλούμενο «conto energia»). Η ενίσχυση δεν μπορεί να σωρευθεί με άλλες περιφερειακές, εθνικές και κοινοτικές διευκολύνσεις |
||||||
|
Ημερομηνία εφαρμογής |
18.7.2008 |
||||||
|
Διάρκεια |
18.9.2008 |
||||||
|
Στόχος |
ΜΜΕ |
||||||
|
Κλάδοι της οικονομίας |
Όλοι οι κλάδοι στους οποίους επιτρέπεται η χορήγηση ενισχύσεων στις ΜΜΕ |
||||||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
||||||
|
Λοιπές πληροφορίες |
Η παρέμβαση πραγματοποιείται μέσω δημόσιου διαγωνισμού με διαδικασία αξιολόγησης και βαθμολόγησης. Το κριτήριο προτεραιότητας συνίσταται στο χαμηλότερο ποσοστό αιτούμενης κρατικής ενίσχυσης σε σχέση με τη μέγιστη ενίσχυση του 20 %. Για τις επιχειρήσεις που βρίσκονται σε περιοχές μη επιλέξιμες για περιφερειακές ενισχύσεις, η μείωση είναι ανάλογη με τη μέγιστη τιμή της χορηγούμενης ενίσχυσης, βλέπε κανονισμό (ΕΚ) αριθ. 70/2001 |
|
Αριθμός ενίσχυσης |
XS 209/08 |
|||||||||
|
Κράτος μέλος |
Ελλάδα |
|||||||||
|
Περιφέρεια |
— |
|||||||||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
«ΕΝΙΣΧΥΣΗ ΤΗΣ ΑΝΤΑΓΩΝΙΣΤΙΚΟΤΗΤΑΣ ΚΑΙ ΤΗΣ ΚΑΙΝΟΤΟΜΙΑΣ ΤΩΝ ΜΙΚΡΟΜΕΣΑΙΩΝ ΕΠΙΧΕΙΡΗΣΕΩΝ ΣΤΟΥΣ ΤΟΜΕΙΣ ΤΗΣ ΜΕΤΑΠΟΙΗΣΗΣ ΚΑΙ ΤΟΥ ΤΟΥΡΙΣΜΟΥ» (3η προκήρυξη) [«ENISHYSI TIS ANTAGONISTIKOTITAS KAI TIS KAINOTOMIAS TON MIKROMESAION EPIHEIRISEON STOYS TOMEIS TIS METAPOIISIS KAI TOY TOYRISMOY» (3i prokiryksi)] |
|||||||||
|
Νομική βάση |
Άρθρο 35 του Ν. 3016/2002 (ΦΕΚ 110 Α'/17-05-2002) ΥΑ 41630/ΕΥΣ9450/7.11.2005 (ΦΕΚ 1651/B'/29.11.05) ΚΥΑ 14871/EYΣ3047/20.4.2005 (ΦΕΚ 575/ΤΒ/28.04.2005) ΥΑ 39059/ΕΥΣ9047/14.10.2005 (ΦΕΚ 1539/Β/8.11.2005) ΚΥΑ 1707/ΕΥΣ443/17.01.2006 (ΦΕΚ 42/Β/19.01.2006) |
|||||||||
|
Είδος μέτρου |
Καθεστώς ενισχύσεων |
|||||||||
|
Προϋπολογισμός |
Προβλεπόμενη ετήσια δαπάνη: 400 εκατ. EUR |
|||||||||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
|||||||||
|
Ημερομηνία εφαρμογής |
15.3.2006 |
|||||||||
|
Διάρκεια |
30.6.2007 |
|||||||||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
|||||||||
|
Κλάδοι της οικονομίας |
Όλοι οι μεταποιητικοί τομείς, τουρισμός |
|||||||||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
|
Αριθμός ενίσχυσης |
XS 211/08 |
|||
|
Κράτος μέλος |
Γερμανία |
|||
|
Περιφέρεια |
Freie und Hansestadt Hamburg |
|||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
|
|||
|
Νομική βάση |
Verordnung (EG) Nr. 70/2001 der Kommission vom 12. Januar 2001 über die Anwendung der Artikel 87 und 88 EG-Vertrag auf staatliche Beihilfen an kleine und mittlere Unternehmen (ABl. EG 13.1.2001 L 10/33 verlängert durch ABl. EU 23.12.2006 L 368/85); Gesetz über die Kreditkommission vom 29.4.1997 (Hamburgisches Gesetz- und Verordnungsblatt 1997, Nr. 18, S. 133) |
|||
|
Είδος μέτρου |
Ad hoc |
|||
|
Προϋπολογισμός |
Προβλεπόμενη συνολική ενίσχυση: 3 450 EUR |
|||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
|||
|
Ημερομηνία εφαρμογής |
14.8.2008 |
|||
|
Διάρκεια |
14.2.2009 |
|||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
|||
|
Κλάδοι της οικονομίας |
Άλλες υπηρεσίες |
|||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
|
Αριθμός ενίσχυσης |
XS 212/08 |
|||
|
Κράτος μέλος |
Γερμανία |
|||
|
Περιφέρεια |
Freie und Hansestadt Hamburg |
|||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
|
|||
|
Νομική βάση |
Verordnung (EG) Nr. 70/2001 der Kommission vom 12. Januar 2001 über die Anwendung der Artikel 87 und 88 EG-Vertrag auf staatliche Beihilfen an kleine und mittlere Unternehmen (ABl. EG 13.1.2001 L 10/33 verlängert durch ABl. EU 23.12.2006 L 368/85); Gesetz über die Kreditkommission vom 29.4.1997 (Hamburgisches Gesetz- und Verordnungsblatt 1997, Nr. 18, S. 133) |
|||
|
Είδος μέτρου |
Ad hoc |
|||
|
Προϋπολογισμός |
Προβλεπόμενη συνολική ενίσχυση: 6 750 EUR |
|||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
|||
|
Ημερομηνία εφαρμογής |
31.7.2008 |
|||
|
Διάρκεια |
31.1.2009 |
|||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
|||
|
Κλάδοι της οικονομίας |
Άλλες υπηρεσίες |
|||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
(1) Το ετήσιο ποσό είναι ενδεικτικό, υπολογίζεται δε βάσει του προϋπολογισμού του μέτρου 123 «Προστιθέμενη αξία στα γεωργικά και δασοκομικά προϊόντα» του προγράμματος αγροτικής ανάπτυξης 2007-2013 (241 εκατ. EUR σε τρέχουσες τιμές).
(2) Οι ακόλουθοι τομείς που αφορούν τη μεταποίηση ή/και την εμπορία των προϊόντων που αναφέρονται στο παράρτημα I της συνθήκης ΕΚ είναι επιλέξιμοι για ενίσχυση:
|
— |
γάλα και γαλακτοκομικά προϊόντα (κυρίως NACE 15.5), |
|
— |
κρέας και προϊόντα κρέατος (κυρίως NACE 15.1), |
|
— |
φρούτα και λαχανικά, συμπεριλαμβανομένων των μανιταριών (κυρίως NACE 15.3), |
|
— |
επεξεργασία μελιού (δεν υπάρχει σαφής ταξινόμηση NACE, αλλά μπορεί να σχετίζεται με την NACE 15.89), |
|
— |
προϊόντα άλεσης δημητριακών, άμυλα, αμυλώδη προϊόντα (κυρίως NACE 15.6), |
|
— |
φυτικά και ζωικά έλαια και λίπη (κυρίως NACE 15.4), |
|
— |
μεταποίηση τεχνικών και ιατρικών καλλιεργειών, συμπεριλαμβανομένων ελαιοφόρων τριαντάφυλλων, βοτάνων και ακατέργαστου καπνού (δεν υπάρχει σαφής ταξινόμηση NACE, αλλά καλύπτεται εν μέρει από τη NACE 24.63), |
|
— |
παρασκευασμένες ζωοτροφές για ζώα εκτρεφόμενα σε αγροκτήματα (ζωοτροφές) (κυρίως NACE 15.71), |
|
— |
γλεύκος σταφυλιών, οίνος και ξύδι (κυρίως NACE 15.87 και 15.93). |
Όλοι οι τομείς που αφορούν την παραγωγή ενέργειας από την επεξεργασία των φυτικών και ζωικών προϊόντων πρωτογενούς και δευτερογενούς βιομάζας που αναφέρονται στο παράρτημα I της συνθήκης ΕΚ, εκτός των αλιευτικών προϊόντων (δεν υπάρχει σαφής ταξινόμηση NACE):
|
— |
οι τομείς της μεταποίησης ή/και εμπορίας προϊόντων δασοκομίας, εκτός της κατασκευής επίπλων (κυρίως NACE 20.10, 20.30, 20.40, 20.51). |
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/79 |
Πληροφορίες που διαβιβάζουν τα κράτη μέλη για τις κρατικές ενισχύσεις που χορηγούνται βάσει του κανονισμού (ΕΚ) αριθ. 70/2001 της Επιτροπής σχετικά με την εφαρμογή των άρθρων 87 και 88 της συνθήκης EK στις κρατικές ενισχύσεις προς μικρές και μεσαίες επιχειρήσεις
(Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ)
(2008/C 276/06)
|
Αριθμός ενίσχυσης |
XS 213/08 |
||||||
|
Κράτος μέλος |
Ηνωμένο Βασίλειο |
||||||
|
Περιφέρεια |
East Midlands |
||||||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
Hathersage Developments Ltd |
||||||
|
Νομική βάση |
RDA Act 1998 |
||||||
|
Είδος μέτρου |
Ad hoc |
||||||
|
Προϋπολογισμός |
Προβλεπόμενη συνολική ενίσχυση: 0,33 εκατ. GBP |
||||||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
||||||
|
Ημερομηνία εφαρμογής |
14.1.2008 |
||||||
|
Διάρκεια |
31.3.2009 |
||||||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
||||||
|
Κλάδοι της οικονομίας |
Επαγγελματικές, επιστημονικές και τεχνικές δραστηριότητες |
||||||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
|
Αριθμός ενίσχυσης |
XS 214/08 |
||||
|
Κράτος μέλος |
Ηνωμένο Βασίλειο |
||||
|
Περιφέρεια |
North East England |
||||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
Python Properties |
||||
|
Νομική βάση |
Industrial Development Act 1982 sections 7 and 11 Local Government Act 2000 section 2 |
||||
|
Είδος μέτρου |
Καθεστώς ενισχύσεων |
||||
|
Προϋπολογισμός |
Προβλεπόμενη ετήσια δαπάνη: 0,3 εκατ. GBP |
||||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
||||
|
Ημερομηνία εφαρμογής |
3.3.2008 |
||||
|
Διάρκεια |
31.12.2008 |
||||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
||||
|
Κλάδοι της οικονομίας |
Όλοι οι μεταποιητικοί τομείς, άλλες υπηρεσίες |
||||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
|
Αριθμός ενίσχυσης |
XS 215/08 |
||||||
|
Κράτος μέλος |
Ηνωμένο Βασίλειο |
||||||
|
Περιφέρεια |
West Midlands |
||||||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
Premium Vehicles Centres of Excellence Projects — Warwick University |
||||||
|
Νομική βάση |
Regional Development Agencies Act 1998 |
||||||
|
Είδος μέτρου |
Καθεστώς ενισχύσεων |
||||||
|
Προϋπολογισμός |
Προβλεπόμενη ετήσια δαπάνη: 2,2 εκατ. GBP |
||||||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
||||||
|
Ημερομηνία εφαρμογής |
15.8.2008 |
||||||
|
Διάρκεια |
31.12.2013 |
||||||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
||||||
|
Κλάδοι της οικονομίας |
Όλοι οι μεταποιητικοί τομείς |
||||||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
|
Αριθμός ενίσχυσης |
XS 219/08 |
||||
|
Κράτος μέλος |
Κάτω Χώρες |
||||
|
Περιφέρεια |
— |
||||
|
Τίτλος του καθεστώτος ενίσχυσης ή επωνυμία της εταιρείας που λαμβάνει μεμονωμένη ενίσχυση |
Subsidieregeling innovatiekredieten-module van de Experimentele kaderregeling subsidies innovatieprojecten |
||||
|
Νομική βάση |
Kaderwet EZ subsidies |
||||
|
Είδος μέτρου |
Καθεστώς ενισχύσεων |
||||
|
Προϋπολογισμός |
Προβλεπόμενη ετήσια δαπάνη: 20,3 εκατ. EUR |
||||
|
Μέγιστη ένταση ενίσχυσης |
Σύμφωνα με το άρθρο 4 παράγραφοι 2 έως 6 και το άρθρο 5 του κανονισμού |
||||
|
Ημερομηνία εφαρμογής |
5.7.2008 |
||||
|
Διάρκεια |
5.7.2012 |
||||
|
Στόχος |
Μικρομεσαίες επιχειρήσεις |
||||
|
Κλάδοι της οικονομίας |
Όλοι οι τομείς που είναι επιλέξιμοι για ενισχύσεις προς ΜΜΕ |
||||
|
Όνομα και διεύθυνση της χορηγούσας αρχής |
|
V Γνωστοποιήσεις
ΔΙΟΙΚΗΤΙΚΕΣ ΔΙΑΔΙΚΑΣΙΕΣ
Επιτροπή
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/82 |
Προκήρυξη διαγωνισμού που δημοσιεύθηκε από την Ιταλία βάσει του άρθρου 4 παράγραφος 1 στοιχείο δ) του κανονισμού (ΕΟΚ) αριθ. 2408/92 του Συμβουλίου για την εκτέλεση των τακτικών αεροπορικών γραμμών Αλμπένγκα — Ρώμη Φιουμιτσίνο και αντιστρόφως
(Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ)
(2008/C 276/07)
ΕΙΣΑΓΩΓΗ
Η ιταλική κυβέρνηση —το Υπουργείο Υποδομών και Μεταφορών—, δυνάμει του άρθρου 4 του κανονισμού (ΕΟΚ) αριθ. 2408/92, σύμφωνα με τις αποφάσεις που εγκρίθηκαν κατά τη διάσκεψη των υπηρεσιών που διοργάνωσε η Περιφέρεια Λιγουρία, ενέκρινε την παρούσα προκήρυξη διαγωνισμού με σκοπό την ανάθεση της εκτέλεσης αεροπορικών δρομολογίων στη γραμμή: Αλμπένγκα — Ρώμη Φιουμιτσίνο και αντιστρόφως.
Οι προδιαγραφές της υποχρέωσης παροχής δημόσιας υπηρεσίας έχουν δημοσιευθεί στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008.
Εφόσον εντός 30 ημερών από τη δημοσίευση των ανωτέρω υποχρεώσεων, κανένας αερομεταφορέας δεν έχει υποβάλει αίτηση για την έναρξη εκτέλεσης αεροπορικών δρομολογίων στην ανωτέρω γραμμή, σύμφωνα με τις επιβαλλόμενες υποχρεώσεις δημόσιας υπηρεσίας και χωρίς οικονομική αντιστάθμιση, η ιταλική κυβέρνηση —Υπουργείο Υποδομών και Μεταφορών— αποφάσισε, σύμφωνα με τη διαδικασία του άρθρου 4 παράγραφος 1 στοιχείο δ) του κανονισμού (ΕΟΚ) αριθ. 2408/92, να περιορίσει την πρόσβαση στην εν λόγω γραμμή σε έναν και μόνον αερομεταφορέα, τον οποίο θα επιλέξει με διαγωνισμό για να εκτελεί την αεροπορική γραμμή σύμφωνα με τις διατάξεις του ιδίου κανονισμού.
ΓΕΝΙΚΕΣ ΔΙΑΤΑΞΕΙΣ
Η παρούσα προκήρυξη καθορίζει το αντικείμενο του διαγωνισμού, τους όρους συμμετοχής στο διαγωνισμό, τους όρους σχετικά με τη διάρκεια, την τροποποίηση και τη λήξη της σύμβασης, τις κυρώσεις σε περίπτωση αθέτησης των προδιαγραφόμενων διατάξεων και των εγγυήσεων που συνοδεύουν την προσφορά, όπως και σε περίπτωση μη εκτέλεσης της σύμβασης.
Το δικαίωμα εκτέλεσης των δρομολογίων στη συγκεκριμένη γραμμή θα εκχωρηθεί μετά από δημόσιο διαγωνισμό που θα κατακυρωθεί με μειοδοτική προσφορά, η οποία θα περιλαμβάνει την οικονομική αποζημίωση που καθορίζεται στο σημείο 6 της παρούσας προκήρυξης διαγωνισμού.
1. Αντικείμενο της προκήρυξης
Η εκτέλεση τακτικών αεροπορικών δρομολογίων στη γραμμή Αλμπένγκα — Ρώμη Φιουμιτσίνο και αντιστρόφως, με βάση τις επιβαλλόμενες υποχρεώσεις παροχής δημόσιας υπηρεσίας που δημοσιεύθηκαν στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008, σύμφωνα με τις διατάξεις του κανονισμού (ΕΟΚ) αριθ. 2408/92.
2. Συμμετοχή στην πρόσκληση υποβολής προσφορών
Αίτηση συμμετοχής στο διαγωνισμό μπορεί να υποβάλει κάθε κοινοτικός αερομεταφορέας, όπως ορίζει το άρθρο 2 στοιχείο β) του κανονισμού (ΕΟΚ) αριθ. 2408/92, ο οποίος πληροί τις εξής προϋποθέσεις.
Γενικές προϋποθέσεις
|
1. |
Να μην βρίσκεται σε κατάσταση πτώχευσης, εκκαθάρισης αναγκαστικής διαχείρισης, πτωχευτικού συμβιβασμού ή σε οποιαδήποτε παρόμοια διαδικασία για την κήρυξή του σε μια από τις ανωτέρω καταστάσεις. |
|
2. |
Να μην έχει καταδικασθεί σε απαγορευτική κύρωση κατά την έννοια του άρθρου 9 εδάφιο 2 του νομοθετικού διατάγματος αριθ. 231/2001 και να μην του έχει επιβληθεί ποινή, η οποία συνεπάγεται ότι δεν μπορεί να συμβληθεί με δημόσια αρχή. |
|
3. |
Να έχει εκπληρώσει τις υποχρεώσεις του όσον αφορά την καταβολή των εισφορών κοινωνικής ασφάλισης και εργασιακών επιδομάτων. |
|
4. |
Να μην έχει υποβάλει ψευδείς δηλώσεις σχετικά με τους όρους συμμετοχής του σε άλλες διαδικασίες διαγωνισμού για την ανάθεση εκτέλεσης τακτικών γραμμών με βάση υποχρεώσεις παροχής δημόσιας υπηρεσίας. |
Προκειμένου να δηλώσει ότι πληροί τις ανωτέρω προϋποθέσεις, ο υποψήφιος υποβάλλει, όσον αφορά την κατάστασή του σε σχέση με το σημείο 3, βεβαίωση εξόφλησης ασφαλιστικών εισφορών του εκδοθείσα από την INPS ή την INAIL και τη βεβαίωση που προβλέπεται από το άρθρο 17 του νόμου αριθ. 68 της 12η Μαρτίου 1999«Norme per il diritto al lavoro dei disabili»· για τα σημεία 1, 2 και 4, δήλωση η οποία επέχει θέση όρκου σύμφωνα με τα άρθρα 46 και 47 του προεδρικού διατάγματος αριθ. 445 της 28ης Δεκεμβρίου 2000.
Για τους υποψηφίους άλλου κράτους μέλους της Ευρωπαϊκής Ένωσης, πλην της Ιταλίας, τα πιστοποιητικά ή οι βεβαιώσεις πρέπει να έχουν εκδοθεί από διοικητικές αρχές ή οργανισμούς της χώρας καταγωγής και να συνοδεύονται από μετάφρασή τους στην ιταλική γλώσσα, επικυρωμένη από την ιταλική προξενική αρχή, η οποία πιστοποιεί και το γνήσιο του πρωτοτύπου.
Τεχνικές προϋποθέσεις
|
1. |
Άδεια αεροπορικής εκμετάλλευσης εκδοθείσα σύμφωνα με τον κανονισμό (ΕΟΚ) αριθ. 2407/92. |
|
2. |
Υποχρεωτική ασφάλιση αστικής ευθύνης σε περίπτωση συμβάντος, ιδίως έναντι επιβατών, αποσκευών, μεταφερόμενων εμπορευμάτων και τρίτων, σύμφωνα και με τον κανονισμό (ΕΚ) αριθ. 785/2004. |
|
3. |
Πιστοποιητικό αερομεταφορέα (AOC) σύμφωνα με τα κοινοτικά πρότυπα. |
|
4. |
Μη αναγραφή του στην ονομαζόμενη «μαύρη λίστα» των αεροπορικών εταιρειών που δεν πληρούν τα πρότυπα ασφάλειας πτήσεων, όπως αυτή δημοσιεύεται στο δικτυακό τόπο: http://ec.europa.eu/transport/air-ban. |
|
5. |
Σύστημα αναλυτικής λογιστικής με διαχωρισμό των σχετικών δαπανών (όπου περιλαμβάνονται τα πάγια έξοδα και τα έσοδα). |
Σε περίπτωση απώλειας των εν λόγω δικαιολογητικών μετά την υποβολή της αίτησης συμμετοχής στο διαγωνισμό, οι διαγωνιζόμενοι αερομεταφορείς αποκλείονται αυτόματα από την αξιολόγηση των προσφορών τους.
Σε περίπτωση απώλειας των εν λόγω δικαιολογητικών μετά τη σύναψη της σύμβασης που αναφέρεται στο σημείο 5, εφαρμόζονται οι διατάξεις του σημείου 14 και του σημείου 15 προτελευταίο εδάφιο, της παρούσας προκήρυξης διαγωνισμού.
3. Διαδικασία της πρόσκλησης υποβολής προσφορών
Η παρούσα πρόσκληση υποβολής προσφορών υπόκειται στις διατάξεις του άρθρου 4 παράγραφος 1 στοιχεία δ), ε), στ), η) και θ) του κανονισμού (ΕΟΚ) αριθ. 2408/92.
4. Φάκελος της πρόσκλησης υποβολής προσφορών
Ο πλήρης φάκελος της παρούσας προκήρυξης διαγωνισμού, ο οποίος περιλαμβάνει τους ειδικούς κανόνες του διαγωνισμού, την προθεσμία ισχύος των προσφορών και κάθε άλλη χρήσιμη πληροφορία, αποτελεί αναπόσπαστο μέρος του διαγωνισμού μαζί με το υπόδειγμα σύμβασης που αναφέρεται στο σημείο 5 και διατίθεται δωρεάν στην εξής διεύθυνση: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio 118, I-00185 Roma ή μέσω ηλεκτρονικού ταχυδρομείου στην εξής διεύθυνση: trasporto.aereo@enac.rupa.it.
5. Ρυθμιστική σύμβαση εκτέλεσης του δρομολογίου
Η εκτέλεση της δημόσιας υπηρεσίας διέπεται από σύμβαση μεταξύ του αερομεταφορέα και της ENAC, η οποία θα συνταχθεί σύμφωνα με το υπόδειγμα που περιλαμβάνει ο φάκελος του διαγωνισμού.
6. Οικονομική αντιστάθμιση
Το ύψος της οικονομικής αντιστάθμισης, με βάση τον διαγωνισμό ανάθεσης εκτέλεσης μεταφορών στη συγκεκριμένη τακτική γραμμή, είναι 979 112,85 EUR (εννιακόσιες εβδομήντα εννέα χιλιάδες εκατόν δώδεκα ευρώ και ογδόντα πέντε λεπτά) συμπεριλαμβανομένου του ΦΠΑ.
Στις προσφορές, οι οποίες πρέπει να συνταχθούν όπως καθορίζεται στη συγγραφή υποχρεώσεων, πρέπει να αναγράφεται ρητά, στο μέρος του εντύπου που αφορά την οικονομική προσφορά, το μέγιστο ύψος της οικονομικής αντιστάθμισης που ζητείται, εντός του ορίου που προαναφέρθηκε, για την εκτέλεση της συγκεκριμένης υποχρέωσης.
Το ακριβές ύψος της οικονομικής αντιστάθμισης καθορίζεται εκ των υστέρων στο τέλος του έτους ισχύος της σύμβασης, ανάλογα με το πραγματικό κόστος και έσοδα που θα προκύψουν από την εκτέλεση της γραμμής, βάσει δικαιολογητικών και εντός του μέγιστου ορίου που θα αναφέρεται στην προσφορά και των όσων ορίζονται στη συγγραφή υποχρεώσεων.
Σε κάθε περίπτωση, ο αερομεταφορέας δεν μπορεί να ζητήσει οικονομική αντιστάθμιση υψηλότερη από το όριο που θα καθορίζεται στη σύμβαση, λαμβανομένου υπόψη ότι δεν πρόκειται για αντιπαροχή αλλά για αντιστάθμιση για την ανάληψη υποχρέωσης δημόσιας υπηρεσίας.
Οι πληρωμές για το έτος ισχύος της σύμβασης καταβάλλονται υπό μορφή προκαταβολών και υπολοίπου εξόφλησης, με βάση τους όρους της συγγραφής υποχρεώσεων, με την επιφύλαξη ενδεχόμενων ελέγχων από την ENAC με σκοπό να επαληθευθεί ο προορισμός της χορηγούμενης οικονομικής αντιστάθμισης και η τήρηση των όρων από τον δικαιούχο αερομεταφορέα. Το υπόλοιπο καταβάλλεται μετά από έλεγχο της αναλυτικής λογιστικής του αερομεταφορέα για τη συγκεκριμένη γραμμή και μετά από έλεγχο της τήρησης των όρων παροχής της επιβαλλόμενης δημόσιας υπηρεσίας.
7. Ναύλοι
Στις προσφορές που θα υποβληθούν πρέπει να αναφέρονται οι προβλεπόμενοι ναύλοι, σύμφωνα με όσα καθορίζονται στην ανακοίνωση για την επιβολή παροχής δημόσιας υπηρεσίας που δημοσιεύθηκε στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008.
8. Έναρξη της γραμμής
Η γραμμή θα αρχίσει εντός 15 (δέκα πέντε) ημερών από την ημερομηνία που θα καθορίζεται στη σύμβαση και θα βεβαιωθεί με δήλωση έναρξης της γραμμής, την οποία θα υπογράψουν ο ανάδοχος αερομεταφορέας και η ENAC.
9. Διάρκεια της σύμβασης
Η σύμβαση θα είναι διάρκειας δύο ετών από την ημερομηνία έναρξης των δρομολογίων στη συγκεκριμένη γραμμή.
Ο αερομεταφορέας δεσμεύεται να θέσει στη διάθεση της ENAC το προσωπικό, τα τεχνικά και λογιστικά έγγραφα, τον εξοπλισμό και ο,τιδήποτε άλλο χρειασθεί για τη διεκπεραίωση των εποπτικών δραστηριοτήτων και τον έλεγχο της ορθής τήρησης, εφαρμογής και εκτέλεσης των διατάξεων που περιέχει η ανακοίνωση της Επιτροπής, η προκήρυξη επιβολής των υποχρεώσεων, η παρούσα προκήρυξη, η σύμβαση και η συγγραφή υποχρεώσεων.
Η αθέτηση των υποχρεώσεων που προαναφέρθηκαν συνεπάγεται επιβολή κυρώσεων σύμφωνα με όσα προβλέπονται στο σημείο 11 της παρούσας προκήρυξης.
10. Καταγγελία της σύμβασης
Η σύμβαση μπορεί να καταγγελθεί από ένα από τα συμβαλλόμενα μέρη πριν από την κανονική λήξη ισχύος της μόνον με προειδοποίηση 6 μηνών.
Η σύμβαση καταγγέλλεται χωρίς προειδοποίηση για μη εκπλήρωση της υποχρέωσης δημόσιας υπηρεσίας, εφόσον, μετά από προειδοποιητική επιστολή της ENAC προς τον ενδιαφερόμενο αερομεταφορέα ότι δεν έχει εκπληρώσει εξ ολοκλήρου τις υποχρεώσεις που ανέλαβε, ο αερομεταφορέας δεν αρχίσει την εκτέλεση των υποχρεώσεων δημόσιας υπηρεσίας εντός 30 (τριάντα) ημερών κατ' ανώτατο όριο από την ημερομηνία παραλαβής της επιστολής.
Σε περίπτωση καταγγελίας της σύμβασης από τον αερομεταφορέα, η ENAC έχει το δικαίωμα να προβεί σε έλεγχο, προκειμένου να προτείνει στο Υπουργείο υποδομών και μεταφορών τη σύναψη νέας σύμβασης με τον αμέσως επόμενο αερομεταφορέα από τον κατάλογο υποψηφίων. Οι όροι εκτέλεσης της γραμμής με βάση τις υποχρεώσεις παροχής δημόσιας υπηρεσίας και η οφειλόμενη κατ' αναλογία οικονομική αντιστάθμιση παραμένουν ίδιοι με εκείνους που ίσχυαν πριν την ανάθεση των υποχρεώσεων δημόσιας υπηρεσίας.
11. Αθέτηση της σύμβασης και κυρώσεις
Δεν αποτελεί παρατυπία καταλογιζόμενη στον αερομεταφορέα η μη εκτέλεση του δρομολογίου για τους κάτωθι λόγους:
|
— |
επικίνδυνες μετεωρολογικές συνθήκες, |
|
— |
κλείσιμο ενός των αεροδρομίων των αναφερόμενων στο επιχειρησιακό πρόγραμμα, |
|
— |
προβλήματα ασφαλείας, |
|
— |
απεργία, |
|
— |
περιπτώσεις ανωτάτης βίας. |
Η διακοπή του δρομολογίου για τους ανωτέρω λόγους συνεπάγεται μείωση του ύψους της οικονομικής αντιστάθμισης κατ' αναλογία των πτήσεων που δεν πραγματοποιήθηκαν.
Σε περίπτωση μη παροχής των υπηρεσιών και αθέτησης των υποχρεώσεων που περιέχει η σύμβαση, η ENAC έχει το δικαίωμα να επιβάλει κυρώσεις στον αερομεταφορέα, ανάλογες προς τον αριθμό των παραβιάσεων που διέπραξε, και σύμφωνα με τον τρόπο που περιγράφεται στο υπόδειγμα σύμβασης.
Σε κάθε περίπτωση, το ύψος των κυρώσεων δεν είναι δυνατόν να υπερβεί το 50 % του μέγιστου ύψους της οικονομικής αντιστάθμισης που προβλέπεται στον διαγωνισμό, όπως αναφέρεται στο σημείο 6, με την επιφύλαξη ότι, πέραν του ορίου αυτού, η ENAC έχει το δικαίωμα να καταγγείλει τη σύμβαση λόγω αθέτησής της, με αποτέλεσμα την άμεση ανάκληση της οφειλόμενης οικονομικής αντιστάθμισης.
Ο αριθμός των πτήσεων που ματαιώνονται για λόγους απευθείας καταλογιζόμενους στον αερομεταφορέα δεν πρέπει να υπερβαίνει ετησίως το 2 % του αριθμού των προγραμματισμένων πτήσεων.
Άνω του ορίου αυτού, ο αερομεταφορέας οφείλει να καταθέσει στην ENAC, ως πρόστιμο, το ποσό των 3 000,00 EUR (τριών χιλιάδων ευρώ) για κάθε ματαιωθείσα πτήση που υπερβαίνει το ανωτέρω όριο του 2 %, κατόπιν επίσημης προειδοποίησης του αερομεταφορέα εντός δέκα ημερών από την ημερομηνία του συμβάντος. Ο αερομεταφορέας διαθέτει επτά ημέρες κατ' ανώτατο όριο για να υποβάλει τυχόν αντιρρήσεις του.
Η ENAC θα προβεί, άλλωστε, σε αναθεώρηση του ύψους της οικονομικής αντιστάθμισης συναρτήσει των πτήσεων που δεν εκτελέστηκαν. Τα ποσά που θα εισπραχθούν, όπως προαναφέρθηκε, θα διατεθούν για τη χρηματοδότηση της συνέχειας των μεταφορικών συνδέσεων με την πόλη του Αλμπένγκα.
Η μη τήρηση της προειδοποίησης που προαναφέρθηκε στο σημείο 10 συνεπάγεται την επιβολή προστίμου, το οποίο υπολογίζεται με βάση την προβλεπόμενη οικονομική αντιστάθμιση και το χρονικό διάστημα αθέτησης της προειδοποίησης από τη διακοπή του δρομολογίου, όπως προβλέπεται στο ίδιο σημείο 10, με την εφαρμογή του εξής τύπου:
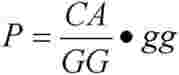
Όπου:
|
P |
= |
πρόστιμο |
|
CA |
= |
ετήσια αντιστάθμιση |
|
GG |
= |
ημέρες του υπό εξέταση έτους (365 ή 366) |
|
gg |
= |
ημέρες αθέτησης προειδοποίησης |
Οι κυρώσεις που αναφέρονται στο παρόν σημείο είναι συσσωρεύσιμες με εκείνες που προβλέπονται αντίστοιχα από κοινοτικούς κανονισμούς και από εθνικές διατάξεις και κανονισμούς.
12. Εγγυήσεις για την προσφορά
Προκειμένου να βεβαιώσει τη σοβαρότητα και την αξιοπιστία της προσφοράς του, ο αερομεταφορέας που συμμετέχει στον παρόντα διαγωνισμό οφείλει να καταθέσει εγγύηση ύψους 2 % της μέγιστης οικονομικής αντιστάθμισης που αναφέρεται στο σημείο 6, υπό μορφή σύστασης εγγύησης ή τραπεζικής ή ασφαλιστικής εγγύησης, κατ' επιλογήν του υποβάλλοντος την προσφορά.
Ο τρόπος σύστασης της ανωτέρω εγγύησης θα καθορισθεί στη συγγραφή υποχρεώσεων και θα αναφέρεται ενδεχομένως στη σύμβαση.
Η ισχύς της εγγύησης είναι διάρκειας τουλάχιστον 180 (εκατόν ογδόντα) ημερών από την καταληκτική ημερομηνία υποβολής των προσφορών, με υποχρέωση από πλευράς του αερομεταφορέα να ανανεώσει την εγγύηση εφόσον, έως την καταληκτική ημερομηνία, δεν έχει ανατεθεί η σύμβαση, κατ'αίτηση της ENAC κατά τη διάρκεια της διαδικασίας αυτής.
Η ENAC προβλέπει, ταυτόχρονα με την κοινοποίησή της προς τους απορριφθέντες αερομεταφορείς σχετικά με την ανάθεση της σύμβασης, την αποδέσμευση της εγγύησής τους.
13. Εγγυήσεις εκτέλεσης και ασφαλιστική κάλυψη
Ο αερομεταφορέας, ο οποίος θα αναλάβει την εκτέλεση δρομολογίων σύμφωνα με τις παρούσες υποχρεώσεις παροχής δημόσιας υπηρεσίας, οφείλει να συστήσει τραπεζική ή ασφαλιστική εγγύηση ύψους 400 000,00 EUR (τετρακοσίων χιλιάδων ευρώ) υπέρ της ENAC, η οποία διατηρεί το δικαίωμα να την χρησιμοποιήσει για να εξασφαλίσει τη συνέχεια της γραμμής.
Η άδεια παραλαβής δίδεται αυτόματα, χωρίς να χρειάζεται έγκριση από την ENAC, μετά από την τακτική εξέταση που αναφέρεται στην τελευταία παράγραφο του σημείου 6.
14. Λήξη και ανάκληση της οικονομικής αντιστάθμισης
Η ανά πάσα στιγμή απώλεια, μετά τη σύναψη της σύμβασης, των γενικών και τεχνικών δικαιολογητικών που αναφέρονται στο σημείο 2 της παρούσας προκήρυξης, καθώς και εκείνων που αναφέρονται στη συγγραφή υποχρεώσεων, συνεπάγεται τη λήξη της ανάθεσης εκτέλεσης του δρομολογίου, την ανάκληση της οικονομικής αντιστάθμισης και την επιστροφή τυχόν μη οφειλόμενων ποσών που εισπράχθηκαν, προσαυξημένων κατά τους νόμιμους φόρους.
Μετά τη λήξη της προθεσμίας ανάθεσης της γραμμής, το Υπουργείο υποδομών και μεταφορών μπορεί να επιτρέψει στην ENAC να συνάψει νέα σύμβαση, για την εναπομένουσα περίοδο εκτέλεσης της γραμμής με τον αμέσως επόμενο συναγωνιζόμενο αερομεταφορέα από τον τελικό κατάλογο επιλεγέντων υποψηφίων.
Τότε, η διάρκεια της σύμβασης αρχίζει από την ημερομηνία έναρξης εκτέλεσης της γραμμής και λήγει την προβλεπόμενη ημερομηνία λήξης της καταγγελθείσας σύμβασης, τηρουμένου του επιχειρηματικού σχεδίου που είχε εγκριθεί κατά την αξιολόγηση της προσφοράς που είχε υποβάλει ο πρώτος ανάδοχος.
15. Καταγγελία της σύμβασης
Σε περίπτωση αθέτησης από πλευράς του αερομεταφορέα των διατάξεων που προβλέπονται στην ανακοίνωση επιβολής των υποχρεώσεων που είχαν δημοσιευθεί στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008, στο διάταγμα επιβολής των υποχρεώσεων, στη σύμβαση, στις διατάξεις της παρούσας προκήρυξης και στη συγγραφή υποχρεώσεων, η ENAC με γραπτή προειδοποίησή της μπορεί να χορηγήσει στον αερομεταφορέα, κατά την έννοια και κατ'εφαρμογή του άρθρου 1454 του αστικού κώδικα, προθεσμία 15 (δέκα πέντε) ημερών από την παραλαβή της προειδοποίησης αυτής να παύσει την αθέτηση των προαναφερθέντων όρων.
Μετά την πάροδο της προθεσμίας αυτής, η ENAC έχει τη δυνατότητα να θεωρήσει αυτοδικαίως ότι η σύμβαση έληξε και να παρακρατήσει οριστικά την εγγύηση που προαναφέρθηκε στο σημείο 13, καθώς και να απαιτήσει από τον αερομεταφορέα άμεση αποζημίωση.
Εξάλλου, σε περίπτωση παραβίασης των υποχρεώσεων και των παροχών που έχει αναλάβει ο αερομεταφορέας σύμφωνα με τη σύμβαση, τις διατάξεις του παρόντος διαγωνισμού και την συγγραφή υποχρεώσεων, η ENAC, κατά την έννοια και κατ' εφαρμογή του άρθρου 1456 του αστικού κώδικα, έχει το δικαίωμα να καταγγείλει τη σύμβαση με γραπτή προειδοποίηση του αερομεταφορέα από πλευράς της.
Σε περίπτωση καταγγελίας της σύμβασης, το Υπουργείο υποδομών και μεταφορών μπορεί να επιτρέψει στην ENAC να προσφύγει στον κατάλογο επιτυχόντων για να συνάψει νέα σύμβαση, για την εναπομένουσα περίοδο εκτέλεσης της γραμμής, με τον αμέσως επόμενο ανταγωνιζόμενο αερομεταφορέα του καταλόγου επιτυχόντων του διαγωνισμού με σκοπό την ανάθεση εκτέλεσης της γραμμής.
Τότε, η διάρκεια της σύμβασης αρχίζει από την ημερομηνία έναρξης εκτέλεσης της γραμμής και λήγει την προβλεπόμενη ημερομηνία λήξης της καταγγελθείσας σύμβασης, τηρουμένου του επιχειρηματικού σχεδίου που είχε εγκριθεί κατά την αξιολόγηση της προσφοράς που είχε υποβάλει ο πρώτος ανάδοχος.
16. Υποβολή των προσφορών
Εντός 30 (τριάντα) ημερών από τη δημοσίευση της παρούσας προκήρυξης στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης, οι προσφορές, οι οποίες πρέπει να είναι σύμφωνες με τη συγγραφή υποχρεώσεων, πρέπει να σταλούν, ειδάλλως θα απορριφθούν, με συστημένη επιστολή με απόδειξη παραλαβής, ή να επιδοθούν ιδιοχείρως έναντι απόδειξης παραλαβής στην εξής διεύθυνση: ENAC-Direzione Generale, viale del Castro Pretorio 118, I-00185 Roma.
Οι προσφορές πρέπει να υποβληθούν εσώκλειστες σε τρεις σφραγισμένους φακέλους, ειδάλλως θα απορριφθούν.
Ο εξωτερικός φάκελος, κλειστός, σφραγισμένος και μονογραφημένος και στα δύο άκρα, ο οποίος θα περιέχει δύο άλλους φακέλους, επίσης σφραγισμένους και μονογραφημένους στα άκρα, θα φέρει την εξής μνεία: «Offerta per la gara in oneri di servizio pubblico sulla rotta: Albenga-Roma Fiumicino e viceversa».
Τα έγγραφα που πρέπει να περιέχουν οι τρεις φάκελοι που προαναφέρθηκαν καθορίζονται στη συγγραφή υποχρεώσεων που αναφέρεται στο σημείο 4 της παρούσας προκήρυξης διαγωνισμού.
Εννοείται ότι η παραλαβή των φακέλων είναι στην αποκλειστική ευθύνη του αποστολέα εάν, για οποιοδήποτε λόγο, δεν φθάσουν μέσα στις προκαθορισμένες προθεσμίες στον προορισμό τους.
Ακόμη και εάν έχει υποβληθεί μία μόνον έγκυρη προσφορά, η σύμβαση είναι δυνατόν να ανατεθεί.
17. Λήξη ισχύος των προσφορών
180 (εκατόν ογδόντα) ημέρες από τη λήξη της προθεσμίας υποβολής των προσφορών.
18. Ανάθεση της σύμβασης
Η ENAC θα φέρει σε πέρας τον διαγωνισμό μέσω επιτροπής που θα συσταθεί επί τούτου και θα απαρτίζεται από έναν διευθύνοντα της ENAC που θα ορίσει ο Γενικός Διευθυντής, από έναν εμπειρογνώμονα σε θέματα αερομεταφορών που θα ορίσει η Περιφέρεια της Λιγουρίας και από έναν πρόεδρο που θα ορισθεί με τη συναίνεση της ENAC και της Περιφέρειας της Λιγουρίας· τα χρέη γραμματείας θα αναλάβει υπάλληλος της ENAC.
19. Επεξεργασία δεδομένων προσωπικού χαρακτήρα
Η χρήση και η επεξεργασία όλων των προσωπικών δεδομένων θα γίνει μόνον για θεσμικούς σκοπούς και θα εξασφαλισθεί η προστασία και η εμπιστευτικότητά τους σύμφωνα με την ισχύουσα νομοθεσία. Προς το σκοπό αυτό, ο ανάδοχος αερομεταφορέας πρέπει να υπογράψει τη σχετική άδεια επεξεργασίας των προσωπικών δεδομένων, σύμφωνα με όσα ορίζει το νομοθετικό διάταγμα αριθ. 196/2003 και οι μετέπειτα τροποποιήσεις και προσθήκες του.
20. Επεξεργασία ευαίσθητων δεδομένων
Η επεξεργασία των ευαίσθητων δεδομένων που θα περιέχουν οι προσφορές που θα υποβληθούν από τους αερομεταφορείς θα γίνει σύμφωνα με όσα προβλέπει ο «Regolamento per il trattamento dei dati sensibili e giudiziari», τον οποίον ενέκρινε το Διοικητικό Συμβούλιο της ENAC στη συνεδρίασή του της 2ας Μαρτίου 2006 και διατίθεται στο δικτυακό τόπο της ENAC «enac-italia.it».
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/86 |
Προκήρυξη διαγωνισμού που δημοσιεύθηκε από την Ιταλία βάσει του άρθρου 4 παράγραφος 1 στοιχείο δ) του κανονισμού (ΕΟΚ) αριθ. 2408/92 του Συμβουλίου για την εκτέλεση των τακτικών αεροπορικών γραμμών Κρότωνας — Μιλάνο Λινάτε και αντιστρόφως
(Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ)
(2008/C 276/08)
EΙΣΑΓΩΓΗ
Η ιταλική κυβέρνηση —το Υπουργείο Υποδομών Μεταφορών—, δυνάμει του άρθρου 4 του κανονισμού (ΕΟΚ) αριθ. 2408/92, σύμφωνα με τις αποφάσεις που εγκρίθηκαν κατά τη διάσκεψη των υπηρεσιών που διοργάνωσε η Περιφέρεια Calabria, ενέκρινε την παρούσα προκήρυξη διαγωνισμού με σκοπό την ανάθεση της εκτέλεσης αεροπορικών δρομολογίων στη γραμμή Κρότωνας — Μιλάνο Λινάτε και αντιστρόφως.
Οι προδιαγραφές της υποχρέωσης παροχής δημόσιας υπηρεσίας έχουν δημοσιευθεί στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008.
Εφόσον εντός 30 ημερών από τη δημοσίευση των ανωτέρω υποχρεώσεων κανένας αερομεταφορέας δεν έχει υποβάλει αίτηση για την παροχή υπηρεσίας αεροπορικής μεταφοράς στην ανωτέρω γραμμή, σύμφωνα με τις επιβαλλόμενες υποχρεώσεις δημόσιας υπηρεσίας και χωρίς οικονομική αντιστάθμιση, η ιταλική κυβέρνηση —Υπουργείο Υποδομών και Μεταφορών— αποφάσισε, σύμφωνα με τη διαδικασία του άρθρου 4 παράγραφος 1 στοιχείο δ) του κανονισμού (ΕΟΚ) αριθ. 2408/92, να περιορίσει την πρόσβαση στην εν λόγω γραμμή σε έναν και μόνον αερομεταφορέα, τον οποίο θα επιλέξει με διαγωνισμό για να εκτελεί την αεροπορική γραμμή σύμφωνα με τις διατάξεις του ιδίου κανονισμού.
ΓΕΝΙΚΕΣ ΔΙΑΤΑΞΕΙΣ
Η παρούσα προκήρυξη καθορίζει το αντικείμενο του διαγωνισμού, τους όρους συμμετοχής στο διαγωνισμό, τους όρους σχετικά με τη διάρκεια, την τροποποίηση και τη λήξη της σύμβασης, τις κυρώσεις σε περίπτωση αθέτησης των προδιαγραφόμενων διατάξεων και των εγγυήσεων που συνοδεύουν την προσφορά, όπως και σε περίπτωση μη εκτέλεσης της σύμβασης.
Το δικαίωμα εκτέλεσης των δρομολογίων στη συγκεκριμένη γραμμή θα εκχωρηθεί μετά από δημόσιο διαγωνισμό που θα κατακυρωθεί με μειοδοτική προσφορά, η οποία θα περιλαμβάνει την οικονομική αποζημίωση που καθορίζεται στο σημείο 6 της παρούσας προκήρυξης διαγωνισμού.
1. Αντικείμενο της προκήρυξης
Αντικείμενο της παρούσας προκήρυξης είναι η εκτέλεση τακτικών αεροπορικών δρομολογίων στη γραμμή Κρότωνας — Μιλάνο Λινάτε και αντιστρόφως, με βάση τις επιβαλλόμενες υποχρεώσεις παροχής δημόσιας υπηρεσίας που δημοσιεύθηκαν στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008, σύμφωνα με τις διατάξεις του κανονισμού (ΕΟΚ) αριθ. 2408/92.
2. Συμμετοχή
Αίτηση συμμετοχής στο διαγωνισμό μπορεί να υποβάλει κάθε κοινοτικός αερομεταφορέας, όπως ορίζει το άρθρο 2 στοιχείο β) του κανονισμού (ΕΟΚ) αριθ. 2408/92, ο οποίος πληροί τις εξής προϋποθέσεις:
Γενικές προϋποθέσεις
|
1. |
Να μην βρίσκεται σε κατάσταση πτώχευσης, εκκαθάρισης αναγκαστικής διαχείρισης, πτωχευτικού συμβιβασμού ή σε οποιαδήποτε παρόμοια διαδικασία για την κήρυξή του σε μια από τις ανωτέρω καταστάσεις. |
|
2. |
Να μην έχει καταδικασθεί σε απαγορευτική κύρωση κατά την έννοια του άρθρου 9 εδάφιο 2 του νομοθετικού διατάγματος αριθ. 231/2001 και να μην του έχει επιβληθεί ποινή, η οποία συνεπάγεται ότι δεν μπορεί να συμβληθεί με δημόσια αρχή. |
|
3. |
Να έχει εκπληρώσει τις υποχρεώσεις του όσον αφορά την καταβολή των εισφορών κοινωνικής ασφάλισης και εργασιακών επιδομάτων. |
|
4. |
Να μην έχει υποβάλει ψευδείς δηλώσεις σχετικά με τους όρους συμμετοχής του σε άλλες διαδικασίες διαγωνισμού για την ανάθεση εκτέλεσης τακτικών γραμμών με βάση υποχρεώσεις παροχής δημόσιας υπηρεσίας. |
Προκειμένου να δηλώσει ότι πληροί τις ανωτέρω προϋποθέσεις, ο υποψήφιος υποβάλλει, όσον αφορά την κατάστασή του σε σχέση με το σημείο 3., βεβαίωση εξόφλησης ασφαλιστικών εισφορών του εκδοθείσα από την INPS ή την INAIL και τη βεβαίωση που προβλέπεται από το άρθρο 17 του νόμου αριθ. 68 της 12ης Μαρτίου 1999«Norme per il diritto al lavoro dei disabili»· για τα σημεία 1, 2 και 4, δήλωση η οποία επέχει θέση όρκου σύμφωνα με τα άρθρα 46 και 47 του προεδρικού διατάγματος αριθ. 445 της 28ης Δεκεμβρίου 2000.
Για τους υποψηφίους άλλου κράτους μέλους της Ευρωπαϊκής Ένωσης, πλην της Ιταλίας, τα πιστοποιητικά ή οι βεβαιώσεις πρέπει να έχουν εκδοθεί από διοικητικές αρχές ή οργανισμούς της χώρας καταγωγής και να συνοδεύονται από μετάφρασή τους στην ιταλική γλώσσα, επικυρωμένη από την ιταλική προξενική αρχή, η οποία πιστοποιεί και το γνήσιο του πρωτοτύπου.
Τεχνικές προϋποθέσεις
|
1. |
Άδεια αεροπορικής εκμετάλλευσης εκδοθείσα σύμφωνα με τον κανονισμό (ΕΟΚ) αριθ. 2407/92. |
|
2. |
Υποχρεωτική ασφάλιση αστικής ευθύνης σε περίπτωση συμβάντος, ιδίως έναντι επιβατών, αποσκευών, μεταφερόμενων εμπορευμάτων και τρίτων, σύμφωνα και με τον κανονισμό (ΕΚ) αριθ. 785/2004. |
|
3. |
Πιστοποιητικό αερομεταφορέα (AOC) σύμφωνα με τα κοινοτικά πρότυπα. |
|
4. |
Μη αναγραφή του στην ονομαζόμενη «μαύρη λίστα» των αεροπορικών εταιρειών που δεν πληρούν τα πρότυπα ασφάλειας πτήσεων, όπως αυτή δημοσιεύεται στο δικτυακό τόπο: http://ec.europa.eu/transport/air-ban. |
|
5. |
Σύστημα αναλυτικής λογιστικής με διαχωρισμό των σχετικών δαπανών (όπου περιλαμβάνονται τα πάγια έξοδα και τα έσοδα). |
Σε περίπτωση απώλειας των εν λόγω δικαιολογητικών μετά την υποβολή της αίτησης συμμετοχής στο διαγωνισμό, οι διαγωνιζόμενοι αερομεταφορείς αποκλείονται αυτόματα από την αξιολόγηση των προσφορών τους.
Σε περίπτωση απώλειας των εν λόγω δικαιολογητικών μετά τη σύναψη της σύμβασης που αναφέρεται στο σημείο 5, εφαρμόζονται οι διατάξεις του σημείου 14 και του σημείου 15 προτελευταίο εδάφιο, της παρούσας προκήρυξης διαγωνισμού.
3. Διαδικασία
Η παρούσα πρόσκληση υποβολής προσφορών υπόκειται στις διατάξεις του άρθρου 4 παράγραφος 1 στοιχεία δ), ε), στ) η) και θ) του κανονισμού (ΕΟΚ) αριθ. 2408/92.
4. Φάκελος της προκήρυξης διαγωνισμού
Ο πλήρης φάκελος της παρούσας προκήρυξης διαγωνισμού, ο οποίος περιλαμβάνει τους ειδικούς κανόνες του διαγωνισμού, την προθεσμία ισχύος των προσφορών και κάθε άλλη χρήσιμη πληροφορία, αποτελεί αναπόσπαστο μέρος του διαγωνισμού μαζί με το υπόδειγμα σύμβασης που αναφέρεται στο σημείο 5 και διατίθεται δωρεάν στην εξής διεύθυνση: ENAC, Direzione Trasporto Aereo, viale del Castro Pretorio 118, I-00185 Roma ή μέσω ηλεκτρονικού ταχυδρομείου στην εξής διεύθυνση: trasporto.aereo@enac.rupa.it.
5. Ρυθμιστική σύμβαση εκτέλεσης του δρομολογίου
Η εκτέλεση της δημόσιας υπηρεσίας διέπεται από σύμβαση μεταξύ του αερομεταφορέα και της ENAC, η οποία θα συνταχθεί σύμφωνα με το υπόδειγμα που περιλαμβάνει ο φάκελος του διαγωνισμού.
6. Οικονομική αντιστάθμιση
Το ύψος της οικονομικής αντιστάθμισης, με βάση τον διαγωνισμό ανάθεσης εκτέλεσης μεταφορών στην συγκεκριμένη τακτική γραμμή, είναι 1 258 178,33 EUR (ένα εκατομμύριο διακόσιες πενήντα οκτώ χιλιάδες εκατόν εβδομήντα οκτώ ευρώ και τριάντα τρία λεπτά) συμπεριλαμβανομένου του ΦΠΑ, ετησίως.
Στις προσφορές, οι οποίες πρέπει να συνταχθούν όπως καθορίζεται στη συγγραφή υποχρεώσεων, πρέπει να αναγράφεται ρητά, στο μέρος του εντύπου που αφορά την οικονομική προσφορά με ετήσια κατανομή, το μέγιστο ύψος της οικονομικής αντιστάθμισης που ζητείται, εντός του ορίου που προαναφέρθηκε, για την εκτέλεση της συγκεκριμένης υποχρέωσης.
Το ακριβές ύψος της οικονομικής αντιστάθμισης καθορίζεται εκ των υστέρων κάθε χρόνο, ανάλογα με το πραγματικό κόστος και έσοδα που θα προκύψουν από την εκτέλεση της γραμμής, βάσει δικαιολογητικών και εντός του μέγιστου ορίου που θα αναφέρεται στην προσφορά και των όσων ορίζονται στην συγγραφή υποχρεώσεων.
Σε κάθε περίπτωση, ο αερομεταφορέας δεν μπορεί να ζητήσει οικονομική αντιστάθμιση υψηλότερη από το όριο που θα καθορίζεται στη σύμβαση, λαμβανομένου υπόψη ότι δεν πρόκειται για αντιπαροχή αλλά για αντιστάθμιση για την ανάληψη υποχρέωσης δημόσιας υπηρεσίας.
Οι ετήσιες πληρωμές καταβάλλονται υπό μορφή προκαταβολών και υπολοίπου εξόφλησης, με βάση τους όρους της συγγραφής υποχρεώσεων, με την επιφύλαξη ενδεχόμενων ελέγχων από την ENAC με σκοπό να επαληθευθεί ο προορισμός της χορηγούμενης οικονομικής αντιστάθμισης και η τήρηση των όρων από τον δικαιούχο αερομεταφορέα. Το υπόλοιπο καταβάλλεται μετά από έλεγχο της αναλυτικής λογιστικής του αερομεταφορέα για τη συγκεκριμένη γραμμή και μετά από έλεγχο της τήρησης των όρων παροχής της επιβαλλόμενης δημόσιας υπηρεσίας.
7. Ναύλοι
Στις προσφορές που θα υποβληθούν πρέπει να αναφέρονται οι προβλεπόμενοι ναύλοι, σύμφωνα με όσα καθορίζονται στην ανακοίνωση για την επιβολή παροχής δημόσιας υπηρεσίας που δημοσιεύθηκε στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008.
8. Έναρξη της γραμμής
Η γραμμή θα αρχίσει εντός 15 (δέκα πέντε) ημερών από την ημερομηνία που θα καθορίζεται στη σύμβαση και θα βεβαιωθεί με δήλωση έναρξης της γραμμής, την οποία θα υπογράψουν ο ανάδοχος αερομεταφορέας και η ENAC.
9. Διάρκεια της σύμβασης
Η σύμβαση θα είναι διάρκειας δύο ετών από την ημερομηνία έναρξης των δρομολογίων στη συγκεκριμένη γραμμή.
Ο αερομεταφορέας δεσμεύεται να θέσει στη διάθεση της ENAC το προσωπικό, τα τεχνικά και λογιστικά έγγραφα, τον εξοπλισμό και οτιδήποτε άλλο χρειασθεί για τη διεκπεραίωση των εποπτικών δραστηριοτήτων και τον έλεγχο της ορθής τήρησης, εφαρμογής και εκτέλεσης των διατάξεων που περιέχει η ανακοίνωση της Επιτροπής, η προκήρυξη επιβολής των υποχρεώσεων, η παρούσα προκήρυξη, η σύμβαση και η συγγραφή υποχρεώσεων.
Η αθέτηση των υποχρεώσεων που προαναφέρθηκαν συνεπάγεται επιβολή κυρώσεων σύμφωνα με όσα προβλέπονται στο σημείο 11 της παρούσας προκήρυξης.
10. Καταγγελία της σύμβασης
Οποιοδήποτε συμβαλλόμενο μέρος μπορεί να καταγγείλει τη σύμβαση με προειδοποίηση 6 (έξι) μηνών χωρίς υποχρέωση οικονομικής αντιστάθμισης ή αποζημίωσης και ούτως ή άλλως το ενωρίτερο 12 (δώδεκα) μήνες από την έναρξη της γραμμής.
Η σύμβαση καταγγέλλεται χωρίς προειδοποίηση για μη εκπλήρωση της υποχρέωσης δημόσιας υπηρεσίας, εφόσον, μετά από προειδοποιητική επιστολή της ENAC προς τον ενδιαφερόμενο αερομεταφορέα ότι δεν έχει εκπληρώσει εξ ολοκλήρου τις υποχρεώσεις που ανέλαβε, ο αερομεταφορέας δεν αρχίσει την εκτέλεση των υποχρεώσεων δημόσιας υπηρεσίας εντός 30 (τριάντα) ημερών κατ' ανώτατο όριο από την ημερομηνία παραλαβής της επιστολής.
Σε περίπτωση καταγγελίας της σύμβασης από τον αερομεταφορέα, η ENAC έχει το δικαίωμα να προβεί σε έλεγχο, προκειμένου να προτείνει στο Υπουργείο υποδομών και μεταφορών τη σύναψη νέας σύμβασης με τον αμέσως επόμενο αερομεταφορέα από τον κατάλογο υποψηφίων. Οι όροι εκτέλεσης της γραμμής με βάση τις υποχρεώσεις παροχής δημόσιας υπηρεσίας και η οφειλόμενη κατ' αναλογία οικονομική αντιστάθμιση παραμένουν ίδιοι με εκείνους που ίσχυαν πριν την ανάθεση των υποχρεώσεων δημόσιας υπηρεσίας.
11. Αθέτηση της σύμβασης και κυρώσεις
Δεν αποτελεί παρατυπία καταλογιζόμενη στον αερομεταφορέα η μη εκτέλεση του δρομολογίου για τους κάτωθι λόγους:
|
— |
επικίνδυνες μετεωρολογικές συνθήκες, |
|
— |
κλείσιμο ενός των αεροδρομίων των αναφερόμενων στο επιχειρησιακό πρόγραμμα, |
|
— |
προβλήματα ασφαλείας, |
|
— |
απεργία, |
|
— |
περιπτώσεις ανωτάτης βίας. |
Η διακοπή του δρομολογίου για τους ανωτέρω λόγους συνεπάγεται μείωση του ύψους της οικονομικής αντιστάθμισης κατ' αναλογία των πτήσεων που δεν πραγματοποιήθηκαν.
Σε περίπτωση μη παροχής των υπηρεσιών και αθέτησης των υποχρεώσεων που περιέχει η σύμβαση, η ENAC έχει το δικαίωμα να επιβάλει κυρώσεις στον αερομεταφορέα, ανάλογες προς τον αριθμό των παραβιάσεων που διέπραξε και σύμφωνα με τον τρόπο που περιγράφεται στο υπόδειγμα σύμβασης.
Σε κάθε περίπτωση, το ύψος των κυρώσεων δεν είναι δυνατόν να υπερβεί το 50 % του μέγιστου ύψους της οικονομικής αντιστάθμισης που προβλέπεται στον διαγωνισμό, όπως αναφέρεται στο σημείο 6, με την επιφύλαξη ότι, πέραν του ορίου αυτού, η ENAC έχει το δικαίωμα να καταγγείλει τη σύμβαση για λόγους αθέτησης της, με αποτέλεσμα την άμεση ανάκληση της οφειλόμενης οικονομικής αντιστάθμισης.
Ο αριθμός των πτήσεων που ματαιώνονται για λόγους απευθείας καταλογιζόμενους στον αερομεταφορέα δεν πρέπει να υπερβαίνει ετησίως το 2 % του αριθμού των προγραμματισμένων πτήσεων.
Άνω του ορίου αυτού, ο αερομεταφορέας οφείλει να καταθέσει στην ENAC, ως πρόστιμο, το ποσό των 3 000,00 EUR (τριών χιλιάδων ευρώ) για κάθε ματαιωθείσα πτήση που υπερβαίνει το ανωτέρω όριο του 2 %, κατόπιν επίσημης προειδοποίησης του αερομεταφορέα εντός δέκα ημερών από την ημερομηνία του συμβάντος. Ο αερομεταφορέας διαθέτει επτά ημέρες κατ' ανώτατο όριο για να υποβάλει τυχόν αντιρρήσεις του.
Η ENAC θα προβεί, άλλωστε, σε αναθεώρηση του ύψους της οικονομικής αντιστάθμισης ανάλογη των πτήσεων που δεν εκτελέστηκαν. Τα ποσά που θα εισπραχθούν όπως προαναφέρθηκε θα διατεθούν για τη χρηματοδότηση της συνέχειας των μεταφορικών συνδέσεων με την πόλη του Crotone.
Η μη τήρηση της προειδοποίησης που προαναφέρθηκε στο σημείο 10 συνεπάγεται την επιβολή προστίμου, το οποίο υπολογίζεται με βάση την ετήσια οικονομική αντιστάθμιση και το χρονικό διάστημα αθέτησης της προειδοποίησης από τη διακοπή του δρομολογίου, όπως προβλέπεται στο ίδιο σημείο 10, με την εφαρμογή του εξής τύπου:
P = CA/GG x gg
όπου:
|
P |
= |
πρόστιμο |
|
CA |
= |
ετήσια αντιστάθμιση |
|
GG |
= |
ημέρες του υπό εξέταση έτους (365 ή 366) |
|
gg |
= |
ημέρες αθέτησης προειδοποίησης |
Οι κυρώσεις που αναφέρονται στο παρόν σημείο είναι συσσωρεύσιμες με εκείνες που προβλέπονται αντίστοιχα από κοινοτικούς κανονισμούς και από εθνικές διατάξεις και κανονισμούς.
12. Εγγυήσεις για την προσφορά
Προκειμένου να βεβαιώσει τη σοβαρότητα και την αξιοπιστία της προσφοράς του, ο αερομεταφορέας που συμμετέχει στον παρόντα διαγωνισμό οφείλει να καταθέσει εγγύηση ύψους 2 % της μέγιστης οικονομικής αντιστάθμισης που αναφέρεται στο σημείο 6, υπό μορφή σύστασης εγγύησης ή τραπεζικής ή ασφαλιστικής εγγύησης, κατ' επιλογήν του υποβάλλοντος την προσφορά.
Ο τρόπος σύστασης της ανωτέρω εγγύησης θα καθορισθεί στη συγγραφή υποχρεώσεων και θα αναφέρεται ενδεχομένως στη σύμβαση.
Η ισχύς της εγγύησης είναι διάρκειας τουλάχιστον 180 (εκατόν ογδόντα) ημερών από την καταληκτική ημερομηνία υποβολής των προσφορών, με υποχρέωση από πλευράς του αερομεταφορέα να ανανεώσει την εγγύηση εφόσον, έως την καταληκτική ημερομηνία, δεν έχει ανατεθεί η σύμβαση, κατ' αίτηση της ENAC κατά τη διάρκεια της διαδικασίας αυτής.
Η ENAC προβλέπει, ταυτόχρονα με την κοινοποίησή της προς τους απορριφθέντες αερομεταφορείς σχετικά με την ανάθεση της σύμβασης, την αποδέσμευση της εγγύησής τους.
13. Εγγυήσεις εκτέλεσης και ασφαλιστική κάλυψη
Ο αερομεταφορέας, ο οποίος θα αναλάβει την εκτέλεση δρομολογίων σύμφωνα με τις παρούσες υποχρεώσεις παροχής δημόσιας υπηρεσίας, οφείλει να συστήσει τραπεζική ή ασφαλιστική εγγύηση ύψους 700 000,00 EUR (επτακοσίων χιλιάδων ευρώ) υπέρ της ENAC, η οποία διατηρεί το δικαίωμα να την χρησιμοποιήσει για να εξασφαλίσει τη συνέχεια της γραμμής.
Η άδεια παραλαβής δίδεται αυτόματα, χωρίς να χρειάζεται έγκριση από την ENAC, μετά από την τακτική εξέταση που αναφέρεται στην τελευταία παράγραφο του σημείου 6.
14. Λήξη και ανάκληση της οικονομικής αντιστάθμισης
Η ανά πάσα στιγμή απώλεια, μετά τη σύναψη της σύμβασης, των γενικών και τεχνικών δικαιολογητικών που αναφέρονται στο σημείο 2 της παρούσας προκήρυξης, καθώς και εκείνων που αναφέρονται στη συγγραφή υποχρεώσεων, συνεπάγεται τη λήξη της ανάθεσης εκτέλεσης του δρομολογίου, την ανάκληση της οικονομικής αντιστάθμισης και την επιστροφή τυχόν μη οφειλόμενων ποσών που εισπράχθηκαν, προσαυξημένων κατά τους νόμιμους φόρους.
Μετά τη λήξη της προθεσμίας ανάθεσης της γραμμής, το Υπουργείο υποδομών και μεταφορών μπορεί να επιτρέψει στην ENAC να συνάψει νέα σύμβαση, για την εναπομένουσα περίοδο εκτέλεσης της γραμμής με τον αμέσως επόμενο συναγωνιζόμενο αερομεταφορέα από τον τελικό κατάλογο επιλεγέντων υποψηφίων.
Τότε, η διάρκεια της σύμβασης αρχίζει από την ημερομηνία έναρξης εκτέλεσης της γραμμής και λήγει την προβλεπόμενη ημερομηνία λήξης της καταγγελθείσας σύμβασης, τηρουμένου του επιχειρηματικού σχεδίου που είχε εγκριθεί κατά την αξιολόγηση της προσφοράς που είχε υποβάλει ο πρώτος ανάδοχος.
15. Καταγγελία της σύμβασης
Σε περίπτωση αθέτησης από πλευράς του αερομεταφορέα των διατάξεων που προβλέπονται στην ανακοίνωση επιβολής των υποχρεώσεων που είχαν δημοσιευθεί στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20.9.2008, στο διάταγμα επιβολής των υποχρεώσεων, στη σύμβαση, στις διατάξεις της παρούσας προκήρυξης και στη συγγραφή υποχρεώσεων, η ENAC με γραπτή προειδοποίησή της μπορεί να χορηγήσει στον αερομεταφορέα, κατά την έννοια και κατ' εφαρμογή του άρθρου 1454 του αστικού κώδικα, προθεσμία 15 (δέκα πέντε) ημερών από την παραλαβή της προειδοποίησης αυτής να παύσει την αθέτηση των προαναφερθέντων όρων.
Μετά την πάροδο της προθεσμίας αυτής, η ENAC έχει τη δυνατότητα να θεωρήσει αυτοδικαίως ότι η σύμβαση έληξε και να παρακρατήσει οριστικά την εγγύηση που προαναφέρθηκε στο σημείο 13, καθώς και να απαιτήσει από τον αερομεταφορέα άμεση αποζημίωση.
Εξάλλου, σε περίπτωση παραβίασης των υποχρεώσεων και των παροχών που έχει αναλάβει ο αερομεταφορέας σύμφωνα με τη σύμβαση, τις διατάξεις της παρούσας προκήρυξης διαγωνισμού και την συγγραφή υποχρεώσεων, η ENAC, κατά την έννοια και κατ' εφαρμογή του άρθρου 1456 του αστικού κώδικα, έχει το δικαίωμα να καταγγείλει τη σύμβαση με γραπτή προειδοποίηση του αερομεταφορέα από πλευράς της.
Σε περίπτωση καταγγελίας της σύμβασης, το Υπουργείο υποδομών και μεταφορών μπορεί να επιτρέψει στην ENAC να προσφύγει στον κατάλογο επιτυχόντων για να συνάψει νέα σύμβαση, για την εναπομένουσα περίοδο εκτέλεσης της γραμμής, με τον αμέσως επόμενο συναγωνιζόμενο αερομεταφορέα του καταλόγου επιτυχόντων του διαγωνισμού με σκοπό την ανάθεση εκτέλεσης της γραμμής.
Τότε, η διάρκεια της σύμβασης αρχίζει από την ημερομηνία έναρξης εκτέλεσης της γραμμής και λήγει την προβλεπόμενη ημερομηνία λήξης της καταγγελθείσας σύμβασης, τηρουμένου του επιχειρηματικού σχεδίου που είχε εγκριθεί κατά την αξιολόγηση της προσφοράς που είχε υποβάλει ο πρώτος ανάδοχος.
16. Υποβολή των προσφορών
Εντός 30 (τριάντα) ημερών από τη δημοσίευση της παρούσας προκήρυξης στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης, οι προσφορές, οι οποίες πρέπει να είναι σύμφωνες με τη συγγραφή υποχρεώσεων, πρέπει να σταλούν, ειδάλλως θα απορριφθούν, με συστημένη επιστολή με απόδειξη παραλαβής, ή να επιδοθούν ιδιοχείρως έναντι απόδειξης παραλαβής στην εξής διεύθυνση: ENAC-Direzione generale, viale del Castro Pretorio 118, I-00185 Roma.
Οι προσφορές πρέπει να υποβληθούν εσώκλειστες σε τρεις σφραγισμένους φακέλους, ειδάλλως θα απορριφθούν.
Ο εξωτερικός φάκελος, κλειστός, σφραγισμένος και μονογραφημένος και στα δύο άκρα, ο οποίος θα περιέχει δύο άλλους φακέλους, επίσης σφραγισμένους και μονογραφημένους στα άκρα, θα φέρει την εξής μνεία: «Offerta per la gara in oneri di servizio pubblico sulla rotta Crotone-Milano Linate e viceversa».
Τα έγγραφα που πρέπει να περιέχουν οι τρεις φάκελοι που προαναφέρθηκαν καθορίζονται στη συγγραφή υποχρεώσεων που αναφέρεται στο σημείο 4 της παρούσας προκήρυξης διαγωνισμού.
Εννοείται ότι η παραλαβή των φακέλων είναι στην αποκλειστική ευθύνη του αποστολέα εάν, για οποιοδήποτε λόγο, δεν φθάσουν μέσα στις προκαθορισμένες προθεσμίες στον προορισμό τους.
Ακόμη και εάν έχει υποβληθεί μία μόνον έγκυρη προσφορά, η σύμβαση είναι δυνατόν να ανατεθεί.
17. Διάρκεια ισχύος των προσφορών
180 (εκατόν ογδόντα) ημέρες από τη λήξη της προθεσμίας υποβολής των προσφορών.
18. Ανάθεση της σύμβασης
Η ENAC θα φέρει σε πέρας τον διαγωνισμό μέσω επιτροπής που θα συσταθεί επί τούτου και θα απαρτίζεται από έναν διευθύνοντα της ENAC που θα ορίσει ο Γενικός Διευθυντής, από έναν εμπειρογνώμονα σε θέματα αερομεταφορών που θα ορίσει η Περιφέρεια της Καλαβρίας και από έναν πρόεδρο που θα ορισθεί με τη συναίνεση της ENAC και της Περιφέρειας της Καλαβρίας· τα χρέη γραμματείας θα αναλάβει υπάλληλος της ENAC.
19. Επεξεργασία προσωπικών δεδομένων
Η χρήση και η επεξεργασία όλων των προσωπικών δεδομένων θα γίνει μόνον για θεσμικούς σκοπούς και θα εξασφαλισθεί η προστασία και η εμπιστευτικότητά τους σύμφωνα με την ισχύουσα νομοθεσία. Προς το σκοπό αυτό, ο ανάδοχος αερομεταφορέας πρέπει να υπογράψει τη σχετική άδεια επεξεργασίας των προσωπικών δεδομένων, σύμφωνα με όσα ορίζει το νομοθετικό διάταγμα αριθ. 196/2003 και οι μετέπειτα τροποποιήσεις και προσθήκες του. Προς το σκοπό αυτό, ο ανάδοχος αερομεταφορέας πρέπει να υπογράψει τη σχετική άδεια επεξεργασίας των προσωπικών δεδομένων, σύμφωνα με όσα ορίζει το νομοθετικό διάταγμα αριθ. 196/2003 και οι μετέπειτα τροποποιήσεις και προσθήκες του.
20. Επεξεργασία ευαίσθητων δεδομένων
Η επεξεργασία των ευαίσθητων δεδομένων που θα περιέχουν οι προσφορές που θα υποβληθούν από τους αερομεταφορείς θα γίνει σύμφωνα με όσα προβλέπει ο «Regolamento per il trattamento dei dati sensibili e giudiziari», τον οποίον ενέκρινε το Διοικητικό Συμβούλιο της ENAC στη συνεδρίασή του της 2ας Μαρτίου 2006 και διατίθεται στο δικτυακό τόπο της ENAC «enac-italia.it».
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/90 |
Προκήρυξη διαγωνισμού που δημοσιεύθηκε από την Ιταλία βάσει του άρθρου 4 παράγραφος 1 στοιχείο δ) του κανονισμού (ΕΟΚ) αριθ. 2408/92 του Συμβουλίου για την εκτέλεση των τακτικών αεροπορικών γραμμών Κροτόνε — Ρώμη Φιουμιτσίνο και αντιστρόφως
(Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ)
(2008/C 276/09)
ΕΙΣΑΓΩΓΗ
Η ιταλική κυβέρνηση —το Υπουργείο Υποδομών Μεταφορών—, δυνάμει του άρθρου 4 του κανονισμού (ΕΟΚ) αριθ. 2408/92, σύμφωνα με τις αποφάσεις που εγκρίθηκαν κατά τη διάσκεψη των υπηρεσιών που διοργάνωσε η Περιφέρεια Καλαβρία, ενέκρινε την παρούσα προκήρυξη διαγωνισμού με σκοπό την ανάθεση της εκτέλεσης αεροπορικών δρομολογίων στη γραμμή Κροτόνε — Ρώμη Φιουμιτσίνο και αντιστρόφως.
Οι προδιαγραφές της υποχρέωσης παροχής δημόσιας υπηρεσίας έχουν δημοσιευθεί στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20ής Σεπτεμβρίου 2008.
Εφόσον, εντός 30 ημερών από τη δημοσίευση των ανωτέρω υποχρεώσεων, κανένας αερομεταφορέας δεν έχει υποβάλει αίτηση για την παροχή υπηρεσίας αεροπορικής μεταφοράς στην ανωτέρω γραμμή, σύμφωνα με τις επιβαλλόμενες υποχρεώσεις δημόσιας υπηρεσίας και χωρίς οικονομική αντιστάθμιση, η ιταλική κυβέρνηση —Υπουργείο Υποδομών και Μεταφορών— αποφάσισε, σύμφωνα με τη διαδικασία του άρθρου 4 παράγραφος 1 στοιχείο δ) του κανονισμού (ΕΟΚ) αριθ. 2408/92, να περιορίσει την πρόσβαση στην εν λόγω γραμμή σε έναν και μόνον αερομεταφορέα, τον οποίο θα επιλέξει με διαγωνισμό για να εκτελεί την αεροπορική γραμμή σύμφωνα με τις διατάξεις του ιδίου κανονισμού.
ΓΕΝΙΚΕΣ ΔΙΑΤΑΞΕΙΣ
Η παρούσα προκήρυξη καθορίζει το αντικείμενο του διαγωνισμού, τους όρους συμμετοχής στο διαγωνισμό, τους όρους σχετικά με τη διάρκεια, την τροποποίηση και τη λήξη της σύμβασης, τις κυρώσεις σε περίπτωση αθέτησης των προδιαγραφόμενων διατάξεων και των εγγυήσεων που συνοδεύουν την προσφορά, όπως και σε περίπτωση μη εκτέλεσης της σύμβασης.
Το δικαίωμα εκτέλεσης των δρομολογίων στη συγκεκριμένη γραμμή θα εκχωρηθεί μετά από δημόσιο διαγωνισμό που θα κατακυρωθεί με μειοδοτική προσφορά, η οποία θα περιλαμβάνει την οικονομική αποζημίωση που καθορίζεται στο σημείο 6 της παρούσας προκήρυξης διαγωνισμού.
1. Αντικείμενο της προκήρυξης
Αντικείμενο της παρούσας προκήρυξης είναι η εκτέλεση τακτικών αεροπορικών δρομολογίων στη γραμμή Κροτόνε — Ρώμη Φιουμιτσίνο και αντιστρόφως, με βάση τις επιβαλλόμενες υποχρεώσεις παροχής δημόσιας υπηρεσίας που δημοσιεύθηκαν στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20ής Σεπτεμβρίου 2008, σύμφωνα με τις διατάξεις του κανονισμού (ΕΟΚ) αριθ. 2408/92.
2. Συμμετοχή
Αίτηση συμμετοχής στο διαγωνισμό μπορεί να υποβάλει κάθε κοινοτικός αερομεταφορέας, όπως ορίζει το άρθρο 2 στοιχείο β) του κανονισμού (ΕΟΚ) αριθ. 2408/92, ο οποίος πληροί τις εξής προϋποθέσεις:
Γενικές προϋποθέσεις
|
1. |
Να μην βρίσκεται σε κατάσταση πτώχευσης, εκκαθάρισης αναγκαστικής διαχείρισης, πτωχευτικού συμβιβασμού ή σε οποιαδήποτε παρόμοια διαδικασία για την κήρυξή του σε μια από τις ανωτέρω καταστάσεις. |
|
2. |
Να μην έχει καταδικασθεί σε απαγορευτική κύρωση κατά την έννοια του άρθρου 9 εδάφιο 2 του νομοθετικού διατάγματος αριθ. 231/2001 και να μην του έχει επιβληθεί ποινή, η οποία συνεπάγεται ότι δεν μπορεί να συμβληθεί με δημόσια αρχή. |
|
3. |
Να έχει εκπληρώσει τις υποχρεώσεις του όσον αφορά την καταβολή των εισφορών κοινωνικής ασφάλισης και εργασιακών επιδομάτων. |
|
4. |
Να μην έχει υποβάλει ψευδείς δηλώσεις σχετικά με τους όρους συμμετοχής του σε άλλες διαδικασίες διαγωνισμού για την ανάθεση εκτέλεσης τακτικών γραμμών με βάση υποχρεώσεις παροχής δημόσιας υπηρεσίας. |
Προκειμένου να δηλώσει ότι πληροί τις ανωτέρω προϋποθέσεις, ο υποψήφιος υποβάλλει, όσον αφορά την κατάστασή του σε σχέση με το σημείο 3, βεβαίωση εξόφλησης ασφαλιστικών εισφορών του εκδοθείσα από την INPS ή την INAIL και τη βεβαίωση που προβλέπεται από το άρθρο 17 του νόμου αριθ. 68 της 12ης Μαρτίου 1999«Norme per il diritto al lavoro dei disabili»· για τα σημεία 1, 2 και 4, δήλωση η οποία επέχει θέση όρκου σύμφωνα με τα άρθρα 46 και 47 του προεδρικού διατάγματος αριθ. 445 της 28ης Δεκεμβρίου 2000.
Για τους υποψηφίους άλλου κράτους μέλους της Ευρωπαϊκής Ένωσης, πλην της Ιταλίας, τα πιστοποιητικά ή οι βεβαιώσεις πρέπει να έχουν εκδοθεί από διοικητικές αρχές ή οργανισμούς της χώρας καταγωγής και να συνοδεύονται από μετάφρασή τους στην ιταλική γλώσσα, επικυρωμένη από την ιταλική προξενική αρχή, η οποία πιστοποιεί και το γνήσιο του πρωτοτύπου.
Τεχνικές προϋποθέσεις
|
1. |
Άδεια αεροπορικής εκμετάλλευσης εκδοθείσα σύμφωνα με τον κανονισμό (ΕΟΚ) αριθ. 2407/92. |
|
2. |
Υποχρεωτική ασφάλιση αστικής ευθύνης σε περίπτωση συμβάντος, ιδίως έναντι επιβατών, αποσκευών, μεταφερόμενων εμπορευμάτων και τρίτων, σύμφωνα και με τον κανονισμό (ΕΚ) αριθ. 785/2004. |
|
3. |
Πιστοποιητικό αερομεταφορέα (AOC) σύμφωνα με τα κοινοτικά πρότυπα. |
|
4. |
Μη αναγραφή του στην ονομαζόμενη «μαύρη λίστα» των αεροπορικών εταιρειών που δεν πληρούν τα πρότυπα ασφάλειας πτήσεων, όπως αυτή δημοσιεύεται στο δικτυακό τόπο: http://ec.europa.eu/transport/air-ban. |
|
5. |
Σύστημα αναλυτικής λογιστικής με διαχωρισμό των σχετικών δαπανών (όπου περιλαμβάνονται τα πάγια έξοδα και τα έσοδα). |
Σε περίπτωση απώλειας των εν λόγω δικαιολογητικών μετά την υποβολή της αίτησης συμμετοχής στο διαγωνισμό, οι διαγωνιζόμενοι αερομεταφορείς αποκλείονται αυτόματα από την αξιολόγηση των προσφορών τους.
Σε περίπτωση απώλειας των εν λόγω δικαιολογητικών μετά τη σύναψη της σύμβασης που αναφέρεται στο σημείο 5, εφαρμόζονται οι διατάξεις του σημείου 14 και του σημείου 15 προτελευταίο εδάφιο, της παρούσας προκήρυξης διαγωνισμού.
3. Διαδικασία
Η παρούσα πρόσκληση υποβολής προσφορών υπόκειται στις διατάξεις του άρθρου 4 παράγραφος 1 στοιχεία δ), ε), στ) η) και θ) του κανονισμού (ΕΟΚ) αριθ. 2408/92.
4. Φάκελος της προκήρυξης διαγωνισμού
Ο πλήρης φάκελος της παρούσας προκήρυξης διαγωνισμού, ο οποίος περιλαμβάνει τους ειδικούς κανόνες του διαγωνισμού, την προθεσμία ισχύος των προσφορών και κάθε άλλη χρήσιμη πληροφορία, αποτελεί αναπόσπαστο μέρος του διαγωνισμού μαζί με το υπόδειγμα σύμβασης που αναφέρεται στο σημείο 5 και διατίθεται δωρεάν στην εξής διεύθυνση: ENAC, Direzione Trasporto Aereo Viale del Castro Pretorio 118, 00185 Roma ή μέσω ηλεκτρονικού ταχυδρομείου στην εξής διεύθυνση: trasporto.aereo@enac.rupa.it.
5. Ρυθμιστική σύμβαση εκτέλεσης του δρομολογίου
Η εκτέλεση της δημόσιας υπηρεσίας διέπεται από σύμβαση μεταξύ του αερομεταφορέα και της ENAC, η οποία θα συνταχθεί σύμφωνα με το υπόδειγμα που περιλαμβάνει ο φάκελος του διαγωνισμού.
6. Οικονομική αντιστάθμιση
Το ύψος της οικονομικής αντιστάθμισης, με βάση τον διαγωνισμό ανάθεσης εκτέλεσης μεταφορών στην συγκεκριμένη τακτική γραμμή, είναι 1 724 666,00 EUR (ένα εκατομμύριο επτακόσιες εικοσιτέσσερις χιλιάδες εξακόσια εξήντα έξι ευρώ) συμπεριλαμβανομένου του ΦΠΑ, ετησίως.
Στις προσφορές, οι οποίες πρέπει να συνταχθούν όπως καθορίζεται στη συγγραφή υποχρεώσεων, πρέπει να αναγράφεται ρητά, στο μέρος του εντύπου που αφορά την οικονομική προσφορά με ετήσια κατανομή, το μέγιστο ύψος της οικονομικής αντιστάθμισης που ζητείται, εντός του ορίου που προαναφέρθηκε, για την εκτέλεση της συγκεκριμένης υποχρέωσης.
Το ακριβές ύψος της οικονομικής αντιστάθμισης καθορίζεται εκ των υστέρων κάθε χρόνο, ανάλογα με το πραγματικό κόστος και έσοδα που θα προκύψουν από την εκτέλεση της γραμμής, βάσει δικαιολογητικών και εντός του μέγιστου ορίου που θα αναφέρεται στην προσφορά και των όσων ορίζονται στην συγγραφή υποχρεώσεων.
Σε κάθε περίπτωση, ο αερομεταφορέας δεν μπορεί να ζητήσει οικονομική αντιστάθμιση υψηλότερη από το όριο που θα καθορίζεται στη σύμβαση, λαμβανομένου υπόψη ότι δεν πρόκειται για αντιπαροχή αλλά για αντιστάθμιση για την ανάληψη υποχρέωσης δημόσιας υπηρεσίας.
Οι ετήσιες πληρωμές καταβάλλονται υπό μορφή προκαταβολών και υπολοίπου εξόφλησης, με βάση τους όρους της συγγραφής υποχρεώσεων, με την επιφύλαξη ενδεχόμενων ελέγχων από την ENAC, με σκοπό να επαληθευθεί ο προορισμός της χορηγούμενης οικονομικής αντιστάθμισης και η τήρηση των όρων από τον δικαιούχο αερομεταφορέα. Η καταβολή του υπολοίπου θα πραγματοποιηθεί μετά από έλεγχο της αναλυτικής λογιστικής του αερομεταφορέα για τη συγκεκριμένη γραμμή και μετά από έλεγχο της τήρησης των όρων παροχής της επιβαλλόμενης δημόσιας υπηρεσίας.
7. Ναύλοι
Στις προσφορές που θα υποβληθούν πρέπει να αναφέρονται οι προβλεπόμενοι ναύλοι, σύμφωνα με όσα καθορίζονται στην ανακοίνωση για την επιβολή παροχής δημόσιας υπηρεσίας που δημοσιεύθηκε στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20ής Σεπτεμβρίου 2008.
8. Έναρξη της γραμμής
Η γραμμή θα αρχίσει εντός 15 (δέκα πέντε) ημερών από την ημερομηνία που θα καθορίζεται στη σύμβαση και θα βεβαιωθεί με δήλωση έναρξης της γραμμής, την οποία θα υπογράψουν ο ανάδοχος αερομεταφορέας και η ENAC.
9. Διάρκεια της σύμβασης
Η σύμβαση θα είναι διάρκειας δύο ετών από την ημερομηνία έναρξης των δρομολογίων στη συγκεκριμένη γραμμή.
Ο αερομεταφορέας δεσμεύεται να θέσει στη διάθεση της ENAC το προσωπικό, τα τεχνικά και λογιστικά έγγραφα, τον εξοπλισμό και ο,τιδήποτε άλλο χρειασθεί για τη διεκπεραίωση των εποπτικών δραστηριοτήτων και τον έλεγχο της ορθής τήρησης, εφαρμογής και εκτέλεσης των διατάξεων που περιέχει η ανακοίνωση της Επιτροπής, η προκήρυξη επιβολής των υποχρεώσεων, η παρούσα προκήρυξη, η σύμβαση και η συγγραφή υποχρεώσεων.
Η αθέτηση των υποχρεώσεων που προαναφέρθηκαν συνεπάγεται επιβολή κυρώσεων σύμφωνα με όσα προβλέπονται στο σημείο 11 της παρούσας προκήρυξης.
10. Καταγγελία της σύμβασης
Οποιοδήποτε συμβαλλόμενο μέρος μπορεί να καταγγείλει τη σύμβαση με προειδοποίηση 6 (έξι) μηνών χωρίς υποχρέωση οικονομικής αντιστάθμισης ή αποζημίωσης και ούτως ή άλλως το ενωρίτερο 12 (δώδεκα) μήνες από την έναρξη της γραμμής.
Η σύμβαση καταγγέλλεται χωρίς προειδοποίηση για μη εκπλήρωση της υποχρέωσης δημόσιας υπηρεσίας, εφόσον, μετά από προειδοποιητική επιστολή της ENAC προς τον ενδιαφερόμενο αερομεταφορέα ότι δεν έχει εκπληρώσει εξ ολοκλήρου τις υποχρεώσεις που ανέλαβε, ο αερομεταφορέας δεν αρχίσει την εκτέλεση των υποχρεώσεων δημόσιας υπηρεσίας εντός 30 (τριάντα) ημερών κατ' ανώτατο όριο από την ημερομηνία παραλαβής της επιστολής.
Σε περίπτωση καταγγελίας της σύμβασης από τον αερομεταφορέα, η ENAC έχει το δικαίωμα να προβεί σε έλεγχο, προκειμένου να προτείνει στο Υπουργείο υποδομών και μεταφορών τη σύναψη νέας σύμβασης με τον αμέσως επόμενο αερομεταφορέα από τον κατάλογο υποψηφίων. Οι όροι εκτέλεσης της γραμμής με βάση τις υποχρεώσεις παροχής δημόσιας υπηρεσίας και η οφειλόμενη κατ' αναλογία οικονομική αντιστάθμιση παραμένουν ίδιοι με εκείνους που ίσχυαν πριν την ανάθεση των υποχρεώσεων δημόσιας υπηρεσίας.
11. Αθέτηση της σύμβασης και κυρώσεις
Δεν αποτελεί παρατυπία καταλογιζόμενη στον αερομεταφορέα η μη εκτέλεση του δρομολογίου για τους κάτωθι λόγους:
|
— |
επικίνδυνες μετεωρολογικές συνθήκες, |
|
— |
κλείσιμο ενός των αεροδρομίων των αναφερόμενων στο επιχειρησιακό πρόγραμμα, |
|
— |
προβλήματα ασφαλείας, |
|
— |
απεργία, |
|
— |
περιπτώσεις ανωτάτης βίας. |
Η διακοπή του δρομολογίου για τους ανωτέρω λόγους συνεπάγεται μείωση του ύψους της οικονομικής αντιστάθμισης κατ' αναλογία των πτήσεων που δεν πραγματοποιήθηκαν.
Σε περίπτωση μη παροχής των υπηρεσιών και αθέτησης των υποχρεώσεων που περιέχει η σύμβαση, η ENAC έχει το δικαίωμα να επιβάλει κυρώσεις στον αερομεταφορέα, ανάλογες προς τον αριθμό των παραβιάσεων που διέπραξε, και σύμφωνα με τον τρόπο που περιγράφεται στο υπόδειγμα σύμβασης.
Σε κάθε περίπτωση, το ύψος των κυρώσεων δεν είναι δυνατόν να υπερβεί το 50 % του μέγιστου ύψους της οικονομικής αντιστάθμισης που προβλέπεται στον διαγωνισμό, όπως αναφέρεται στο σημείο 6, με την επιφύλαξη ότι, πέραν του ορίου αυτού, η ENAC έχει το δικαίωμα να καταγγείλει τη σύμβαση για λόγους αθέτησης της, με αποτέλεσμα την άμεση ανάκληση της οφειλόμενης οικονομικής αντιστάθμισης.
Ο αριθμός των πτήσεων που ματαιώνονται για λόγους απευθείας καταλογιζόμενους στον αερομεταφορέα δεν πρέπει να υπερβαίνει ετησίως το 2 % του αριθμού των προγραμματισμένων πτήσεων.
Άνω του ορίου αυτού, ο αερομεταφορέας οφείλει να καταθέσει στην ENAC, ως πρόστιμο, το ποσό των 3 000,00 EUR (τριών χιλιάδων ευρώ) για κάθε ματαιωθείσα πτήση που υπερβαίνει το ανωτέρω όριο του 2 %, κατόπιν επίσημης προειδοποίησης του αερομεταφορέα εντός δέκα ημερών από την ημερομηνία του συμβάντος. Ο αερομεταφορέας διαθέτει επτά ημέρες κατ' ανώτατο όριο για να υποβάλει τυχόν αντιρρήσεις του.
Η ENAC θα προβεί, άλλωστε, σε αναθεώρηση του ύψους της οικονομικής αντιστάθμισης ανάλογη των πτήσεων που δεν εκτελέστηκαν. Τα ποσά που θα εισπραχθούν όπως προαναφέρθηκε θα διατεθούν για τη χρηματοδότηση της συνέχειας των μεταφορικών συνδέσεων με την πόλη του Crotone.
Η μη τήρηση της προειδοποίησης που προαναφέρθηκε στο σημείο 10 συνεπάγεται την επιβολή προστίμου, το οποίο υπολογίζεται με βάση την ετήσια οικονομική αντιστάθμιση και το χρονικό διάστημα αθέτησης της προειδοποίησης από τη διακοπή του δρομολογίου, όπως προβλέπεται στο ίδιο σημείο 10, με την εφαρμογή του εξής τύπου:
P = CA/GG x gg
όπου:
|
P = |
= |
πρόστιμο |
|
CA = |
= |
ετήσια αντιστάθμιση |
|
GG = |
= |
ημέρες του υπό εξέταση έτους (365 ή 366) |
|
gg = |
= |
ημέρες αθέτησης προειδοποίησης |
Οι κυρώσεις που αναφέρονται στο παρόν σημείο είναι συσσωρεύσιμες με εκείνες που προβλέπονται αντίστοιχα από κοινοτικούς κανονισμούς και από εθνικές διατάξεις και κανονισμούς.
12. Εγγυήσεις για την προσφορά
Προκειμένου να βεβαιώσει τη σοβαρότητα και την αξιοπιστία της προσφοράς του, ο αερομεταφορέας που συμμετέχει στον παρόντα διαγωνισμό οφείλει να καταθέσει εγγύηση ύψους 2 % της μέγιστης οικονομικής αντιστάθμισης που αναφέρεται στο σημείο 6, υπό μορφή σύστασης εγγύησης ή τραπεζικής ή ασφαλιστικής εγγύησης, κατ' επιλογήν του υποβάλλοντος την προσφορά.
Ο τρόπος σύστασης της ανωτέρω εγγύησης θα καθορισθεί στη συγγραφή υποχρεώσεων και θα αναφέρεται ενδεχομένως στη σύμβαση.
Η ισχύς της εγγύησης είναι διάρκειας τουλάχιστον 180 (εκατόν ογδόντα) ημερών από την καταληκτική ημερομηνία υποβολής των προσφορών, με υποχρέωση από πλευράς του αερομεταφορέα να ανανεώσει την εγγύηση εφόσον, έως την καταληκτική ημερομηνία, δεν έχει ανατεθεί η σύμβαση, κατ' αίτηση της ENAC κατά τη διάρκεια της διαδικασίας αυτής.
Η ENAC προβλέπει, ταυτόχρονα με την κοινοποίησή της προς τους απορριφθέντες αερομεταφορείς σχετικά με την ανάθεση της σύμβασης, την αποδέσμευση της εγγύησής τους.
13. Εγγυήσεις εκτέλεσης και ασφαλιστική κάλυψη
Ο αερομεταφορέας, ο οποίος θα αναλάβει την εκτέλεση δρομολογίων σύμφωνα με τις παρούσες υποχρεώσεις παροχής δημόσιας υπηρεσίας, οφείλει να συστήσει τραπεζική ή ασφαλιστική εγγύηση ύψους 700 000,00 EUR (επτακοσίων χιλιάδων ευρώ) υπέρ της ENAC, η οποία διατηρεί το δικαίωμα να την χρησιμοποιήσει για να εξασφαλίσει τη συνέχεια της γραμμής.
Η άδεια παραλαβής δίδεται αυτόματα, χωρίς να χρειάζεται έγκριση από την ENAC, μετά από την τακτική εξέταση που αναφέρεται στην τελευταία παράγραφο του σημείου 6.
14. Λήξη και ανάκληση της οικονομικής αντιστάθμισης
Η ανά πάσα στιγμή απώλεια, μετά τη σύναψη της σύμβασης, των γενικών και τεχνικών δικαιολογητικών που αναφέρονται στο σημείο 2 της παρούσας προκήρυξης, καθώς και εκείνων που αναφέρονται στη συγγραφή υποχρεώσεων, συνεπάγεται τη λήξη της ανάθεσης εκτέλεσης του δρομολογίου, την ανάκληση της οικονομικής αντιστάθμισης και την επιστροφή τυχόν μη οφειλόμενων ποσών που εισπράχθηκαν, προσαυξημένων κατά τους νόμιμους φόρους.
Μετά τη λήξη της προθεσμίας ανάθεσης της γραμμής, το Υπουργείο υποδομών και μεταφορών μπορεί να επιτρέψει στην ENAC να συνάψει νέα σύμβαση, για την εναπομένουσα περίοδο εκτέλεσης της γραμμής με τον αμέσως επόμενο συναγωνιζόμενο αερομεταφορέα από τον τελικό κατάλογο επιλεγέντων υποψηφίων.
Τότε, η διάρκεια της σύμβασης αρχίζει από την ημερομηνία έναρξης εκτέλεσης της γραμμής και λήγει την προβλεπόμενη ημερομηνία λήξης της καταγγελθείσας σύμβασης, τηρουμένου του επιχειρηματικού σχεδίου που είχε εγκριθεί κατά την αξιολόγηση της προσφοράς που είχε υποβάλει ο πρώτος ανάδοχος.
15. Καταγγελία της σύμβασης
Σε περίπτωση αθέτησης από πλευράς του αερομεταφορέα των διατάξεων που προβλέπονται στην ανακοίνωση επιβολής των υποχρεώσεων που είχαν δημοσιευθεί στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης C 241 της 20ής Σεπτεμβρίου 2008, στο διάταγμα επιβολής των υποχρεώσεων, στη σύμβαση, στις διατάξεις της παρούσας προκήρυξης και στη συγγραφή υποχρεώσεων, η ENAC με γραπτή προειδοποίησή της μπορεί να χορηγήσει στον αερομεταφορέα, κατά την έννοια και κατ' εφαρμογή του άρθρου 1454 του αστικού κώδικα, προθεσμία 15 (δέκα πέντε) ημερών από την παραλαβή της προειδοποίησης αυτής να παύσει την αθέτηση των προαναφερθέντων όρων.
Μετά την πάροδο της προθεσμίας αυτής, η ENAC έχει τη δυνατότητα να θεωρήσει αυτοδικαίως ότι η σύμβαση έληξε και να παρακρατήσει οριστικά την εγγύηση που προαναφέρθηκε στο σημείο 13, καθώς και να απαιτήσει από τον αερομεταφορέα άμεση αποζημίωση.
Εξάλλου, σε περίπτωση παραβίασης των υποχρεώσεων και των παροχών που έχει αναλάβει ο αερομεταφορέας σύμφωνα με τη σύμβαση, τις διατάξεις της παρούσας προκήρυξης διαγωνισμού και την συγγραφή υποχρεώσεων, η ENAC, κατά την έννοια και κατ' εφαρμογή του άρθρου 1456 του αστικού κώδικα, έχει το δικαίωμα να καταγγείλει τη σύμβαση με γραπτή προειδοποίηση του αερομεταφορέα από πλευράς της.
Σε περίπτωση καταγγελίας της σύμβασης, το Υπουργείο υποδομών και μεταφορών μπορεί να επιτρέψει στην ENAC να προσφύγει στον κατάλογο επιτυχόντων για να συνάψει νέα σύμβαση, για την εναπομένουσα περίοδο εκτέλεσης της γραμμής, με τον αμέσως επόμενο συναγωνιζόμενο αερομεταφορέα του καταλόγου επιτυχόντων του διαγωνισμού με σκοπό την ανάθεση εκτέλεσης της γραμμής.
Τότε, η διάρκεια της σύμβασης αρχίζει από την ημερομηνία έναρξης εκτέλεσης της γραμμής και λήγει την προβλεπόμενη ημερομηνία λήξης της καταγγελθείσας σύμβασης, τηρουμένου του επιχειρηματικού σχεδίου που είχε εγκριθεί κατά την αξιολόγηση της προσφοράς που είχε υποβάλει ο πρώτος ανάδοχος.
16. Υποβολή των προσφορών
Εντός 30 (τριάντα) ημερών από τη δημοσίευση της παρούσας προκήρυξης στην Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης, οι προσφορές, οι οποίες πρέπει να είναι σύμφωνες με τη συγγραφή υποχρεώσεων, πρέπει να σταλούν, ειδάλλως θα απορριφθούν, με συστημένη επιστολή με απόδειξη παραλαβής, ή να επιδοθούν ιδιοχείρως έναντι απόδειξης παραλαβής στην εξής διεύθυνση: ENAC, Direzione generale, viale del Castro Pretorio 118, 00185 Roma.
Οι προσφορές πρέπει να υποβληθούν εσώκλειστες σε τρεις σφραγισμένους φακέλους, ειδάλλως θα απορριφθούν.
Ο εξωτερικός φάκελος, κλειστός, σφραγισμένος και μονογραφημένος και στα δύο άκρα, ο οποίος θα περιέχει δύο άλλους φακέλους, επίσης σφραγισμένους και μονογραφημένους στα άκρα, θα φέρει την εξής μνεία: «Offerta per la gara in oneri di servizio pubblico sulla rotta Crotone-Roma Fiumicino e viceversa».
Τα έγγραφα που πρέπει να περιέχουν οι τρεις φάκελοι που προαναφέρθηκαν καθορίζονται στη συγγραφή υποχρεώσεων που αναφέρεται στο σημείο 4 της παρούσας προκήρυξης διαγωνισμού.
Εννοείται ότι η παραλαβή των φακέλων είναι στην αποκλειστική ευθύνη του αποστολέα εάν, για οποιοδήποτε λόγο, δεν φθάσουν μέσα στις προκαθορισμένες προθεσμίες στον προορισμό τους.
Ακόμη και εάν έχει υποβληθεί μία μόνον έγκυρη προσφορά, η σύμβαση είναι δυνατόν να ανατεθεί.
17. Διάρκεια ισχύος των προσφορών
180 (εκατόν ογδόντα) ημέρες από τη λήξη της προθεσμίας υποβολής των προσφορών.
18. Ανάθεση της σύμβασης
Η ENAC θα φέρει σε πέρας τον διαγωνισμό μέσω επιτροπής που θα συσταθεί επί τούτου και θα απαρτίζεται από έναν διευθύνοντα της ENAC που θα ορίσει ο Γενικός Διευθυντής, από έναν εμπειρογνώμονα σε θέματα αερομεταφορών που θα ορίσει η Περιφέρεια της Καλαβρίας και από έναν πρόεδρο που θα ορισθεί με τη συναίνεση της ENAC και της Περιφέρειας της Καλαβρίας· τα χρέη γραμματείας θα αναλάβει υπάλληλος της ENAC.
19. Επεξεργασία προσωπικών δεδομένων
Η χρήση και η επεξεργασία όλων των προσωπικών δεδομένων θα γίνει μόνον για θεσμικούς σκοπούς και θα εξασφαλισθεί η προστασία και η εμπιστευτικότητά τους σύμφωνα με την ισχύουσα νομοθεσία. Προς το σκοπό αυτό, ο ανάδοχος αερομεταφορέας πρέπει να υπογράψει τη σχετική άδεια επεξεργασίας των προσωπικών δεδομένων, σύμφωνα με όσα ορίζει το νομοθετικό διάταγμα αριθ. 196/2003 και οι μετέπειτα τροποποιήσεις και προσθήκες του.
20. Επεξεργασία ευαίσθητων δεδομένων
Η επεξεργασία των ευαίσθητων δεδομένων που θα περιέχουν οι προσφορές που θα υποβληθούν από τους αερομεταφορείς θα γίνει σύμφωνα με όσα προβλέπει ο «Regolamento per il trattamento dei dati sensibili e giudiziari», τον οποίον ενέκρινε το Διοικητικό Συμβούλιο της ENAC στη συνεδρίασή του της 2ας Μαρτίου 2006 και διατίθεται στο δικτυακό τόπο της ENAC «enac-italia.it».
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/94 |
ΠΡΌΣΚΛΗΣΗ ΥΠΟΒΟΛΉΣ ΠΡΟΤΆΣΕΩΝ — EACEA/29/08
Ευρωπαϊκές ενώσεις που δραστηριοποιούνται στον τομέα της εκπαίδευσης και κατάρτισης σε ευρωπαϊκό επίπεδο
(2008/C 276/10)
1. Στόχοι και περιγραφή
Σκοπός της παρούσας πρόσκλησης υποβολής προτάσεων είναι η υποστήριξη των δραστηριοτήτων ευρωπαϊκών ενώσεων που δραστηριοποιούνται στον τομέα της εκπαίδευσης και της κατάρτισης ή των οποίων ο στόχος εντάσσεται σε πολιτική της Ευρωπαϊκής Ένωσης.
Το πρόγραμμα δράσης στον τομέα της διά βίου μάθησης (το «πρόγραμμα διά βίου μάθησης») (1) και, πιο συγκεκριμένα, το «υποπρόγραμμα Jean Monnet», αποτελεί τη νομική βάση.
Για την υλοποίηση της κύριας δράσης 3 του προγράμματος Jean Monnet, οι στόχοι της παρούσας πρόσκλησης υποβολής προτάσεων είναι οι εξής:
|
— |
η υποστήριξη της ύπαρξης ευρωπαϊκών ενώσεων υψηλού επιπέδου που δραστηριοποιούνται στον τομέα της εκπαίδευσης και της κατάρτισης, |
|
— |
η υποστήριξη των ευρωπαϊκών ενώσεων που συμβάλλουν στην υλοποίηση του προγράμματος εργασίας «Εκπαίδευση και κατάρτιση 2010» (2), |
|
— |
η υποστήριξη των ευρωπαϊκών ενώσεων που συμβάλλουν στην αύξηση της γνώσης και της ευαισθητοποίησης για τη διαδικασία της ευρωπαϊκής ολοκλήρωσης μέσω της εκπαίδευσης και της κατάρτισης. |
Η κοινοτική χρηματοδότηση στο πλαίσιο της παρούσας πρόσκλησης υποβολής προτάσεων λαμβάνει τη μορφή ετήσιων λειτουργικών επιδοτήσεων για το 2009 για την κάλυψη ορισμένων λειτουργικών και διοικητικών δαπανών των επιλεγμένων ευρωπαϊκών ενώσεων.
Ο Εκτελεστικός Οργανισμός Εκπαίδευσης, Οπτικοακουστικών Θεμάτων και Πολιτισμού («ο Οργανισμός»), ο οποίος ενεργεί στο πλαίσιο των αρμοδιοτήτων που του έχουν ανατεθεί από την Ευρωπαϊκή Επιτροπή («η Επιτροπή») είναι αρμόδιος για τη διαχείριση της παρούσας πρόσκλησης υποβολής προτάσεων.
2. Επιλέξιμοι υποψήφιοι
Μια ευρωπαϊκή ένωση είναι επιλέξιμη εάν πληροί τις ακόλουθες προϋποθέσεις:
|
— |
είναι μη κερδοσκοπικός οργανισμός, |
|
— |
βρίσκεται και έχει νομική προσωπικότητα και έδρα για διάστημα μεγαλύτερο των δύο ετών (στις 23 Δεκεμβρίου 2008) σε μία από τις επιλέξιμες χώρες (τα 27 κράτη μέλη της Ευρωπαϊκής Ένωσης, την Ισλανδία, το Λιχτενστάιν, τη Νορβηγία και την Τουρκία), |
|
— |
διεξάγει την πλειονότητα των δραστηριοτήτων του στα κράτη μέλη της Ευρωπαϊκής Ένωσης, σε χώρες που ανήκουν στον Ευρωπαϊκό Οικονομικό Χώρο ή/και στις υποψήφιες για ένταξη χώρες, |
|
— |
υφίσταται ως φορέας που επιδιώκει έναν σκοπό γενικού ευρωπαϊκού ενδιαφέροντος, όπως ορίζεται στο άρθρο 162 των κανόνων εφαρμογής του Δημοσιονομικού Κανονισμού που θεσπίστηκε από τον κανονισμό (ΕΚ, Ευρατόμ) αριθ. 2342/2002 της Επιτροπής (3), ο οποίος τροποποιήθηκε πρόσφατα με τον κανονισμό (ΕΚ) αριθ. 478/2007, |
|
— |
δραστηριοποιείται στον τομέα της εκπαίδευσης και της κατάρτισης σε ευρωπαϊκό επίπεδο και επιδιώκει σαφείς και καθορισμένους στόχους που ορίζονται στα άρθρα του επίσημου καταστατικού ιδρύσεώς του, |
|
— |
διεξάγει δραστηριότητες που είναι συμβατές με τις προτεραιότητες του προγράμματος εργασίας «Εκπαίδευση και κατάρτιση 2010» ή/και συμβάλλει στην αύξηση της γνώσης και της ευαισθητοποίησης για τη διαδικασία της ευρωπαϊκής ολοκλήρωσης μέσω της εκπαίδευσης και της κατάρτισης, |
|
— |
περιλαμβάνει ενώσεις-μέλη που έχουν την έδρα τους σε τουλάχιστον 12 διαφορετικά κράτη μέλη της Ευρωπαϊκής Ένωσης (4). Οι εν λόγω ενώσεις-μέλη πρέπει να έχουν καθεστώς «πλήρους μέλους» (συνδεδεμένα μέλη και παρατηρητές δεν προσμετρώνται ως «πλήρη μέλη») σε διεθνικό, εθνικό, περιφερειακό ή τοπικό επίπεδο. |
Σημείωση: Τα φυσικά πρόσωπα, οι μεμονωμένοι ανάδοχοι, τα μεμονωμένα ανώτατα εκπαιδευτικά ιδρύματα ή οι δημόσιες αρχές και ιδρύματα που αποτελούν τμήμα της διοικητικής δομής των κρατών μελών δεν θεωρούνται «ενώσεις».
3. Κριτήρια ανάθεσης
Οι επιλέξιμες αιτήσεις θα αξιολογούνται με βάση την ποιότητα ενός λεπτομερούς 12 μηνου προγράμματος εργασίας για το 2009 και θα εφαρμόζονται τα εξής κριτήρια ανάθεσης:
|
— |
η συνάφεια, η σαφήνεια και η συνεκτικότητα των βραχυπρόθεσμων στόχων (12 μηνών), |
|
— |
η ποιότητα της διαχείρισης του προγράμματος εργασίας (σαφήνεια και συνεκτικότητα των δράσεων και του προϋπολογισμού που προτείνεται για την επίτευξη των στόχων, χρονοδιάγραμμα), |
|
— |
ο πιθανός αντίκτυπος των δράσεων στην εκπαίδευση ή/και κατάρτιση σε ευρωπαϊκό επίπεδο (ιδιαίτερα ο βαθμός στον οποίο οι αιτούσες ευρωπαϊκές ενώσεις συμβάλλουν στην υλοποίηση του προγράμματος εργασίας «Εκπαίδευση και κατάρτιση 2010» ή/και στην αύξηση της γνώσης και της ευαισθητοποίησης για τη διαδικασία της ευρωπαϊκής ολοκλήρωσης. |
Μια λεπτομερέστερη περιγραφή των πληροφοριών που πρέπει να παρασχεθούν από τον αιτούντα για κάθε κριτήριο ανάθεσης διατίθενται στον δικτυακό τόπο: http://eacea.ec.europa.eu/index.htm, και χρήζει προσεκτικής ανάγνωσης.
4. Προϋπολογισμός και διάρκεια του προγράμματος
Ο συνολικός ενδεικτικός κοινοτικός προϋπολογισμός για τη συγχρηματοδότηση των ευρωπαϊκών ενώσεων στο πλαίσιο της παρούσας πρόσκλησης ανέρχεται σε 600 000 EUR.
Η μέγιστη λειτουργική επιδότηση ανά ένωση για ένα ετήσιο πρόγραμμα εργασιών 12 μηνών (που αντιστοιχεί σε ένα δημοσιονομικό έτος) δεν θα υπερβαίνει το ποσό των 100 000 EUR.
Οι υποψήφιες ενώσεις μπορούν να επιλέξουν μεταξύ δύο συστημάτων συγχρηματοδότησης:
|
α) |
χρηματοδότηση βάσει προϋπολογισμού: η συνήθης χρηματοδότηση των επιλέξιμων δαπανών για τις οποίες η κοινοτική οικονομική ενίσχυση δεν μπορεί να υπερβαίνει το 75 % των συνολικών επιλέξιμων δαπανών που ορίζονται στον προϋπολογισμό για το πρόγραμμα εργασίας της ένωσης· |
|
β) |
χρηματοδότηση κατ' αποκοπή: χρηματοδότηση κατ' αποκοπή για την οποία η κοινοτική οικονομική ενίσχυση δεν μπορεί να υπερβαίνει το 75 % της συνοπτικής προσωρινής κατάστασης εσόδων — εξόδων για το σχετικό έτος. |
Η περίοδος επιλεξιμότητας των δαπανών για ένα πρόγραμμα εργασιών διάρκειας έως και 12 μηνών θα ξεκινά μεταξύ 1ης Ιανουαρίου 2009 και 1ης Απριλίου 2009 και δεν μπορεί να παρατείνεται πέραν του τέλους του δημοσιονομικού έτους του δικαιούχου.
5. Προθεσμία και υποβολή προτάσεων
Η προθεσμία για την υποβολή αιτήσεων είναι η 23η Δεκεμβρίου 2008 (ημερομηνία σφραγίδας ταχυδρομείου) και οι αιτήσεις πρέπει να αποστέλλονται στην ακόλουθη διεύθυνση:
|
Εκτελεστικός Οργανισμός Εκπαίδευσης, Οπτικοακουστικών Θεμάτων και Πολιτισμού |
|
Διά βίου μάθηση: Erasmus, Jean Monnet |
|
Πρόσκληση υποβολής προτάσεων — EACEA/29/08 |
|
κ. Ralf RAHDERS |
|
Γραφείο: BOUR 2/61 |
|
Avenue du Bourget 1 |
|
B-1140 Brussels |
Δεκτές γίνονται μόνο οι αιτήσεις που υποβάλλονται στο επίσημο έντυπο αίτησης, δεόντως υπογεγραμμένες από το άτομο που δικαιούται να συνάπτει νομικά δεσμευτικές υποχρεώσεις εκ μέρους του αιτούντος οργανισμού και οι οποίες περιλαμβάνουν όλα τα στοιχεία και τα παραρτήματα που ορίζονται στις οδηγίες για τους αιτούντες. Αιτήσεις που αποστέλλονται μέσω τηλεομοιοτυπίας ή ηλεκτρονικού ταχυδρομείου θα απορρίπτονται.
6. Επιπρόσθετες πληροφορίες
Οι οδηγίες για τους αιτούντες και το έντυπο αίτησης διατίθενται στον δικτυακό τόπο του οργανισμού: http://eacea.ec.europa.eu.
Περαιτέρω πληροφορίες διατίθενται από:
|
Εκτελεστικός οργανισμός εκπαίδευσης, οπτικοακουστικών θεμάτων και πολιτισμού |
|
Κυρία Ilona POKORNA |
|
E-mail: Ilona.Pokorna@ec.europa.eu |
|
Τηλέφωνο (απευθείας γραμμή): (32-2) 295 83 94 |
(1) Βλέπε απόφαση αριθ. 1720/2006/EΚ του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου, της 15ης Νοεμβρίου 2006, για τη θέσπιση προγράμματος δράσης στον τομέα της διά βίου μάθησης.
http://eur-lex.europa.eu/LexUriServ/site/en/oj/2006/c_327/c_32420061230en00590067.pdf
(2) Βλέπε: http://ec.europa.eu/education/policies/2010/et_2010_en.html
(3) Σύμφωνα με τον εν λόγω ορισμό, οργανισμός που επιδιώκει σκοπό γενικού ευρωπαϊκού ενδιαφέροντος είναι:
|
— |
είτε ένας ευρωπαϊκός οργανισμός με αποστολή την εκπαίδευση, την κατάρτιση, την ενημέρωση ή την έρευνα και τη μελέτη των ευρωπαϊκών πολιτικών, καθώς και ένας ευρωπαϊκός οργανισμός τυποποίησης, |
|
— |
είτε ένα ευρωπαϊκό δίκτυο που εκπροσωπεί οργανισμούς μη κερδοσκοπικού χαρακτήρα που δραστηριοποιούνται στα κράτη μέλη ή σε υποψήφιες για ένταξη χώρες και προωθούν αρχές και πολιτικές σύμφωνες με τους στόχους των συνθηκών. |
(4) Επιπλέον, η ευρωπαϊκή ένωση μπορεί να περιλαμβάνει ενώσεις-μέλη που έχουν την έδρα τους σε άλλες χώρες που συμμετέχουν στο πρόγραμμα διά βίου μάθησης (εκτός των κρατών μελών της Ευρωπαϊκής Ένωσης).
ΔΙΑΔΙΚΑΣΙΕΣ ΠΟΥ ΑΦΟΡΟΥΝ ΤΗΝ ΕΦΑΡΜΟΓΗ ΤΗΣ ΠΟΛΙΤΙΚΗΣ ΑΝΤΑΓΩΝΙΣΜΟΥ
Επιτροπή
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/97 |
Προηγούμενη γνωστοποίηση συγκέντρωσης
(Υπόθεση COMP/M.5368 — MidAmerican/Constellation)
Υπόθεση υποψήφια για απλοποιημένη διαδικασία
(Κείμενο που παρουσιάζει ενδιαφέρον για τον ΕΟΧ)
(2008/C 276/11)
|
1. |
Στις 23 Οκτωβρίου 2008, η Επιτροπή έλαβε γνωστοποίηση μιας σχεδιαζόμενης συγκέντρωσης σύμφωνα με το άρθρο 4 του κανονισμού (EK) αριθ. 139/2004 του Συμβουλίου (1) με την οποία η επιχείρηση MidAmerican Energy Holdings Company («MidAmerican», Ηνωμένες Πολιτείες της Αμερικής), που ελέγχεται από την επιχείρηση Berkshire Hathaway, αποκτά με την έννοια του άρθρου 3 παράγραφος 1 στοιχείο β) του κανονισμού του Συμβουλίου έλεγχο επί της επιχείρησης Constellation Energy group Inc. («Constellation», Ηνωμένες Πολιτείες της Αμερικής) με αγορά μετοχών. |
|
2. |
Οι επιχειρηματικές δραστηριότητες των εν λόγω επιχειρήσεων είναι:
|
|
3. |
Κατόπιν προκαταρκτικής εξέτασης, η Επιτροπή διαπιστώνει ότι η γνωστοποιηθείσα πράξη θα μπορούσε να εμπίπτει στο πεδίο εφαρμογής του κανονισμού (EK) αριθ. 139/2004. Εντούτοις, επιφυλάσσεται να λάβει τελική απόφαση επί του σημείου αυτού. Σύμφωνα με την ανακοίνωση της Επιτροπής σχετικά με μια απλοποιημένη διαδικασία αντιμετώπισης ορισμένων συγκεντρώσεων βάσει του κανονισμού (ΕΚ) αριθ. 139/2004 του Συμβουλίου (2) σημειώνεται ότι η παρούσα υπόθεση είναι υποψήφια για να αντιμετωπιστεί βάσει της διαδικασίας που προβλέπεται στην ανακοίνωση. |
|
4. |
Η Επιτροπή καλεί τους ενδιαφερόμενους τρίτους να υποβάλουν στην Επιτροπή ενδεχόμενες παρατηρήσεις για τη σχεδιαζόμενη συγκέντρωση. Οι παρατηρήσεις πρέπει να φθάσουν στην Επιτροπή το αργότερο εντός δέκα ημερών από την ημερομηνία της παρούσας δημοσίευσης, με την ένδειξη COMP/M.5368 — MidAmerican/Constellation. Οι παρατηρήσεις μπορούν να σταλούν στην Eπιτροπή με φαξ [αριθμός (32-2) 296 43 01 ή 296 72 44] ή ταχυδρομικά στην ακόλουθη διεύθυνση:
|
(1) ΕΕ L 24 της 29.1.2004, σ. 1.
(2) ΕΕ C 56 της 5.3.2005, σ. 32.
|
31.10.2008 |
EL |
Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης |
C 276/s3 |
ΣΗΜΕΊΩΣΗ ΓΙΑ ΤΟΝ ΑΝΑΓΝΏΣΤΗ
Τα θεσμικά όργανα αποφάσισαν να μην εμφανίζουν πλέον στα κείμενά τους τη μνεία της τελευταίας τροποποίησης των πράξεων στις οποίες παραπέμπουν.
Εάν δεν υπάρχει μνεία περί του αντιθέτου, οι πράξεις στις οποίες γίνεται παραπομπή στα κείμενα που δημοσιεύονται στο παρόν τεύχος νοούνται στην εκάστοτε ισχύουσα μορφή τους.