1992L0065 — DA — 03.07.2004 — 007.002
Dette dokument er et dokumentationsredskab, og institutionerne påtager sig intet ansvar herfor
Ændret ved:
Ændret ved:
|
A1
|
Tiltrædelsesakt for Østrig, Finland og Sverige
|
C 241
|
21
|
29.8.1994
|
|
|
(tilpasset ved Rådets beslutning 95/1EF, Euratom, EKSF)
|
L 001
|
1
|
..
|
|
►A2
|
Akt vedrørende vilkårene for Den Tjekkiske Republiks, Republikken Estlands, Republikken Cyperns, Republikken Letlands, Republikken Litauens, Republikken Ungarns, Republikken Maltas, Republikken Polens, Republikken Sloveniens og Den Slovakiske Republiks tiltrædelse og tilpasningerne af de traktater, der danner grundlag for Den Europæiske Union
|
L 236
|
33
|
23.9.2003
|
Berigtiget ved:
▼B
RÅDETS DIREKTIV 92/65/EØF
af 13. juli 1992
om dyresundhedsmæssige betingelser for samhandel med og indførsel til Fællesskabet af dyr samt sæd, æg og embryoner, der for så vidt angår disse betingelser ikke er underlagt specifikke fællesskabsbetingelser som omhandlet i bilag A, del I, til direktiv 90/425/EØF
RÅDET FOR DE EUROPÆISKE FÆLLESSKABER HAR —
under henvisning til Traktaten om Oprettelse af Det Europæiske Økonomiske Fællesskab, særlig artikel 43,
under henvisning til forslag fra Kommissionen (
1
),
under henvisning til udtalelse fra Europa-Parlamentet (
2
),
under henvisning til udtalelse fra Det Økonomiske og Sociale Udvalg (
3
), og
ud fra følgende betragtninger:
Levende dyr og produkter af animalsk oprindelse er opført på listen over produkter i Traktatens bilag II; afsætningen af dyr og produkter af animalsk oprindelse er en indkomstkilde for en del af landbrugsbefolknignen;
for at sikre en rationel udvikling af denne sektor og øge produktiviteten bør der fastsættes dyresundhedsmæssige betingelser for dyr og produkter af animalsk oprindelse gældende for hele Fællesskabet;
Fællesskabet bør vedtage foranstaltninger med henblik på gradvis oprettelse af det indre marked i løbet af perioden indtil den 31. december 1992;
for at nå de ovennævnte mål har Rådet fastsat dyresundhedsmæssige bestemmelser for kvæg, svin, får og geder, enhovede dyr, fjerkræ og rugeæg, fisk og fiskerivarer, toskallede bløddyr, tyresæd og ornesæd, kvægembryoner, fersk kød, fjerkrækød, kødprodukter, vildtkød og kaninkød;
der bør vedtages dyresundhedsmæssige bestemmelser for afsætning af dyr og produkter af animalsk oprindelse, som endnu ikke er omfattet af ovennævnte bestemmelser;
det bør fastsættes, at dette direktiv finder anvendelse, uden at det begrænser anvendelsen af Rådets forordning (EØF) nr. 3626/82 af 3. december 1982 om gennemførelse i Fællesskabet af konventionen om international handel med udryddelsestruede vilde dyr og planter (
4
);
for så vidt angår visse tekniske aspekter, bør der henvises til Rådets direktiv 64/432/EØF af 26. juni 1964 om veterinærpolitimæssige problemer ved handel inden for Fællesskabet med kvæg og svin (
5
) og Rådets direktiv 85/511/EØF af 18. november 1985 om fællesskabsforanstaltninger til bekæmpelse af mund- og klovesyge (
6
);
med hensyn til gennemførelse og opfølgning af kontrollen og de beskyttelsesforanstaltninger, der skal iværksættes, bør der henvises til de almindelige bestemmelser i Rådets direktiv 90/425/EØF af 26. juni 1990 om veterinærkontrol og zooteknisk kontrol i samhandelen med visse levende dyr og produkter inden for Fællesskabet med henblik på gennemførelse af det indre marked (
7
);
medmindre andet bestemmes, bør samhandelen med dyr og produkter af animalsk oprindelse liberaliseres, uden at dette berører muligheden for eventuelt at indføre beskyttelsesforanstaltninger;
som følge af den betydelige risiko for spredning af sygdomme, som de pågældende dyr udsættes for, bør der for visse dyr og produkter af animalsk oprindelse opstilles særlige krav i forbindelse med afsætningen heraf, navnlig når dyrene eller produkterne sælges til områder, der har en høj dyresundhedsmæssig status;
den særlige situation, der kendetegner Det Forenede Kongerige Storbritannien og Nordirland og Irland, som, fordi de er øer, i meget lang tid har væres rabiesfrie, gør det berettiget at indføre særlige bestemmelser, som skal sikre, at afsætning i Det Forenede Kongerige og Irland af hunde og katte, som ikke stammer fra de pågældende to lande, ikke medfører en risiko for, at der bringes rabies ind i de to lande, uden at ophævelsen af veterinærkontrollen ved medlemsstaternes grænser berøres;
et sundhedscertifikat er den mest hensigtsmæssige måde til at sikre og kontrollere, at disse krav overholdes;
for at den sundhedsmæssige situation i Fællesskabet kan opretholdes, bør de dyr og produkter af animalsk oprindelse, der er omfattet af dette direktiv, når de afsættes, være underlagt minimumskravene i forbindelse med handel, og det bør kontrolleres, at kravene overholdes i overensstemmelse med principperne og reglerne i Rådets direktiv 90/675/EØF af 10. december 1990 om fastsættelse af principperne for tilrettelæggelse af veterinærkontrollen for tredjelandsprodukter, der føres ind i Fællesskabet (
8
);
der bør fastsættes en procedure for tilrettelæggelse af et snævert samarbejde mellem medlemsstaterne og Kommissionen i Den Stående Veterinærkomité;
den frist for gennemførelse af direktivet, som i artikel 29 er fastsat til den 1. januar 1994, berører ikke afskaffelsen af veterinærkontrollen ved grænserne pr. 1. januar 1993 —
UDSTEDT FØLGENDE DIREKTIV:
KAPITEL I
Generelle bestemmelser
Artikel 1
▼M7
I dette direktiv fastsættes de dyresundhedsmæssige betingelser, der skal gælde for samhandel med og indførsel til Fællesskabet af dyr samt sæd, æg og embryoner, der med hensyn til dyresundhedsmæssige betingelser ikke er underlagt specifikke fællesskabsbestemmelser som omhandlet i bilag F.
▼B
Anvendelsen af dette direktiv begrænser ikke anvendelsen af de bestemmelser, der er fastsat i henhold til forordning (EØF) nr. 3626/82.
Dette direktiv berører ikke de nationale bestemmelser vedrørende selskabsdyr, men opretholdelsen af disse bestemmelser berører på den anden side ikke afskaffelsen af veterinærkontrollen ved grænserne mellem medlemsstaterne.
Artikel 2
1. I dette direktiv forstås ved:
|
a)
|
samhandel : samhandel som defineret i artikel 2, stk. 3, i direktiv 90/425/EØF
|
|
b)
|
dyr : eksemplarer af andre arter end dem, der er nævnt i direktiv 64/432/EØF, 90/426/EØF (
9
), 90/539/EØF (
10
), 91/67/EØF (
11
), 91/68/EØF (
12
), 91/492/EØF (
13
) og 91/493/EØF (
14
)
|
|
c)
|
organ, institut eller center, der er officielt godkendt : et permanent, geografisk afgrænset anlæg, som er godkendt i overensstemmelse med artikel 13, hvor en eller flere dyrearter sædvanligvis holdes eller opdrættes med kommercielt eller andet sigte og udelukkende med et eller flere af følgende mål for øje:
— udstilling af nævnte dyr og oplysning af offentligheden
— videnskabelig grundforskning eller anvendt forskning eller opdræt af dyr til sådanne forskningsformål
|
|
d)
|
anmeldelsespligtige sygdomme : de sygdomme, der er opført i bilag A.
|
2. Desuden finder definitionerne, bortset fra definitionen på godkendte centre og organer, i artikel 2 i direktiv 64/432/EØF, 91/67/EØF og 90/539/EØF tilsvarende anvendelse.
KAPITEL II
Bestemmelser om samhandel
Artikel 3
Medlemsstaterne sørger for, at samhandel med de i artikel 1, stk. 1, omhandlede dyr ikke forbydes eller begrænses af andre dyresundhedsmæssige årsager end dem, der følger af anvendelsen af dette direktiv eller andre fællesskabsforskrifter, særlig eventuelle beskyttelsesforanstaltninger.
▼
Indtil der foreligger fællesskabsbestemmelser på området, kan Sverige opretholde sine nationale regler om slanger og krybdyr.
▼B
Artikel 4
Medlemsstaterne træffer de nødvendige foranstaltninger til, at dyr, der er omhandlet i artikel 5 til 10 i dette direktiv, i overensstemmelse med artikel 4, stk. 1, litra a), i direktiv 90/425/EØF kun kan gøres til genstand for samhandel, når de opfylder betingelserne i artikel 5 til 10 og kommer fra bedrifter eller handlende, der er omhandlet i artikel 12, stk. 1 og 3, og som den kompetente myndighed har ladet registrere, og som med henblik herpå forpligter sig til følgende, jf. dog artikel 13 og de særlige bestemmelser, der skal vedtages i medfør af artikel 24:
— regelmæssigt at lade dyrene undersøge i overensstemmelse med artikel 3, stk. 3, i direktiv 90/425/EØF
— over for den kompetente myndighed — ud over udbrud af anmeldelsespligitge sygdomme — at anmelde udbrud af sygdomme, der er nævnt i bilag B, for hvilke den pågældende medlemsstat har indført et sygdomsbekæmpelses- eller overvågningsprogram
— at overholde de nationale særforanstaltninger for bekæmpelse af en sygdom, som har særlig betydning for en given medlemsstat, og for hvilken der findes et program i overensstemmelse med artikel 14 eller en afgørelse i overensstemmelse med artikel 15, stk. 2
— kun at bringe dyr på markedet med henblik på samhandel, når disse ikke frembyder noget tegn på sygdom og kommer fra bedrifter eller distrikter, der ikke er underkastet noget forbud af dyresundhedsmæssige hensyn og for såvidt angår dyr, som ikke ledsages af et sundhedscertifikat eller et handelsdokument som omhandlet i artikel 5 til 11, kun at bringe dyr på markedet, som ledsages af en erklæring fra lederen af bedriften om, at de pågældende dyr ved afsendelsen ikke frembyder noget tegn på sygdom, og at bedriften ikke er underkastet dyresundhedsmæssige restriktioner
— at overholde kravene til sikring af dyrenes velfærd.
Artikel 5
1. Medlemsstaterne sørger for, at samhandel med aber (simiae og prosimiae) kun sker fra og til organer, institutter eller centre, som er officielt godkendt af medlemsstatens kompetente myndigheder i overensstemmelse med artikel 13, og at de ledsages af et sundhedscertificat i overensstemmelse med modellen i bilag E, som er udfyldt af embedsdyrlægen ved oprindelsesorganet, -instituttet eller -centret, med henblik på at garantere for dyrenes sundhedstilstand.
2. Den kompetente myndighed i en medlemsstat kan som undtagelse fra kravene i stk. 1 tillade salg til godkendte organer, institutter og centre for aber, der ejes af en privatperson.
Artikel 6
A. Uden at kravene i artikel 14 og 15 berøres deraf, sørger medlemsstaterne for, at klovdyr af andre arter end dem, der er omhandlet i direktiv 64/432/EØF, 90/426/EØF og 91/68/EØF, kun kan gøres til genstand for samhandel, hvis de opfylder følgende krav:
1) Generelt:
a) de skal være identificeret i overensstemmelse med artikel 3, stk. 1, litra c), i direktiv 90/425/EØF
b) de må ikke skulle fjernes som led i et program for udryddelse af en smitsom sygdom
c) de må ikke være vaccineret mod mund- og klovesyge, og de skal opfylde de relevante krav i direktiv 85/511/EØF og i artikel 4a i direktiv 64/432/EØF
d) de skal stamme fra en bedrift som omhandlet i artikel 3, stk. 2, litra b) og c), i direktiv 64/432/EØF, der ikke har været underkastet dyresundhedsmæssige foranstaltninger, navnlig foranstaltninger vedtaget i medfør af direktiv 85/511/EØF, 80/217/EØF (
15
) og 91/68/EØF, og på hvilken de skal have opholdt sig til stadighed siden fødslen eller de sidste 30 dage inden afsendelsen
▼M7
e) de skal være ledsaget af et certifikat efter modellen i bilag E, del 1, som indeholder følgende erklæring:

▼M7 —————
▼B
2) For så vidt angår vilde drøvtyggere:
a) de skal stamme fra en bestand, der er officielt fri for tuberkulose eller officielt fri for eller fri for brucellose i overensstemmelse med direktiv 64/432/EØF eller direktiv 91/68/EØF, og for så vidt angår de dyresundhedsmæssige betingelser opfylde de relevante krav for kvæg i artikel 3, stk. 2, litra c), d), f), g) og h), i direktiv 64/432/EØF eller i artikel 3 i direktiv 91/68/EØF
▼M7
b) hvis de ikke kommer fra en bestand, der opfylder betingelserne i litra a), skal de komme fra en bedrift, hvor der ikke er konstateret tilfælde af brucellose eller tuberkulose i de seneste 42 dage inden indladningen, og hvor dyrene i løbet af de 30 dage, der går forud for afsendelsen, med negativt resultat har været underkastet en prøve for brucellose og tuberkulose
▼
c) der kan vedtages bestemmelser om leukose i henhold til fremgangsmåden i artikel 26.
▼B
3) For så vidt angår dyr af svinefamilien:
a) de må ikke komme fra et distrikt, som er underkastet forbudsforanstaltninger i forbindelse med forekomst af afrikansk svinepest i medfør af artikel 9a i direktiv 64/432/EØF
b) de skal komme fra en bedrift, der ikke er omfattet af restriktioner i medfør af direktiv 80/217/EØF på grund af klassisk svinepest
c) de skal komme fra en bestand, der er fri for brucellose i henhold til kravene i direktiv 64/432/EØF, og opfylde de relevante dyresundhedskrav for svin i direktiv 64/432/EØF
d) hvis de ikke kommer fra en bestand, der opfylder betingelserne i litra c), skal de i løbet af de 30 dage, der går forud for afsendelsen, med negativt resultat have været underkastet en prøve, der skal vise, at de ikke har antistoffer mod brucellose.
▼M7 —————
▼M7
4) Kravene til prøver omhandlet i denne artikel og prøvekriterierne kan fastsættes efter proceduren i artikel 26. Disse afgørelser skal tage hensyn til drøvtyggere, som opdrættes i Fællesskabets arktiske regioner.
De nationale bestemmelser finder fortsat anvendelse, indtil de i første afsnit omhandlede afgørelser er truffet.
▼B
B. Direktiv 64/432/EØF ændres således:
1) I artikel 2, litra b) og c), indføjes efter »kvæg«: »(herunder også af arterne Bubalus bubalus)«.
2) Følgende artikel indsættes:
»Artikel 10a
Sundhedscertifikaterne, hvortil modellen er gengivet i bilag F, kan efter fremgangsmåden i artikel 12 ændres eller suppleres bl.a. med henblik på at tage hensyn til kravene i artikel 6 i direktiv 92/65/EØF.«
Artikel 7
A. Medlemsstaterne sørger for, at andre fugle end dem, der er omhandlet i direktiv 90/539/EØF, kun kan gøres til genstand for samhandel, hvis de opfylder følgende krav:
1) Generelt:
a) de skal komme fra en bedrift, hvor der ikke er konstateret fjerkræinfluenza i de 30 dage, der går forud for afsendelsen
b) de skal komme fra en bedrift eller et område, som ikke er underkastet restriktioner som led i bekæmpelsen af Newcastle disease
indtil de fællesskabsforanstaltninger, der er omhandlet i artikel 19 i direktiv 90/539/EØF, er blevet gennemført, finder de nationale krav med hensyn til bekæmpelse af Newcastle disease anvendelse under overholdelse af Traktatens almindelige bestemmelser
c) de skal i overensstemmelse med artikel 10, stk. 1, tredje led, i direktiv 91/496/EØF, hvis de er indført fra et tredjeland, have været i karantæne på den bedrift, som de er bragt til efter indførslen på Fællesskabets område.
2) For fugle af papegøjefamilien gælder endvidere følgende:
a) de må ikke komme fra en bedrift, hvor der er diagnosticeret psittacosis (Clamydia psittaci), eller have været i kontakt med dyr fra en sådan bedrift.
Forbudsperioden skal være på mindst to måneder efter det senest diagnosticerede tilfælde og behandling under en efter fremgangsmåden i artikel 26 anerkendt dyrlægekontrol
b) de skal være identificeret i overensstemmelse med artikel 3, stk. 1, litra c), i direktiv 90/425/EØF.
Metoderne til identifikation af fugle af papegøjefamilien, herunder navnlig syge fugle, fastsættes efter fremgangsmåden i artikel 26
c) de skal ledsages af et handelsdokument, som er attesteret af en embedsdyrlæge eller den dyrlæge, der har ansvaret for den bedrift eller den handelsvirksomhed, hvorfra de kommer, og som den kompetente myndighed har givet beføjelse hertil.
B. I artikel 2, stk. 2, nr. 2, i Rådets direktiv 91/495/EØF af 27. november 1990 om sundhedsmæssige og dyresundhedsmæssige problemer i forbindelse med produktion og afsætning af kaninkød og kød af opdrættet vildt (
16
) indføjes »samt strudsfugle (ratitae)« i tredje linje efter »de … i direktiv 90/539/EØF omhandlede arter«.
I artikel 2, stk. 2, nr. 1, i Rådets direktiv 90/539/EØF af 15. oktober 1990 om dyresundhedsmæssige betingelser for samhandelen inden for Fællesskabet med fjerkræ og rugeæg samt for indførsel heraf fra tredjelande (
17
) indføjes »samt strudsfugle (ratitae)« efter »og agerhøns«.
Artikel 8
Medlemsstaterne sørger for, at bier (Apis mellifica) kun kan gøres til genstand for samhandel, hvis de opfylder følgende krav:
a) de skal komme fra et distrikt, som ikke har fået pålagt forbud i forbindelse med udbrud af amerikansk bipest.
Forbudsperioden skal være på mindst 30 dage efter det senest konstaterede tilfælde og efter det tidspunkt, hvor alle bistader inden for en radius på 3 km er blevet kontrolleret af den kompetente myndighed, og alle inficerede bistander er blevet enten afbrændt eller behandlet og godkendt af denne myndighed.
Efter fremgangsmåden i artikel 26 og efter udtalelse fra Den Videnskabelige Veterinærkomité kan de krav, som gælder for bier (Apis melifera), eller tilsvarende krav også finde anvendelse på humlebier
b) de skal ledsages af et sundhedscertifikat i overensstemmelse med modellen i bilag E, som er påført en attestering fra den kompetente myndighed af, at de i litra a) omhandlede krav er opfyldt.
Artikel 9
1. Medlemsstaterne sørger for, at hareagtige gnavere kun gøres til genstand for samhandel, hvis de opfylder følgende krav:
a) de må ikke komme fra en bedrift eller have været i kontakt med dyr fra en bedrift, hvor der har været udbrud af eller mistanke om rabies inden for den seneste måned
b) de skal komme fra en bedrift, hvor ingen dyr viser kliniske tegn på myxomatose.
2. De medlemsstater, der kræver et sundhedscertifikat i forbindelse med hareagtige gnaveres bevægelser på deres område, kan kræve, at dyr, der indføres på deres område, skal ledsages af et sundhedscertifikat i overensstemmelse med modellen i bilag E, som er påført følgende attestering:
»Undertegnede … attesterer, at ovennævnte dyr opfylder kravene i artikel 9 i direktiv 92/65/EØF, og at dyrene ikke har vist kliniske tegn på sygdom ved undersøgelsen.«
Denne attestering udstedes af embedsdyrlægen eller den dyrlæge, der har tilsynet med oprindelsesbedriften, og til hvem den kompetente myndighed har delegeret denne kompetence, eller, når der er tale om industrielt opdræt, af embedsdyrlægen.
De medlemsstater, der ønsker at gøre brug af denne mulighed, meddeler på forhånd dette til Kommissionen, som skal sikre sig, at det i stk. 1 nævnte krav er opfyldt.
3. Irland og Det Forenede Kongerige kan kræve, at der forelægges et sundhedscertifikat, hvori det attesteres, at kravet i stk. 1, litra a), er opfyldt.
Artikel 10
1. Medlemsstaterne sørger for, at samhandel forbydes med
►M5
————— ◄ minke og ræve, som kommer fra en bedrift eller har været i kontakt med dyr fra en bedrift, hvor der har været udbrud af eller mistanke om rabies inden for de seneste seks måneder, medmindre de er underkastet et systematisk vaccinationsprogram.
▼M5
2. Katte, hunde og fritter kan kun gøres til genstand for samhandel, hvis de opfylder kravene i artikel 5 og 16 i Europa-Parlamentets og Rådets forordning (EF) nr. 998/2003 af 26. maj 2003 om dyresundhedsmæssige betingelser for ikke-kommerciel transport af selskabsdyr og om ændring af Rådets direktiv 92/65/EØF (
18
).
Den attest, der skal ledsage dyrene, skal desuden godtgøre, at der 24 timer inden afsendelsen er foretaget en klinisk undersøgelse af en dyrlæge, der er bemyndiget af den kompetente myndighed, og at undersøgelsen viste, at dyrene er sunde og kan tåle transporten til bestemmelsesstedet.
3. Som en undtagelse fra stk. 2 skal katte, hunde og fritter opfylde betingelserne i artikel 6 og 16 i forordning (EF) nr. 998/2003, når de er bestemt til Irland, Det Forenede Kongerige eller Sverige.
Den attest, der skal ledsage dyrene, skal desuden godtgøre, at der 24 timer inden afsendelsen er foretaget en klinisk undersøgelse af en dyrlæge, der er bemyndiget af den kompetente myndighed, og at undersøgelsen viste, at dyrene er sunde og kan tåle transporten til bestemmelsesstedet.
▼A2
4. Irland, Cypern, Malta og Det Forenede Kongerige kan med forbehold af stk. 2 og 3 fastholde deres nationale karantænebestemmelser for alle kødædere,
►M5
bortset fra de arter, der er omhandlet i stk. 2 og 3, ◄ primater, flagermus og andre dyr, der er modtagelige for rabies, og som er omfattet af direktivet, og for hvilke det kan påvises, at de er født på oprindelsesbedriften og holdt i fangenskab siden deres fødsel, idet opretholdelsen af disse bestemmelser dog ikke må berøre ophævelsen af veterinærkontrollen ved grænserne mellem medlemsstaterne.
▼B
5. Beslutning 90/638/EØF ændres således:
1) Følgende led tilføjes i artikel 1:
— »for så vidt angår programmerne for rabiesbekæmpelse, opfyldte kriterierne i bilag III«
.
2) Følgende bilag indsættes:
»BILAG III
Kriterier for rabiesprogrammer
Rabiesprogrammer skal mindst omfatte følgende:
a) Kriterierne i nr. 1 til 7, i bilag I.
b) Detaljerede oplysninger om den eller de områder, hvor oral immunisering af ræve finder sted, og om områdets eller områdernes naturlige grænser. Området eller områderne skal dække mindst 6 000 km2 eller en medlemsstats samlede område og kan omfatte tilgrænsende områder i tredjelande.
c) Detaljerede oplysninger om de anvendte vacciner, distributionssystemet, tætheden og hyppigheden af udlægningen af lokkemad.
d) I givet fald alle detaljer i, omkostninger ved og målsætningen for de foranstaltninger til genopretning eller bevaring af flora og fauna, som gennemføres af frivillige organisationer på det område, som disse projekter dækker.«
6. Rådet, der træffer afgørelse med kvalificeret flertal på forslag af Kommissionen, udpeger et bestemt institut, der skal opstille de nødvendige kriterier for standardisering af de serologiske tests, og bestemmer dets opgaver.
7. Medlemsstaterne sørger for, at udgifterne til anvendelse af serologiske tests dækkes af importørerne.
▼M5 —————
▼
Artikel 10a
For så vidt angår rabies, ændres artikel 9 og 10 i henhold til fremgangsmåden i artikel 26 efter fremlæggelse af den relevante dokumentation, for at tage højde for situationen i Finland og Sverige, således at de samme bestemmelser finder anvendelse på dem som på medlemsstater, som befinder sig i en tilsvarende situation.
▼B
Artikel 11
1. Medlemsstaterne søger for, at der med forbehold af de afgørelser, der skal træffes i henhold til artikel 21 og 23, kun handles med sæd, æg og embryoner, der opfylder betingelserne i stk. 2, 3 og 4.
2. Fåre-, gede- og hestesæd skal med forbehold af eventuelle kriterier, der skal overholdes ved opførelsen af enhovede dyr i stambøger, for så vidt angår visse specifikke racer:
— være opsamlet og behandlet til kunstig insemination på en station eller et center, der er sundhedsgodkendt i henhold til bilag D, kapitel I, eller — for så vidt angår får og geder som en undtagelse fra ovenstående — på en bedrift, der opfylder kravene i direktiv 91/68/EØF
— være opsamlet fra dyr, der opfylder betingelserne i bilag D, kapitel II (dyrenes egnethed og rutinekontrol)
— være opsamlet, behandlet og konserveret efter bestemmelserne i bilag D, kapitel III
— være ledsaget under transport til en anden medlemsstat af et sundhedscertifikat i overensstemmelse med en model, der skal udarbejdes efter fremgangsmåden i artikel 26.
3. Æg og embryoner fra får/geder, svin og enhovede dyr skal:
— være opsamlet af et opsamlingshold, der er godkendt af medlemsstatens kompetente myndighed, og behandlet i et egnet laboratorium og skal stamme fra donorer, der opfylder betingelserne i bilag D, kapitel IV
— være behandlet og opbevaret efter bestemmelserne i bilag D, kapitel III
— være ledsaget ved forsendelse til en anden medlemsstat af et sundhedscertifikat i overensstemmelse med en model, der skal udarbejdes efter fremgangsmåden i artikel 26.
Sæd, der anvendes til insemination af donorer, skal være i overensstemmelse med stk. 2 for så vidt angår får, geder og enhovede dyr og med direktiv 90/429/EØF for så vidt angår svin. Der kan eventuelt fastsættes yderligere garantier efter fremgangsmåden i artikel 26.
4. Kommissionen aflægger inden den 31. december 1997 rapport, eventuelt med passende forslag om denne artikels anvendelse, bl.a. under hensyn til den videnskabelige og teknologiske udvikling.
Artikel 12
1. Kontrolreglerne i direktiv 90/425/EØF finder anvendelse, navnlig hvad angår tilrettelæggelse og opfølgning af den kontrol, der skal udøves, på de i dette direktiv omhandlede dyr og æg, sæd og embryoner, som er ledsaget af et sundhedscertifikat. De øvrige dyr skal komme fra bedrifter, der med hensyn til kontrollen på oprindelses- og bestemmelsesstedet er underkastet reglerne i nævnte direktiv.
2. Artikel 10 i direktiv 90/425/EØF anvendes på dyr, sæd og embryoner, der er omhandlet i dette direktiv.
3. I forbindelse med handel gælder bestemmelserne i artikel 12 i direktiv 90/425/EØF ligeledes for handelsvirksomheder, der permanent eller lejlighedsvis er i besiddelse af dyr som omhandlet i artikel 7, 9 og 10.
4. De oplysninger, som skal gives til bestemmelsesstedet i henhold til artikel 4, stk. 2, i direktiv 90/425/EØF, skal for dyr, sæd, æg eller embryoner, som i henhold til dette direktiv ledsages af et sundhedscertifikat, finde sted over ANIMO-systemet.
5. Med forbehold af de særlige bestemmelser, der er omhandlet i dette direktiv, foretager den kompetente myndighed den kontrol, som den finder passende, hvis den har mistanke om, at dette direktiv ikke er overholdt, eller nærer tvivl om sundheden hos de dyr eller kvaliteten af sæd, æg og embryoner, som omhandles i artikel 1.
6. Medlemsstaterne træffer passende administrative eller strafferetlige foranstaltninger med henblik på at straffe enhver overtrædelse af bestemmelserne i dette direktiv, især når det fastslås, at de udstedte certifikater eller dokumenter ikke svarer til de i artikel 1 nævnte dyrs virkelige tilstand, at identifikationen af de pågældende dyr eller mærkningen af sæd, æg og embryoner ikke er i overensstemmelse med dette direktiv, eller at dyrene eller produkterne ikke har været underkastet den i dette direktiv fastsatte kontrol.
Artikel 13
1. Ved samhandel med dyr af arter, som er modtagelige for de i bilag A nævnte sygdomme eller de i bilag B nævnte sygdomme, hvis modtagerlandet har fået de garantier, der er nævnt i artikel 14 og 15, samt samhandel med sæd, æg og embryoner af sådanne dyr fra og til organer, institutter og centre, som er godkendt i henhold til bilag C, skal der forevises et transportdokument med oplysninger i den i bilag E viste model. Der skal i dokumentet, som den dyrlæge, der har tilsynet med oprindelsesorganet, -instituttet eller -centret, skal udfylde, gøres opmærksom på, at dyret, sæden, æggene eller embryonerne hidrører fra et organ, institut eller center, som et godkendt i henhold til bilag C, og dokumentet skal ledsage dem under transporten.
2.
a) For at blive godkendt skal organer, institutter og centre for så vidt angår anmeldelsespligtige sygdomme over for vedkommende medlemsstats myndigheder fremlægge fornøden dokumentation for, at de opfylder kravene i bilag C.
b) Efter at have modtaget sådan fornøden dokumentation i tilknytning til en ansøgning om godkendelse eller forlængelse af en godkendelse undersøger den kompetente myndighed sagen på grundlag af de meddelte oplysninger og eventuelt tillige på grundlag af resultatet af kontrol på stedet.
c) Den kompetente myndighed tilbagekalder en godkendelse i overensstemmelse med bilag C, punkt 3.
d) Hver medlemsstat sender Kommissionen en liste over godkendte organer, institutter og centre og giver underretning om alle ændringer i listen. Kommissionen videresender disse oplysninger til de øvrige medlemsstater.
▼
e) Sverige har to år fra datoen for tiltrædelsestraktatens ikrafttræden til at gennemføre de foreskrevne foranstaltninger vedrørende organer, institutter og centre.
▼B
Artikel 14
1. Såfremt en medlemsstat — enten direkte eller gennem opdrætterne — opstiller eller har opstillet et fakultativt eller obligatorisk program til bekæmpelse eller overvågning af en af de i bilag B nævnte sygdomme, kan den forelægge Kommissionen dette program med oplysning om navnlig følgende:
— situationen med hensyn til den pågældende sygdom på dens område
— det forhold, at der er pligt til at give underretning om sygdommen
— programmets berettigelse under hensyn til sygdommens alvor og programmets cost/benefit-fordele
— det geografiske område, hvor programmet skal anvendes
— de forskellige former for status, som bedrifter og anlæg kan have, de krav, der skal opfyldes for hver enkelt art, når indsættelse i bestanden sker, og fremgangsmåderne ved foretagelse af tests
— procedurerne for kontrol med programmet, herunder oplysning om, i hvor høj grad opdrætterne er inddraget i gennemførelsen af bekæmpelses- eller overvågningsprogrammet
— de konsekvenser, der må drages, hvis en bedrift af den ene eller den anden grund mister sin status
— de foranstaltninger, der skal træffes, såfremt der ved kontrol foretaget i henhold til programmet konstateres positive resultater
— den ikke-diskriminerende karakter af forholdet mellem samhandelen på den pågældende medlemsstats område og samhandelen inden for Fællesskabet.
2. Kommissionen gennemgår de programmer, medlemsstaterne forelægger. Programmerne kan godkendes efter fremgangsmåden i artikel 26 og under overholdelse af kriterierne i stk. 1. Efter samme fremgangsmåde skal de generelle eller begrænsede yderligere garantier, der kan kræves i samhandelen, defineres samtidig med eller senest tre måneder efter fremlæggelsen af programmerne. Disse garantier må ikke være mere omfattende end dem, som medlemsstaten anvender på sit eget område.
3. De af medlemsstaterne forelagte programmer kan ændres eller suppleres efter fremgangsmåden i artikel 26. Efter samme fremgangsmåde kan de i stk. 2 nævnte garantier ændres.
Artikel 15
1. En medlemsstat, der mener at være helt eller delvis fri for en af de i bilag B nævnte sygdomme, som dyr, der er omhandlet i dette direktiv, er modtagelige for, forelægger Kommissionen behørigt materiale til dokumentation heraf. Den gør navnlig rede for følgende:
— sygdommens art og udviklingen i dens forekomst på medlemsstatens område
— resultaterne af overvågningstests baseret på en serologisk, mikrobiologisk, patologisk eller epidemiologisk undersøgelse
— hvor lang tid der har været pligt til at anmelde sygdommen over for de kompetente myndigheder
— hvor lang tid der har været foretaget overvågning
— i givet fald den periode, i hvilken der har været forbud mod at vaccinere mod sygdommen, og det geografiske område, der er omfattet af forbuddet
— reglerne for kontrol med, at sygdommen ikke forekommer.
2. Kommissionen gennemgår det dokumentationsmateriale, der er nævnt i stk. 1, og forelægger derefter Den Stående Veterinærkomité en afgørelse om godkendelse eller afvisning af den plan, medlemsstaten har fremlagt. Hvis planen godkendes, defineres de generelle eller begrænsede yderligere garantier, der kan kræves i samhandelen, efter fremgangsmåden i artikel 26. De må ikke være mere omfattende end dem, som medlemsstaten anvender på sit eget område.
Indtil afgørelse herom er truffet, kan den berørte medlemsstat i samhandelen opretholde de relevante krav, der er nødvendige for bevarelsen af dens status.
3. Den pågældende medlemsstat giver Kommissionen meddelelse om enhver ændring i det i stk. 1 nævnte godtgørelsesmateriale. På baggrund af de meddelte oplysninger kan de garantier, der måtte være fastsat i henhold til stk. 2, ændres eller ophæves efter fremgangsmåden i artikel 26.
KAPITEL III
Bestemmelser vedrørende indførsel i Fællesskabet
Artikel 16
Bestemmelserne vedrørende indførsel af dyr, sæd, æg og embryoner, der er omfattet af dette direktiv, skal mindst svare til dem, der er fastsat i kapitel II.
▼M5
Betingelserne for indførsel af katte, hunde og fritter skal mindst svare til betingelserne i kapitel III i forordning (EF) nr. 998/2003.
Den attest, der skal ledsage dyrene, skal desuden godtgøre, at der 24 timer inden afsendelsen er foretaget en klinisk undersøgelse af en dyrlæge, der er bemyndiget af den kompetente myndighed, og at undersøgelsen viste, at dyrene er sunde og kan tåle transporten til bestemmelsesstedet.
▼B
Artikel 17
1. For at sikre ensartet anvendelse af artikel 16 anvendes bestemmelserne i det følgende.
2. Der kan kun foretages indførsel i Fællesskabet af dyr og sæd, æg og embryoner, som nævnt i artikel 11, der opfylder følgende krav:
a) stammer fra et tredjeland på den liste, der skal opstilles i henhold til stk. 3, litra a)
b) ledsages af et sundhedscertifikat, der svarer til en model, som skal udarbejdes efter fremgangsmåden i artikel 26, og er underskrevet af den kompetente myndighed i udførselslandet, hvor det attesteres, at pågældende dyr, sæd, æg og embryoner opfylder de eventuelle yderligere betingelser eller tilsvarende garantier, der er nævnt i stk. 4, eller kommer fra godkendte organer, institutter, centre eller opsamlingsstationer, som giver de nævnte garantier.
3. Efter fremgangsmåden i artikel 26 fastlægges:
▼M7
a) en liste over de tredjelande eller dele af tredjelande, der er i stand til at give medlemsstaterne og Kommissionen garantier svarende til dem, der er fastsat i kapitel II, for så vidt angår dyr, sæd, æg og embryoner,
samt
b) en liste over de opsamlingsstationer, for hvilke disse tredjelande kan give de i artikel 11 omhandlede garantier, jf. dog Kommissionens beslutning 94/63/EF af 31. januar 1994 om en liste over tredjelande, hvorfra medlemsstaterne tillader indførsel af sæd, æg og embryoner af får og geder samt æg og embryoner af svin (
19
).
Kommissionen underretter medlemsstaterne om ethvert forslag om ændring af listerne over opsamlingsstationer, og medlemsstaterne har, fra datoen for modtagelse af de foreslåede ændringer at regne, ti arbejdsdage til at indsende skriftlige bemærkninger til Kommissionen.
Hvis der ikke indkommer bemærkninger fra medlemsstaterne inden for perioden på ti arbejdsdage, anses de foreslåede ændringer for at være accepteret af medlemsstaterne, og import tillades i overensstemmelse med de ændrede lister, når Kommissionen giver de kompetente myndigheder i medlemsstaterne og det pågældende tredjeland meddelelse om, at ændringerne er offentliggjort på Kommissionens websted.
Hvis der indkommer skriftlige bemærkninger fra mindst én medlemsstat inden for perioden på ti arbejdsdage, underretter Kommissionen medlemsstaterne og Den Stående Komité for Fødevarekæden og Dyresundhed på komitéens næste møde med henblik på, at der træffes en beslutning efter proceduren i artikel 26, stk. 2.
▼B
c) specifikke dyresundhedsmæssige betingelser især med det sigte at beskytte Fællesskabet mod visse eksotiske sygdomme — eller garantier, der svarer til dem, der er fastsat i dette direktiv.
De specifikke betingelser og tilsvarende garantier, der fastsættes for tredjelande, må ikke være gunstigere end de i kapitel II fastsatte.
4. På den i stk. 3 nævnte liste kan kun medtages tredjelande eller dele af tredjelande:
a) hvorfra indførsel ikke er forbudt:
— fordi der er fri for sygdomme som nævnt i bilag A, eller for enhver anden sygdom, der betragtes som eksotisk i Fællesskabet
— i medfør af artikel 6, 7 og 14 i direktiv 72/462/EØF og artikel 17 i direktiv 91/495/EØF og 71/118/EØF (
20
) eller — for så vidt angår de øvrige dyr, der er omhandlet i dette direktiv — på grundlag af en afgørelse truffet efter fremgangsmåden i artikel 26 og under hensyn til deres sundhedstilstand
b) som under hensyn til lovgivningen og dets veterinær- og kontroltjenesters struktur, disses beføjelser og det tilsyn, de er undergivet, anses for egnede, jf. artikel 3, stk. 2, i direktiv 72/462/EØF, til at garantere gennemførelsen af den gældende lovgivning
c) hvis veterinærtjeneste er i stand til at garantere overholdelsen af sundhedskrav, der mindst svarer til dem, der er fastsat i kapitel II.
5. Eksperter fra Kommissionen og fra medlemsstaterne efterprøver ved kontrol på stedet, om de garantier, som tredjelandet har givet med hensyn til produktions- og afsætningsbetingelser, kan betragtes som svarende til dem, der gælder i Fællesskabet.
Medlemsstaternes eksperter, der skal foretage denne kontrol, udpeges af Kommissionen på forslag af medlemsstaterne.
Kontrollen foretages på Fællesskabets vegne og for dettes regning.
6. Indtil den kontrol, der er omhandlet i stk. 5, er blevet iværksat, finder de nationale bestemmelser vedrørende inspektion i tredjelande fortsat anvendelse, idet manglende overholdelse af garantierne i henhold til stk. 3, der konstateres under en sådan inspektion, meddeles Den Stående Veterinærkomité.
Artikel 18
1. Medlemsstaterne sørger for, at dyr, sæd, æg og embryoner, der er omhandlet i dette direktiv, kun indføres i Fællesskabet, hvis:
— de er ledsaget af et certifikat, der undstedes af embedsdyrlægen.
— Modellen til certifikatet udarbejdes, alt efter hvilken art der er tale om, efter fremgangsmåden i artikel 26
— de har gennemgået den kontrol, der er omhandlet i direktiv 90/675/EØF og 91/496/EØF (
21
), med tilfredsstillende resultat
— de før indladningen til Fællesskabets område har gennemgået en kontrol foretaget af en embedsdyrlæge til sikring af, at de transportbetingelser, der er omhandlet i direktiv 91/628/EØF (
22
), overholdes, navnlig for så vidt angår forsyning med vand og foder
— de for så vidt angår dyr, der er omhandlet i artikel 5 til 10, underkastes karantæne efter regler, der fastsættes i henhold til fremgangsmåden i artikel 26.
2. Indtil gennemførelsesbestemmelserne til denne artikel er fastsat, gælder de nationale regler for indførsel fra tredjelande, for hvilke der ikke er vedtaget fællesskabsregler, for så vidt de ikke er gunstigere end de i kapitel II indeholdte regler.
Artikel 19
Efter fremgangsmåden i artikel 26 fastlægges:
a) de særlige dyresundhedsmæssige betingelser for indførsel i Fællesskabet, arten og indholdet af ledsagedokumenterne for dyr til zoologiske haver, cirkus, forlystelsesparker eller forsøgslaboratorier, alt efter hvilke dyrearter der er tale om
b) yderligere garantier ud over dem, der er fastsat for de forskellige dyrearter, der er omhandlet i dette direktiv, navnlig for at beskytte de berørte fællesskabsarter.
Artikel 20
Principperne og reglerne i direktiv 90/675/EØF finder navnlig anvendelse med hensyn til tilrettelæggelse og opfølgning af den kontrol, som medlemsstaterne skal foretage, og til de beskyttelsesforanstaltninger, der skal iværksættes.
Indtil gennemførelsen af de beslutninger, der er nævnt i artikel 8, nr. 3, og i artikel 30 i direktiv 91/496/EØF, finder de hidtil gældende nationale gennemførelsesbestemmelser til artikel 8, nr. 1 og 2, i nævnte direktiv fortsat anvendelse med forbehold af de i stk. 1 nævnte regler og principper.
KAPITEL IV
Almindelige og afsluttende bestemmelser
Artikel 21
De eventuelle modeller til certifikater, som skal anvendes i samhandelen, samt de dyresundhedsmæssige betingelser, som dyr, sæd, æg og embryoner, der ikke er omhandlet i artikel 5 til 11, skal opfylde for at kunne gøres til genstand for samhandel, fastsættes i fornødent omfang efter fremgangsmåden i artikel 26.
Artikel 22
Bilagene ændres efter behov efter fremgangsmåden i artikel 26.
▼
Bilag B tages op til fornyet behandling før tiltrædelsestraktatens ikrafttræden, navnlig med henblik på at ændre listen over sygdomme til at omfatte sygdomme, som drøvtyggere og svin kan få, samt sygdomme som kan overføres via sæd, æg og embryoner fra svin.
▼B
Artikel 23
Efter fremgangsmåden i artikel 26 kan der eventuelt som en undtagelse
►M7
————— ◄ kapitel II fastsættes særlige betingelser for geografisk bevægelse for dyr i forbindelse med cirkusser og markeder og samhandel med dyr, sæd, æg og embryoner til zoologiske haver.
Artikel 24
1. Medlemsstaterne kan lade indførsel til deres område af dyr (herunder volierefugle) og sæd, æg og embryoner, som er omhandlet i dette direktiv, og som er ført over et tredjelands område i transit, være betinget af, at der forevises et sundhedscertifikat, som godtgør, at kravene i dette direktiv er overholdt.
2. De medlemsstater, der gør brug af muligheden i stk. 1, underretter Kommissionen og de øvrige medlemsstater herom gennem Den Stående Veterinærkomité.
Artikel 25
I bilag A til direktiv 90/425/EØF tilføjes:
»Rådets direktiv 92/65/EØF af 13. juli 1992 om dyresundhedsmæssige betingelser for samhandel med og indførsel i Fællesskabet af dyr, sæd, æg og embryoner, der for så vidt angår disse betingelser ikke er underlagt de specifikke fællesskabsbestemmelser, der er fastsat i bilag A, afsnit I i direktiv 90/425/EØF (EFT nr. L 268 af 14. 9. 1992, s. 54.«
▼M7
Artikel 26
1. Kommissionen bistås af Den Stående Komité for Fødevarekæden og Dyresundhed, der er nedsat ved artikel 58 i Europa-Parlamentets og Rådets forordning (EF) nr. 178/2002 (
23
).
2. Når der henvises til dette stykke, anvendes artikel 5 og 7 i afgørelse 1999/468/EF.
Det tidsrum, der nævnes i artikel 5, stk. 6, i afgørelse 1999/468/EF (
24
), fastsættes til tre måneder.
3. Komitéen vedtager selv sin forretningsorden.
▼B
Artikel 27
De medlemsstater, der iværksætter en alternativ kontrolordning, som giver garantier svarende til dem, der kræves i dette direktiv for bevægelser på deres område med dyr, sæd, æg og embryoner, der er omfattet af direktivet, kan gensidigt indrømme undtagelse fra artikel 6, litra A, nr. 1, litra f), artikel 8, litra b), og artikel 11, stk. 1, litra d).
Artikel 28
Der kan efter fremgangsmåden i artikel 26 for et tidsrum af tre år vedtages overgangsforanstaltninger for at lette overgangen til den nye kontrolordning, der er fastsat i dette direktiv.
Artikel 29
1. Medlemsstaterne sætter de nødvendige love og administrative bestemmelser i kraft for at efterkomme dette direktiv siden den 1. januar 1994. De underretter straks Kommissionen herom.
Når medlemsstaterne vedtager disse love og administrative bestemmelser, skal de indeholde en henvisning til dette direktiv, eller de skal ved offentliggørelsen ledsages af en sådan henvisning. De nærmere regler for denne henvisning fastsættes af medlemsstaterne.
2. Medlemsstaterne meddeler Kommissionen teksten til de vigtigste retsforskrifter, som de vedtager på det område, der er omfattet af dette direktiv.
3. Den frist for gennemførelsen af direktivet, som er fastsat til den 1. januar 1994, berører ikke afskaffelsen af veterinærkontrollen ved grænserne som fastsat i direktiv 89/662/EØF og 90/425/EØF.
Artikel 30
Dette direktiv er rettet til medlemsstaterne.
▼M6
BILAG A
Sygdomme, der er anmeldelsespligtige i henhold til dette direktiv
|
Sygdom
|
Orden/familie/primært berørte arter
|
|
Afrikansk hestepest
|
Dyr af hestefamilien
|
|
Afrikansk svinepest
|
Suidae og Tayassuidae
|
|
Aviær influenza
|
Aves
|
|
Amerikansk bipest
|
Apis
|
|
Miltbrand
|
Bovidae, Camelidea, Cervidae, Elephantidae, Equidae og Hippopotamidae
|
|
Bluetongue
|
Antilocapridae, Bovidae, Cervidae, Giraffidae og Rhinocerotidae
|
|
Brucella abortus
|
Antilocapridae, Bovidae, Camelidae, Cervidae, Giraffidae, Hippopotamidae og Tragulidae
|
|
Brucella melitensis
|
Antilocapridae, Bovidae, Camelidae, Cervidae, Giraffidae, Hippopotamidae og Tragulidae
|
|
Brucella ovis
|
Camelidae, Tragulidae, Cervidae, Giraffidae, Bovidae og Antilocapridae
|
|
Brucella suis
|
Cervidae, Leporidae, Ovibos moschatus, Suidae og Tayassuidae
|
|
Klassisk svinepest
|
Suidae og Tayassuidae
|
|
Oksens ondartede lungesyge
|
Kvæg (herunder zebu, bøffel, bison og yak)
|
|
Ebola
|
Menneskeaber
|
|
Mund- og klovesyge
|
Artiodactyla og indiske elefanter
|
|
Infektiøs hæmatopoietisk nekrose
|
Salmonidae
|
|
Lumpy skin disease
|
Bovidae og Giraffidae
|
|
Abekopper
|
Rodentia og menneskeaber
|
|
Mycobacterium bovis
|
Mammalia, især Antilocapridae, Bovidae, Camelidae, Cervidae, Giraffidae og Tragulidae
|
|
Newcastle disease
|
Aves
|
|
Pest hos små drøvtyggere
|
Bovidae og Suidae
|
|
Teschener syge
|
Suidae
|
|
Psitacosis
|
Psittaciformes
|
|
Rabies
|
Carnivora og Chiroptera
|
|
Rift valley fever
|
Bovidae, Camelus-arter og Rhinocerotidae
|
|
Kvægpest
|
Artiodactyla
|
|
Lille stadebille (Aethina tumida)
|
Apis og Bombus
|
|
Fåre- og gedekopper
|
Bovidae
|
|
Smitsom blæreudslæt hos svin
|
Suidae og Tayassuidae
|
|
Tropilaelaps-mide (Tropilaelaps spp)
|
Apis
|
|
Vesikulær stomatitis
|
Artiodactyla og Equidae
|
|
TSE
|
Bovidae, Cervidae, Felidae og Mustelidae
|
▼B
BILAG B
LISTE OVER SYGDOMME, FOR HVILKE NATIONALE PROGRAMMER KAN ANERKENDES I HENHOLD TIL DETTE DIREKTIV
|
Mink
|
Virus enteritis
Aleutian-syge
|
|
Bier
|
Amerikansk bipest
Trachemide-syge (varroatose)
|
|
Aber og dyr af kattefamilien
|
Tuberkulose
|
|
Drøvtyggere
|
Tuberkulose
|
|
Hareagtige gnavere
|
Myxomatosis
Kaninens virale og hæmoragiske sygdomme
Tularæmi
|
▼M3
BILAG C
BETINGELSER FOR GODKENDELSE AF ORGANER, INSTITUTTER OG CENTRE
1) For at et organ, institut eller center som defineret i artikel 2, stk. 1, litra c), kan godkendes officielt i henhold til dette direktivs artikel 13, stk. 2, skal det opfylde følgende krav:
a) det skal være klart afgrænset og adskilt fra sine omgivelser eller de indespærrede dyr og være således beliggende, at det ikke udgør nogen sundhedsrisiko for landbrugsbedrifter, hvis sundhedsmæssige status kunne bringes i fare
b) det skal have passende midler til at indfange, indespærre og isolere dyr og passende karantænefaciliteter og godkendte procedurer for dyr af ikke-godkendt oprindelse
c) det skal være fri for de i bilag A nævnte sygdomme og for de i bilag B nævnte sygdomme, når det pågældende land har et program i henhold til artikel 14. For at et organ, institut eller center kan erklæres fri for disse sygdomme, skal myndighederne vurdere de registre over den dyresundhedsmæssige status, der mindst er blevet ført i de foregående tre år, og resultaterne af de kliniske prøver og laboratorieprøver, som organet, instituttet eller centret har underkastet dyrene. Som undtagelse fra dette krav godkendes nye etablissementer dog, hvis de dyr, der indgår i bestanden, stammer fra godkendte etablissementer
d) det skal løbende føre registre over:
i) antallet af dyr af hver art i etablissementet og deres identitet (alder, køn, art og individuel identifikation, hvis det er muligt)
ii) antallet dyr, som tilgår eller fragår etablissementet, og deres identitet (alder, køn, art og individuel identifikation, hvis det er muligt) tillige med oplysninger om deres oprindelse eller destination, transporten fra eller til etablissementet og dyrenes sundhedsstatus
iii) resultaterne af blodprøver og alle andre diagnoseprocedurer
iv) sygdomstilfælde og den eventuelle behandling deraf
v) resultaterne af post mortem-undersøgelser af dyr, som er døde i etablissementet, herunder dødfødte dyr
vi) de iagttagelser, der er gjort i løbet af en eventuel isolations- eller karantæneperiode
e) det skal enten have en ordning med et kvalificeret laboratorium om udførelse af post mortem-undersøgelser eller have et eller flere egnede lokaler, hvor disse undersøgelser kan udføres af en kvalificeret person, som arbejder under den godkendte dyrlæge
f) det skal enten have ordninger eller faciliteter på stedet til at bortskaffe kadavere af dyr, som er døde af en sygdom eller aflivet
g) det skal ved kontrakt eller et andet retligt instrument sikre, at der tilknyttes en dyrlæge, som er godkendt og kontrolleres af myndighederne, og som:
i) med de fornødne ændringer opfylder kravene i artikel 14, stk. 3, litra B, i direktiv 64/432/EØF
ii) sørger for, at den fornødne sygdomsovervågning og de fornødne kontrolforanstaltninger i forbindelse med landets sygdomssituation godkendes af myndighederne og gennemføres i organet, på instituttet eller centret. Foranstaltningerne skal omfatte følgende:
— en årlig sygdomsovervågningsplan, der omfatter kontrol af dyrene for zoonoser
— klinisk undersøgelse, laboratorieundersøgelse og post mortem-undersøgelse af dyr, der mistænkes for at være ramt af overførbare sygdomme
— eventuelt vaccination af modtagelige dyr mod smitsomme sygdomme, udelukkende i overensstemmelse med EF-bestemmelserne
iii) sikrer sig, at mistænkelige dødsfald eller tilstedeværelse af et symptom, der tyder på, at dyr har pådraget sig en eller flere af de i bilag A og B nævnte sygdomme, omgående anmeldes til myndighederne, hvis den pågældende sygdom er anmeldelsespligtig i medlemsstaten
iv) sikrer sig, at tilkomne dyr om nødvendigt er blevet isoleret i overensstemmelse med kravene i dette direktiv og eventuelle instrukser fra myndighederne
v) er ansvarlig for den daglige overholdelse af dyresundhedskravene i dette direktiv og i EF-bestemmelserne om dyrs velfærd under transport og om bortskaffelse af animalsk affald
h) det skal, hvis det holder dyr, som er bestemt til forsøgslaboratorier, opfylde betingelserne i artikel 5 i direktiv 86/609/EØF.
2) Godkendelsen bevares, når følgende krav er opfyldt:
a) organet/instituttet/centret er under tilsyn af en af myndighederne udpeget embedsdyrlæge, der:
i) besøger organet, instituttet eller centret mindst en gang om året
ii) kontrollerer den godkendte dyrlæges arbejde og gennemførelsen af den årlige sygdomsovervågningsplan
iii) sikrer sig, at bestemmelserne i dette direktiv overholdes
b) kun dyr fra et andet godkendt organ, institut eller center må overføres til etablissementet, jf. bestemmelserne i dette direktiv
c) embedsdyrlægen kontrollerer:
— at bestemmelserne i dette direktiv er opfyldt
— at der ved de kliniske undersøgelser, post mortem-undersøgelserne og laboratorieundersøgelserne af dyrene ikke er påvist nogen af de sygdomme, der er nævnt i bilag A og B
d) organet, instituttet eller centret skal efter godkendelsen opbevare de i punkt 1, litra d), nævnte registre i mindst ti år.
3) Uanset artikel 5, stk. 1, i dette direktiv og punkt 2, litra b), ovenfor kan dyr, herunder aber (simiae og prosimiae), der ikke kommer fra et godkendt organ, institut eller center, dog bringes ind i et godkendt organ, institut eller center, hvis dyrene sættes i karantæne under officiel kontrol og i overensstemmelse med myndighedernes instrukser, inden de indsættes i bestanden.
Når det gælder aber (simiae og prosimiae), skal karantænekravene i OIE-sundhedskodeksen (kapitel 2.10.1 og tillæg 3.5.1) overholdes.
Når det gælder alle andre dyr, der sættes i karantæne i henhold til punkt 2, litra b), skal karantæneperioden være på mindst 30 dage i forbindelse med de sygdomme, der er nævnt i bilag A.
4) Dyr, der holdes af et godkendt organ, institut eller center, må kun forlade dette, hvis det overføres til et andet godkendt organ, institut eller center i samme medlemsstat eller en anden medlemsstat. Skal de ikke overføres til et godkendt organ, institut eller center, må de kun forlade stedet, hvis de opfylder myndighedernes krav, så der ikke bliver risiko for eventuel sygdomsspredning.
5) Når en medlemsstat har krav på supplerende garantier i henhold til EF-bestemmelserne, kan den fastsætte supplerende krav og bestemmelser om udstedelse af certifikat for de modtagelige arter, der skal overføres til det godkendte organ, institut eller center.
6) Godkendelsen suspenderes helt eller delvis, trækkes tilbage eller fornyes efter følgende procedurer:
a) Finder myndighederne, at kravene i punkt 2 ikke er blevet opfyldt, eller at der er sket et ændring, som ikke længere er omfattet af artikel 2 i dette direktiv, suspenderes eller trækkes godkendelsen tilbage.
b) Ved anmeldelse af mistanke om en af sygdommene i bilag A eller B, suspenderer myndighederne godkendelsen af organet, instituttet eller centret, indtil mistanken er officielt afkræftet. Afhængig af, hvilken sygdom det drejer sig om, og risikoen for overførsel af sygdommen kan suspensionen vedrøre hele etablissementet eller kun visse dyrekategorier, der er modtagelige for den pågældende sygdom. Myndighederne sikrer sig, at der træffes de nødvendige foranstaltninger til at bekræfte eller afkræfte mistanken og til at undgå spredning af sygdommen i overensstemmelse med EF-bestemmelserne om foranstaltninger, der skal træffes vedrørende den pågældende sygdom og handelen med dyr.
c) Når den sygdom, der er mistanke om, bekræftes, godkendes organet, instituttet eller centret først igen, når betingelserne i punkt 1 i dette bilag, bortset fra punkt 1, litra c), atter er opfyldt efter udryddelse af sygdommen og infektionskilderne på stedet, herunder rengøring og desinfektion.
d) Myndighederne underretter Kommissionen om suspensionen, tilbagetrækningen eller fornyelsen af godkendelsen af et organ, institut eller center.
▼C2
BILAG D
▼M1
KAPITEL I
I. Betingelser for godkendelse af sædopsamlingsstationer
Sædopsamlingsstationer skal:
1) være under tilsyn af sædopsamlingsstationens dyrlæge
2) mindst have
a) aflåselige faciliteter til opstaldning og, hvis det er påkrævet til heste, et motionsareal, som er fysisk adskilt fra opsamlingsfaciliteterne, behandlings- og opbevaringsrummene
b) isolationsfaciliteter, der ikke står i direkte forbindelse med de normale faciliteter til opstaldning
c) sædopsamlingsfaciliteter, herunder et særskilt rum til rengøring og decinficering eller sterilisering af udstyr
d) et sædbehandlingsrum, der er adskilt fra opsamlingsfaciliteterne, og som ikke nødvendigvis skal befinde sig samme sted
e) et sædopbevaringsrum, som ikke nødvendigvis skal befinde sig samme sted
3) være bygget eller isoleret på en sådan måde, at enhver kontakt med dyr uden for undgås
4) være bygget således, at hele stationen, bortset fra kontorlokalerne og, når det gælder dyr af hestefamilien, motionsarealet, let kan rengøres og desinficeres.
II. Betingelser for tilsyn med sædopsamlingsstationer
For så vidt angår sædopsamlingsstationer,
1) skal der føres tilsyn med, at de kun holder dyr af de arter, hvis sæd skal opsamles;
der kan dog indsættes andre husdyr, hvis de ikke udgør nogen smittefare for de arter,
hvis sæd skal opsamles, og de opfylder de betingelser, der er fastsat af sædopsamlingsstationens dyrlæge; hvis opsamlingsstationen, når det gælder heste, ligger samme sted som en station for kunstig sædoverføring eller bedækning, må hopper, prøvehingste og hingste til bedækning kun indsættes, hvis de opfylder kravene i bilag D, kapitel II, punkt A. 1, 2, 3 og 4
2) skal det kontrolleres, at der føres et register over:
— art, race, fødselsdato og identifikation af hvert dyr, der befinder sig på stationen
— eventuel flytning af dyr, der indsættes på eller forlader stationen
— dyrenes sygehistorie og alle diagnostiske prøver og resultaterne heraf samt behandlinger og vaccinationer
— dato for opsamling og behandling af sæd
— sædens bestemmelsessted
3) skal en embedsdyrlæge i avlssæsonen mindst én gang om året, når det gælder dyr i sæsonavl, og ellers to gange om året aflægge kontrolbesøg for at tage stilling til og efterprøve alle forhold i forbindelse med godkendelses- og tilsynsbetingelserne
4) der føres tilsyn med, at uvedkommende ikke får adgang til stationen; besøg kan endvidere finde sted efter tilladelse fra tyrestationens dyrlæge
5) skal stationerne have et kompetent personale, der har den relevante uddannelse i desinfektions- og hygiejneteknik med henblik på forebyggelse af sygdomsspredning
6) skal der føres tilsyn for at sikre,
— at ingen af dyrene på stationen anvendes til bedækning mindst 30 dage inden den første sædopsamling og i opsamlingsperioden
— at opsamling, behandling og opbevaring af sæd kun finder sted i rum, der er afsat til disse formål
— at alle utensilier, der kommer i kontakt med sæden eller donordyret under opsamling eller behandling, desinficeres eller steriliseres ordentligt inden brugen eller er nye engangsutensilier, der kasseres efter brugen
— hvis opsamlingsstationen, når det gælder dyr af hestefamilien, ligger samme sted som en station for kunstig sædoverføring eller bedækning, skal der være skarp adskillelse mellem instrumenter og udstyr til kunstig sædoverføring eller bedækning og instrumenter og udstyr, der kommer i kontakt med donordyr eller andre dyr på opsamlingsstationen, og sæden
— at produkter af animalsk oprindelse såsom fortyndingsmidler, tilsætningsstoffer eller fyldstoffer, der anvendes ved behandling af sæden, ikke udgør nogen smittefare eller forinden har undergået en behandling, således at smittefare elimineres
— at der, når det gælder frossen eller kølet sæd, anvendes kryogene stoffer, som ikke tidligere har været anvendt til andre produkter af animalsk oprindelse
— at beholdere til opbevaring eller transport af sæd desinficeres eller steriliseres inden brugen eller er nye engangsbeholdere, der kasseres efter brugen
7) skal det sikres, at hver portion sæd er forsynet med uudslettelig mærkning, således at oprindelsesmedlemsstat, opsamlingsdato, donordyrets art, race og identitet og navnet og/eller nummeret på den godkendte station, der har opsamlet sæden, kan fastslås.
▼C2
KAPITEL II
Krav, der skal være opfyldt på sædopsamlingsstationer
Krav i forbindelse med indsættelse af donorhandyr
▼M1
A. HINGSTE
Der må til opsamling af sæd kun benyttes hingste, for hvis vedkommende stationens dyrlæge finder det godtgjort, at følgende krav er opfyldt:
1) de må ikke udvise nogen tegn på infektiøse eller kontagiøse sygdomme på indsættelsestidspunktet og den dag, hvor sæden opsamles
2) de skal komme fra en medlemsstats eller et tredjelands område eller, hvis der er tale om regionalisering, fra en del af en medlemsstats eller et tredjelands område og fra en bedrift under veterinærtilsyn, og områder og bedrifter skal opfylde kravene i Rådets direktiv 90/426/EØF
3) de skal i 30 dage inden sædopsamlingen have opholdt sig på bedrifter, hvor ingen dyr af hestefamilien har vist kliniske tegn på equin viral arteritis i den pågældende periode
4) de skal i 60 dage inden sædopsamlingen have opholdt sig på bedrifter, hvor ingen dyr af hestefamilien har vist kliniske tegn på kontagiøs equin metritis i den pågældende periode
5) de må ikke have været anvendt til bedækning i 30 dage inden den første sædopsamling og i opsamlingsperioden
6) de skal underkastes følgende prøver, der gennemføres og attesteres i et laboratorium, som er anerkendt af den kompetente myndighed i henhold til programmet i punkt 7:
i) en agargelimmunodiffusionsprøve (Coggins test) for equin infektiøs anæmi med negativt resultat
ii) enten en serumneutralisationsprøve for equin viral arteritis med negativt resultat ved en serumfortynding på 1: 4 eller en virusisolationsprøve for equin viral arteritis, der er udført med negativt resultat på en aliquot af hele donorhingstens sæd
iii) en prøve for kontagiøs equin metritis, der er udført ved to lejligheder med syv dages mellemrum ved isolering af Taylorella equigenitalis fra præejakulationsvæske eller en sædprøve og fra genitalsvaberprøver, der mindst er taget fra den urethrale fossa, herunder den urethrale sinus, og penis, herunder fossa glandis, med negativt resultat i hvert enkelt tilfælde
7) de skal have været underkastet et af følgende prøveprogrammer:
i) når der indsamles sæd med henblik på handel med frisk eller kølet sæd:
— og donorhingsten til stadighed opholder sig på opsamlingsstationen i mindst 30 dage inden første sædopsamling og i opsamlingsperioden, og ingen dyr af hestefamilien på opsamlingsstationen kommer i direkte kontakt med dyr af hestefamilien med lavere sundhedsstatus end donorhingsten, gennemføres de i punkt 6 nr. i), ii) og iii) krævede prøver mindst 14 dage efter påbegyndelsen af den ovennævnte periode og mindst en gang om året ved avlssæsonens begyndelse
— og donorhingsten ikke til stadighed opholder sig på opsamlingsstationen, og/eller andre dyr af hestefamilien på opsamlingsstationen kommer i direkte kontakt med dyr af hestefamilien med lavere sundhedsstatus, gennemføres de i punkt 6 nr. i), ii) og iii) krævede prøver senest 14 dage inden første sædopsamling og mindst en gang om året ved avlssæsonens begyndelse. Desuden gentages den i punkt 6 nr. i) krævede prøve med højst 120 dages mellemrum i sædopsamlingsperioden. Den i punkt 6 nr. ii) krævede prøve gennemføres senest 30 dage inden hver sædopsamling, medmindre det ved en virusisolationsprøve, der gennemføres en gang om året, bekræftes, at en hingst, der er seropositiv over for equin viral arteritis, ikke er virusudskiller
ii) når der opsamles sæd med henblik på handel med frosset sæd, anvendes prøveprogrammerne i punkt 7 nr. i), første og andet led, eller alternativt gennemføres de i punkt 6 nr. i), ii) og iii) krævede prøver i løbet af den obligatoriske sædopbevaringsperiode på 30 dage og senest 14 dage efter opsamlingen af sæden uanset hingstens status med hensyn til opholdet på opsamlingsstationen.
▼C2
B. FÅR OG GEDER
1. Kun får og geder på stationer eller bedrifter, som til embedsdyrlægens tilfredshed opfylder følgende krav, må anvendes til opsamling af sæd:
a) de skal være sunde og raske på opsamlingsdagen
b) de skal opfylde betingelserne i artikel 4, 5 og 6, i direktiv 91 /68/EØF om samhandel inden for Fællesskabet.
Donordyrene skal desuden i løbet af de 30 dage, der går forud for sædopsamlingen, underkastes følgende prøver med negativt resultat:
— en undersøgelse for brucellose (Brucella melitentis) i overensstemmelse med bilag C til direktiv 91/68/EØF
— en undersøgelse for smitsom epididymitis hos væddere (Brucella ovis) i overensstemmelse med bilag D til direktiv 91/68/EØF
— en virusisolationsundersøgelse for Border disease
c) dyrene skal have været underkastet de nødvendige prøver og den nødvendige kontrol til sikring af, at kravene i litra a) og b) er overholdt.
2. Undersøgelserne i punkt 1 skal foretages af et laboratorium, som medlemsstaten har godkendt.
▼M1
C. Hvis en af prøverne i afsnit A eller B er positiv, skal dyret isoleres, og den sæd, som er opsamlet fra det efter den seneste negative prøve, må ikke omsættes. Det samme gælder den sæd, der er opsamlet fra de andre dyr på bedriften eller opsamlingsstationen siden datoen for den positive prøve. Samhandelen må først genoptages, når sundhedsstatus er genoprettet.
▼M1
KAPITEL III
Krav gældende for sæd, æg og embryoner
Sæd, æg og embryoner skal være opsamlet, behandlet og konserveret efter følgende principper:
a) Vask af æg og embryoner skal, også for hestes vedkommende, foregå i henhold til betingelser, der skal fastsættes efter proceduren i artikel 26. Indtil disse betingelser er vedtaget, er internationale normer gældende.
Ægs og embryoners zona pellucida skal være intakt før og efter vask.
Kun æg og embryoner fra samme donor må vaskes samtidig.
Efter vask skal hele overfladen på hvert ægs eller embryons zona pellucida undersøges i en forstørrelse på mindst 50 gange og garanteres intakt og fri for vedhængende materiale.
b) De medier og væsker, der anvendes ved opsamling, behandling (undersøgelse, vask m.v.), konservering eller frysning af æg og embryoner, skal steriliseres efter godkendte metoder og håndteres således, at de forbliver sterile.
Der skal tilsættes antibiotika til opsamlings-, vaske- og konserveringsmedier, når det gælder æg og embryoner, og til fortyndingsmidler, når det gælder sæd.
Om nødvendigt fastsættes de nærmere regler efter proceduren i artikel 26.
c) Alle materialer, der anvendes til opsamling, behandling, konservering eller frysning af sæd, æg og embryoner, skal desinficeres eller steriliseres inden brugen, eller der skal anvendes nye engangsmaterialer, der kasseres efter brugen.
d) Der kan fastlægges supplerende prøver efter proceduren i artikel 26, især med hensyn til væskerne til opsamling eller vask, for at fastslå, at de ikke indeholder patogener.
e) Æg og embryoner, der har bestået den i litra a) fastsatte undersøgelse, samt sæd skal anbringes i sterile beholdere, som er behørigt identificeret, kun indeholder produkter fra samme donor og straks forsegles.
Identifikationen, der skal fastlægges efter proceduren i artikel 26, skal sikre, at mindst oprindelseslandet, opsamlingsdatoen, donordyrets art, race og identitet og navnet og/eller nummeret på opsamlingsstationen/-holdet kan fastslås.
f) Sæd, æg og embryoner, der er frosset, skal anbringes i sterile beholdere med flydende kvælstof, som ikke frembyder nogen risiko for kontamination af produktet.
g) Sæd, æg og embryoner, der er frosset, skal opbevares under godkendte forhold i en periode på mindst 30 dage før afsendelse.
h) Sæd, æg og embryoner skal transporteres i beholdere, der er blevet rengjort, desinficeret eller steriliseret inden brugen eller er nye engangsbeholdere, der kasseres efter brugen.
KAPITEL IV
Hundonordyr
Hundyr må kun anvendes til opsamling af embryoner og æg, hvis embedsdyrlægen finder det godtgjort, at de og de besætninger, som de stammer fra, opfylder kravene i de relevante direktiver vedrørende samhandelen inden for Fællesskabet med levende avls- og brugsdyr af de pågældende arter.
Bestemmelserne i Rådets direktiv 64/432/EØF gælder for svin, og bestemmelserne i Rådets direktiv 91/68/EØF gælder for får og geder.
Ud over de krav, der er fastsat ved Rådets direktiv 90/426/EØF, gælder det, at dyr af hestefamilien inden opsamlingen af æg eller embryoner skal have opholdt sig på bedrifter, hvor der ikke har været kliniske tegn på kontagiøs equin metritis i 60 dage. De må ikke anvendes til naturlig bedækning i de sidste 30 dage inden opsamlingen af æg eller embryoner.
▼M3
BILAG E
Del 1


Del 2
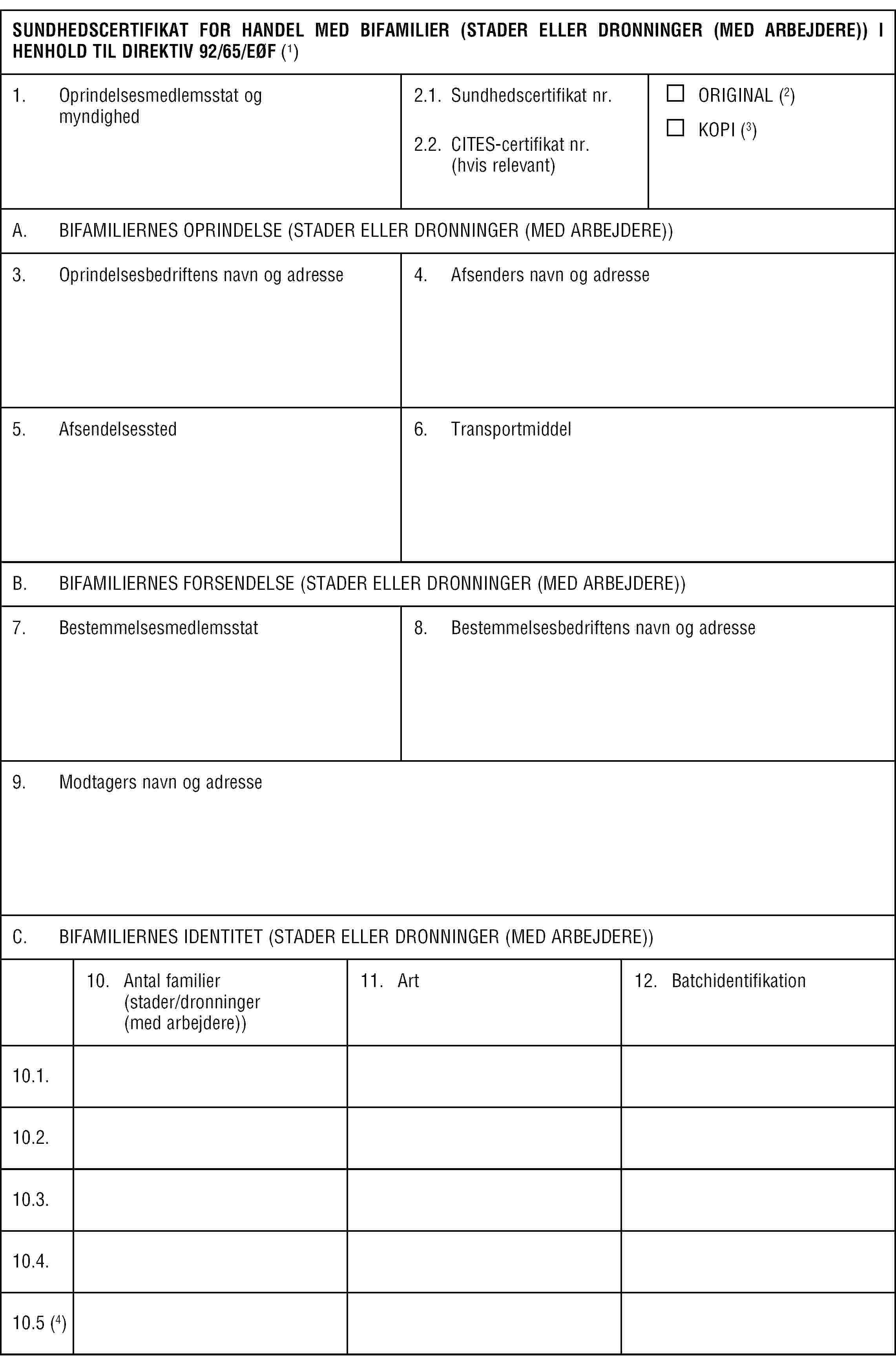

Del 3
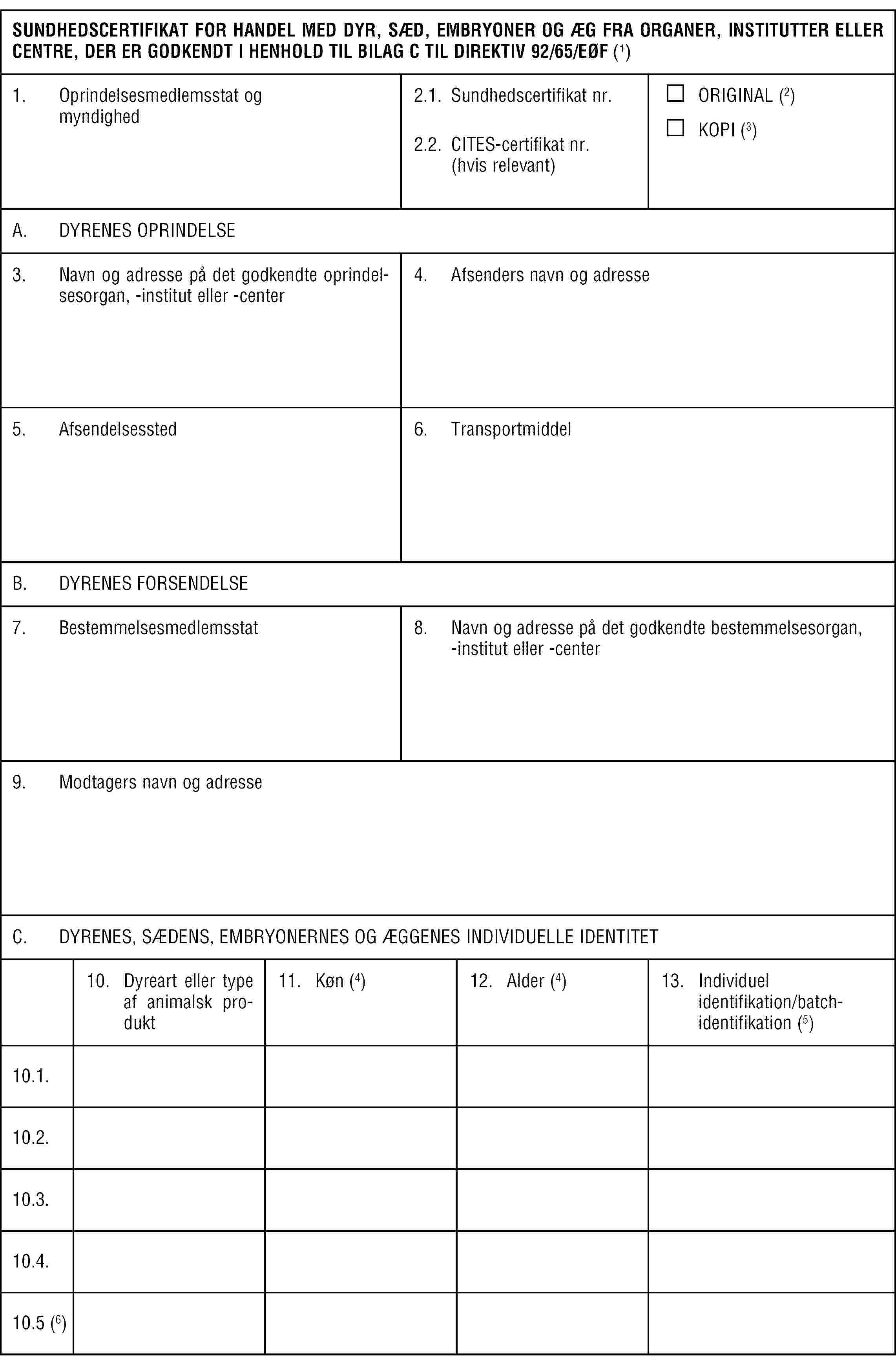

▼M7
BILAG F
Rådets direktiv 64/432/EØF af 26. juni 1964 om veterinærpolitimæssige problemer ved handelen inden for Fællesskabet med kvæg og svin
Rådets direktiv 88/407/EØF af 14. juni 1988 om fastsættelse af de veterinærpolitimæssige krav i forbindelse med handelen inden for Fællesskabet med frosset tyresæd og indførsel heraf
Rådets direktiv 89/556/EØF af 25. september 1989 om fastsættelse af veterinærpolitimæssige betingelser i forbindelse med handel inden for Fællesskabet med embryoner af tamkvæg samt med indførsel heraf fra tredjelande
Direktiv 90/426/EØF af 26. juni 1990 om dyresundhedsmæssige betingelser for enhovede dyrs bevægelser og indførsel af enhovede dyr fra tredjelande
Rådets direktiv 90/429/EØF af 26. juni 1990 om fastsættelse af de dyresundhedsmæssige krav i forbindelse med handelen inden for Fællesskabet med ornesæd og indførsel heraf
Rådets direktiv 90/539/EØF af 15. oktober 1990 om dyresundhedsmæssige betingelser for samhandelen inden for Fællesskabet med fjerkræ og rugeæg samt indførsel heraf fra tredjelande
Rådets direktiv 91/67/EØF af 28. januar 1991 om dyresundhedsmæssige betingelser for afsætning af akvakulturdyr og -produkter
Rådets direktiv 91/68/EØF af 28. januar 1991 om dyresundhedsmæssige betingelser for samhandelen med får og geder inden for Fællesskabet
Rådets direktiv 2004/68/EF af 26. april 2004 om dyresundhedsbestemmelser for import til Fællesskabet af visse levende hovdyr og om ændring af direktiv 90/426/EØF og 92/65/EØF.






