EUR-Lex Access to European Union law

This document is an excerpt from the EUR-Lex website
Document 32010R0206
Commission Regulation (EU) No 206/2010 of 12 March 2010 laying down lists of third countries, territories or parts thereof authorised for the introduction into the European Union of certain animals and fresh meat and the veterinary certification requirements (Text with EEA relevance)
Регламент (EC) № 206/2010 на Комисията от 12 март 2010 година за установяване на списъци на трети страни, територии или части от тях, от които е разрешен вносът в Европейския съюз на някои животни и прясно месо и за определяне на изискванията за ветеринарното сертифициране (текст от значение за ЕИП)
Регламент (EC) № 206/2010 на Комисията от 12 март 2010 година за установяване на списъци на трети страни, територии или части от тях, от които е разрешен вносът в Европейския съюз на някои животни и прясно месо и за определяне на изискванията за ветеринарното сертифициране (текст от значение за ЕИП)
OJ L 73, 20.3.2010, p. 1–121
(BG, ES, CS, DA, DE, ET, EL, EN, FR, IT, LV, LT, HU, MT, NL, PL, PT, RO, SK, SL, FI, SV)
Special edition in Croatian: Chapter 03 Volume 046 P. 93 - 213
 No longer in force, Date of end of validity: 20/04/2021; отменен от 32020R0692
No longer in force, Date of end of validity: 20/04/2021; отменен от 32020R0692
- Date of document:
- 12/03/2010
- Date of effect:
- 09/04/2010; влизане в сила дата на публикуване + 20 виж член 21
- Date of end of validity:
- 20/04/2021; отменен от 32020R0692
- Author:
- Европейска комисия
- Form:
- Регламент
- Additional information:
- отнася се за ЕИП
- Treaty:
- Договор за функционирането на Европейския съюз
- Legal basis:
-
- 31992L0065 - A17P2PTB) 31992L0065 - A17P3PTA) 31992L0065 - A17P3PTC)L1 31992L0065 - A18P1TIRE4 31992L0065 - A19
- 32002L0099 - A08 32002L0099 - A09P2PTB) 32002L0099 - A09P4
- 32004L0068 - A03P1L1 32004L0068 - A03P1L2 32004L0068 - A06P1L1 32004L0068 - A07PTE) 32004L0068 - A08 32004L0068 - A10L1 32004L0068 - A13P1
- 32004R0852 - A12
- 32004R0853 - A09
- 32004R0854 - A11P1 32004R0854 - A16
- 32004R0882 - A48P1
- Link
- Link
- Link
- Select all documents mentioning this document No data available in the table
- Modifies:
-
Relation Act Comment Subdivision concerned From To Repeal 32003D0881 Implicit repeal 32005D0060 09/04/2010
No data available in the table
- Modified by:
-
Relation Act Comment Subdivision concerned From To Corrected by 32010R0206R(01) (BG, CS, DA, DE, EL, EN, ES, ET, FI, FR, HU, IT, LT, LV, MT, NL, PL, PT, RO, SK, SL, SV) Corrected by 32010R0206R(02) (CS) Corrected by 32010R0206R(03) (BG) Corrected by 32010R0206R(04) (FR) Corrected by 32010R0206R(05) (EL) Corrected by 32010R0206R(06) (SL) Modified by 32010R0810 заместване член 19 19/09/2010 Modified by 32010R0810 поправка приложение II 19/09/2010 Modified by 32010R0810 заместване приложение IV.1 19/09/2010 Modified by 32011R0144 поправка приложение II 10/03/2011 Modified by 32011R0144 поправка приложение I 10/03/2011 Modified by 32011R0342 заместване приложение II параграф 1 12/04/2011 Modified by 32011R0801 заместване приложение II.1 13/08/2011 Modified by 32011R1112 поправка приложение II параграф 1 05/11/2011 Modified by 32012R0497 поправка приложение I 03/07/2012 Modified by 32012R0546 поправка приложение I P. 1 16/07/2012 Modified by 32012R0546 поправка приложение II P. 1 16/07/2012 Addition 32012R0644 член 12 BIS 06/08/2012 Modified by 32012R0644 приложение I 06/08/2012 Modified by 32012R1036 поправка приложение II P1 28/11/2012 Modified by 32012R1160 поправка приложение I P. 2 28/12/2012 Modified by 32013R0071 поправка приложение II P.1 15/02/2013 Modified by 32013R0071 поправка приложение I P.2 15/02/2013 Modified by 32013R0102 поправка приложение I 25/02/2013 Modified by 32013R0191 заместване приложение II P2 PT II.3 26/03/2013 Modified by 32013R0196 поправка приложение II P. 1 28/03/2013 Modified by 32013R0482 поправка приложение II стр. 1 28/05/2013 Modified by 32013R0519 поправка приложение I P.I 01/07/2013 Modified by 32013R0519 поправка приложение II P.I 01/07/2013 Modified by 32013R0556 добавка член 17 BI 01/07/2013 Modified by 32013R0780 добавка член 3 BI 04/09/2013 Modified by 32013R0780 отменяне член 1.3 04/09/2013 Modified by 32013R0780 добавка член 3 TR 04/09/2013 Modified by 32013R0780 заместване член 8 точка B) 04/09/2013 Modified by 32013R0780 добавка член 13 BI 04/09/2013 Modified by 32013R0780 добавка приложение VI 04/09/2013 Modified by 32013R0780 заместване член 4 04/09/2013 Modified by 32013R0780 заместване член 11.1 04/09/2013 Modified by 32013R0780 добавка член 3 QT 04/09/2013 Replaced by 32013R0854 TXT приложение I P.2 25/09/2013 Replaced by 32013R1044 приложение IV P.2 15/11/2013 Derogated in 32014R0750 приложение I 2 12/07/2014 Derogated in 32014R0750 член 2 B 12/07/2014 Derogated in 32014R0750 приложение I 1 12/07/2014 Modified by 32014R1218 поправка приложение II P. 2 04/12/2014 Modified by 32014R1218 поправка приложение I P. 1 04/12/2014 Modified by 32014R1218 поправка приложение I P. 2 04/12/2014 Modified by 32015R0604 поправка приложение II 17/04/2015 Modified by 32015R0604 поправка приложение I 17/04/2015 Modified by 32015R0917 добавка приложение I стр. 1 17/06/2015 Modified by 32016R0535 добавка приложение II стр. 1 текст 26/04/2016 Modified by 32016R0535 добавка приложение II стр. 2 текст 26/04/2016 Modified by 32016R0922 заместване приложение II стр. 1 текст 01/07/2016 Modified by 32016R1248 заместване приложение II стр. 1 текст 18/08/2016 Modified by 32016R1832 заместване приложение II стр. 2 точка II.1.7 07/11/2016 Modified by 32017R0384 поправка приложение I стр. 1 текст 27/03/2017 Modified by 32017R0384 поправка приложение I стр. 2 текст 27/03/2017 Modified by 32017R0384 поправка приложение II стр. 1 текст 27/03/2017 Modified by 32017R0731 поправка приложение II стр. 2 01/07/2017 Modified by 32017R0731 поправка приложение I стр. 2 01/07/2017 Modified by 32019R0585 добавка приложение I част 1 текст Modified by 32019R0585 добавка приложение II част 1 текст Modified by 32019R1162 заместване приложение II част 1 текст 28/07/2019 Modified by 32019R1162 заместване приложение I част 1 текст 28/07/2019 Modified by 32019R1162 заместване приложение I част 2 текст 28/07/2019 Modified by 32019R1162 отменяне, анулиране приложение I част 1 текст 28/07/2019 Modified by 32019R1162 отменяне, анулиране приложение II част 1 текст 28/07/2019 Modified by 32019R1762 добавка приложение II част 1 текст Modified by 32019R1762 добавка приложение I част 1 текст Modified by 32019R2124 отменяне, анулиране член 17 параграф 2 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 12a параграф 1 буква (e) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17 параграф 1 буква (d) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 12a параграф 2 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17 параграф 3 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17a параграф 1 буква (c) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17 параграф 1 буква (c) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 12a параграф 1 буква (d) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 12a параграф 4 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17a параграф 2 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17a параграф 1 буква (d) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17 параграф 1 буква (b) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17a параграф 1 буква (b) 14/12/2019 Modified by 32019R2124 отменяне, анулиране член 17a параграф 3 14/12/2019 Modified by 32020R0386 отменяне, анулиране приложение II част 1 текст 30/03/2020 Repealed by 32020R0692 21/04/2021 Modified by 32020R2204 добавка приложение II част 1 текст 01/01/2021 Modified by 32020R2204 заместване приложение I част 1 текст 01/01/2021 Modified by 32020R2204 добавка приложение II част 1 FOOTNOTE 01/01/2021 Modified by 32020R2204 заместване приложение II част 2 текст 01/01/2021 Modified by 32020R2204 добавка приложение I част 1 текст 01/01/2021 Modified by 32020R2204 добавка приложение I част 1 FOOTNOTE 01/01/2021 - Instruments cited:
- Link
- EUROVOC descriptor:
- Subject matter:
- Directory code:
|
20.3.2010 |
BG |
Официален вестник на Европейския съюз |
L 73/1 |
РЕГЛАМЕНТ (EC) № 206/2010 НА КОМИСИЯТА
от 12 март 2010 година
за установяване на списъци на трети страни, територии или части от тях, от които е разрешен вносът в Европейския съюз на някои животни и прясно месо и за определяне на изискванията за ветеринарното сертифициране
(текст от значение за ЕИП)
ЕВРОПЕЙСКАТА КОМИСИЯ,
като взе предвид Договора за функционирането на Европейския съюз,
като взе предвид Директива 92/65/ЕИО на Съвета от 13 юли 1992 г. за определяне на ветеринарно-санитарните изисквания относно търговията и вноса в Общността на животни, сперма, яйцеклетки и ембриони, които не са предмет на ветеринарно-санитарните изисквания, определени в специалните правила на Общността, посочени в приложение А, раздел I към Директива 90/425/ЕИО (1), и по-специално член 17, параграф 2, буква б), член 17, параграф 3, буква а), член 17, параграф 3, буква в), първа алинея, член 18, параграф 1, четвърто тире и член 19 от нея,
като взе предвид Директива 2002/99/ЕО на Съвета от 16 декември 2002 г. относно установяване на ветеринарно-санитарни правила, регулиращи производството, преработката, разпространението и пускането на пазара на продукти от животински произход за консумация от човека (2), и по-специално член 8, член 9, параграф 2, буква б) и член 9, параграф 4 от нея,
като взе предвид Директива 2004/68/ЕО на Съвета от 26 април 2004 г. относно определяне на ветеринарно-санитарните правила за внос и транзит в Общността на някои живи копитни животни, за изменение на Директиви 90/426/ЕИО и 92/65/ЕИО и за отмяна на Директива 72/462/ЕИО (3), по-специално член 3, параграф 1, алинеи първа и втора, член 6, параграф 1, алинея първа, член 7, буква д), член 8, член 10, алинея първа и член 13, параграф 1 от нея,
като взе предвид Регламент (ЕО) № 852/2004 на Европейския парламент и на Съвета от 29 април 2004 г. относно хигиената на храните (4), и по-специално член 12 от него,
като взе предвид Регламент (ЕО) № 853/2004 на Европейския парламент и на Съвета от 29 април 2004 г. относно определяне на специфични хигиенни правила за храните от животински произход (5), и по-специално член 9 от него,
като взе предвид Регламент (EО) № 854/2004 на Европейския парламент и на Съвета от 29 април 2004 г. за определяне на специфичните правила за организирането на официален контрол върху продуктите от животински произход, предназначени за човешка консумация (6), и по-специално член 11, параграф 1 и член 16 от него,
като взе предвид Регламент (EО) № 882/2004 на Европейския парламент и на Съвета от 29 април 2004 г. относно официалния контрол, провеждан с цел осигуряване на проверка на съответствието със законодателството в областта на фуражите и храните и правилата за опазване здравето на животните и хуманното отношение към животните (7), и по-специално член 48, параграф 1 от него,
като има предвид, че:
|
(1) |
В Директива 72/462/ЕИО на Съвета от 12 декември 1972 г. относно проблемите при ветеринарно-санитарните проверки при вноса на животни от рода на говедата, овцете, козите и свинете, на прясно месо или месни продукти от трети страни (8) се предвижда да бъде съставен списък на страните или на части от тях, от които държавите-членки разрешават вноса на някои видове живи животни и на прясно месо от някои видове животни. |
|
(2) |
Съответно беше прието Решение 79/542/ЕИО на Съвета от 21 декември 1976 г. относно съставянето на списък на трети страни или на части от трети страни и относно определяне на ветеринарно-санитарните и здравните условия и ветеринарното сертифициране за внос в Общността на някои живи животни и прясно месо от тях (9). С посоченото решение се установяват санитарните условия за внос в Европейския съюз на живи животни, с изключение на еднокопитни, и за вноса на прясно месо от такива животни, включително месо от еднокопитни, но без месни заготовки. С приложения I и II към посоченото решение се установяват също и списъци на трети страни и на части от тях, от които могат да се внасят в Съюза някои видове живи животни и прясно месо от тях, както и образци на ветеринарни сертификати. |
|
(3) |
От датата на приемането на посоченото решение, в други актове на Съюза бяха въведени множество нови изисквания в областта на здравето на животните и на общественото здраве, които създават нова регулаторна рамка в тази област. Освен това, Директива 72/462/EИО бе отменена с Директива 2004/68/ЕО. |
|
(4) |
В член 20 от Директива 2004/68/ЕО се предвижда, че правилата за прилагане по отношение на вноса, определени в съответствие с решенията, приети съгласно Директива 72/462/ЕИО, inter alia Решение 79/542/ЕИО, остават в сила, докато не бъдат заменени с мерките, приети по силата на новата регулаторна рамка. |
|
(5) |
В съответствие с член 4, параграф 3 от Директива 2004/41/ЕО на Европейския парламент и на Съвета от 21 април 2004 г. за отмяна на някои директиви, отнасящи се до хигиената на храните и здравните условия при производството и пускането на пазара на някои продукти от животински произход, предназначени за консумация от човека, и за изменение на Директиви 89/662/ЕИО и 92/118/ЕИО на Съвета и на Решение 95/408/ЕО на Съвета (10), веднага щом необходимите разпоредби въз основа на Регламенти (ЕО) № 852/2004, (ЕО) № 853/2004, (ЕО) №854/2004 или на Директива 2002/99/ЕО бъдат приети, правилата за прилагане, приети въз основа на Директива 72/462/ЕИО, ще престанат да се прилагат. |
|
(6) |
Решение 79/542/ЕИО беше няколкократно изменяно и разпоредбите за вноса, основаващи се на новата регулаторна рамка, вече са включени в Решение 79/542/ЕИО. От съображения за яснота и прозрачност, мерките, които са предвидени в Решение 79/542/ЕИО, следва да бъдат включени в нов законов акт. Настоящият регламент включва всички разпоредби на Решение 79/542/ЕИО. Следователно, с влизането в сила на настоящия регламент Решение 79/542/ЕИО губи сила и поради това престава да се прилага, като предстои изрично да бъде отменено. |
|
(7) |
В Директива 92/65/ЕИО се определят ветеринарно-санитарните изисквания относно търговията и вноса в Съюза на животни, сперма, яйцеклетки и ембриони, които не са предмет на ветеринарно-санитарните изисквания, определени в конкретните актове на Съюза, цитирани в приложение Е към посочената директива. Съгласно посочената директива, въпросните живи животни, сперма, яйцеклетки и ембриони могат да се внасят в Съюза само от трета страна, която е включена в списъка, съставен в съответствие с процедурата, описана в посочената директива. Освен това подобни живи животни следва да бъдат придружени от здравен сертификат, който отговаря на образеца, съставен в съответствие с горепосочената процедура. |
|
(8) |
В Директива 96/93/ЕО на Съвета от 17 декември 1996 г. относно сертифицирането на животни и животински продукти (11) се определят правилата, които трябва да бъдат спазвани при издаването на ветеринарни сертификати, изисквани от ветеринарното законодателство за предотвратяване на заблуди и измами при сертифицирането. Целесъобразно е да се гарантира, че официалните инспектори или ветеринарните лекари от трети страни прилагат правила и принципи, които са най-малкото еквивалентни на предвидените в посочената директива. Някои трети страни, изброени в приложение II към настоящия регламент, предоставиха достатъчни гаранции за наличието и прилагането на подобни правила и принципи. Поради това е подходящо да се разреши въвеждането на някои видове живи животни от посочените трети страни в Съюза, при условие, че специфичната санитарна ситуация в тях не налага допълнителни ограничения. |
|
(9) |
С Директива 2002/99/ЕО се установяват ветеринарно-санитарни правила относно въвеждането в Съюза от трети страни на продукти от животински произход и на предназначени за консумация от човека продукти, получени от тях. В съответствие с посочената директива, трябва да бъдат съставени списъци на третите страни или на регионите от трети страни, от които е разрешен вносът на определени продукти от животински произход и този внос трябва да отговаря на определени изисквания на ветеринарното сертифициране. |
|
(10) |
В Директива 2004/68/ЕО са определени ветеринарно-санитарните правила за внос и транзит в Съюза на някои живи копитни животни. Вносът на посочените живи копитни животни и транзитът им в Съюза са разрешени единствено от трети страни и територии, които присъстват в списъка или списъците, съставени в съответствие с процедурата, описана в посочената директива, а въпросният внос трябва да отговаря на определени изисквания на ветеринарното сертифициране |
|
(11) |
Освен разпоредбите на член 17, параграф 2, последна алинея от Директива 92/65/ЕО, живи животни и продукти от животински произход, по отношение на които са приложими Директиви 92/65/ЕО, 2002/99/ЕО и 2004/68/ЕО, трябва да се внасят в Съюза или да преминават транзитно през нея само ако са придружени от ветеринарен сертификат и ако отговарят на съответните изисквания, посочени в законодателството на Съюза. |
|
(12) |
С оглед на гореизложеното за прилагането на директиви 92/65/ЕИО, 2002/99/ЕО и 2004/68/ЕО е целесъобразно в настоящия регламент да се включат списъци на трети страни, територии и части от тях и да се предвидят специфични условия за внос, в това число и образци на ветеринарни сертификати за някои видове живи животни и прясно месо от някои видове живи животни. |
|
(13) |
В интерес на последователността на законодателството на Съюза в настоящия регламент следва също така да се отчетат и изискванията в областта на общественото здраве, залегнали в други актове на ЕС и по-специално в Регламенти (ЕО) № № 852/2004, 853/2004 и 854/2004, в които са установени правила относно хигиената на хранителните продукти и храните от животински произход и правила за организирането на официален контрол върху продуктите от животински произход, предназначени за консумация от човека, както и изискванията на Директива 96/23/ЕО на Съвета от 29 април 1996 г. относно мерките за наблюдение на определени вещества и остатъци от тях в живи животни и животински продукти (12) и тези на Регламент (ЕО) № 999/2001 на Европейския парламент и на Съвета от 22 май 2001 г. относно определяне на правила за превенция, контрол и ликвидиране на някои трансмисивни спонгиформни енцефалопатии (13). |
|
(14) |
В Регламент (ЕО) № 882/2004 се установяват общи правила относно официалния контрол, провеждан в областта на фуражите и храните, и правилата за опазване здравето на животните и хуманното отношение към животните. Член 48 от него оправомощава Комисията да приема списък на трети страни, от които е разрешен вносът на специфични продукти в Съюза. В Регламент (ЕО) № 854/2004 се определят специфични правила за организирането на официален контрол върху продуктите от животински произход, предназначени за консумация от човека, в това число изготвяне на списъци с трети страни, от които е разрешен вносът на продукти от животински произход. Посочените правила предвиждат, че списъкът може да бъде комбиниран с други списъци, изготвени за целите на общественото здраве и здравето на животните. |
|
(15) |
Поради това образците на сертификати, установени в приложенията към настоящия регламент, следва да включват удостоверения за това, че са изпълнени изискванията във връзка с общественото здраве, посочени в Директива 96/23/ЕО и регламенти (ЕО) № № 999/2001, 852/2004, 853/2004 и 854/2004. |
|
(16) |
Образците на сертификати, установени в приложенията към настоящия регламент, следва също така да включват удостоверения за това, че са изпълнени изискванията във връзка с хуманното отношение към животните, посочени в Директива 93/119/ЕО на Съвета от 22 декември 1993 г. относно защитата на животните по време на клане или умъртвяване (14) и Регламент (ЕО) № 1/2005 на Съвета от 22 декември 2004 г. относно защитата на животните по време на транспортиране и свързаните с това операции (15). |
|
(17) |
За да се гарантира, че здравето на живите животни, въведени в Съюза, не е застрашено по време на транспортирането им от третата страна на произход към Съюза, следва да се установят определени изисквания във връзка с транспорта на живи животни, включително изисквания относно събирателните центрове. |
|
(18) |
В интерес на осигуряването на защитата на здравето на животните в Съюза, живите животни следва да бъдат превозвани директно до тяхното местоназначение в Съюза. |
|
(19) |
Прясното месо, въведено в Съюза за транзит към друга трета страна, създава пренебрежим риск за общественото здраве. Такова месо все пак следва да съответства на всички приложими ветеринарно-санитарни изисквания. Поради това следва да се определят съответни специфични разпоредби във връзка с транзита на прясното месо и с неговото съхраняване преди транзита. |
|
(20) |
Поради географското положение на Калининград, засягащо единствено Латвия, Литва и Полша, за транзита през Съюза на пратки от и към Русия следва да бъдат предвидени специални условия. |
|
(21) |
Следва да се разреши въвеждането в Съюза на пратки прясно месо, с изключение на карантия и мляно месо, от отгледани в стопанства дивечови животни от разред Чифтокопитни, произхождащи от уловени диви животни. С цел да се изключи всякакъв възможен риск за здравето на животните, който може да се създаде с подобно въвеждане, е целесъобразно посочените животни да бъдат отделени от дивите животни за период от три месеца преди въвеждането в Съюза на подобни пратки. Съответно, това обстоятелство следва да бъде взето предвид в образеца на ветеринарен сертификат за такива пратки (RUF). |
|
(22) |
В Решение 2003/881/ЕО на Комисията от 11 декември 2003 г. относно ветеринарно-санитарните условия и изискванията за издаване на сертификати за внос на пчели (Apis mellifera и Bombus spp.) от някои трети страни (16) се определят ветеринарно-санитарните условия и изискванията за издаване на сертификати за внос на пчели от някои трети страни. В интерес на опростяването на законодателството на Съюза, мерките, установени в посоченото Решение, следва да бъдат включени в настоящия Регламент. Следователно Решение 2003/881/ЕО следва да бъде отменено. |
|
(23) |
Целесъобразно е да се определи преходен период, за да се позволи на държавите-членки и индустрията да предприемат необходимите мерки, за да се съобразят с изискванията, установени с настоящия регламент. |
|
(24) |
Мерките, предвидени в настоящия регламент, са в съответствие със становището на Постоянния комитет по хранителната верига и здравето на животните, |
ПРИЕ НАСТОЯЩИЯ РЕГЛАМЕНТ:
ГЛАВА I
ПРЕДМЕТ, ОБХВАТ И ОПРЕДЕЛЕНИЯ
Член 1
Предмет и обхват
1. С настоящия регламент се установяват изискванията за ветеринарно сертифициране при въвеждане в Съюза на пратки, които съдържат следните видове живи животни или прясно месо:
|
а) |
копитни животни; |
|
б) |
животните, посочени в списъка в част 2 от приложение IV; |
|
в) |
прясно месо, предназначено за консумация от човека, с изключение на месни заготовки от копитни и еднокопитни. |
2. С настоящия регламент се създават списъци на трети страни, територии или части от тях, от които е разрешено въвеждането в Съюза на пратките, посочени в параграф 1.
3. Настоящият регламент не се прилага по отношение на въвеждането в Съюза на дивечови животни:
|
а) |
за спектакли или изложби, където подобни живи животни не се държат или отглеждат обичайно; |
|
б) |
които участват в циркови трупи; |
|
в) |
предназначени за одобрен орган, институт или център, съгласно определението в член 2, параграф 1, буква в) от Директива 92/65/ЕИО. |
4. Настоящият регламент се прилага, без да се засягат каквито и да било други специфични изисквания, установени в други актове на Съюза или в споразумения, сключени между Съюза и трети страни.
Член 2
Определения
За целите на настоящия регламент се прилагат следните определения:
|
а) |
„копитни животни“ означава копитни животни, така както са определени в член 2, буква г) от Директива 2004/68/ЕО; |
|
б) |
„прясно месо“ означава прясно месо, така, както е определено в точка 1.10 от приложение I към Регламент (ЕО) № 853/2004; |
|
в) |
„еднокопитни животни“ означава еднокопитни животни, така както са определени в член 2, буква б) от Директива 90/426/ЕИО (17) на Съвета; |
|
г) |
„стопанство“ означава ферма или друго официално контролирано селскостопанско, промишлено или търговско предприятие, включително зоологически градини, увеселителни паркове и резервати за диви животни или ловни резервати, където обичайно се държат и отглеждат живи животни. |
ГЛАВА II
УСЛОВИЯ ЗА ВЪВЕЖДАНЕТО НА ЖИВИ ЖИВОТНИ В СЪЮЗА
Член 3
Общи условия за въвеждането на копитни животни в Съюза
Пратки от копитни животни се въвеждат в Съюза само ако отговарят на следните условия:
|
а) |
те са с произход от някоя от изброените в графи 1, 2 и 3 на таблицата в част 1 от приложение I трети страни, територии или части от тях, за които има отговарящ на въпросната пратка образец на ветеринарен сертификат, вписан в графа 4 на таблицата в част 1 от приложение I; |
|
б) |
те са придружени от съответен ветеринарен сертификат, съставен в съответствие с подходящия образец на ветеринарен сертификат, установен в част 2 на приложение I, като се отчитат специфичните условия, посочени в графа 6 от таблицата в част 1 от посоченото приложение, попълнен и подписан от официален ветеринарен лекар в третата страна износител; |
|
в) |
те удовлетворяват изискванията, установени във ветеринарния сертификат, посочен в буква б), в това число:
|
Член 4
Условия относно събирателните центрове за някои пратки копитни животни
Пратки от копитни животни, съставени от живи животни от повече от едно стопанство, се въвеждат в Съюза само ако са събрани в събирателни центрове, одобрени от компетентния орган на третата страна на произход в съответствие с изискванията, установени в част 5 от приложение I.
Член 5
Протоколи за стандартизация на материали и процедури за вземане на проби от копитни животни и изследването им
В случаите, когато ветеринарните сертификати, вписани в графа 4 от таблицата в част 1 от приложение I, съдържат изискване за вземане на проби и изследване за болестите, изброени в част 6 от посоченото приложение, с оглед на въвеждането в Съюза на пратки копитни животни, такива вземания на проби и изследвания се провеждат от компетентния орган на третата страна на произход или под негов контрол в съответствие с протоколите за стандартизация на материалите и процедурите за вземането на проби и изследванията, установени в част 6 от посоченото приложение.
Член 6
Специални условия за определени пратки копитни животни, внесени в Сен Пиер и Микелон и въведени в Съюза
Пратки от копитни животни от видовете, изброени в таблицата в част 7 от приложение I, които са били въведени в Сен Пиер и Микелон преди по-малко от шест месеца от датата на изпращане от Сен Пиер и Микелон към Съюза, се въвеждат в Съюза само ако:
|
а) |
животните удовлетворяват изискванията по отношение на престоя и карантината, установени в глава 1 от посочената част; |
|
б) |
животните са били подложени на изследване в съответствие с изискванията по отношение ветеринарно-санитарните изследвания, установени в глава 2 от посочената част. |
Член 7
Общи условия за въвеждането на определени видове пчели в Съюза
1. Пратки от пчели от видовете, изброени в таблица 1 на част 2 от приложение IV, се въвеждат в Съюза само от трети страни или територии:
|
а) |
изброени в списъка в част 1 от приложение II; |
|
б) |
в които наличието на американски гнилец, малък кошерен бръмбар (Aethina tumida) и кошерен акар Tropilaelaps (Tropilaelaps spp.) е предмет на задължително съобщаване по територията на цялата засегната трета страна или територия. |
2. Чрез дерогация от параграф 1, буква а), пратки от пчели могат да бъдат въвеждани в Съюза от част от трета страна или територия, изброени в част 1 от приложение II, която е:
|
а) |
географски и епидемиологично изолирана част от третата страна или територия |
|
б) |
посочена в третата графа на таблицата в раздел 1 на част 1 от приложение IV. |
Когато е приложена посочената дерогация, въвеждането в Съюза на пратки пчели от всички други части на засегнатата трета страна или територия, невключени в третата графа от таблицата в раздел 1 на част 1 от приложение IV, се забранява.
3. Пратките пчели от видовете, изброени в таблица 1 на част 2 от приложение IV се състоят от:
|
а) |
клетки с пчелни майки (Apis mellifera и Bombus spp.), всяка от които съдържа само една пчелна майка и най-много 20 придружаващи пчели работнички; или |
|
б) |
контейнери със земни пчели (Bombus spp.), всеки от които съдържа колония от най-много 200 възрастни земни пчели. |
4. Пратките пчели от видовете, изброени в таблица 1 на част 2 от приложение IV:
|
а) |
се придружават от съответния ветеринарен сертификат, съставен в съответствие с подходящия образец на ветеринарен сертификат, определен в част 2 от приложение IV, попълнен и подписан от официален инспектор от третата страна износител; |
|
б) |
съответстват на ветеринарно-санитарните изисквания, установени във ветеринарния сертификат, посочен в буква а). |
Член 8
Общи условия по отношение на транспортирането на живи животни към Съюза
В периода между натоварването в третата страна на произход и пристигането на входния граничен инспекционен пункт, през който се осъществява въвеждането в Съюза, пратките живи животни не се:
|
а) |
транспортират заедно с живи животни, които:
|
|
б) |
разтоварват, или – при транспорт по въздуха – прехвърлят на друго въздухоплавателното средство, или транспортират с пътен или железопътен транспорт, или придвижват на собствен ход през трета страна, територия или част от тях, които не са изброени в графи 1, 2 и 3 от таблицата, посочена в част 1 от приложение I, или за които в графа 4 от таблицата в част 1 от приложение I не е указан образец на ветеринарен сертификат, който отговаря на съответната пратка; |
Член 9
Времетраене на периода на транспортиране към Съюза на живи животни
Пратките живи животни се въвеждат в Съюза само когато пратките пристигат на входния граничен инспекционен пункт за въвеждане в Съюза в рамките на 10 дни от датата на издаване на съответния ветеринарен сертификат.
При транспорт по море въпросният период от 10 дни се удължава с допълнителен период, който отговаря на продължителността на пътуването по море, удостоверен със съставена в съответствие с част 3 от приложение I и подписана от капитана на кораба декларация, чийто оригинал се прилага към ветеринарния сертификат.
Член 10
Специални условия по отношение на напръскването на пратките живи животни, транспортирани по въздуха към Съюза
Когато пратки живи животни, с изключение на пратки пчели, се транспортират по въздуха, сандъкът или контейнерът, в който те се транспортират, както и заобикалящата ги площ, се напръскват с подходящ инсектицид.
Напръскването се провежда непосредствено преди затварянето на вратите на въздухоплавателното средство след натоварването и след каквото и да било друго последващо отваряне на вратите в трета страна, докато въздухоплавателното средство достигне крайното си местоназначение.
Капитанът на въздухоплавателното средство удостоверява, че е проведено напръскване, като подписва декларация, съставена в съответствие с част 4 от приложение I, чийто оригинал се прилага към ветеринарния сертификат.
Член 11
Условия, които се прилагат след въвеждането в Съюза на някои пратки копитни животни
1. След въвеждането в Съюза на пратки копитни животни, предвидени за отглеждане и разплод или за зоологически градини, увеселителни паркове или за природни резервати или ловни резервати, те незабавно се транспортират до съответните обекти по местоназначение.
Копитните животни остават в посочените стопанства за период от най-малко 30 дни, освен ако не бъдат директно изпратени в кланица.
2. След въвеждането им в Съюза пратките от копитни животни, предвидени за незабавно клане, се отвеждат незабавно до кланицата по местоназначение, където се заколват в рамките на пет работни дни, считано от датата на пристигане в кланицата.
Член 12
Специални условия относно транзита през трети страни на определени пратки копитни животни
В случаите, когато се прилага специфично условие I от част 1 от приложение I с цел да се даде възможност посочените в упоменатото условие пратки копитни животни с произход от дадена държава-членка и предназначени за друга държава-членка да преминават транзитно през трета страна, територия или част от нея, вписана в таблицата в част 1 от приложение I, но за която в графа 4 от посочената таблица не е указан съответен образец на ветеринарен сертификат за пратки от въпросните копитни животни, се прилагат следните условия:
|
а) |
за животни от рода на едрия рогат добитък за угояване:
|
|
б) |
за копитни животни за незабавно клане се прилага член 11, параграф 2. |
Член 13
Условия, които се прилагат след въвеждането в Съюза на пратките пчели, посочени в член 7
1. Пратките от пчелни майки, посочени в член 7, параграф 3, буква а) се транспортират незабавно до определеното място на крайно местоназначение, където кошерите се поставят под контрола на компетентния орган, а пчелните майки се преместват в нови клетки, преди да бъдат придадени в местните колонии;
2. Клетките, пчелите работнички и другите материали, които са придружавали пчелните майки от третата страна на произход, се изпращат в лаборатория, посочена от компетентния орган, за проверка за наличието на:
|
а) |
малък кошерен бръмбар (Aethina tumida), яйца или ларви от него; |
|
б) |
признаци за кошерен акар (Tropilaelaps spp.). |
След тази лабораторна проверка клетките, пчелите работнички и целият инвентар се унищожават.
3. Пратките от земни пчели (Bombus spp.), посочени в член 7, параграф 3, буква б), се транспортират незабавно до определеното място на крайно местоназначение.
Посочените земни пчели могат да останат в контейнера, в който са били въведени в Съюза, до края на жизнения цикъл на колонията.
Посоченият контейнер и инвентарът, които е придружавал земните пчели от третата страна на произход, се унищожават най-късно в края на жизнения цикъл на колонията.
ГЛАВА III
УСЛОВИЯ ЗА ВЪВЕЖДАНЕТО НА ПРЯСНО МЕСО В СЪЮЗА
Член 14
Общи условия за вноса на прясно месо
Пратки от прясно месо, предназначено за консумация от човека, се въвеждат в Съюза само ако отговарят на следните условия:
|
а) |
те са с произход от някоя от изброените в графи 1, 2 и 3 на таблицата в част 1 от приложение II трети страни, територии или части от тях, за които има отговарящ на въпросната пратка образец на ветеринарен сертификат, вписан в графа 4 на таблицата в част 1 от приложение II; |
|
б) |
те се представят на входния граничен инспекционен пункт за въвеждане в Съюза, придружени от съответния ветеринарен сертификат, съставен в съответствие с подходящия образец на ветеринарен сертификат, установен в част 2 от приложение II, като се отчитат специфичните условия, посочени в графа 6 от таблицата в част 1 от посоченото приложение, попълнен и подписан от официален ветеринарен лекар в третата страна износител; |
|
в) |
те удовлетворяват изискванията, установени във ветеринарния сертификат, посочен в буква б), в това число:
|
Член 15
Условия, които се прилагат след вноса на неодрани кланични трупове на чифтокопитен дивеч
В съответствие с член 8, параграф 2 от Директива 97/78/ЕО на Съвета (18) пратките неодрани кланични трупове на чифтокопитен дивеч, предназначени за консумация от човека след последваща преработка, се изпращат незабавно в преработващото предприятие по местоназначение.
Член 16
Транзит и складиране на прясно месо
Въвеждането в Съюза на пратки прясно месо, които не са предвидени за внос в Съюза, а са предназначени за трета страна чрез незабавно транзитно изпращане или след складиране в Съюза в съответствие с член 12, параграф 4 и член 13 от Директива 97/78/ЕО се разрешава само ако пратките отговарят на следните условия:
|
а) |
те са с произход от някоя от изброените в графи 1, 2 и 3 на таблицата в част 1 от приложение II трети страни, територии или части от тях, за които има отговарящ на въпросната пратка образец на ветеринарен сертификат, вписан в графа 4 на таблицата в част 1 от приложение II; |
|
б) |
те съответстват на специфичните ветеринарно-санитарни изисквания по отношение на въпросната пратка, установени в съответния образец на ветеринарен сертификат, посочен в буква а). |
|
в) |
те се придружават от ветеринарен сертификат, съставен в съответствие с подходящия образец на ветеринарен сертификат, определен в приложение III, попълнен и подписан от официален ветеринарен лекар от третата страна износител; |
|
г) |
та са одобрени за транзит, включително и за складиране според случая, с общия входен ветеринарен документ, посочен в член 2, параграф 1 от Регламент (ЕО) на Комисията № 136/2004 (19), подписан от официалния ветеринарен лекар на граничния инспекционен пункт, през който се осъществява въвеждането в Съюза. |
Член 17
Дерогация за транзит през Латвия, Литва и Полша
1. Чрез дерогация от член 16 се разрешава директният или през друга трета страна пътен или железопътен транзит през Съюза между определените гранични инспекционни пунктове в Латвия, Литва и Полша, изброени в Решение 2009/821/ЕО на Комисията (20), на пратки с произход от Русия или предназначени за Русия, при условие, че са спазени следните условия:
|
а) |
пратката е запечатана с пломба със сериен номер на граничния инспекционен пункт на въвеждане в Съюза от ветеринарните служби на компетентния орган; |
|
б) |
документите, придружаващи пратката съгласно член 7 от Директива 97/78/ЕО, са подпечатани с надпис „САМО ЗА ТРАНЗИТНО ПРЕМИНАВАНЕ ДО РУСИЯ ПРЕЗ ЕС“ на всяка страница от официалния ветеринарен лекар на компетентния орган, отговорен за граничен инспекционен пункт на въвеждане в Съюза; |
|
в) |
процедурните изисквания, предвидени в член 11 от Директива 97/78/ЕО, са спазени; |
|
г) |
пратката е сертифицирана като приемлива за транзитно преминаване в общия входен ветеринарен документ от официалния ветеринарен лекар на граничния инспекционен пункт на въвеждане в Съюза. |
2. Не се разрешава разтоварването или складирането по смисъла на член 12, параграф 4 или член 13 от Директива 97/78/ЕО на такива пратки на територията на Съюза.
3. Компетентният орган извършва редовен одит, за да гарантира, че броят на пратките и количествата продукти, напускащи територията на Съюза, съответства на броя и количествата, които са влезли.
ГЛАВА IV
ОБЩИ, ПРЕХОДНИ И ЗАКЛЮЧИТЕЛНИ РАЗПОРЕДБИ
Член 18
Сертифициране
Ветеринарните сертификати, които се изискват съгласно настоящия регламент, се попълват в съответствие с обяснителните бележки, установени в приложение V.
Това изискване не изключва обаче използването на електронно сертифициране или на други съгласувани системи, хармонизирани на равнището на Съюза.
Член 19
Преходни разпоредби
За преходен период, продължаващ до 30 юни 2010 г. пратките от живи животни и прясно месо, предвидени за консумация от човека, за които са издадени съответните ветеринарни сертификати в съответствие с решения 79/542/ЕИО или 2003/881/ЕО, могат да продължат да бъдат въвеждани в Съюза.
Член 20
Отмяна
Решение 2003/881/ЕО се отменя.
Член 21
Влизане в сила
Настоящият регламент влиза в сила на двадесетия ден след публикуването му в Официален вестник на Европейския съюз.
Настоящият регламент е задължителен в своята цялост и се прилага пряко във всички държави-членки.
Съставено в Брюксел на 16 март 2010 година.
За Комисията
Председател
José Manuel BARROSO
(1) ОВ L 268, 14.9.1992 г., стр. 54.
(2) ОВ L 18, 23.1.2003 г., стр. 11.
(3) ОВ L 139, 30.4.2004 г., стр. 321.
(4) ОВ L 139, 30.4.2004 г., стр. 1.
(5) ОВ L 139, 30.4.2004 г., стр. 55.
(6) ОВ L 139, 30.4.2004 г., стр. 206.
(7) ОВ L 165, 30.4.2004 г., стр. 1.
(8) OВ L 302, 31.12.1972 г., стр. 28.
(9) ОВ L 146, 14.6.1979 г., стр. 15.
(10) ОВ L 157, 30.4.2004 г., стр. 33.
(11) ОВ L 13, 16.1.1997 г., стр. 28.
(12) ОВ L 125, 23.5.1996 г., стр. 10.
(13) ОВ L 147, 31.5.2001 г., стр. 1.
(14) ОВ L 340, 31.12.1993 г., стр. 21.
(15) ОВ L 3, 5.1.2005 г., стр. 1.
(16) ОВ L 328, 17.12.2003 г., стр. 26.
(17) ОВ L 224, 18.8.1990 г., стр. 42.
(18) ОВ L 24, 30.1.1998 г., стр. 9.
(19) ОВ L 21, 28.1.2004 г., стр. 11.
(20) ОВ L 296, 12.11.2009 г., стр. 1
ПРИЛОЖЕНИЕ I
КОПИТНИ ЖИВОТНИ
ЧАСТ 1
Списък на трети страни, територии или части от тях (1)
|
Код по ISO и име на третата страна |
Код на територията |
Описание на третата страна, територията или частта от нея |
Ветеринарен сертификат |
Специфични условия |
|||||||
|
Образец/и |
ДГ |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
||||||
|
CA – Канада |
CA-0 |
Цялата страна |
POR-X |
|
IVb IX |
||||||
|
CA-1 |
Цялата страна без долината Оканаган в Британска Колумбия, определена както следва:
|
BOV-X, OVI-X, OVI-Y RUM (2) |
A |
||||||||
|
CH – Швейцария |
CH-0 |
Цялата страна |
|
|
|||||||
|
CL – Чили |
CL-0 |
Цялата страна |
BOV-X, OVI-X, RUM |
|
|
||||||
|
POR-X, SUI |
B |
|
|||||||||
|
GL – Гренландия |
GL-0 |
Цялата страна |
OVI-X, RUM |
|
V |
||||||
|
HR – Хърватия |
HR-0 |
Цялата страна |
BOV-X, BOV-Y, RUM, |
|
|
||||||
|
IS – Исландия |
IS-0 |
Цялата страна |
OVI-X, OVI-Y BOV-X, BOV-Y RUM, OVI-X, OVI-Y |
|
|
||||||
|
POR-X, POR-Y |
B |
||||||||||
|
ME — Черна гора |
ME-0 |
Цялата страна |
|
|
I |
||||||
|
MK – Бивша югославска република Македония (4) |
MK-0 |
Цялата страна |
|
|
I |
||||||
|
NZ – Нова Зеландия |
NZ-0 |
Цялата страна |
BOV-X, BOV-Y, RUM, POR-X, POR-Y OVI-X, OVI-Y |
|
III V |
||||||
|
PM – Сен Пиер и Микелон |
PM-0 |
Цялата страна |
BOV-X, BOV-Y, RUM, OVI-X, OVI-Y CAM |
|
|
||||||
|
RS – Сърбия (5) |
RS-0 |
Цялата страна |
|
|
I |
||||||
Специфични условия (вж. бележките под линия във всеки сертификат):
|
„I“ |
: |
за транзит през територията на трета страна на живи животни, предназначени за незабавно клане или на животни за угояване от рода на едрия рогат добитък, изпратени от държава-членка и с местоназначение друга държава-членка в камиони, запечатани с пломба със сериен номер. Номерът на пломбата трябва да бъде въведен в здравния сертификат, издаден в съответствие с образеца, установен в приложение Е към Директива 64/432/ЕИО (6) за живи животни от рода на едрия рогат за клане и угояване и в съответствие с образец I от приложение Д към Директива 91/68/ЕИО (7) за овце и кози за клане. Освен това пломбата трябва да бъде цяла при пристигането на определения за влизане в Съюза граничен инспекционен пункт и номерът ѝ да е регистриран в интегрираната компютризирана ветеринарна система на Съюза (TRACES). Сертификатът трябва да бъде подпечатан на изходния пункт на Съюза от компетентните ветеринарни органи преди транзитното преминаване през една или повече трети страни с печат, носещ следния надпис: „САМО ЗА ТРАНЗИТ МЕЖДУ РАЗЛИЧНИ ЧАСТИ НА ЕВРОПЕЙСКИЯ СЪЮЗ ПРЕЗ БИВША ЮГОСЛАВСКА РЕПУБЛИКА МАКЕДОНИЯ/ЧЕРНА ГОРА/СЪРБИЯ (8) (9)“ Животните за угояване от рода на едрия рогат добитък трябва да бъдат директно транспортирани до стопанството на местоназначение, определено от компетентния ветеринарен орган на местоназначението. Посочените животни не трябва да бъдат местени от посоченото стопанство, освен за незабавно клане. |
|
„II“ |
: |
територия, призната за официално свободна от туберкулоза за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат BOV-X. |
|
„III“ |
: |
територия, призната за официално свободна от бруцелоза за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат BOV-X. |
|
„IVa“ |
: |
територия, призната за официално свободна от ензоотична левкоза по говедата (ЕЛГ) за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат BOV -X. |
|
„IVb“ |
: |
територия с одобрени стопанства, признати за официално свободни от ензоотична левкоза по говедата (ЕЛГ) за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат BOV -X. |
|
„V“ |
: |
територия, призната за официално свободна от бруцелоза за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат OVI-X. |
|
„VI“ |
: |
Географски ограничения: |
|
„VII“ |
: |
територия, призната за официално свободна от туберкулоза за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат RUM. |
|
„VIII“ |
: |
територия, призната за официално свободна от бруцелоза за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат RUM. |
|
„IX“ |
: |
територия, призната за официално свободна от болестта на Ауески за целите на износа в Съюза на животни, сертифицирани в съответствие с образеца на сертификат POR-Х. |
ЧАСТ 2
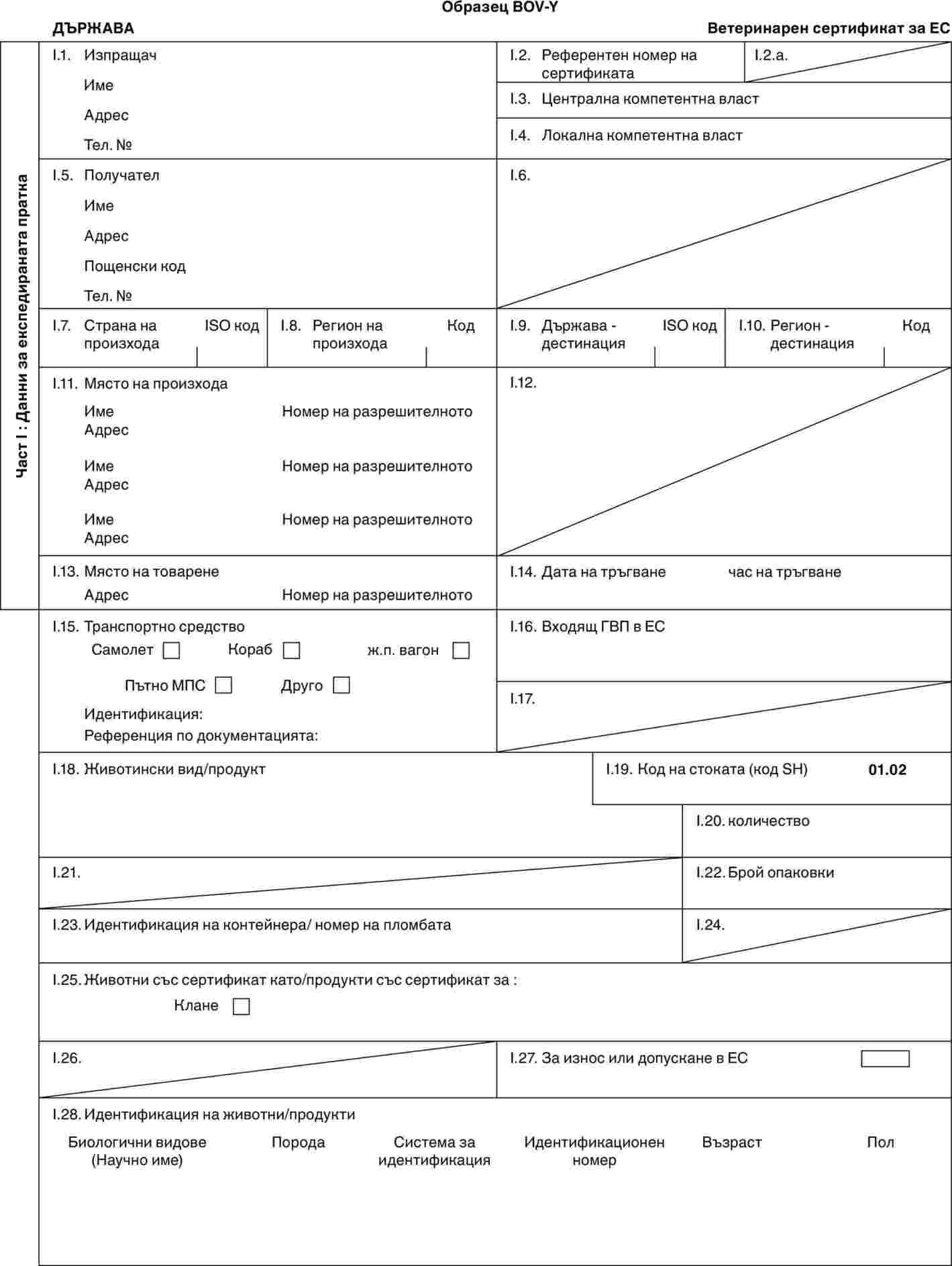
Образци на ветеринарни сертификати
Образци:
|
„BOV-X“ |
: |
образец на ветеринарен сертификат за домашни животни от рода на едрия рогат добитък (включително видовете Bubalus и Bison, и техните кръстоски), предназначени за отглеждане и/или разплод след внос. |
|
„BOV-Y“ |
: |
образец на ветеринарен сертификат за домашни животни от рода на едрия рогат добитък (включително видовете Bubalus и Bison и техните кръстоски), предназначени за незабавно клане след внос. |
|
„OVI-X“ |
: |
образец на ветеринарен сертификат за домашни животни от рода на овцете (Ovis aries) и домашни животни от рода на козите (Capra hircus), предназначени за отглеждане и/или разплод след внос. |
|
„OVI-Y“ |
: |
образец на ветеринарен сертификат за домашни животни от рода на овцете (Ovis aries) и домашни животни от рода на козите (Capra hircus), предназначени за незабавно клане след внос. |
|
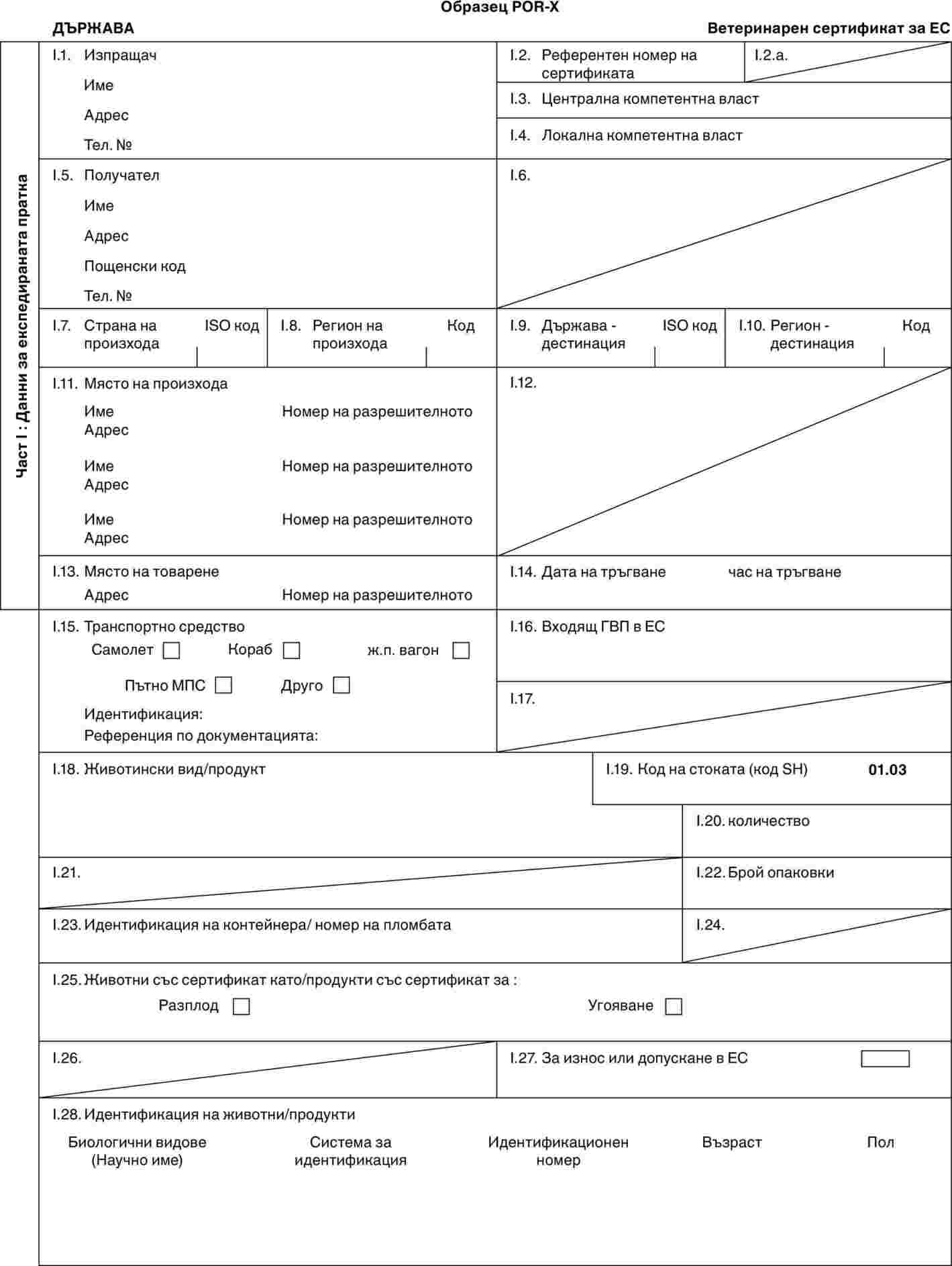
„POR-X“ |
: |
образец на ветеринарен сертификат за домашни животни от рода на свинете (Sus scrofa), предназначени за отглеждане и/или разплод след внос; |
|
„POR-Y“ |
: |
образец на ветеринарен сертификат за домашни животни от рода на свинете (Sus scrofa), предназначени за незабавно клане след внос. |
|
„RUM“ |
: |
образец на ветеринарен сертификат за животни от разред Чифтокопитни (без животни от рода на едрия рогат добитък (включително видовете Bubalus и Bison и техните кръстоски), Ovis aries, Capra hircus, Свине и Пекари) и от семействата Носорози и Слонове. |
|
„SUI“ |
: |
образец на ветеринарен сертификат за дивечови животни от семейства Свине, Пекари и Тапирови. |
|
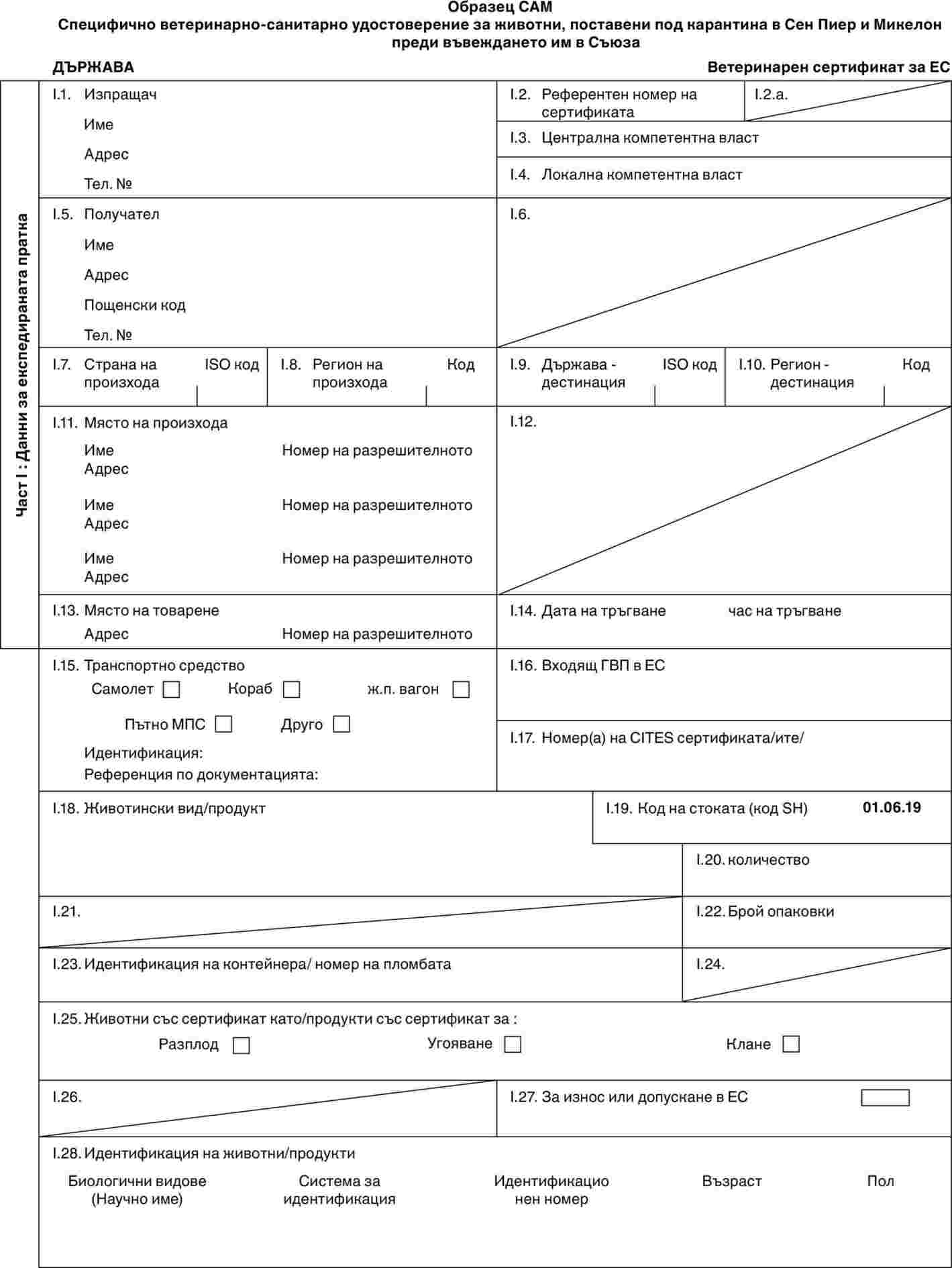
„CAM“ |
: |
образец на специално удостоверение за животни, внесени от Сен Пиер и Микелон съгласно условията, предвидени в част 7 от приложение I. |
ДГ (Допълнителни гаранции):
|
„A“ |
: |
гаранции по отношение на изследванията за син език и епизоотична хеморагична болест, проведени върху животни, сертифицирани в съответствие с образеца на сертификат BOV-X (точка II.2.8 Б), OVI-X (точка II.2.6 Г) и RUM (точка II.2.6). |
|
„B“ |
: |
гаранции по отношение на изследванията за везикулозна болест по свинете и класическа чума по свинете, проведени върху животни, сертифицирани в съответствие с образеца на сертификат POR-X (точка II.2.4 Б) и SUI (точка II.2.4 Б). |
|
„C“ |
: |
гаранции по отношение на изследването за бруцелоза, проведено върху животни, сертифицирани в съответствие с образеца на сертификат POR-X (точка II.2.4 В) и SUI (точка II.2.4 В). |





































ЧАСТ 3
Допълнение за транспортиране на животни по море
(Да се попълни и приложи към ветеринарния сертификат, когато транспортирането към граница на Съюза включва, дори само за част от пътуването, транспортиране с кораб.)
|
Декларация от капитана на кораба |
|
|
Аз, долуподписаният капитан на кораб (име …), декларирам, че животните, описани в приложения ветеринарен сертификат № …, са пребивавали на борда на кораба по време на пътуването от … в … (страната износител) до … в Съюза и че корабът не е правил престой извън … (страната износител) по маршрута към Съюза с изключение на: … (междинни пристанища по маршрута). Освен това по време на пътуването посочените животни не са били в контакт с други животни на борда с по-нисък здравен статус. Съставено в … на … |
|
|
(пристанище на пристигане) |
(дата на пристигане) |
|
(печат) |
(Подпис на капитана) |
|
(Име с главни букви и длъжност) |
|
ЧАСТ 4
Допълнение за транспортиране на животни по въздуха
(Да се попълни и приложи към ветеринарния сертификат, когато транспортирането към граница на Съюза включва, дори само за част от пътуването, транспортиране по въздуха)
|
Декларация от капитана на въздухоплавателното средство |
|
|
Аз, долуподписаният капитан на въздухоплавателно средство (име …) декларирам, че сандъкът или контейнерът, съдържащ посочените в приложения ветеринарен сертификат № … животни, както и зоната около посочения сандък или контейнер, бяха обработени с инсектицид преди заминаването. Съставено в … на … |
|
|
(Летище на заминаване) |
(Дата на заминаване) |
|
(печат) |
(подпис на капитана) |
|
(Име с главни букви и длъжност) |
|
ЧАСТ 5
Условия за одобряване на събирателни центрове (посочени в член 4)
За да бъдат одобрени, събирателните центрове трябва да отговарят на следните изисквания:
|
I. |
Те трябва да са под контрола на официален ветеринарен лекар. |
|
II. |
Всеки един от тях трябва да е разположен в центъра на район с диаметър най-малко 20 km, където в съответствие с официалните данни не е имало случай на шап най-малко 30 дни преди тяхното използване като одобрени събирателни центрове. |
|
III. |
Преди всяко използване като одобрени събирателни центрове те трябва да бъдат почистени и дезинфекцирани с дезинфектант, официално разрешен в страната износител като ефикасен за борба с болестта шап. |
|
IV. |
В тях трябва да има, като се вземе предвид капацитета им за прием на животни:
|
|
V. |
Когато са в действие, в тях трябва да има достатъчно ветеринарни лекари за изпълнението на всички задължения, посочени в част 5. |
|
VI. |
Те трябва да приемат само животни, които са били индивидуално идентифицирани, така че да се гарантира проследимостта. За тази цел, когато се приемат животни, собственикът на събирателния център или длъжностното лице, отговарящо за центъра, трябва да гарантира, че животните са надлежно идентифицирани и придружени от здравни документи или сертификати за въпросните видове и категории. Освен това, собственикът на събирателния център или длъжностното лице, отговарящо за центъра, записва в регистър или база данни и съхранява в продължение на най-малко три години името на собственика, произхода на животните, датата на тяхното влизане и напускане, идентификационния номер на животните или регистрационния номер на стадото на произход и стопанството на местоназначение, както и регистрационния номер на превозвача и регистрационния номер на камиона, доставящ или взимащ животни от събирателния център. |
|
VII. |
Всички животни, преминаващи през събирателните центрове, трябва да отговарят на здравните условия, установени за внос на съответната категория животни в Съюза. |
|
VIII. |
Животни, предназначени за въвеждане в Съюза, които минават през събирателен център, трябва в рамките на шест дни от пристигането в събирателния център да бъдат натоварени и отправени директно към границата на страната износител:
|
|
IX. |
Където условията за износ на животни в Съюза изискват да бъде направено изследване в определен период от време преди натоварването, този период включва всеки период за събиране, с продължителност до шест дни, считано от момента на пристигането на животните в одобрения център за събиране. |
|
Х. |
Третата страна износител трябва да определи центровете, одобрени за животни за разплод и отглеждане и центровете, одобрени за животни за клане, и да уведоми Комисията и компетентните централни органи на държавите-членки за имената и адресите на такива съоръжения. Тази информация трябва редовно да се актуализира. |
|
XI. |
Третата страна износител определя процедурата за официален надзор на одобрените събирателни центрове и осигурява осъществяването на такъв надзор. |
|
XII. |
Одобрените събирателни центрове трябва да бъдат редовно инспектирани от компетентния орган на третата страна, за да се проверява, дали изискванията за одобрение, установени в точки I—XI, продължават да се спазват. Ако инспекциите покажат, че условията вече не се изпълняват, статутът на одобрен център може да бъде отменен. Статутът на одобрен център може да бъде възстановен, когато компетентният орган на третата страна бъде напълно удовлетворен от съответствието на центъра с условията, посочени в точки I—XI. |
ЧАСТ 6
Протоколи за стандартизация на материали и процедури за изследване
(посочени в член 5)
Туберкулоза
Единичната интрадермална туберкулинова проба, при която се използва говежди туберкулин, се изпълнява в съответствие с приложение Б към Директива 64/432/ЕИО. В случая на животни от семейство Свине, единичната интрадермална туберкулинова проба, при която се използва птичи туберкулин, се изпълнява в съответствие с приложение Б към Директива 64/432/ЕИО, освен когато областта на инжектиране е хлабавата кожа в основата на ухото.
Бруцелоза (Brucella abortus)
Изследванията със серум аглутинационен тест, тест за свързване на комплемента, тест с буфериран бруцелозен антиген и тест с използване на ензимно свързан имуносорбентен анализ (ELISA) се провеждат в съответствие с приложение В към Директива 64/432/ЕИО.
Бруцелоза (Brucella melitensis)
Изследването се провежда в съответствие с приложение В към Директива 91/68/ЕИО.
Ензоотична левкоза по говедата (ЕЛГ)
Изследванията с агар-гел имунодифузия и по метода на ензимно-свързания имуносорбентен анализ (ELISA) се провеждат в съответствие с глава II, точки А и В от приложение Г към Директива 64/432/ЕИО.
Син език
Блокиращият или конкурентният ELISA тест се извършват в съответствие със следния протокол:
С конкурентния ELISA тест с използване на моноклонално антитяло 3-17-A3 е възможно да се идентифицират антителата срещу всички известни серотипове на вируса на болестта син език.
Принципът на теста е прекъсването на реакцията между антигена на син език и груповото специфично моноклонално антитяло (3-17-A3) чрез добавянe на тест-серум. Антителата на болестта син език, налични в тест-серума, блокират реактивността на моноклоналното антитяло и водят до намаляване на очакваното проявяване на оцветяването след добавяне на маркирано с ензим антимише антитяло и на хромоген/субстрат. Серумите могат да бъдат изпитвани при разреждане 1:5 (метод на точковия тест — допълнение 1) или могат да бъдат титрувани (метод на титруване на серума — допълнение 2) за достигане до крайната точка на разреждане. Стойности на инхибиране над 50 % могат да бъдат смятани за положителни.
Материали и реактиви:
|
1. |
Подходящи микротитърни плаки за ELISA. |
|
2. |
Антиген: доставен като екстрахиран клетъчен концентрат, приготвен, както е описано по-долу, и съхраняван при температура –20 °C или –70 °C. |
|
3. |
Блокиращ буфер: фосфатно буфериран физиологичен разтвор (PBS), съдържащ 0,3 % отрицателен по отношение на син език серум от възрастни говеда, 0,1 % (v/v) Tween-20 (доставен като сироп на полиоксиетилен сорбитон монолаурат) в PBS. |
|
4. |
Моноклонално антитяло: 3-17-A3 (доставено като супернатант от хибридомна тъканна култура), насочено срещу групово специфичния полипептид VP7, съхраняван при температура–20 °C или лиофилизиран и разреден в пропорция 1/100 с блокиращ буфер преди употреба. |
|
5. |
Конюгат: заешки антимиши глобулин (адсорбиран и елюиран), конюгиран с пероксидаза от хрян и съхраняван на тъмно при температура 4 °C. |
|
6. |
Хромоген и субстрат: Ортофенилен диамин (ОФД-хромоген) при крайна концентрация от 0,4 mg/ml в стерилна дестилирана вода. Водороден пероксид (30 % w/v-субстрат) 0,05 % v/v, добавени непосредствено преди употреба (5μl H2 O2 на 10 ml ОФД). (да се борави внимателно с ОФД — да се носят гумени ръкавици — предполагаем мутаген). |
|
7. |
Едномоларна сярна киселина: 26,6 ml киселина, добавена към 473,4 ml дестилирана вода. (Важно! Винаги се прибавя киселината към водата и никога — водата към киселината). |
|
8. |
Орбитален шейкър. |
|
9. |
Четец за плаки ELISA (тестът може да бъде отчитан визуално). |
Схема на теста
Cc: Контролна проба с конюгат (без серум / без моноклонално антитяло); C++: силно положителна серумна контролна проба; C+: слабо положителна серумна контролна проба; C-: отрицателна серумна контролна проба; Cm: контролна проба с моноклонално антитяло (без серум).
ДОПЪЛНЕНИЕ 1:
Точково разреждане(1:5) формат (40 серумни проби/плака)
|
|
Контролни проби |
Teст-серуми |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
|
A |
Cc |
C- |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Б |
Cc |
C- |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
В |
C++ |
C++ |
|
|
|
|
|
|
|
|
|
|
|
Г |
C++ |
C++ |
|
|
|
|
|
|
|
|
|
|
|
Д |
C+ |
C+ |
|
|
|
|
|
|
|
|
|
|
|
Е |
C+ |
C+ |
|
|
|
|
|
|
|
|
|
|
|
Ж |
Cm |
Cm |
|
|
|
|
|
|
|
|
|
40 |
|
З |
Cm |
Cm |
|
|
|
|
|
|
|
|
|
40 |
ДОПЪЛНЕНИЕ 2:
Формат на титруване на серума(10 серумни проби/плака)
|
|
Контролни проби |
Teст-серуми |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
|
A |
Cc |
C- |
1:5 |
|
|
|
|
|
|
|
|
1:5 |
|
Б |
Cc |
C- |
1:10 |
|
|
|
|
|
|
|
|
1:10 |
|
В |
C++ |
C++ |
1:20 |
|
|
|
|
|
|
|
|
1:20 |
|
Г |
C++ |
C++ |
1:40 |
|
|
|
|
|
|
|
|
1:40 |
|
Д |
C+ |
C+ |
1:80 |
|
|
|
|
|
|
|
|
1:80 |
|
Е |
C+ |
C+ |
1:160 |
|
|
|
|
|
|
|
|
1:160 |
|
Ж |
Cm |
Cm |
1:320 |
|
|
|
|
|
|
|
|
1:320 |
|
З |
Cm |
Cm |
1:640 |
|
|
|
|
|
|
|
|
1:640 |
Протокол на изследването:
|
Контролна проба с конюгат (Cс) |
: |
ямки 1A и 1B съдържат празна проба, състояща се от антиген на син език и конюгат. Тя може да бъде използвана за калибриране на четеца на плаки ELISA. |
|
Контролна проба с моноклонално антитяло (Cm) |
: |
Графи 1 и 2, редове Ж и З представляват контролната проба с моноклонално антитяло, съдържаща антиген на син език, моноклонално антитяло и конюгат. В тези ямки се появява максималното оцветяване. Средната отчетена оптическа плътност от тази контролна проба е 0 % от стойността на инхибиране. |
|
Положителна проба (C++, C+) |
: |
Графи 1 и 2, редове В-Г-Д-Е. В тези ямки има антиген на син език, съответно силно и слабо положителен антисерум, моноклонално антитяло и конюгат. |
|
Отрицателна контролна проба (C–) |
: |
Ямки 2A и 2Б са отрицателните проби, които съдържат антиген на син език, негативен по отношение на син език антисерум, моноклонално антитяло и конюгат. |
|
Тест-серуми |
: |
За обширни серологични изследвания и бърз скрининг серумите могат да се изследват при единично разреждане от 1:5 (допълнение 1). Като алтернатива, могат да бъдат изследвани 10 серума при разреждане, вариращо от 1:5 до 1:640 (допълнение 2). Това ще даде определени индикации за титъра на антитела в изследваните серуми. |
Процедура:
|
1. |
Антиген на син език се разрежда до предварително титруваната концентрация в PBS, разбърква се за кратко с ултразвукова бъркалка, за да се диспергират вирусните агрегати (ако не е наличен ултразвуков апарат, се бърка енергично с пипета) и се прибавят по 50 μl към всички ямки на плаката за ELISA. За диспергиране на антигена се почукват страните на плаката. |
|
2. |
Инкубира се на 37 °C в продължение на 60 минути в орбитален шейкър. Плаките се измиват три пъти чрез напълване и изпразване на ямките с нестерилен PBS и се изсушават с помощта на попивателна хартия. |
|
3. |
Контролни ямки: Прибавят се 100 µl блокиращ буфер към ямките с контролна проба конюгат (Cc). Прибавят се по 50 µl положителни и отрицателни контролни серумни проби при разреждане 1:5 (10 µl серумни проби + 40 µl блокиращ буфер), към съответните ямки C–, C + и C++. Прибавят се 50 µl блокиращ буфер към контролните ямки с моноклонално антитяло. Метод на точковото титруване: добавя се от всеки тест-серум, разреден в съотношение 1:5 с блокиращ буфер, за да се дублират ямките на графи 3—12 (10 µl серум +40 µl блокиращ буфер), или Метод за титруване на серума: приготвят се серии двукратни разреждания на всяка от пробите за анализ (от 1:5 до 1:640) в блокиращ буфер в осем ямки на единични графи 3—12. |
|
4. |
Веднага след прибавянето на тест-серумите се разрежда моноклоналното антитяло в съотношение 1:100 в блокиращ буфер и се добавят 50 µl към всички ямки на плаката, освен в тази за празната проба. |
|
5. |
Инкубира се на 37 °C в продължение на 60 минути в орбитален шейкър. Плаката се измива три пъти с PBS и се изсушава с попивателна хартия. |
|
6. |
Разрежда се заешки антимиши концентрат до съотношение 1/5 000 в блокиращ буфер и се добавят 50 µl към всички ямки на плаката. |
|
7. |
Инкубира се на 37 °C в продължение на 60 минути в орбитален шейкър. Плаката се измива три пъти с PBS и се изсушава с попивателна хартия. |
|
8. |
Разтопява се О-фенилендиамин дихидрохлорид (ОФД) и непосредствено преди употреба се добавят 5 µl водороден пероксид с концентрация 30 % за всеки 10 ml ОФД. Добавят се 50 µl към всички ямки на плаката. Изчаква се в продължение на приблизително 10 минути оцветяването да се прояви и реакцията се спира с едномоларна сярна киселина (50 µl на ямка). Оцветяване следва да се появи в контролните ямки, съдържащи моноклонално антитяло и в онези ямки, които съдържат серуми без антитела на син език. |
|
9. |
Плаките се преглеждат и описват визуално или с използване на спектрофотометричен четец. |
Анализ на резултатите:
Като се използва софтуерният пакет се отпечатват стойностите на оптичната плътност (ОП) и изразеното в проценти инхибиране (ПИ) за тест-серумите и контролните серуми въз основа на средната регистрирана стойност от контролните ямки с антиген. Данните, изразени като стойности на ОП или ПИ, се използват за определяне дали изследването е осъществено в рамките на приемливи граници. Стойностите на горните контролни граници (ГКГ) и долните контролни граници (ДКГ) на ОП за контролната проба с моноклонално антитяло (антиген с добавено моноклонално антитяло, но без добавяне на тест-серум) са между 0,4 и 1,4. Всяка плака, която не отговаря на горните критерии, трябва да се отхвърли.
Ако не е налице компютърен софтуерен пакет, стойностите на ОП се отпечатват, като се използва принтерът на ELISA.. Изчислява се средната стойност на ОП за контролните ямки с антиген, която се приравнява на 100 % от стойността. Определят се 50 % от стойността на ОП и се пресмята за всяка проба дали е положителна или отрицателна.
Процентна стойност на инхибиране (ПИ) = 100 – (ОП на всяка тестова проба/средно ОП на Cm) × 100.
Стойностите на ПИ съответно за дублираните отрицателни контролни ямки със серум и дублираните празни ямки трябва да бъдат съответно между +25 %и –25 % и +95 % и + 105 %. Ако плаката не попадне в тези граници, това не я прави невалидна, но подсказва развиването на оцветяване на заден план. При силните и при слабите положителни контролни серуми трябва да се отчитат стойности на ПИ съответно между +81 % и + 100 %, и между +51 % и + +80 %.
Диагностичният праг за тест-серумите е 50 % (50 % за ПИ или 50 % за ОП). Проби, при които се отчитат по-ниски от 50 % стойности на ПИ се считат за отрицателни. Проби, при които се отчитат стойности на ПИ над и под прага за дублиращите ямки, се считат за съмнителни; такива проби могат да се изследват повторно по метода точковия тест и/или чрез титруване. Положителните проби могат също да се титруват, за да се получи представа доколко положителна е пробата.
Визуално отчитане: Положителните и отрицателните проби се различават лесно с просто око; слабо положителните или силно отрицателните проби могат да бъдат по-трудни за интерпретиране без използване на апаратура.
Приготвяне на антиген на син език за ELISA:
|
1. |
40-60 плоски шишета (колби на Ру) със сливащи се бъбречни клетки на новородени хамстери BHK-21 се изплакват три пъти със среда на Eagle, която не съдържа серум, и се инфектират с вирус на син език от серотип 1 в среда на Eagle, несъдържаща серум. |
|
2. |
Инкубират се при 37 °C и се изследват ежедневно за цитопатичен ефект (ЦПЕ). |
|
3. |
Когато ЦПЕ обхване 90 до 100 % от слоя от клетки във всяко шише, вирусът се събира чрез разклащане на шишето, за да се отделят залепналите за стъклото клетки. |
|
4. |
Шишетата се подлагат на центрофугиране при 2 000 до 3 000 об./мин., за да се раздробят клетките. |
|
5. |
Супернатантът се отстранява и клетките се поставят отново в суспензия от приблизително 30 ml PBS, съдържащ 1 % „Sarkosyl“ и 2 ml фенилметилсулфонил флуорид (лизиращ буфер). Това може да бъде причина клетките да образуват гел, като за намаляване на този ефект може да бъде добавен повече лизиращ буфер. (NB: фенилметилсулфонил флуоридът е опасен — с него трябва да се борави с изключителна предпазливост.) |
|
6. |
Чрез използване на ултразвукова сонда в продължение на 60 секунди при амплитуда 30 микрона клетките се разрушават. |
|
7. |
Центрофугира се при 10 000 об./мин. в продължение на 10 минути. |
|
8. |
Супернатантът се съхранява при температура +4 °C, а останалата маса от клетки се поставя в 10 до 20 ml лизиращ буфер за получаване на нова суспензия. |
|
9. |
Въздейства се с ултразвук и се избистря общо три пъти, като при всеки етап супернатантът се съхранява. |
|
10. |
Супернатантите се обединяват и центрофугират при 24 000 об./мин. (100,000 g) в продължение на 120 минути при +4 °C върху подложка от 5 ml 40 % захароза (w/v в PBS), като се използват епруветки за центрофугиране Beckmann от 30 ml и ротор SW 28. |
|
11. |
Супернатантът се отстранява, епруветките се изплакват старателно и клетъчната маса отново се поставя в PBS, като чрез въздействие с ултразвук се получава суспензия. Антигенът се съхранява като аликвотни части при температура –20 °C. |
Титруване на антиген на син език за ELISA:
Антиген на син език за ELISA се титрува чрез индиректен метод ELISA. Двукратно разреденият антиген се титрува при константно разреждане (1/100) на моноклоналното антитяло 3-17-A3. Следва се посоченият по-долу протокол:
|
1. |
Разреден в PBS в съотношение 1:20 антиген на син език се титрува на микротитърна плака в серии от двукратно разредени проби (50 µl/ямка), като се използва многоканална пипета. |
|
2. |
Пробите се инкубират в продължение на един час на 37 °C върху орбитален шейкър. |
|
3. |
Плаките се измиват три пъти с PBS. |
|
4. |
Добавят се 50 µl моноклонално антитяло 3-17-A3 (разредено 1/100) към всяка ямка на микротитърната плака. |
|
5. |
Пробите се инкубират в продължение на един час на 37 °C върху орбитален шейкър. |
|
6. |
Плаките се измиват три пъти с PBS. |
|
7. |
Към всяка ямка на микротитърна плака се добавят 50 µl заешки антимиши глобулин, конюгиран с пероксидаза от хрян, разредена до предварително титрувана оптимална концентрация. |
|
8. |
Пробите се инкубират в продължение на един час на 37 °C върху орбитален шейкър. |
|
9. |
Добавят се субстрат и хромоген, както е описано по-горе. Реакцията се спира след 10 минути чрез добавяне на едномоларна сярна киселина (50 µl/ямка). |
При конкурентния анализ моноклоналното антитяло трябва да е в излишък, поради това се избира разреждане на антиген, което попада в титърната крива (не в областта на платото), която дава приблизително 0,8 ОП след 10 минути.
Изследването с агар-гел имунодифузия се провежда в съответствие със следния протокол:
Антиген:
Преципитиращият антиген се приготвя във всякаква система за клетъчна култура, която благоприятства бързото размножаване на референтен щам на вируса на син език. Препоръчват се клетки от клетъчни култури тип BHK или Vero. Антигенът е наличен в супернатанта в края на вирусния растеж, но за да бъде ефективен, се изисква 50 до 100-кратна концентрация. Това може да бъде постигнато чрез всяка стандартна процедура за концентриране на протеин; вирусът в антигена може да бъде инактивиран чрез добавянето на 0,3 % (v/v) бета-пропиолактон.
Известен положителен контролен серум:
Като се използват международните референтни серум и антиген, се произвежда национален стандартен серум, който е стандартизиран за оптимална пропорция по отношение на международния референтен серум, лиофилизиран и използван при всяко изследване като известен контролен серум.
Тест-серум
|
Процедура |
: |
1 % агароза, приготвена в боратен или натриев барбитолов буфер, с pH 8,5—9,0, се изсипва в блюдо на Петри до минимална дълбочина от 3,0 mm. В агара се изрязват седем сухи ямки, всяка с диаметър 5,0 mm. Конфигурацията се състои от една централна ямка и шест ямки, подредени около нея в кръг с радиус 3 cm. Централната ямка се запълва със стандартния антиген. Периферните ямки 2, 4 и 6 се пълнят с известен положителен серум, а ямки 1, 3 и 5 се пълнят с тест-серуми. Системата се инкубира в продължение на най-много 72 часа при стайна температура в затворена влажна камера. |
|
Тълкуване |
: |
Тест-серумът е положителен, ако образува специфична линия на преципитация с антигена и формира непрекъсната идентификационна линия с контролния серум. Тест-серумът е отрицателен, ако не формира специфична линия с антигена и ако не изкривява линията на контролния серум; блюдата на Петри трябва да се изследват на тъмен фон и при индиректно осветление. |
Епизоотична хеморагична болест (ЕХБ)
Изследването с агар-гел имунодифузия се провежда в съответствие със следния протокол:
Антиген:
Преципитиращият антиген се приготвя във всякаква система за клетъчна култура, която благоприятства бързото размножаване на подходящ серотип/ове на вируса на епизоотичната хеморагична болест. Препоръчват се клетки от типа BHK или Vero. Антигенът е наличен в супернатанта в края на вирусния растеж, но за да бъде ефективен, се изисква 50 до 100-кратна концентрация. Това може да бъде постигнато чрез всяка стандартна процедура за концентриране на протеин; вирусът в антигена може да бъде инактивиран чрез добавянето на 0,3 % (v/v) бета-пропиолактон.
Известен положителен контролен серум:
Като се използват международните референтни серум и антиген, се произвежда национален стандартен серум, който е стандартизиран за оптимална пропорция по отношение на международния референтен серум, лиофилизиран и използван при всяко изследване като известен контролен серум.
Тест-серум
|
Процедура |
: |
1 % агароза, приготвена в боратен или натриев барбитолов буфер, с pH 8,5—9,0, се изсипва в блюдо на Петри до минимална дълбочина от 3,0 mm. В агара се изрязват седем сухи ямки, всяка с диаметър 5,0 mm. Конфигурацията се състои от една централна ямка и шест ямки, подредени около нея в кръг с радиус 3 cm. Централната ямка се запълва със стандартния антиген. Периферните ямки 2, 4 и 6 се пълнят с известен положителен серум, ямки 1, 3 и 5 се пълнят с тест-серуми. Системата се инкубира в продължение на най-много 72 часа при стайна температура в затворена влажна камера. |
|
Тълкуване |
: |
Тест-серумът е положителен, ако образува специфична линия на преципитация с антигена и формира непрекъсната идентификационна линия с контролния серум. Тест-серумът е отрицателен, ако не формира специфична линия с антигена и ако не изкривява линията на контролния серум; блюдата на Петри трябва да се изследват на тъмен фон и при индиректно осветление. |
Заразен ринотрахеит по говедата (ЗРГ)/заразен пустулозен вулвовагинит (ЗПВВ)
А) Изследването чрез серум неутрализационния тест се извършва в съответствие със следния протокол:
|
Серум |
: |
Всички серуми се инактивират чрез загряване до 56 °C в продължение на 30 минути преди употреба. |
|
Процедура |
: |
При изследването за константна серум-неутрализация по отношение на различни вируси върху микротитърни плаки се използват клетки от тип MDBK или други възприемчиви клетки. Colorado, Oxford или всеки друг референтен щам на вируса се използва при 100 TCID50 на 0,025 ml; инактивирани неразредени серумни проби се смесват с равен обем (0,025 ml) вирусна суспензия. Смесите вирус/серум се инкубират в продължение на 24 часа при температура 37 °C в микротитърни плаки, преди да бъдат добавени клетките от типа MDBK. Клетките се използват при концентрация, при която се след 24 часа се образува цялостен монослой. |
|
Проверки |
: |
i) тест за вирусна инфекциозност, ii) проверки за серотоксичност, iii) проверки в незаразени клетъчни култури, iv) референтни антисеруми. |
|
Тълкуване |
: |
Резултатите от изследването за неутрализация и титърът на използвания в изследването вирус се отчитат след три до шест дни инкубиране при температура 37 °C. Серумните титри се смятат за отрицателни, ако няма неутрализиране при разреждане 1/2 (неразреден серум). |
Б) Всеки друг вид изследване, одобрен в рамките на Решение 2004/558/ЕО (10).
Шап
А) Събирането на езофагеални/фарингеални проби и изследването на същите се извършва в съответствие със следния протокол:
|
Реактиви |
: |
Преди вземането на пробите се приготвя транспортна среда. От нея се разпределят обеми от два ml в толкова контейнера, колкото са животните, от които ще се вземат проби. Използваните контейнери трябва да издържат на замразяване върху твърд CO2 или в течен азот. Пробите се получават чрез използване на специално конструиран слюнков колектор или „пробанг“. За получаване на проба пробанг-чашката се прекарва през устата, над гърба на езика и надолу в горната част на хранопровода. Правят се опити да се изстърже повърхностния епител на горния хранопровод и фаринкса чрез движения, насочени странично и дорзално. След това пробангът се издърпва, за предпочитане след като животното е преглътнало. Чашката трябва да е пълна и да съдържа смес от слуз, слюнка, хранопроводна течност и клетъчни остатъци. Трябва да се внимава всяка проба да съдържа известно количество видим клетъчен материал. Трябва да се избягва грубо манипулиране, което причинява кървене. Пробите от някои животни могат да бъдат силно замърсени от преживна маса. Такива проби трябва да се отстранят и устата на животното да се изплакне с вода или за предпочитане с физиологичен разтвор, преди да се повтори вземането на проба. |
|
Обработване на пробите |
: |
оценява се качеството на всяка проба, събрана в чашката на пробанга, и 2 ml от пробата се добавят към равен обем транспортна среда в контейнер, който може да издържи на замразяване. Контейнерите се затварят плътно, запечатват се, дезинфекцират се и се етикетират. Пробите се държат охладени (+4 °C) и се изследват в рамките на три до четири часа или се поставят върху сух лед (–69 °C) или течен азот и се държат замразени докато бъдат изследвани. Между две взимания на проби пробангът се дезинфекцира и измива три пъти с чиста вода. |
|
Изследване за вируса на шап |
: |
пробите се инкубират в култури от първични клетки от щитовидна жлеза на говеда, като се използват най-малко три епруветки на проба. Могат да бъдат използвани и други възприемчиви клетки, напр. първични клетки от бъбреци на говеда или свине, но трябва да се има предвид, че те са по-малко чувствителни към някои щамове на вируса на шап. Епруветките се инкубират при температура 37 °C в ролерен апарат и в рамките на 48 часа ежедневно се изследват за наличието на цитопатичен ефект (ЦПЕ). Ако са отрицателни, културите са прехвърлят на случаен принцип върху нови култури и се изследват повторно в продължение на 48 часа. Специфичността на всеки ЦПЕ трябва да бъде потвърдена. |
Препоръчвана транспортна среда:
|
1. |
0,08-моларен фосфатен буфер с pH 7,2, съдържащ 0,01 % говежди серумен албумин, 0,002 % фенолно червено и антибиотици. |
|
2. |
Среда за тъканна култура (напр. минимална основна среда (MEM) на Eagle), съдържаща 0,04-моларен Hepes буфер, 0,01 % говежди серумен албумин и антибиотици, с pH 7,2. |
|
3. |
Към транспортната среда трябва да бъдат добавяни антибиотици, напр. пеницилин 1 000 IU, неомицин сулфат 100 IU, полимиксин B сулфат 50 IU, микостатин 100 IU (на ml краен продукт). |
Б) Вирус неутрализационният тест се изпълнява в съответствие със следния протокол:
|
Реактиви |
: |
Запасен антиген за вируса на шап се приготвя в клетъчни култури или върху говежди езици и се съхранява при температура –70 °C или по-ниска или при температура –20 °C след прибавяне на 50 % глицерин. Това е запасният антиген. При тези условия шапният вирус е стабилен и за период от няколко месеца неговите титри се променят незначително. |
|
Процедура |
: |
Изследването се провежда в плоскодънни микротитърни плаки за тъканни култури, като се използват възприемчиви клетки като IB-RS-2, BHK-21 или клетки от телешки бъбрек. Серумите за изследването се разреждат в съотношение 1/4 със свободна от серуми среда за клетъчни култури с добавяне на 100 IU/ml неомицин или друг подходящ антибиотик. Серумите се инактивират при температура 56 °C в продължение на 30 минути и се използват количества от 0,05 ml за приготвяне на двойни серии върху микротитърни плаки, като се използват дозиращи тръбички от 0,05 ml. Към всяка ямка се добавя предварително титруван вирус, също разреден в свободна от серум среда за клетъчна култура и съдържащ 100 TCID50/0,05 ml. След инкубиране на 37 °C в продължение на един час, което позволява да се осъществи неутрализацията, към всяка ямка се добавя 0,05 ml от суспензията на клетки, съдържаща 0,5 до 1,0 × 106 клетки на 1 ml в среда за клетъчна култура, съдържаща серум, свободен от антитела на шап, и плаките се запечатват. Плаките се инкубират на 37 °C. Обикновено в рамките на 24 часа монослоевете се сливат. ЦПЕ е обичайно достатъчно напреднал за 48 часа за микроскопско отчитане на изследването. По това време може да бъде направено окончателно микроскопско отчитане или плаките могат да бъдат фиксирани и оцветени за макроскопско отчитане, например като се използва разтвор, съдържащ 10 % формалин, физиологичен разтвор и 0,05 % метиленово синьо. |
|
Проверки |
: |
Проверките при всяко изследване включват хомоложен антисерум с известен титър, клетъчна проверка, проверка на серумната токсичност, проверка на средата и титруване на вируса, въз основа на които се изчислява действителното количество на вирус в изследването. |
|
Тълкуване |
: |
Ямки с данни за ЦПЕ се считат за инфектирани и неутрализиращите титри се изразяват като реципрочна стойност на крайното разреждане на серума, наличен в смесите серум/вирус при крайна точка от 50 %, изчислена по метода на Spearman-Karber. (Karber, G., 1931, Archiv fuer Experimentelle Pathologie und Pharmokologie, 162, 480.). Изследванията се считат за валидни, когато действителното количество от вируса, използвано във всяка ямка при изследването, е между 101,5 и 102,5 TCID50 и когато титърът на референтния серум не е по-висок от двукратната стойност на неговия очакван титър, изчислен по начина на предишните титрувания. Когато проверките са извън тези граници, изследванията се повтарят. Краен титър, равен на 1/11 или по-малко, се приема за отрицателен. |
В) Откриването и количественото определяне на дадено антитяло чрез ELISA се извършва в съответствие със следния протокол:
|
Реактиви |
: |
Заешки антисеруми срещу антиген 146S от седем типа на вируса на шап, използвани при предварително определена оптимална концентрация в карбонатен/бикарбонатен буфер с pH 9,6. Антигените се приготвят от избрани щамове на вируса, отгледани върху монослоеве от клетки BHK-21. Непречистените супернатанти се използват и предварително се титруват съгласно протокола, но без серум, за се получи разреждане, което след добавяне на равен обем на PBST (фосфатно буфериран физиологичен разтвор, съдържащ 0,05 % Tween-20 и индикатор фенолно червено) биха дали оптическа плътност между 1,2 и 1,5. Могат да се използват инактивирани вируси. PBST се използва като разредител. Антисеруми от морски свинчета се приготвят чрез заразяване на морски свинчета с антиген 146S на всеки серотип. Предварително определената оптимална концентрация се приготвя в PBST, съдържащ 10 % нормален говежди серум и 5 % нормален заешки серум. Използва се заешки имуноглобулин против морски свинчета в комбинация с пероксидаза от хрян, разтворен в PBST, съдържащ 10 % нормален говежди серум и 5 % нормален заешки серум, при предварително определена оптимална концентрация. Тест-серумите се разреждат с PBST. |
Процедура:
|
1. |
Плаките за ELISA са покриват със слой от 50 µl заешки антивирусни серуми за една нощ във влажна камера при стайна температура. |
|
2. |
На плаки с множество U-образни ямки (носещи плаки) се приготвят петдесет микролитра двойни серии разреждания с фактор 2 на всеки тест-серум, като се започва с разреждане 1/4. Към всяка ямка се добавят петдесет микролитра постоянна доза антиген и смесите се оставят за една нощ при температура 4 °C. Добавянето на антиген намалява началното разреждане на антигена до 1/8. |
|
3. |
Плаките за ELISA се измиват пет пъти с PBST. |
|
4. |
Петдесет микролитра от смесите серум/антиген се пренасят от носещите плаки върху покритите със заешки серум плаки за ELISA, и се инкубират при температура 37 °C в продължение на един час на ротационен шейкър. |
|
5. |
След измиване, към всяка ямка се добавят 50 µl антисерум от морски свинчета срещу използвания в точка 4 антиген. Плаките се инкубират при температура 37 °C за един час върху ротационен шейкър. |
|
6. |
Плаките се измиват и към всяка ямка се добавят 50 µl заешки имуноглобулин против морски свинчета в комбинация с пероксидаза от хрян. Плаките се инкубират при температура 37 °C в продължение на един час върху ротационен шейкър. |
|
7. |
Плаките се измиват и към всяка ямка се добавят 50 µl ортофенилен диамин, съдържащ 0,05 % H2O2 (30 % w/v). |
|
8. |
Реакцията се спира след 15 минути с 1,25-моларна H2SO4. |
Плаките се отчитат спектрофотометрично при 492 nm с четец за ELISA, свързан към микрокомпютър.
|
Проверки |
: |
За всеки използван антиген 40 ямки не съдържат серум, а разреден в PBST антиген. Двойни серии разреждания с фактор 2 от хомоложен говежди референтен антисерум. Двойни серии разреждания с фактор 2 от отрицателен говежди серум. |
|
Тълкуване |
: |
Титрите за определено антитяло се изразяват като крайното разреждане на тест-серумите, даващи 50 % от средната стойност на ОП, отчетени в контролните ямки с вирус, където отсъства тест-серум. Титрите над 1/40 се считат за положителни. |
|
Препратки |
: |
Hamblin C, Barnett ITR and Hedger RS (1986), „A new enzyme-linked immunosorbent assay (ELISA) for the detection of antibodies against foot-and-mouth disease virus. I. Development and method of ELISA.“, Journal of Immunological Methods, 93, 115 до 121.11. |
Болест на Ауески
А) Изследването чрез серум неутрализационния тест се извършва в съответствие със следния протокол:
|
Серум |
: |
Всички серуми се инактивират чрез загряване до 56 °C в продължение на 30 минути преди употреба. |
|
Процедура |
: |
При изследването за константна серум-неутрализация на различни вируси върху микротитърни плаки се използват клетки от типа MDBK или други възприемчиви клетки. Вирусът на болестта на Ауески се използва при 100 TCID50 на 0,025 ml; инактивирани неразредени серумни проби се смесват с равен обем (0,025 ml) вирусна суспензия. Смесите вирус/серум се инкубират в продължение на два часа при температура 37 °C в микротитърни плаки, преди да бъдат добавени подходящите клетки. Клетките се използват при концентрация, при която се след 24 часа се образува цялостен монослой. |
|
Проверки |
: |
i) изследване за вирусна инфекциозност, ii) проверки за серумна токсичност, iii) проверки на незаразени клетъчни култури, iv) референтни антисеруми. |
|
Тълкуване |
: |
Резултатите от неутрализационен тест и титърът на използвания в теста вирус се отчитат след три до седем дни инкубиране при 37 °C. Серумни титри, по-ниски от 1/2 (неразреден серум) се смятат за негативни. |
Б) Всеки друг вид изследване, одобрен в рамките на Решение 2008/185/ЕО (11).
Трансмисивен гастроентерит
Изследването чрез серум неутрализационния тест се извършва в съответствие със следния протокол:
|
Серум |
: |
Всички серуми се инактивират чрез загряване до 56 °C в продължение на 30 минути преди употреба. |
|
Процедура |
: |
При изследването за константна серум-неутрализация на различни вируси върху микротитърни плаки се използват клетки А72 (кучешки тумор) или други чувствителни системи от клетки. Вирусът на трансмисивния гастроентерит се използва при 100 TCID50 на 0,025 ml; инактивирани неразредени серумни проби се смесват с равен обем (0,025 ml) вирусна суспензия. Смесите вирус/серум се инкубират в продължение на 30 до 60 минути при температура 37 °C в микротитърни плаки, преди да бъдат добавени подходящите клетки. Клетките се използват при концентрация, при която след 24 часа се образува цялостен монослой. Във всяка клетка се слага 0,1 ml клетъчна суспензия. |
|
Проверки |
: |
i) изследване за вирусна инфекциозност, ii) проверки за серумна токсичност, iii) проверки на незаразени клетъчни култури, iv) референтни антисеруми. |
|
Тълкуване |
: |
Резултатите от неутрализационния тест и титърът на използвания в теста вирус се отчитат след три до пет дни инкубиране при температура 37 °C. Серумни титри, по-ниски от 1/2 (крайно разреждане) се считат за отрицателни. Ако отделни неразредени серумни проби са токсични спрямо тъканните култури, тези серуми могат да бъдат разредени в съотношение 1/2, преди да бъдат използвани в изследването. Такова разреждане е еквивалентно на крайно разреждане от 1/4 на серума. В тези случаи серумни титри, по-ниски от 1/4 (крайно разреждане), се считат за отрицателни. |
Везикулозна болест по свинете
Изследванията за везикулозна болест по свинете (ВБС) се извършват в съответствие с Решение 2000/428/ЕО (12).
Класическа чума по свинете
Изследванията за класическа чума по свинете се извършват в съответствие с Решение 2002/106/ЕО (13).
Извършването на изследвания за класическа чума по свинете трябва да следва насоките, изложени в Ръководството за диагностични тестове и ваксини за сухоземни животни на OIE — глава 2.1.13.
Оценката на чувствителността и специфичността на серологичните тестове за класическа чума по свинете трябва да се извършва в национална лаборатория, в която функционира схема за осигуряване на качеството. Трябва да се докаже, че използваните тестове позволяват да се разпознават от слабо до силно положителни референтни серуми, както и да дават възможност да се откриват антитела в ранната фаза на болестта и при възстановяване от болестта.
ЧАСТ 7
Ветеринарно-санитарни условия във връзка с карантината и вноса на животни, внасяни в Сен Пиер и Микелон в рамките на период, по-кратък от шест месеца преди въвеждането им в Съюза
(посочени в член 6)
Засегнати животински видове
|
Таксон |
||
|
РАЗРЕД |
СЕМЕЙСТВО |
РОД И ВИД |
|
Чифтокопитни |
Камили |
Camelus spp., Lama spp., Vicugna spp. |
ГЛАВА 1
Пребиваване и карантина
1. Животните, внасяни в Сен Пиер и Микелон, трябва да пребивават в одобрена карантинна станция за период от най-малко 60 дни, преди да бъдат изпратени за въвеждане в Съюза. Посоченият период може да бъде удължен поради изисквания, свързани с изследването при отделни видове. Освен това, животните трябва да отговарят на следните изисквания:
|
а) |
в карантинната станция могат да влизат отделни пратки. При влизане в карантинната станция обаче, всички животни от един и същ вид в карантинното съоръжение трябва да се разглеждат като една група и с тях да се борави като с такава. Карантинният период за цялата група трябва да започва в момента, когато последното животно е влязло в карантинното съоръжение. |
|
б) |
в карантинната станция всяка конкретна група животни трябва да бъде държана в изолация и без да влиза в пряк или непряк контакт с каквито и да било други животни, включително такива от други пратки, които евентуално се намират там. Всяка пратка животни трябва да бъде държана в одобрената карантинна станция и да бъде предпазвана от насекоми преносители на зараза. |
|
в) |
ако по време на карантинния период изолирането на група животни бъде нарушено и се допусне контакт с други животни, карантинният период трябва да започне отначало и да продължи толкова, колкото е било първоначално определено при влизането в карантинната станция. |
|
г) |
животни, които са предназначени за въвеждане в Съюза и които преминават през карантинна станция, трябва да бъдат натоварени и изпратени директно за Съюза:
|
2. Помещенията за карантина трябва да съответстват поне на минималните стандарти, посочени в приложение Б към Директива 91/496/ЕИО (14), а също и на следните условия:
|
а) |
те трябва да са под контрола на официален ветеринарен лекар; |
|
б) |
те трябва да са разположени в центъра на район с диаметър най-малко 20 km, в който в съответствие с официалните данни не е имало случай на шап най-малко 30 дни преди тяхното използване като карантинни станции; |
|
в) |
преди всяко използване като карантинни станции те трябва да се почистват и дезинфекцират с дезинфектант, официално разрешен в Сен Пиер и Микелон и признат за ефикасен за борба с посочените в глава 2 болести; |
|
г) |
в тях трябва да работят, като се вземе предвид капацитета им за прием на животни:
|
|
д) |
когато са в действие, в тях трябва да има достатъчно ветеринарни лекари за изпълнението на всички задължения; |
|
е) |
те трябва да приемат само животни, които са били индивидуално идентифицирани, така че да се гарантира проследимостта. За тази цел, когато се приемат животни, собственикът на карантинната станция или длъжностното лице, отговарящо за нея, трябва да гарантира, че животните са надлежно идентифицирани и придружени от здравни документи или сертификати за въпросните видове и категории. Освен това, собственикът на карантинната станция или длъжностното лице, отговарящо за нея, записва в регистър или база данни и съхранява в продължение на най-малко три години името на собственика, произхода на животните в пратката, датите на влизане и напускане на животните в пратката, идентификационния номер на животните в пратката и тяхното местоназначение. |
|
ж) |
компетентният орган трябва да определи процедурата за официален надзор на карантинните станции и да направи така, че да се осъществява такъв надзор; посоченият надзор трябва да включва редовни инспекции, за да се осигури, че изискванията за одобрение продължават да се спазват. В случай на оттегляне на одобрението вследствие на неизпълнение на посочените изисквания, одобрението може да бъде възстановено само когато компетентният орган бъде удовлетворен от съответствието на съоръженията в карантинната станция с всички условия, посочени в точки а)—ж). |
ГЛАВА 2
Ветеринарно-санитарни изследвания
1. ОБЩИ ИЗИСКВАНИЯ
Животните трябва да бъдат подложени на следните изследвания, които се провеждат върху кръвни проби, взети, ако не е посочено друго, не по-рано от 21 дни преди датата на започване на периода на изолация.
Лабораторните изследвания трябва да се провеждат в одобрена лаборатория в Съюза, а всички лабораторни изследвания и резултатите от тях, ваксинациите и проведените третирания трябва да бъдат приложени към здравния сертификат.
За да се сведат до минимум интервенциите върху животните, взимането на проби, изследванията и всякакви ваксинации трябва да бъдат групирани във възможно най-кратък срок, като се спазват минималните времеви интервали, които се изискват от протоколите за изследване, установени в част 2 от настоящата глава.
2. СПЕЦИФИЧНИ ИЗИСКВАНИЯ
2.1 Семейство Камили
2.1.1 Туберкулоза
|
а) |
Изследване, което да бъде извършено: сравнителна проба за интрадермална реакция с използване на говежди пречистен протеинов дериват (ППД) и птичи ППД в съответствие със стандартите за производство на говежди и птичи туберкулини, както е описано в точка 2.1.2 от приложение Б към Директива 64/432/ЕИО. Изследването трябва да бъде направено в областта зад рамото (аксиларната област), като се следва техниката, описана в точка 2.2.4 от приложение Б към Директива 64/432/ЕИО. |
|
б) |
Срокове за провеждане: животните трябва да бъдат изследвани до два дни от датата на пристигане в карантинната станция и 42 дни след датата на първото изследване. |
|
в) |
Тълкуване на изследванията реакцията се счита за:
|
|
г) |
Възможни действия след провеждане на изследването: Ако интрадермалната реакция към говежди ППД на едно животно е положителна, то се изключва от групата, а другите животни следва да бъдат повторно изследвани, като се започне най-рано на 42-рия ден след датата на първото положително изследване, което се приема за първо изследване, така, както е определено в буква б). Ако при повече от едно животно от групата се появи положителен резултат, износът на цялата група за Съюза се отказва. Ако при едно или повече животни от групата се появи неясна реакция, цялата група следва да бъде повторно изследвана, като се започне най-рано на 42-рия ден след датата на първото положително изследване, което се приема за първо изследване, така, както е определено в буква б). |
2.1.2 Бруцелоза:
|
а) |
Изследване, което да бъде извършено:
|
|
б) |
Срокове за провеждане: животните трябва да бъдат изследвани до два дни от датата на пристигането им в карантинната станция и 42 дни след датата на първото изследване. |
|
в) |
Тълкуване на изследванията Положителна реакция на изследването е тази, определена в приложение В към Директива 64/432/ЕИО. |
|
г) |
Възможни действия след провеждане на изследването: Животните, чийто резултат от изследването е положителен, се изваждат от групата, а останалите животни се изследват повторно, като се започне най-рано на 42-рия ден след датата, на която е проведено първото положително изследване; посоченото изследване се счита за първо изследване, както е определено в буква б). Единствено животните, чиито резултати от две последователни изследвания, проведени, както е описано в буква б), са отрицателни, се допускат за въвеждане в Съюза. |
2.1.3 Син език и епизоотична хеморагична болест
|
а) |
Изследване, което да бъде извършено: изследване чрез агар-гел имунодифузия, както е описано в част 6 от приложение I към Регламент (ЕС) № 206/2010 (SANCO/4787/2009). В случай на положителна реакция, животните следва да се изследват с конкурентен тест ELISA, както е описано в част 6 от приложение I към Регламент (ЕС) № 206/2010 (SANCO/4787/2009), за да се направи разграничаване между двете болести. |
|
б) |
Срокове за провеждане: Животните трябва да бъдат изследвани на два пъти, като резултатите от изследванията трябва да бъдат отрицателни: първото изследване се прави до два дни от датата на пристигането в карантинната станция, а второто — най-малко 21 дни след датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването:
|
2.1.4 Шап
|
а) |
Изследване, което да бъде извършено: диагностични тестове (с пробанг и серологични), при които се използва ELISA и (вирус неутрализационни) (ВН) техники в съответствие с протоколите, описани в част 6 от приложение I към Регламент (ЕС) № 206/2010 (SANCO/4787/2009). |
|
б) |
Срокове за провеждане: животните трябва да бъдат изследвани на два пъти, при което резултатите от изследванията трябва да бъдат отрицателни: първото изследване се прави до два дни след датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако някое животно покаже положителен резултат при изследването за шап, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. Забележка: Всяко откриване на антитела срещу структурни или неструктурни протеини на вируса на шап следва да се счита за резултат от предишна инфекция с шап, без значение какъв е ваксинационният статус на животното. |
2.1.5 Чума по говедата
|
а) |
Изследване, което да бъде извършено: конкурентният тест ELISA, както е описан в Ръководството за диагностични тестове и ваксини за сухоземни животни на OIE, последно издание, е препоръчваният при международна търговия тест, а също и тестът на първи избор в случая. Може да се използва и изследване чрез серум неутрализационен тест или други признати тестове в съответствие с протоколите, описани в съответните раздели на ръководството на OIE. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако някое животно покаже положителен резултат при изследването за чума по говедата, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. |
2.1.6 Везикулозен стоматит
|
а) |
Изследване, което да бъде извършено: ELISA, вирус неутрализационен тест или други признати тестове в съответствие с протоколите, описани в съответните раздели на ръководството на OIE. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако някое животно покаже положителен резултат при изследването за везикулозен стоматит, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. |
2.1.7 Треска от долината Рифт
|
а) |
Изследване, което да бъде извършено: ELISA; вирус неутрализационен тест или други признати тестове в съответствие с протоколите, описани в съответните раздели на ръководството на OIE. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако при някое животно се появят признаци за експозиция на причинителя на треска от долината Рифт, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. |
2.1.8 Заразен нодуларен дерматит
|
а) |
Изследване, което да бъде извършено: Серология с използване на ELISA; вирус неутрализационен тест или други признати тестове в съответствие с протоколите, описани в съответните раздели на ръководството на OIE. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако при някое животно се появят признаци за експозиция на заразен нодуларен дерматит, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. |
2.1.9 Кримска-Конго хеморагична треска:
|
а) |
Изследване, което да бъде извършено: ELISA, вирус неутрализационен тест, имунофлуоресцентен тест или друг признат тест. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако при някое животно се появят признаци за експозиция на причинителя на Кримска-конго хеморагична треска, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. |
2.1.10 Сура (Trypanosoma evansi (T. evansi))
|
а) |
Изследване, което да бъде извършено: паразитният агент може да бъде идентифициран в концентрирани кръвни проби в съответствие с протоколите, описани в съответните раздели на ръководството на OIE. |
|
б) |
Срокове на провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: Ако у едно животно от пратката бъде открита T. evansi, то не може да бъде въведено в Съюза. Останалите животни от групата се подлагат на вътрешно и външно противопаразитно третиране, като се използват подходящи вещества, ефикасни срещу T. evansi. |
2.1.11 Злокачествена катарална треска:
|
а) |
Изследване, което да бъде извършено: Откриване на вирусна ДНК въз основа на идентификация чрез имунофлуоресцентни или имуноцитохимични методи, като се използват протоколите, описани в съответните раздели на ръководството на OIE. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: ако при някое животно се появят признаци за експозиция на злокачествена катарална треска, в такъв случай нито едно животно от карантинната станция не може да бъде въведено в Съюза. |
2.1.12 Бяс
Ваксинация: може да бъде направена ваксинация срещу бяс, ако държавата-членка по местоназначение изиска това, а от животното се взема кръвна проба и се провежда серум неутрализационен тест за откриване на антитела.
2.1.13 Ензоотична левкоза по говедата (само в случай, че животните са предназначени за държава-членка или регион, официално свободни от ензоотична левкоза по говедата, както е посочено в член 2, параграф 2, буква к) от Директива 64/432/ЕИО)
|
а) |
Изследване, което да бъде извършено: изследване чрез агар-гел имунодифузия за ензоотична левкоза по говедата или блокиращ тест ELISA, в съответствие с протоколите, описани в ръководството на OIE, последно издание. |
|
б) |
Срокове за провеждане: животните следва да бъдат изследвани два пъти: първото изследване се прави до два дни от датата на пристигането им в карантинната станция, а второто — най-малко 42 дни от датата на първото изследване. |
|
в) |
Възможни действия след провеждане на изследването: животните, при които резултатът от изследването, описано в буква а) е положителен, се изваждат от групата животни в карантинната станция, а останалите животни се изследват повторно, като се започне най-рано от 21-рия ден след датата, на която е проведено първото положително изследване. посоченото изследване се счита за първо изследване, така, както е определено в буква б). Могат да бъдат въведени в Съюза единствено животните, които сa показали отрицателни резултати при две последователни изследвания, проведени, както е описано в буква б). |
(1) Без да се засягат специфичните изисквания за сертифициране, предвидени в което и да е приложимо споразумение между Съюза и трети страни.
(2) Единствено за живи животни, различни от онези, които принадлежат към видовете от семейство Плътнороги.
(3) Сертификати в съответствие със Споразумението между Европейската общност и Конфедерация Швейцария относно търговията със селскостопански продукти, ОВ L 114, 30.4.2002 г., стр. 132.
(4) Бивша югославска република Македония: окончателната номенклатура за тази страна ще бъде договорена след провежданите понастоящем преговори на равнище ООН.
(5) Не е включено Косово, което в момента е под управлението на международна администрация по силата на Резолюция 1244 от 10 юни 1999 г. на Съвета за сигурност на ООН.
(6) ОВ 121, 29.7.1964 г., стр. 1977/64.
(7) ОВ L 46, 19.2.1991 г., стр. 19.
(8) Ненужната страна се зачерква.
(9) В Сърбия не е включено Косово, което в момента е под управлението на международна администрация по силата на Резолюция 1244 от 10 юни 1999 г. на Съвета за сигурност на ООН.
(10) ОВ L 249, 23.7.2004 г., стр. 20.
(11) ОВ L 59, 4.3.2008 г., стр. 19.
(12) ОВ L 167, 7.7.2000 г., стр. 22.
ПРИЛОЖЕНИЕ II
ПРЯСНО МЕСО
ЧАСТ 1
Списък на трети страни, територии или части от тях (1)
|
Код по ISO и име на третата страна |
Код на територията |
Описание на третата страна, територията или частта от нея |
Ветеринарен сертификат |
Специфични условия |
Крайна дата (2) |
Начална дата (3) |
|||||
|
Образец/и |
ДГ |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
||||
|
AL — Албания |
AL-0 |
Цялата страна |
— |
|
|
|
|
||||
|
AR – Аржентина |
AR-0 |
Цялата страна |
EQU |
|
|
|
|
||||
|
AR-1 |
Провинции: Buenos Aires, Catamarca, Corrientes (с изключение на департаменти Berón de Astrada, Capital, Empedrado, General Paz, Itati, Mbucuruyá, San Cosme и San Luís del Palmar) Entre Ríos, La Rioja, Mendoza, Misiones, Част от Neuquén (с изключение на територията, включена в AR-4), Част от Río Negro (с изключение на територията, включена в AR-4), San Juan, San Luis, Santa Fe, Tucuman, Cordoba, La Pampa, Santiago del Estero, Chaco, Formosa, Jujuy и Salta, с изключение на 25-километровата буферна зона от границата с Боливия и Парагвай, която се простира от област Santa Catalina в провинция Jujuy, до област Laishi в провинция Formosa |
BOV |
A |
1 |
|
18 март 2005 година |
|||||
|
RUF |
A |
1 |
|
1 декември 2007 година |
|||||||
|
AR-2 |
Chubut, Santa Cruz и Tierra del Fuego |
BOV, OVI, RUW, RUF |
|
|
|
1 март 2002 г. |
|||||
|
AR-3 |
Corrientes: департаменти Berón de Astrada, Capital, Empedrado, General Paz, Itati, Mbucuruyá, San Cosme и San Luís del Palmar |
BOV RUF |
A |
1 |
|
1 декември 2007 г. |
|||||
|
AR-4 |
Част от Río Negro (с изключение на: в Avellaneda – зоната, разположена на север от междуселищен път 7 и на изток от междуселищен път 250; в Conesa – зоната, разположена на изток от междуселищен път 2; в El Cuy – зоната, разположена на север от междуселищен път 7, от мястото, на което се пресича с междуселищен път 66, до границата с департамент Avellaneda, и в San Antonio – зоната, разположена на изток от междуселищни пътища 250 и 2) Част от Neuquén (с изключение на: в Confluencia –зоната, разположена на изток от междуселищен път 17, и в Picun Leufú –зоната, разположена на изток от междуселищен път 17) |
BOV, OVI, RUW, RUF |
|
|
|
1 август 2008 г. |
|||||
|
AU – Австралия |
AU-0 |
Цялата страна |
BOV, OVI, POR, EQU, RUF, RUW, SUF, SUW |
|
|
|
|
||||
|
BA – Босна и Херцеговина |
BA-0 |
Цялата страна |
— |
|
|
|
|
||||
|
BH – Бахрейн |
BH-0 |
Цялата страна |
— |
|
|
|
|
||||
|
BR – Бразилия |
BR-0 |
Цялата страна |
EQU |
|
|
|
|
||||
|
BR-1 |
Щат Minas Gerais Щат Espíritо Santo; Щат Goiás; Щат Mato Grosso; Щат Rio Grande Do Sul, Щат Mato Grosso Do Sul (с изключение на определената 15-километрова строго наблюдавана гранична зона в общините Porto Murtinho, Caracol, Bela Vista, Antônio João, Ponta Porã, Aral Moreira, Coronel Sapucaia, Paranhos, Sete Quedas, Japorã, и Mundo Novo, и посочената строго наблюдавана зона в общините Corumbá и Ladário). |
BOV |
A и H |
1 |
|
1 декември 2008 г. |
|||||
|
BR-2 |
Щат Santa Catarina |
BOV |
A и H |
1 |
|
31януари 2008 г. |
|||||
|
BR-3 |
Щати Paraná и São Paulo |
BOV |
A и H |
1 |
|
1 август 2008 г. |
|||||
|
BW – Ботсуана |
BW-0 |
Цялата страна |
EQU, EQW |
|
|
|
|
||||
|
BW-1 |
Зони за ветеринарен контрол на болести 3в, 4б, 5, 6, 8, 9 и 18 |
BOV, OVI, RUF, RUW |
F |
1 |
|
1 декември 2007 г. |
|||||
|
BW-2 |
Зони за ветеринарен контрол на болести 10, 11, 13 и 14 |
BOV, OVI, RUF, RUW |
F |
1 |
|
7 март 2002 г. |
|||||
|
BW-3 |
Зона за ветеринарен контрол на болести 12 |
BOV, OVI, RUF, RUW |
F |
1 |
20 октомври 2008 г. |
20 януари 2009 г. |
|||||
|
BY – Беларус |
BY-0 |
Цялата страна |
— |
|
|
|
|
||||
|
BZ – Белиз |
BZ-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
CA – Канада |
CA-0 |
Цялата страна |
BOV, OVI, POR, EQU, SUF, SUW RUF, RUW, |
G |
|
|
|
||||
|
CH – Швейцария |
CH-0 |
Цялата страна |
* |
|
|
|
|
||||
|
CL – Чили |
CL-0 |
Цялата страна |
BOV, OVI, POR, EQU, RUF, RUW, SUF |
|
|
|
|
||||
|
CN – Китай |
CN-0 |
Цялата страна |
— |
|
|
|
|
||||
|
CO – Колумбия |
CO-0 |
Цялата страна |
EQU |
|
|
|
|
||||
|
CR – Коста Рика |
CR-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
CU – Куба |
CU-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
DZ – Алжир |
DZ-0 |
Цялата страна |
— |
|
|
|
|
||||
|
ET – Етиопия |
ET-0 |
Цялата страна |
— |
|
|
|
|
||||
|
FK – Фолкландски острови |
FK-0 |
Цялата страна |
BOV, OVI, EQU |
|
|
|
|
||||
|
GL – Гренландия |
GL-0 |
Цялата страна |
BOV, OVI, EQU, RUF, RUW |
|
|
|
|
||||
|
GT – Гватемала |
GT-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
HK — Хонконг |
HK-0 |
Цялата страна |
— |
|
|
|
|
||||
|
HN – Хондурас |
HN-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
HR – Хърватия |
HR-0 |
Цялата страна |
BOV, OVI, EQU, RUF, RUW |
|
|
|
|
||||
|
IL – Израел |
IL-0 |
Цялата страна |
— |
|
|
|
|
||||
|
IN — Индия |
IN-0 |
Цялата страна |
— |
|
|
|
|
||||
|
IS – Исландия |
IS-0 |
Цялата страна |
BOV, OVI, EQU, RUF, RUW |
|
|
|
|
||||
|
KE – Кения |
KE-0 |
Цялата страна |
— |
|
|
|
|
||||
|
MA – Мароко |
MA-0 |
Цялата страна |
EQU |
|
|
|
|
||||
|
ME — Черна гора |
ME-0 |
Цялата страна |
BOV, OVI, EQU |
|
|
|
|
||||
|
MG — Мадагаскар |
MG-0 |
Цялата страна |
— |
|
|
|
|
||||
|
MK – Бивша югославска република Македония (4) |
MK-0 |
Цялата страна |
OVI, EQU |
|
|
|
|
||||
|
MU – Мавриций |
MU-0 |
Цялата страна |
— |
|
|
|
|
||||
|
MX – Мексико |
MX-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
NA – Намибия |
NA-0 |
Цялата страна |
EQU, EQW |
|
|
|
|
||||
|
NA-1 |
На юг от линията на санитарния кордон, който се простира от Palgrave Point на запад до Gam на изток |
BOV, OVI, RUF, RUW |
F |
1 |
|
|
|||||
|
NC — Нова Каледония |
NC-0 |
Цялата страна |
BOV, RUF, RUW |
|
|
|
|
||||
|
NI – Никарагуа |
NI-0 |
Цялата страна |
— |
|
|
|
|
||||
|
NZ – Нова Зеландия |
NZ-0 |
Цялата страна |
BOV, OVI, POR, EQU, RUF, RUW, SUF, SUW |
|
|
|
|
||||
|
PA – Панама |
PA-0 |
Цялата страна |
BOV, EQU |
|
|
|
|
||||
|
PY – Парагвай |
PY-0 |
Цялата страна |
EQU |
|
|
|
|
||||
|
PY-1 |
Цялата страна, с изключение на определената 15 километрова строго наблюдавана зона навътре от външните граници |
BOV |
A |
1 |
|
1 август 2008 година |
|||||
|
RS – Сърбия (5) |
RS-0 |
Цялата страна |
BOV, OVI, EQU |
|
|
|
|
||||
|
RU — Русия |
RU-0 |
Цялата страна |
— |
|
|
|
|
||||
|
RU-1 |
Област Мурманск, автономен окръг Ямоло-Ненец |
RUF |
|
|
|
|
|||||
|
SV – Ел Салвадор |
SV-0 |
Цялата страна |
— |
|
|
|
|
||||
|
SZ – Свазиленд |
SZ-0 |
Цялата страна |
EQU, EQW |
|
|
|
|
||||
|
SZ-1 |
Областта на запад от огражденията на т. нар. „червена линия“, която се простира северно от река Usutu до границата с Южна Африка западно от Nkalashane, |
BOV, RUF, RUW |
F |
1 |
|
|
|||||
|
SZ-2 |
Зоните за ветеринарно наблюдение на шапа и контрол на ваксинирането в съответствие с акта, публикуван в законово известие № 51 от 2001 г. |
BOV, RUF, RUW |
F |
1 |
|
4 август 2003 г. |
|||||
|
TH – Тайланд |
TH-0 |
Цялата страна |
— |
|
|
|
|
||||
|
TN – Тунис |
TN-0 |
Цялата страна |
— |
|
|
|
|
||||
|
TR — Турция |
TR-0 |
Цялата страна |
— |
|
|
|
|
||||
|
TR-1 |
Провинции Amasya, Ankara, Aydin, Balikesir, Bursa, Cankiri, Corum, Denizli, Izmir, Kastamonu, Kutahya, Manisa, Usak, Yozgat и Kirikkale |
EQU |
|
|
|
|
|||||
|
UA – Украйна |
UA-0 |
Цялата страна |
— |
|
|
|
|
||||
|
US – Съединени щати |
US-0 |
Цялата страна |
BOV, OVI, POR, EQU, SUF, SUW, RUF, RUW |
G |
|
|
|
||||
|
UY – Уругвай |
UY-0 |
Цялата страна |
EQU |
|
|
|
|
||||
|
BOV, |
A |
1 |
|
1ноември 2001 г. |
|||||||
|
OVI |
A |
1 |
|
|
|||||||
|
ZA – Южна Африка |
ZA-0 |
Цялата страна |
EQU, EQW |
|
|
|
|
||||
|
ZA-1 |
Цялата страна с изключение на:
|
BOV, OVI, RUF, RUW |
F |
1 |
|
|
|||||
|
ZW — Зимбабве |
ZW-0 |
Цялата страна |
— |
|
|
|
|
||||
„1“ Ограничения по категории: Не се разрешава вносът на карантия в Съюза (с изключение, що се отнася до видовете, принадлежащи към едрия рогат добитък, на диафрагма и челюстни мускули). |
|||||||||||
ЧАСТ 2
Образци на ветеринарни сертификати
Образец/образци:
|
„BOV“ |
: |
Образец на ветеринарен сертификат за прясно месо, включително мляно месо, от домашни животни от рода на едрия рогат добитък (включително видовете Bison и Bubalus, и техните кръстоски). |
|
„OVI“ |
: |
Образец на ветеринарен сертификат за прясно месо, включително мляно месо, от домашни животни от рода на овцете (Ovis aries) и домашни животни от рода козите (Capra hircus). |
|
„POR“ |
: |
Образец на ветеринарен сертификат за прясно месо, включително мляно месо, от домашни животни от рода на свинете (Sus scrofa). |
|
„EQU“ |
: |
Образец на ветеринарен сертификат за прясно месо, без мляно месо, от домашни нечифтокопитни животни (Equus caballus, Equus asinus и техните кръстоски). |
|
„RUF“ |
: |
Образец на ветеринарен сертификат за прясно месо, без карантия и мляно месо, от отглеждани в стопанства дивечови животни от разред Чифтокопитни (без животни от рода на едрия рогат добитък (включително видовете Bubalus и Bison, и техните кръстоски), Ovis aries, Capra hircus, Свине и Пекари) и от семействата Носорози и Слонове. |
|
„RUW“ |
: |
Образец на ветеринарен сертификат за прясно месо, без карантия и мляно месо, от дивечови животни на свобода, от разред Чифтокопитни (без животни от рода на едрия рогат добитък (включително видовете Bubalus и Bison, и техните кръстоски), Ovis aries, Capra hircus, Свине и Пекари) и към семействата Носорози и Слонове. |
|
„SUF“ |
: |
Образец на ветеринарен сертификат за прясно месо, без карантия и мляно месо, от отглеждани в стопанства дивечови животни, принадлежащи към семействата Свине, Пекари или Тапирови. |
|
„SUW“ |
: |
Образец на ветеринарен сертификат за прясно месо, без карантия и мляно месо, от дивечови животни на свобода, от семейства Свине, Пекари или Тапирови. |
|
„EQW“ |
: |
Образец на ветеринарен сертификат за прясно месо, без карантия и мляно месо, от диви нечифтокопитни животни, принадлежащи към подрод Hippotigris (зебра). |
ДГ (Допълнителни гаранции)
|
„A“ |
: |
гаранции по отношение на зреенето, измерването на pH и обезкостяването на прясно месо, с изключение на карантия, сертифицирано в съответствие с образците на ветеринарни сертификати BOV (точка II.2.6), OVI (точка II.2.6), RUF (точка II.2.7) и RUW (точка II.2.4). |
|
„C“ |
: |
гаранции по отношение на лабораторното изследване за откриване на класическа чума по свинете в кланични трупове, от които е добито прясно месо, сертифицирано в съответствие с образеца на ветеринарен сертификат SUW (точка II.2.3 Б). |
|
„D“ |
: |
гаранции по отношение на хранителните отпадъци в стопанството/ата, давани на животните, от които е било добито прясно месо, сертифицирано в съответствие с образеца на ветеринарен сертификат POR (точка II.2.3, буква г)) |
|
„E“ |
: |
гаранции по отношение на изследването за откриване на туберкулоза у животните, от които е било добито прясно месо, сертифицирано в съответствие с образеца на ветеринарен сертификат BOV (точка II.2.4, буква г). |
|
„F“ |
: |
гаранции по отношение на зреенето и обезкостяването на прясно месо, с изключение на карантия, сертифицирано в съответствие с образците на ветеринарни сертификати BOV (точка II.2.6), OVI (точка II.2.6), RUF (точка II.2.6) и RUW (точка II.2.7). |
|
„G“ |
: |
гаранции по отношение на 1, изключването на карантия и гръбначен мозък; и 2, изследването и произхода на животни от семейство Плътнороги по отношение на хроничното линеене, както е посочено в образците на ветеринарни сертификати RUF (точка II.1.7) и RUW (точка II.1.8). |
|
„H“ |
: |
допълнителни гаранции, изисквани за Бразилия, по отношение на контактите между животни, програмите за ваксинация и наблюдението. Тъй като в щата Santa Catarina в Бразилия не се провеждат ваксинации срещу болестта шап обаче, препратката към програма за ваксинация не е приложима за месото, добито от животни, произхождащи от този щат и заклани там. |



















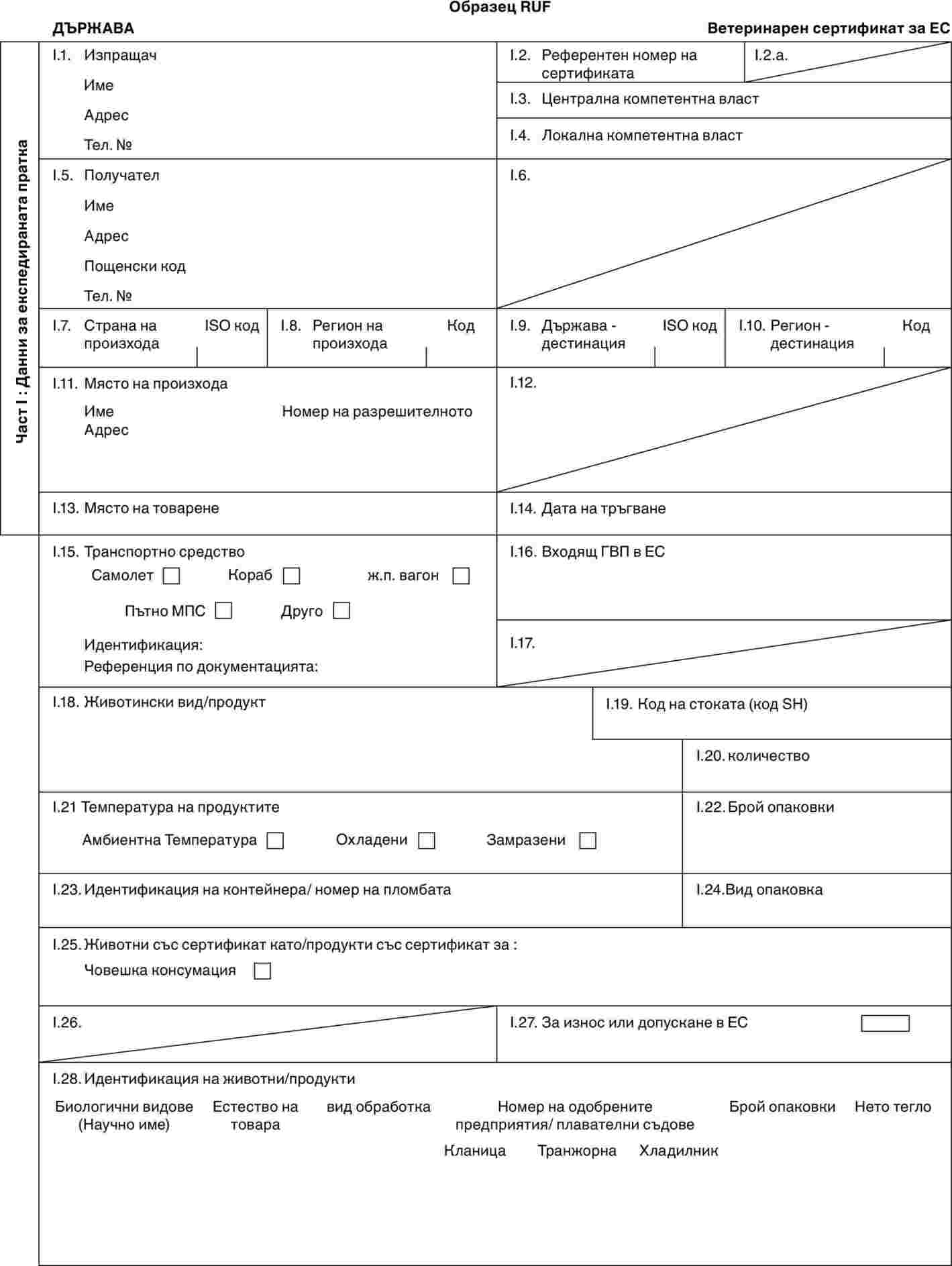
















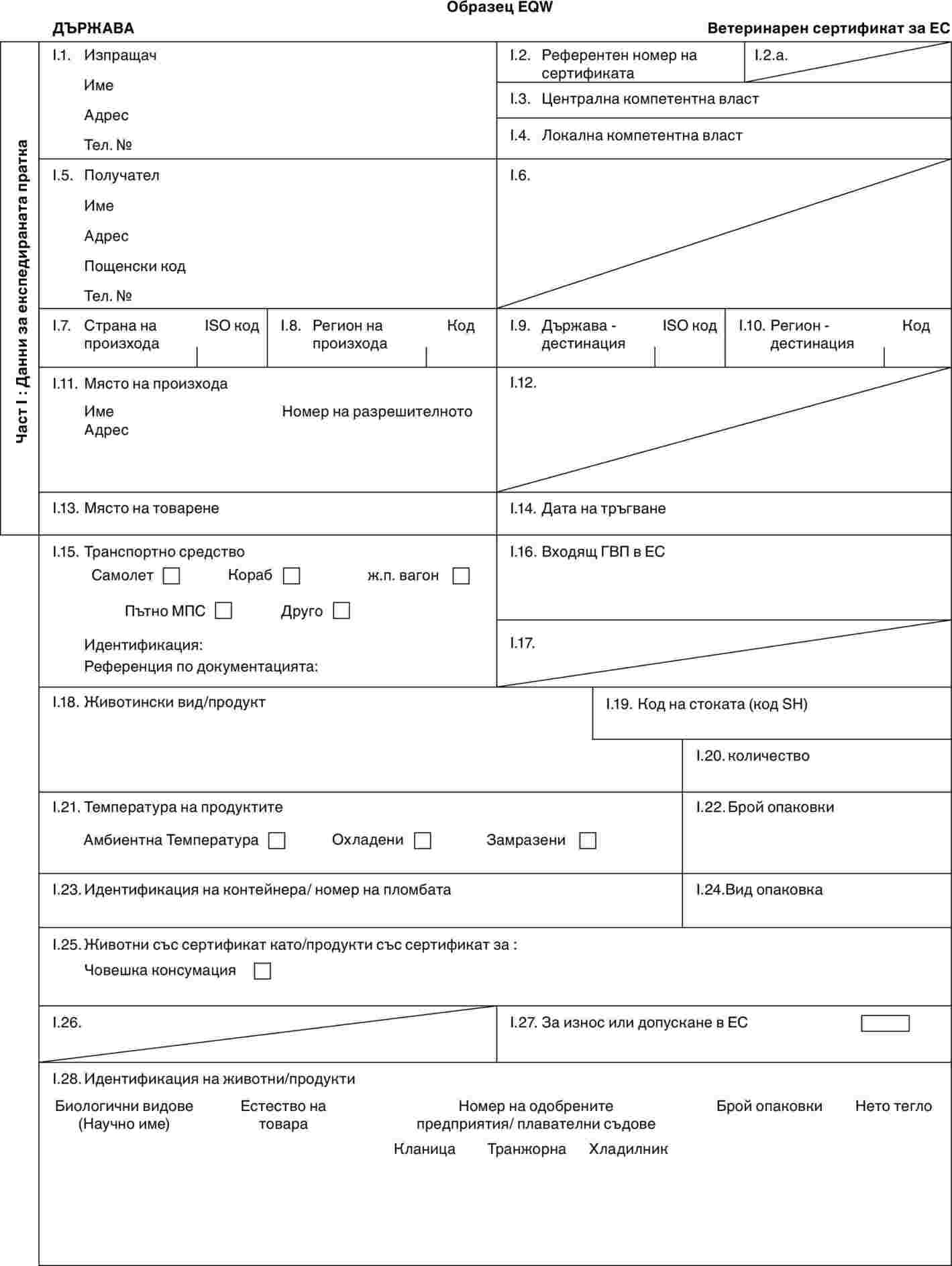


(1) Без да се засягат специфичните изисквания за сертифициране, които са предвидени в споразуменията на Съюза с трети страни.
(2) Месо от животни, заклани на посочената в графа 7 дата или преди нея, може да бъде внасяно в Съюза за период от 90 дни от тази дата. Пратките, намиращи се на плавателни съдове в открито море, могат да бъдат внасяни в Съюза, ако са сертифицирани преди датата, посочена в графа 7, в продължение на 40 дни от тази дата (N.B.: липсата на дата в графа 7 означава, че няма ограничения за време).
(3) Може да бъде внасяно в Съюза само месо от животни, заклани на датата, посочена в графа 8, или след нея (липсата на дата в графа 8 означава, че няма ограничения за време).
(4) Бивша югославска република Македония; временен код, който по никакъв начин не нарушава окончателната номенклатура за тази страна, която ще бъде одобрена след приключване на преговорите по този въпрос, които се провеждат понастоящем в Организацията на обединените нации.
(5) Не е включено Косово, което в момента е под управлението на международна администрация по силата на Резолюция 1244 от 10 юни 1999 г. на Съвета за сигурност на ООН.
|
* |
Изисквания в съответствие със Споразумението между Европейската общност и Конфедерация Швейцария относно търговията със селскостопански продукти (ОВ L 114, 30.4.2002 г., стр. 132). |
|
- |
Не са предвидени сертификати и вносът на прясно месо е забранен (с изключение на видовете, които са посочени на реда, отнасящ се за цялата страна). |
„1“ Ограничения по категории:
Не се разрешава вносът на карантия в Съюза (с изключение, що се отнася до видовете, принадлежащи към едрия рогат добитък, на диафрагма и челюстни мускули).
ПРИЛОЖЕНИЕ III
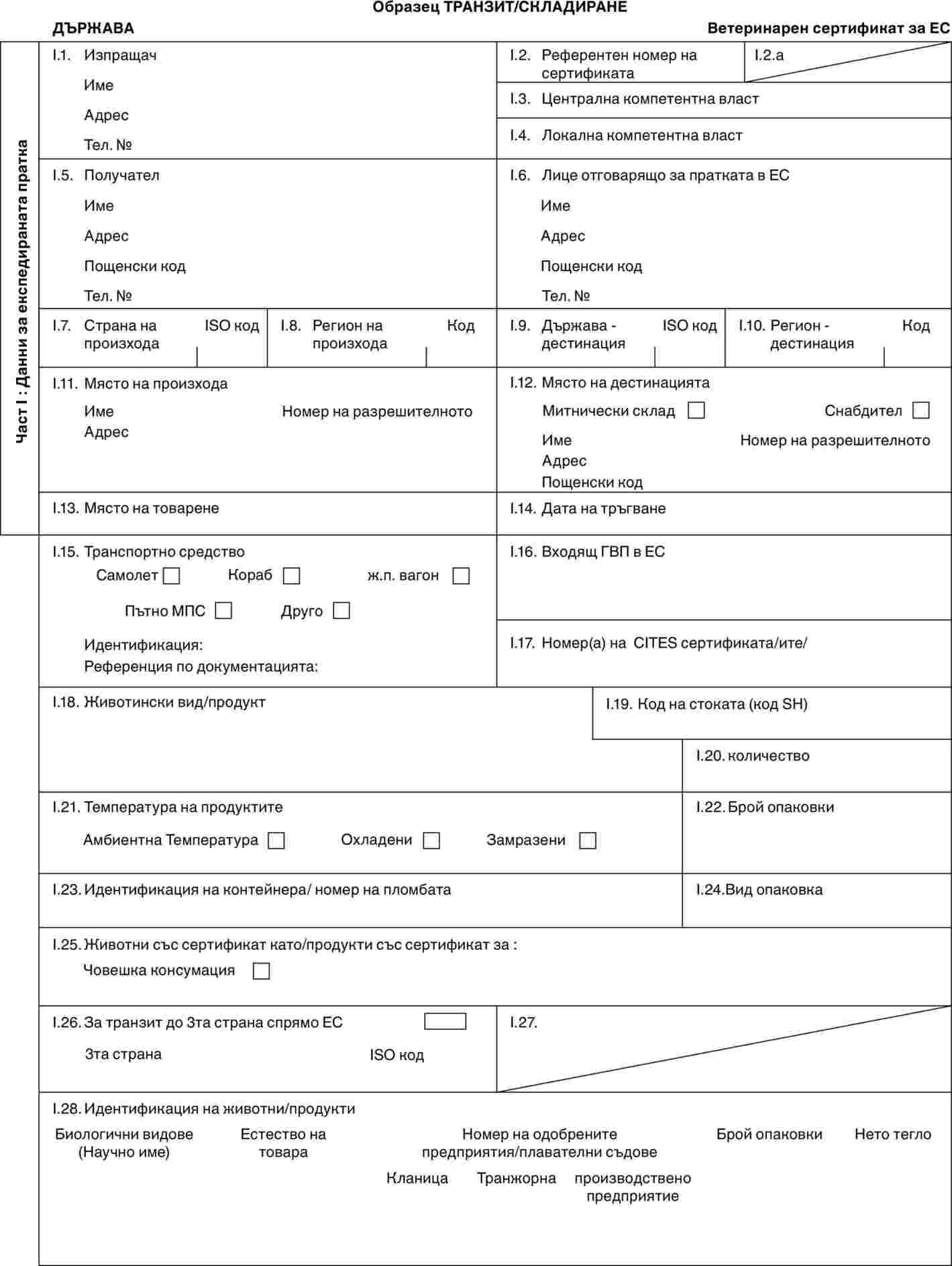


ПРИЛОЖЕНИЕ IV
ЖИВОТНИ, ПОСОЧЕНИ В ЧЛЕН 1, ПАРАГРАФ 1, БУКВА б)
ЧАСТ 1
Списък на трети страни, територии или части от тях
РАЗДЕЛ 1
Части от третите страни или територии, посочени в член 7, параграф 2
|
Страна/територия |
Код на частта от страната/територията |
Описание на частта от страната/територията |
|
US –Съединени щати |
US-A |
Щат Hawaii |
ЧАСТ 2
Таблици на животните и съответстващите им образци на ветеринарни сертификати
|
Таблица 1: |
|
|||||||
|
||||||||
|
Разред |
Семейство |
Родове/видове |
||||||
|
Ципокрили |
Пчели |
Apis mellifera, Bombus spp. |
||||||
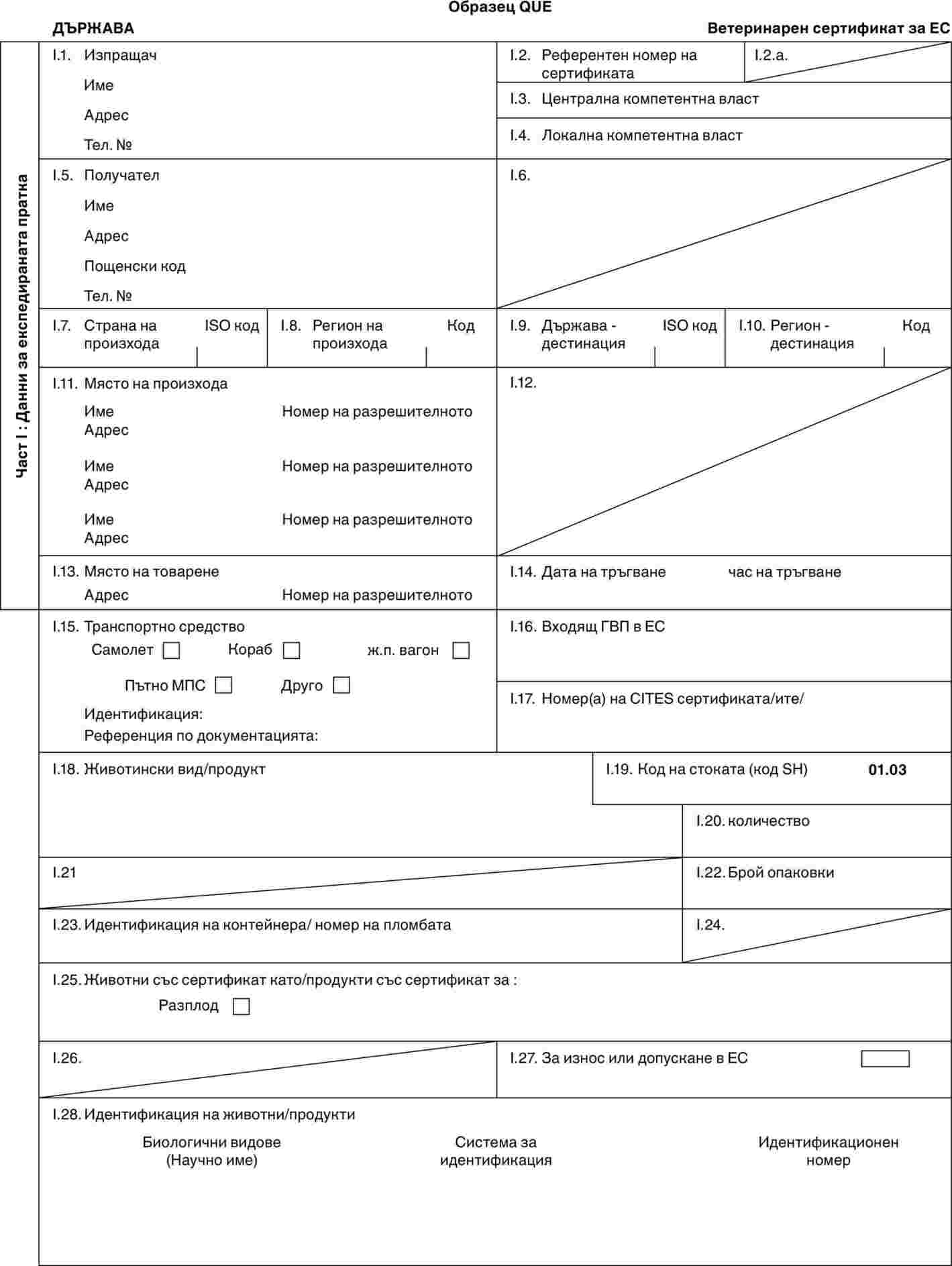

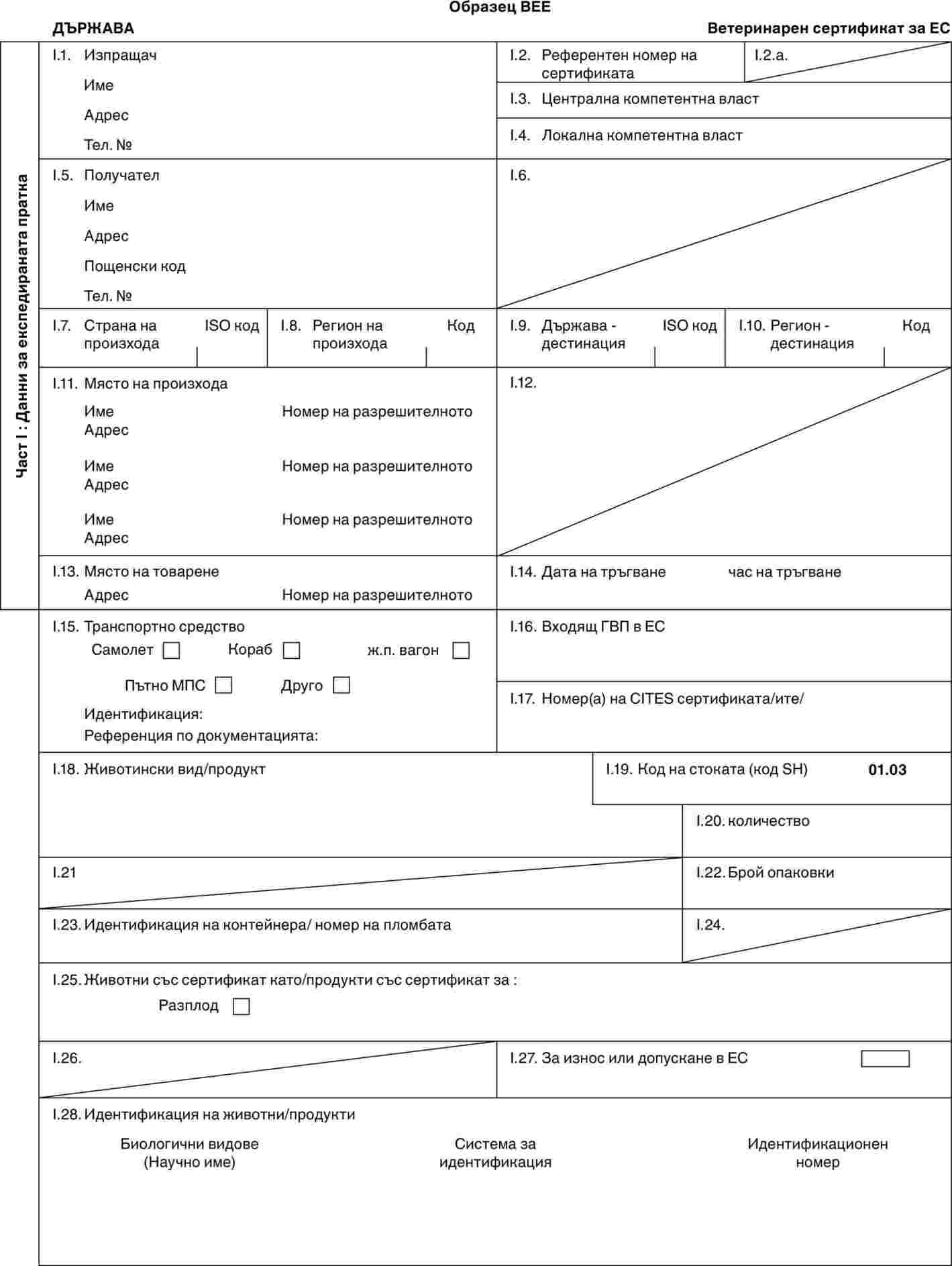

ПРИЛОЖЕНИЕ V
Обяснителни бележки за попълването на ветеринарните сертификати
(посочени в член 18)
|
а) |
Ветеринарни сертификати се съставят от третата страна износител въз основа на образците, посочени в част 2 от приложения I, II и IV, както и на приложение III според оформлението на образеца, който отговаря на съответните живи животни/видове прясно месо. Те съдържат, в указаната в образеца номерирана последователност, удостоверенията, които се изискват за всяка трета страна и — когато е необходимо — допълнителните гаранции, изисквани за третата страна износител или за част от нея. Ако държавата-членка по местоназначение налага допълнителни сертификационни изисквания за съответните живи животни/видове прясно месо, в оригиналния формуляр на ветеринарния сертификат се включват и удостоверения, че посочените изисквания са удовлетворени. |
|
б) |
В случаите, когато в даден образец на сертификат е посочено, че определено твърдение се оставя според случая, твърденията, които не отговарят на действителността, се зачеркват, парафират и подпечатват от сертифициращия служител, или напълно се заличават от сертификата. |
|
в) |
Трябва да се осигури отделен и уникален сертификат за живите животни/прясното месо, изнасяни/о от територия или територии на една и съща страна износител, посочена в графи 2 и 3 на част 1 от приложения I, II или IV, които са изпратени на едно и също местоназначение и се транспортират в един и същ железопътен вагон, камион, самолет или кораб. |
|
г) |
Оригиналът на всеки сертификат се съставя на един лист хартия или — ако необходимият текстът е по-дълъг —, сертификатът се съставя в такава форма, че всички необходими листове хартия да съставляват единно и неделимо цяло. |
|
д) |
Ветеринарният сертификат се съставя най-малко на един от официалните езици на държавата-членка, в която ще се извърши инспекцията на граничния пункт на въвеждане на пратката в Съюза, и на езика на държавата-членка по местоназначение. Посочените държави-членки могат обаче да разрешат и съставянето на сертификат на официалния език на друга държава-членка, придружен, ако е необходимо, от официален превод. |
|
е) |
Ако по причини, свързани с идентификацията на артикулите от пратката (таблица в точка I.28 от образеца на ветеринарен сертификат), към сертификата се прилагат допълнителни листове, като тези листове също се считат за част от оригинала на сертификата чрез полагането на подписа и печата на сертифициращия служител върху всяка страница. |
|
ж) |
Когато сертификатът, включително допълнителните таблици, посочени в буква е), съдържа повече от една страница, всяка страница се номерира (номер на страница) от (общ брой на страниците) в долния край на страницата, а в горния край на страницата се нанася референтният номер на сертификата, който е бил определен от компетентния орган. |
|
з) |
Оригиналът на сертификата трябва да бъде попълнен и подписан от официален ветеринарен лекар или от друг определен официален инспектор, когато това се изисква от образеца на ветеринарния сертификат. В случая на живи животни сертификатът трябва да бъде попълнен и подписан в рамките на 24 часа преди натоварване на пратката за въвеждане в Съюза. Компетентните органи на третата страна износител гарантират, че сертифицирането е извършено при спазване на правила, еквивалентни на установените в Директива 96/93/ЕО (1). Цветът на подписа е различен от този на печатния текст. Това изискване се прилага също и към печатите, с изключение на онези, които са релефни или с воден знак. |
|
и) |
Референтният номер на сертификата, посочен в клетки I.2 и II.a., трябва да бъде издаден от компетентния орган. |








